OPTIMASI PREPARASI SENYAWA BERTANDA
186RE-PORFIRIN
UNTUK PENGOBATAN KANKER
Maskur, Dadang Hafid
Pusat Radioisotop dan Radiofarmaka -BATAN Serpong e-mail: maskur@batan.go.id
A.Mutalib
UNPAD Fakultas MIPA -Bandung
ABSTRAK
OPTIMASI PREPARASI SENYAWA BERTANDA 186RE-PORFIRIN UNTUK PENGOBATAN KANKER. Porfirin dan turunannya telah banyak dipelajari sebagai
fotosensitizer untuk terapi fotodinamik sebagai salahsatu metode pengobatan kanker maupun tumor. Namun, metode tersebut memiliki kekurangan, hanya mampu mengobati kanker dengan kedalaman < 1 cm dan harus terletak di permukaan kulit atau selaput lender. Oleh karena itu, untuk solusinya perlu dibuat porfirin bertanda radionuklida (Renium-186). Penelitian optimasi penandaan 186Re-porfirin telah dilakukan terhadap 2 jenis porfirin (Porfirin TMPyP dan porfirin pita 4) dengan variasi jumlah SnCl2, pH dan suhu reaksi. Secara teori, melalui molecular modeling diketahui
gugus karboksilat pada substituent meso porfirin memungkinkan dapat dilabel dengan radionuklida sebagai kandidat kit radiofarmaka. Namun, dari hasil penelitian yang telah dilakukan belum diperoleh hasil penandaan yang optimal, porfirin (TMPyP) tidak dapat bereaksi dengan 186Re, hasil penandaan terbaik hanya 2,35%. Sedangkan penandaan 186Re terhadap porfirin pita 4 dapat terjadi penandaan meskipum belum diperoleh kondisi optimum. Kondisi terbaik yang diperoleh yaitu jumlah SnCl2 1 mg, pH
8, inkubasi 1 jam dan suhu 50 C dengan hasil penandaan 21,77%.
Kata kunci: Rhenium 186, porfirin, kanker
ABSTRACT
PREPARATION OF 186RE-PORPHYRIN COMPOUNDS FOR CANCER TREATMENT. Porphyrine and its derivatives have been widely studied as a
photosensitizer for photodynamic therapy as one of the main methods of cancer treatment. However, these methods have shortages is to treat cancer with a depth <1 cm only and must be located on the surface of the skin or mucus membranes. Therefore, to solution should be labeled with radionuclide (Rhenium-186). The 186Re- porphyrins labeling study was carried out on 2 types of porphyrins (porphyrins TMPyP and porphyrins band 4) with variations in the amount of SnCl2, pH and temperature of
the reaction. In theory, through molecular modeling of known carboxylate groups on the porphyrin meso substituent could potentially be labeled with radionuclides as a candidate of radiopharmaceutical kits. However, the results showed that porphyrin (TMPyP) did not react with 186Re, the best labeling results was only 2.35%. Labeling of tape 4 porphyrin with Re was occured, but optimum conditions has not obtained yet. The best conditions obtained for labelling are 1 mg SnCl2, pH 8, 1 hour incubation at
temperature of 50 oC resulting of 21.77% yield.
Keywords: Rhenium-186, porphyrin, cancer
PENDAHULUAN
orfirn dan turunannya telah banyak dipelajari sebagai fotosensitizer untuk terapi fotodinamik sebagai salahsatu metode pengobatan kanker
maupun tumor[1,2]. Turunan porfirin ini memiliki toksisitas yang rendah untuk jaringan yang sehat dan kelarutannya di dalam air rendah[3]. Untuk meningkatkan kelarutan porfirin dalam air, telah banyak penelitian mensintesis turunan porfirin yang
dimodifikasi strukturnya, bentuk kationiknya, serta memformulasinya dengan suatu pembawa yang dapat meningkatkan kelarutan porfirin dalam air[3,4,5]. Namun, terapi pengobatan kanker melalui teknik fotosensitizer memiliki kekurangan, hanya mampu mengobati kanker dengan kedalaman < 1cm dan harus terletak di permukaan kulit atau selaput lendir.[6]. Oleh karena itu, solusinya perlu dibuat porfirin bertanda radionuklida (Renium-186) sehingga pengobatan bisa dilakukan melalui kedokteran nuklir bukan terapi fotodinamik. Contoh Struktur Kimia turunan Porfirin adalah sebagai berikut:
Gambar1. Porfirin pita 4
Gambar2. Porfirin TMPyP
Senyawa porfirin dapat dimodifikasi struktur kimianya, baik pada meso-substituennya, atau pada pusat molekulnya dengan ion logam, sehingga senyawa tersebut dengan mudah dilabel radionuklida pemancar maupun . Senyawa turunan kationik porfirin dapat digunakan sebagai ligan dalam pembuatan kit radiofarmaka untuk diagnosis dan terapi kanker. Namun demikian, karena radionuklida baik pemancar maupun seperti 99mTc dan 188Re memiliki radius atom yang cukup besar maka koordinasi radionuklida tersebut dengan keempat inner nitrogen sangat sulit dilakukan dan membutuhkan waktu yang lama[7]. Secara teori yang telah dibuktikan melalui molecular modeling ternyata gugus karboksilat pada substituent meso memungkinkan porfirin
T3,4BCPzP dan T3,4BCImP dapat dilabel dengan radionuklida sebagai kandidat kit radiofarmaka[6]. Renium-186 merupakan radionuklida pemancar partikel dan sinar sehingga dapat digunakan untuk pencitraan dengan kamera gama (imaging) selama terapi berlangsung. Renium berada dalam satu kelompok teknesium (grup VIIA) dan keduanya memiliki karakter yang hampir sama .
186
Re-Porfirin diketahui pula sebagai radiofarmaka yang digunakan untuk terapi tumor. Renium-186 disiapkan dengan mengiradiasi logam Renium-185 dengan pengkayaan > 97 % pada flux netron 3,7 x 1013cm-2 det-1 selama 3 hari. Karakterisai porfirin non radioaktif dilakukan menggunakan spektrofotometer UV-vis, dan untuk menentukan kemurnian radiokimia 186RePorfirin yang terbentuk serta jumlah pengotor ReO4
dan ReO2, digunakan
perunut radioaktif 186Re. Pelabelan 186Re-Porfirin mengacu pada metode Haladar D Sharma, et. All[8]. Preparasi kompleks 186Re-Porfirin disiapkan menggunakan dua jenis turunan porfirin yang dimodifikasi (pita 4 dan TMPyP) dengan memvariasikan berbagai kondisi reaksi, seperti pH, dan jumlah stanoklorida dihidrat. Uji kemurnian radiokimia menggunakan kromatografi lapis tipis dengan fase diam kertas Whatman, fase gerak aseton dan NaCl 0,9%. Kertas kromatogram dianalisis menggunakan TLC scaner BIOSCAN.
TATA KERJA Bahan dan Peralatan
Bahan utama yang digunakan dalam penelitian ini adalah Porfirin TMPyP, porfirin pita 4 hasil sintesis ITB. Radionuklida 186Re, Amonium perenat, HNO3, gas N2, kertas pH, SnCl2, HCl,
aquabides, kertas whattman 1, aseton, salin
Peralatan yang digunakan adalah bejana kromatografi, TLC scanner BIOSCAN USA, spektrofotometri UV-Vis (Jasco-Japan), FTIR (Jasco-Japan), vortex (thermoline), dose calibrator Atomlab sebagai pengukur konsentrasi radioaktivitas, perangkat kromatografi, kertas whaman-1 untuk kromatografi
Pembuatan Radionuklida 186Re
Target ReO2 yang sudah di Iradiasi di
reaktor nuklir dimasukkan ke dalam hotcell, kemudian dilakukan pemotongan inner kapsul dengan pemotong yang ada didalam hotcell. Setelah itu botol quatrz yang berisi target ReO2 dikeluarkan
untuk selanjutnya dilakukan pemotongan kembali. Setelah dipotong, ReO2 dituangkan kedalam gelas
piala 100 ml . Setelah itu ditambahkan 3 ml HNO3 4
N selanjutnya gelas piala dipindahkan ke hotplate . Kemudian dipanaskan hingga kisat. Setelah kisat, ditambahkan 3 ml aquabidest, dan dipanaskan lagi hingga kisat. Penambahan aquabidest dan
pengkisatan dilakukan berulang hingga pH≥3. Setelah kering, ditambahkan 3 ml aquabidest dan larutan dipindahkan ke dalam botol dan dipipet 10 µL larutan 186ReO4 dimasukkan ke dalam tabung
mikro untuk dilakukan pengukuran radioaktivitas menggunakan Dose Calibrator.
Preparasi reduktor SnCl2
Ligan SnCl2 sebanyak 6,1 mg ditimbang
dan dimasukkan kedalam vial 3 ml. Ke dalam vial, ditambahkan 400 l HCl 1N lalu dipanaskan hingga hampir kisat. Setelah itu ditambahkan aquabides yang telah dijenuhkan gas N2 hingga volume larutan
menjadi 305 µl maka dihasilkan larutan SnCl2 0,02
mg/l (50 l=1mg). Preparasi Ligan Porfirin
Porfirin pita 4 / porfirin TMPyP sebanyak 2,4 mg ditimbang dan dimasukkan ke dalam tabung
mikro. Kemudian ditambahkan kedalamnya 240 l aquabides yang telah dijenuhkan gas N2. Setelah itu
divortex hingga larut sehingga dihasilkan larutan porfirin 0,01 mg/l (40l0,4 mg)
Preparasi Amonium Perenat
Amonium perenat sebanyak 2,04 mg ditimbang dan dimasukkan ke dalam tabung mikro. Ditambahkan 204 l aquabides yang telah dijenuhkan gas N2. Kemudian diaduk dengan vortek
hingga larut sempurna menghasilkan larutan Amonium Perenat 0,01 mg/l (10 l ≈ 0,1 mg). Proses Penandaan 186Re-porfirin
Cara kerja proses penandaan 186Re-Porfirin secara detail dapat dilihat pada diagram alir proses seperti pada Gambar 3.
HASIL DAN PEMBAHASAN
Gambar 4. Kromatogram Porfirin pita 4
Dari Gambar 4 dan 5, hasil analisis menggunakan spektrofotometri UV-Vis diketahui bahwa spektra dari porfirin pita 4 dan porfirin TMPyP terdapat perbedaan serapan. Pada Porfirin pita 4, terdapat tiga puncak yaitu pada panjang gelombang 416, 516, dan 678 nm. Sedangkan porfirin TMPyP mempunyai lima puncak, yaitu pada panjang gelombang 218, 260, 422, 518, dan 584 nm. Hal ini menunjukkan keduanya mempunyai struktur kimia yang berbeda.
Pada penelitian dan pengembangan senyawa bertanda Re-186 porfirin, digunakan berbagai jenis instrument, yaitu spektrofotometer UV-Vis dan FTIR untuk karakterisasi porfirin sebelum penandaan, sedangkan setelah penandaan menggunakan alat Dose Calibrator, kromatografi unit, dan TLC scanner. Adapun hasilnya ditampilkan pada gambar 4 dan 5.
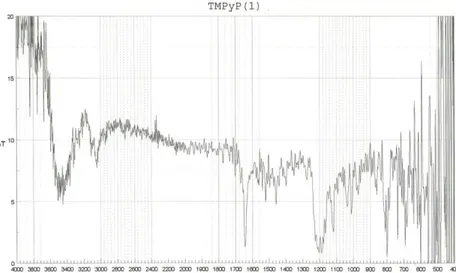
Gambar 5. Kromatogram Porfirin TMPyP
Dari Gambar 6 dapat diketahui bahwa porfirin TMPyP dapat diidentifikasi menggunakan FTIR. Adapun gugus fungsinya adalah NH(3500, 1600), C=C (3040), C-N (980), SO3(1200, 1100)
Cm-1
Dari Gambar 7 dapat diketahui bahwa porfirin pita 4 dapat diidentifikasi menggunakan FTIR. Adapun gugus fungsinya adalah OH(3400), C=C (3040), CO (1400), C-N (980) Cm-1
Dari Gambar 8 dapat diketahui bahwa porfirin mempunyai spektra yang hampir mirip namun ada beberapa perbedaan mendasar, yaitu porfirin pita 4 mempunyai gugus fungsi SO3 yang
ditunjukkan oleh spectra pada bilangan gelombang 1200 dan 1100 Cm-1 sedangkan pada porfirin TMPyP tidak ada. Hal ini sesuai dengan struktur kimia porfirin yang ditunjukkan pada gambar 1 dan 2.
Gambar 7. Spektra porfirin pita 4 menggunakan FTIR
Gambar 8. Overlay Spektra porfirin TMPyP dan pita 4 menggunakan FTIR
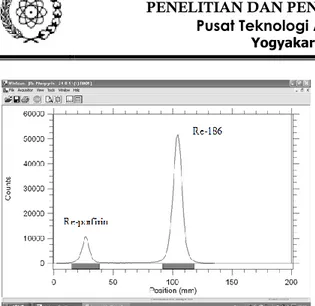
Pasca penandaan 186Re-porfirin, penentuan kemurnian radiokimia hasil penandaan diidentifikasi menggunakan kromatografi kertas dan dicacah menggunakan TLC scanner, hasilnya ditunjukkan pada gambar 9.
Pengujian radiokimia 186Re dilakukan dengan cara kromatografi lapis tipis menggunakan kertas whatman 1 sebagai fasa diam dan campuran aseton:salin = 1:1 sebagai fasa gerak. Paska elusi, radiokromatogram diidentifikasi menggunakan TLC scaner dan hasilnya ditunjukkan pada Gambar 9, yaitu 186Re pada Rf 0,9 -1,0.
Pengujian radiokimia 186Re Porfirin dilakukan dengan cara kromatografi menggunakan kertas whatman 1 sebagai fasa diam dan campuran aseton:salin = 1:1 sebagai fasa gerak. Paska elusi, radiokromatogram diidentifikasi menggunakan TLC
scaner dan hasilnya ditunjukkan pada Gambar 10, yaitu 186Re-porfirin pada Rf 0,0 -0,1.
Gambar 10. Radiokromatogram 186Re-porfirin Pada penelitian ini telah dilakukan optimasi penandaan 186Re-porfirin dengan berbagai variasi, yaitu jumlah SnCl2, pH, Suhu, jenis porfirin
(TMPyP dan pita 4), dan tanpa porfirin sebagai kontrol. Hasil penandaan selengkapnya ditunjukkan pada gambar 11 sampai 15.
Dari Gambar 11, diketahui bahwa hasil penandaan 186Re-porfirin(TMPyP) sangat dipengaruhi oleh jumlah SnCl2. Reaksi penandaan
yang telah dilakukan adalah porfirin (TMPyP) 0,4 mg ditambahkan SnCl2 bervariasi yaitu 1-15 mg
dan ternyata semakin besar jumlah reduktor SnCl2
diperoleh hasil kemurnian penandaan 186
Re-porfirin(TMPyP) yang semakin besar. Namun, hal ini perlu dibuktikan apakah yang terbentuk itu komplek 186Re-porfirin(TMPyP) atau hanya
186
ReO2. Untuk memastikan hal tersebut maka telah
dilakukan proses penandaan yang langkah kerjanya seperti penandaan 186Re-porfirin(TMPyP) tetapi tanpa porfirin. Hasil penandaan ditunjukkan pada gambar 12.
Dari Gambar 12 kontrol penandaan 186 Re-porfirin tanpa Re-porfirin diketahui bahwa tanpa porfirin ternyata juga terbentuk kromatogram pada RF =0-0.1 , dan semakin besar jumlah SnCl2 maka
semakin besar pula prosentasenya. Hal ini menunjukkan bahwa pada proses tersebut terbentuk ReO2 koloid. Hal ini memperjelas bahwa penandaan 186
Re-porfirin(TMPyP) yang ditunjukkan pada Gambar 10 bukan menghasilkan komplek 186 Re-porfirin(TMPyP) melainkan hanya terbentuk ReO2
koloid.
Disamping itu, dari Gambar 12 juga diketahui bahwa hanya penambahan SnCl2
sebanyak 1 mg yang tidak mengakibatkan terbentuknya ReO2 koloid. Untuk selanjutnya,
SnCl2 1 mg digunakan sebagai jumlah SnCl2
optimum untuk penandaan 186Re-porfirin(TMPyP) dengan variasi pH dan hasilnya ditunjukkan pada gambar 13.
Gambar 11. Grafik hasil penandaan 186Re-porfirin(TMPyP) variasi jumlah SnCl2
Gambar 12. Grafik hasil penandaan 186Re-porfirin tanpa porfirin dengan memvariasikan jumlah SnCl2
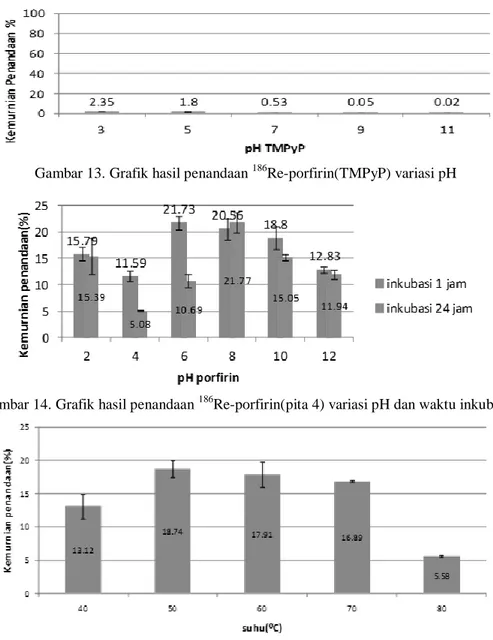
Gambar 13. Grafik hasil penandaan 186Re-porfirin(TMPyP) variasi pH
Gambar 14. Grafik hasil penandaan 186Re-porfirin(pita 4) variasi pH dan waktu inkubasi
Gambar 15. Grafik hasil penandaan 186Re-porfirin(pita 4) variasi suhu reaksi
Dari Gambar 13 diketahui bahwa setelah dilakukan penandaan 186Re-porfirin(TMPyP) dengan variasi pH 3-11 ternyata hasilnya hampir tidak terjadi penandaan 186Re-porfirin(TMPyP). Prosentase penandaan terbesar hanya 2,35% yaitu pada pH 3. Dari hasil tersebut dapat disimpulkan bahwa porfirin TMPyP tidak dapat bereaksi dengan
186
Re. Oleh karena itu, maka dilakukan penandaan
186
Re terhadap jenis senyawa porfirin yang lain, porfirin pita 4 dan hasilnya ditunjukkan pada gambar 14.
Dari Gambar 14 diketahui bahwa telah dilakukan optimasi penandaan 186Re-porfirin (pita 4) dengan variasi pH pada rentang 2-12 dengan waktu inkubasi 1 dan 2 jam. Dari gambar tersebut diketahui bahwa pH penandaan terbaik adalah 6-8 namun setelah diinkubasi 24 jam ternyata yang
relatif stabil adalah pada pH 8. Pada pH tersebut ,
186
Re-porfirin(pita 4) saat diinkubasi 1 jam =20,56% dan setelah diinkubasi 24 jam =21,77%. Sedangkan pada pH 6, pada saat inkubasi 1 jam prosentase penandaan =21,73%, namun setelah diinkubasi 24 jam terjadi penurunan drastis yaitu 10,69%. Dari data tersebut dapat disimpulkan bahwa pH optimum penandaan 186Re-porfirin(pita 4) adalah pH 8.
Setelah diperoleh kondisi jumlah SnCl2
optimum (1 mg), pH optimum (8), jenis porfirin (pita 4) maka selanjutnya dilakukan optimasi suhu reaksi penandaan 186Re-porfirin(pita 4) dan hasilnya seperti ditunjukkan pada gambar 15.
Dari Gambar 15 diketahui telah dilakukan optimasi penandaan 186Re-porfirin(pita 4) variasi suhu reaksi dari 40 sampai 80 C dan ternyata
diperoleh kondisi suhu reaksi optimum adalah 50C. Hal ini kemungkinan ketika suhu reaksi lebih besar dari 50 oC maka Renium valensi 5 hasil reduksi SnCl2 akan teroksidasi kembali menjadi
valensi 7 sehingga mengurangi terjadinya pembentukan komplek 186Re-porfirin.
KESIMPULAN
Telah dilakukan penelitian optimasi penandaan 186Re-porfirin terhadap 2 jenis porfirin (Porfirin TMPyP dan porfirin pita 4) dengan variasi jumlah SnCl2, pH dan suhu reaksi. Dari hasil
penelitian diketahui bahwa porfirin (TMPyP) tidak dapat bereaksi dengan 186Re, hasil penandaan terbaik hanya 2,35%. Sedangkan penandaan 186Re terhadap porfirin pita 4 dapat terjadi penandaan meskipum belum diperoleh kondisi optimum. Kondisi terbaik yang diperoleh yaitu jumlah SnCl2
1 mg, pH 8, inkubasi 1 jam dan suhu 50 C dengan hasil penandaan 21,77%, sehingga masih perlu dilakukan optimasi lebih lanjut untuk memperoleh hasil yang lebih baik.
DAFTAR PUSTAKA
1. Bonnett. R., Chemical Aspect of Photodynamic Therapy, vol I, Gordon and Breach Science Publishers, hal. 159,166-168, Amsterdam, 2000. 2. Hargus, J.A., Naturally –Derived Porphyrin and Chlorin Photosensitizers for Photodynamics Theraphy. Thesis Department of Chemistry, Lousiana State University, Lousiana, Page 1, 2005.
3. Kralova J, Kejik Z, Briza T, Pouckova P, Kral A, Martasek P, Kral V: Porphyrin-cyclodextrin conjugates as a nanosystem for versatile drug delivery and multimodal cancer therapy. J Med Chem, 53 (1): 128-138, 2010.
4. Schiavon, M.A., Iwamoto, L.S., Ferreira, A.G., Iamamoto, Y., Zanoni, M.V.B.,Assis, M.D. Synthesis and Characterization of a Novel Series of Meso (Nitrophenyl) and Meso (CarboxyPhenyl) Substituted Porphyrins, (2000). J. Braz. Chem. Soc., Vol. 11, No.5, 458-466
5. Tjahjono, D.H., T. Yamamoto, S. Ichimoto, N. Yoshioka and H. Inoue, 2000. Synthesis and DNA-binding properties of bisdiazoliumylporphyrins. J. Chem. Soc. Perkin Trans., 1: 3077-3081.
6. N.M.P. Susanti, R.E. Kartasasmita, A. Musadad, and D.H. Tjahjono, Molecular Modeling of cationic porphyrins as ligand of radiopharmaceutical kit.
7. Tjahjono, D.H., R.E. Kartasasmita, A. Nawawi, S. Mima, T. Akutsu, N. Yoshioka and H. Inoue,
2006. Binding of tetrakis-(pyrazoliumyl)porphyrin and its copper(II) and zinc(II) complexes to poly(dG-dC)2 and poly(dA-dT)2. J. Biol. Inorg. Chem., 11: 527-538.
8. SARMA H.D., DAS T., BENERJEE S., VENKATESH M., VIDYASAGAR P.B., AND MISHRA K.P., Evaluation of Novel 188Re Labellled Phorphyrin in Mice Tumor Model, Cancer Biotheraphy and Radiopharmaceuticals, vol 25, Number 1, 2010:47-54.
TANYA JAWAB Tri Haryanto
Dari hasil kesimpulan menunjukkan kondisi terbaik hasil penandaan 21.77%. Berapa target kemurnian yang ingin dicapai dan bagaimana cara mencapainya?
Maskur
Kondisi terbaik kemurnian radiokimia saat ini
diperoleh 21.77% padahal yang ingin dicapai >95%. Oleh karena itu rencana selanjutnya akan dilakukan penandaan 186Re Porfirin dengan porfirin pita 4 (hasil sintesis ITB fakultas farmasi) dengan metode sintesis yang berbeda.
Sunardi
Mengapa menggunakan metode ini padahal disebutkan banyak kekurangan, apa kelebihannya?
Maskur
Yang banyak kekurangannya adalah pengobatan kanker menggunakan porfirin dengan metode fotodinamik terapi. Oleh karena itu kita mencari solusi pengobatan kanker menggunakan senyawa bertanda 186Re porfirin yang dilakukan di instalasi kedokteran nuklir. Untuk mewujudkan hal tersebut maka harus dibuat senyawa bertanda 186Re porfirin, namun hingga saat ini kemurnian radiokimia yang dicapai masih kecil (21.77%) sehingga perlu optimasi lebih lanjut. Adapun
kelebihan metode pengobatan kanker
menggunakan senyawa bertanda dibanding pengobatan menggunakan terapi fotodinamik adalah dengan senyawa bertanda maka dapat mendeteksi dan terapi terhadap kanker yang letaknya di bagian dalam dan kedalaman knker > 1 cm, sedangan pengobatan melalui terapi fotodinamik hanya mampu menerapi kanker padat di permukaan (kulit atau selaput lender) dan kedalaman < 1 cm.