BAB II
TINJAUAN PUSTAKA
2.1 Polietilen Glikol (PEG)
Polietilen glikol adalah polimer yang dapat dirumuskan oleh formula
HOCH2(CH2OCH2)nCH2OH. Nilai n dapat berkisar dari 1 sampai nilai yang
sangat besar, karena itu berat molekul dari PEG ini dapat berkisar antara
150-10.000. Senyawa yang memiliki berat molekul dari 150-700 berbentuk cairan,
dimana senyawa yang berat molekulnya 1.000-10.000 berbentuk padatan.
Senyawa glikol dengan berat molekul yang rendah biasanya digunakan untuk
larutan kental dimana campuran glikol ini biasanya dimanfaatkan sebagai basis
salep larut air (Grosser, et al., 2011).
Polietilen glikol 400 adalah polietilen glikol H(O-CH2-CH2)n OH
dimana harga n antara 8,2 dan 9,1. Pemerian: cairan kental jernih, tidak
berwarna atau praktis tidak berwarna, bau khas lemah, agak higroskopik.
Kelarutan: larut dalam air, dalam etanol (95%) P, dalam aseton P, dalam glikol
lain dan dalam hidrokarbon aromatik, praktis tidak larut dalam eter P dan
dalam hidrokarbon alifatik. Bobot molekul rata-rata: 380-420. Kandungan
Lembab: Sangat higroskopis walaupun higroskopis turun dengan
meningkatnya bobot molekul, titik beku 4-8ºC (Depkes RI, 1979).
Polietilen glikol 4.000, 6.000 dan 8.000 berbentuk serbuk putih dengan
tekstur seperti lilin dan berwarna seperti parafin. Sangat larut dalam air dan
Polietilen glikol dapat menunjukkan aktivitas oksidasi jika terjadi
inkompatibilitas. Aktivitas anti bakteri dari bactricin atau benzilpenicilin dapat
dikurangi jika diformulasi dengan salep yang mengandung basis PEG ini.
(Sweetman, 2009)
Salah satu polimer yang umum digunakan pada pembuatan dispersi
padat adalah PEG. PEG disebut juga makrogol, merupakan polimer sintetik
dari oksietilen dengan rumus struktur H(OCH2CH2)nOH, dimana n adalah
jumlah rata-rata gugus oksietilen. PEG umumnya memiliki bobot molekul
antara 200-300.000. Penamaan PEG umumnya ditentukan dengan bilangan
yang menunjukkan bobot molekul rata-rata. Konsistensinya sangat dipengaruhi
oleh bobot molekul. PEG dengan bobot molekul 200-600 (PEG 200-600)
berbentuk cair, PEG 1500 semi padat, dan PEG 3000-20.000 atau lebih berupa
padatan semi kristalin dan PEG dengan bobot molekul lebih besar dari 100.000
berbentuk seperti resin pada suhu kamar. Umumnya PEG dengan bobot
molekul 1.500-20.000 yang digunakan untuk pembuatan dispersi padat (Leuner
dan Dressman, 2000; Rowe, et al., 2003).
PEG merupakan salah satu jenis bahan pembawa yang sering digunakan
sebagai bahan tambahan dalam suatu formulasi untuk meningkatkan pelarutan
obat yang sukar larut. Bahan ini merupakan salah satu jenis polimer yang dapat
membentuk komplek polimer pada molekul organik apabila ditambahkan
dalam formulasi. Cangkang kapsul dengan menggunakan basis polietilen glikol
memiliki beberapa keuntungan karena sifatnya yang inert, tidak mudah
2.2Interaksi Uap Air-Padatan
Molekul air terdiri dari dua atom hidrogen, yang berikatan secara
kovalen dengan atom pusat oksigen. Molekul air saling menarik satu sama lain
melalui ikatan hidrogen, yang melibatkan polaritas dari molekul air
(Airaksinen, 2005).
Uap air yang diadsorpsi pada permukaan disebut adsorbat, sedangkan
zat padat yang mengadsorpsi uap air tersebut disebut adsorben. Kecenderungan
adsorpsi pada permukaan zat padat sangat tergantung pada tekanan uap air,
temperatur dan perbedaan energi pengikatan interfacial. Proses adsorpsi terjadi
antara molekul air dengan bagian hidrofilik permukaan zat padat melalui ikatan
hidrogen (Airaksinen, 2005).
2.3 Kesetimbangan Kandungan Uap Air
Hubungan antara kelembaban dan kandungan uap air pada temperatur
yang sama (isoterm) dikenal sebagai kesetimbangan isoterm sorpsi uap air
(Equilibrium Moisture Sorption Isotherm) seperti yang dikemukakan oleh Bell
dan Labuza (1992). Masing-masing produk mempunyai kesetimbangan
kandungan uap air yang unik karena perbedaan interaksi (efek koligatif larutan,
efek kapiler, dan interaksi permukaan) antara air dengan komponen padat pada
kandungan uap air yang berbeda. Peningkatan aw biasanya diikuti dengan
peningkatan kandungan uap air, walaupun tidak secara linier. Kesetimbangan
kandungan uap air biasanya berbentuk sigmoidal untuk kebanyakan makanan,
walaupun makanan tersebut mengandung gula dalam jumlah besar (Fontana,
Informasi mengenai mekanisme sorpsi uap air pada suatu bahan dapat
diketahui dari bentuk kesetimbangan kandungan uap airnya, karena hal itu
sangat tergantung pada interaksi antara molekul air dengan suatu bahan padat.
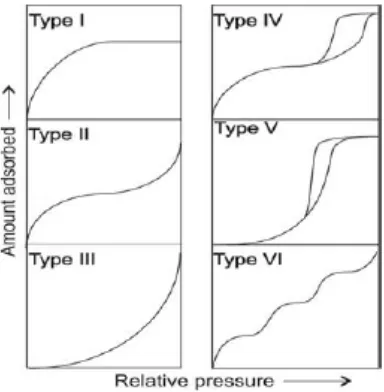
Isoterm sorpsi fisis ini dapat digolongkan menjadi 6 tipe utama (I-VI),
berdasarkan klasifikasi IUPAC. Isoterm tipe V dan VI tidak umum untuk
dijumpai (Sing, et al., 1985).
Tipe I adalah tipe Langmuir, yang ditandai oleh adanya adsorpsi yang
terbatas yang diasumsikan sebagai terbentuknya suatu lapisan tunggal yang
sempurna. Tipe I memiliki adsorben dengan mikropori yang luas
permukaannya relatif kecil, yang dapat menyimpan banyak uap air pada RH
yang rendah (Sing, et al., 1985).
Isoterm tipe II, bentuk sigmoi85dal atau bentuk S umumnya
berhubungan dengan sorpsi lapisan tunggal-multi lapisan pada bahan dengan
permukaan yang tidak berpori atau makropori. Isoterm tipe II dan IV
menunjukkan pengikatan tertentu pada kelembaban rendah yang diikuti dengan
adsorpsi yang rendah pada kelembaban menengah, selanjutnya meningkat lagi
pada kelembaban yang lebih tinggi. Adanya histeresis menunjukkan adanya
mesopori dan umum terjadi pada isoterm tipe II dan IV (Sing, et al., 1985).
Berbeda dengan isoterm tipe IV, isoterm tipe II tidak memiliki
penyerapan yang stabil pada aw yang tinggi. Isoterm tipe IV terjadi karena
tertutupnya mesopori yang diikuti dengan kondensasi kapiler atau pengisian
Isoterm tipe III dan V menandakan adanya interaksi adsorbent-adsorbat
yang lemah dan ditandai dengan penyerapan yang rendah pada kelembaban
rendah dan terjadi peningkatan yang pesat pada kelembaban yang lebih tinggi.
Isoterm tipe VI, isoterm bertingkat dimana terjadi sorpsi tingkat demi tingkat
pada permukaan bahan tidak berpori yang seragam. Klasifikasi isoterm sorpsi
uap air dan berbagai bentuknya dapat dilihat pada Gambar 2.1 (Sing, et al.,
1985).
Gambar 2.1. Klasifikasi isoterm sorpsi uap air dan berbagai bentuknya (Sing, et al., 1985).
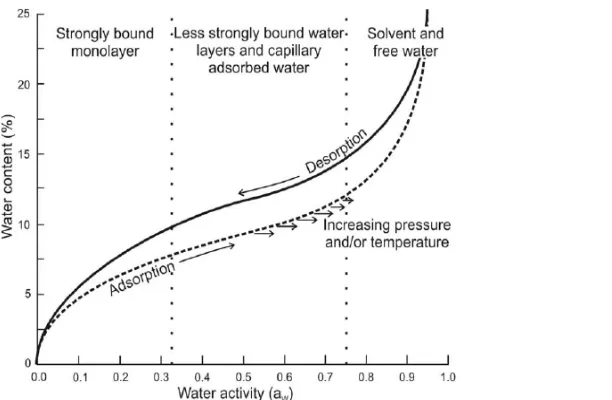
Kesetimbangan dari adsorpsi uap air (dimulai dari keadaan kering)
tidak sama persis dengan kesetimbangan yang dihasilkan dari desorpsi uap air
(dimulai dari keadaan basah). Fenomena dari kandungan uap air yang berbeda
dengan aw yang sama ini dikenal sebagai histeresis sorpsi uap air (moisture
sorption hysteresis) dan dimiliki oleh kebanyakan makanan. Skema histeresis
antara adsorpsi dan desorpsi uap air dapat dilihat pada Gambar 2.2. (Fontana,
Gambar 2.2. Skema histeresis antara adsorpsi dan desorpsi uap air (Chaplin, 2005).
Ada beberapa alasan hal ini dapat terjadi, seperti perbedaan pengisian
dan pengosongan uap air pada pori-pori, pengembangan bahan polimer, transisi
keadaan gelas dan karet, dan supersaturasi beberapa zat terlarut selama
desorpsi. Kesetimbangan kandungan uap air ini biasanya digambarkan dalam
bentuk grafik, dengan memplot kandungan uap air sebagai suatu fungsi aw atau
dalam suatu bentuk persamaan (Fontana, 2000).
Ada lebih dari 70 persamaan yang telah dikembangkan untuk
memprediksi kesetimbangan kandungan uap air ini. Model GAB
(Guggenheim-Anderson-de Boer) merupakan salah satu model yang telah
diterima secara luas untuk bahan dengan aktivitas air dari 0,1 sampai 0,9.
m= C1 k m0 aw
(1- k aw)(1- k aw+ C1 k aw)
Di mana C1 dan k adalah suatu konstanta dan mo adalah kadar uap air lapisan
non-linear terkomputerisasi ataupun dalam bentuk persamaan polinomial (Fontana,
2000).
2.4Stabilitas Fisik Cangkang Kapsul Umum 2.4.1 Warna
Warna, merupakan salah satu aspek yang mempengaruhi penilaian
konsumen terhadap kualitas produk. Warna suatu bahan dapat berasal dari
warna alamiahnya atau warna yang terjadi selama proses pengolahannya
(Morales dan van Boekoel, 1998).
Temperatur dan kadar uap air yang relatif tinggi selama proses
pengolahan dan penyimpanan yang berkepanjangan merupakan salah satu
faktor utama yang menyebabkan terjadinya reaksi pengcoklatan (enzimatik dan
non-enzimatik) (Bell dan Labuza, 1992).
Reaksi pengcoklatan adalah suatu reaksi dimana suatu bahan berubah
menjadi coklat, baik melalui proses enzimatik maupun non-enzimatik.
Pengcoklatan enzimatik ini melibatkan polifenol oksidase atau enzim lain yang
menghasilkan melanin, sehingga menimbulkan warna coklat. Sedangkan
pengcoklatan non-enzimatik dapat menimbulkan warna coklat tanpa adanya
aktivitas enzim (Marshall, et al., 2000).
Reaksi Maillard merupakan suatu reaksi kimia pengcoklatan
non-enzimatik antara gula pereduksi dengan protein atau asam amino. Tergantung
pada jenis bahan dan jalannya reaksi, perubahan warna yang terjadi bisa dari
kuning lemah sampai coklat gelap. Banyak faktor yang mempengaruhi reaksi
Maillard, seperti temperatur, aktivitas air, pH, kadar uap air dan komposisi
2.4.2 Kerapuhan
Perlu diketahui bahwa cangkang kapsul bukan tidak reaktif, secara
fisika atau kimia. Perubahan kondisi penyimpanan seperti temperatur dan
kelembaban dapat mempengaruhi sifat kapsul. Dengan terjadinya kenaikan
temperatur dan kelembaban dapat menyebabkan kapsul mengikat/melepaskan
uap air. Sebagai akibatnya kapsul dapat menjadi rapuh atau lunak (Margareth,
et al., 2009).
Laju pengeringan kapsul juga mempengaruhi kekerasan dan kerapuhan
kapsul, kemampuan pelarutan, dan kecenderungan untuk melekat satu sama
lain. Kadar uap air yang rendah pada kapsul dapat menghambat pertumbuhan
mikroba. Jika kadar uap air pada kapsul gelatin kurang dari 10%, kapsul
cenderung menjadi rapuh, dan sebaliknya jika kadar air lebih tinggi dari 18%
kapsul gelatin melunak. Kondisi penyimpanan yang direkomendasikan untuk
bentuk sediaan kapsul gelatin berkisar 15 - 30°C dan 30% - 60% kelembaban
relatif (RH) (Margareth, et al., 2009).
Perubahan kerapuhan kapsul oleh kelembaban relatif telah dipelajari
oleh Kontny dan Mulski (1989). Pemantauan terhadap karakteristik kapsul
yang disimpan pada kelembaban yang bervariasi membuktikan bahwa
kelembaban merupakan salah satu parameter yang penting dalam pembuatan
dan penyimpanan kapsul. Kriteria yang diterima bahwa kerapuhan kapsul yang
signifikan tidak boleh terdeteksi pada kapsul yang disimpan pada kelembaban
uap air gelatin dan sifat kapsul gelatin keras dapat dilihat pada Gambar 2.3.
(Kontny dan Mulski, 1989).
Gambar 2.3. Kelembaban relatif (RH), kandungan uap air gelatin dan sifat kapsul gelatin keras (Kontny dan Mulski, 1989)
2.5 Disolusi
Uji disolusi yaitu uji pelarutan in vitro mengukur laju dan jumlah
pelarutan obat dalam suatu media “aqueous” dengan adanya satu atau lebih
bahan tambahan yang terkandung dalam produk obat. Pelarutan obat
merupakan bagian penting sebelum kondisi absorbsi sistemik (Shargel dan
Andrew, 1988). Faktor-faktor yang mempengaruhi disolusi dibagi atas 3
kategori yaitu:
a. Faktor-faktor yang berhubungan dengan sifat fisikokimia obat, meliputi:
i. Efek kelarutan obat. Kelarutan obat dalam air merupakan faktor utama
dalam menentukan laju disolusi. Kelarutan yang besar menghasilkan
ii. Efek ukuran partikel. Ukuran partikel berkurang dapat memperbesar
luas permukaan obat yang berhubungan dengan medium, sehingga
laju disolusi meningkat.
b. Faktor-faktor yang berhubungan dengan sifat fisikokimia obat, meliputi:
i. Efek kelarutan obat. Kelarutan obat dalam air merupakan faktor utama
dalam menentukan laju disolusi. Kelarutan yang besar menghasilkan
laju disolusi yang cepat.
ii. Efek ukuran partikel. Ukuran partikel berkurang dapat memperbesar
luas permukaan obat yang berhubungan dengan medium, sehingga
laju disolusi meningkat.
c. Faktor-faktor yang berhubungan dengan sediaan obat, meliputi:
i. Efek formulasi. Laju disolusi suatu bahan obat dapat dipengaruhi bila
dicampur dengan bahan tambahan. Bahan pengisi, pengikat dan
penghancur yang bersifat hidrofil dapat memberikan sifat hidrofil
pada bahan obat yang hidrofob, oleh karena itu disolusi bertambah,
sedangkan bahan tambahan yang hidrofob dapat mengurangi laju
disolusi.
ii. Efek faktor pembuatan sediaan. Metode granulasi dapat mempercepat
laju disolusi obat-obat yang kurang larut. Penggunaan bahan pengisi
yang bersifat hidrofil seperti laktosa dapat menambah hidrofilisitas
bahan aktif dan menambah laju disolusi.
i. Tegangan permukaan medium disolusi. Tegangan permukaan
mempunyai pengaruh nyata terhadap laju disolusi bahan obat.
Surfaktan dapat menurunkan sudut kontak, oleh karena itu dapat
meningkatkan proses penetrasi medium disolusi ke matriks. Formulasi
tablet dan kapsul konvensional juga menunjukkan penambahan laju
disolusi obat-obat yang sukar larut dengan penambahan surfaktan
kedalam medium disolusi.
ii. Viskositas medium. Semakin tinggi viskositas medium, semakin kecil
laju disolusi bahan obat.
iii. pH medium disolusi. Larutan asam cenderung memecah tablet sedikit
lebih cepat dibandingkan dengan air, oleh karena itu mempercepat laju
disolusi (Gennaro, 2000). Obat-obat asam lemah disolusinya kecil
dalam medium asam, karena bersifat nonionik, tetapi disolusinya
besar pada medium basa karena terionisasi dan pembentukan garam
yang larut (Martin, dkk., 1993).
United States Pharmacopeia (USP) XXXII memberi beberapa metode
resmi untuk melaksanakan uji pelarutan yaitu:
a. Metode Keranjang (Basket)
Metode keranjang terdiri atas keranjang silindrik yang ditahan oleh
tangkai motor. Keranjang menahan cuplikan dan berputar dalam suatu labu
bulat yang berisi media pelarutan. Keseluruhan labu tercelup dalam suatu
bak yang bersuhu konstan 37ºC. Kecepatan berputar dan posisi keranjang
standar kalibrasi pelarutan untuk meyakinkan bahwa syarat secara
mekanik dan syarat operasi telah dipenuhi.
b. Metode Dayung (Paddle)
Metode dayung terdiri atas suatu dayung yang dilapisi khusus,
yang berfungsi memperkecil turbulensi yang disebabkan oleh pengadukan.
Dayung diikat secara vertikal ke suatu motor yang berputar dengan suatu
kecepatan yang terkendali. Tablet atau kapsul diletakkan dalam labu
pelarutan yang beralas bulat yang juga berfungsi untuk memperkecil
turbulensi dari media pelarutan. Alat ditempatkan dalam suatu bak air
yang bersuhu konstan, seperti pada metode basket dipertahankan pada
37ºC. Posisi dan kesejajaran dayung ditetapkan dalam USP. Metode
dayung sangat peka terhadap kemiringan dayung. Pada beberapa produk
obat, kesejajaran dayung yang tidak tepat secara drastis dapat
mempengaruhi hasil pelarutan. Standar kalibrasi pelarutan yang sama
digunakan untuk memeriksa peralatan sebelum uji dilaksanakan.
c. Metode Disintegrasi yang Dimodifikasi
Metode ini dasarnya memakai disintegrasi USP “basket and rack” dirakit
untuk uji pelarutan. Bila alat ini dipakai untuk pelarutan maka cakram
dihilangkan. Saringan keranjang juga diubah sehingga selama pelarutan
partikel tidak akan jatuh melalui saringan. Metode ini jarang digunakan
dan dimasukkan dalam USP untuk suatu formulasi obat lama. Jumlah
pengadukan dan getaran membuat metode ini kurang sesuai untuk uji
2.6 Natrium Diklofenak 2.6.1 Uraian bahan
Rumus Bangun :
Gambar 2.4. Rumus bangun natrium diklofenak (Depkes RI, 1995) Rumus Molekul : C14H10Cl2NNaO2
Nama Kimia : Asam benzenasetat, 2-[(2,6-diklorofenil)amin] -
garam monosodium
Nama lain : Natrium [o-(2,6-dikloroanilino)fenil]asetat
Berat Molekul : 318,13 (USP XXXII, 2009).
Pemerian : Serbuk kristal putih atau sedikit kuning, agak
higroskopis
Kelarutan : Sedikit larut dalam air, mudah larut dalam
metanol, larut dalam etanol (9%), sedikit larut
dalam aseton (British Pharmacopoeia, 2009).
pKa : 4,2 (Moffats, 2005).
2.6.2 Farmakologi natrium diklofenak
Diklofenak mempunyai aktivitas analgesik, antipiretik, dan antiradang
Natrium diklofenak berpotensi terhadap COX-2 lebih besar daripada
diklofenak tampaknya dapat mengurangi konsentrasi intrasel dari asam
arakidonat bebas dalam leukosit, mungkin dengan mengubah pelepasan
ataupun penyerapannya. Selektivitas dari diklofenak terhadap COX-2
menyerupai celecoxib. Namun, efek merugikan terhadap gastrointestinal serius
tidak berbeda antara celecoxib dan diklofenak (Grosser, et al., 2011).
2.6.3 Farmakokinetika natrium diklofenak
Diklofenak secara cepat diserap ketika diberikan sebagai larutan oral,
tablet salut gula, suppositoria rektal, atau dengan injeksi intramuskular.
Penyerapannya lebih lambat ketika diberikan sebagai tablet salut enterik,
terutama saat bentuk sediaan tersebut diberikan bersamaan dengan makanan.
Walaupun diklofenak yang diberikan secara oral diserap sempurna, diklofenak
akan mengalami metabolisme lintas pertama sehingga sekitar 50% dari obat
mencapai sirkulasi sistemik dalam bentuk yang tidak berubah (Sweetman,
2009). Diklofenak juga diserap secara perkutan. Pada konsentrasi terapetik
sekitar 99% obat terikat pada protein plasma. Diklofenak menembus cairan
sinovial di mana konsentrasinya dapat bertahan bahkan didistribusikan ke
dalam ASI. Waktu paruh plasmanya sekitar 1 hingga 2 jam. Diklofenak
dimetabolisme menjadi 4’-hidroksidiklofenak, 5-hidroksidiklofenak,
3’-hidroksidiklofenak dan 4’,5-di3’-hidroksidiklofenak. Diklofenak diekskresikan
dalam bentuk glukoronida dan konjugat sulfat, sebagian besar dalam urin
(sekitar 60%) juga dalam empedu (sekitar 35%); kurang dari 1% diekskresikan
2.7 Kapsul
Kapsul adalah sediaan padat dimana obat ditutup dalam suatu cangkang
yang keras maupun lunak. Cangkang tersebut biasanya dibuat dari gelatin;
tetapi cangkang tersebut juga dapat dibuat dari pati ataupun zat lain yang
cocok. Kapsul cangkang keras berukuran dari No. 5, yang paling kecil, hingga
No. 000, yang paling besar, kecuali untuk ukuran penggunaan veteriner.
Bagaimanapun, ukuran No. 00 merupakan ukuran terbesar yang secara umum
dapat diterima oleh pasien (USP XXXII, 2009). Kapsul tidak berasa, mudah
pemberiannya, mudah pengisiannya tanpa persiapan atau dalam jumlah yang
besar secara komersil. Didalam praktek peresepan, penggunaan kapsul gelatin
keras diperbolehkan sebagai pilihan dalam meresepkan obat tunggal atau
kombinasi obat pada perhitungan dosis yang dianggap baik untuk pasien secara
individual. Fleksibilitasnya lebih menguntungkan daripada tablet. Beberapa
pasien menyatakan lebih mudah menelan kapsul daripada tablet, oleh karena
itu lebih disukai bentuk kapsul bila memungkinkan. Pilihan ini telah
mendorong pabrik farmasi untuk memproduksi sediaan kapsul dan di pasarkan,
walaupun produknya sudah ada dalam bentuk sediaan tablet (Gennaro, 2000).
2.7.1 Kapsul delayed-release
Kapsul dapat disalut, atau, lebih umumnya, granul yang dienkapsulasi
dapat disalut untuk menahan pelepasan obat dalam cairan lambung dimana
suatu penundaan penting untuk mengurangi masalah yang mungkin terjadi
pada inaktivasi obat atapun iritasi mukosa lambung. Istilah “delayed-release”
untuk menunda pelepasan dari bahan obat hingga kapsul melewati lambung
(USP XXXII, 2009). Tabel penerimaan beberapa sediaan delayed release dapat
dilihat pada Tabel 2.1.
Tabel 2.1. Tabel penerimaan sediaan delayed release menurut USP XXXII No. Sediaan Medium Persyaratan
1 Kapsul delayed
release Aspirin
Asam Terdisolusi tidak lebih dari 10% Basa pH
6,8
Terdisolusi tidak kurang dari 75% dalam waktu 90 menit
2
Tablet delayed release Natrium diklofenak
Asam Terdisolusi tidak lebih dari 10% Basa pH
6,8
Terdisolusi tidak kurang dari 75% dalam waktu 45 menit
3
Tablet delayed release
Diritromisin
Asam Terdisolusi tidak lebih dari 10% Basa pH
6,8
Terdisolusi tidak kurang dari 80% dalam waktu 45 menit
4
Kapsul delayed release
Eritromisin
Asam Terdisolusi tidak lebih dari 10% Basa pH
6,8
Terdisolusi tidak kurang dari 80% dalam waktu 120 menit
5
Kapsul delayed release
Lansoprazole
Asam Terdisolusi tidak lebih dari 10% Basa pH
6,8
Terdisolusi tidak kurang dari 80% dalam waktu 60 menit
6
Kapsul delayed release
Omeprazole
Asam Terdisolusi tidak lebih dari 15% Basa pH
7,6
Terdisolusi tidak kurang dari 75% dalam waktu 30 menit
7
Tablet delayed release
Sulfasalazin
Asam Terdisolusi tidak lebih dari 10% Basa pH
7,5
Terdisolusi tidak kurang dari 85% dalam waktu 60 menit
8
Kapsul delayed release
Pankrealipase
Asam Terdisolusi tidak lebih dari 10%
Basa pH 6 Terdisolusi tidak kurang dari 75% dalam waktu 60 menit
2.8 Natrium Alginat
Natrium alginat merupakan produk pemurnian karbohidrat yang
tidak larut dalam etanol dan eter. Alginat ini diperoleh dari spesies Macrocystis
pyrifera, Laminaria, Ascophyllum dan Sargassum. Struktur alginat dapat
dilihat pada Gambar 2.5(Belitz dan Grosch, 1987).
Gambar 2.5. Struktur alginat
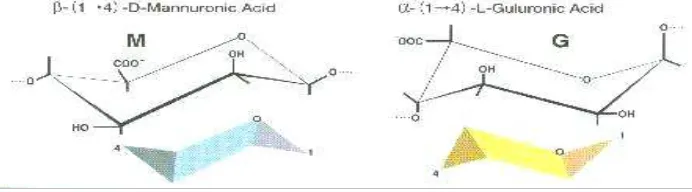
Asam alginat adalah kopolimer biner yang terdiri dari residu β
-D-mannuronat (M) dan α-L-asam guluronat (G) yang tersusun dalam blok-blok
yang membentuk rantai linear (Grasdalen, et al., 1979). Kedua unit tersebut
berikatan pada atom C1 dan C4 dengan susunan homopolimer dari
masing-masing residu (MM dan GG) dan suatu blok heteropolimer dari dua residu
(MG). Struktur G: α- L asam guluronat dan M: β- D asam mannuronat dapat
dilihat pada Gambar 2.6. (Thom, et al., 1980).
Gambar 2.6. Struktur G: α-l asam guluronat dan M: β-d asam mannuronat Asam alginat tidak larut dalam air, karena itu yang digunakan dalam
dari natrium alginat adalah mempunyai kemampuan membentuk gel dengan
penambahan larutan garam-garam kalsium seperti kalsium glukonat, kalsium
tartrat dan kalsium sitrat (Thom, et al., 1982). Pembentukan gel alginat dengan
ion kalsium, disebabkan oleh adanya ikatan silang membentuk khelat antara
ion kalsium dan anion karboksilat pada blok G-G melalui mekanisme antar
rantai. Natrium alginat mempunyai rantai poliguluronat menunjukkan sifat
pengikatan ion kalsium yang lebih besar (Morris, et al., 1980).
Untuk kepentingan farmasetik digunakan natrium alginat, dimana
larutannya dalam air bereaksi netral sampai asam lemah. Sediaan alginat paling
stabil pada daerah pH 6-7, pada pH 4,5 asam bebasnya akan mengendap.
Pemanasan yang kuat dan lama, terutama >70oC dihindari, karena akan mengalami kehilangan viskositas akibat terjadinya polimerisasi. Sediaan
disimpan dingin dan dilindungi dari cahaya dalam wadah tertutup baik (Voight,
1994).
Di Laboratorium Farmasi Fisik Fakultas Farmasi USU dalam beberapa
tahun terakhir telah dikembangkan kapsul yang tahan terhadap asam lambung.
Cangkang kapsul ini dibuat dari natrium alginat dengan kalsium klorida
menggunakan cetakan. Telah terbukti bahwa cangkang kapsul alginat tahan
atau tidak pecah dalam cairan lambung buatan (pH 1,2). Kapsul mengembang
dan pecah dalam cairan usus buatan yaitu pH 4,5 dan pH 6,8 (Bangun, dkk.,
2005)
Utuhnya cangkang kapsul kalsium alginat di dalam medium pH 1,2
masih utuh, sedangkan pelepasan kalsium kemungkinan berasal dari kalsium
yang terperangkap dalam kapsul dan terikat dengan manuronat saja. Hal itu
berarti kalsium guluronat yang bertanggung jawab terhadap keutuhan kapsul di
dalam medium pH 1,2 (Bangun, dkk., 2005).
Cangkang kapsul kalsium alginat dapat mengembang dan pecah di
dalam medium pH 4,5 dan 6,8 (cairan usus buatan). Hal ini disebabkan terjadi
pertukaran ion kalsium dari kalsium alginat (kalsium guluronat) dengan ion
natrium yang terdapat pada cairan usus buatan, sehingga terbentuk natrium
alginat (natrium guluronat). Pembentukan natrium alginat pada kapsul dapat
menyebabkan kapsul bersifat hidrofilik, sehingga mudah menyerap air,