ABSTRAK
Telah dilakukan percobaan sol liofi yang termasuk dalam sistem koloid. Sistem koloid ini merupakan suatu bentuk campuran (sistem dispersi) dari dua atau lebih zat yang bersifat homogen, namun memiliki ukuran partikel terdispersi yang cukup besar. Percobaan ini bertujuan untuk mempelajari sifat sol lofil dan menentukan titik isoelektrik melalui pengamatan viskositas. Percobaan ini untuk mengetahui sifat sol liofiil yang menggunakan bahan-bahan seperti akuades, asam sitrat, binatrium hidrogen fosfat dan juga gelatin serta menggunakan metode viskometer Ostwald. Hasil percobaan ini dengan pH berturut-turut 2,2 ; 3,0 ; 4,4 ; 5,0 ; 6,0 ; dan 7,0 ; diperoleh viskositas adalah sebesar 1,352 kg/m.s ;0,939 kg/m.s ;1,335 kg /m. s ;1,443 kg/m.s ;1,305 kg/m.s ;1,301 kg/m. Percobaan ini diperoleh titik isoelektiknya yaitu pada pH 3.
Kata Kunci: Gelatin, Titik Isoeletrik, Viskometer Oswald dan Sol liofil.
I. Data Pengamatan
larutan (gram) t1 t2 t3 1 Air 26,39 26,23 26,12 47,88 2 2 51,47 51,64 51,48 48,11 3 3 35,77 35,91 35,77 48,16 4 4 35,21 35,13 34,93 48,11 5 5 33,93 34,06 34,42 48,13 6 6 34,15 34,56 34,38 48,13 7 7 34,72 35,41 35,31 48,14
II. Hasil dan Pembahasan 2.1 Pembahasan
Koloid merupakan campuran dari dua atau lebih zat yang salah satunya tersuspensi sebagai jumlah besar partikel yang sangat kecil dalam fasa kedua. Zat yang terdispersi dari medium penyangga dapat berupa kombinasi gas, cairan atau padatan (Oxtoby, 2001). Adapun jenis-jenis koloid berdasarkan fasa terdispersi dengan fasa terdissopsi antara lain (Martin, 1983) :
1. Koloid liofil yaitu koloid yang memiliki daya tarik kuat dengan medium pendispersinya sehingga sulit stabil. Jika medium air disebut juga fasa koloid liofil, karena afinitasnya terhadap dispersi, bahan-bahan tersebut membentuk dispersi koloid. Jadi koloid liofil merupkan koloid yang diperoleh dengan melarutkan bahan dengan pelarut yang digunakan.
2. Koloid liofob merupakan koloid yang daya tarikna kecil terhadap medium pendispersinya sehingga tidak stabil. Pada mediumnya air disebut koloid hidrofob. Hal ini karena tidak adanya selimut pelarut disekeliling partikel.
3. Koloid gabungan yaitu zat yang aditif permukaan yang memiliki dua daerah yng melakukan aktivitas larutan aktif dalam molekul air yang sama dengan suatu medium cair dengan komponen yang rendah.
Sistem koloid, baik fase terdispersi maupun media pendispersi dapat berupa zat padat, cair atau gas. Berdasarkan hubungan antara kedua fase tersebut, berikut ada beberapa sistem koloid ( Soekardjo, 2002) :
Fase dispersi
Medium
dispersi Nama Contoh
Padat Cair Sol Au, As2s3,S dan H2O
Cair Cair Emulsi Air dalam benzen
Padat Padat Sol padat Zat warna dalam gelas Cair Padat Emulsi padat Aspal, kuarsa
Gas Padat Busa padat Batu apung, lava
Padat gas Aerosol padat Asap, uap NH4Cl
Sol merupakan sistem koloid yang fase terdispesinya zat padat dan medium pendispersinya zat cair. Berdasarkan kemampuan fase terdispersi untuk menarik medium pendispersinya, sol dibedakan atas sol liofil dan sol liofob. Sol liofil mempunyai fase terdipersi yang suka dengan medium pendispersinya sedangkan fase terdispersinya sol liofob tidak suka terhadap medium pendispersinya (Sumardjo, 2006).
Sistem koloid sangat penting dalam kehidupan sehari-hari. Sebagai contoh, hampir semua bahan pangan mengandung partikel dengan ukuran koloid, seperti protein, karbohidrat, dan lemak. Emulsi seperti susu juga termasuk koloid. Dalam bidang farmasi, kebanyakan produknya juga berupa koloid, misalnya krim, salep adalah emulsi. Bidang industri yaitu cat, semen, dan industri karet untuk membuat ban semuanya melibatkan sistem koloid. Semua bentuk seperti spray untuk serangga, cat, hair spray dan sebagainya adalah juga koloid. Berdasarkan peranan yang cukup penting dalam kehidupan sehari-hari maka dilakukan percobaan sol liofil dengan tujuan agar dapat mempelajari sifal sol liofil dan menentukan titik isoelektrik melalui pengamatan viskositas.
Percobaan ini dimulai dengan menyiapkan semua bahan yang diperlukan pada percobaan ini yaitu disiapkan 5 gram gelatin dalam 6 tempat, kemudian dibuat larutan Na2HPO4 0,2 M dengan cara melarutkan 1,42 gram padatan Na2HPO4 dalam 50 mL. Selain itu, dibuat juga larutan asam sitrat 0,1 M dengan cara melarutkan 0,96 gram padatan asam sitrat dalam 50 mL.
Setelah semua bahan telah disiapkan. Selanjutnya, dibuat larutan dalam 7 buah gelas beaker dengan variasi pH dimana masing-masingnya ditambahkan larutan Na2HPO4 0,2 M dan asam sitrat 0,1 M sesuai volume yang telah ditetapkan yaitu :
Perlakuan I : 0,20 mL larutan Na2HPO4 0,2 M + 9,80 Asam sitrat 0,1 M Perlakuan II : 2,06 mL larutan Na2HPO4 0,2 M + 7,94 Asam sitrat 0,1 M Perlakuan III : 3,86 mL larutan Na2HPO4 0,2 M + 6,14 Asam sitrat 0,1 M Perlakuan IV : 5,15 mL larutan Na2HPO4 0,2 M + 4,85 Asam sitrat 0,1 M Perlakuan V : 6,32 mL larutan Na2HPO4 0,2 M + 3,68 Asam sitrat 0,1 M Perlakuan VI : 8,24 mL larutan Na2HPO4 0,2 M + 1,76 Asam sitrat 0,1 M
Gambar 2.2 Pemipetan Na2HPO4 dan C6H8O7
Kemudian, pada masing-masing perlakuan ditambahkan 0,5 gram gelatin. Percobaan ini sol liofil digunakan gelatin ini berperan sebagai fase yang
terdispersi dan gelatin untuk membentuk sol sedangkan asam sitrat dan Na2HPO4 sebagai fasa pendispersinya. Fasa terdispersi yaitu zat terlarutnya sedangkan medium pendispersi yaitu zat terlarutnya dengan pH tertentu. Adapun pH campuran Na2HPO4 dan asam sitrat yang dipakai adalah sebagai berikut : 2,2 ; 3,0 ; 4,4 ; 5,0 ; 6,0 ; dan 7,0. Tujuan dari variasi pH adalah untuk menentukan titik isoelektrik melalui viskositas sol liofil.
Gambar 2.3 Saat ditambahkan gelatin dan pemisahan larutan dengan busanya
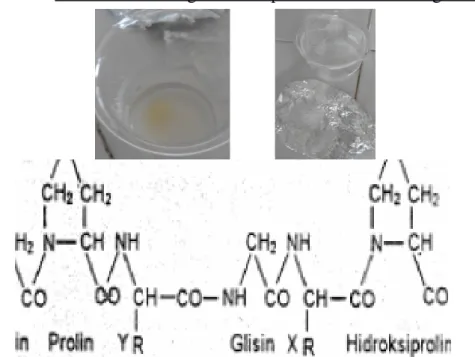
Gelatin adalah derivat protein dari serat kolagen yang ada pada kulit, tulang, dan tulang rawan. Gelatin mudah larut pada suhu 71,1oC dan cenderung membentuk gel pada suhu 48,9 oC. Pemanasan yang dilakukan untuk melarutkan gelatin sekurang-kurangnya 49oC atau biasanya pada suhu 60 – 70oC. Gelatin memiliki sifat dapat berubah secara reversible dari bentuk sol ke gel, membengkak atau mengembang dalam air dingin, dapat membentuk film, mempengaruhi viskositas suatu bahan, dan dapat melindungi sistem koloid (Miskah,dkk. 2010). Adapun struktur dari gelatin yaitu :
Gelatin juga bersifat amfoter artinya gelatin dapat larut dalam larutan asam maupun basa sehingga dalam lingkungan asam, gelatin terionisasi bermuatan positif dan dalam lingkungan basa, gelatin terionisasi bermutan negatif. Reaksi dalam larutan asam dan basa yaitu :
Asam : HOOC-R-NH2 + H+ HOOC-R-NH3+ Basa : HOOC-R-NH2 + OH- -OOC-R-NH2 + H2O
Selanjutnya, larutan tersebut dipanaskan hingga gelatinnya larut. Pemanasan dilakukan agar mempercepat reaksinya. Setelah itu, dipindahkan larutan tersebut ke dalam labu ukur 50 mL dan ditepatkan. Larutan tersebut kemudian diukur pH nya menggunakan pH meter. Sehingga dari percobaan ini diperoleh pH sebesar : 2 ;3 ;4 ;5 ;6 ; dan 7. Adanya variasi pH ini akan dapat menunjukkan titik isoelektriknya.
Kemudian larutan sol liofil tersebut diukur massa jenis dengan menggunakan piknometer yang 25 mL. Piknometer adalah alat yang digunakan untuk mengukur nilai massa jenis atau densitas dari fluida (While,1988). Pertama-tama timbang piknometer kosong, lalu diisi sol liofil dan ditimbang lagi. Untuk mendapatkan berat sol liofil, maka berat piknometer yang berisi sol liofil dikurangi dengan berat piknometer kosong. Sehingga massa jenis berat sol liofil dibagi dengan volume piknometer (dalam percobaan ini 25 mL). Percobaan ini diperoleh massa jenis masing-masing yaitu sebesar 0,9904 gr/mL ;0,9900 gr/mL ;0,9892 gr/mL ;0,9912 gr/mL 0,9888 gr/mL ;0,9904 gr/mL . Massa jenis air adalah 0,9904 gr/mL . Secara teori, massa jenisnya akan berbanding terbalik dengan pH.
Selanjutnya, di ukur viskositasnya menggunakan viskometer Ostwald. Konversi konstan C untuk penentuan viskositas kinetik (Yaitu, μ / ρ) yang disediakan oleh produsen untuk viskometer Ostwald adalah 0,01 (tanpa kisaran suhu tertentu). Dengan konstanta C, viskositas kinetik bisa ditentukan setelah waktu transit AT adalah diukur. Viskometer Ostwald, menggunakan tabung au-berbentuk dengan dua tabung vertical (Lee,dkk. 2012). Penggunaan viskometer Ostwald yaitu dengan cara dipipetkan larutan tadi ke dalam viskometer. Kemudian
dihisap larutan tersebut dengan menggunakan bulb hingga melewati batas m. Siapkan stopwatch, lalu kendurkan larutan tersebut dan biarkan menalir melewati batas n. Kemudian dicatat waktu yang diperlukan oleh larutan untuk mengalir dari batas m ke n.
Gambar 2.4 Viskometer dan Stopwatch
Viskositas adalah tahanan yang timbul karena adanya gesekan antara molekul-molekul didalam zat cair yang mengalir. Percobaan ini, di peroleh viskositas pada variasi pH tersebut yaitu sebesar 1,352 kg/m.s ;0,939 kg/m.s ; 1,335 kg /m. s ;1,443 kg/m.s ;1,305 kg/m.s ;1,301 kg/m.s Gelatin memiliki viskositas yang lebih besar dibandingkan dengan viskositas air. Percobaan ini di peroleh viskositas air sebesar 0,798 kg/m.s.
Setelah mengetahui waktu yang diperlukan untuk mengalir dari batas m ke n sebanyak 7 kali, kemudian larutan yang berada dalam viscometer Ostwald tersebut dimasukkan kedalam piknometer .
Hasil perhitungan diperoleh hubungan antara pH dengan viskositas yaitu berbanding terbalik dimana semakin rendah pH maka larutannya akan semakin kental atau viskositasnya semakin tinggi. Akan tetapi pada percobaan ini di peroleh hasil yang berbanding lurus antara massa jenis dan pH. Hal ini dikarenakan kurangnya ketelitian dalam pengukuran menggunakan viskometer Ostwald.
Berdasarkan grafik, diperoleh titik isoelektriknya terletak pada pH 3. Karena pada pH 3 mempunyai viskositas yang rendah, dan viskositas sol liofil tersebut turun secara drastis, kemudian viskositas sol liofil selanjutnya naik lagi, seiring dengan naiknya pH sol liofil. Titik isoelektrik adalah derajat keasaman atau pH ketika suatu makromolekul bermuatan nol akibat bertambahnya proton atau kehilangan muatan oleh reaksi asam-basa. Pada koloid, jika pH sama dengan titik isoelektrik, maka sebagian atau semua muatan pada partikelnya akan hilang selama proses ionisasi terjadi. Jika pH berada pada kondisi di bawah titik isoelektrik, maka matan partikel koloid akan bermuatan positif. Sebaliknya jika pH berada di atas titik isoelektrik maka muatan koloid akan berubah menjadi netral atau bahkan menjadi negatif (Anonim A, 2014).
II.2 Perhitungan 1. Pembuatan larutan
a. Larutan natrium hidrogen fosfat M = massaMr X volume1000 massa = M x Mr x volume1000 = 0,2 M x 142 g molx 50 mL 1000 = 1,42 gram b. Larutan asam sitrat
M = massaMr X volume1000 massa = M x Mr x volume1000 = 0,1 M x 192 g molx 50 mL 1000 = 0,96 gram 2. Penentuan massa jenis
a. Massa jenis air
Diketahui : V. Air = 25 mL m. pikno + air = 47,89 mL m. pikno kosong = 23,0292 mL air = (m. pikno+air )−(m. piknokosong) V . air = g mL = (47,88 mL)−(23,12 mL)25 mL = 0,9904 mLg b. Massa jenis sol
sol = (m. piko+sol)−(m. piknokosong )V . air = mLg
pH 2 sol = 0,9904 mLg pH 3 sol = 0,9900 g mL pH 4 sol = 0,9892 mLg pH 5 sol = 0,9912 mLg pH 6 sol = 0,9888 mLg pH 7 sol = 0,9904 mLg
3. Penentuan viskositas tiap pH 4. Diketahui : . Air = 0,798 m. skg
5. t. rata-rata air = t 1+t 2+t 33 = sekon
6. = 26,39+26,23+26,123 = 26,25 sekon 7. t. rata-rata sol = t 1+t 2+t 33 = sekon
pH 2 t. rata-rata = 51,53 sekon pH 3 t. rata-rata = 35,82 sekon pH 4 t. rata-rata = 35,09 sekon pH 5 t. rata-rata = 37,85 sekon pH 6 t. rata-rata = 34,30 sekon pH 7 t. rata-rata = 34,15 sekon
Sehingga viskositas sol dapat dihitung dengan rumus :
. Sol = t . air x . air X t . sol x . sol . Air = m. skg
pH 2 . Sol = 1,352 kg m. s pH 3 . Sol = 0,939 kg m. s pH 4 . Sol = 1,335 kg m. s pH 5 . Sol = 1,443 kg m. s pH 6 . Sol = 1,305 kg m. s pH 7 . Sol = 1,301 kg m. s
II.3 Jawaban Pertanyaan
1. Sifat-sifat khusus disperse koloid yaitu Efek Tyndall, Gerak Brown, Adsorpsi dan Elektroforesis. Perbedaan sifat-sifat ini dengan suatu larutan yaitu, pada efek Tyndall pertikel koloid akan menghamburkan cahaya yang melewatinya sedangkan partikel larutan terlalu kecil untuk memantulkan cahaya. Pada gerak Brown partikel koloid dapat bergerak acak didalam medium pendispersinya sedangkan pada larutan tidak terdapat dispersi. Pada Adsorpsi materi bentuk koloid meempunyai luas permukaan yang sangat besar, sehingga dapat menarik zat-zat asing untuk menempel pada permukaannya. Elektrforesis adalah pergerakan partikel koloid pada pengaruh medan listrik. 2. Factor yang mempengaruhi kestabilan sol liofil adalah partikel zat padat yang
tersolvasi atau zat padat yang larut memiliki selubung molekul zat pelarut pada permukaannya. Jika pelarut atau medium pendispersinya adalah air maka disebut terhidrasi.
3. Zwitter ion adalah suatu senyawa yang mempunyai gugus fungsi yang bersifat asam dan basa.
4. Viskositas sol liofil lebih besar daripada sol liofob, hal ini dikarenakan sol liofil memiliki viskositas yang lebih besar daripada medium pendispersinya, sedangkan sol liofob viskositasnya hamper sama dengan medium pendispersinya.
II.4 Grafik
1 2 3 4 5 6 7 8 0 0.5 1 1.5 2 f(x) = 0.03x + 1.16 R² = 0.08
hubungan antara viskositas terhadap pH
y
Linear (y)
pH Viskositas
III. Kesimpulan dan Saran 7.1 Kesimpulan
Hasil percobaan dengan pH berturut-turut 2,2 ; 3,0 ; 4,4 ; 5,0 ; 6,0 ; dan 7,0 ; diperoleh viskositas adalah sebesar 1,352 kg/m.s ;0,939 kg/m.s ;1,335 kg /m. s ;1,443 kg/m.s ;1,305 kg/m.s ;1,301 kg/m.s dan massa jenisnya adalah 0,9904 gr/mL ;0,9900 gr/mL ;0,9892 gr/mL ;0,9912 gr/mL 0,9888 gr/mL ;0,9904 gr/mL . Massa jenis air adalah 0,9904 gr/mL. Titik isoelektrik pada percobaan ini terletak pada larutan yang mempunyai pH 3.
7.2 Saran
Saran untuk percobaan selanjutnya disarankan untuk mengganti gelatin dengan amilum, dilakukan variasi pH larutan dan konsentrasi larutan dengan skala berjauhan untuk melihat perbandingan hasil dari beberapa percobaan yang sudah dilakukan dan agar dapat menggunakan fasa pendispersinya yang lain selain Na2HPO4.
DAFTAR PUSTAKA
Anonim A. 2014. Http://Id.Wikipedia.Org/Wiki/Titik_Isoelektrik. Diakses Pada Tanggal 23 April 2016
Lee, D. H., Jung, J. M., Kim, S. Y., Kim, K. T., & Cho, Y. I. 2012.
Comparison Tests For Plasma Viscosity Measurements. International Communications In Heat And Mass Transfer, 39(10), 1474-1477.
Martin,A.1983. Farmasi Fisik. UI Press. Jakarta.
Miskah, S., Ramadianti, I. M., & Hanif, A. F. 2013. Pengaruh Konsentrasi
CH3COOH & HCl Sebagai Pelarut dan Waktu Perendaman pada
Pembuatan Gelatin Berbahan Baku Tulang/Kulit Kaki Ayam. Jurnal
Teknik Kimia, 17(1).
Oxtoby, D.W. Gillis, H.P dan Nachtrieb, N. H.2001. Prinsip-Prinsip Kimia Modern. Erlangga. Jakarta.
Soekardjo. 2002. Kimia Dasar. UGM-Press. Yogyakarta
Sumardjo, D.2006. Pengantar Kimia Buku Panduan Kuliah Mahasiswa Kondekteran. Buku Kedokteran EGC. Jakarta.
While, Frank M. 1988. Mekanika Fluida Edisi Ke-2 Jilid 1. Jakarta : Erlangga.