BAB II
TINJAUAN PUSTAKA
2.1 Sabun
2.1.1 Pengertian Sabun
Sabun adalah senyawa garam dari asam-asam lemak tinggi, seperti
natrium stearat, C17H35COO-Na+. Aksi pencucian dari sabun banyak dihasilkan
dari kekuatan pengemulsian dan kemampuan menurunkan tegangan permukaan
dari air. Konsep ini dapat di pahami dengan mengingat kedua sifat dari anion
sabun (Achmad, 2004).
2.1.2 Komposisi Sabun
Sabun konvensional dibuat dari lemak dan minyak alami dengan garam
alkali. Sabun deterjen dibuat dari bahan sintetik. Menurut Wasitaatmadja (1997),
sabun konvensional dan sabun deterjen biasanya mengandung:
1. Surfaktan
Surfaktan adalah bahan terpenting dari sabun. Prinsip kerjanya jika
dilarutkan kedalam cairan cenderung memekat pada permukaan cairan tersebut.
Kesanggupan ini disebut dengan sifat fisiokimia yang dualistik (ambifilik), yaitu
yang mempunyai bagian yang senang pada pelarut (filik) dan bagian yang tidak
senang pada pelarut (fobik). Jika pelarutnya air, maka surfaktan akan berada
dibatas antara air dan yang dilarutkan dan tegak lurus terhadap batas tersebut
dengan bagian yang bersifat filik berada dalam air.
Besarnya bagian fobik dan filik menentukan potensi surfaktan. Bila salah
karena akan larut pada salah satu bahan pelarut atau yang dilarutkan. Selain
sebagai pelarut, surfaktan juga dapat bekerja sebagai pembasah, pembentuk busa,
dan pengemulsi. Pada sabun surfaktan bekerja sebagai pelarut (kotoran dan
lemak), pengemulsi, dan pembentuk busa.
2. Pelumas
Untuk menghindari rasa kering pada kulit diperlukan bahan yang tidak
saja meminyaki kulit tetapi juga berfungsi untuk membentuk sabun yang lunak,
misal asam lemak bebas, fatty alcohol, gliserol, lanolin, paraffin lunak, cocoa butter, dan minyak almond, bahan sintetik ester sulfosuksinat, asam lemak isotionat, asam lemak etanolamid, polimer JR, dan carbon resin (polimer akrilat). Bahan-bahan tersebut selain meminyaki kulit juga dapat menstabilkan busa dan
berfungsi sebagai peramas (plasticizers). 3. Antioksidan dan Sequestering Agents
Untuk menghindari kerusakan lemak terutama bau tengik, dibutuhkan
bahan penghambat oksidasi, misalnya stearil hidrazid dan butilhydroxy toluene
(0,02%-0,1%). Sequestering agents dibutuhkan untuk mengikat logam berat yang
mengkatalisis oksidasi EDTA.
4. Deodorant
Deodorant dalam sabun mulai dipergunakan sejak tahun 1950, namun oleh
karena khawatir efek samping, penggunaanya dibatasi. Bahan yang digunakan
adalah TTC (trichloro carbanilide) dan 2-hidroxy 2,4,4-trichlorodiphenyl ester
5. Warna
Kebanyakan sabun toilet berwarna cokelat, hijau biru, putih, atau krem.
Pewarna sabun diperbolehkan sepanjang memenuhi syarat dan peraturan yang
ada, pigmen yang digunakan biasanya stabil dan konsentrasinya kecil sekali
(0,01%-0,5%). Titanium dioksida 0,01% ditambahkan pada berbagai sabun untuk
menimbulkan efek berkilau. Akhir-akhir ini dibuat sabun tanpa warna dan
transparan.
6. Parfum
Isi sabun tidak lengkap jika tidak ditambahkan parfum sebagai pewangi.
Pewangi ini harus berada dalam pH dan warna yang berbeda pula.
7. Pengontrol pH
Penambahan asam lemak yang lemah, misalnya asam sitrat, dapat
menurunkan pH sabun.
8. Bahan tambahan khusus
Berbagai bahan tambahan untuk memenuhi kebutuhan pasar, produsen,
maupun segi ekonomi dapat dimasukkan ke dalam formula sabun. Saat ini
dikenal berbagai macam sabun khusus, misalnya:
a. Superfatty yang menambah lanolin atau paraffin.
b. Antiseptik (medicated = carbolic) yang menambahkan bahan antiseptik, misalnya: fenol, kresol, dan sebagainya.
2.1.3 Fungsi Sabun
Fungsi sabun dalam aneka ragam cara adalah sebagai bahan pembersih.
membasahi bahan yang dicuci dengan lebih efektif. Sabun bertindak sebagai suatu
zat pengemulsi untuk mendispersikan minyak dan lemak dan sabun teradsorpsi
pada butiran kotoran (Keenan, dkk., 1980).
Sifat utama dari bahan dasar sabun harus dapat menurunkan tegangan
permukaan. Bahan yang dapat menurunkan tegangan permukaan pada air secara
efektif disebut surface active agents atau surfaktan. Surfaktan mempunyai fungsi penting dalam proses membersihkan, seperti menghilangkan bau dan mengikat
kotoran sehingga kotoran tersebut dapat dibuang (Qisti, 2009).
Minyak atau lemak atau asam lemak sangat cocok untuk produk surfaktan
karena struktur molekulnya yang sangat spesifik. Bagian ekor hidrokarbon
bersifat hidrofob (benci air) dan bagian kepala ion (ion karboksilat) bersifat
hidrofil (suka air) (Wibraham dan Michael, 1992).
Kotoran yang menempel pada kulit umumnya adalah minyak, lemak dan
keringat. Zat-zat ini tidak dapat larut dalam air karena sifatnya yang non polar.
Sabun digunakan untuk melarutkan kotoran-kotoran pada kulit tersebut. Sabun
memiliki gugus non polar yaitu gugus –R yang akan mengikat kotoran, dan gugus
–COONa yang akan mengikat air karena sama-sama gugus polar. Kotoran yang
sudah dibersihkan dengan sabun tidak dapat lepas karena terikat pada sabun dan
sabun terikat pada air (Qisti, 2009).
2.1.4 Proses pembuatan sabun
Sabun dapat dibuat melalui dua proses, yaitu:
Saponifikasi melibatkan hidrolisis ikatan ester gliserida yang
menghasilkan pembebasan asam lemak dalam bentuk garam dan gliserol. Garam
dari asam lemak berantai panjang adalah sabun (Stepen, 2004).
. Reaksi kimia pada proses saponifikasi adalah sebagai berikut:
Dari reaksi diatas terbentuk gliserol dan sabun. Sabun merupakan garam
Na atau K dari asam lemak. Sabun Na dan K larut dalam air. Sabun Na (sabun
keras) digunakan untuk mencuci dan sabun K (sabun lunak) digunakan untuk
mandi (Panil, 2008).
2. Netralisasi
Netralisasi adalah proses untuk memisahkan asam lemak bebas dari
minyak atau lemak, dengan cara mereaksikan asam lemak bebas dengan basa atau
pereaksi lainnya sehingga membentuk sabun (Ketaren, 2008).
bebas
2.1.5 Klasifikasi Sabun
Sabun diklasifikasikan menjadi tiga kelompok. Sabun dengan kualitas A
lemak terbaik dan mengandung sedikit alkali atau tidak mengandung alkali bebas.
Sabun A ini umumnya digunakan untuk sabun mandi (toilet soap) yang biasa kita
kenal. Sabun kualitas B merupakan sabun yang dibuat dengan menggunakan
bahan baku yang berasal dari minyak atau lemak dangan kualitas yang lebih
rendah dan mengandung sedikit alkali, namun tidak menyebabkan iritasi pada
kulit. Sabun B ini biasanya digunakan untuk mencuci pakaian dan piring. Sabun
dengan kualitas C merupakan sabun yang dibuat dengan minyak atau lemak yang
berwarna gelap (kualitas rendah) dan mengandung alkali yang relatif tinggi (Qisti,
2009).
Menurut Tjokronegoro dan Utama (2001), terdapat 3 macam sabun yaitu:
1. Sabun biasa: bersifat alkali dengan pH 9-10.
2. Syndets. Synthetic detergents dengan pH 5,5-7.
3. Sabun khusus yang ditambah bahan-bahan tertentu dengan berbagai tujuan.
2.1.6Efek Samping Sabun
Menurut Wasitaatmadja (1997), sabun dapat memberikan efek samping
pada kulit seperti:
1. Daya Alkalinisasi Kulit
Daya alkalinisasi sabun dianggap sebagai faktor terpenting dari efek
samping sabun. Reaksi basa yang terjadi pada sabun konvensional yang
melepaskan ion OH sehingga pH larutan sabun ini berada antara 9-12 dianggap
sebagai penyebab iritasi pada kulit. Bila kulit terkena cairan sabun, pH kulit akan
naik beberapa menit setelah pemakaian meskipun kulit telah dibilas dengan air.
menjadi normal kembali. Alkalinisasi dapat menimbulkan kerusakan kulit bila
kontak berlangsung lama.
2. Daya Pembengkakan dan Pengeringan Kulit
Kontak air (pH) pada kulit yang lama akan menyebabkan lapisan tanduk
kulit membengkak akibat kenaikan permeabilitas kulit terhadap air. Cairan yang
mengandung sabun dengan pH alkalis akan mempercepat hilangnya mantel asam
pada lemak kulit permukaan sehingga pembengkakan kulit akan terjadi lebih
cepat. Kerusakan lapisan lemak kulit dapat menambah kekeringan kulit akibat
kegagalan sel kulit mengikat air.
3. Daya Denaturasi Protein dan Ionisasi
Reaksi kimia sabun dapat mengendapkan ion kalsium (K) dan magnesium
(Mg) di lapisan atas kulit. Pada kulit yang kehilangan lapisan tanduk,
pengendapan K+ dan Mg+ akan mengakibatkan reaksi alergi. Pengendapan K+ dan Mg+ di atas lapisan epidermis akan menutup folikel rambut dan kelenjar palit sehingga menimbulkan infeksi oleh kuman yang larut dalam minyak.
4. Daya Antimikrobial
Sabun yang mengandung surfaktan, terutama kation, mempunyai daya
antimikroba, apalagi bila ditambah bahan antimikroba. Daya antimikroba ini
terjadi pula akibat kekeringan kulit, pembersihan kulit, daya pemisah surfaktan,
5. Daya Antiperspirasi
Kekeringan kulit juga dibantu oleh penekanan perspirasi. Pada percobaan
dengan larutan natrium lauril sulfat, didapat penurunan produksi kelenjar keringat
antara 25-75%.
6. Lain-lain
Efek samping lain berupa dermatitis kontak iritan, dermatitis kontak
alergik, atau kombinasi keduanya.
2.2 Sabun Mandi
2.2.1 Pengertian Sabun Mandi
Dalam Standar Nasional Indonesia (1994) sabun mandi adalah garam
natrium atau kalium dari minyak nabati dan atau lemak hewani berbentuk padat,
lunak, atau cair, berbusa digunakan sebagai pembersih, dengan menambahkan zat
pewangi, dan bahan lainnya yang tidak membahayakan kesehatan (SNI, 1994).
2.2.2 Syarat Mutu Sabun Mandi
Syarat mutu sabun mandi menurut Standar Nasional Indonesia
06-3532-1994 dapat dilihat pada Tabel 1.
Tabel 1: Syarat mutu sabun mandi
No Uraian Tipe I Tipe II Seperfat
1 Kadar air, % Maks. 15 Maks. 15 Maks. 15
2 Jumlah asam lemak, % >70 64-70 >70
3 Alkali bebas
Dihitung sebagai NaOH, %
Dihitung sebagai KOH, %
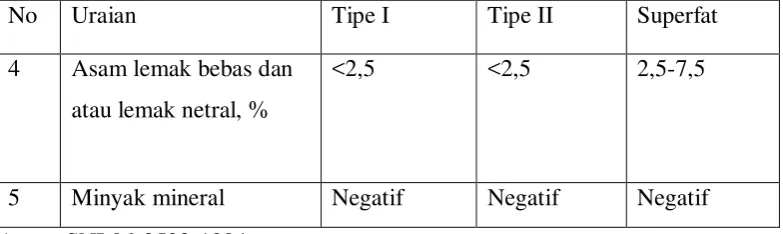
Tabel 1 lanjutan syarat mutu sabun mandi
No Uraian Tipe I Tipe II Superfat
4 Asam lemak bebas dan
atau lemak netral, %
<2,5 <2,5 2,5-7,5
5 Minyak mineral Negatif Negatif Negatif
Acuan SNI 06-3532-1994
1. Kadar Air
Kadar air merupakan bahan yang menguap pada suhu dan waktu tertentu.
Maksimal kadar air pada sabun adalah 15%, hal ini disebabkan agar sabun yang
dihasilkan cukup keras sehingga lebih efisien dalam pemakaian dan sabun tidak
mudah larut dalam air. Kadar air akan mempengaruhi kekerasan dari sabun (Qisti,
2009).
2. Jumlah Asam Lemak
Jumlah asam lemak merupakan jumlah total seluruh asam lemak pada
sabun yang telah atau pun yang belum bereaksi dengan alkali. Sabun yang
berkualitas baik mempunyai kandungan total asam lemak minimal 70%, hal ini
berarti bahan-bahan yang ditambahkan sebagai bahan pengisi dalam pembuatan
sabun kurang dari 30%. Tujuannya untuk meningkatkan efisiensi proses
pembersihan kotoran berupa minyak atau lemak pada saat sabun digunakan.
Bahan pengisi yang biasa ditambahkan adalah madu, gliserol, waterglass, protein susu dan lain sebagainya. Tujuan penambahan bahan pengisi untuk memberikan
bentuk yang kompak dan padat, melembabkan, menambahkan zat gizi yang
3. Alkali Bebas
Alkali bebas merupakan alkali dalam sabun yang tidak diikat sebagai
senyawa. Kelebihan alkali bebas dalam sabun tidak boleh lebih dari 0,1% untuk
sabun Na, dan 0,14% untuk sabun KOH karena alkali mempunyai sifat yang keras
dan menyebabkan iritasi pada kulit. Kelebihan alkali bebas pada sabun dapat
disebabkan karena konsentrasi alkali yang pekat atau berlebih pada proses
penyabunan. Sabun yang mengandung alkali tinggi biasanya digunakan untuk
sabun cuci (Qisti, 2009).
4. Asam Lemak Bebas
Asam lemak bebas merupakan asam lemak pada sabun yang tidak terikat
sebagai senyawa natrium atau pun senyawa trigliserida (lemak netral). Tingginya
asam lemak bebas pada sabun akan mengurangi daya membersihkan sabun,
karena asam lemak bebas merupakan komponen yang tidak diinginkan dalam
proses pembersihan. Sabun pada saat digunakan akan menarik komponen asam
lemak bebas yang masih terdapat dalam sabun sehingga secara tidak langsung
mengurangi kemampuannya untuk membersihkan minyak dari bahan yang
berminyak (Qisti, 2009).
5. Minyak Mineral
Minyak mineral merupakan zat atau bahan tetap sebagai minyak, namun
saat penambahan air akan terjadi emulsi antara air dan minyak yang ditandai
dengan kekeruhan. Minyak mineral adalah minyak hasil penguraian bahan
organik oleh jasad renik yang terjadi berjuta-juta tahun. Minyak mineral sama
minyak tanah, solar, oli, dan sebagainya. Kekeruhan pada pengujian minyak
mineral dapat disebabkan juga oleh molekul hidrokarbon dalam bahan (Qisti,
2009).
Keberadaan minyak mineral pada sabun sangat tidak diharapkan, karena
akan mempengaruhi proses emulsi sabun dengan air (Qisti, 2009).
2.3Sabun Mandi Pemutih
Sabun mandi pemutih adalah sabun mandi yang ditambahkan bahan
tambahan tertentu yang dapat mencerahkan kulit, misalnya Titanium dioksida.
Titanium dioksida (TiO) dalam sabun berfungsi sebagai pemutih sabun dan kulit.
TiO2 adalah zat warna putih yang mempunyai sifat: indeks refraksi tinggi,
tidak menyerap sinar tampak, mudah diproduksi sesuai keinginan, stabilitas
tinggi dan non toksik (Andreas, 2009).
2.4 Penetapan Kadar Air
Penetapan kadar air dapat dilakukan dengan beberapa cara. Hal ini
tergantung pada sifat bahannya. Pada umumnya penentuan kadar air dilakukan
dengan mengeringkan bahan dalam oven pada suhu 105-110oC selama 3 jam atau sampai didapat berat konstan. Selisih berat sebelum dan sesudah pengeringan
adalah banyaknya air yang diuapkan (Winarno, 1992).
Pengeringan sampai bobot tetap berarti pengeringan harus dilanjutkan
hingga pada perbedaan dua kali penimbangan berturut-turut tidak lebih dari 0,50
mg untuk tiap gram zat yang digunakan, penimbangan kedua dilakukan setelah
Suatu bahan yang telah mengalami pengeringan ternyata lebih bersifat
higroskopis dari pada bahan asalnya. Oleh karena itu selama pendinginan sebelum
penimbangan, bahan selalu ditempatkan dalam ruang tertutup yang kering,
misalnya dalam eksikator atau desikator yang telah diberi zat penyerap air.
Penyerapan air/uap air ini dapat menggunakan kapur aktif, asam sulfat, silika gel,
alumunium oksida, kalium klorida, kalium hidroksida, kalium sulfat atau barium
oksida (Sudarmadji, 1989).
Untuk bahan-bahan yang tidak tahan panas, seperti bahan berkadar gula
tinggi, minyak, daging, kecap dan lain-lain pemanasan dilakukan dalam oven
vakum dengan suhu yang lebih rendah. Kadang-kadang pengeringan dilakukan
tanpa pemanasan, bahan dimasukkan dalam eksikator dengan H2SO4 pekat
sebagai pengering, hingga mencapai berat konstan (Winarno, 1992).
Penentuan kadar air dari bahan-bahan yang mudah menguap (volatile) seperti sayuran dan susu, menggunakan cara destilasi dengan pelarut tertentu,
misalnya toluene, xylol, dan heptana yang berat jenisnya lebih kecil dari pada air.
Prinsip penentuan kadar air dengan destilasi adalah menguapkan air dengan
pembawa cairan kimia yang mempunyai titik didih lebih tinggi daripada air dan
tidak dapat campur dengan air serta mempunyai berat jenis lebih rendah dari pada
air (Sudarmadji, 1989).
Contoh (sampel) dimasukkan kedalam tabung bola (flask), kemudian dipanaskan. Air dan pelarut menguap, diembunkan, dan jatuh pada tabung
dibagian bawah, sehingga jumlah air yang diuapkan dapat dilihat pada skala
tabung Aufhauser tersebut (Winarno, 1992 ).
Untuk bahan dengan kadar gula tinggi, atau kadar air dapat diukur dengan
menggunakan refraktometer disamping penentuan padatan terlarutnya pula.
Dalam hal ini air dan gula dianggap komponen-komponen yang mempengaruhi
indeks refraksi (Winarno, 1992).
Disamping cara-cara fisis, ada juga cara-cara kimia untuk menentukan
kadar air. Mc Neil mengukur kadar air berdasarkan volume gas asetilen yang
dihasilkan dari reaksi kalsium kalbida dengan bahan yang akan diperiksa. Cara ini
dipergunakan untuk bahan-bahan seperti sabun, tepung, kulit, bubuk biji panili,
dan sari buah (Winarno, 1992).
Karl fischer pada tahun 1935 menggunakan cara pengeringan berdasarkan
reaksi kimia air dengan titrasi langsung dari bahan basah dengan larutan iodine,
sulfur dioksida, dan piridina dalam metanol. Perubahan warna menunjukkan titik
akhir titrasi (Winarno, 1992).
2.5 Gravimetri
Gravimetri merupakan cara pemeriksaan jumlah zat yang paling tua
dibandingkan dengan cara pemeriksaan kimia lainnya. Analisis gravimetri
merupakan cara analisis kuantitatif berdasarkan berat tetap (berat konstan)
(Gandjar dan Rohman, 2007).
Gravimetri dapat digunakan untuk menentukan hampir semua anion dan
kation anorganik serta zat-zat netral seperti air, belerang dioksida, karbon dioksida
dengan mudah secara gravimetri. Contoh-contohnya antara lain: penentuan kadar
laktosa dalam susu, salisilat dalam sediaan obat, fenolftalein dalam obat pencahar,
nikotina dalam pestisida, kolesterol dalam biji-bijian dan benzaldehida dalam
buah-buahan tertentu. Jadi, sebenarnya cara gravimetri merupakan salah satu cara
yang paling banyak dipakai dalam pemeriksaan kimia (Rivai, 1995).
Menurut Widodo dan Lusiana (2010), berdasarkan macam hasil yang
ditimbang, metode gravimetri dibedakan dalam kelompok metode evolusi gas
dan metode pengendapan.
a. Metode evolusi gas
Pada cara evolusi bahan direaksikan dengan cara pemanasan atau
ditambah pereaksi tertentu sehingga timbul/menghasilkan gas. Pada umumnya
yang dicari adalah banyaknya gas yang dihasilkan dari reaksi tersebut. Untuk
mencari atau menentukan banyaknya gas yang terjadi dapat dilakukan:
1. Secara tidak langsung
Penimbangan analit setelah bereaksi, berat gas diperoleh sebagai selisih
analit sebelum dan sesudah reaksi.
2. Cara langsung
Gas yang terjadi dari hasil reaksi ditimbang setelah diserap oleh suatu
bahan khusus sebagai adsorben gas tersebut. Penimbangan pada metode langsung
adalah penimbangan adsorben. Berat gas diketahui dari selisih berat penimbangan
b. Metode pengendapan
Dalam cara pengendapan, analit yang direaksikan dengan pereaksi tertentu
sehingga terjadi suatu endapan, dan endapan inilah yang ditimbang. Atas cara
pembentukan endapan maka gravimetri dibedakan menjadi dua macam.
1. Endapan dibentuk dari reaksi analit dengan suatu pereaksi, endapan biasanya
berupa senyawa, sehingga baik kation maupun anion akan diendapkan, bahan
pengendap dapat sebagai bahan anorganik maupun bahan organik. Cara ini
dikenal sebagai cara gravimetri.
2. Endapan dibentuk secara elektrokimia, dengan perkataan lain analit
dielektrolisis sehingga terjadi logam sebagai endapan. Cara ini dikenal sebagai
elektrogravimetri.
Menurut Widodo dan Lusiana (2010), tahapan analisis gravimetri meliputi:
1. Pelarutan analit.
2. Pengaturan kondisi larutan: pH, temperatur.
3. Pengendapan.
4. Menumbuhkan kristal endapan.
5. Penyaringan dan pencucian endapan.
6. Pemanasan atau pemijaran endapan untuk mendapatkan endapan kering dengan
susunan tertentu yang stabil dan spesifik.
7. Pendinginan dan penimbangan endapan.