Dosen : Dr. Yetria Rilda
TIO PUTRA WENDARI
1530412008
Nanosain dan Teknologi
Pascasarjana Universitas Andalas
Jurusan Kimia
Efek Ukuran Nano
Terhadap Sifat
Nanosains - Nanoteknologi
NanoScience
Didefinisikan sebagai studi fenomena dan manipulasi material pada skala atomik,
molekuler dan makromolekuler dimana sifatnya berbeda secara signifikan daripada
material pada skala besarnya
Nanoteknologi
Mengapa sifat-sifat pada nanomaterial berbeda ??
Ada 2 faktor prinsipnya menyebabkan sifat dari nanomaterial berbeda secara
signifikan dengan material lain :
1. Peningkatan area permukaan spesifiknya
2. Efek Quantum confinement
Faktor-faktor ini dapat mengubah atau meningkatkan sifat-sifat seperti :
reaktivitas, kekuatan dan sifat listriknya.
Nanopartikel sangat menarik karena sifat barunya (seperti reaktivitas kimiawi dan
sifat optik) yang ditunjukkan dibandingkan dengan partikel yang lebih besar dari
material yang sama
Sebagai contoh : TiO
2dan ZnO menjadi berwarna bening pada skala nano dan dapat
diaplikasikan sebagai sunscreens
Nano material memiliki sifat yang berbeda dari material bulknya. Kebanyakan
material dengan struktur nano berupa kristalin alaminya dan memiliki sifat yang unik
Sifat fisika
Struktur kristal dari nanopartikel sama dengan struktur bulknya dengan parameter kisi yang berbeda
Jarak antaratomik berkurang seiring naiknya ukuran diakrenakan oleh gaya elektrostatik jarak jauh
dan daya tolak antar inti jarak dekat.
Titik leleh dari nanopartikel menurun seiring meningkatnya ukuran
Nanomaterial
Sifat kimiawi
Struktur elektronik dari nanopartikel bergantung pada ukuran dan kemampuan dari nanopartikel
tersebut untuk bereaksi bergantung pada ukuran klaster
Luas permukaan yang lebih besar dibandingkan rasio volume dari nanopartikel memiliki efek yang
Electrical properties
Struktur elektronik dari nanomaterial berbeda dari material bulknya.
Densiti tingkat energi pada pita konduksi berubah.
Saat jarak energi antara 2 level energi lebih daripada KBT , E gap terbentuk.
Nanoklaster dengan ukuran yang berbeda akan memiliki struktur elektronik yang berbeda dan
pemisahan level energi yang berbeda
Suatu partikel dengan diameter antara 1-100 nanometer (109 meter) atau memiliki 10-106
atom/molekul per partikelnya.
Nanopartikel umumnya memiliki sifat-sifat seperti :
1. Memiliki luas permukaan yang besar dengan volume yang kecil 2. Memiliki partikel yang lebih reaktif
3. Memiliki sifat yang berbeda dibandingkan ukuran bulk nya 4. Umumnya membentuk sebuah kluster.
Klasifikasi nanomaterial
• Kumpulan unit (atom atau molekul) yang terdiri dari 50 unit.
Cluster
• Cairan stabil yang menggandung partikel berukuran 1-1000 nm.
Colloid
• Padatan yang berukuran 1-1000 nm.
Nanoparticle
• Padatan yang berbentuk singel kristal berukuran nano.
Nanocrystall
• 3D : partikel ; 2D: lapis tipis ; 1D: kawat tipis
Nanostructural
• Sama dengan material nanostruktur.
Nanophase
• Partikel yang menunjukkan pengaruh ukuran setidaknya dalam 1D
Ukuran nano dari suatu material sangat berpengaruh terhadap sifat material tersebut,
antara lain :
1.
Luas permukaan
2.
Atom Pada Permukaan
3.
Reaktivitas
4.
Sifat Elektronik
5.
Efisiensi Fotokatalitik
Hampir semua bidang dalam kedokteran, elektronik, fashion, dll sangat bergantung
pada bidang nanoteknologi.
Salah satu konsep penting dalam memahami nanopartikel melibatkan
rasio luas
permukaan : volume
.
Saat sebuah objek semakin besar, peningkatan ukuran permukaannya tidak sebanding
dengan peningkatan volumenya, begitu sebaliknya. Hal ini sangat berpengaruh pada
reaksi katalisis
1.
Luas Permukaan
Dengan volume material yang sama, material nanopartikel memiliki luas permukaan tang jauh
lebih besar.
Persen efektif dari permukaan atom sebagai fungsi dari diameter partikel.
Ukuran partikel persen dispersi dari atom logam pada permukaan, sebagai sisi aktif reaktan. Berperan penting dalam bidang katalis
Atom pada permukaan material nano akan tersusun lebih banyak dan rapat sehingga akan
berpengaruh dalam sifat material terutama fotokatalis.
3.
Reaktivitas - Quntum Well
Bentuk energi pada permukaan jika atom
pada permukaan bulk akan memiliki
permbedaan dengan reaktivitas permukaan
dengan banyak atom yang tersusun pada
Hamiltonian: penjumlahan dari total energi kinetik dari seluruh partikel,
serta energi potensial dari partikel-partikel yang berkaitan dengan sistem.
Biasanya dinyatakan per unit volume
Hamiltonian suatu elektron di dalam padatan:
Keterlibatan interaksi interatomic yang meningkatkan level energi single-atom
energy band ketika single atom bulk solid
Salah satu efek paling langsung mengurangi ukuran bahan
untuk rentang nanometer adalah munculnya efek
kuantisasi karena
confinement
gerakan elektron.
Ini menyebabkan energi level akan memiliki ciri tersendiri
dengan adanya faktor ukuran nano
Efek ukuran nanopartikel akan mempengaruhi efek struktur,
termodinamika, elektronika, spektroskopi, elektronik, atau
sifat kimia lainnya.
Efek ukuran nanopartikel dapat dilkasifikasikan menjadi 2 :
1.
Efek ukuran spesifik, seperti jumlah atom dalam kluster
metal.
2.
Efek ukuran nanostruktur yang lebih besar.
Disamping merupakan kurva jumlah atom
Fe dari nanopartikel
spherical
pada
permukaan dan
bulk
(interiornya)
Disini terlihat bahwa keunggulan dari
nanopartikel terletak pada jumlah atom Fe berukuran 1-5 nm pada permukaannya yang sangat tinggi, yang notabene merupakan atom yang akan menjadi katalisator dari suatu reaksi
Ukuran partikel Fe pada permukaan yang
semakin kecil memungkinkan semakin banyak atom Fe yang mampu mengkatalisis reaksi
Ukuran nanopartikel yang kecil juga
meningkatkan reaktivitas dari nanopartikel itu sendiri.
Bentuk Partikel
(a) Nanokristalin MgO (b) Mikrokristalin MgO (c) MgO bulk
.... Lanjutan (efek bentuk dalam fotokatalis)
Semakin nano ukuran suatu katalis, maka akan semakin banyak permukaan (sisi aktif) yang berperan dalam reaksi katalitik tersebut.
Medis
• Seng oksida sebagai campuran dengan + 0.5% iron (III) oksida (Fe2O3) disebut kalamina dan
digunakan di dalam berbagai jenis obat kulit
sifat antimikroba • Drug delivery vehicles
Dengan ukuran nano, dinilai lebih efisien dalam transport obat ke sumber penyakit.
Tabir surya menghalangi sinar UV-A (320-400 nm) / UV-B (280-320 nm) – melindungi kulit dan mencegah kanker kulit
Industri Polimer
Sekitar 50% dari ZnO digunakan dalam industri polimer. Proses vulkanisasi karet ban mobil
meningkatkan konduktivitas bahan (ban) dan anti bakteri-jamur (tekstil)
Nanopartikel ZnO Semakin banyak partikel nano ZnO pada permukaan Peningktakan efek konduktivitas dan anti
Aplikasi Nanomaterial
Source : Small wonder Nanotechnology and cosmetic
Agen pengcoatingan
Cat anti korosi pada logam Campuran warna cat/ lukisan yang lebih beragam Nanoscale
terhadap emisi.
Sensor
Pendeteksian perubahan arus listrik adanya absorpsi molekul gas pada permukaan nanorod
respon sensor menghasilkan data. Deteksi gas Hidrogen hingga 10 ppm
Piezoelektrisitas
Kemampuan kristal untuk merenggang sehingga menghasilkan energi listrik dikarenakan susunan atom yang rapat pada permukaan nanomaterial.
Kosmetik
Campuran ZnO sebagai bahan make up, sabun pasta gigi, deodoran
Semakin besar ukuran (mikro), ZnO terlihat semakin putih Ukuran nanopartikel warna menjadi transparant (natural).
Anti bakteria agent, sunblock, dll
Nano
Tio Putra Wendari
1530412008
Kimia
Dosen : Dr. Yetria Rilda, MS
Sebuah semikonduktor dapat mengalami proses eksitasi elektron dengan adanya energi cahaya yang lebih tinggi dibandingkan energi gap, dan banyak membentuk pasangan elektron-hole.
Photo-Induced
Fotokatalis Fotovoltaik Fotoelektrik Fotoelektrokemikal
Adanya Proses kimia yang “dikatalisis” oleh material padatan yang diberikan energi berupa gelombang elektromagnetik dengan panjang gelombang UV hingga Sinar tampak.
Semikonduktor
Absorpsi Cahaya Difusi Rekombinan
Degradasi Perangkapan muatan
Initial Step Absorpsi
Photo-Induced
Material padatan
Foton (hv) UV-Vis
Pengaruh Ukuran nanokristal terhadap
Strukutral dan Sifat Elektronik dari fotokatalis.
Pengaruh Nanostruktur pada proses ”Initial
Step” dari reaksi fotokatalis dan pengaruh ukuran partikel dan bentuk morfologi
terhadap pengukuran katalitik.
Semikonduktor memiliki perbedaan energi valensi dan pita konduksi, sebesar 1-3.5 eV
Tahapan reaksi pada semikonduktor :
1. Penyerapan foton dengan energi yang sama atau
lebih besar dari celah pita dari semikonduktor (misalnya, 3,2 eV untuk TiO2)
2. Menghasilkan sepasang pembawa muatan, yaitu elektron-hole (e / h +) pasangan.
Foto-katalitik semikonkonduktor biasanya oksida,
Seperti : TiO2, ZnO, WO3, CeO2, orAxByOz, tetapi juga
sulfida, MoSx, WSx, atau BiSx, atau nitrida, TaNx, SiNx, atau GEnx.
Dalam proses fotokatalitis,
Generation satu elektron terkestasi pada pita valensi (VB) akan membentuk hole.
Hole dan elektron akan mengalami transfer muatan dengan spesies absorben pada permukaan semikonduktor dengan pembentukan radikal yang akan mebgoksidasi senyawa organik atau mereduksi senyawa logam.
Rekombinan Proses kembalinya elektron dan bergabung dengan hole pada pita valensi, umumnya menghasilkan radiasi (sinar).
Dieperlukan masa hidup elektron dan hole yang lama
Proses traping elektron dan hole Mekanisme reaksi :
D
n++
e
−cb
→
D
(n−1)+electron trapping
D
n++
h
+vb
→
D
(n+1)+hole trapping
• Intrinsik vacancy Oxygen pada nanostruktur oksida
• Ekstrinsi Penambahan dopant/ impuritis
Sintesis Organik
Oksidasi hidrokarbon rantai lurus dan siklik Degradasi polutan
Mineralisasi senyawa organik
Disinfektan/destruksi dari material biologi Detoksifikasi senyawa anorganik dan removal ion
Reaksi Spesial
Fotofiksasi Nitrogen Fotoreduksi CO2
Fotospliting air untuk produksi H2
Proses Elektronik pada semikonduktor
Fotokatalis yang baik memiliki sifat :
Fotoaktif
Dapat menyerap sinar UV/Visible
Inert terhadap reaksi kimia/biologi
Murah
Nontoksik
Struktur Elektronik Luas Permukaan
Sisi aktif
Pengaruh ukuran kristal dari semikonduktor
Karakteristik Morfologi (bola, elips, jarum, prismatik,
dan batang) sangat mempengaruhi aktivitas fotokatalitik
Pengaruh ukuran partikel terhadap fotoreaktivitas semikonduktor dengan adanya 2 pendekatan:
(1) Dijelaskan bahwa peningkatan yeild kuantum ketika ukuran partikel menurun. Efek ini bisa
berhubungan dengan luas permukaan yang meningkat dari partikel yang diameter lebih kecil atau ke potensial redoks disempurnakan pita konduksi elektron, dan mungkin karena konsentrasi situs permukaan jenuh
(2) Kenaikan yield kuantum sebagai ukuran partikel menurun karena harga rekombinasi
elektron-lubang di permukaan yang lambat karena meningkatkan pemisahan pengisi foto yang dihasilkan (334). Juga, efek ini bisa disebabkan permukaan kepadatan spesiasi dan permukaan cacat, yang sangat terkait dengan metode persiapan (335.336).
Penelitian-penelitian terbaru menyarankan
Keberadaan ukuran partikel optimum untuk reaksi fotokatalitik, dengan adanya efek ukuran partikel efektif pada penyerapan cahaya dan efisiensi hamburan, rekombinan pembawa muatan, dan luas permukaan.
Ukuran partikel memegang peranan penting terhadap sifat-sifat struktur dari berbagai material., seperti simetri kisi dan parameter sel.
ketika ukuran partikel menurun, jumlah atom permukaan dan atom antarmuka meningkat, menghasilkan regangan / stres dan gangguan struktural.
Contoh efek ukuran yang mempengaruhi reaksi fotokatalis :
Fasa kristalin
Sifat/jumlah pusat defek
Cacat sangat diperlukan dikarenakan memiliki sifat perangkap (elektron/hole) atau sebagai pusat rekombinasi.
Permukaan kimia
Sangat berpengaruh dakam transfer muatan ke molekul dan efisiensi proses generation dari elektron dan hole.
Efek ukuran pada struktur dan stabilitas dari partikel berhubungan dengan keseimbangan energi antara permukaan dan bulk.
Reaksi fotokatalis dimulai dengan penyerapan foton dan diikuti generasi pasangan elektron-hole. Elektron dan hole ini dapat berekombinan secara cepat pada ukuran bulk.
CACAT PADA STRUKTUR dapat berperan sebagai “trapping center” tergantung pada lokasi cacat. Ukuran partikel nano dapat berkontribusi untuk rekombinasi muatan terperangkap sendiri, karena kedekatan spasial pusat perangkap permukaan. Mereka tertarik dengan gaya elektrostatik, menghindari stabilisasi pemisahan muatan.
Seperti pada TiO2
Penangkap elektron pada semikonduktor TiO2
berupa ion Ti4+ dana kekosongan oksida.
Ion Ti4+ dapat dibagi menjadi 2 tipe sisi
penangkap :
Pada dalam nanopartikel
Pada permukaan nanopartikel
Ion Ti4+ berinteraksi dengan elektron eksitasi
untuk memebentuk Ti3+.
TiIV−OH + e−cb → TiIII−OH (17.8)
TiIII−OH + h+vb → TiIV−OH
Absorption of Light: Charge Separation
Penyerapan cahaya dengan energi yang lebih tinggi dibandingkan band gap akan menyebabkan eksitasi/ pemisahan elektron ke pita konduksi (CB), menghasilkan hole pada Pita Valensi (VB).
MOx + hν MO→ x(e−cb + h+vb) MOX = semikonduktor
Adanya efek “quantum confinement
”
proses penyerapan cahaya memiliki ciri
tersendiri tergantung pada ukuran partikel
semikonduktor.
Band gap behavior versus size for TiO2, ZnO, and MoS2
materials.
A.Proses Fotokatalis : Pada proses ini
dihasilkan spesies aktif radikal melalui
reaksi kimia dengan bantuan
penyinaran.
TiO
2+ h
v
TiO
2+ h
Vb++ e
cb-h
Vb++ >Ti
(IV)OH
[>Ti
(IV)OH
●]
+e
cb-+ >Ti
(IV)OH
[>Ti
(III)OH]
[>Ti
(IV)OH
●]
++ Red
[>Ti
(IV)OH
●]
++
Red
●e
cb-+ Ox
[>Ti
(IV)OH + Ox
●-B. Radikal bebas yang dihasilkan dari reaksi
fotokatalis akan menyerang senyawa
organik target dengan jalan memutus ikatan
rangkap yang ada senyawa organik
seperti
zat warna, bakteri, dan jamur.
Reaksi dari trapping e- dan h+
Mn+ + e−cb − M→ (n−1)+ electron trapping
Mn+ + h+vb − M→ (n+1)+ hole trapping
Perlakuan trapping pada elektron/hole saja tidak efektif karena spesies muatan yang ditangkap akan segera berekombinasi dengan pasangan spesies muatannya
Meningkatkan waktu hidup dari charge carrier
Menghindari proses rekombinasi
Pendopingan semikonduktor
Mampu melakukan
trapping e- dan h+
Kemampuan ion dopan sebagai
penangkap muatan bergantung kepada:
Konsentrasi dopan
Level energi pada kisi semikonduktor
Konfigurasi elektronik d dan f
Distribusi antarpartikel
Konsentrasi donor elektron
Kation dopan yang melakukan trapping
akan mengganggu keseimbangan konfigurasi elektroniknya, menyebabkan ketidakstabilan
Elektron dan hole yang terbentuk dilibatkan dalam reaksi kimia stelah terjadinya
transfer muatan pada permukaan.
Porses trapping dan transfer muatan harus bersaing lebih dulu terjadi dibandingkan
proses deeksitasi /relaksasi yang menyebabkan rekombinan muatan.
Rekombinasi Elektron-hole
Transfer muatan ke permukaan
2 Tahapan proses setelah pembentukan muatan
Proses relaksasi/ rekombinasi suatu material semikonduktor akan
menghasilkan
energi dalam bentuk radiasi/panas .
e
−cb
+
h
+v
b
− MO
→
x
+ energy (17.28)
e
−Tr +
h
+v
b
− MO
→
x
+ energy (17.29)
e
−
cb
+
h
+Tr − MO
→
x
+ energy (17.30)
e
−Tr +
h
+Tr − MO
→
x
+ energy
Dimana CB = pita konduksI, VB = Pita valensi, Tr = muatan terperangkap
Dalam reaksi kimia fotokatalis, pembawa muatan harus melakukan kontak
dengan molekul gas/ cairan untuk terjadinya proses degradasi atau
transfromasi kimia. Transfer
Pada reaksi fotokatalis oksigen akan selalu hadir sebagai media reaksi sebagai
akseptor elektron utama. Elektron ditransfer ke molekul oksigen pada
permukaan katalismenghasilkan superoksida atau hidrogen peroksida radikal.
Pendeposisian logam mulia (Pt, Au, Ag dll) pada permukaan semikonduktor dapat meningkatkan efisiensi fotokatalitik dengan bertindak mirip seperti
Pendeposisian juga meningkatkan laju transfer elektron ke oksigen dan meningkatkan nilai hasil kuantum
Jumlah deposit yang terlalu banyak akan menurunkan efisiensi dan mengurangi jumlah cahaya yang masuk akibat efek UV shielding pada logam mulia
Nilai peningkatan efisiensi fotokatalitik terhadap pelapisan logam dapat dihitung dengan rumus dibawah:
Efek Pelapisan Logam Pada Semikonduktor
�������=���� ������ ������ ����� �����
���������� ����� ����������
Oksida campuran yang terdiri dari semikonduktor yang didispersikan kedalam support inert
seperti silika, alumina atau zirkonia telah dibuat
Support pada semikonduktor dilakukan agar semikonduktor lebih stabil dan memiliki luas
permukaan yang besar.
Dispersi TiO2 pada silika terbukti menstabilkan fasa anatase TiO
2
Heterojucntions merupakan campuran dari 2 semikonduktor yang memiliki level energi dan nilai
Logam transisi seperti V, Nb dan Ta pada tingkat oksidasi tertingginya dpaat membentuk klaster
anion logam-oskigen yang disebut sebagai polioksometalat (POM)/polioksoanion
Klasifikasi POM adalah:
Senyawa isopoli dengan rumus umum MxOq-y, dihasilkan melalui kondensasi asam dari
MoO2-4/WO2-4 murni
Contoh: MO7O6-24
Senyawa heteropoli dengan rumus umum AqMxOq-y, dihasilkan melalui kondensasi asam dari
MoO2-4/WO2-4 dan suatu heteroatom (A = P, Si, As dll)
Conth: PW12O3-40
Senyawa heteropoli yang mengandung rasio campuran Mo:W yang berbeda dari MoO2-4/WO2-4
dan suatu heteroatom
Contoh: P2W15Mo3O6-62
POM yang disubstitusi dengan logam transisi dengan mensubstitusi Mo dengan logam transisi dan
ligan
Contoh:
[PW11O39Mn(H2O)6-POM merupakan oksidan yang efektif yang mnunjukkan trasnformasi redox multielektron yang
berlangsung cepat dan reversible pada kondisi biasa
Preparation Of Multifunctional
Cationized Cotton Fabric
Based On Tio
2
Nanomaterials
A. Farouk, S. Sharaf , M.M. Abd El-Hady∗
Degradasi Metilen Biru (Self-Cleaning)
C16H18N3SCl + 51/2 O2 HCl + H2SO4 + 3 HNO3 + 16 CO2 + 6 H2O
Anti-mikroba Anti UV
Anti air
Fotokatalis
Egap Konduktor : 0 – 1 eV
Semikonduktor : 1 – 3 eV Isolator : > 4 eV
Nano-TiO
2Katun Multifungsi (Non-Toksik)
• Efek penyebaran pembawa muatan
Semakin kecil ukuran partikel, meningkatakan efesiensi fotokatalis
semakin sedikit waktu yang diperlukan untuk “photo-induced electrons” tersebar dari kristal ke permukaan substrat yang mengurangi kemungkinan rekombinan elektron dan hole.
• Efek luas permukaan
Peningkatan luas permukaan dengan penurunan ukuran partikel akan meningkatkan aktivitas katalis. Peningkatan disebabkan adanya penambahan permukaan reaktif untuk adsorpsi substrat.
• Coupled-Photocatalyst
Meningkatkan pemisahan muatan sehingga memperpanjang energi pemisahan fotokatalis
Bahan :
• Kain katun (100%) 2x2 cm
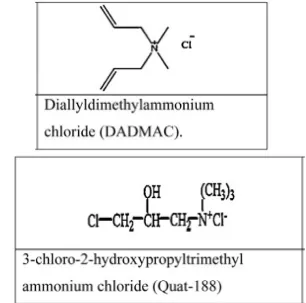
• 3-Chloro-2-hydroxypropyl trimethyl ammonium chloride (Quat 188) • Diallyl dimethyl ammonium chloride (DADMAC)
• 1,2,3,4-butane tetracarboxylic acid (BTCA) • Stearic acid
• Ethanol
• Sodium hypophosphite (SHP) • SiO2 nanoparticles
• Titanium Dioxide P25 (campuran fasa anatase/rutile)
Kain katun
• Dikationisasi menggunakan metode pad-batch menggunakan 20 g/L Quat-188 dan 8 g/L NaOH
(Dilakukan untuk DADMAC – NaOH)
Fig. 1. Chemical structures of Quat-188 and DADMAC. Kain katun terkationisasi
• Ditempatkan dalam kantong tertutup selama 24 pada suhu ruang
• Diperas
• Disimpan dalam kantong pada suhu ruang selama 24 jam
• Sampel dicuci dengan air dingin + asam asetat
• Dicuci beberapa kali dengan air dingin
• Dikeringkan pada suhu kamar
Kain katun terkationisasi
Larutan BTCA 30 g/L
• Dicampurkan dan distirrer 0,5% Nano-TiO2 Natrium Hipofosfit 6% w/w
• Disuspensikan dalam etanol
Larutan Campuran
• Kain Katun kationisasi dilapisi dengan 2x dip-nip
• Diperas
• Dikeringkan pada 80oC 5 menit
• Dikeringkan pada 180oC 3 menit
• Dibilas dengan air panas dan kemudian air dingin
• Dikeringkan pada suhu kamar
Katun tekstil terlapisi
Larutan BTCA 30 g/L
• Dicampurkan dan distirrer 0,5% Nano-TiO2 Natrium Hipofosfit 6% w/w
• Disuspensikan dalam etanol • Diultrasonik selama 30 menit
Larutan Campuran
• Kain Katun kationisasi dilapisi dengan 2x dip-nip • Diperas
• Dikeringkan pada 80oC 5 menit • Dikeringkan pada 180oC 3 menit
• Dibilas dengan air panas dan kemudian air dingin • Dikeringkan pada suhu kamar
Katun tekstil terlapisi
0,5% Nano-SiO2
• Dicelupkan dalam asam stearat 1wt% yang terlarut dalam aseton selama 10 menit
Kain Katun Terlapisi
Larutan Campuran
• Kain Katun kationisasi dilapisi dengan 2x dip-nip
• Diperas
• Dikeringkan pada 80oC 5 menit
• Dikeringkan pada 180oC 3 menit
• Dibilas dengan air panas dan kemudian air dingin
• Dikeringkan pada suhu kamar
Katun tekstil terlapisi
• Transmission Electron Microscopy
Penentuan ukuran partikel dan kehomogenan TiO2/SiO2
• Scanning Electron Microscopy/EDX
Morfologi partikel TiO2/SiO2 • X-Ray Diffraction
Penentuan fasa kristal TiO2/SiO2
• Tensile Strength
Penentuan kekakuan kain katun terlapisi
• Kekasaran Permukaan
Penentuan kekasaran kain setelah dilapisi
• Permibilitas udara
Penentuan kemampuan dilewati angin
• Faktor UV Protektor
Kemampuan menahan sinar UV
• Pengukuran anti basah
Kemampuan kain anti air
Suggested mechanism of the reaction of cationized cotton fabric with BTCA/TiO2 nanoparticles. Chemical structures of the cationized cotton.
(a) TiO2 on DADMAC cationized cotton (b) TiO2\SiO2 nanomaterials on
DADMAC cationized cotton
(c) TiO2 on Quat cationized cotton (d) TiO2\SiO2 nanomaterials on Quat
cationized cotton fabrics.
Pola XRD
Pola XRD menunjukan puncak yang khas dari senyawa TiO2 dan SiO2 pada katun,
The morphology of SiO2 nanoparticles and TiO2/SiO2 nanomaterials.
Effect of cationization/or nanoparticles treatments on the UV protection properties of cotton fabrics.
UV Protection
Sifat anti UV dari katun tekstil muncul dengan adanya lapisan TiO
2dan SiO
2Effect of cationization/or nanoparticles treatments on the antibacterial properties of cotton fabrics.
Anti Bakteri
Nanopartikel TiO
2dan SiO
2berperan dalam reaksi fotokatalitik dengan
terbentuknya hole dan e
-yang akan bereaksi mendegradasi protein yang
(A) Decolorization of MB dye on cotton fabric surface
(B) UV–vis absorption spectra of decolourization of methylen blue (10 mg/l) after 1 h
UV-irradiation.
Panel (B) is untreated cotton sample
(1) Quat cationized cotton treated with TiO2 nanoparticles
(2) DADMAC cationized cotton treated with TiO2 nanoparticles
(3) Quat cationized cotton treated with TiO2/SiO2 nanomaterials
(4) DADMAC cationized cotton treated TiO2/SiO2 nanomaterials.
Schematic illustration of preparation of hydrophobic surfaces on cotton fabric.
Sifat Hidrofobik
Shows drop penetration time (TEGEWA test) for cotton fabrics before and after treatment with stearic acid as hydrophobic additive [after 2 washing cycles].
Kesimpulan
Berdasarkan teori mengenai efek nanopartikel dan aplikasi nanomaterial dalam bidang
tekstil, dapat disimpulkan bahwa :
1.
Efek ukuran nano dari suatu material berpengaruh terhadap struktur, sifat elektronik,
luas permukaan, reaktivitas dari material.
2.
Sifat material berukuran bulk akan sangat berbeda dengan material bersifat nano.
3.
Material fotokatalis sangat bdipengaruhi dengan ukuran partikel, dimana semakin nano
ukuran fotokatalis maka akan semakin reaktif.
4.
Dari hasil penelitian mengenai faktor ukuran partikel dalam fotokatalis, TiO
2berukuran
nano sangat berpengaruh dalam terbentuknya hole dan elektron tereksitasi.
5.
Material semikonduktor sangat menarik dikembangkan sebagai fotokatalis dikarenakan