BAB II
TINJAUAN PUSTAKA
2.1 Uraian Bahan 2.1.1 Parasetamol
Menurut Ditjen BKAK., (2014) uraian tentang parasetamol sebagai berikut: Rumus struktur :
Gambar 2.1 Struktur Parasetamol Rumus Molekul : C8H9NO2 Berat Molekul : 151,16
Nama Kimia : 4-hidroksifenil asetamid.
Kandungan : Tidak kurang dari 98,0% dan tidak lebih dari 101,0% C8H9NO2 dihitung terhadap zat anhidrat.
Pemerian : Serbuk hablur, putih, tidak berbau, rasa sedikit agak pahit. Kelarutan : Larut dalam air mendidih, dalam natrium hidroksida
1 N, dan mudah larut dalam etanol.
Mekanisme kerja sebagai analgesik dengan cara menghambat prostaglandin sehingga mencegah sensitisasi reseptor rasa sakit oleh mediator-mediator rasa sakit. Sebagai antipiretik parasetamol dapat meningkatkan eliminasi panas pada penderita suhu tinggi dengan cara menimbulkan dilatasi pembuluh darah perifer dan mobilisasi air sehingga terjadi pengenceran darah dan pengeluaran keringat. Penurunan suhu tersebut adalah hasil kerja obat pada sistem saraf pusat yang melibatkan pusat kontrol suhu di hipotalamus (Tan dan Rahardja, 2007).
2.1.2 Ibuprofen
Menurut Ditjen BKAK., (2014) uraian tentang ibuprofen sebagai berikut: Rumus Struktur :
Gambar 2.2 Struktur Ibuprofen Rumus Molekul : C13H18O2 Berat Molekul : 206,28
Nama Kimia : 2-(p-isobutilfenil) asam propionat
Kandungan : Tidak kurang dari 97,0% dan tidak lebih dari 103,0% dihitung terhadap zat anhidrat.
Pemeriaan : Serbuk hablur, putih hingga hampir putih, berbau khas lemah
Kelarutan : Praktis tidak larut dalam air, sangat mudah larut dalam etanol, dalm methanol, dalam aseton, dan dalam kloroform, sukar larut dalam etil asetat.
Ibuprofen adalah turunan asam propionat golongan obat Non-Steroidal Anti Inflammatory Drugs (NSAIDs) yang mempunyai aktivitas antirematik, antiradang dan analgesik-antipiretik, digunakan terutama untuk mengurangi rasa nyeri akibat keradangan pada berbagai kondisi rematik dan artritis (Tan dan Rahardja, 2007).
2.2 Beberapa Metode Lain Penetapan Kadar Campuran Parasetamol dan Ibuprofen
Beberapa penelitian yang telah menetapan kadar campuran parasetamol dan ibuprofen dengan beberapa metode lain dapat dilihat pada Tabel 2.1.
Tabel 2.1. Beberapa Metode Lain Penetapan Kadar Campuran Parasetamol dan Ibuprofen
Berdasarkan Tabel 2.1 diatas penetapan kadar campuran parasetamol dan ibuprofen dengan KCKT dilakukan oleh Damayanti, dkk., (2003). Penggunaan KCKT relatif lebih mahal dan memerlukan tahap pemisahan sehingga memerlukan waktu yang lebih lama. Harshini, dkk., (2014) menggunakan metode spektrofotometri UV untuk penetapan kadar campuran parasetamol dan ibuprofen
dengan pelarut etanol. Dibandingkan dengan pelarut metanol-air, pelarut etanol menghasilkan spektrum senyawa yang tidak tersembunyi dalam suatu bentuk spektrum besar yang saling tumpang tindih. Andrianto (2009) menetapkan kadar parasetamol dan ibuprofen secara spektrofotometri ultraviolet metode panjang gelombang berganda dengan pelarut metanol.
Dibandingkan dengan pelarut campuran dapar posfat pH 7,2-etanol (91:9), parasetamol dan ibuprofen lebih cepat larut serta tidak mengubah spekrum dari masing-masing zat.
2.3 Spektrofotometri
Spektrofotometri adalah metode pengukuran yang didasarkan pada interaksi cahaya dengan materi. Suatu alat yang mengukuran panjang gelombang dan intensitas sinar ultraviolet - visible yang diserap oleh sampel disebut spektrofotometer ultraviolet - visibel. Ultraviolet berada pada panjang gelombang 200 − 400 nm, sedangkan visibel berada pada panjang gelombang 400 − 800 nm
(Dachriyanus, 2004).
Spektrofotometri sesuai dengan namanya adalah alat yang terdiri dari spektrometer dan fotometer. Spektrofotometri menghasilkan sinar dari spektrum dengan panjang gelombang tertentu, dan fotometer adalah alat pengukur in.tensitas cahaya yang ditransmisikan atau yang diabsorbsi (Khopkar, 2008). Ketika cahaya (monokromatik atau heterogen) mengenai medium homogen, suatu bagian dari dari cahaya yang ada akan dipantulkan, sebagian diserap medium, dan sisanya ditransmisikan, atau diteruskan (Day dan Underwood, 1998).
elektron tereksitasi lebih tinggi. Besarnya serapan radiasi tersebut sebanding dengan banyaknya molekul analit yang mengabsorpsi sehingga dapat digunakan untuk analisis kuantitatif (Setiadarma, dkk., 2004).
Menurut Gandjar dan Rohman (2007), metode spektrofotometri ultraviolet-visibel digunakan untuk menetapkan kadar senyawa obat dalam jumlah yang cukup banyak. Cara untuk menetapkan kadar sampel adalah dengan menggunakan perbandingan absorbansi sampel dengan absorbansi baku, atau dengan menggunakan persamaan regresi linier yang menyatakan hubungan antara konsentrasi baku dengan absorbansinya. Persamaan kurva baku selanjutnya digunakan untuk menghitung kadar dalam sampel.
2.3.1. Hukum Lambert-Beer
Menurut Hukum Lambert, serapan berbanding lurus terhadap ketebalan sel yang disinari. Sedangkan menurut Beer, serapan berbanding lurus dengan konsentrasi. Kedua pernyataan ini dapat dijadikan satu dalam Hukum Lambert-Beer, sehingga diperoleh bahwa serapan berbanding lurus terhadap konsentrasi dan ketebalan sel, hukum Lambert-Beer menyatakan bahwa intensitas yang diteruskan oleh larutan zat penyerap berbanding lurus dengan tebal dan konsentrasi larutan (Gandjar dan Rohman, 2007). Hukum Lambert-Beer umumnya dikenal dengan persamaan sebagai berikut:
A = a.b.c (g/liter) Dimana: A = absorbansi
a = absorptivitas b = tebal kuvet (cm)
c = konsentrasi
2.3.2 Komponen Spektrofotometer
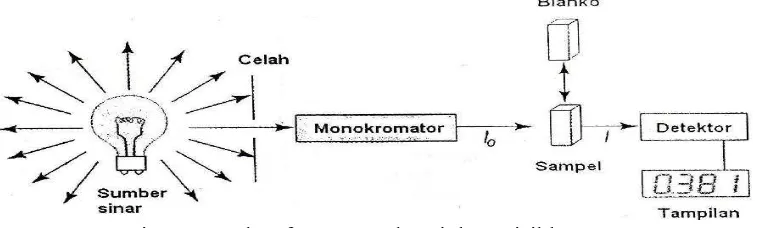
Spektrofotometer yang sesuai untuk pengukuran di daerah spektrum ultraviolet – visibel terdiri atas suatu sistem optik dengan kemampuan menghasilkan sinar monokromatis dalam jangkauan panjang gelombang 200 – 800 nm (Cairns, 2004). Suatu diagram sederhana spektrofotometer Ultraviolet - Visible ditunjukkan pada Gambar 2.3.
Gambar 2.3. Diagram spektrofotometer ultraviolet - visible i. Sumber cahaya
Sumber cahaya atau lampu yang digunakan adalah dua lampu terpisah yang digunakan secara bersama-sama, yang mencakup seluruh daerah ultraviolet-visible. Untuk senyawa yang menyerap pada daerah ultraviolet diperlukan lampu deuterium sedangkan untuk senyawa yang menyerap pada daerah visible digunakan lampu tungsten (Cairns, 2004).
ii. Celah
Celah dibuat dari logam yang kedua ujungnya diasah dengan sama (Khopkar, 1985).
iii. Monokromator
iv. Tempat sampel
Kuvet yang digunakan untuk tempat sampel pada pengukuran didaerah ultraviolet - visible biasanya terbuat dari silika atau glas (Cairns, 2004). v. Detektor
Peranan detekor adalah memberikan respon terhadap cahaya pada berbagai panjang gelombang (Khopkar, 1985).
Biasanya spektrofotometer dilengkapi dengan software yang berfungsi untuk mengolah data yang dapat dioperasikan malalui komputer yang telah terhubung dengan spektrofotometer. Spektrofotometri derivatif merupakan metode manipulatif terhadap spektra pada spektrofotometri UV-Visible (Watson, 2005).
2.3.3 Kegunaan Spektofotometri Ultraviolet
Kegunaan spektrofotometri ultraviolet dalam analisis kualitatif sangat terbatas karena rentang daerah rcadiasi yang relatif sempit hanya dapat mengakomodasi sedikit sekali puncak absorpsi maksimum dan minimum, karena itu identifikasi senyawa yang tidak diketahui tidak memungkinkan untuk dilakukan (Satiadarma, dkk., 2004).
Metode spektrofotometri memiliki beberapa keuntungan antara lain kepekaan yang tinggi, ketelitian yang baik, mudah dilakukan, cepat pengerjaannya dan dapat digunakan untuk menentukan senyawa campuran (Munson, 1984).
Ct Cs At As
sebagai berikut:Keterangan: As = Absorbansi baku pembanding At = Absorbansi zat dalam sampel Cs = Konsentrasi baku pembanding Ct = Konsentrasi zat dalam sampel
Penentuan kadar senyawa organik yang mempunyai struktur kromofor atau mengandung gugus kromofor, serta mengabsorpsi radiasi ultraviolet penggunaanya cukup luas (Satiadarma, dkk., 2004).
Spektrofotometer ini merupakan peralatan yang berbiaya murah sampai sedang dan mempunyai kepekaan analisis cukup tinggi. Karena luasnya ragam bahan farmasi dan bahan biokimia yang menyerap radiasi ultraviolet - visibel, maka metode ini banyak dipakai dalam analisis farmasi dan analisis klinik (Munson, 1984).
2.4 Analisis Multikompenen dengan Spektrofotometri Ultraviolet
Analisis kuantitatif campuran dua komponen merupakan teknik pengembangan analisis kuantitaif komponen tunggal. Prinsip pelaksanaanya adalah mencari absorban atau beda absorban di tiap-tiap komponnen yang memberikan korelasi yang linier terhadap konsentrasi, sehingga akan dapat dihitung masing-masing kadar campuran zat tersebut secara serentak atau salah satu komponen komponen dalam campurannya dengan komponen lainnya (Mulja dan Suharman, 1995).
a. Kemungkinan I
Gambar 2.4 Spektrum absorban senyawa X dan Y
Pada Gambar 2.4 diatas menunjukkan terjadi kemungkinan spektrum tidak tumpang tindih pada dua panjang gelombang yang digunakan. X dan Y semata-mata diukur masing-masing pada panjang gelombang 1 dan 2.
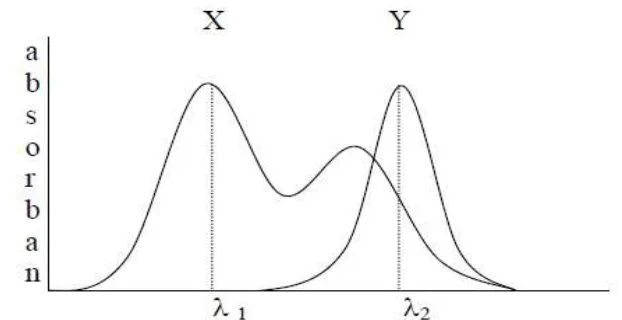
b. Kemungkinan II
Gambar 2.5 Spektrum absorban senyawa X dan Y, spektrum X bertumpang tindih pada spektrum Y
imi dikurangkan dari absorban terukur larutan pada 2 sehingga akan diperoleh absorban yang disebabkan oleh Y, kemudian konsentrasi Y dapat diukur dengan cara yang umum.
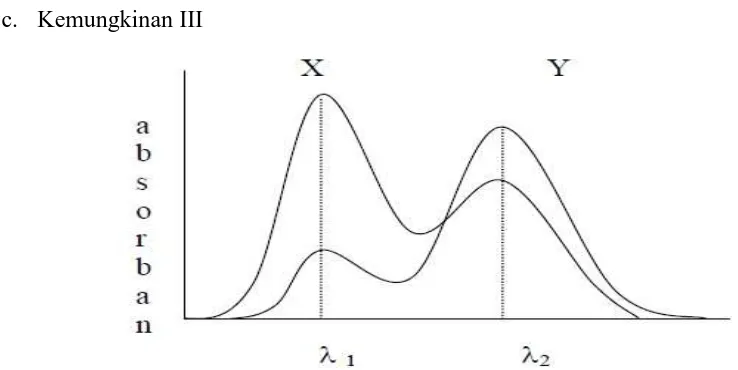
c. Kemungkinan III
Gambar 2.6 Spektrum absorban senyawa X dan Y saling tumpang tindih
Pada Gambar 2.6 spektrum X dan Y saling tumpang tindih secara keseluruhan. Pada absorbansi maksimum dari komponen X pada 1, komponen Y memiliki absorbansi tersendiri. Begitu juga komponen Y pada 2 , komponen X
memiliki absorbansi sendiri.
Menurut Andrianto (2009) pada penetapan kadar campuran multikomponen sulit dilakukan, sehingga untuk mengatasi hal itu diperkenalkan analisis multikomponen menggunakan prinsip persamaan regresi berganda melalui perhitungan matriks dengan metode pengamatan beberapa panjang gelombang berganda.
pemisahan komponen zat aktif karena kadar komponen kedua zat dapat ditetapkan secara bersama-sama (Andrianto, 2009).
2.5 Validasi Metode Analisis
Tujuan utama yang harus dicapai dari suatu kegiatan analisis kimia adalah dihasilkannya data hasil uji yang absah (valid). Secara sederhana hasil uji yang absah dapat digambarkan sebagai hasil uji yang mempunyai akurasi (accuracy) dan presisi (precission) yang baik. Validasi adalah suatu tindakan penilaian terhadap parameter tertentu pada prosedur penetapan yang dipakai untuk membuktikan bahwa parameter tersebut memenuhi persyaratan untuk penggunaannya (Harmita, 2004). Parameter analisis yang ditentukan pada validasi adalah akurasi, presisi, batas deteksi, batas kuantitasi, kelinieran, dan rentang (Gandjar dan Rohman, 2007).
2.5.1 Akurasi
Akurasi (kecermatan) adalah ukuran yang menunjukkan derajat kedekatan hasil analisis dengan kadar analit sebenarnya. Rentang nilai % akurasi analit yang dapat diterima adalah 90%-110% (Ditjen BKAK., 2014). Rentang ini bersifat fleksibel tergantung dari analit yang diperiksa, jumlah sampel, dan kondisi laboratorium. Akurasi bisa juga dilakukan dengan perhitungan matriks dari serapan komponen obat dan serapan campuran komponnen (Andrianto, 2009).
2.5.2 Presisi
Presisi merupakan ukuran keterulangan metode analisis dan biasanya
diekspresikan sebagai simpangan baku relatif dari sejumlah sampel yang berbeda
dan dinyatakan memiliki presisi yang baik apabila KV < 2% (Gandjar dan Rohman, 2007).
2.5.3 Linearitas
Linearitas suatu metode merupakan ukuran seberapa baik kurva kalibrasi yang menghubungkan antara konsentrasi (X) dengan serapan (Y). Linearitas dapat diukur dengan melakukan pengukuran tunggal pada konsentrasi yang berbeda-beda. Data yang diperoleh selanjutnya dapat ditentukan nilai kemiringan (slope), intersep, dan koefisien korelasinya (Gandjar dan Rohman, 2007; Watson, 2005). Suatu koefisien korelasi -1≤ r ≤ 1 dianggap menunjukkan linearitas. Persamaan suatu garis lurus menghasilkan Y = aX + b (Gandjar dan Rohman, 2007).
2.5.4 Rentang