27
EFEK PERBEDAAN SUHU INKUBASI TERHADAP PENETASAN
TELUR DAN KELANGSUNGAN HIDUP LARVA
IKAN KELABAU
THE EFFECT OF DIFFERENT INCUBATORY TEMPERATURE TO
THE EGG HATCHING AND SURVIVAL OF KELABAU LARVAE
1)
Rusila,
2)Muhammad, dan
3)Noor Arida Fauzana
1)Fakultas Perikanan dan Kelautan Program Studi Budidaya Perairan Universitas Lambung Mangkurat Jalan A. Yani Km 36,5 Simp 4, Banjarbaru, Indonesia
email : ejurnal.bpfpk@gmail.com
ABSTRAK
Penelitian ini bertujuan untuk mengetahui efek perbedaan suhu inkubasi terhadap penetasan telur dan kelangsungan hidup larva ikan kelabau (Osteochilus melanopleurus). Penetasan telur dan pemeliharaan larva dilakukan di akuarium ukuran 60x30x40 cm pada suhu 280C
(Perlakuan A), 300C (Perlakuan B) dan 320C (Perlakuan C) dengan padat tebar telur ±640
telur/akuarium. Hasil penelitian menunjukkan perlakuan terbaik diameter telur yaitu pada suhu inkubasi 32oC (2,114 mm) dan waktu penetasan ikan kelabau tercepat pada suhu
inkubasi 32oC (11 jam 56 menit). Perlakuan terbaik terhadap kelangsungan hidup larva ikan
kelabau pada suhu28oC yaitu 78,05%, diikuti suhu 30oC (66.19%), dan 32oC (45.37%).
Kata kunci :Kelabau, suhu inkubasi, penetasan telur dan kelangsungan hidup
ABSTRACT
This research aimed to find out the effect of different incubatory temperature to the egg hatching and survival of kelabau larvae (osteochilus melanopleurus). The egg hatching and larval rearing were conducted in aquarium with size 60x30x40 cm at the temperature 280C (treatment A), 300C (treatment B) and 320C (treatment C) with dense stocking egg ±640 egg/aquarium. The research results showed the best treatment diameter of eggs was when the incubatory temperature on 320C (2,114 mm) and the fastest time hatching of kelabau was when the incubatory temperature on 320C (11 hours 56 minutes). The best treatment against the survival of kelabau larvae was at 280C which was 78,05%, followed 300C (66.19%) , and 320C (45.37%).
28
PENDAHULUAN
Provinsi Kalimantan Selatan memiliki sungai-sungai dan perairan rawa yang luas sehingga terdapat beraneka ragam spesies ikan lokal yang hidup dan berkembang biak di wilayah ini. Ikan kelabau (Osteochilus melanopleurus)
merupakan salah satu jenis ikan lokal benilai ekonomis, hidup di perairan umum yang terdapat di daerah Kalimantan dan Sumatera. Sampai sekarang ikan kelabau masih belum dibudidayakan, produksinya masih terbatas tergantung pada musim-musim penangkapan (Mardani, 2014).
Populasi ikan kelabau dikhawatirkan terus berkurang bahkan punah yang diakibatkan oleh penangkapan yang dilakukkan secara terus-menerus yang tidak memperhatikan norma konservasi, sehingga ikan kelabau perlu dibudidayakan. Budidaya ikan kelabau memiliki beberapa permasalahan diantaranya adalah pada siklus reproduksinya membutuhkan habitat pemijahan yang terkontrol artinya lingkungan tempat pemijahan ikan harus sesuai dengan habitat aslinya. Menurut Andriyanto, Slamet & Ariawan (2013) salah satu faktor lingkungan yang dapat menentukan keberhasilan pemijahan adalah suhu pada saat inkubasi telur, Suhu dapat mempengaruhi pertumbuhan rata-rata dan menentukan waktu penetasan serta berpengaruh langsung pada proses perkembangan embrio dan larva. Perubahan temperatur perairan dan amplitude ketinggian permukaan air yang disebabkan pergantian musim dapat
menjadi pemicu untuk ikan melakukan pemijahan, terutama pada ikan di wilyah tropis (Zairin, Furuka & Aida, 2001). Suhu air rendah akan mengakibatkan proses penetasan pada telur ikan menjadi lambat karena lapisan kulit luar akan mengerut yang pada akhirnya menghambat proses kembang biak telur. Suhu penetasan yang rendah mengakibatkan waktu inkubasi telur akan semakin lama, sehingga embrio yang telah berkembang sempurna berada lama di dalam telur dan mempengaruhi daya tetas telur (Yustina Arnentis & Darmawanti, 2003).
Setijaningsih & Sidi (2011) melaporkan bahwa keberhasilan pemijahan ikan kelabau terjadi pada kisaran suhu 26º-28ºC dengan waktu ovulasi 13 jam dari penyuntikan kedua. Jumlah fekunditas rata-rata antara 39.862 butir per kg induk, tingkat penetasan antara dengan diameter saat ovulasi 1,4-1,5 mm dan berkembang sampai 2,7–3,3 mm setelah dibuahi.
Kegiatan pembenihan ikan lokal seperti ikan kelabau menjadi penting dilakukan melalui pendekatan manipulasi lingkungan. Perubahan suhu memberikan pengaruh yang sangat kuat terhadap proses fisiologis dan biologis. Faktor kualitas air terutama suhu air dapat menimbulkan pengaruh yang besar terhadap daya tetas dan kelangsungan hidup telur karena lapisan kulit luar telur akan mengerut karena suhu air rendah yang pada akhirnya akan menghambat proses kembang biak telur yang erat hubungannya dengan transfuse oksigen ke dalam telur.
29
Penelitian ini bertujuan untuk mengetahui efek perbedaan suhu inkubasi terhadap penetasan dan kelangsungan hidup ikan kelabau (Osteochilus
melanopleurus).
METODE PENELITIAN
Tempat dan Waktu Penelitian
Penelitian ini dilaksanakan di
Balai Perairan Budidaya Air Tawar
(BPBAT)
Mandiangin
Kecamatan
Karang
Intan
Kabupaten
Banjar
Provinsi Kalimantan Selatan. Secara
keseluruhan masa persiapan hingga
penyusunan laporan memerlukan waktu
selama 3 bulan.
Alat dan Bahan
Alat dan bahan yang digunakan
dalam penelitian adalah akuarium,
bakstyrofoam,
aerator,
heater,
mesinpompa
air,
serok,
sendok,
thermometer, mangkuk, cawan petri,
selang, penggaris, DO meter dan pH
meter,
buluayam,
spuit,
corongkacapiramida,
mikroskopmerkdino lite premier. Bahan
yang
digunakan
adalah
indukikankelabau, ovaprim, aquabidest,
natriumklorida, artemia, garamdan air.
Manajemen Penelitian
1. PersiapanAlatdanBahan
Akuarium berukuran 60x30x40 cm yang digunakan untuk penetasan telur dan pemeliharaan larva dibersihkan dan diisi air dengan volume 72 liter dan ketinggian air 35 cm, selanjutnya dipasang perangkat aerator dan heater. Air yang digunakan sebagai media hidup ikan adalah air sumur.
Induk kelabau yang digunakan merupakan koleksi BPBAT Mandiangin Kabupaten Banjar yang berasal dari sungai Kapuas. Induk betina yang digunakan mempunyai berat 0,5 kg sedangkan berat induk jantan yaitu 0,7 kg.
2. PemjahandanPembuahanIkan
Kelabau
Induk betina disuntik 2 kali dengan dosis penyuntikan hormon ovaprim 0,5 mL/kg dengan interval penyuntikan pertama dan kedua 6 jam. Penyuntikan hormon ovaprim untuk induk jantan dosisnya 0,3 mL/kg bersamaan dengan penyuntikan ke 2 induk betina.
Pengambilan sperma dilakukan dengan cara mengurut induk jantan. Sperma kemudian diencerkan dengan larutan Natrium Chlorida (NaCL). Setelah pengambilan sperma, induk betina distripping untuk mengeluarkan telurnya dan ditampung di baskom. Telur yang sudah ditampung dicampur dengan sperma dan diaduk dengan bulu ayam, kemudian air bersih dimasukkan sedikit demi sedikit sebanyak 5 kali sampai telur bersih dan mengembang, lalu dipindahkan ke akuarium yang berukuran 60x30x40 cm
30
yang telah dipersiapkan.Telur ditetaskan dalam akuarium dengan padat ±640 butir/akuarium. Telur diambil menggunakan gelas ukur dengan perhitungan volumetrik, satu gelas ukur dengan kapasitas 5 mL berisi ±640 telur ikan kelabau.
3. PenetasanTelur
Wadah penetasan telur berupa
akuarium,
setiap
akuarium
diatur
suhunya menggunakan heater sesuai
perlakuan. Telur diambil menggunakan
gelas
ukur
dengan
perhitungan
volumetrik. Hasil perhitungan satu
gelas ukur dengan kapasitas 5 mL berisi
±640
telur
ikan
kelabau
dan
dimasukkan ke dalam akuarium.
4. MasaPemeliharaan Larva
Tahap
selanjutnya
setelah
melakukan proses pemijahan yaitu
pemeliharaan larva, masa pemeliharaan
larva dimulai setelah telur menetas
menjadi larva hingga proses pendederan
dengan kurun waktu 7 hari. Telur yang
baru menetas menjadi larva akan
mendapatkan asupan makanan dari
kuning telur yang dibawanya hingga
umur 3 - 4 hari. Sebelum cadangan
kuning telur (yolk) tersebut habis, maka
larva akan diberikan pakan alami
berupa artemia sebanyak 60 mL
(±10.950 ekor) dengan pemberian
naupli artemia 3 kali sehari pada pagi,
siang dan sore yaitu pukul 07.00, 12.00,
17.00 Wita
Perlakuan
Perlakuan yang digunakan dalam
penelititanEfekPerbedaanSuhuInkubasit
erhadapPenetasanTelurdanKelangsunga
nHidup
Larva
IkanKelabau
(Osteochilusmelanopleurus) adalah :
1. Perlakuan A (
Suhu inkubasi 28°C).
2. Perlakuan B (
Suhu inkubasi30°C).
3. Perlakuan C (
Suhu inkubasi32°C).
Penelitian
ini
menggunakanRancanganAcakLengkap
(RAL) dengan 3perlakuan (A,B,C)
dan
3
ulangan
(1,2,3),
sehinggamenghasilkan
9
unit
percobaan.
Parameter Pengamatan
Parameter yang diamati pada penelitian ini adalah perkembangan telur, diameter telur, waktu penetasan telur, daya tetas telur, kelangsungan hidup dan kualitas air.
Perkembangan telur dan diameter telur di amati menggunakan Mikroskop yang telah diinstal pada perangkat komputer.Daya tetas diamati dengan menghitung jumlah telur yang berhasil menetas dengan rumus Kestemont (1988):
Daya tetas (%)=Jumlah telur yang menetasx 100 Jumlah telur yang diinkubasi
Tingkat kelangsungan hidup ikan dihitung menurut Effendi (2000), sebagai berikut :
31
SR = --- x 100 No
Keterangan :
SR = Tingkat kelangsungan hidup (%) Nt = Jumlah larva ikan kelabau pada saat tebar (ekor)
No = Jumlah larva ikan kelabau pada saat panen (ekor)
Data penunjang yang diukur dalam penelitian ini adalah DO dan pH. Parameter tersebut diukur masing-masing menggunakan DO meter dan pH meter.
HASIL DAN PEMBAHASAN A. Perkembangan Telur
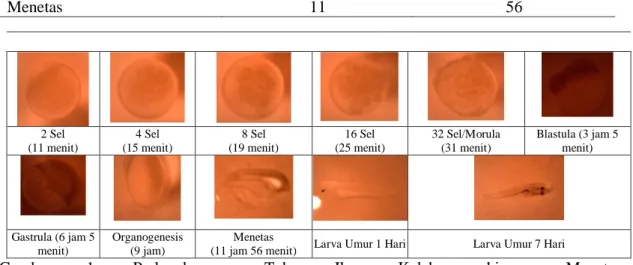
Hasil penelitian menunjukkan bahwa waktu yang diperlukan untuk perkembangan telur ikan kelabau setelah dibuahi hingga menetas adalah 11 jam 56 menit . Waktu perkembangan telur ikan kelabau disajikan pada Tabel 1 dan gambar perkembangannya pada Gambar 1.
Tabel 1. Fase Perkembangan Telur Ikan Kelabau
Perkembangan Telur Waktu Perubahan Fase
Jam Menit
Pembelahan zygot (2 sel) 00 11
Pembelahan zygot (4 sel) 00 15
Pembelahan zygot (8 sel) 00 19
Pembelahan zygot (16 sel) 00 25
Stadia morula (32 sel) 00 31
Stadia brastula 03 05
Stadia grastula 06 05
Stadia organogenesis 09 00
Menetas 11 56
Gambar 1. Perkembangan Telur Ikan Kelabau hingga Menetas
Proses embriogenesis dimulai dari stadia pembelahan sel telur, morula, blastula, gastrula, dan organogenesis yang selanjutnya menetas. Pembelahan merupakan proses pembelahan zigot menjadi unit-unit sel kecil. Pembelahan sel
telur ikan kelabau terjadi selama 31 menit setelah telur dibuahi, kemudian 11 jam 56 menit setelah pembuahan telur ikan kelabau menetas. Waktu yang diperlukan telur dari dibuahi hingga menetas pada penelitian ini lebih cepat dibanding penelitian yang
2 Sel (11 menit) 4 Sel (15 menit) 8 Sel (19 menit) 16 Sel (25 menit) 32 Sel/Morula (31 menit) Blastula (3 jam 5 menit) Gastrula (6 jam 5 menit) Organogenesis (9 jam) Menetas
32
dilaporkan Muttaqien (2016) yaitu 18 jam.Effendi (2002) mengemukakan bahwa faktor luar yang utama mempengaruhi pengeraman ialah suhu perairan, pencahayaan, gas (zat asam arang) yang dapat menyebabkan kematian embrio.
Selama masa inkubasi tahap perkembangan embrio berlangsung secara normal, pembentukan semua organ tubuh hampir sempurna ketika telur akan menetas. Waktu yang diperlukan untuk pembelahan zygot lebih cepat dibanding pada stadia morulla hingga organogenesis dan kemudian menetas. Telur ikan kelabau membelah secara meroblastis yaitu hanya bagian bagian sitoplasma yang membelah sedangkan kuning telurnya tidak ikut membelah.Telur mudah pecah pada masa
pembelahan zigot karena chorion yang lemah,pada tahap selanjutnya chorion menjadi semakin keras dan warna telur berubah menjadi putih susu. Hal ini menunjukan bahwa telur mempunyai perlindungan untuk menjaga gangguan dari luar selama proses perkembangan telur sampai telur menetas. Waktu penetasan telur, embrio sering merubah posisinya dalam cangkang, pergerakan-pergerakan tersebut untuk memecah cangkang dan terjadi penetasan.
B. Diameter Telur
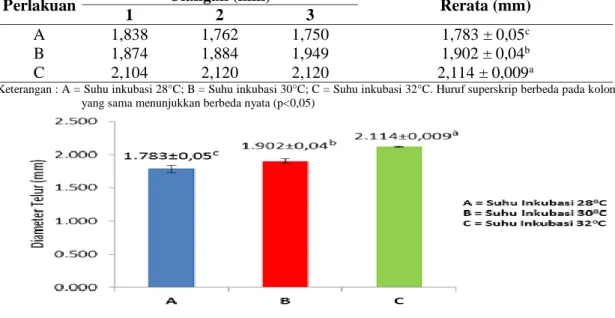
Rata-rata diameter telur ikan kelabau berkisar mulai 1,783 sampai 2,114 mm. Diameter telur ikan pada masing - masing perlakuan disajikan pada Tabel 2 dan rerata diameter telur ikan kelabau pada Gambar 2
Tabel 2. Rerata Diameter Telur Ikan Kelabau
Perlakuan Ulangan (mm) Rerata (mm)
1 2 3
A 1,838 1,762 1,750 1,783 ± 0,05c
B 1,874 1,884 1,949 1,902 ± 0,04b
C 2,104 2,120 2,120 2,114 ± 0,009a
Keterangan : A = Suhu inkubasi 28°C; B = Suhu inkubasi 30°C; C = Suhu inkubasi 32°C. Huruf superskrip berbeda pada kolom yang sama menunjukkan berbeda nyata (p<0,05)
Gambar 2. Rerata Diameter Telur Ikan Kelabau Hasil analisis keragaman (Anova)
Fhitung > Ftabel menunjukkan bahwa
perlakuan berpengaruh nyata terhadap diameter telur ikan kelabau, artinyaperbedaan suhu inkubasi
berpengaruh nyata terhadap diameter telur ikan kelabau.
Hasil uji BNJ menyatakan bahwa perlakuan C (32oC) berbeda sangat nyata
33
(32oC) berbeda sangat nyata dengan
perlakuan B (30oC), perlakuan B (30oC)
berbeda sangat nyata dengan perlakuan A (28oC).
Perlakuan C dengan suhu inkubasi 32ºC ternyata mempunyai diameter telur yang lebih besar dibandingkan perlakuan A (28 ºC ) dan perlakuan B (30 ºC). Hal ini di karenakan suhu berpengaruh terhadap lapisan kulit luar telur, selaras dengan pernyataan Yustina, Arnentis & Darmawanti (2003) bahwa suhu air rendah akan mengakibatkan proses penetasan pada telur ikan akan menjadi lambat karena lapisan kulit luar akan mengerut yang pada akhirnya menghambat proses kembang biak telur, dan waktu inkubasi telur akan semakin lama, sehingga embrio yang telah berkembang sempurna berada lama di dalam telur.
Diameter telur setiap spesies ikan berbeda antar individu, karena diameter telur dipengaruhi oleh lingkungan dan ketersediaan nutrisi (Basri, 2002). Selain itu juga diameter telur ada hubungannya dengan fekunditas, makin banyak telur
yang dipijahkan (fekunditas), maka ukuran diameter telurnya makin kecil, demikian pula sebaliknya (Tang & Affandi, 2001).
Effendie (2002), menyatakan bahwa semakin berkembang gonad, maka ukuran diameter telur yang ada didalamnya semakin besar sebagai hasil pengendapan kuning telur, hidrasi, dan pembentukan butir-butir minyak. Unus (2009), mengemukakan bahwa semakin besar ukuran diameter telur akan semakin baik, karena dalam telur tersebut tersedia makanan cadangan sehingga larva ikan akan bertahan lama. Larva yang berasal dari telur yang besar memiliki keuntungan karena memiliki cadangan kuning telur yang lebih banyak sebagai sumber energi sebelum memperoleh makanan dari luar. C. Waktu Penetasan Telur
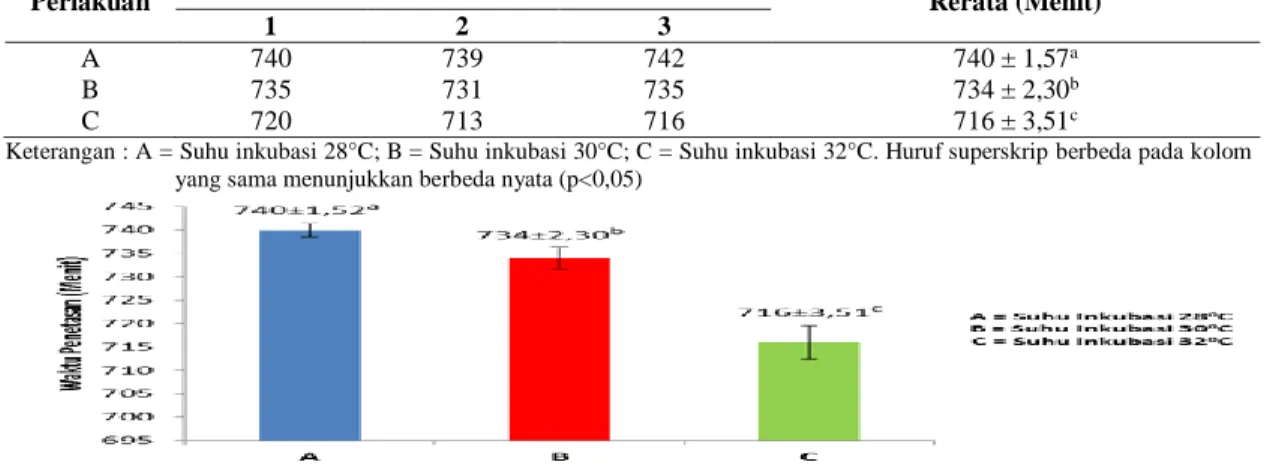
Rata-rata waktu penetasan telur ikan kelabau berkisar mulai 716 menit (11 jam 56 menit) sampai 740 menit (12 jam 20 menit). Waktu penetasan telur ikan pada masing-masing perlakuan disajikan pada Tabel 3 dan Rerata waktu penetasan telur ikan kelabau pada Gambar 3. Tabel 3. Rerata Waktu Penetasan Telur Ikan Kelabau
Perlakuan Ulangan (Menit) Rerata (Menit)
1 2 3
A 740 739 742 740 ± 1,57a
B 735 731 735 734 ± 2,30b
C 720 713 716 716 ± 3,51c
Keterangan : A = Suhu inkubasi 28°C; B = Suhu inkubasi 30°C; C = Suhu inkubasi 32°C. Huruf superskrip berbeda pada kolom yang sama menunjukkan berbeda nyata (p<0,05)
Gambar 3. Rerata Waktu Penetasan Telur Ikan Kelabau
740±1,52a 734±2,30b 716±3,51c 680 700 720 740 760 A B C W akt u P enet asa n (M e n it ) A = Suhu Inkubasi 280C…
34
Hasil uji BNJ memperlihatkan bahwa perlakuan C (32oC) berbeda sangat
nyata dengan perlakuan A (28oC),
perlakuan C (32oC) berbeda sangat nyata
dengan perlakuan B (30oC), perlakuan B
(30oC) berbeda nyata dengan perlakuan A
(28oC).
Penelitian ini menunjukkan bahwa ada pengaruh suhu terhadap waktu penetasan, ada kecenderungan bahwa semakin tinggi suhu semakin cepat pula penetasan telur ikan kelabau, hal tersebut sesuai dengan yang dijelaskan Sukendi (2003) dalam Putri, Muslim dan Fitrani (2013) bahwa penetasan telur akan lebih cepat pada suhu tinggi, karena pada suhu tinggi proses metabolisme akan terjadi lebih cepat sehingga perkembangan embrio juga akan lebih cepat dan pergerakan embrio dalam cangkang akan lebih intensif maka terjadi penetasan lebih cepat.
Andriyanto, Slamet & Ariawan (2013) menyatakan bahwa salah satu faktor lingkungan yang dapat menentukan keberhasilan pemijahan adalah suhu pada saat inkubasi telur, suhu dapat
mempengaruhi pertumbuhan rata-rata dan menentukan waktu penetasan serta berpengaruh langsung pada proses perkembangan embrio dan larva.Perubahan temperatur perairan dan amplitude ketinggian permukaan air yang disebabkan pergantian musim dapat menjadi pemicu untuk ikan melakukan pemijahan terutama pada ikan wilayah tropis (Zairin, Furuka & Aida, 2001). Yustina, Arnentis & Darmawanti (2003) menambahkan bahwa suhu air rendah akan mengakibatkan proses penetasan menjadi lambat, suhu penetasan yang rendah mengakibatkan waktu inkubasi telur akan semakin lama, sehingga embrio yang telah berkembang sempurna berada lama didalam telur dan mempengaruhi daya tetas telur.
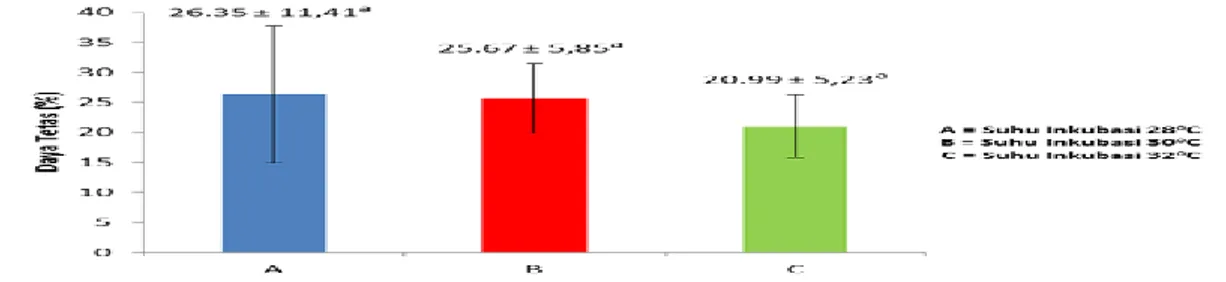
B. Daya Tetas Telur
Rata-rata daya tetas telur ikan kelabau berkisar antara 20,99-26,35%. Daya tetas telur ikan pada masing-masing perlakuan disajikan pada Tabel 4 dan rerata waktu penetasan telur ikan kelabau pada Gambar 4.
Tabel 4. Rerata Daya Tetas Telur Ikan Kelabau
Perlakuan Ulangan (%) Rerata (%)
1 2 3
A 39.53 20.00 19.53 26.35 ± 11,41a
B 19.37 26.71 30.93 25.67 ± 5,85a
C 15.31 25.62 22.03 20.99 ± 5,23a
Keterangan : A = Suhu inkubasi 28°C; B = Suhu inkubasi 30°C; C = Suhu inkubasi 32°C. Huruf superskrip yang sama pada kolom yang sama menunjukkan tidak berbeda nyata (p>0,05)
35
Hasil penelitian menunjukkan bahwa daya tetas telur ikan kelabau tidak berpengaruh nyata antara perlakuan, hal ini mengindikasikan bahwa perlakuan yang diterapkan masih dalam kisaran yang sesuai. Menurut Sutisna &Sutarmanto (1995) bahwa penetasan terjadi dengan cara penghancuran chorion oleh enzim yang dilakukan oleh kelenjar ektoderm dan oleh gerakan-gerakan embrio akibat peningkatan suhu, intensistas cahaya dan pengurangan oksigen terlarut, Tang & Affandi (2001) menambahkan bahwa, pada suhu yang terlalu tinggi atau terlalu rendah dapat menghambat proses penetasan telur, bahkan suhu yang terlalu ekstrim dapat menyebabkan kematian embrio dan kegagalan penetasan. Meskipun demikian nilai tersebut masih sangat rendah, begitu pula jika dibandingkan dengan penelitian
yang telah dilaporkan Muttaqien (2016) pada kisaran suhu 27,2-280C diperoleh
rerata daya tetas telur ikan kelabau 14,04-38,29%.
Rendahnya tingkat penetasan pada penelitian ini diduga berkaitan dengan kualitas telur. Waktu pemijahan ikan kelabau saat penelitian dilakukkan sudah melewati musim pemijahan yaitu pada musim kemarau (bulan Mei), sementara di alam ikan kelabau memijah pada saat awal musim penghujan (September - Maret). C. Kelangsungan Hidup Larva
Rata-rata Kelangsungan hiduplarva ikan kelabau berkisar antara 45,37-78,05%. Kelangsungan hidup larva ikan pada masing-masing perlakuan disajikan pada Tabel 5 dan rerata kelangsungan hidup larva ikan kelabau pada Gambar 5.
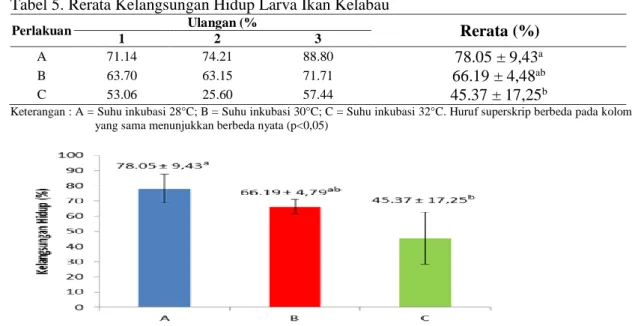
Tabel 5. Rerata Kelangsungan Hidup Larva Ikan Kelabau
Perlakuan 1 Ulangan (% 2 3 Rerata (%)
A 71.14 74.21 88.80 78.05 ± 9,43a
B 63.70 63.15 71.71 66.19 ± 4,48ab
C 53.06 25.60 57.44 45.37 ± 17,25b
Keterangan : A = Suhu inkubasi 28°C; B = Suhu inkubasi 30°C; C = Suhu inkubasi 32°C. Huruf superskrip berbeda pada kolom yang sama menunjukkan berbeda nyata (p<0,05)
Gambar 5. Rerata Kelangsungan Hidup Larva Ikan Kelabau Hasil uji Normalitas Liliefors dan
Homogenitas Ragam Barlett menunjukkan bahwa data menyebar normal dan homogen. Hasil analisis keragaman Anova
Fhitung > Ftabel menunjukkan bahwa
perlakuan berpengaruh nyata terhadap daya tetas telur ikan kelabau, artinya perbedaan
36
suhu inkubasi berpengaruh nyata terhadap kelangsungan hidup larva ikan kelabau.
Hasil uji Duncan menyatakan bahwa perlakuan C tidak berbeda nyata dengan perlakuan B, perlakuan C berbeda nyata dengan perlakuan A, perlakuan B tidak berbeda nyata dengan perlakuan A .
Suhu air yang berbeda pada media pemeliharaan larva ikan Kelabau menyebabkan tingkat kelangsungan hidup yang berbeda. Rata-rata tingkat kelangsungan hidup larva ikan kelabau berkisaran antara 45,37 - 78,05%. Persentase kelangsungan hidup tertinggi adalah perlakuan A, yakni 78,05%, kemudian disusul oleh perlakuan B, yakni sebesar 66,19%, yang terendah perlakuan C, yakni 45,37%. Nilai kisaran rata-rata persentase kelangsungan hidup ini cukup baik apabila dibandingkan dengan penelitian yang dilakukan oleh Akbar (2015) mengenai kelangsungan hidup larva ikan kelabau, yang mana hasil kelangsungan hidupnya <34,13%. Namun, apabila dibandingkan dengan penelitian yang dilakukan oleh Muttaqien (2016) maka hasilnya tidak jauh berbeda.
Hasil penelitian Muttaqien (2016), rata-rata tingkat kelangsungan hidup larva kelabau berkisar antara 21,83% - 79,73%. Persentase kelangsungan hidup tertinggi adalah perlakuan C (ketinggian air 35 cm/akuarium) yakni 79,73%, kemudian perlakuan B (ketinggian air 25 cm/akuarium) yakni sebesar 65,10% dan yang terendah pada perlakuan A (ketinggian air 15 cm/akuarium) yakni
sebesar 21,83%. Hasil penelitian ini menunjukkan bahwa semakin tinggi suhu media pemeliharaan larva semakin rendah tingkat kelangsungan hidup larva ikan kelabau.
Menurut Effendi (2004), kelangsungan hidup ikan adalah persentase ikan yang hidup dari seluruh ikan yang dipelihara setelah melewati masa pemeliharaan. Daya kelangsungan hidup ikan sangat bergantung kepada daya adaptasi ikan terhadap makanan yang baik, keadaan fisik ikan yang cukup kuat, kualitas makanan yang diberikan cukup baik, dan kualitas air yang cukup mendukung pertumbuhan. Hal lain yang diduga menyebabkan kematian adalah ketidakmampuan larva beradaptasi dengan baik pada suhu air yang berfluktuasi. Air dengan suhu yang berfluktuasi dapat mengakibatkan ikan stress dan mengakibatkan kematian bagi ikan. Morioka et al. (2008), menambahkan bahwa kematian larva dapat disebabkan oleh kanibalisme larva dengan padat tebar yang tinggi, ukuran larva yang bervariasi, kemampuan berlindung, dan kondisi pencahayaan. Kondisi lingkungan yang tidak menunjang (diluar kisaran normal) seperti terlalu tinggi suhu, adanya cahaya langsung dan lainnya dapat mengakibatkan kematian terutama pada masa transisi atau kritis.
F. Kualitas Air
Hasil pengukuran kualitas air pada penelitian diketahui bahwa pH awal 8,18 dan pH akhir 8,12 dan oksigem terlarut
37
(DO) awal dan akhir masing-masing 5,7 dan 5,1 mg/L
Hasil pengukuran rerata konsentrasi pH pada masa pemeliharaan berkisar antara 8,12 – 8,18 dan dapat dikatakan bersifat basa. Menurut Cholik (1986) pH yang cocok untuk semua jenis ikan berkisar antara 6,7-8,6.
Menurut Effendie (2003) kadar DO 1,0 – 5,0 mg/l ikan dapat bertahan hidup tetapi pertumbuhan terganggu, sedangkan kadar DO > 5,0 mg/l kadar DO yang disukai oleh semua organisme perairan.Oksigen terlarut untuk penetasan telur menurut (Wijayanti et al., 2011) telur ikan nilem dapat berkembang dan menetas dengan baik pada media dengan kandungan oksigen terlarut sebesar 4,0-4,2 ppm hingga 6,0-7,7 ppm. Kandungan oksigen terlarut (DO) selama penelitian masih berada dalam kisaran yang cukup baik.
KESIMPULAN
P
erlakuan
terbaik
terhadap
inkubasi telur ikan kelabau pada suhu
32
oC dengan diameter telur 2,114 mm
dan waktu penetasan 11 jam 56 menit.
Perlakuan
terbaik
terhadap
kelangsungan hidup larva ikan kelabau
pada suhu 28
oC (78,05%), diikuti suhu
30
oC (66.19%), dan 32
oC (45.37 %).
DAFTAR PUSTAKA
Akbar, Muhammad. 2015. Pengaruh Padat
Penebaran yang Berbeda
Terhadap Laju Pertumbuhan dan Kelangsungan Hidup Larva Ikan
Kelabau (Osteochilus
melanopleurus)yang Dipelihara dalam Akuarium. Kementerian Riset, Teknologi dan Pendidikan Tinggi Universitas Lambung Mangkurat, Fakultas Perikanan dan Kelautan. Banjarbaru.
Ali, Muhammad dan R.S Junianto, 2014. Pengaruh Lanjut Suhu pada Penetasan Telur terhadap Pertumbuhan dan Kelangsungan Hidup Benih Ikan Baung (Hemibagrus nemurus). Prosiding
Seminar Nasional Lahan
Suboptimal 2014. Palembang.
Andriyanto, W., B. Slamet dan I. M. D. J. Ariawan. 2013. Perkembangan Embrio dan Rasio Penetasan Telur Ikan Kerapu Raja Sunu (Plectropomalaevis) pada Suhu Media Berbeda. Jurnal Ilmu dan
Tekonologi Kelautan Tropis. 5 (1) :
192-207.
Basri, 2002. Penambahan Vitamin E Pada Pakan Buatan Induk Dalam Usaha Peningkatan Kecepatan Kematangan Gonad, Fekunditas, Kondisi Telur, Fertilitas dan Daya Tetas Telur Ikan Gurami (Ospheronemus gourami Lacepede). Fisheries Journal garing. I (11) : 56-82.
Cholik, F., dan A. Rahmat, 1986.
Manjemen kualitas Air Pada Kolam Budidaya Ikan. Direktorat
Jenderal Perikanan Research Centre. Jakarta. 51 halaman. Effendi, I. 2004. Pengantar Akuakultur.
Penebar Swadaya. Jakarta.
Effendi, M. I.,2002. Biologi Perikanan. Yayasan Pustaka Nusatama. Yogyakarta. 163 halaman.
Effendie, H. 2003. Telaah Kualitas Air
Bagi Pengelolaan Sumberdaya dan LingkunganPerairan. Penerbit Kanisius. Yogyakarta.
Hanafiah, K. A. 1993. Rancangan Percobaan Teori dan Aplikasi.
Fakultas Pertanian Universitas Sriwijaya. Palembang. 238 halaman.
Kestemont, P. 1988. Effect of Hormonal
Treatment on Induced Ovulation inGudgeon Gabio gabio L. Aquaculture, 63 : 373 - 385.
38
Kristanto, A. H., S. Asih, M. F. Sukadi & Yosmaniar. 2008. Prospek ikan kelabau (Osteochilus melanopleura Blkr), tengalan (Puntius bulu) dan Tengadak (Puntius sp) Sebagai Ikan Budidaya Baru. Prosiding
Seminar Nasional Perikanan 2008.
Sekolah Tinggi Perikanan Jakarta. Hal 133-135.
Mardani. 2014. Pengaruh Sumber Makanan yang Berbeda Terhadap Pertumbuhan Ikan Kelabau Padi (Osteochilus melanopleurus) yang Dipelihara Dalam Hapa di kolam.
Jurnal Ilmu Hewani Tropika Vol 3.
No. 1. Juni 2014. Universitas Kristen Palangkaraya.
Melianawati, R., P.T.Imanto dan M. Suastika, 2010. Perencanaan Waktu Tetas Telur Ikan Kerapu dengan Penggunaan Suhu Inkubasi yang Berbeda. Jurnal Ilmu dan Teknologi Kelautan Tropis 2 (2):
83-91.
Morioka, S., Ito, S., Kitamura, S., Vongvichith, B. 2008. Growth and
Morphological Development of Laboratory-Reared Larval and Juvenile Climbing PerchAnabas testudineus. Ichthyol Res. The
Ichthyological Society of Japan. Japan.
Muttaqien, Gusti Adly Adrian. 2016.
Variasi Ketinggian Air Untuk Daya Tetas Telur dan Kelangsungan Hidup Larva Ikan Kelabau
(Osteochilus melanopleura BLKR). Penelitian Skripsi. Fakultas Perikanan Dan Ilmu Kelautan ULM Banjarbaru.
Nugraha, D.N., M.N. Supardjo dan Subiyanto, 2012. Pengaruh Perbedaan Suhu terhadap Perkembangan Embrio, Daya Tetas Telur dan Kecepatan Penyerapan Kuning Telur Ikan Black Ghost (Apteronotus albifrons) pada Skala
Laboratorium. Journal of Management of Aquatic Resources 1 (1): 1-6.
Putri, D.A, Muslim dan M.Fitrani, 2013. Persentase Penetasan Telur Ikan Betok (Anabas testudineus) dengan Suhu Inkubasi yang Berbeda.
Jurnal Akuakultur Rawa Indonesia 1 (2): 184-191.
Setijaningsih, L., S. Asih. 2011. Keberhasilan Pembenihan Ikan Kelabau (Osteochilus
Melanopleura Blkr) sebagai Upaya
Konservasi Ikan Lokal Melalui Manipulasi Lingkungan dan Hormon. Balai Penelitian Budidaya Air Tawar. Prosiding Forum Nasional Pemacuan Sumber Daya Ikan III.
Sutisna, Dedy Heryadi dan Ratno Sutarmanto. 1995. Pembenihan
Ikan Air Tawar. Penerbit Kanisius.
Yogyakarta.
Tang, U.M. dan Affandi, R. 2001. Biologi
Reproduksi Ikan. Pusat Penelitian
Kawasan Pantai dan Perairan Iniversitas Riau, Pekanbaru. 153 hal.
Unus, F. 2009. Kajian Biologi Reproduksi
Ikan Malalugis Biru
(Decagteruslmacarellus cuutier) di Perairan Kabupaten Banggai Kepulauan. Disertasi. Program Pasca Sarjana Universitas Hasanuddin. Makasar. 105 Halaman.
Yustina, Arnentis dan Darmawanti. 2003.
Daya Tetas dan Laju Pertumbuhan Larva Ikan Hias Betta splendens di Habitat Buatan. Laboratorium Biologi. PMIPA,FKIP. Universitas
Riau. Jurnal Natur Indonesia. Zairin M Jr, Furukawa K, Aida K. 2001.
Induction of Spawning in the Tropical Walking Catfish, Clarias batrachus by temperature.