PENDAHULUAN
Isoflavon termasuk ke dalam golongan flavonoid yang memiliki distribusi terbatas dibandingkan dengan flavonoid. Flavonoid banyak ditemukan pada berbagai jenis tanaman, sedangkan isoflavon umumnya hanya terdapat pada kacang-kacangan, seperti kedelai. Kedelai memiliki kandungan isoflavon (genistein dan daidzein), fitosterol, asam fitat, asam lemak, saponin, asam fenolat, lesitin, dan inhibitor protease yang merupakan zat antioksidan dan dapat berkhasiat sebagai obat (Messina dalam Gilani & Anderson 2002). Kandungan isoflavon dalam kedelai lebih tinggi dibandingkan dengan tanaman bahan pangan lainnya. Pada kedelai, kandungan isolavon yang lebih tinggi terdapat pada biji kedelai, khususnya pada bagian hipokotil yang akan tumbuh menjadi tanaman (Anderson 1997).
Selama proses pengolahan, baik melalui proses fermentasi maupun non-fermentasi, senyawa isoflavon dapat mengalami transformasi, terutama melalui proses hidrolisis, sehingga dapat diperoleh senyawa isoflavon bebas (aglikon) yang memiliki aktivitas lebih tinggi dibandingkan dengan isoflavon dalam bentuk terikat (glikon). Senyawa aglikon tersebut adalah genistein, daidzein, dan sistein (Pawiroharsono 1994). Genistein dan daidzein mempunyai peran potensial dalam mencegah, mengurangi, atau menurunkan berbagai macam penyakit kronis, seperti jantung koroner, osteoporosis, kanker payudara, kanker prostat, kanker usus besar, kanker paru-paru, kanker kulit, dan kanker darah.
Genistein dan daidzein dikenal merupakan senyawa fitoestrogen, karena mempunyai sejumlah aktivitas estrogen. Estrogen dapat digunakan untuk pengobatan gejala pascamenopouse dan penghambat ovulasi untuk kontrasepsi (Murphy 1981). Kandungan zat dalam kedelai juga diyakini oleh masyarakat cukup berkhasiat untuk menyembuhkan penyakit diabetes, ginjal, anemia, rematik, diare, hepatitis, dan hipertensi.
Kedelai dapat diolah menjadi beberapa macam produk, antara lain susu kedelai, tempe, tauco, dan tahu. Proses pembuatan tahu memperoleh hasil samping berupa limbah cair dan limbah padat. Penggunaan limbah cair tahu masih terbatas, yaitu sebagian kecil digunakan sebagai biang tahu atau digunakan sebagai media pertumbuhan beberapa jenis bakteri. Hasil penelitian Ernita
(1995), menyebutkan bahwa limbah cair tahu masih mengandung senyawa isoflavon yaitu genistein dan daidzein. Limbah padat tahu, yaitu ampas tahu pada umumnya digunakan sebagai makanan ternak atau diolah menjadi oncom merah. Oncom merah merupakan makanan yang banyak dikonsumsi oleh masyarakat karena dapat menjadi sumber energi dan protein. Oncom merah dibuat dari ampas tahu yang diperkirakan masih mengandung senyawa-senyawa isoflavon seperti genistein dan daidzein. Jika kandungan genistein dan daidzein pada oncom merah cukup tinggi, maka oncom merah sangat baik digunakan sebagai makanan, karena proses pembuatannya lebih mudah dan harganya relatif lebih murah dibandingkan dengan produk olahan kedelai yang lain. Dengan demikian, ampas tahu dapat lebih bermanfaat bagi manusia daripada hanya digunakan sebagai makanan ternak. Oleh sebab itu, dalam penelitian ini akan dilakukan penentuan kadar genistein dan daidzein pada kedelai, ampas tahu, serta oncom merah menggunakan kromatografi cair kinerja tinggi (KCKT), dengan terlebih dahulu memurnikan ekstrak menggunakan flash chromatography.
Kedelai, ampas tahu, dan oncom merah yang dianalisis pada penelitian diharapkan mengandung genistein dan daidzein dengan kadar yang cukup tinggi, sehingga ampas tahu dan oncom merah dapat bernilai ekonomi.
TINJAUAN PUSTAKA
Kedelai
Kedelai merupakan tanaman semusim dengan tinggi berkisar 10–200 cm, berupa semak rendah, tegak, berdaun lebat, dapat bercabang sedikit atau banyak tergantung kultivar. Tanaman ini tumbuh baik pada tanah dengan pH 4.5 dan daerah pertumbuhannya tidak lebih dari 500 m di atas pemukaan laut. Nama botani kedelai yang dibudidayakan adalah Glycine max (Gambar 1), dengan klasifikasi sebagai berikut:
Ordo : Polypetale
Famili : Leguminosae Sub-famili : Papilionidae
Genus : Glycine
Gambar 1 Tanaman kedelai.
Kedelai sebagai bahan makanan mempunyai nilai gizi yang cukup tinggi dan merupakan sumber protein, lemak, vitamin, mineral, dan serat yang paling baik. Kandungan protein kedelai sekitar 30–50% (b/b), tetapi kadar karbohidratnya hanya sekitar 22–29% (b/b). Kadar lemaknya antara 16–20% (b/b), sedangkan kadar total gula sekitar 7.97% (b/b) (Liu 1997). Hasil utama dari kedelai adalah bijinya. Biji kedelai juga mengandung mineral-mineral kalsium, fosfor, besi, dan klor. Bentuk biji ada yang bundar, lonjong, gepeng, dan bulat telur. Warnanya tergantung dari varietas, ada yang hitam, kuning kehijauan, putih kekuningan, dan kuning gading (Gambar 2).
Gambar 2 Bentuk dan warna kacang kedelai. Ampas Tahu
Tahu merupakan makanan tradisional terbuat dari kedelai yang sudah lama dikenal di Indonesia dan memegang peranan penting dalam pola makan sehari-hari masyarakat. Proses pembuatan tahu terdapat pada Lampiran 1. Ampas tahu merupakan suatu limbah yang dihasilkan oleh industri pengolahan tahu dalam jumlah cukup banyak yang masih memiliki nilai gizi cukup tinggi. Limbah ini biasanya dimanfaatkan sebagai makanan ternak atau digunakan sebagai bahan utama dalam pembuatan oncom merah.
Ampas tahu merupakan produk olahan dari tahu yang kemungkinan sifat proteinnya hampir sama dengan tahu dan kedelai,
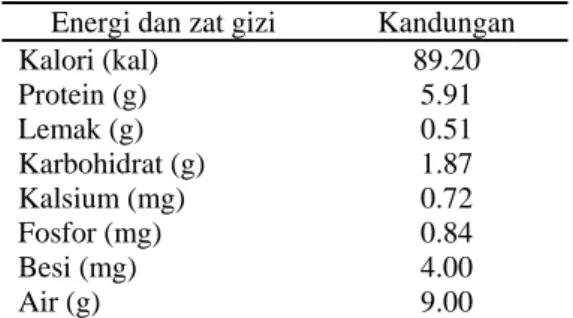
walaupun telah mengalami banyak perubahan karena perlakuan tertentu selama proses pembuatan tahu, seperti pemanasan. Protein ampas tahu masih mengandung 17% dari jumlah protein kedelai. Jika kadar protein kedelai sekitar 35%, maka protein yang terdapat pada ampas tahu sekitar 6% (Shurtleff & Aoyagi 1977). Kandungan kalori ampas tahu sangat tinggi, yaitu sebesar 89.20 kal dengan kadar lemak yang cukup rendah, yaitu 0.51 g/100g. Ampas tahu juga masih mengandung karbohidrat dan mineral-mineral logam, seperti kalsium, fosfor, dan besi walaupun dengan kadar yang cukup rendah (Tabel 1).
Tabel 1 Komposisi gizi ampas tahu per 100 g bahan basah.
Energi dan zat gizi Kandungan
Kalori (kal) 89.20 Protein (g) 5.91 Lemak (g) 0.51 Karbohidrat (g) 1.87 Kalsium (mg) 0.72 Fosfor (mg) 0.84 Besi (mg) 4.00 Air (g) 9.00
Sumber: Direktorat Gizi Depkes RI 1993
Oncom Merah
Oncom merah merupakan salah satu makanan tradisional yang proses pembuatannya dilakukan dengan fermentasi. Bahan baku yang umum digunakan dalam proses pembuatan oncom adalah bungkil kacang tanah atau ampas tahu. Bungkil kacang tanah adalah ampas yang berasal dari kacang tanah yang telah diambil minyaknya dengan proses pemerasan mekanis atau proses ekstraksi, sedangkan ampas tahu merupakan residu pengolahan kedelai menjadi tahu.
Ampas tahu sebenarnya masih mempunyai nilai gizi yang cukup tinggi, tetapi kebanyakan sifat organoleptiknya kurang disukai. Ampas tahu dengan proses fermentasi (oncom merah) lebih disukai sebagai makanan daripada tanpa fermentasi. Proses pembuatan oncom termasuk jenis fermentasi media padat, yaitu fermentasi yang menyertakan penggunaan substrat padat sebagai sumber karbon, nitrogen, dan energi.
Oncom merah terbuat dari kapang Neurospora sitophila yang memiliki warna jingga, merah, dan merah muda (Gambar 3). Kapang oncom dapat mengeluarkan enzim lipase dan protease yang aktif selama proses
fermentasi dan memegang peranan penting dalam penguraian pati menjadi gula, penguraian lemak, serta pembentukan sedikit alkohol dan berbagai ester yang berbau sedap dan harum. Dengan adanya proses fermentasi, maka struktur kimia bahan-bahan yang bersifat kompleks, akan terurai menjadi senyawa-senyawa yang sederhana, sehingga lebih mudah dicerna dan dimanfaatkan oleh tubuh (Siswono 2002).
Kapang Neurospora sitophila telah dibuktikan dapat mencegah terjadinya efek flatulensi (kembung perut). Selama proses fermentasi oncom, kapang akan menghasilkan enzim alpha-galaktosidase yang dapat menguraikan raffinosa dan stakiosa kedelai sampai pada level yang sangat rendah, sehingga tidak berdampak pada terbentuknya gas.
Gambar 3 Oncom merah. Isoflavon
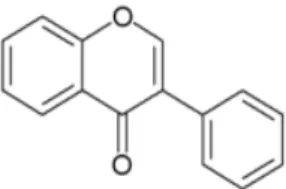
Isoflavon termasuk golongan senyawa flavonoid yang penyebarannya terbatas dan banyak terdapat pada tanaman kacang-kacangan, terutama kedelai (Harborne 1973). Isoflavon yang terdiri atas struktur dasar C6-C3-C6, secara alami disintesis oleh tumbuh-tumbuhan dan senyawa asam amino aromatik fenilalanin atau tirosin. Biosintesis ini berlangsung secara bertahap dan melalui sederetan senyawa antara, yaitu asam sinamat, asam kumarat, kalkon, dan isoflavon. Berdasarkan biosintesis tersebut, maka isoflavon digolongkan sebagai senyawa metabolit sekunder yang berfungsi mengendalikan pertumbuhan (fitohormon) dan mempertahankan diri dari makhluk lain, seperti insektisida (Achmadi et al. 1990). Isoflavon pada kedelai seperti genistein dan daidzein memiliki aktivitas estrogenik, antijamur, dan antikanker (Rakes & Russet 2001). Struktur umum isoflavon sebagai berikut:
Isoflavon terdiri atas 4 bentuk, yaitu aglikon, glikosida, malonil glikosida, dan asetil glikosida, yang masing-masing bentuk tersebut memiliki 3 jenis isomer. Bentuk aglikon terdiri atas genistein, daidzein, dan glisitein. Bentuk glikosida terdiri atas genistin, daidzin, dan glisitin. Malonil glikosida terdiri atas 6”-O-malonilgenistin, 6”-O -malonildaidzin, dan 6”-O-malonilglisitin. Asetil glikosida terdiri atas 6”-O -asetilgenistin, 6”-O-asetildaidzin, dan 6”-O -asetilglisitin (Gugger dalam Gilani & Anderson 2002). Jenis isoflavon yang paling banyak ditemukan dalam protein dan produk makanan kedelai adalah genistein dan daidzein (Friedman & Brandon 2001). Struktur molekul kedua senyawa tersebut dapat dilihat di bawah ini.
Genistein Daidzein Ekstrak kedelai mengandung lebih dari 35% genistein dan daidzein yang berada dalam bentuk glikosidanya, hanya 8–20% daidzein dan 13–19% genistein berada dalam bentuk bebas (Petterson & Kiesling 1984). Isoflavon yang berada dalam bentuk bebas bersifat kurang polar, sehingga cenderung lebih mudah larut dalam pelarut organik. Isoflavon dalam bentuk terikat bersifat lebih polar, sehingga mudah larut dalam air. Bentuk terikat ini dapat berupa isoflavon O-glikosida atau C-glikosida. Isoflavon di alam sering terdapat dalam bentuk O-glikosida (Markham 1982).
Isoflavon O-glikosida terbentuk dengan adanya ikatan hemiasetal inti isoflavon dengan glukosa. Oleh karena itu, senyawa ini menjadi kurang reaktif dan lebih mudah larut dalam air. Ikatan hemiasetal ini dapat dilepaskan dengan reaksi hidrolisis menggunakan HCl. Isoflavon C-glikosida terbentuk karena gula terikat langsung pada inti benzena isoflavon dengan ikatan karbon-karbon. Oleh karena itu, isolavon C-glikosida
Kromatografi lapis tipis (KLT) merupakan cara analisis cepat yang memerlukan bahan sangat sedikit, baik penyerap maupun cuplikannya. KLT dapat digunakan untuk memisahkan senyawa-senyawa yang sifatnya hidrofobik seperti lipida-lipida dan hidrokarbon yang sulit dikerjakan dengan kromatografi kertas. KLT juga dapat berguna untuk mencari eluen untuk kromatografi kolom, analisis fraksi yang diperoleh dari kromatografi kolom, identifikasi senyawa secara kromatografi, dan isolasi senyawa murni skala kecil. Pelarut yang dipilih untuk pengembang disesuaikan dengan sifat kelarutan senyawa yang dianalisis. Data yang diperoleh dari KLT adalah nilai Rf yang
berguna untuk penggabungan fraksi-fraksi. lebih tahan terhadap asam dibandingkan
dengan isoflavon O-glikosida (Ernita 1995). Teknik Pemisahan Isoflavon
Isolasi isoflavon dapat dilakukan dengan ekstraksi menggunakan beberapa jenis pelarut, umumnya digunakan eter atau etil asetat. Larutan HCl ditambahkan sebelum proses ekstraksi untuk menghidrolisis glikon-glikon dari isoflavon (Markham 1982). Penambahan larutan HCl pada proses hidrolisis dapat meningkatkan efisiensi ekstraksi isoflavon (Murphy 1981). Ekstraksi isoflavon juga dapat menggunakan pelarut organik, seperti metanol dan etanol yang telah dipanaskan, atau direfluks di dalam alkohol, sehingga menghasilkan konversi yang lengkap dari bentuk malonil glikosida, asetil glikosida, dan aglikon (Jackson & Rupasinghe dalam Gilani & Anderson 2002).
Teknik analisis untuk penentuan kadar isoflavon pada kedelai dapat menggunakan metode High Performance Liquid Chromatography (HPLC) atau Gas Chromatography (GC) sebagai metode utama, tetapi metode lain juga dapat digunakan, seperti Capillary Electrophoresis (CE), Time Resolved Fluoroimmunoassay (TR-FIA), luminescent immunoassays, ELISA, dan RIA (Jackson & Rupasinghe dalam Gilani & Anderson 2002).
Kondisi yang paling baik untuk menghidrolisis senyawa-senyawa isoflavon dari kedelai adalah dengan menggunakan larutan HCl 4 N, suhu sekitar 70°C selama 2 jam (Nicollier & Thompson 1982). Pemisahan dapat dilakukan dengan flash chromatography (kromatografi kilat) dan kromatografi lapis tipis (KLT). Flash chromatography digunakan untuk memisahkan suatu campuran. Flash chromatography menggunakan tekanan udara untuk menggerakkan pelarut melalui kolom (Gambar 4). Menurut Still et al. (1978), flash chromatography digerakkan tekanan udara hibrida antara tekanan sedang dan kolom kromatografi yang pendek, yang telah dioptimasi untuk pemisahan senyawa secara cepat. Tekanan udara akan membuat waktu pemisahan dengan flash chromatography lebih singkat dibandingkan dengan kromatografi kolom gravitasi. Adsorben yang digunakan pada teknik ini memiliki ukuran partikel yang lebih kecil, sekitar 200–400 mesh. Eluat yang ditampung dari hasil flash chromatography pada penelitian berdasarkan volume retensi. Pemurnian komponen hasil flash chromatography dilakukan dengan menggunakan metode kromatografi lapis tipis.
Kromatografi Cair Kinerja Tinggi (KCKT) Kromatografi adalah suatu istilah umum yang digunakan untuk bermacam-macam teknik pemisahan yang didasarkan atas partisi sampel diantara suatu fasa gerak yang bisa berupa gas ataupun cair dan fasa diam yang juga bisa berupa cairan ataupun suatu padatan. Kromatografi cair kinerja tinggi (KCKT) atau High Pressure Liquid Chromatography (HPLC) termasuk ke dalam kromatografi cair. KCKT merupakan suatu teknik kromatografi dengan fase gerak cairan dan fase diam berupa cairan atau padatan.
Kromatografi cair kinerja tinggi dapat digunakan untuk analisis, baik secara kualitatif maupun kuantitatif. Analisis kualitatif berdasarkan waktu retensi, sedangkan analisis kuantitatif berdasarkan luas puncak. Teknik ini memiliki banyak kelebihan dibandingkan dengan metode lain. Menurut Snyder & Kirkland (1979), kelebihan KCKT, yaitu mampu memisahkan molekul-molekul dari suatu campuran, mudah melaksanakannya, kecepatan analisis dan kepekaan yang tinggi, dapat dihindari terjadinya dekomposisi/ kerusakan bahan yang dianalisis, resolusi yang baik, dapat digunakan bermacam-macam detektor, dan kolom dapat digunakan kembali.
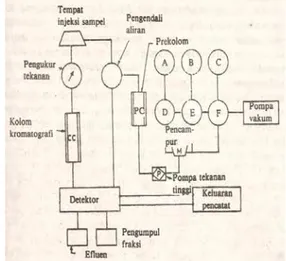
Komponen yang perlu diperhatikan dalam sistem KCKT adalah reservoir, pompa, injektor, kolom, integrator, dan detektor. Sampel yang diinjeksikan akan bergerak melalui kolom dan komponen sampel yang berada di dalam kolom akan dideteksi oleh suatu detektor. Signal yang terukur akan ditampilkan dalam bentuk kromatogram pada rekorder. Diagram alir KCKT dapat dilihat pada Gambar 5.
Gambar 5 Diagram alir KCKT.
BAHAN DAN METODE
Penelitian dilaksanakan dari bulan April sampai September 2008, di Pusat Studi Biofarmaka, LPPM IPB dan Laboratorium Kimia Analitik Departemen Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Bahan dan Alat
Bahan-bahan yang digunakan adalah kedelai, ampas tahu, dan oncom merah yang diperoleh dari pabrik pengolahan tahu di desa Cibadak (Ciampea), HCl 4 N, etanol, etil asetat, kloroform, metanol, air destilata, standar genistein dari Sigma, standar daidzein dari Fluka, dan plat KLT.
Alat-alat yang digunakan adalah botol vial, cawan porselen, peralatan kaca, corong pisah, bejana kromatografi, lampu UV, pompa vakum, rotavapor, instrumen flash chromatography Buchi C-60, instrumen KCKT dengan merk Waters.
Metode
Penelitian terdiri atas beberapa tahap, yaitu (1) penentuan kadar air; (2) ekstraksi; (3)
pemurnian; (4) penentuan kadar genistein dan daidzein (Lampiran 2)
Penentuan kadar air
Cawan porselen dikeringkan di oven pada suhu 105°C selama 1 jam, setelah itu didinginkan di desikator dan bobot cawan kosong ditimbang. Tiga gram contoh (kedelai, ampas tahu, dan oncom) dimasukkan ke dalam cawan dan dikeringkan di oven pada suhu 105°C selama 48 jam, setelah itu didinginkan di desikator dan ditimbang sampai bobotnya tetap. Penentuan kadar air dilakukan sebanyak 3 kali ulangan (triplo). Kadar air = Bobot awal – Bobot akhir x 100% Bobot awal
Ekstraksi
Sampel kedelai sebanyak 200 g direfluks menggunakan campuran HCl dan etanol dengan nisbah 1:8 selama 2 jam pada suhu 70°C. Campuran disaring dengan menggunakan pompa vakum dan kertas saring Whatman nomor 41. Filtrat yang diperoleh kemudian dipekatkan menggunakan rotavapor. Setelah itu, dilakukan pemisahan dengan etil asetat menggunakan corong pisah. Fraksi etil asetat yang diperoleh kemudian disaring, dan dipekatkan dengan rotavapor. Rendemen ekstrak dihitung menggunakan rumus sebagai berikut:
Rendemen ekstrak = a × 100% (1-kadar air) x b Keterangan: a = bobot ekstrak
b = bobot contoh
Hal yang sama dilakukan untuk ampas tahu dan oncom merah dengan bobot 600 g. Pemurnian komponen
Pemurnian ekstrak dilakukan dengan menggunakan flash chromatography. Sebanyak 0.5 gram ekstrak ditambah 1 mL eluen kloroform:metanol (9:1) diinjeksikan ke dalam alat flash chromatography dengan laju alir 0.3 mL/menit. Fase gerak yang digunakan adalah kloroform:metanol dengan nisbah 9:1 (Rinawati 1995). Fraksi-fraksi hasil flash chromatography ditampung berdasarkan volume retensi setiap 5 mL.
Fraksi-fraksi tersebut ditotolkan pada KLT analitik, kemudian dielusi menggunakan fase gerak kloroform:metanol (9:1). Setelah selesai dielusi, plat KLT diangkat, dikeringkan, dan