FORMULASI SEDIAAN SERUM KOSMETIK KOMBINASI EKSTRAK KELOPAK BUNGA ROSELA (Hibiscus sabdariffa L.) DENGAN MINYAK BIJI BUNGA MATAHARI (Helianthus annuus L.) SERTA UJI AKTIVITAS ANTIOKSIDAN SEDIAAN
DENGAN METODE DPPH
SKRIPSI
OLEH:
NURYA HAPIPAH SYOVIA INDAH NIM 171501180
PROGRAM STUDI SARJANA FARMASI FAKULTAS FARMASI
UNIVERSITAS SUMATER UTARA MEDAN
2021
ii
FORMULASI SEDIAAN SERUM KOSMETIK KOMBINASI EKSTRAK KELOPAK BUNGA ROSELA (Hibiscus sabdariffa L.) DENGAN MINYAK BIJI BUNGA MATAHARI (Helianthus annuus L.) SERTA UJI AKTIVITAS ANTIOKSIDAN SEDIAAN
DENGAN METODE DPPH
SKRIPSI
Diajukan sebagai salah satu syarat untuk memperoleh gelar Sarjana Farmasi pada Fakultas Farmasi Universitas Sumatera Utara
OLEH:
NURYA HAPIPAH SYOVIA INDAH NIM 171501180
PROGRAM STUDI SARJANA FARMASI FAKULTAS FARMASI
UNIVERSITAS SUMATER UTARA MEDAN
2021
PENGESAHAN SKRIPSI
FORMULASI SEDIAAN SERUM KOSMETIKKOMBINASI EKSTRAK KELOPAK BUNGA ROSELA (Hibisclls sabtlariffa L.) DENGAN MINYAK BIJI BUNGA MATAHARI (Helio1ltlllls am"m ... L.) SERTA U.lI AKTIVITAS ANTIOKSIDAN SEDIAAN
DENGAN METODE DPPH
OLEII:
NURYA IIAPII'AII SYOVIA INOAII NIM 171501180
Dipcrtahankan di Hadapan Pcnguji Skripsi Fakultas Farmasi Universitas Sumatera Utara Pada TanggaJ:
a;-,
Imam BagusSumanui,S.Farm.,M.Si.,Apt.
1\TJP 198212242014041001 Pcmbimbing
n,
~
Bayu Eko Prasetyo, S.Farm., M.Sc., Apt NIP 1984101220 19G31 009Ketua Program S di Sarjana Farmasi,
Dr. Sumaiyah, S.Si., M.Si., Apt.
NfI'I97712262008122002
111
Panitia Penguji:
Prof. D . Dra. Julia Reveny, M.Si., Apt.
NIPI95 07101986012001
n,/tf!MSi'
NIP 195310301980031002 Ap'~':'S'F'= " M.S;"APt.
NlP 19821224201404100A
iv
KATA PENGANTAR
Puji dan syukur kepada Allah SWT atas segala limpahan rahmat dan karunia- Nya serta kekuatan sehingga penulis dapat menyelesaikan penelitian dan penyusunan skripsi ini, serta tidak lupa shalawat dan salam untuk baginda Rasululullah SAW. Skripsi ini diajukan sebagai salah satu syarat untuk memperoleh gelar Sarjana Farmasi di Fakultas Farmasi Universitas Sumatera Utara dengan judul “Formulasi Sediaan Serum Kosmetik Kombinasi Ekstrak Kelopak Bunga Rosela merah (Hibiscus sabdariffa L.) Dengan Minyak Biji Bunga Matahari (Helianthus annuus L.) Serta Uji Aktivitas Antioksidan Dengan Metode DPPH”.
Pada kesempatan ini penulis mengucapkan terima kasih yang tulus dan ikhlas Kepada Bapak Imam Bagus Sumantri, S.Farm., M.Si., Apt dan Bapak Bayu Eko Prasetyo, S.Farm., M.Sc., Apt selaku pembimbing yang telah ikhlas dan sabar membimbing selama penelitian hingga selesainya penyusunan skripsi ini. Ucapan terima kasih juga penulis sampaikan kepada Ibu Prof. Dr. Dra. Julia Reveny, M.Si., Apt. selaku ketua penguji, dan Bapak Dr. Panal Sitorus, M.Si., Apt. sebagai anggota penguji yang telah memberikan kritik dan saran demi menyempurnakan skripsi ini. Penulis juga ingin menyampaikan rasa terima kasih kepada Dekan Fakultas Farmasi Universitas Sumatera Utara yaitu Ibu Khairunnisa, M.Pharm., Ph.D., Apt yang telah memberikan fasilitas selama masa pendidikan serta seluruh bapak dan Ibu dosen Fakultas Farmasi Universitas Sumatera Utara yang telah memberikan ilmu selama masa perkuliahan, dan juga ucapan terimakasih kepada bapak Imam Bagus Sumantri, S.Farm., M.Si., Apt. selaku penasehat akademik yang selalu memberi bimbingan selama masa perkuliahan.
P nulis ingin mcngucapknn tcrimnknsih dan pcnghargnan yang tuhls kcpada yalnndn Mnksum Nnsution. dan Ihunda Samsinar, serta kepadaabangda Anuar Ra. yid. Amri. Jayadi, Juni Adisaputra. Rinaldi Arif. Juliun Antomi, dan kakanda Iclti Kh limni. Nelli Erfina, dan Nurjannah serta seluruh keluarga besar alas doa, dukungnn dan pcngorbanan baik moril maupun materil selama perkuliahan hingga JXl1ydt:saian skripsi ini. Pcnulis jugamcngucapkan tcrima kasih kepadaseluruh snhnbat scrtn tcmnn-h.:mal1 yang sclalu saling mendukung dan memberikan scmangat yang tinda hcnliselamu masa pcrkuliahan lerkhususnya untuk grup Secret yaa, dan Urgentt.Serta ucapan lenmakasih unluk leman seperdopingan saya yaitu Annisa Hami Leslan, Nahda Aulia, dan Gebrina Riska yang sarna-sarna berjuang, dan membenkan semangat dari awal penelitian hingga penyusunan sknpsi ini dapat diselesaikan dengan baik.
Penulis menyadan sepenuhnya bahwa penulisan skripsi ini masih jauh dan kesempumaan, oleh karena ilu penulis mengharapkan saran dan kritik yang membangun demi kesempumaan shipsi ini.Akhir kata penulis berharap semoga sknpsi ini bermanfaat bagi ilmu pengetahuan khususnya di bidang farmasi.
v
Medan, 08 November2021 Penulis,
Nurya Hapipah Syovia Indah NIM 171501180
SURAT PEUNVATAAN OIUSINILITAS Saya yang bertanda tangan di bawah ini:
Nnma : Nurya Hapipah Syovia Indah
Nomor Induk Mahasiswa : 171501180 Program Studi : Sarjana Farmasi
Judul Skripsi : Formulasi Sediaan Serum KosmetikKombinasi Ekstrak Kelopak Bunga Rosela (Hihiscus sahJarijJa L.) Dengan Minyak Biji Bunga Matahari (He/ianthus annulls L.) Serta Uji Aktivitas Antioksidan Sediaan Dengan Metode DPPH.
Dengan ini menyatakan bahwa skripsi ini ditulis berdasarkan data dari hasil perkerjaan yang saya lakukan sendiri, dan bukan plagiat. Apabila dikemudian hari didalam skripsi saya ditemukan plagiat karena kesalahan saya sendiri, maka saya bersedia mcnerima sanksi apapun oleh Program Studi Sarjana Farmnsi Fakllltas Farmasi Universitas Sumatcra Utara. Saya tidak akan mcnllntut pihak manaplll1 dan bukan menjadi tanggungjawab pembimbing.
Demikianlah surat pemyataan ini saya pcrbuat dengan sebenamya dan dalam keadaan sehat untuk dapat digunakan jib diperlukan sebagaimana mestinya.
Medan,08 November 2021 Yang membuat pcrnyatnan,
in Indah
VI
vii
FORMULASI SEDIAAN SERUM KOSMETIK KOMBINASI EKSTRAK KELOPAK BUNGA ROSELA (Hibiscus sabdariffa L.) DENGAN MINYAK
BIJI BUNGA MATAHARI (Helianthus annuus L.) SERTA UJI AKTIVITAS ANTIOKSIDAN SEDIAAN DENGAN METODE DPPH
ABSTRAK
Latar Belakang : Kelopak bunga rosela merah memiliki kandungan antioksidan yang bermanfaat melindungi tubuh dari kerusakan akibat radikal bebas.
Dikombinasikan dengan minyak biji bunga matahari yang sering digunakan masyarakat untuk kecantikan karena mengandung vitamin E yang baik untuk kulit. Kelopak bunga rosela merah dan minyak biji bunga matahari dikombinasikan dalam sediaan serum kosmetik yang sedang berkembang dan popular dimasyarakat.
Tujuan : Untuk mengetahui aktivitas antioksidan sediaan serum kombinasi ekstrak kelopak bunga rosela merah dan minyak biji bunga matahari dengan metode pemerangkapan radikal bebas DPPH serta uji evaluasi sediaan.
Metode : Metode penelitian yang dilakukan meliputi pengolahan sampel, skrining fitokimia, uji karakterisasi, pembuatan minyak biji bunga matahari, pembuatan ekstrak etanol kelopak bunga rosela merah, pembuatan sediaan serum kombinasi ekstrak kelopak bunga rosela merah dengan konsentrasi 0,6% (FI), 0,8% (F2), 1,0% (F3) dengan minyak biji bunga matahari 2 % serta sediaan serum tanpa penambahan ekstrak (F0/blanko), pengujian aktivitas antioksidan sediaan menggunakan metode peredaman DPPH, dan evaluasi sediaan serum meliputi homogenitas, pengamatan stabilitas selama 12 minggu penyimpanan pada suhu kamar, pengukuran pH, pengamatan viskositas, pengukuran daya sebar, dan uji iritasi.
Hasil : Sediaan serum kosmetik kombinasi ekstrak etanol kelopak bunga Rosela merah (Hibiscus sabdariffa L.) dengan masing-masing konsentrasi dan minyak biji bunga Matahari (Helianthus annuus) memiliki potensi aktivitas sebagai antioksidan terhadap DPPH. Dengan aktivitas antioksidan dengan nilai IC50 FI sebesar 82,08 µg/mL, F2 sebesar 78,68 µg/mL, F3 sebesar 75,84 µg/mL. Dan hasil evaluasi setiap formula homogen, stabil selama penyimpanan selama 12 minggu pada suhu kamar, dengan pH rentang yang diperoleh 5,1-6,3, viskositas pada rentang 461,7-498,3 mPa.s, dan diameter daya sebar dalam rentang 5,6-6,7 cm.
Kesimpulan : Hasil uji aktivitas antioksidan pada masing-masing formula diperoleh bahwa aktivitas antioksidan pada F3 lebih besar dibanding dengan aktivitas antioksidan pada F2 dan FI, dan aktivitas antioksidan dari F2 lebih besar dibanding dengan aktivitas antioksidan FI. Sehingga diperoleh urutan terbaik sediaan serum yaitu F3, F2, dan F1.
Kata Kunci : antioksidan, IC50, kelopak bunga rosela, minyak biji bunga matahari, serum
viii
FORMULATION OF COSMETIC SERUM PREPARATIONS COMBINATION ROSELA MERAH PETAL EXTRACT (Hibiscus sabdariffa L.) WITH SUNFLOWER SEED OIL (Helianthus annuus L.) AND
TESTING THE ACTIVITY OF ANTIOXIDANT PREPARATIONS WITH DPPH METHOD
ABSTRACT
Background : Rosela petals have antioxidant content that is useful to protect the body from free radical damage. Combined with sunflower seed oil which is often used by the public for beauty because it contains vitamin E which is good for the skin. Rosela petals and sunflower seed oil are combined in a growing and popular cosmetic serum preparation in society.
Objective: Knowing the antioxidant activity of serum preparations, the combination of rosela petal extract and sunflower seed oil with the DPPH free radical imaging method and preparation evaluation tests..
Methods: The research methods conducted include sample processing, phytochemical screening, characterization test, sunflower seed oil manufacturing, rosela petal ethanol extract, 2% sunflower petal combination serum preparations and serum preparations without extract addition (F0/blanko), testing of dosage antioxidant activity using DPPH damping method, and evaluation of serum preparations including homogeneity, Stability observations during 12 weeks of storage at room temperature, pH measurements, viscosity observations, scatter power measurements, and irritation tests.
Result : Cosmetic serum preparations combination rosela petal ethanol extract (Hibiscus sabdariffa L.) with each concentration and sunflower seed oil (Helianthus annuus) has potential activity as an antioxidant against DPPH. With antioxidant activity with an IC50 FI value of 82.08 μg/mL, F2 of 78.68 μg/mL, F3 of 75.84 μg/mL. And the evaluation results of each formula are homogeneous, stable during storage for 12 weeks at room temperature, with pH range obtained 5.1-6.3, viscosity in the range of 461.7-498.3 mPa.s, and scatter power diameter in the range of 5.6-6.7 cm.
Conclusion: The results of antioxidant activity test in each formula obtained that antioxidant activity in F3 is greater than the antioxidant activity in F2 and FI, and antioxidant activity of F2 is greater than the antioxidant activity of FI. So obtained the best order of serum preparations namely F3, F2, and F1.
Keywords: antioxidant, IC50, rosela petals, serum, sunflower seed oil.
ix
DAFTAR ISI
HALAMAN SAMPUL ... i
HALAMAN JUDUL ... ii
HALAMAN PENGESAHAN ... iii
KATA PENGANTAR ... iv
HALAMAN PERNYATAAN ORSINILITAS ... v
ABSTRAK ... vii
ABSTRACT ... viii
DAFTAR ISI ... xi
DAFTAR GAMBAR ... xii
DAFTAR TABEL ... xiii
DAFTAR LAMPIRAN ... xiv
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Rumusan Masalah ... 4
1.3 Hipotesis Penelitian... 4
1.4 Tujuan Penelitian ... 5
1.5 Manfaat Penelitian ... 5
1.6 Kerangka Pikir Penelitian ... 5
BAB 2 TINJAUAN PUSTAKA ... 7
2.1 Tanaman Rosela ... 7
2.1.1 Sistematika Tanaman ... 7
2.1.2 Nama lain Tanaman ... 7
2.1.3 Morfologi Tanaman ... 8
2.1.4 Kandungan kimia tanaman ... 9
2.1.5 Manfaat tanaman ... 9
2.2 Tanaman Bunga Matahari ... 10
2.2.1 Sistematika Tanaman ... 10
2.2.2 Morfologi Tanaman ... 10
2.2.3 Kandungan Kimia ... 11
2.2.4 Manfaat Tanaman ... 11
2.3 Ekstraksi ... 11
2.4 Serum Kosmetik. ... 13
2.5 Morfologi Bahan ... 15
2.6 Metode DPPH sebagai Pengujian Antioksidan ... 17
2.7 Bagian-Bagian Dari Alat Spektro UV-Vis ... 20
BAB 3 METODE PENELITIAN ... 23
3.1 Jenis Penelitian ... 23
3.2 Alat dan Bahan ... 23
3.2.1 Alat ... 23
3.2.2 Bahan. ... 24
3.3 Prosedur Penelitian. ... 25
3.3.1 Pembuatan Simplisia ... 25
3.3.1.1 Pengambilan Sampel ... 25
3.3.1.2 Identifikasi Sampel ... 25
3.3.1.3 Pembuatan Simplisia ... 25
3.3.1.4 Pembuatan Minyak Biji Bunga Matahari ... 25
3.3.2 Pembuatan Pereaksi ... 26
x
3.3.2.1 Pereaksi Asam klorida 2N ... 26
3.3.2.2 Pereaksi Asam Sulfat 2N ... 26
3.3.2.3 Pereaksi Besi (3) Klorida ... 26
3.3.2.4 Pereaksi Bouchardat ... 26
3.3.2.5 Pereaksi Dragendroff ... 26
3.3.2.6 Pereaksi Mayer ... 26
3.3.2.7 Pereaksi Molish ... 27
3.3.2.8 Pereaksi Timbal (2) Asetat 0,4M ... 27
3.3.3 Skrining Fitokimia Simplisia Sampel... 27
3.3.3.1 Pemeriksaan Alkaloid ... 27
3.3.3.2 Pemeriksaan Flavonoid ... 28
3.3.3.3 Pemeriksaan Glikosida ... 28
3.3.3.4 Pemeriksaan Saponin ... 29
3.3.3.5 Pemeriksaan Tanin ... 29
3.3.3.6 Pemeriksaan Steroid/Triterpenoid ... 29
3.3.4 Pemeriksaan Karakteristik Simplisia Sampel... 30
3.3.4.1 Pemeriksaan Makroskopik dan Organoleptik ... 30
3.3.4.2 Mikroskopik ... 30
3.3.4.3 Penetapan Kadar Air ... 30
3.3.4.4 Penetapan Sari Larut Dalam Air ... 31
3.3.4.5 Penetapan Sari Larut Dalam Etanol ... 31
3.3.4.6 Penetapan Kadar Abu Total ... 31
3.3.4.7 Penetapan Kadar Abu Tidak Larut Asam ... 32
3.3.4.8 Skrining Fitokimia Minyak ... 32
3.3.5 Pembuatan Ekstrak Sampel ... 33
3.3.6 Pembuatan Formulasi Serum ... 33
3.3.6.1 Formulasi Orientasi ... 33
3.3.6.2 Formula Orientasi sediaan serum kosmetik kombinasi ekstrak etanol 96 % kelopak bunga Rosela dan minyak biji bunga Matahari ... 34
3.3.6.3 Prosedur Formulasi ... 35
3.3.7 Karakterisasi Fisik Sediaan ... 35
3.3.7.1 Pengamatan Organoleptik ... 35
3.3.7.2 Pemeriksaan Homogenitas ... 35
3.3.7.3 Pemeriksaan Tipe Emulsi Serum ... 36
3.3.7.4 Pengukuran PH ... 36
3.3.7.5 Viskositas ... 36
3.3.7.6 Uji Daya Sebar ... 36
3.3.7.7 Uji Iritasi ... 37
3.3.8 Pengujian Aktivitas Antioksidan ... 38
3.3.8.1 Prinsip Metode DPPH ... 38
3.3.8.2 Pembuatan LIB DPPH 0.5mM ... 38
3.3.8.3 Pembuatan Larutan Blanko ... 38
3.3.8.4 Pengukuran Panjang Gelombang Serapan Maksimum DPPH ... 38
3.3.8.5 Penentuan waktu kerja (operating time) ... 38
3.3.8.6 Pembuatan larutan induk baku serum kosmetik ... 38
3.3.8.7 Pembuatan larutan uji serum kosmetik ... 39
3.3.8.8 Pembuatan larutan induk baku vitamin C ... 39
3.3.8.9 Pembuatan larutan uji vitamin C ... 39
3.3.8.10 Pengukuran serapan ... 39
xi
3.3.8.11 Penentuan persen inhibisi, nilai IC50 ... 40
BAB IV HASIL DAN PEMBAHASAN ... 41
4.1 Hasil Identifikasi Tanaman ... 41
4.1.1 Hasil Identifikasi Tanaman Rosela ... 41
4.1.2 Hasil Identifikasi Tanaman bunga Matahari... 41
4.2 Hasil Karakterisasi Simplisia ... 41
4.2.1 Hasil Pemeriksaan Makroskopik ... 41
4.2.2 Hasil Pemeriksaan Mikroskopik ... 41
4.2.3 Hasil Karakterisasi Simplisia Kelopak Rosela ... 42
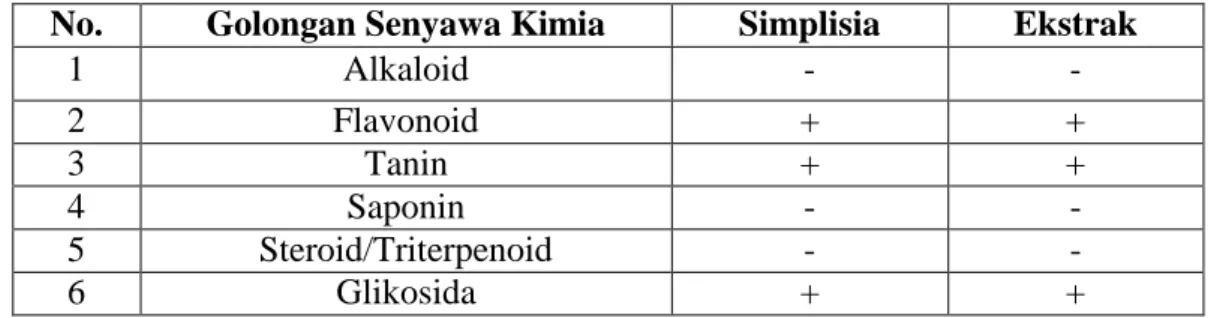
4.3 Hasil Skrining Fitokimia ... 43
4.4 Hasil Ekstraksi Kelopak Rosela ... 44
4.5 Alasan modifikasi formula ... 44
4.6 Hasil Evaluasi Sediaan ... 46
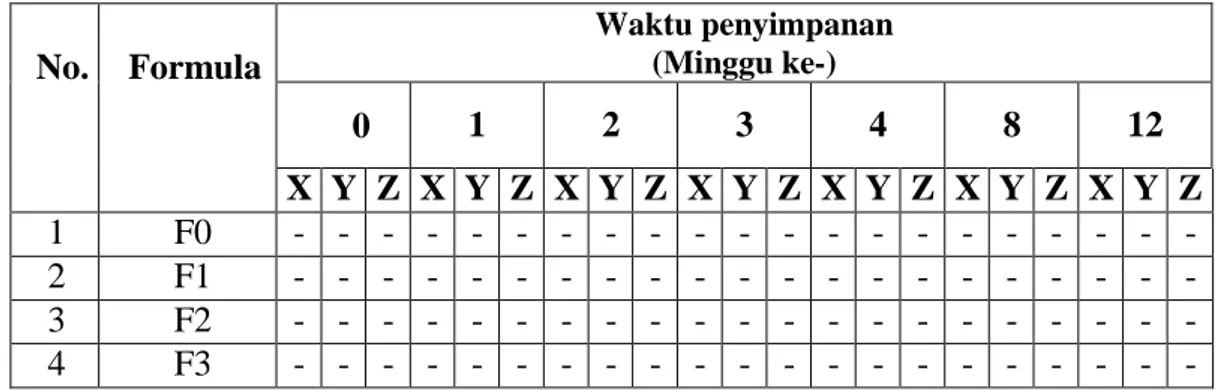
4.6.1 Hasil Uji Stabilitas Fisik ... 46
4.6.2 Hasil Pemeriksaan Homogenitas ... 48
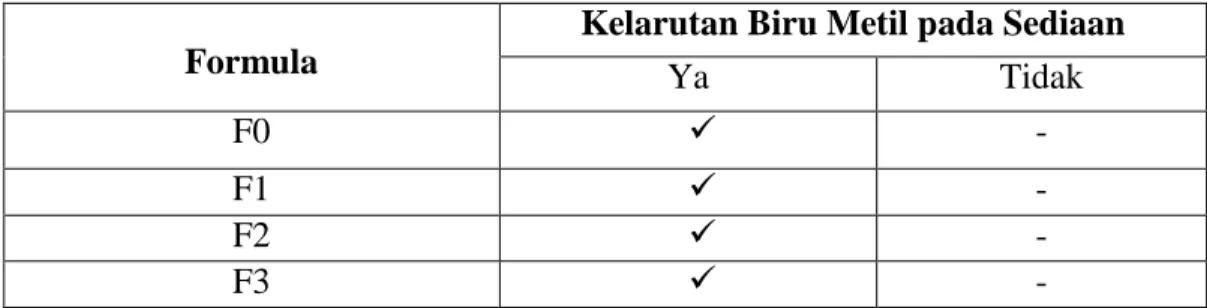
4.6.3 Hasil penentuan tipe emulsi ... 48
4.6.4 Hasil Pengukuran pH sediaan ... 49
4.6.5 Hasil Pengukuran Viskositas ... 51
4.6.6 Hasil Uji Diameter Daya Sebar Sediaan Serum ... 52
4.6.7 Hasil Uji Iritasi ... 53
4.7 Hasil Analisis Aktivitas Antioksidan... 54
4.7.1 Hasil Penentuan Panjang Gelombang Serapan Maksimum ... 54
4.7.2 Hasil Penentuan Waktu Kerja (Operating Time) ... 55
4.7.3 Hasil Analisis Uji Aktivitas ... 57
4.7.3.1 Hasil Analisis Uji Aktivitas Antioksidan Ekstrak Kelopak Bunga Rosela ... 57
4.7.3.2 Hasil Analisis Uji Aktivitas Antioksidan Sediaan Serum Kombinasi Ekstrak Kelopak Bunga Rosela Dan Minyak Biji Bunga Matahari ... 58
4.7.4 Hasil Analisis Nilai IC50(Inhibitory Concentration) ... 63
BAB V KESIMPULAN DAN SARAN ... 66
5.1 Kesimpulan ... 66
5.2 Saran ... 66
DAFTAR PUSTAKA ... 67
xii
DAFTAR GAMBAR
1.1 Kerangka Pikir Penelitian ... 6
2.1 Reaksi DPPH dengan senyawa antioksidan ... 18
4.1 Grafik lama penyimpanan terhadap pH serum... 50
4.2 Grafik lama penyimpanan terhadap viskositas sediaan serum ... 51
4.3 Grafik diameter daya sebar (cm) ... 52
4.4 Spektrum pengukuran serapan maksimum larutan DPPH 40 µg/mL dalam metanol ... 55
4.5 Grafik Operating Time ... 56
4.6 Grafik Hasil Uji Aktivitas Antioksidan ekstrak etanol bunga rosela ... 57
4.7 Grafik Hasil Uji Aktivitas Antioksidan Sediaan Serum Kosmetik Formulasi 0 (tanpa kombinasi ekstrak kelopak bunga rosela 0.6% dan minyak biji bunga matahari 2 %) ... 58
4.8 Grafik Hasil Uji Aktivitas Antioksidan Sediaan Serum Kosmetik Formulasi I (kombinasi ekstrak kelopak bunga rosela 0.6% dan minyak biji bunga matahari 2 %)... 59
4.9 Grafik Hasil Uji Aktivitas Antioksidan Sediaan Serum Kosmetik Formulasi 2 (kombinasi ekstrak kelopak bunga rosela 0.8% dan minyak biji bunga matahari 2 %)... 60
4.10 Grafik Hasil Uji Aktivitas Antioksidan Sediaan Serum Kosmetik Formulasi 3 (kombinasi ekstrak kelopak bunga rosela 0.8% dan minyak biji bunga matahari 2 %)... 61
4.11 Grafik % Aktivitas Peredaman radikal bebas DPPH Oleh Vitamin C ... 62
xiii
DAFTAR TABEL
2.1 Kategori nilai IC50 sebagai antioksidan ... 19
3.1 Formula serum kosmetik konsentrasi dalam (%v/v)... 33
4.1 Hasil karakteristik simplisia kelopak rosela (Hibiscus sabdariffa L.) ... 42
4.2 Hasil skrining fitokimia simplisia kelopak rosela ... 43
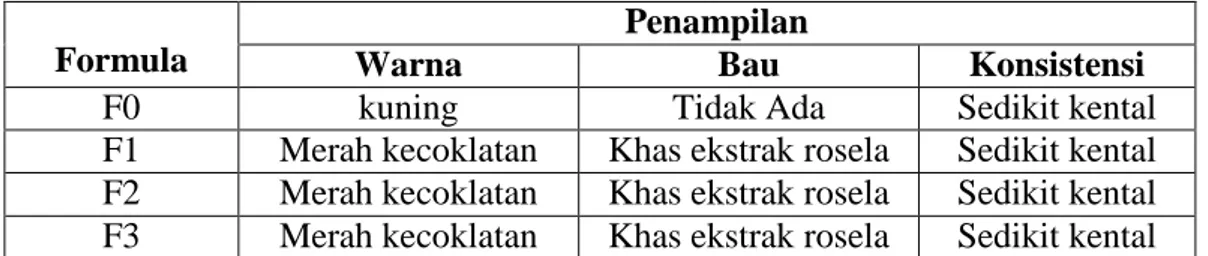
4.3 Data organoleptis sediaan serum ... 46
4.4 Data hasil evaluasi stabilitas sediaan serum kosmetik ... 47
4.5 Data pengamatan homogenitas sediaan serum ... 48
4.6 Data penentuan tipe emulsi sediaan serum menggunakan biru metil ... 49
4.7 Data pengukuran pH sediaan serum ... 49
4.8 Data pengukuran Viskositas sediaan serum (mPa.s) ... 51
4.9 Hasil pengukuran diameter daya sebar sediaan serum (cm) ... 52
4.10 Hasil Uji Iritasi ... 53
4.11 Data persen peredaman DPPH formula 1 ... 59
4.12 Data persen peredaman DPPH formula 2 ... 60
4.13 Data persen peredaman DPPH formula 3 ... 61
4.14 Data persen peredaman DPPH vitamin C ... 62
4.15 Hasil persamaan regresi linier dan hasil analisis IC50 yang diperoleh dari formulasi kombinasi ekstrak etanol 96% dan minyak biji bunga matahari ... 63
xiv
DAFTAR LAMPIRAN
1. Surat Hasil Identifikasi Tanaman rosela ... 70
2. Surat Hasil Identifikasi biji bunga matahari ... 71
3. Surat Pertsetujuan Komite Etik ... 72
4. Surat Pernyataan Persetujuan Menjadi Sukarelawan ... 73
5. Bagan Kerja ... 74
6. Pembuatan simplisia kelopak bunga rosela merah ... 75
7. Pembuatan ekstrak dari simplisia kelopak bunga rosela ... 76
8. Pembuatan minyak biji bunga matahari ... 77
9. Bagan pengujian aktivitas antioksidan ... 78
10. Gambar Sampel ... 79
11. (Lanjutan) ... 80
12. Mikroskopik kelopak bunga rosela ... 81
13. Gambar mikroskopik sel minyak pada biji bunga matahari ... 82
14. Gambar alat yang digunakan pada penelitian ini ... 82
15. Gambar uji karakteristik serbuk simplisia kelopak bunga rosela... 84
16. Skrining fitokimia simplisia kelopak bunga rosela merah ... 85
17. Skrining fitokimia ekstrak etanol 96% kelopak bunga rosela ... 86
18. Perhitungan kadar air sampel ... 88
19. Perhitungan kadar sari larut dalam air serbuk simplisia ... 89
20. Perhitungan kadar sari larut dalam etanol serbuk simplisia ... 90
21. Perhitunag kadar abu total sampel ... 90
22. Perhitungan kadar abu tidak larut dalam asam sampel ... 92
23. Perhitungan dosisi ekstrak kelopak bunga rosela untuk formula sediaan serum ... 93
24. Pembuatan larutan DPPH konsentrasi 200 ppm ... 93
25. Pembuatan larutan DPPH blanko 40 ppm ... 93
26. Pembuatan larutan uji serum ... 94
27. Pembuatan larutan uji vitamin C ... 96
28. Data Operating Time ... 98
29. Hasil Uji Aktivitas Antioksidan ... 99
30. Perhitungan Persen Peredaman Dan Nilai IC50 ... 102
31. Gambar sediaan serum ... 114
32. Gambar uji homogenitas sediaan ... 114
33. Gambar uji tipe emulsi ... 114
1 BAB I PENDAHULUAN 1.1 Latar Belakang
Rosela (Hibiscus sabdariffa L.) adalah tanaman asli dari daerah yang terbentang dari India hingga Malaysia yang kini telah menyebar luas di semua negara tropis dan sub tropis, termasuk Indonesia. Rosela mulai dilirik oleh masyarakat karena banyak manfaat yang diperoleh masyarakat setelah mengkonsumsi produk-produk yang terbuat dari kelopak bunga rosela merah salah satunya untuk zat warna merah alami misalnya pada industri makanan maupun kosmetik (Ali, dkk., 2013).
Rosela merah (Hibiscus sabdariffa L.) merupakan tanaman obat yang memiliki khasiat mencegah penuaan dini (anti-aging) karena adanya kandungan antioksidan. Senyawa bioaktif utama yang berperan sebagai antioksidan adalah antosianin, flavonoid, polifenol dan asam askorbat. Zat antioksidan dalam rosela merah dapat menangkap reactive oxigen species (ROS) dan radikal bebas, menurunkan O2 reaktif, metabolisme peroksidasi lemak menjadi produk non radikal, dan mencegah generasi radikal bebas (Rodina, dkk., 2016).
Rosela merah yang memiliki kandungan antioksidan yang tinggi. Semakin pekat warna merah pada kelopak bunga rosela merah, rasanya akan semakin asam dan kandungan antosianin (antioksidan) semakin tinggi. Antosianin disini berperan menjaga kerusakan sel akibat penyerapan sinar ultraviolet berlebih. Ia melindungi sel-sel tubuh dari perubahan akibat radikal bebas. Tetapi hati-hati sebab kadar antioksidan tersebut menjadi berkurang bila mengalami proses pemanasan dan pengeringan. Antioksidan adalah molekul yang berkemampuan memperlambat ataupun mencegah oksidasi molekul lain. Kandungan antioksidan
2
yang rendah dapat menyebabkan stres oksidatif dan merusak sel-sel tubuh. Oleh karena itu efek pengobatan rosela merah ini terhadap berbagai penyakit merupakan efek dari Antioksidannya (Ali, dkk., 2013).
Masyarakat Indonesia memiliki berbagai macam tradisi antara lain menjadikan bahan-bahan alami sebagai obat tradisional, salah satunya yaitu penggunaan minyak biji bunga matahari. Biji bunga matahari dipilih karena mengandung vitamin E yang dapat membantu melindungi kulit dari oksidasi sel yang merusak kulit, ß- sitosterol yang dapat membantu memproduksi melanin dan antioksidan sebagai penangkal radikal bebas (Arantika, 2018).
Antioksidan adalah senyawa yang dapat menangkap radikal bebas. Radikal bebas dihasilkan karena beberapa faktor, seperti asap, debu, polusi, kebiasaan mengkonsumsi makanan cepat saji yang tidak seimbang antara karbohidrat, protein dan lemaknya. Senyawa antioksidan akan mendonorkan satu elektronnya pada pada radikal bebas yang tidak stabil sehingga radikal bebas ini bisa dinetralkan dan tidak lagi mengganggu metabolisme tubuh (Rahmi, 2017).
Metode yang biasa digunakan untuk mengetahui aktivitas antioksidan tanaman yaitu dengan menggunakan metode radikal bebas DPPH. Tujuan metoda ini adalah sebagai parameter konsentrasi yang ekuivalen memberikan efek 50%
(IC50). Karena adanya elektron yang tidak berpasangan, DPPH memberikan serapan kuat, ketika elektron menjadi berpasangan, absorbansi akan menurun.
Keberadaan senyawa antioksidan dapat mengubah warna larutan DPPH dari ungu menjadi kuning (Dehpour, dkk. 2009).
Salah satu dari bentuk sediaan kosmetik yang telah berkembang akhir-akhir ini adalah sediaan serum. Serum merupakan sediaan dengan viskositas rendah, karena viskositasnya yang rendah serum dikategorikan sebagai sediaan emulsi.
3
Serum memiliki kelebihan yaitu memiliki konsentrasi bahan aktif tinggi sehingga efeknya lebih cepat diserap kulit, dapat memberikan efek yang lebih nyaman dan lebih mudah menyebar dipermukaan kulit karena viskositasnya yang tidak terlalu tinggi (Kurniawati, 2018).
Berdasarkan uraian diatas, maka peneliti tertarik untuk melakukan pembuatan formulasi sediaan serum kosmetik kombinasi ekstrak kelopak bunga rosela merah (Hibiscus sabdariffa L.) dan minyak biji bunga matahari (Helianthus annuus L) serta melakukan uji aktivitas antioksidan formulasi serum tersebut dengan menggunakan metode DPPH.
4 1.2 Rumusan Masalah
Berdasarkan uraian diatas, maka yang menjadi perumusan masalah penelitian ini adalah:
a. Apakah kombinasi ekstrak etanol kelopak bunga rosela merah (Hibiscus sabdariffa L.) dan minyak biji bunga matahari (Helianthus annuus L.) dapat diformulasikan dalam bentuk sediaan serum kosmetik ?
b. Apakah sediaan serum kosmetik kombinasi ekstrak etanol kelopak bunga rosela merah (Hibiscus sabdariffa L.) dan minyak biji bunga matahari (Helianthus annuus L.) memiliki potensi aktivitas sebagai antioksidan terhadap DPPH?
1.3 Hipotesis Penelitian
Berdasarkan perumusan masalah diatas, maka dibuat hipotesis penelitian sebagai berikut:
a. Kombinasi ekstrak etanol kelopak bunga rosela merah (Hibiscus sabdariffa L.) dan minyak biji bunga matahari (Helianthus annuus L.) dapat diformulasikan dalam bentuk sediaan serum kosmetik
b. Sediaan serum kosmetik kombinasi ekstrak etanol kelopak bunga rosela merah (Hibiscus sabdariffa L.) dan minyak biji bunga matahari (Helianthus annuus L.) memiliki potensi aktivitas sebagai antioksidan terhadap DPPH.
5 1.4 Tujuan Penelitian
Berdasarkan hipotesis di atas, tujuan penelitian adalah sebagai berikut:
a. Untuk mengetahui kombinasi ekstrak etanol kelopak bunga rosela merah (Hibiscus sabdariffa L.) dan minyak biji bunga matahari (Helianthus annuus L.) dapat diformulasikan dalam bentuk sediaan serum kosmetik
b. Untuk mengetahui sediaan serum kosmetik kombinasi ekstrak kelopak bunga rosela merah (Hibiscus sabdariffa L.) dan minyak biji bunga matahari (Helianthus annuus L.) memiliki potensi aktivitas sebagai antioksidan terhadap DPPH
1.5 Manfaat Penilitian
Berdasarkan tujuan penelitian di atas, maka manfaat penelitian adalah sebagai berikut:
a. Memberikan informasi tentang aktivitas antioksidan dengan metode DPPH pada sediaan serum kosmetik dari kombinasi ekstrak etanol kelopak bunga rosela merah (Hibiscus sabdariffa L.) dan minyak biji bunga Matahari (Helianthus annuus L.) pada masing konsentrasi dari ekstrak.
b. Memberikan informasi pemanfaatan lain dari kelopak bunga rosela merah dan minyak biji bunga matahari dalam bidang kosmetik.
1.6 Kerangka Pikir Penelitian
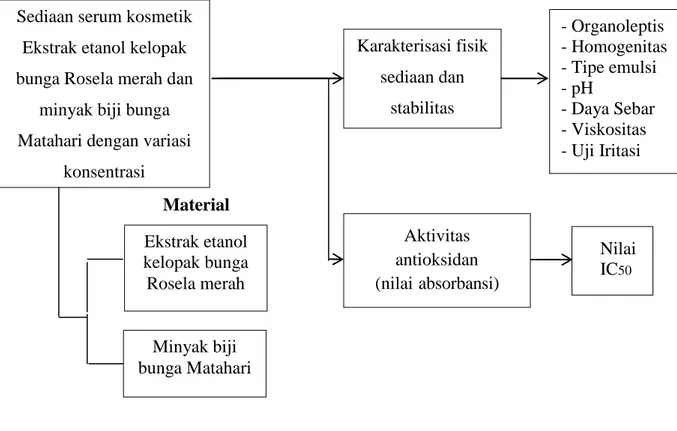
Kerangka pikir dalam penelitian ini adalah terdapat dua variabel yaitu variabel bebas dan variabel terikat. Variabel bebas yaitu Sediaan serum kosmetik Ekstrak etanol kelopak bunga rosela merah (Hibiscus sabdariffa L.) dan minyak biji bunga matahari (Helianthus annuus L.) dan sebagai variabel terikat adalah
6
Karakterisasi fisik sediaan dan stabilitas dan Aktivitas antioksidan (nilai absorbansi). Kerangka pikir penelitian dapat di lihat pada Gambar 1.1.
Variabel Bebas Variabel Terikat Parameter
Material
Gambar 1.1 Kerangka pikir Penelitian Sediaan serum kosmetik
Ekstrak etanol kelopak bunga Rosela merah dan
minyak biji bunga Matahari dengan variasi
konsentrasi
- Organoleptis - Homogenitas - Tipe emulsi - pH
- Daya Sebar - Viskositas - Uji Iritasi
Ekstrak etanol kelopak bunga Rosela merah
Minyak biji bunga Matahari
Karakterisasi fisik sediaan dan
stabilitas
Aktivitas antioksidan (nilai absorbansi)
Nilai IC50
7 BAB 2
TUNJAUAN PUSTAKA 2.1 Tanaman Rosela
Rosela merah (Hibiscus sabdariffa L.) adalah tanaman asli dari daerah yang terbentang dari India hingga Malaysia yang kini telah menyebar luas di semua negara tropis dan sub tropis, termasuk Indonesia. Rosela merah mulai dilirik oleh masyarakat karena banyak manfaat yang diperoleh masyarakat setelah mengkonsumsi produk-produk yang terbuat dari kelopak bunga rosela merah salah satunya untuk zat warna merah alami misalnya pada industri makanan maupun kosmetik (Ali, dkk., 2013).
2.1.1 Sistematika Tanaman
Secara lengkap sistematika bunga rosela merah (Hisbiscus sabdariffa L.) hasil identifikasi sampel dari Herbarium Medanense (MEDA) Fakultas Matematika dan Ilmu Pengetahuan Alam (FMIPA) Universitas Sumatera Utara adalah:
Kingdom : Plantae
Divisi : Spermatophyta Subdivisi : Angiospermae Kelas : Dicotyledoneae Ordo : Malvales Famili : Malvaceae Genus : Hibiscus
Spesies : Hisbiscus sabdariffa L.
2.1.2 Nama lain Tanaman
Di Indonesia, tanaman rosela merah dikenal dengan beberapa nama yaitu,
8
susur, rosel /rosela, merambos hijau (Jateng), asam jarot (Padang), asam rejang (Muara enim).
Nama asing rosela merah di beberapa negara seperti di Inggris adalah roselle, rozelle, sorrel, red sorrel, white sorel Jamaica sorrel. Indian sorrel guinea sorrel, sou-sour, quensland jelly plant, jelly okra, lemon bush, dan florida cranberry, di Perancis disebut juga oseille rouge atau oseille de guinea, di Jerman dan Italia adalah karkade, di India dikenal patwa, red roselle, Lal ambari, goku, di Jepang dikenal roselle, di Malaysia disebut asam susur dan kachieb priew di Thailand serta sudan tea di Afrika Timur dan Zuring di Belanda (Mandasari, A., 2009).
2.1.3 Morfologi Tanaman
Rosela merah merupakan Tanaman semak umur satu tahun, tinggi Tanaman mencapai 2,4 m. Batang berwarna merah, berbentuk bulat dan berbulu; daun berseling 3-5 helai dengan panjang 7,5-12,5 cm berwarna hijau, ibu tulang daun kemerahan, tangkai daun pendek. Bentuk helaian daun bersifat anisofili (polimorfik), helaian daun yang terletak dibagian pangkal batang tidak berbagi, bentuk daun bulat telur, tangkai daun pendek. Daun-daun di bagian cabang dan ujung batang berbagi, menjadi 3 toreh, lebar toreh daun 2,5 cm, tepi daun beringgit, daun penumpu bentuk benang; panjang tangkai daun 0,3-12cm, hijau hingga merah; pangkal daun meruncing, tepi daun beringgit, pangkal daun tumpul hingga meruncing, sedikit berambut.
Bunga tunggal, kuncup bunga tumbuh dari bagian ketiak daun, tangkai bunga berukuran 5-20 mm; kelopak bunga berlekatan, tidak gugur, tetap mendukung buah, berbentuk lonceng; mahkota bunga berlepasan, berjumlah 5 petal, mahkota bunga berbentuk bulat telur terbalik, warna kuning, kuning kemerahan; benang sari terletak pada suatu kolom pendukung benang sari,panjang kolom pendukung
9
benang sari sampai 20 mm, kepala sari berwarna merah, panjang tangkai sari 1 mm; tangkai putik berada di dalam kolom pendukung benang sari, jumlah kepala putik 5 buah, warna merah (Badan POM, 2010).
2.1.4 Kandungan Kimia
Kelopak bunga rosela merah diteliti mengandung beberapa macam vitamin, yaitu vitamin C, B1, B2, dan vitamin A, juga 18 asam amino. Kelopak bunga rosela merah juga mengandung flavonoid, yaitu gossipetin dan antosianin, sianidin-3-sambubiosida, delfinidin, delfinidin-3-glukosida, pektin, protein, sukrosa, serat, asam sitrat dan asam malat (Mandasari, A., 2009).
2.1.5 Manfaat Tanaman
Rosela merah (Hibiscus sabdariffa L.) merupakan tanaman obat yang memiliki khasiat mencegah penuaan dini (anti-aging) karena adanya kandungan antioksidan (Rodina, dkk., 2016).
Kelopak bunga rosella mengandung flavonoid, saponin dan tannin yang dapat berkhasiat sebagai antibakteri yang memiliki konsentrasi hambat minimum terhadap bakteri penyebab pioderma dan akne yang merupakan dua masalah kulit yang umum terjadi. Pioderma disebabka bakteri gram negatif Pseudomonas aeruginosa, sedangkan akne disebabkan infeksi bakteri gram positif Propionibacterium acnes (Nafisa. S., dkk, 2021).
Bunga rosela merah mempunyai manfaat lain seperti anti- hipertensi, kram otot dan anti- infeksi bakteri. Kelopak bunga rosela merah berfungsi untuk meningkatkan daya tahan tubuh manusia terhadap serangan penyakit karena mengandung vitamin C (Syamsul. D, dan Supriyanto, 2017).
10 2.2 Biji Bunga Matahari
2.2.1 Sistematika Tanaman
Secara lengkap sistematika bunga matahari (Helianthus annuus L.) hasil identifikasi sampel dari Herbarium Medanense (MEDA) Fakultas Matematika dan Ilmu Pengetahuan Alam (FMIPA) Universitas Sumatera Utara adalah:
Kingdom : Plantae
Divisi : Angiospermae
Kelas : Asteridae
Ordoo : Asterales
Famili : Asteraceae
Genus : Helianthus
Spesies : Helianthus annuus L.
2.2.2 Morfologi Tanaman
Tanaman ini tumbuh tahunan mempunyai bentuk tegak dan kokoh dengan ketinggian hingga 1-3 meter. Akarnya berserat dan merupakan akar lateral. Biji bunga matahari memiliki kulit yang agak keras, berbentuk pipih memanjang, warna putih keabuan atau hitam. Bunga matahari merupakan bunga majemuk yang tersusun dari ratusan dan ribuan bunga kecil pada satu bonggolnya, sedangkan pada bunga tunggal hanya terdapat satu bunga saja pada ujung tangkai tanaman. Selain itu, tanaman ini juga mempunyai bunga yang besar dan berbentuk pita. Warna bunganya kuning terang. Ciri khas dari bunga ini setiap berbunga akan mengikuti arah cahaya matahari. Daunnya bertangkai panjang dan besar seperti bunganya dan saling berhadapan atau selang seling. Batang yang berdiri tegak lurus (monopodial), umumnya mempunyai tinggi 0,3-5 meter. Bagian batangnya terlihat berbulu, bentuk batangnya bulat (Putri, 2016).
11 2.2.3 Kandungan Kimia
Studi fitokimia pada tanaman bunga matahari (Helianthus annuus L.) menunjukkan adanya karbohidrat, flavonoid, tanin, alkaloid, saponin, fitosterol, steroid, dan fixed oil. Penelitian fitokimia menunjukkan ekstrak metanol biji bunga matahari (Helianthus annuus L.) mempunyai kandungan karbohidrat, flavanoid, tanin, alkaloid, saponin, fitosterol, steroid, pati, glikosida dan protein (Dwivedi, dkk., 2014).
2.2.4 Manfaat Tanaman
Biji bunga matahari mengandung vitamin E yang dapat membantu melindungi kulit dari oksidasi sel yang merusak kulit, ß- sitosterol yang dapat membantu memproduksi melanin dan antioksidan sebagai penangkal radikal bebas (Arantika, 2018).
Minyak biji, tunas, dan herbal tingtur dari tanaman bunga matahari (Helianthus annuus L.) telah digunakan untuk antiinflamasi, antipiretik, astringent, katarsis, diuretik, emolien, ekspektoran, stimulan, vermifuge, dan tujuan pengobatan luka. Pada ekstrak etanol daun tanaman bunga matahari (Helianthus annuus L.) mempunyai aktivitas sebagai antidiare, antihistamin, dan juga mengandung antioksidan (Dwived, dkk., 2015).
2.3 Ekstraksi
Ditjen POM (1995), membagi beberapa metode ekstraksi dengan menggunakan pelarut yaitu :
a. Cara Dingin 1.Maserasi
12
Maserasi ialah proses pengekstrakan simplisia dengan menggunakan pelarut dengan beberapa kali pengocokkan atau pengadukan pada temperatur ruang (kamar) secara teknologi termasuk ekstraksi dengan prinsip metode pencapaian konsentrasi pada keseimbangan. Maserasi kinetik berarti dilakukan pengadukan yang kontinyu (terus-menerus). Remaserasi berarti dilakukan pengulangan penambahan pelarut setelah dilakukan penyaringan maserat pertama dan seterusnya.
2.Perkolasi
Perkolasi adalah ektraksi dengan pelarut yang selalu baru sampai sempurna (exhaustive extraction) yang umumnya dilakukan pada temperatur ruang. Proses ini terdiri dari tahapan pengembangan bahan, tahap maserasi antara, tahap perkolasi sebenarnya (penetesan/penampungan ekstrak), terus-menerus sampai diperoleh ekstrak (perkolat) yang jumlahnya 1-5 kali bahan.
b. Cara Panas 1.Refluks
Refluks merupakan ekstraksi dengan pelarut pada temperatur titik didihnya, selama waktu tertentu dan jumlah pelarut terbatas yang relatif konstan dengan adanya pendingin balik. Umumnya dilakukan pengulangan proses pada residu pertama sampai 3-5 kali dapat termasuk proses ekstraksi sempurna.
2. Soxhletasi
Soxhletasi adalah ekstraksi dengan menggunakan pelarut yang selalu baru yang umumnya dilakukan dengan alat khusus sehingga terjadi ekstraksi kontinyu dengan jumlah pelarut relatif konstan dengan adanya pendingin balik.
3. Digesti
13
Digesti merupakan maserasi kinetik (dengan pengadukan kontinyu) pada temperatur yang lebih tinggi dari temperatur ruangan (kamar), yaitu secara umum dilakukan pada temperatur 40-50.
4. Infusa
Infusa adalah ekstraksi dengan pelarut air pada temperatur penangas air mendidih, temperatur terukur 90-98ºC selama waktu tertentu (15-20 menit).
5.Dekok
Dekok adalah infus yang waktunya lebih lama (lebih dari 30 menit) dan temperatur sampai titik didih air.
2.4 Serum Kosmetik
Definisi kosmetik dalam Peraturan Mentri Kesehatan RI No.
1176/MenKes/permenkes/VIII/2010 adalah sediaan atau bahan yang siap untuk digunakan pada bagian luar badan (epidermis, rambut, kuku, bibr, dan organ kelamin bagian luar) gigi, dan rongga mulut untuk membersihkan, menambah daya tarik, mengubah penampakan, melindungi supaya tetap dalam keadaan baik, memperbaiki bau badan tetapi tidak dimaksudkan untuk mengobati atau menyembuhkan suatu penyakit. Kosmetik berasal dari bahasa yunani
“kosmetikos” yang berarti keterampilan, menghias, mengatur.
Serum merupakan sediaan dengan viskositas rendah, karena viskositasnya yang rendah serum dikategorikan sebagai sediaan emulsi. Serum memiliki kelebihan yaitu memiliki konsentrasi bahan aktif tinggi sehingga efeknya lebih cepat diserap kulit, dapat memberikan efek yang lebih nyaman dan lebih mudah menyebar dipermukaan kulit karena viskositasnya yang tidak terlalu tinggi (Kurniawati, 2018).
14
Emulsi adalah sediaan yang mengandung bahan obat cair atau larutan obat, terdispersi dalam cairan pembawa, distabilkan dengan zat pengemulsi atau surfaktan yang cocok. Emulsi juga merupakan sediaan yang mengandung dua zat yang tidak tercampur, biasanya air dan minyak, dimana cairan yang zat terdispersi menjadi butir-butir kecil dalam cairan yang lain (Anief, 2015).
Zat pengemulsi (emulgator) merupakan komponen yang paling penting agar memperoleh emulsa yang stabil. Semua emulgator bekerja dengan membentuk film (lapisan) disekeliling butir-butir tetesan yang terdispersi dan film ini berfungsi agar mencegah terjadinya koalesen dan terpisahnya cairan dispers sebagai fase terpisah. Terbentuk dua macam tipe emulsi yaitu emulsi tipe M/A dimana tetes minyak terdispersi dalam fase air dan tipe A/M dimana fase intern adalah air dan fase ekstern adalah minyak (Anief, 2015).
Menurut Anief (2015) Ketidakstabilan dalam emulsi farmasi dapat digolongkan sebagai berikut:
a. Flokulasi dan creaming
Creaming merupakan pemisahan dari emulsi menjadi beberapa lapis cairan, dimana masing-masing lapis mengandung fase dispers yang berbeda.
b. Koalesen dan pecahnya emulsi (cracking dan breaking)
Creaming adalah proses yang bersifat dapat kembali, berbeda dengan proses cracking (pecahnya emulsi) yang bersifat tidak dapat kembali pada creaming, flokul fase dispers mudah didispers kembali dan terjadi campuran homogen bila digojok perlahan-lahan. Sedang pada cracking, penggojokan sederhana akan gagal untuk mengemulsi kembali butir-butir tetesan dalam bentuk emulsi yang stabil.
c. Inversi
Peristiwa berubahnya sekonyong-konyong tipe emulsi M/A ke tipe A/M atau
15 sebaliknya.
2.5 Morfologi Bahan a. Tween 80
Tween 80 disebut juga sebagai polisorbat 80 (polioksietilen 20 sorbitan monooleat). Tween 80 memiliki karakteristik cairan berminyak berwarna kuning pada suhu 250C dan suhu hangat, serta berasa pahit. Tween 80 larut dalam etanol dan air, tidak larut dalam minyak mineral dan minyak nabati. Tween 80 memiliki bobot jenis 1,08g/cm3 dan nilai HLB 15. Tween 80 berfungsi sebagai pengemulsi, surfaktan nonionik, solubilizing agent, agen pensuspensi, dan agen pembasa.
Tween 80 stabil untuk elektrolit dan asam serta basa lemah, saponifikasi terjadi dengan asam dan basa kuat. Tween 80 harus disimpan dalam wadah tertutup baik, terlindung dari cahaya, dingin, dan kering (Rowe, dkk., 2009).
b. Natrium Carboxymethylcellulose (Na CMC)
Natrium Carboxymethylcellulose (Na CMC) merupakan garam dari poli karboksi-metil-eter dari selulosa. Na CMC memiliki pemerian yakni berwarna putih, tidak berbau, tidak berasa, berbentuk serbuk granular, dan higroskopis setelah mengalami pengeringan. Na CMC cukup stabil, meskipun memiliki sifat higroskopis. Kondisi dibawah kelembaban tinggi maka Na CMC dapat menyerap air (>50%) dalam jumlah besar. Na CMC merupakan salah satu gelling agent yang memiliki sifat plasebo dan tidak bereaksi dengan komponen lain dalam formulasi (Rowe, dkk., 2009). Penggunaan sebagai emulgator dalam kadar 0,5 % - 1 % (Anief, 2015).
c. Natrium sitrat
16
Natrium sitrat, baik sebagai dihidrat atau anhidrat, adalah banyak digunakan dalam formulasi farmasi. Ini digunakan dalam produk makanan, terutama untuk mengatur pH solusi. Konsentrasi yang natrium sitrat yang dapat digunakan sebagai buffering agent adalah 0,3 %- 2, 0 % (Rowe, dkk., 2009).
d. Nipagin
Nipagin biasanya digunakan sebagai bahan pengawet atau preservatif, mencegah kontaminasi, kerusakan dan pembusukan oleh bakteri atau fungi dalam formulasi sediaan farmasetika, produk makanan dan kosmetik. Rentang pH berkisar antara 4-8. Dalam sediaan topikal, konsentrasi nipagin yang umum digunakan adalah 0,02-0,3%. Bahan ini dapat larut pada air panas, etanol dan metanol (Rowe, dkk, 2009).
e. Nipasol (Propil paraben)
Nipasol (Propil paraben) berbentuk serbuk putih, kristal, tidak berbau, dan tidak berasa. Propil paraben banyak digunakan sebagai pengawet antimikroba dalam kosmetik, produk makanan, dan formulasi sediaan farmasi. Propil paraben menunjukan aktivitas antimikroba antara pH 4-8. Efikasi pengawet menurun dengan meningkatnya pH karena pembentukan anion fenolat. Paraben lebih aktif terhadap ragi dan jamur daripada terhadap bakteri. Mereka juga lebih aktif terhadap bakteri gram positif dibandingkan dengan bakteri gram negatif (Rowe, 2009).
f. Aquades
Aquades merupakan cairan jernih, tidak berwarna, tidak berbau, tidak mempunyai rasa, titik didih pada 100°C dan titik beku pada 10°C, biasa digunakan sebagai pelarut (Rowe, 2009).
17
2.6 Metode DPPH Sebagai Pengujian Antioksidan
Antioksidan adalah senyawa yang dapat menangkap radikal bebas. Radikal bebas dihasilkan karena beberapa faktor, seperti asap, debu, polusi, kebiasaan mengkonsumsi makanan cepat saji yang tidak seimbang antara karbohidrat, protein dan lemaknya. Senyawa antioksidan akan mendonorkan satu elektronnya pada pada radikal bebas yang tidak stabil sehingga radikal bebas ini bisa dinetralkan dan tidak lagi mengganggu metabolisme tubuh (Rahmi, H., 2017).
Ada sejumlah besar metode untuk menentukan kapasitas antioksidan berdasarkan prinsip yang berbeda: pengumpulan radikal peroksil (Oxygen Radical Absorbance capacity, ORAC); Total Radical-trapping Antioxidant Power (TRAP); daya pereduksi logam (Ferric Reducing Antioksidant Power, FRAP);
Cupric Reducing Antioksidant Power (CUPRAC); pengumpulan radikal hidroksil
(uji deoxiribose); pengumpulan radikal organik (2,2-Azino-bis (3-ethylbenz- thiazoline-6-sulfonic acid, ABTS); 1,1-difenil-2-pikrilhidrazil (DPPH), dan lain-
lain (Marinova dan Batchvarov., 2011).
Metode yang biasa digunakan untuk mengetahui aktivitas antioksidan tanaman yaitu dengan menggunakan metoda radikal bebas DPPH. Tujuan metoda ini adalah sebagai parameter konsentrasi yang ekuivalen memberikan efek 50%
(IC50). Karena adanya elektron yang tidak berpasangan, DPPH memberikan serapan kuat, ketika elektron menjadi berpasangan, absorbansi akan menurun.
Keberadaan senyawa antioksidan dapat mengubah warna larutan DPPH dari ungu menjadi kuning (Dehpour, dkk., 2009).
Salah satu uji yang dapat dilakukan untuk menentukan potensi antioksidan suatu senyawa adalah dengan menguji kemampuannya dalam meredam senyawa radikal DPPH. DPPH merupakan radikal bebas yang stabil pada suhu kamar dan
18
sering digunakan untuk menilai aktivitas antioksidan beberapa senyawa atau ekstrak bahan alam (Gurav, dkk., 2007).
DPPH menerima elektron atau radikal hidrogen akan membentuk molekul diamagnetik yang stabil. Interaksi antioksidan dengan DPPH baik secara transfer elektron atau radikal hidrogen pada DPPH, akan menetralkan radikal bebas dari DPPH dan membentuk reduksi DPPH. Warna larutan berubah dari ungu tua menjadi kuning terang dan absorbansi pada panjang gelombang 516 nm akan hilang jika semua elektron pada radikal bebas DPPH menjadi berpasangan.
Perubahan ini dapat diukur sesuai dengan jumlah elektron atau atom hidrogen yang ditangkap oleh molekul DPPH akibat adanya zat reduktor. Suatu zat mempunyai sifat antioksidan bila nilai IC50 kurang dari 200 ppm. Bila nilai IC50
yang diperoleh berkisar antara 200-1000 ppm, maka zat tersebut kurang aktif namun masih berpotensi sebagai zat antioksidan (Molyneux, 2004).
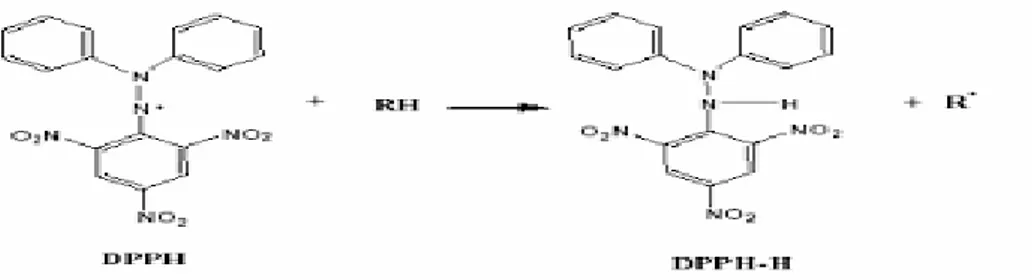
Menurut Prakash, dkk (2001) Sebuah metode sederhana yang telah dikembangkan untuk menentukan aktivitas antioksidan makanan menggunakan radikal 1,1 difenil-2-pikrilhidrazil (DPPH) yang stabil. Elektron ganjil pada radikal bebas DPPH memberikan serapan kuat maksimum pada 517 nm dan berwarna ungu. Warna berubah dari ungu menjadi kuning karena absorptivitas molar radikal DPPH pada 517 nm berkurang ketika elektron ganjil radikal DPPH dipasangkan dengan hidrogen dari radikal bebas. Gambar Reaksi DPPH dengan senyawa antioksidan ditunjukkan pada gambar dibawah ini :
Gambar 2.1 Reaksi DPPH dengan senyawa antioksidan
19
Terbentuknya senyawa radikal, baik radikal bebas endogen maupun eksogen terjadi melalui sederetan reaksi. Mula-mula terjadi pembentukan awal radikal bebas (inisiasi), lalu perambatan atau terbentuknya radikal baru (propagasi), dan tahap terakhir yaitu pemusnahan atau pengubahan senyawa radikal menjadi non radikal (terminasi) (Rahmatussolihat, 2009).
Parameter yang dipakai untuk menunjukan aktivitas antioksidan adalah harga konsentrasi efisien atau Effective Concentration (EC50) atau Inhibitory Concentration (IC50) yaitu konsentrasi suatu zat antioksidan yang dapat menyebabkan 50% DPPH kehilangan karakter radikal atau konsentrasi suatu zat antioksidan yang memberikan % penghambatan 50%. Harga EC50 atau IC50 yang rendah berarti aktivitas antioksidan tinggi (Williams, dkk, 1989).
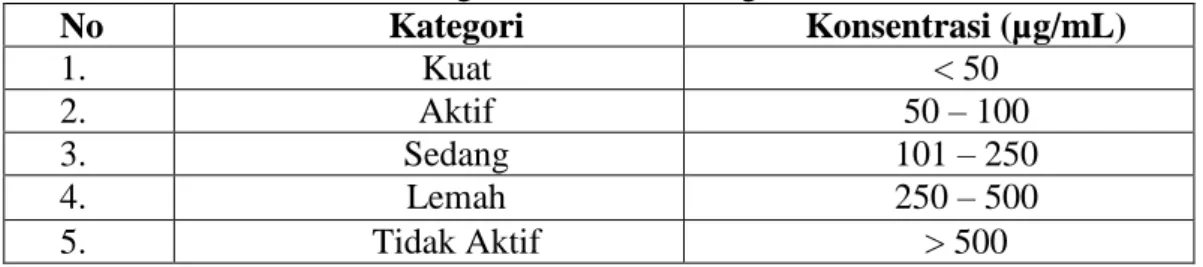
Tabel 2.1 Kategori nilai IC50 sebagai antioksidan
No Kategori Konsentrasi (µg/mL)
1. Kuat < 50
2. Aktif 50 – 100
3. Sedang 101 – 250
4. Lemah 250 – 500
5. Tidak Aktif > 500
(Lung dan Destiani, 2017).
Menurut Scherer dan Godoy (2009). Nilai AAI (Antioxidant Activity Index) dapat ditentukan dengan cara konsentrasi DPPH yang digunakan dalam uji (ppm) dibagi dengan nilai IC50 yang diperoleh (ppm). Nilai AAI <0,5 menandakan aktivitas antioksidan lemah, AAI >0,5-1 menandakan aktivitas antioksidan sedang, AAI >1-2 menandakan aktivitas antioksidan kuat, dan AAI >2 menandakan aktivitas antioksidan sangat kuat.
20
2.7 Bagian-bagian dari alat Spektrofotometer UV-Vis
Menurut Suarsa (2015), Bagian-bagian dari alat spektrofotometer UV-Vis terdiri dari:
A. Sumber cahaya :
1) Lampu Tungsten (Wolfram) : Lampu ini digunakan untuk mengukur sampel pada daerah tampak. Bentuk lampu ini mirip dengna bola lampu pijar biasa. Memiliki panjang gelombang antara 350-2200 nm. Spektrum radiasianya berupa garis lengkung. Umumnya memiliki waktu 1000 jam pemakaian.
2) Lampu Deuterium : Lampu ini dipakai pada panjang gelombang 190-380 nm. Spektrum energi radiasinya lurus, dan digunakan untuk mengukur sampel yang terletak pada daerah uv. Memiliki waktu 500 jam pemakaian.
B. Monokromator
Monokromator berfungsi sebagai penyeleksi panjang gelombang yaitu mengubah cahaya yang berasal dari sumber sinar polikromatis menjadi cahaya monaokromatis. Jenis monokromator yang saat ini banyak digunakan adalan gratting atau lensa prisma dan filter optik. Jika digunakan grating maka cahaya akan dirubah menjadi spektrum cahaya. Sedangkan filter optik berupa lensa berwarna sehingga cahaya yang diteruskan sesuai dengan warnya lensa yang dikenai cahaya. Ada banyak lensa warna dalam satu alat yang digunakan sesuai dengan jenis pemeriksaan. Monokromator, terdiri atas:
1) Prisma, berfungsi mendispersikan radiasi elektromagnetik sebesar mungkin supaya di dapatkan resolusi yang baik dari radiasi polikromatis.
2) Kisi difraksi, berfungsi menghasilkan penyebaran dispersi sinar secara merata, dengan pendispersi yang sama, hasil dispersi akan lebih baik. Selain itu kisi
21
difraksi dapat digunakan dalam seluruh jangkauan spektrum.
3) Celah optis, berfungsi untuk mengarahkan sinar monokromatis yang diharapkan dari sumber radiasi. Apabila celah berada pada posisi yang tepat, maka radiasi akan dirotasikan melalui prisma, sehingga diperoleh panjang gelombang yang diharapkan.
4) Filter, berfungsi untuk menyerap warna komplementer sehingga cahaya yang diteruskan merupakan cahaya berwarna yang sesuai dengan panjang gelombang yang dipilih.
C. Tempat sampel Spektrofotometer UV-VIS
Tempat sampel Spektrofotometer UV-VIS menggunakan kuvet sebagai wadah sampel yang akan dianalisis. Kuvet biasanya terbuat dari kuarsa atau gelas, namun kuvet dari kuarsa yang terbuat dari silika memiliki kualitas yang lebih baik. Hal ini disebabkan yang terbuat dari kaca dan plastik dapat menyerap UV sehingga penggunaannya hanya pada spektrofotometer sinar tampak (VIS). Kuvet biasanya berbentuk persegi panjang dengan lebar 1 cm. Kuvet yang baik harus memenuhi beberapa syarat sebagai berikut :
1) Permukaannya harus sejajar secara optis
2) Tidak berwarna sehingga semua cahaya dapat di transmisikan 3) Tidak ikut bereaksi terhadap bahan-bahan kimia
5) Tidak rapuh
6) Bentuknya sederhana D. Detektor
Detektor berfungsi menangkap cahaya yang diteruskan dari sampel dan mengubahnya menjadi arus listrik. Macam-macam detektor yang biasa digunakan:
1. Phototube dengan jangkauan panjang gelombang ( λ) 150 – 1000 nm
22
2. Photomultiplier dengan jangkauan panjang gelombang ( λ) 150 – 1000 nm Syarat-syarat sebuah detektor :
a. Kepekaan yang tinggi
b. Perbandingan isyarat atau signal dengan bising tinggi c. Respon konstan pada berbagai panjang gelombang.
d. Waktu respon cepat dan signal minimum tanpa radiasi.
e. Signal listrik yang dihasilkan harus sebanding dengan tenaga radiasi.
23 BAB 3
METODOLOGI PENELITIAN
3.1 Jenis Penelitian
Metode yang digunakan dalam penelitian ini adalah metode eksperimental (Experimental Research). Tahap penelitian meliputi penyiapan bahan tanaman, identifikasi Tanaman, pengumpulan dan pengolahan tanaman, pembuatan simplisia, karakterisasi simplisia, pembuatan ekstrak secara maserasi, skrining fitokimia pada ekstrak kelopak bunga rosela merah, pembuatan minyak buji bunga matahari, formulasi serum kosmetik kombinasi ekstrak bunga rosela merah dan minyak biji bunga matahari, pengujian aktivitas antioksidan serum kosmetik dengan metode pemerangkapan radikal bebas DPPH (1,1-difenil-2- pikrilhidrazil), penentuan mutu fisik sediaan serum (pengamatan organoleptis, pengamatan tipe emulsi, uji homogenitas, pengukuran pH, pengujian daya sebar, uji iritasi, pengukuran viskositas dan penentuan stabilitas sediaan. Penelitian ini dilakukan di Laboratorium Biologi Farmasi Universitas Sumatera Utara, dan Laboratorium Farmasetika Dasar Farmasi Universitas Sumatera Utara, Medan.
3.2 Alat dan Bahan 3.2.1 Alat
Alat-alat yang digunakan dalam penelitian ini adalah alat-alat gelas, aluminium foil (Total Wrap), alat tanur (Nabertherm), blender (Philips), batang pengaduk, Beaker glass (Pyrex), blender (Philips), botol ekstrak, cawan porselin, deg glass, gelas ukur (Oberoi), Hotplate (Hanna), kaca arloji, kertas perkamen, kertas saring, klem, kondensor, koran, krus porselen, kuvet, labu tentukur (Iwaki), lemari pengering, lumpang dan alu, magnetic stirrer, neraca analitik (Mettler
24
Toledo), object glass, oven (Memmert), penangas air, pH meter (ATC), pH indikator (Nesco), pipet tetes, pot plastik, rotary evaporator (Haake D), screw press machine, serbet, spatula, spektrofotometer UV-Visibel (Shimadzu), spuit (One-med), statif, sudip, tisu, dan viscometer NDJ-85.
3.2.2 Bahan
Bahan-bahan yang digunakan pada penelitian ini yaitu, akuades, etanol 96%, simplisia kelopak Bunga Rosela merah, dan minyak biji bunga Matahari. alfa naftol, amil alkohol, asam asetat anhidrat, asam klorida pekat, asam nitrat pekat, asam sulfat pekat, besi (3) klorida, biru metil, CMC Na, ekstrak etanol 96%
kelopak bunga rosela merah, etanol 96%, iodium, isopropanol, kalium iodida, kloroform, larutan dapar pH asam (pH 4,01), larutan dapar pH netral (pH 7,01), metanol, metil paraben, minyak biji bunga matahari, N-Heksan, natrium hidroksida, natrium sitrat, preaksi bouchardat, pereasksi meyer, pereasksi molish, propil paraben, raksa (2) klorida, serbuk DPPH (1.1-difenil-2-pikrilhidrazil), serbuk magnesium, serbuk seng, setil alkohol, sorbitol, timbal (2) asetat dan toluene, dan tween 80.
25 3.3 Prosedur Penelitian
3.3.1 Preparasi sampel 3.3.1.1 Pengambilan Sampel
Pengambilan sampel dilakukan secara purposif yaitu tanpa membandingkan dengan Tanaman yang sama dari daerah lain. Kelopak Bunga Rosela merah diperoleh di jl. Purwojoyo Kecamatan Pancur Batu, Deli Serdang, Sedangkan biji bunga Matahari diperoleh dari Jakarta.
3.3.1.2 Identifikasi Sampel
Identifikasi tanaman kelopak bunga rosela merah dan biji bunga matahari dilakukan di Herbarium Medanense (MEDA) Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas Sumatera Utara.
3.3.1.3 Pembuatan Simplisia
Kelopak bunga rosela merah segar dibersihkan, dicuci bersih dengan air mengalir dan ditiriskan, lalu ditimbang dan diperoleh berat basah. Kemudian di keringkan di dalam lemari pengering dengan suhu 30-40˚C hingga kering dan rapuh, kemudian ditimbang berat keringnya. Selanjutnya simplisia kering di blender sampai menjadi serbuk dan disimpan dalam wadah yang terlindung dari sinar matahari sebelum dilakukan proses ekstraksi (Depkes RI, 1985).
3.3.1.4 Pembuatan Minyak Biji Bunga Matahari
Pembuatan minyak biji bunga matahari dilakukan dengan metode pengepresan panas menggunakan screw compression machine dengan suhu 90⁰C.
Minyak yang diperoleh kemudian ditampung dan diendapkan selama 7 hari. Hasil minyak kemudian disaring dan ditimbang beratnya.
26 3.3.2 Pembuatan pereaksi
3.3.2.1 Pereaksi Asam Klorida 2N
Sebanyak 16,67 mL asam klorida pekat dilarutkan dalam air suling hingga volume 100 mL (Ditjen POM, 1979).
3.3.2.2 Pereaksi Asam Sulfat 2 N
Sebanyak 5,4 mL asam sulfat pekat kemudian diencerkan dengan air suling hingga 100 mL (Ditjen POM, 1979).
3.3.2.3 Pereaksi Besi (3) Klorida 1%
Sebanyak 1 g besi (3) ditimbang, kemudian dilarutkan dalam air secukupnya hingga diperoleh larutan 100 mL (Depkes RI, 1995).
3.3.2.4 Pereaksi Bouchardat
Sebanyak 4 g kalium iodida ditimbang, kemudian dilarutkan dalam 20 mL air suling, ditambahkan iodium sebanyak 2 g dan dicukupkan dengan air suling hingga 100 mL (Ditjen POM, 1995).
3.3.2.5 Pereaksi Dragendorff
Sebanyak 8 g bismut (3) nitrat dilarutkan dalam asam nitrat 20 mL kemudian dicampur dengan larutan kalium iodida sebanyak 27,2 g dalam 50 mL air suling.
Didiamkan campuran sampai memisah sempurna. Larutan jernih diambil dan diencerkan dengan air secukupnya hingga 100 mL (Depkes RI, 1980).
3.3.2.6 Pereaksi Mayer
Sebanyak 1,3 g merkuri (2) klorida dilarutkan dalam 60 mL air suling.
Kemudian pada wadah lain sebanyak 5 g kalium iodide dilarutkan dalam 10 mL air lalu campurkan keduanya dan ditambahkan air suling hingga 100 mL (Depkes RI, 1980).
27 3.3.2.7 Pereaksi Molish
Sebanyak 3 g alfa-naftol ditimbang, kemudian dilarutkan dalam asam nitrat 0,5 N hingga volume 100 mL (Depkes RI, 1980).
3.3.2.8 Pereaksi Timbal (2) asetat 0,4M
Sebanyak 15,7 g timbal (2) asetat dilarutkan dalam air bebas karbondioksida hingga 100 ml (Ditjen POM, 1979).
3.3.3 Skrining Fitokimia Simplisia Sampel
Skrining fitokimia serbuk simplisia sampel meliputi pemeriksaan senyawa golongan alkaloid, flavonoid, glikosida, saponin, tanin, dan steroid/triterpenoid.
3.3.3.1 Pemeriksaan Alkaloid
Serbuk simplisia ditimbang sebanyak 0,5 g kemudian ditambahkan 1 ml asam klorida 2 N dan 9 ml air suling, dipanaskan diatas penangas air selama 2 menit, didinginkan dan disaring. Filtrat yang diperoleh dipakai untuk test alkaloid.
Diambil 3 tabung reaksi, lalu kedalam nya dimasukkan 0,5 filtrat.
Pada masing-masing tabung reaksi :
a. Ditambahkan 2 tetes pereaksi Mayer, akan terbentuk endapan menggumpal berwarna putih atau kuning
b. Ditambahkan 2 tetes pereaksi Bouchardat, akan terbentuk endapan berwarna coklat sampai kehitaman.
c. Ditambahkan 2 tetes pereaksi Dragendroff, akan terbentuk endapan berwarna coklat atau jingga kecoklatan.
Alkoloid positif jika terjadi endapan atau kekeruhan pada dua dari 3 percobaan diatas (Depkes RI, 1995).
28 3.3.3.2 Pemeriksaan Flavonoid
Sebanyak 0,5 g simplisia disari dengan 10 ml etanol, lalu direfluks selama 10 menit. Kemudian disaring panas – panas melalui kertas saring kecil berlipat.
Filtrat diencerkan dengan 10 ml air. Setelah dingin ditambahkan 5 ml eter, dikocok hati-hati dan didiamkan. Lapisan metanol diambil, lalu diuapkan pada suhu 40°C, sisanya dilarutkan dalam 5 ml etil asetat, disaring. Filtrat digunakan untuk uji flavonoida dengan cara sebagai berikut :
a. Sebanyak 1 ml larutan percobaan diuapkan hingga kering, sisa dilarutkan dalam 1 sampai 2 ml etanol 96%, lalu ditambahkan 0,5 g serbuk seng dan 2 ml asam klorida 2 N, didiamkan selama 1 menit. Ditambahkan 10 ml asam klorida pekat, dalam waktu 2 sampai 5 menit terjadi warna merah intensif, menunjukkan adanya flavonoida.
b. Sebanyak 1 ml larutan percobaan diuapkan hingga kering, sisa dilarutkan dalam 1 ml etanol 96%, lalu ditambahkan 0,1 g serbuk magnesium dan 10 ml asam klorida pekat, terjadi warna merah jingga, menunjukkan adanya flavonoida (Depkes RI, 1995).
3.3.3.3 Pemeriksaan Glikosida
Serbuk simplisia ditimbang sebanyak 3 g, lalu disari dengan 30 ml campuran etanol 96 % garis air (7: 3) dan 10 ml asam klorida 2N, direfluks selama 2 jam, didinginkan dan disaring. Diambil 20 ml filtrat, ditambahkan 20 ml air suling dan 20 ml timbal (2) aseatat 0,4 M, dikocok, didiamkan selama 5 menit lalu disaring.
Filtrat disari dengan 20 ml campuran kloforoform-isopropanol (3:2) sebanyak 3 kali pada kumpulan sari lapisan isopropanol diuapkan pada suhu tidak lebih dari 50˚C sisanya dilarutkan dengan 2 ml metanol untuk larutan percobaan. 0,1 ml larutan percobaan diuapkan diatas penangas air pada sisa ditambahkan 2 ml air
29
dan 5 tetes Molish, kemudian ditambahkan hati-hati 2 ml hati-hati asam sulfat, terbentuk cincin berwarna ungu pada batas cairan, menunjukkan adanya ikatan gula (Depkes, 1995).
3.3.3.4 Pemeriksaan Saponin
Serbuk simplisia ditimbang sebanyak 0,5 g dan dimasukkan kedalam tabung reaksi, lalu ditambahkan 10 ml air panas, didinginkan, kemudian dikocok kuat- kuat selama 10 menit jika terbentuk busa setinggi 1 – 10 cm yang stabil tidak kurang dari 10 menit dan buih tidak hilang dengan penambahan 1 tetes asam klorida 2N menunjukkan adanya saponin (Depkes RI,1995).
3.3.3.5 Pemeriksaan Tanin
Serbuk simplisia ditimbang sebanyak 1 g. Dididihkan selama 3 menit dalam air suling lalu didinginkan dan disaring. Pada filtrat ditambahkan 1 – 2 tetes pereaksi besi (3) klorida 1% b/v. Jika terjadi warna biru kehitaman atau hijau kehitaman menunjukkan adanya tanin (Farnsworth, 1966).
3.3.3.6 Pemeriksaan Steroid/Triterpenoid
Sebanyak 1 g sampel dimaserasi dengan 10 mL n-heksana selama 2 jam, lalu disaring. Filtrat diuapkan dalam cawan penguap, pada sisa ditambahkan 2 tetes asam asetat anhidrida dan 1 tetes asam sulfat pekat. Timbul warna biru atau hijau menunjukkan adanya steroid dan timbul warna merah, pink atau ungu menunjukkan adanya triterpenoid (Farnsworth, 1966).
30
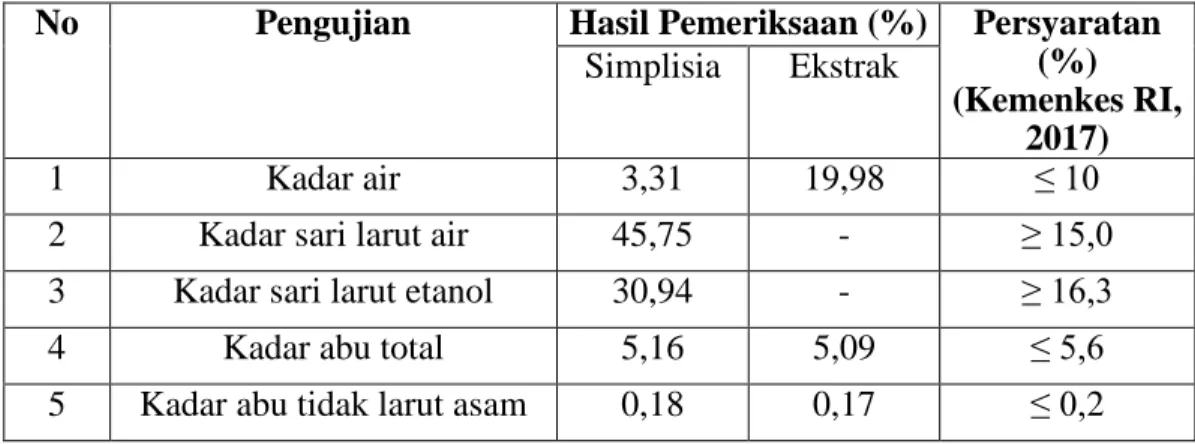
3.3.4 Pemeriksaan Karakteristik Simplisia Sampel
Pemeriksaan karakteristik simplisia meliputi pemeriksaan makroskopik, mikroskopik, penetapan kadar air, penetapan kadar sari larut dalam air, penetapan kadar sari larut dalam etanol, penetapan kadar abu total, dan penetapan kadar abu tidak larut dalam asam (Depkes RI, 1995).
3.3.4.1 Pemeriksaan Makroskopik dan Organoleptik
Pemeriksaan makroskopik dan organoleptik dilakukan dengan mengamati bentuk, bau, warna, dan rasa dari simplisia kelopak bunga rosela merah dan biji bunga matahari.
3.3.4.2 Pemeriksaan Mikroskopik
Pemeriksaan mikroskopik terhadap serbuk simplisia dilakukan dengan cara menaburkan serbuk simplisia diatas kaca objek kemudiaan meneteskan kloral hidrat, lalu ditutup dengan kaca penutup dan dilihat di bawah mikroskop.
3.3.4.3 Penetapan Kadar Air
Penetapan kadar air dilakukan dengan metode Azeotropi (destilasi toluen).
a. Penjenuhan Toluen
Sebanyak 200 mL toluena dan 2 mL air suling dimasukkan ke dalam labu alas bulat, didestilasi selama 2 jam. Setelah itu toluen dibiarkan mendingin selama 30 menit dan volume air pada tabung penerima dibaca dengan ketelitian 0,05 ml.
b. Penetapan Kadar Air Simplisia
Sebanyak 5 g serbuk simplisia yang telah ditimbang seksama dimasukkan ke dalam labu alas bulat, lalu dipanaskan hati-hati selama 15 menit. Setelah toluen mendidih, kecepatan tetesan diatur 2 tetes per detik, sampai sebagian air terdestilasi, kemudian kecepatan destilasi dinaikkan hingga 4 tetes per detik.
31
Setelah semua air terdestilasi, bagian dalam pendingin dibilas dengan toluen.
Destilasi dilanjutkan selama 5 menit, kemudian tabung penerima dibiarkan dingin sampai suhu kamar. Setelah air dan toluen memisah sempurna, volume air dibaca dengan ketelitian 0,05 mL. Selisih kedua volume air dibaca dengan kandungan air yang terdapat dalam bahan yang diperiksa. Kadar air dihitung dalam persen (WHO, 1998).
3.3.4.4 Penetapan Sari Larut Dalam Air
Sebanyak 5 g serbuk simplisia, dimaserasi selama 24 jam dalam 100 ml air kloroform (2,5 ml kloroform dan air suling sampai 1 liter) dalam labu bersumbat sambil dikocok sesekali selama 6 jam pertama kemudian dibiarkan selama 18 jam, lalu disaring. Sejumlah 20 ml filtrat pertama diuapkan sampai kering dalam cawan penguap yang berdasar rata- rata yang telah ditara dan sisa dipanaskan pada suhu 105˚C samapai bobot tetap. Kadar dalam persen sari yang larut dalam air dihitung terhadap bahan yang telah dikeringkan (Depkes RI, 1995).
3.3.4.5 Penatapan Kadar Sari Larut Dalam Etanol
Sebanyak 5 g serbuk simplisia dimaserasi selama 24 jam dalam 100 ml etanol 96 % dalam labu bersumbat sambil dikocok sesekali selama 6 jam pertama, kemudian dibiarkan selama 18 jam kemudian disaring cepat untuk menghindari penguapan etanol. Sejumlah 20 ml filtrat di uapkan sampai kering dalam cawan penguap yang berdasar rata yang telah dipanaskan dan di tara. Sisa dipanaskan pada suhu105˚C sampai bobot tetap. Kadar dalam persen sari yang larut dalam etanol 96 persen dihitung terhadap bahan yang telah dikeringkan (Depkes, 1995).
3.3.4.6 Penetapan Kadar Abu Total
Sebanyak 2 g serbuk simplisia dimasukkan dalam krus porselin yang telah dipijar dan ditara, kemudian ditarakan. Krus dipijar perlahan-lahan sampai arang