BAB 2
TINJAUAN PUSTAKA 2.1 Definisi
Artritis Reumatoid (AR) adalah suatu penyakit autoimun dan
merupakan poliartritis inflamasi yang bersifat kronis (artritis yang
mempengaruhi 5 atau lebih sendi). AR adalah penyakit multisistemik
kronis yang ditandai dengan peradangan pada membran sinovial
diartrosis yang dapat diikuti oleh kerusakan tulang rawan, erosi tulang,
serta pelemahan dan penghancuran ligamen, tendon, dan kapsul sendi
(Harris, 1989; Colletti, et al., 1997; Silman & Hochberg, 2001; Takatsu, et
al., 2005; Centers for Disease Control and Prevention, 2012).
Menurut American Rheumatism Association (ARA), AR adalah suatu penyakit kronik, biasanya ditandai dengan inflamasi di lapisan sendi atau
disebut juga sinovium. Penyakit ini dapat menyebabkan kerusakan sendi
jangka panjang, nyeri kronik, kehilangan fungsi dan kecacatan. World Health Organization (WHO) mendefinisikan AR sebagai suatu penyakit sistemik kronik yang melibatkan persendian, jaringan penghubung, otot,
tendon, dan jaringan fibrosa. Penyakit ini merupakan kondisi kecacatan
kronik yang menyebabkan rasa nyeri dan deformitas. Sedangkan,
Perhimpunan Dokter Spesialis Penyakit Dalam Indonesia
mendefinisikannya sebagai penyakit inflamasi sistemik kronik yang
terutama mengenai sendi diartrodial. Penyakit ini termasuk penyakit
autoimun dengan etiologi yang tidak diketahui (Rani, et al., 2008).
Menurut WHO, gangguan pendengaran adalah berkurangnya
kemampuan mendengar baik sebagian atau seluruhnya, pada salah satu
atau kedua telinga, baik derajat ringan atau lebih berat dengan ambang
pendengaran rerata lebih dari 26 dB pada frekuensi 500, 1000, 2000 dan
4000 Hz (Kolegium Ilmu Kesehatan T.H.T.K.L., 2008). Gangguan
pendengaran pada AR dapat berupa tuli konduktif (Conductive Hearing
maupun tuli campuran (mixed Hearing Loss/mixed HL) (Doig, et al., 1971;
Reiter, et al., 1980; Elwany, ElGarf, & Kamel, 1986; Colletti, et al., 1997;
Ozcan, et al., 2002; Atcherson & Prout, 2003; American
Speech-Language-Hearing Association, 2005; Dikici, et al., 2009).
2.2 Anatomi Kavum Timpani
Kavum timpani terutama berisi udara yang mempunyai ventilasi ke
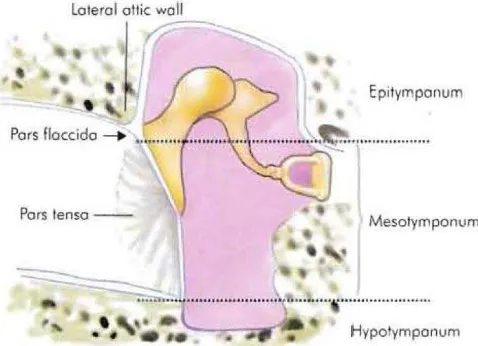
nasofaring melalui tuba eustachius. Menurut ketinggian batas superior dan
inferior membran timpani (Gambar 2.1), kavum timpani dibagi menjadi tiga
bagian, yaitu epitimpanum atau attik yang merupakan bagian kavum
timpani yang lebih tinggi dari batas superior membran timpani,
mesotimpanum yang merupakan ruangan di antara batas atas dengan
batas bawah membran timpani, dan hipotimpanum yaitu bagian kavum
timpani yang terletak lebih rendah dari batas bawah membran timpani
(Helmi, 2005; Lalwani, 2007; Dhingra, 2010).
Gambar 2.1 Pembagian Kavum Timpani (Dhingra, 2010)
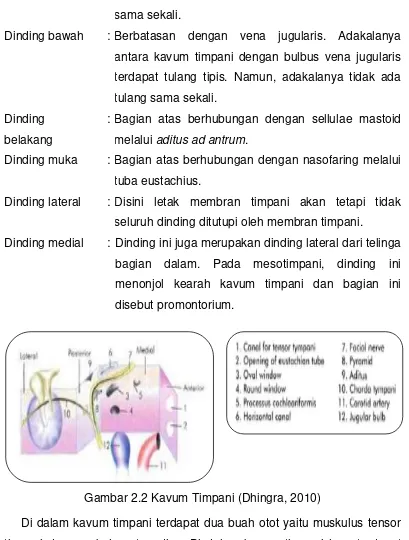
Secara skematis, kavum timpani (Gambar 2.2) diibaratkan seperti
kubus atau kotak korek api dengan enam dinding, yaitu (Austin, 1997;
Soetirto, Hendarmin, & Bashiruddin, 2007):
Dinding atas : Berupa tulang tipis yang membatasi dura yang
sama sekali.
Dinding bawah : Berbatasan dengan vena jugularis. Adakalanya
antara kavum timpani dengan bulbus vena jugularis
terdapat tulang tipis. Namun, adakalanya tidak ada
tulang sama sekali.
Dinding
belakang
: Bagian atas berhubungan dengan sellulae mastoid
melalui aditus ad antrum.
Dinding muka : Bagian atas berhubungan dengan nasofaring melalui
tuba eustachius.
Dinding lateral : Disini letak membran timpani akan tetapi tidak
seluruh dinding ditutupi oleh membran timpani.
Dinding medial : Dinding ini juga merupakan dinding lateral dari telinga
bagian dalam. Pada mesotimpani, dinding ini
menonjol kearah kavum timpani dan bagian ini
disebut promontorium.
Gambar 2.2 Kavum Timpani (Dhingra, 2010)
Di dalam kavum timpani terdapat dua buah otot yaitu muskulus tensor
timpani dan muskulus stapedius. Di dalam kavum timpani juga terdapat
tiga buah tulang pendengaran (osikel), dari luar ke dalam: maleus, inkus,
dan stapes (Austin, 1997; Helmi, 2005; Dhingra, 2010). Tulang-tulang
pendengaran, membentuk suatu sistem pengungkit yang meneruskan
unit, memberikan respon rotasi terhadap gerakan membran timpani
melalui suatu aksis yang merupakan suatu garis antara ligamentum
maleus anterior dan ligamentum inkus pada ujung prosesus brevis.
Gerakan-gerakan tersebut tetap dipelihara berkesinambungan oleh sendi
inkudomaleus. Gerakan rotasi tersebut diubah menjadi gerakan seperti
piston pada stapes melalui sendi inkudostapedius (Austin, 1997).
Baik sendi inkudomaleus (Gambar 2.3) maupun inkudostapedius
(Gambar 2.4) merupakan sendi diartrodial. Epitel telinga tengah terdapat
pada permukaan luar kapsul sendi tersebut, sedangkan di permukaan
dalamnya terdapat membran sinovial. Kapsul sendi terdiri atas jaringan
fibrosa dengan kandungan serat elastis yang banyak. Diskus artikular
merupakan ruang di kedua ujung artikular yang sebagian besarnya terdiri
atas fibrokartilago (Wenig & Michaels, 2007).
Gambar 2.3 Sendi Inkudomaleus (Wenig & Michaels, 2007)
Gambar 2.4 Sendi Inkudostapedius (McCall, et al., 2010)
2.3 Anatomi Telinga Dalam
Telinga dalam terletak sebelah medial dari telinga tengah di dalam
pars petrosa tulang temporal (Donaldson, 1990; Dhingra, 2010). Telinga
dalam disebut juga dengan labirin. Labirin terdiri dari:
1. Labirin bagian tulang yang merupakan susunan ruangan yang terdapat
dalam pars petrosa tulang temporal dan merupakan salah satu tulang
yang terkeras di tubuh. Labirin tulang terdiri dari vestibulum, kanalis
semisirkularis, dan koklea. Bagian ini berisi cairan perilimfe yang tinggi
natrium dan rendah kalium.
2. Labirin bagian membran yang merupakan susunan kantong-kantong
dan duktus yang saling berhubungan dan terdapat di dalam labirin
tulang. Labirin membran terdiri dari sakulus, utrikulus, kanalis
semisirkularis, dan koklea. Bagian ini berisi cairan endolimfe yang
tinggi kalium dan rendah natrium (Wright, 1997; Gulya, 2003).
Labirin bagian tulang dan membran memiliki bagian vestibularis dan
bagian koklearis. Bagian vestibularis berhubungan dengan keseimbangan,
sementara bagian koklearis merupakan organ pendengaran. Koklea terdiri
dari organ sensorik yaitu organ corti. Koklea merupakan saluran yang
berbentuk spiral dengan dua setengah putaran yang panjangnya kurang
lebih 35 cm. Aksis dari spiral tersebut dikenal sebagai modiolus (Austin,
1997; Pawlowsky, 2004; Lim, 2006).
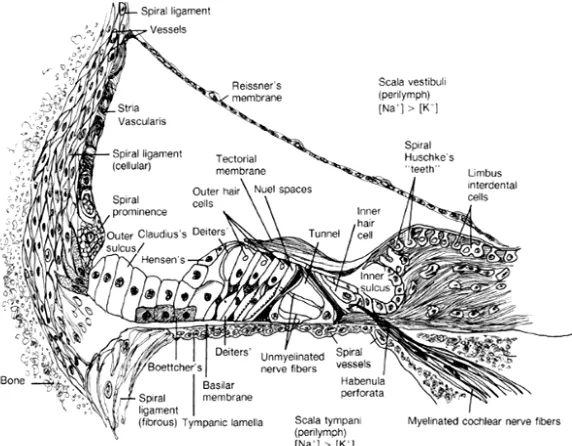
Gambar 2.5 Duktus Koklea (Bailey, Johnson, & Newlands, 2006)
Segitiga dari duktus koklea seperti yang diperlihatkan pada Gambar
2.5, sisi dasarnya membentuk batas antara skala media dan skala timpani
yaitu membran basilaris dan lamina spiralis pars osseus termasuk
spiralis, stria vaskularis, prominensia spiralis dan sulkus eksternal sebagai
sisi lateralnya. Sisi miringnya adalah membran reissner dan membran
basilaris (Mills, Khariwala, & Weber, 2006).
Koklea terbagi menjadi 3 ruang yaitu skala vestibuli, skala media, dan
skala timpani. Skala vestibuli dan skala timpani adalah labirin tulang dari
koklea yang berisi cairan perilimfe. Skala vestibuli dan skala timpani saling
berhubungan di helikotrema pada apeks koklea. Pada bagian basis
koklea, skala vestibuli berakhir di foramen ovale dan skala timpani pada
foramen rotundum. Skala media yang berisikan cairan endolimfe berada
diantara skala vestibuli dan skala timpani (Mills, Khariwala, & Weber,
2006). Stria vaskularis terdiri dari 3 lapisan sel yaitu sel marginal, sel
intermediet, dan sel basal. Sel-sel stria vaskularis merupakan
satu-satunya sel yang berhubungan dengan pembuluh darah di koklea. Stria
vaskularis bertanggung jawab menjaga konsentrasi ion kalium dalam
cairan endolimfe dan menjaga potensial positif endolimfe pada skala
media agar tetap tinggi (Austin, 1997; Wright, 1997).
Organ corti merupakan rumah dari sel sensoris pendengaran. Organ
corti terletak di sepanjang membran basilaris dan menonjol dari basis ke
apeks koklea. Pada organ corti terdapat sel-sel yang terdiri dari sel
sensoris (sel rambut dalam dan sel rambut luar), sel pendukung (sel
deiter, sel phalangeal dalam), ujung saraf aferen dan eferen, sel pilar dan
sel hansen. Di dalam organ corti terdapat kira-kira 15.500 sel rambut.
Sel-sel ini dikelompokkan menjadi Sel-sel rambut luar yang berjumlah 3.500 Sel-sel
dan sel rambut dalam yang berjumlah 12.000 sel. Sel rambut dalam dan
luar memegang peranan penting pada perubahan energi mekanik menjadi
energi listrik. Fungsi sel rambut dalam sebagai mekanoreseptor utama
yang mengirimkan sinyal syaraf ke neuron pendengaran ganglion spiral
dan pusat pendengaran sedangkan fungsi sel rambut luar adalah
meningkatkan puncak gelombang berjalan dengan meningkatkan aktivitas
membran basilaris. Peningkatan gerakan ini disebut cochlear amplifier
Vaskularisasi
Telinga dalam mendapat vaskularisasi dari a.labirintin cabang dari
a.serebellaris anterior, tetapi dapat juga sebagai cabang langsung dari
a.basilaris atau a.vertebralis. Arteri ini memasuki meatus akustikus
internus dan terpisah menjadi a.vestibularis anterior a.koklearis komunis
yang bercabang pula menjadi a.koklearis dan a.vestibulokoklearis.
A.vestibularis anterior memperdarahi vestibularis, utrikulus, dan sebagian
duktus semisirkularis. A.koklearis berjalan mengitari n.akustikus di kanalis
akustikus internus dan di dalam koklea mengitari modiolus.
A.vestibulokoklearis sampai di modiolus dan terpisah menjadi cabang
terminal vestibular dan cabang koklear. Cabang vestibular memperdarahi
sakulus, sebagian besar kanalis semisirkularis dan ujung basal koklea.
Cabang koklear memperdarahi ganglion spiralis, lamina spiralis ossea,
limbus dan ligamentum spiralis. Vena dialirkan ke v.labirintin yang
diteruskan ke sinus petrosus inferior atau sinus sigmoideus. Vena-vena
melewati akuaduktus vetibularis dan koklearis ke sinus petrosus superior
dan inferior (Austin, 1997; Wright, 1997).
Persarafan
N.vestibulokoklearis yang dibentuk oleh bagian koklearis dan
vestibularis, di dalam meatus akustikus internus bersatu pada sisi lateral
akar n.fasialis dan memasuki batas antara pons dan medulla. Sel-sel
sensoris vestibularis dipersarafi n.koklearis dengan ganglion vestibularis
n.koklearis dengan ganglion spiralis corti terletak di modiolus. Pada dasar
meatus akustikus internus terletak ganglion vestibulare (Donaldson, 1990;
Austin, 1997).
2.4 Fisiologi Pendengaran
Proses mendengar diawali dengan ditangkapnya energi bunyi oleh
daun telinga dalam bentuk gelombang. Setelah memasuki meatus
eksterna, bunyi akan menggetarkan membran timpani selanjutnya
melalui osikula, akhirnya getaran yang telah diperkuat daya dorongnya
diteruskan ke dalam perlimfe yang terdapat dalam koklea. Bila frekuensi
getaran yang masuk sangat rendah (frekuensi subsonik), maka lintasan
gelombangnya adalah: fenestra ovalis → skala vestibuli → helikotrema →
skala timpani → fenestra rotundum . Lintasan ini tidak berlaku jika
frekuensi bunyi lebih tinggi. Untuk frekuensi bunyi sonik (16 – 20.000 Hz),
lintasannya sebagai berikut: fenestra ovalis → skala vestibuli → duktus
koklearis → skala timpani → fenestra rotundum (Kolegium Ilmu Kesehatan
T.H.T.K.L., 2008).
Duktus koklearis merupakan bagian labirin membran. Bila pintasan
gelombang bunyi menggerakkan membran basilaris maka akan terjadi
efek gesekan membran tektoria terhadap rambut-rambut sel sensorik
pada organ corti. Pergerakan sel rambut tersebut akan menimbulkan
reaksi biokimiawi di dalam sel sensorik sehingga timbul muatan listrik
negatif pada dinding sel. Ujung-ujung saraf kedelapan yang menempel
pada dasar sel-sel sensorik akan menampung impuls yang terbentuk.
Lintasan impuls auditorik selanjutnya adalah: ganglion spiralis corti →
nervus VIII → nukleus koklearis → kolikulus inferior → korpus genikulatum
medial → korteks auditori (area 39 -40) di lobus temporalis serebrum
(Kolegium Ilmu Kesehatan T.H.T.K.L., 2008).
2.5 Epidemiologi dan Genetika
AR merupakan penyakit autoimun yang paling sering dijumpai yaitu
sebanyak 0,5-1% populasi. Penyakit ini biasanya menyerang kelompok
dewasa produktif berumur 20-40 tahun. Perempuan kira-kira 2,5-3 kali
lebih sering daripada laki-laki (Brooker, 1988; Abdel-Nasser, Rasker, dan
Valkenburg, 1997; Carter, 2005; Takatsu, et al., 2005; Alamanos,
Voulgari, dan Drosos, 2006; Junior, et al., 2006). AR ditemukan di seluruh
dunia dan dijumpai pada semua ras. Serangan awal paling sering terjadi
pada dekade keempat dan kelima, dengan 80% dari semua pasien
wanita berusia 60-64 tahun dijumpai enam kali lebih banyak daripada
wanita berusia 18-29 tahun (Lipsky, 2008).
Studi keluarga menunjukkan pengaruh genetik. AR berat pada saudara
kandung pasien AR ditemukan kira-kira empat kali lebih banyak. Hal ini
dihubungkan dengan keberadaan autoantibodi faktor reumatoid. Sekitar
10% pasien AR akan mempunyai saudara kandung yang juga menderita
AR. Pada kembar monozigotik, kemungkinan menderita AR adalah sekitar
empat kali lebih banyak daripada kembar dizigotik (Lipsky, 2008).
Pada tahun 2005, sekitar 1,5 juta orang dewasa Amerika Serikat (AS)
yang berusia ≥18 menderita AR atau sebanyak 0,6%. Terjadi penurunan
dari perkiraan sebelumnya yaitu sebanyak 2,1 juta orang pada tahun
1990. Sistem perawatan kesehatan AS pada tahun 2001-2005
memperkirakan bahwa 1,5 juta orang dewasa AS menderita AR
(Lawrence, et al., 1998; Sacks, Luo, & Helmick, 2010). Dilakukan survei
dengan nyeri muskuloskeletal pada total populasi pedalaman sebanyak
4683 orang dan kota sebanyak 1071 orang, dengan umur ≥15 tahun di
Jawa Tengah. Prevalensi untuk AR definitif yang memenuhi kriteria ARA
di kawasan pedalaman adalah sebanyak 0,2% dan di kawasan perkotaan
adalah sebanyak 0,3% (Darmawan, et al., 1992).
Pada penelitian yang dilakukan Ozcan, et al. (2002), pada kelompok
penderita AR gangguan pendengaran dijumpai sebesar 51,4%,
sedangkan pada kelompok kontrol gangguan pendengaran hanya sebesar
14,3%. Pada pasien dengan AR, baik SNHL maupun CHL telah
dilaporkan. SNHL merupakan temuan yang sering pada pasien AR,
walaupun CHL dan mixed HL juga dapat ditemukan. SNHL dilaporkan lebih sering dijumpai yaitu sebanyak 24-60%. CHL juga telah dilaporkan
pada pasien dengan AR, namun dengan prevalensi yang lebih rendah
yaitu sebanyak 0-24,3%. Sedangkan mixed HL dijumpai sebanyak 10-10,8% (Doig, et al., 1971; Reiter, et al., 1980; Walek, Fritze, & Kolarz,
1980; Elwany, ElGarf, & Kamel, 1986; Kastanioudakis, et al., 1995;
2.6 Etiologi
Walaupun faktor penyebab maupun patogenesis AR yang sebenarnya
hingga kini belum diketahui dengan pasti, faktor genetik seperti produk
kompleks histokompatibilitas utama (Major Histocompatibility
Complex/MHC) kelas II Human Leukocyte Antigen DR4 Locus (HLA-DR4) dan beberapa faktor lingkungan telah lama diduga berperan dalam
timbulnya penyakit ini (Daud, 2006; Junior, et al., 2006).
a. Kompleks histokompatibilitas utama kelas II
Telah lama diketahui bahwa AR lebih sering dijumpai pada kembar
monozigotik dibandingkan dengan kembar dizigotik. Akan tetapi bukti
terkuat yang menunjukkan bahwa AR memiliki predisposisi genetik
diketahui dari terdapatnya hubungan antara produk kompleks
histokompatibilitas utama kelas II, khususnya HLA-DR4 dengan AR
seropositif. Data dari beberapa penelitian menunjukkan bahwa pasien
yang mempunyai HLA-DR4 memiliki risiko relatif 4:1 untuk menderita
penyakit ini (Daud, 2006).
b. Hubungan hormon sex dengan AR
Berbagai obeservasi telah menimbulkan dugaan bahwa hormon sex
merupakan salah satu faktor predisposisi penyakit ini. Sebagai contoh,
prevalensi AR diketahui 3 kali lebih banyak diderita kaum wanita
dibandingkan dengan kaum pria. Rasio ini dapat mencapai 5:1 pada
wanita usia subur. Demikian pula remisi seringkali dijumpai pada pasien
AR yang sedang hamil (Daud, 2006).
c. Faktor infeksi sebagai penyebab AR
Sejak tahun 1930, faktor infeksi telah diduga merupakan penyebab
AR. Dugaan faktor infeksi sebagai penyebab AR juga timbul karena
umumnya onset penyakit ini terjadi secara mendadak dan timbul disertai
dengan gambaran inflamasi yang mencolok. Dengan demikian timbul
dugaan kuat bahwa penyakit ini sangat mungkin disebabkan oleh
tercetusnya suatu proses autoimun oleh suatu antigen tunggal atau
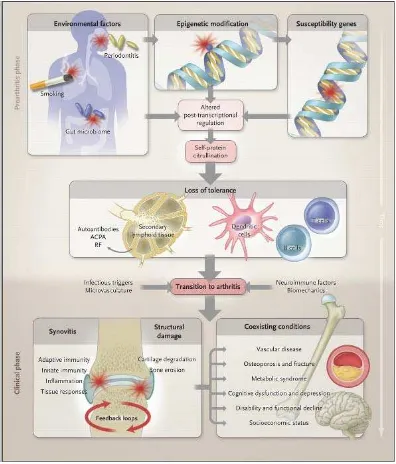
penyebab AR antara lain adalah bakteri, mikoplasma, atau virus (Daud, 2006). Selengkapnya, dideskripsikan pada Gambar 2.6.
Gambar 2.6 Tahapan Perkembangan AR (McInnes & Schett,
2.7 Patologi dan Patogenesis
2011)
Destruksi jaringan sendi terjadi melalui dua cara. Pertama adalah
destruksi yang disebabkan produksi protease, kolagenase, dan
enzim-enzim hidrolitik lainnya. Enzim-enzim-enzim ini memecah kartilago, ligamen,
dengan radikal oksigen dan metabolit asam arakidonat oleh leukosit
polimorfonuklear dalam cairan sinovial. Proses ini diduga sebagai bagian
dari respon autoimun terhadap antigen yang diproduksi secara lokal
(Carter, 2005).
Kedua, destruksi jaringan yang terjadi melalui kerja pannus reumatoid.
Pannus merupakan jaringan granulasi yang terdiri dari makrofag yang
teraktivasi, sel fibroblas yang berproliferasi, dan jaringan mikrovaskular
yang terbentuk dari sinovium yang meradang dan kemudian meluas ke
sendi. Di sepanjang pinggir pannus terjadi destruksi kolagen dan
proteoglikan melalui produksi enzim oleh sel di dalam pannus tersebut
(Carter, 2005, Daud, 2006).
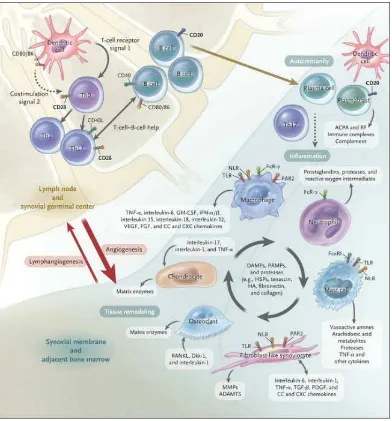
2.7.1 Proses imunologi sinovial dan inflamasi
Sinovitis terjadi bila leukosit menginfiltrasi kompartemen sinovial.
Akumulasi leukosit tersebut berasal dari migrasi bukan berasal dari
proliferasi lokal. Migrasi sel tersebut disebabkan oleh aktivasi endotel
pembuluh-pembuluh mikro sinovial, yang meningkatkan ekspresi
molekul-molekul perlengketan (yang meliputi integrin, selektin, dan anggota
superfamili imunoglobulin) dan kemokin. Oleh karena itu, neoangiogenesis
yang dipicu oleh kondisi hipoksik lokal, sitokin, dan limfangiogenesis
merupakan ciri khas sinovitis pada stadium dini. Perubahan lingkungan
mikro ini dipadu dengan penyusunan kembali arsitektur sinovial dan
aktivasi fibroblas lokal, menyebabkan pembentukan jaringan inflamasi
sinovial (Shah & Clair, 2012).
Interaksi antara sel dendrit, sel T, dan sel B terjadi terutama pada
kelenjar getah bening. Keadaan ini menimbulkan reaksi autoimun
terhadap self protein yang mengandung sitrulin. Pada membran sinovial dan sumsum tulang di dekatnya, sistem imun adaptif dan bawaan berpadu
meningkatkan pemodelan ulang dan kerusakan jaringan. Loop feedback
positif dimediasi oleh interaksi antara leukosit, Fibroblast-Like Synoviocyte
mengakibatkan fase kronis (Shah & Clair, 2012). Selengkapnya,
dideskripsikan pada Gambar 2.7.
Gambar 2.7 Proses Sistem Imun dalam Sendi pada AR (McInnes & Schett,
2.7.2 Kerusakan tulang rawan
2011)
Sinovium hiperplastik adalah kontributor utama kerusakan tulang rawan
pada AR. Kehilangan efek protektif normal dari sinovium (misalnya,
penurunan ekspresi lubrisin) mengubah sifat-sifat ikatan protein
permukaan tulang rawan, yang meningkatkan perlengketan dan invasi
14 dan 16 oleh FLS tersebut meningkatkan kerusakan ikatan kolagen tipe
II. Proses ini mengubah kandungan glikosaminoglikan dan retensi air yang
secara langsung menyebabkan disfungsi biomekanik. MMP-14 ternyata
merupakan MMP dominan yang diekspresikan oleh FLS untuk
mendegradasikan matriks kolagen tulang rawan. Enzim matriks lainnya
mendegradasi aggrecan dan karenanya semakin mengurangi integritas tulang rawan (Shah & Clair, 2012).
Inhibitor enzim endogen seperti Tissue Inhibitors of Metalloproteinase
(TIMP) gagal menghambat proses kehancuran ini. Selain itu, tulang rawan
artikular itu sendiri mempunyai potensi regeneratif yang terbatas.
Kondrosit mengatur secara fisiologik pembentukan dan pembelahan
matriks. Dengan pengaruh sitokin sinovial (terutama interleukin-1 dan
17A) dan intermediat nitrogen reaktif, tulang rawan kehilangan kondrosit
secara progresif. Proses ini pada akhirnya menyebabkan kehancuran
permukaan tulang rawan dengan tampilan radiografik berupa penyempitan
ruang sendi (McInnes & Schett,
2.7.3 Erosi tulang
2011;Shah & Clair, 2012).
Erosi tulang terjadi dengan cepat dan menyerang 80% pasien dalam
setahun setelah diagnosis ditegakkan. Hal ini berhubungan dengan
inflamasi yang berkepanjangan. Sitokin sinovial, terutama faktor
perangsang koloni makrofag dan Receptor Activator NF-κB Ligand
(RANKL) meningkatkan diferensiasi dan invasi osteoklas ke permukaan
periosteal yang dekat dengan tulang rawan sendi. Tumor Necrosis Factor-α (TNF-α) serta interleukin-1, 6, dan 17 memperkuat diferensiasi dan
aktivasi osteoklas tersebut. Osteoklas mempunyai bagian enzimatik asam
yang dapat menghancurkan jaringan yang mengalami mineralisasi, yang
meliputi tulang rawan yang mengalami mineralisasi dan tulang subkondral.
Kehancuran jaringan ini menimbulkan lubang-lubang resorpsi yang dalam,
Faktor-faktor mekanis juga memicu tempat tertentu untuk mengalami
erosi. Dengan demikian, tempat ‘yang rentan secara mekanis’ seperti
metakarpal kedua dan ketiga rentan terhadap erosi. Inflamasi yang
menerobos tulang kortikal memungkinkan akses sinovial ke sumsum
tulang. Hal ini menyebabkan inflamasi di sumsum tulang, dimana agregat
sel T dan sel B menggantikan lemak sumsum secara perlahan-lahan.
Pada AR, tulang periartikular yang mengalami erosi menunjukkan sedikit
bukti perbaikan, berbeda dengan tulang pada artropati akibat inflamasi
lainnya (Shah & Clair, 2012).
2.7.4 Patogenesis gangguan pendengaran pada AR
Patogenesis gangguan pendengaran pada AR belum diketahui secara
pasti. Sendi inkudomaleus dan inkudostapedius adalah sendi diartrodial
(diartrosis sejati), sehingga dapat dikenai lesi rematoid yang sama
sebagaimana sendi diartrodial lain pada tubuh. Pada persendian
tulang-tulang pendengaran pasien AR, dijumpai disolusi
Vaskulitis, neuritis, kerusakan sel rambut koklea, ototoksisitas obat
yang digunakan dalam pengobatan, dan akumulasi deposit imun pada
telinga bagian dalam dihubungkan dengan kejadian SNHL. Meskipun tidak
ada referensi langsung bagi mekanisme tersebut, telah diketahui bahwa
penyakit autoimun dapat menghasilkan gangguan pendengaran perseptif
sebagai akibat dari perubahan degeneratif pada organ corti (Heyworth &
Liyanage, 1972; Coutinho & Duarte, 2002; Dikici, et al., 2009).
material diskus
bersamaan dengan proliferasi pada permukaan diskus dan artikular,
dengan pembentukan jaringan seperti pannus (Kakani, Mehra, & Deodhar,
1990; Magaro, Zoli, & Altomonte, 1990; Colletti, et al., 1997; Frade &
Martin, 1998; Salvinelli, et al., 2006; Dikici, et al., 2009).
Mekanika abnormal di telinga tengah telah dikemukakan sebagai
kemungkinan penyebab CHL. Kelemahan mekanisme transduser telinga
tengah, yang disebabkan oleh keterlibatan ligamentum suspensorium
diajukan sebagai penyebab CHL tersebut. Inflamasi pada tahap aktif
penyakit dan fibrosis dalam rangkaian tulang pendengaran dapat
menyebabkan kurangnya elastisitas dan munculnya komponen konduktif
pada gangguan pendengaran (Schleuning, et al., 2006; Dikici, et al.,
2009). Reiter, et al. (1980) juga mengutarakan peningkatan kekakuan
persendian pada rangkaian tulang pendengaran tanpa penurunan
stabilitas ligamennya. Selain itu, vaskulitis dapat mengakibatkan perfusi
yang tidak adekuat pada tulang pendengaran terutama pada prosessus
longus inkus. Nekrosis pada struktur ini dapat menyebabkan diskontinuitas
tulang pendengaran (Colletti, et al., 1997).
Namun, ada juga peneliti yang mengemukakan bahwa kekakuan
persendian inkudomaleus dan inkudostapedius yang terjadi tidak
menyebabkan perubahan dalam konduksi suara ke koklea. Ini disebabkan
persendian tersebut utuh secara fungsional selama transmisi suara.
Keadaan ini dapat menjelaskan keadaan
2.8 Manifestasi Klinis
pendengaran yang normal
meskipun terjadi peningkatan kekakuan sendi di telinga tengah (Dikici, et
al., 2009).
Potensi inflamasi sendi yang menyebabkan kerusakan tulang rawan, erosi tulang, dan perubahan integritas sendi merupakan petanda penyakit
ini. Manifestasi artikular AR dapat dibagi menjadi gejala inflamasi akibat
aktivitas sinovitis yang bersifat reversibel dan gejala akibat kerusakan
struktur pesendian yang bersifat ireversibel. Poliartritis yang terjadi bersifat
simetris dan mengenai sendi perifer. Deformitas sendi dapat terjadi akibat
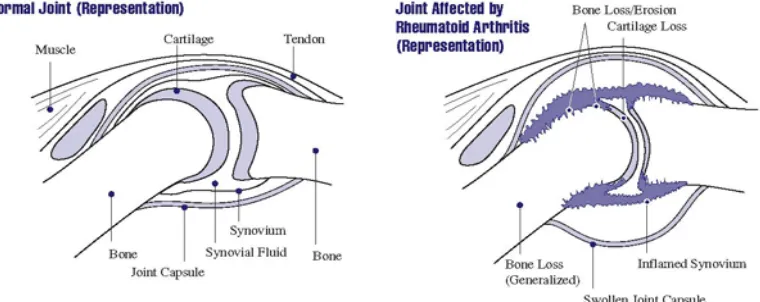
inflamasi yang menetap. Perbandingan antara sendi normal dan sendi
yang terkena AR diperlihatkan pada Gambar 2.8. AR dapat pula
menyerang organ-organ lain di luar sendi (manifestasi ekstraartikular)
seperti vaskulitis dan neuropati akibat vaskulitis (Kasper, et al., 2005;
Gambar 2.8 Perbandingan antara Sendi Normal dan yang Terkena AR (National Institute of Arthritis, Musculoskeletal and Skin Diseases, 2009)
Manifestasi otologi penyakit AR dapat melibatkan telinga luar, tengah,
dan dalam. Nodul reumatoid, yang berupa lesi kutan atau subkutan dapat
dijumpai pada telinga luar. Manifestasi telinga tengah dicirikan dengan
CHL, sedangkan manifestasi telinga dalam berupa SNHL. Komponen
konduktif dapat berkembang lebih lambat daripada komponen
sensorineural. Hal ini menyebabkan
2.9 Diagnosis AR
mixed HL. Gangguan pendengaran pada pasien AR dapat bermanifestasi sebagai gangguan pendengaran
bilateral ringan pada frekuensi tinggi. Tinitus bilateral atau unilateral dapat
dijumpai. Meskipun demikian, pendengaran yang normal juga dapat
dijumpai pada penyakit ini (Dikici, et al., 2009; Bewly & Ruckenstein,
2014).
Diagnosis AR ditegakkan berdasarkan kriteria ARA tahun 1978.
Menurut ARA 1987, diagnosis AR dapat dikatakan positif apabila terdapat
sekurang-kurangnya empat dari kriteria-kriteria yang sekurang-kurangnya
sudah berlangsung selama 6 minggu (Arnett, et al., 1988; Daud, 2006).
Tabel 2.1 Kriteria Diagnosis menurut ARA 1987 (Arnett, et al., 1988; Daud, 2006; Salvinelli, et al., 2006)
No. Kriteria Definisi
1. Kaku pagi hari Kekakuan pada pagi hari pada persendian dan sekitarnya, sekurang-kurangnya selama 1 jam sebelum perabaikan maksimal
2. Artritis pada tiga daerah
persendian atau lebih
Pembengkakan jaringan lunak atau persendian atau lebih fusi (bukan pertumbuhan tulang) pada sekurang-kurangnya tiga sendi secara bersamaan yang diobservasi oleh seorang dokter
3. Artritis pada
persendian tangan
Sekurang-kurangnya terjadi pembengkakan satu persendian tangan seperti yang tertera di atas
4. Artritis simetris Keterlibatan sendi yang sama seperti yang tertera pada kriteria 2 pada kedua belah sisi (keterlibatan PIP, MCP, atau MTP bilateral dapat diterima walaupun tidak mutlak bersifat simetris)
5. Nodul reumatoid Nodul subkutan pada penonjolan tulang atau permukaan ekstensor atau daerah juksta artikuler yang diobservasi oleh seorang dokter
6. Faktor reumatoid dalam serum
Terdapatnya titer abnormal faktor reumatoid serum yang diperiksa dengan cara memberikan hasil positif kurang dari 5% kelompok kontrol yang diperiksa
7. Perubahan gambaran radiologis
Perubahan gambaran radiologis yang khas pada AR pada pemeriksaan sinar-x tangan posterior atau pergelangan tangan yang harus menunjukkan adanya erosi atau dekalsifikasi tulang yang berlokasi pada sendi atau daerah yang berdekatan dengan sendi (perubahan akibat osteoartritis saja tidak memenuhi persyaratan).
2.10 Diagnosis Gangguan Pendengaran pada AR
Melalui anamnesis, dapat diketahui riwayat gangguan pendengaran
maupun tinitus. Dapat diketahui pula riwayat infeksi telinga, trauma,
penggunaan obat ototoksik, komplikasi sistemik dari penyakit kronis lain,
maupun gejala penyakit telinga lain. Pada pemeriksaan otoskopi,
Pemeriksaan audiometri nada murni
Dengan menggunakan audiometri nada murni, dapat dijumpai jenis
gangguan pendengaran CHL, SNHL, maupun mixed HL (Doig, et al., 1971; Reiter, et al., 1980; Elwany, ElGarf, & Kamel, 1986; Colletti, et al.,
1997; Ozcan, et al., 2002; Dikici, et al., 2009). Melalui pemeriksaan ini,
dapat dijumpai peningkatan ambang pendengaran pada frekuensi 8000
Hz (Baradaranfar & Doosti, 2010). Ambang pendengaran meningkat
bersamaan dengan peningkatan usia, Laju Endap Darah (LED), dosis
kumulatif metotreksat, faktor reumatoid (Reumatoid Factor/RF), Protein
C-Reaktif (C-Reactive Protein/CRP), jumlah trombosit, dan durasi penyakit
pada pasien dengan nodul reumatoid. Ambang pendengaran dijumpai
lebih tinggi pada pria dibandingkan dengan wanita (Dikici, et al., 2009).
Pemeriksaan timpanometri
Dengan menggunakan nada probe 660 Hz ditemukan penurunan kekakuan sendi. Nekrosis pada prosesus longus inkus akibat vaskulitis,
dapat menyebabkan diskontinuitas tulang pendengaran yang
digambarkan dengan timpanogram tipe Ad. Sebaliknya, peningkatan
kekakuan tulang-tulang pendengaran juga bisa ditemukan, yang
digambarkan dengan timpanogram tipe As pada pasien AR kronis dengan
menggunakan nada probe 220 Hz (Moffat, et al., 1977; Elwany, ElGarf, & Kamel, 1986; Siamopoulou-Mavridou, et al., 1990; Colletti, et al., 1997;
Takatsu, et al., 2005; Dikici, et al., 2009).
Pemeriksaan Transient Evoked OtoAcoustic Emission (TEOAE)
Dapat dijumpai penurunan nilai TEOAE bersamaan dengan
peningkatan usia, jumlah trombosit, dosis kumulatif metotreksat, dan
durasi penyakit. Namun, nilai TEOAE dapat meningkat ketika nilai Protein
C-Reaktif dan faktor reumatoid meningkat. Nilai TEOAE lebih rendah pada
2.11 Diagnosis Banding
Gangguan pendengaran yang disebabkan oleh AR dapat didiagnosis
banding dengan:
1. Penyebab gangguan pendengaran konduktif lain yang diakibatkan oleh
gangguan mekanisme hantaran di telinga luar atau telinga tengah,
antara lain: terdapat cairan di telinga tengah, otitis media, otitis media
serosa, gangguan fungsi tuba eustachius, perforasi membran timpani,
impaksi serumen, otitis eksterna, benda asing, atau malformasi telinga
luar dan tengah.
2. Penyebab gangguan pendengaran sensorineural lain yang diakibatkan
oleh kelainan di koklea, N.VIII, dan pusat pendengaran di korteks
serebri, antara lain: obat ototoksik, proses penuaan, trauma kepala,
malformasi telinga dalam, dan terpapar bising.
3. Penyebab gangguan pendengaran campuran lain yang diakibatkan
gangguan konduktif dan sensorineural. (Yellin, 1991; Feldman 1997,
Atcherson & Prout, 2003; Soetirto, Hendarmin, & Bashirudddin, 2010;
American Speech-Language-Hearing Association, 2005)
2.12 Matrix Metalloproteinase-3 (MMP-3)
MMP-3 (Stromelysin-1, Progelatinase) dideskripsikan pertama kali
pada tahun 1985 sebagai protein 51-kDa yang disekresikan oleh fibroblas
kelinci. MMP-3 dibedakan dari kolagenase karena tidak mampu
mendegradasikan kolagen tipe I. MMP-3 mempunyai struktur MMP dasar
dengan domain serupa hemopexin. Proenzim laten 51-kDa bisa diaktifkan
dengan pengangkatan prodomain proteolitik, misalnya dengan serin
protease, tripsin-2, dan matriptase, yang menghasilkan enzim aktif 43-kDa
pada manusia. Kadar MMP-3 ditingkatkan oleh interleukin 1b dan
2.12.1 Aktivitas biologi MMP-3
MMP-3 adalah anggota famili proteinase ekstraselular. Protein ini
terlibat dalam penguraian matriks ekstraselular pada proses fisiologi
normal, seperti perkembangan embrio, reproduksi, dan pemodelan ulang
jaringan, serta dalam proses penyakit, seperti artritis dan kanker. Ini
disebabkan oleh spesifisitas substratnya yang luas. Target MMP-3
meliputi kolagen, fibronektin, laminin, plasminogen, e-cadherin dan MMP
lainnya (berpartisipasi dalam aktivasi pro MMP) (Nagase, Visse, &
Murphy, 2006; Enzo Life Sciences, 2014;
Kultur tulang rawan pelat pertumbuhan terbukti menghasilkan vesikel
matriks yang mengandung pro MMP-3 dan MMP-3 aktif. Kondrosit dari
zona pertumbuhan menghasilkan vesikel membran dengan kandungan
MMP yang lebih tinggi, yang mengindikasikan bahwa enzim ini terlibat
dalam pemodelan ulang matriks ekstraselular pada zona sel hipertrofik
pada pelat pertumbuhan tulang panjang. Sebuah studi tentang neuron
dopaminergik menunjukkan adanya peranan pro-apoptotik dari MMP-3
intrasel aktif. Selama apoptosis, pro MMP-3 dibelah untuk menjadi bentuk
aktif secara katalitik oleh serin proteinase. Ketiadaan aktivitas MMP-3
intrasel melindungi sel-sel dopaminergik dari apoptosis. Penghambatan
aktivitas MMP-3 melemahkan aktivasi caspase-3, enzim pengeksekusi
dalam apoptosis (Olsen, et al., 2011).
2.12.2 Susunan domain
MMP-3 mempunyai susunan domain yang serupa dengan susunan
domain kolagenase (Nagase, Visse, & Murphy, 2006). Gen MMP-3
(Gambar 2.9) berlokasi pada lengan panjang (q) dari kromosom 11 pada
posisi 22.3 (lokasi sitogenetik: 11q22.3) (Genetics Home Reference,
Gambar 2.9 Gen MMP3 (Genetics Home Reference, 2014).
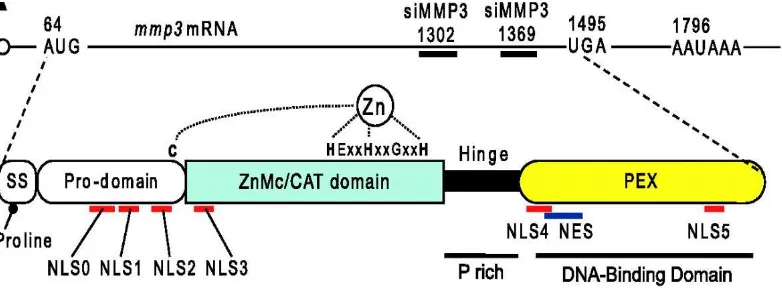
mRNA MMP-3 (Gambar 2.10) digambarkan secara skematis di atas
dengan kodon permulaan AUG, kodon stop UAG dan posisi target siRNA (siMMP3-1369 dan siMMP3-1302). SS mengindikasikan rangkaian sinyal
sekresi yang mengandung pemutus helix prolin pada asam amino kelima.
Prodomain (Pro) juga ditandai sebagai dugaan domain pengikat
peptidoglikan. Domain katalitik (CAT) juga ditandai sebagai domain zinc-dependent metazincine (ZnMc), yang dikonservasi di antara metalloproteinase yang tergantung zink. Daerah engsel adalah domain
penghubung yang dicirikan oleh struktur kaya prolin. Domain PEX terbukti
merupakan domain pengikat DNA. Domain NES yang mengandung empat
leucine juga ada ditemukan (Eguchi, et al., 2008).
2.13 MMP-3 sebagai Petanda Penyakit AR dan Gangguan Pendengaran pada AR
Pada AR, MMP-1, MMP-3, MMP-9, dan MMP MT1 diproduksi secara
berlebihan. MMP ini disekresikan ke dalam sinovium dan menyerang
tulang rawan yang terendam dengan cairan sinovial. Konsentrasi MMP-3
dalam cairan sinovial reumatoid lebih tinggi daripada MMP lainnya dan
dalam beberapa studi terbukti bersifat memprediksi kehancuran sendi
(Carrasco & Barton, 2010).
MMP-3 merupakan proteinase yang disekresikan oleh fibroblas dan
kondrosit sinovial. Aktivitasnya menyebabkan degradasi protein inti
aggrecan, protein tulang rawan, fibronektin, serta kolagen tipe IV, VII, IX dan XI. MMP-3 ada dalam cairan sinovial AR dan diekspresikan secara
berlebihan. Polimorfisme MMP-3 berhubungan dengan kerusakan sendi
yang lebih parah pada AR. Dalam hal lainnya, konsentrasi MMP-3 serum
diajukan sebagai prediktor untuk kehancuran sendi pada AR dini atau AR
yang sudah lanjut. Konsentrasi MMP-3 yang bersirkulasi tampaknya telah
ditentukan secara genetik
Selama ini, diagnosis AR didasarkan pada manifestasi-manifestasi
klinik. Akan tetapi, sering sulit mendiagnosis AR pada fase yang sangat
dini dan dalam banyak kasus kerusakan yang ireversibel terjadi pada
waktu diagnosis ditegakkan. Karena itu, pemeriksaan laboratorium yang
sensitif dan spesifik di awal masa perjalanan penyakit diperlukan untuk
diagnosis dan intervensi lebih dini. Selama bertahun-tahun, telah diteliti
biomarker potensial untuk diagnosis dan prognosis AR dalam jumlah yang
sangat besar tetapi hanya test autoantibodi (RF) dan penanda inflamasi
(LED dan CRP) diperiksa sekarang ini secara rutin dalam praktek klinik
(Carrasco & Barton, 2010). Perihal gangguan pendengaran pada pasien
AR, pada penelitian yang dilakukan oleh Takatsu, et al., ditemukan bahwa
SNHL pada pasien AR tersebut berhubungan signifikan dengan LED
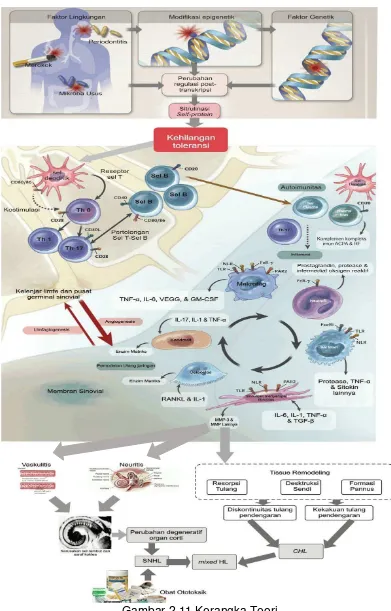
2.14 Kerangka Teori
Keterangan Gambar 2.11:
Reumatoid artritis melibatkan interaksi yang kompleks antara faktor genetik dan faktor lingkungan. Faktor genetik yang diidentifikasi meliputi
HLA-DRB1 dan HLA-DR4. Sedangkan faktor lingkungan meliputi merokok dan bentuk lain dari stres bronkus (misalnya, paparan silika), agen
penginfeksi (seperti virus Epstein–Barr, cytomegalovirus, proteus, dan
Escherichia coli), serta periodontitis (Porphyromonas gingivalis). Hilangnya toleransi terhadap neoepitopes tersebut memunculkan respon
ACPA (McInnes & Schett,
Sinovitis terjadi ketika leukosit memasuki kompartemen sinovial.
Migrasi leukosit diperantarai oleh aktivasi endotel di dalam pembululuh
darah mikro sinovial, yang meningkatkan ekspresi molekul adhesi
(termasuk integrin, selektin, dan anggota superfamili imunoglobulin) dan
kemokin. Termasuk didalamnya MMP-3 yang disekresikan ke dalam
sinovium dan menyerang tulang rawan yang terendam dengan cairan
sinovial. Konsentrasi MMP-3 dalam cairan sinovial reumatoid lebih tinggi
daripada MMP lainnya. Oleh karena itu, neoangiogenesis yang
disebabkan oleh kondisi hipoksia lokal dan sitokin, dan limfangiogenesis
yang tidak cukup (yang membatasi jalan keluar selular) merupakan
karakteristik synovitis (McInnes & Schett, 2011).
Perubahan lingkungan mikro ini berkombinasi dengan reorganisasi
arsitektur sinovial yang sangat buruk dan aktivasi fibroblas lokal. Ini
menyebabkan penumpukan jaringan inflamasi sinovial pada artritis
reumatoid (McInnes & Schett,
2011).
2011). Hal ini menyebabkan resorpsi tulang,
destruksi sendi, dan pembentukan pannus yang berlanjut dengan
diskontinuitas tulang pendengaran dan kekakuan tulang pendengaran. Ini
bermanifestasi sebagai CHL (Dikici, et al., 2009). Vaskulitis, neuritis, dan
ototoksisitas obat yang digunakan untuk pengobatan penyakit ini juga
dapat menyebabkan degenerasi organ corti yang bermanifestasi sebagai
SNHL. Jika kedua jenis gangguan pendengaran ini terjadi maka dapat
2.15 Kerangka Konsep
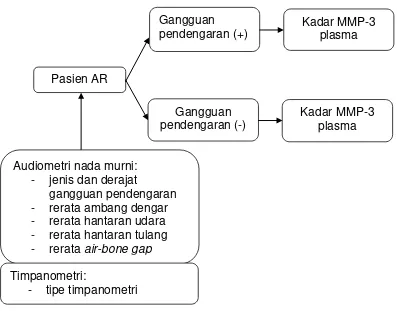
Gambar 2.12 Kerangka Konsep
Keterangan Gambar 2.12:
Dilakukan pemeriksaan audiometri nada murni pada pasien AR untuk
mengetahui jenis dan derajat gangguan pendengaran serta untuk
mengetahui rerata ambang hantaran udara, ambang hantaran tulang, air-bone gap dan ambang dengar. Dilakukan pula pemeriksaan timpanometri untuk mengetahui rerata compliance dan tekanan telinga tengah. Kemudian diteliti perbedaan kadar MMP-3 pada pasien AR dengan
gangguan pendengaran dan pasien AR tanpa gangguan pendengaran.
2.16 Hipotesis Penelitian
Hipotesis penelitian ini adalah: terdapat hubungan kadar MMP-3
dengan gangguan pendengaran pada pasien AR. Audiometri nada murni:
- jenis dan derajat
gangguan pendengaran - rerata ambang dengar - rerata hantaran udara - rerata hantaran tulang - rerata air-bone gap
Timpanometri:
- tipe timpanometri Pasien AR
Gangguan pendengaran (+)
Gangguan pendengaran (-)
Kadar MMP-3 plasma