BAB 2. TINJAUAN PUSTAKA
2.1. Infeksi parasit soil-transmitted helminth 2.1.1. Definisi
Infeksi STH banyak ditemukan pada masyarakat yang tinggal di negara
berkembang, terutama di daerah pedesaan. Soil-transmitted helminth (STH)
adalah golongan cacing usus (Nematoda Usus) yang dalam
perkembangannya membutuhkan tanah untuk menjadi bentuk infektif.1 Terdapat 3 jenis infeksi STH dengan habitat pada usus manusia yang paling
sering ditemukan, yaitu:12
1) Cacing gelang (roundworm/ A. lumbricoides)
2) Cacing cambuk (whipworm/ T. trichiura)
3) Cacing tambang (hookworm/ Necator americanus dan Ancylostoma
duodenale)
2.1.2. Epidemiologi
Berdasarkan laporan terakhir oleh de Silva et al. pada tahun 2003
diperkirakan infeksi A. lumbricoides sebesar 1,221 miliar, T. trichiura 795 juta,
dan cacing tambang 740 juta terjadi di seluruh dunia.1 Infeksi STH yang paling banyak terdapat di negara Cina dan Asia Timur, Sub-Sahara Afrika,
pada tahun 1987 sebesar 78,6%. Data prevalensi penyakit kecacingan di
Indonesia pada tahun 2002 sampai 2006 secara berurutan adalah sebesar
33,3%, 33,0%, 46,8%, 28,4%, dan 32,6%.13
Berdasarkan data UNICEF tahun 2002 dengan penggunaan GIS
didapatkan prevalensi tinggi kejadian infeksi STH di Indonesia terdapat di
wilayah Irian Jaya (50 sampai 79.9%) dan Sumatera Utara (57% sampai
100%) serta prevalensi rendah di wilayah Jawa Timur (0.1 sampai 19.9%).
Berdasarkan spesiesnya maka prevalensi di Sumatera Utara 50% sampai
79.9% untuk ascariasis, 80% sampai 100% untuk trichuriasis, dan 50%
sampai 79.9% untuk infeksi cacing tambang.5 Data terbaru mengenai prevalensi kecacingan di beberapa wilayah Sumatera Utara juga
menunjukkan prevalensi tinggi infeksi STH, dimana di Kelurahan Tembung
tahun 2007 sebesar 73%;14 Sibolga tahun 2008 dijumpai sebesar 55.8%;15 Samosir tahun 2008 sebesar 56.4%;16 bahkan pada tahun 2011 terjadi peningkatan di Kabupaten Deli Serdang sebesar 84.4%.17
Kejadian ascariasis dan trihuriasis terbesar ditemukan pada anak yang
berusia 5 sampai 15 tahun dan akan menurun pada usia dewasa. Sebaliknya
infeksi cacing tambang mulai meningkat pada usia 20 tahun dan terus
mengalami peningkatan pada usia dewasa.4
Infeksi STH lebih berakibat pada tingkat kesakitan (disability)
menggunakan disability-adjusted life years (DALY). Infeksi A. lumbricoides
dan T. trichiura masing-masing menyebabkan hilangnya DALY sebesar 10.5
juta dan 6.4 juta DALY setiap tahunnya.18
2.1.3. Faktor risiko
Baik faktor lingkungan maupun penjamu mempengaruhi berat
ringannya infeksi STH.4 Terdapat beberapa faktor risiko kejadian infeksi STH sebagai berikut:
a) Perilaku, rumah tangga, dan pekerjaan
Intensitas infeksi cacing tambang tertinggi ditemukan pada orang dewasa.
Pekerjaan yang berhubungan dengan pertanian merupakan denominator
infeksi cacing tambang.6
b) Kemiskinan, sanitasi, dan urbanisasi
Transmisi infeksi STH bergantung pada lingkungan yang telah tercemar
tinja dan mengandung telur. Akibatnya, infeksi STH sangat erat kaitannya
dengan kemiskinan, sanitasi yang buruk, dan kurangnya akses
penyediaan air bersih. Pencemaran tanah terutama oleh telur cacing A.
lumbricoides banyak terjadi di daerah pedesaan, pemukiman penduduk di
Penggunaan GIS dan remote sensing akhir-akhir ini dapat
mengidentifikasi batasan distribusi infeksi STH berdasarkan pola suhu
dan curah hujan.20 d) Etnis dan budaya
Ditemukan prevalensi infeksi A. lumbricoides yang tinggi pada suku Bantu
dibandingkan suku Baka (Pygmy) di Republik Afrika Tengah, sama seperti
pada suku Melayu atau suku India di Malaysia dibandingkan suku Cina. Di
India, Nawalinski et al. menemukan prevalensi tinggi infeksi cacing
tambang pada kalangan Muslim dibandingkan orang Hindu meskipun
kedua kalangan tersebut tinggal berdekatan dan memiliki pola perilaku
yang berhubungan dengan faktor risiko tidak jauh berbeda.21 e) Pola makan
Meskipun STH bukan merupakan infeksi yang ditularkan melalui
makanan, namun telur A. lumbricoides dan larva cacing tambang akan
melekat pada sayur-sayuran, dimana sayur-sayuran tersebut akan
disebarkan ke pasar tanpa proses seleksi terlebih dahulu. Suatu survei di
Jepang menemukan bahwa telur A. lumbricoides ditemukan pada 1 178
dari 2 750 item sayur-sayuran yang dijual di 40 toko di Tokyo.21 f) Genetik
Hingga saat ini belum diidentifikasi adanya gen yang dapat
mengenai genom akhir-akhir ini menemukan adanya kromosom 1 dan 13
sebagai pengendali infeksi A. lumbricoides.22
2.1.4. Gejala klinis
Gejala klinis infeksi STH dapat dibagi dalam manifestasi akut yang berkaitan
dengan migrasi larva melalui kulit dan visera, dan manifestasi akut serta
kronik sebagai akibat dari cacing dewasa masuk ke saluran gastrointestinal.
Manusia merupakan hospes definitif dari cacing tersebut. Di dalam tubuh,
infeksi STH akan mempengaruhi pemasukan, pencernaan, penyerapan, dan
metabolisme makanan.23
Manifestasi dari infeksi STH bervariasi dari gejala ringan sampai berat.
Gejala intestinal ringan yang timbul berupa nausea, muntah, diare, nyeri
perut, konstipasi, dan kehilangan nafsu makan. Sedangkan gejala yang lebih
berat antara lain obstruksi usus, malnutrisi, perdarahan kronis, anemia, serta
kolitis dengan tinja berlendir dan darah.23
2.1.4.1. Migrasi larva
Migrasi larva STH menimbulkan reaksi pada jaringan yang dilaluinya.
Misalnya, larva A. lumbricoides yang meninggal saat migrasi melalui hepar
dapat menimbulkan eosinophilic granuloma. Gangguan karena larva
perdarahan kecil pada dinding alveolus berakibat timbulnya gangguan pada
paru yang disertai dengan batuk, demam, dan eosinofilia. Pada foto toraks
tampak infiltrat yang menghilang dalam waktu 3 minggu. Keadaan ini disebut
sindrom Löffler. Pada keadaan tertentu cacing dewasa mengembara ke
saluran empedu dan pankreas, sehingga menyebabkan kolesistitis atau
pankreatitis. Gejala lain yang dapat ditimbulkan akibat migrasi larva A.
lumbricoides adalah gejala alergi seperti demam, urtikaria, dan penyakit
granulomatosa.23,24
2.1.4.2. Parasit di saluran gastrointestinal
Umumnya manifestasi klinis akibat infeksi STH di saluran gastrointestinal
terjadi bila intensitasnya sedang dan tinggi.
2.1.4.2.1. Ascariasis
Gejala yang timbul dapat disebabkan oleh cacing dewasa. Gangguan yang
disebabkan cacing dewasa biasanya ringan. Kadang-kadang penderita
mengalami gejala gangguan usus ringan seperti mual, nafsu makan
berkurang, diare atau konstipasi. Pada infeksi berat, terutama pada anak
dapat terjadi malabsorbsi sehingga memperberat keadaan malnutrisi. Efek
yang serius terjadi bila cacing ini menggumpal dalam usus sehingga terjadi
distensi abdomen, dan rasa kram pada perut. Bahkan jika cacing bermigrasi
ke dinding usus maka akan bermanifestasi sebagai peritonitis.23,24
2.1.4.2.2. Trichuriasis
Cacing T. trichiura pada manusia terutama hidup di sekum, akan tetapi dapat
juga ditemukan di kolon asendens. Pada infeksi berat, terutama pada anak,
cacing ini tersebar di seluruh kolon dan rektum. Kadang-kadang terlihat di
mukosa rektum yang mengalami prolapsus akibat penderita mengejan saat
defekasi. Cacing ini memasukkan kepalanya ke dalam mukosa usus, hingga
terjadi trauma yang menimbulkan iritasi dan peradangan mukosa usus. Pada
tempat perlekatannya dapat terjadi perdarahan. Di samping itu cacing ini
menghisap darah hospesnya, sehingga dapat menyebabkan anemia. Cacing
dewasa T. trichiura diperkirakan menghisap darah sekitar 0.005 mL darah/
cacing/ hari. Infeksi ringan biasanya tidak memberikan gejala klinis yang jelas
atau sama sekali tanpa gejala. Terkadang penderita memiliki riwayat rasa
nyeri tersamar yang dirasakan pada regio abdomen kuadran kanan bawah.
Penderita terutama anak-anak dengan infeksi T. trichiura yang berat dan
menahun, menunjukkan gejala-gejala seperti diare yang sering disertai
dengan sindrom disentri, anemia, berat badan turun, dan kadang-kadang
disertai prolapsus rektum. Infeksi kronis dapat menyebabkan terhambatnya
Infeksi berat T. trichiura sering disertai dengan infeksi cacing lainnya atau
protozoa.23,25
2.1.5. Diagnosis
Diagnosis ditegakkan dengan menemukan telur atau cacing dewasa dalam
tinja segar. Metode yang direkomendasikan adalah pemeriksaan sampel tinja
dengan teknik hapusan tebal kuantitatif Kato-Katz dan McMaster. Metode ini
dapat mengukur intensitas infeksi dengan memperkirakan jumlah telur per
gram tinja (egg per gram feces/ epg).26-28
2.1.6. Pengobatan
Terdapat 4 intervensi utama dalam pengobatan infeksi STH mencakup:
1. Pemberian obat antihelmintik
Pemberian obat antihelmintik (deworming) bertujuan untuk mengurangi
morbiditas dengan mengurangi angka kesakitan akibat infeksi STH.
Pemberian obat antihelmintik secara periodik terhadap kelompok yang
berisiko tinggi dapat menurunkan angka kesakitan dan memperbaiki
kesehatan serta pertumbuhan anak. Selain itu untuk ascariasis dan
dikurangi kejadian transmisinya dari waktu ke waktu. Obat yang
direkomendasikan untuk kontrol infeksi STH adalah benzimidazole
antihelmintik (BZAs), albendazole (dosis tunggal: 400 mg, kecuali dosis
200 mg untuk anak usia 12-24 bulan), mebendazole (dosis tunggal: 500
mg), levamisole, atau pirantel pamoat.18,29,30 2. Perbaikan sanitasi
Bertujuan untuk mengendalikan transmisi dengan mengurangi
kontaminasi pada tanah dan air. Hal ini merupakan intervensi utama untuk
mengurangi angka kejadian infeksi STH, namun strategi ini hanya efektif
jika dapat menjangkau populasi yang luas. Jangkauan populasi yang luas
ini yang menjadi kendala karena membutuhkan biaya yang besar. Lebih
lanjut lagi, intervensi tersebut membutuhkan waktu bertahun-tahun
bahkan hingga puluhan tahun agar dapat menjadi efektif.6,31 3. Edukasi kesehatan
Bertujuan untuk mengurangi kejadian transmisi dan reinfeksi dengan
mempromosikan perilaku sehat. Cara sederhana dengan mengajarkan
penggunaan jamban dan perilaku bersih. Tanpa adanya perubahan
kebiasaan buang air besar, pemberian obat antihelmintik secara periodik
diketahui tidak dapat mengurangi transmisi infeksi STH. Edukasi
kesehatan merupakan cara yang sederhana namun dapat menurunkan
4. Cara pengendalian baru
Tingginya kejadian reinfeksi setelah pemberian terapi antihelmintik pada
daerah endemis tinggi serta berkurangnya efikasi pengobatan
antihelmintik secara periodik diperkirakan karena adanya resistensi
terhadap obat-obat antihelmintik tersebut. Penelitian terbaru sedang
mengembangkan cara baru untuk mengendalikan infeksi STH melalui
program pengembangan vaksin untuk infeksi cacing tambang yang
mengandung antigen larva Ancylostoma–secreted protein (ASP) 2. Vaksin
ini terbukti efektif dalam pencegahan pada model hewan. Hal ini
diharapkan dapat memutuskan penyebaran infeksi STH. Akan tetapi
vaksin tersebut masih dalam proses pengembangan agar dapat
digunakan pada manusia.4,29
2.2. Eosinofil
2.2.1. Fungsi eosinofil
Eosinofil merupakan leukosit yang berasal dari sumsum tulang dimana
perkembangan dan diferensiasi akhirnya berada dibawah kontrol beberapa
sitokin seperti interleukin 3 (IL-3), granulocyte-macrophage colony-
stimulating factor (GM-CSF), dan interleukin 5 (IL-5). Granulocyte
macrophage-colony stimulating factor (GM-CSF) dan IL-3 menstimulasi
berperan lebih spesifik pada eosinofil dimana bertanggung jawab dalam
eosinofilopoiesis.7,32
Eosinofil memiliki diameter 8 µm dengan nukleus yang biasanya
bilobus, terkadang bisa memiliki 3 atau lebih lobus. Ciri khas eosinofil adalah
memiliki granul kristaloid yang besar, biasanya disebut granul spesifik atau
sekunder. Granul kristaloid dikelilingi oleh membran dan mengandung protein
dasar yang sangat kationik, dengan berat polipeptida 18 000 sampai 21 000
dalton. Protein dasar kationik tersebut diketahui memiliki aktivitas bakterisidal
dan helmintotoksik. Selain itu eosinofil memiliki 4 tipe granul lainnya yaitu
granul primer, granul kecil, badan lemak, dan vesikel sekretori kecil.32,33
Eosinofil membahayakan karena efek proinflamasi, namun dapat
menguntungkan karena efek antiparasitik.34 Meskipun salah satu fungsi eosinofil adalah untuk memfagosit dan membunuh bakteri, namun eosinofil
tidak dapat menghilangkan infeksi bakteri tanpa adanya bantuan neutrofil.32 Hipotesis mengenai fungsi utama eosinofil untuk melindungi pejamu dari
infeksi organisme seperti STH berdasarkan beberapa penemuan sebagai
berikut:35
a) Eosinofil berdegranulasi dan dapat membunuh cacing secara in vitro
dengan adanya antibodi dan/atau komplemen
c) Sejumlah besar eosinofil seringkali terlihat berhubungan erat dengan
cacing yang masih utuh bahkan telah mati secara in vivo
d) Eosinofil secara jelas berdegranulasi di sekitar atau pada permukaan
cacing secara in vivo
Disamping berfungsi sebagai efektor perifer, eosinofil juga mengatur
respon imun dengan meningkatkan pelepasan sitokin dan kemokin. Eosinofil
berperan dalam beragam reseptor permukaan sel untuk memberi sinyal pada
sel sehubungan dengan proses kemotaksis, adhesi, respiratory burst,
degranulasi, produksi sitokin dan kemokin, apoptosis maupun bertahan
hidup, dimana semuanya berhubungan dengan eosinophil-mediated tissue
inflammatory responses ketika terjadi infeksi cacing.36
2.2.2. Kondisi yang berhubungan dengan peningkatan nilai eosinofil
Istilah eosinofilia (dahulu dikenal dengan istilah granulosit eosinofilik) adalah
peningkatan eosinofil > 450 eosinofil/µl yang diukur dari darah perifer.33 Peningkatan nilai eosinofil dalam darah perifer dapat muncul pada beragam
penyakit (lihat Tabel 2.1.), maka untuk menegakkan penyebab dibutuhkan
anamnesis yang lengkap. Penyebab peningkatan nilai eosinofil yang paling
obat myelosupresif, interferon alfa, antihistamin, kromolin, siklosporin,
inhibitor dan antagonis leukotrien, serta inhibitor fosfodiesterase.34
Nilai eosinofil dapat diketahui dengan melakukan pemeriksaan apusan
darah tepi dan pemeriksaan darah vena di laboratorium.8 Nilai eosinofil mengikuti variasi diurnal dengan nilai terendah pada jam 10 pagi hingga
siang hari dan mencapai 2 kali dari nilai terendah antara tengah malam
hingga pukul 4 subuh.7,37
Kejadian eosinofilia merupakan kelainan darah yang umum terjadi di
daerah tropis. Prevalensi kejadian eosinofilia di Kisaran sebesar 7.7%
dibandingkan dengan negara di Eropa 2.8%. Prevalensi yang tinggi juga
ditemukan di India (W. Bengal) sebesar 26.7% dibandingkan dengan negara
di Eropa sebesar 2.1%. Diperkirakan bahwa kejadian eosinofilia pada
masyarakat pedesaan tersebut berhubungan dengan tingginya insidensi
Tabel 2.1. Beberapa keadaan penyebab eosinofilia8 Alergi
Rinitis alergi Asma
Urtikaria akut dan kronik
Pemphigoid
Reaksi hipersensitivitas obat Infeksi
Infeksi cacing yang berinvasi ke jaringan Trichinosis
Penyakit Hodgkin dan limfoma sel T Leukemia myelogenik akut Graft vs host reaction Omenn syndrome
Trombocytopenia with absent radii
Vaskulitis
Post-iradiasi abdomen
2.3. Hubungan antara nilai eosinofil dan infeksi soil-transmitted helminth
Pada awal tahun 1939, eosinofil dianggap berperan sebagai respon imun
pada infeksi cacing. Kejadian eosinofilia pada infeksi selain sebagai reaksi
patologi juga merupakan reaksi imunitas protektif.38 Banyak ilmuwan menganggap bahwa fungsi utama eosinofil adalah perlindungan terhadap
parasit, meskipun hanya sedikit bukti studi in vivo yang membuktikan hal
tersebut. Eosinofil juga muncul dalam jumlah besar pada mamalia jika terjadi
lesi inflamasi terkait dengan infeksi cacing atau kondisi alergi.39
Eosinofil timbul dalam sumsum tulang dari sel prekursor
haematopoietik CD34. Pada tahap awal diferensiasi, eosinofil dikendalikan
oleh sitokin GM-CSF dan IL-3, yang juga mengendalikan perkembangan
granulosit lain seperti neutrofil, basofil, dan sel mast. Tahap selanjutnya dari
diferensiasi dan pematangan, sebagian besar eosinofil dikendalikan oleh
sitokin IL-5, yang diproduksi oleh sel T aktif dan sel mast.39,40 Respon T-helper 2 (Th2) jelas terlibat dalam infeksi STH, dimana memberikan
kemungkinan adanya kelangsungan hidup pada penderita infeksi STH
sekaligus melindungi terhadap superinfeksi.41,42
Pada individu yang normal, eosinofil ditemukan dalam jaringan,
terutama yang berinteraksi dengan dunia luar, seperti di kulit, permukaan
Eosinofil merupakan sel yang berdiferensiasi akhir setelah meninggalkan
sumsum tulang dengan umur paruh waktu sekitar 18 jam.32
Masa hidup eosinofil pada jaringan normal tidak diketahui pasti,
namun diperkirakan dapat bertahan selama beberapa hari bahkan minggu.
Eosinofil hanya bertahan hidup beberapa jam dalam sirkulasi darah. Pada
infeksi STH, eosinofil dikeluarkan lebih cepat dari sumsum tulang dengan
terstimulasi kurang lebih dalam 1 jam. Kelangsungan hidup eosinofil dalam
jaringan juga meningkat dan laju eosinofilopoiesis dalam sumsum tulang
meningkat secara dramatis.32,43-45 Diketahui bahwa IL-3, IL-5, dan GM-CSF dapat menghambat proses apoptosis eosinofil selama kurang lebih 12
sampai 14 hari secara in vitro dan pada penderita sinusitis. Sebaliknya tanpa
adanya sitokin tersebut, eosinofil hanya dapat bertahan kurang dari 48 jam.34 Eosinofil sangat cepat mengalami pergantian pada lesi inflamasi
dimana hanya bertahan hidup 4 sampai 5 hari.39 Diketahui bahwa apoptosis pada eosinofil yang dipicu oleh helminth-derived excretory-secretory products
(ESP) dapat menyebabkan inflamasi jaringan berat yang turut berperan
dalam melawan infeksi kecacingan.46
Studi di Jepang membuktikan adanya hubungan signifikan ascariasis
dengan derajat eosinofilia.47 Namun tidak terdapat perubahan signifikan nilai eosinofilia pada trichuriasis, bahkan jika terjadi migrasi cacing ke mukosa
cacing tambang, T. trichiura, dan koinfeksi adalah 10%, 15.1%, 13%, dan
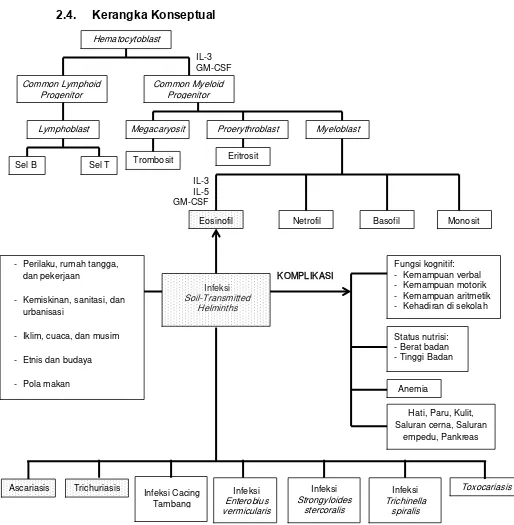
2.4. Kerangka Konseptual
Keterangan: yang diamati dalam penelitian
Gambar 2.1. Kerangka konseptual Lymphoblast
- Kemiskinan, sanitasi, dan urbanisasi - Kemampuan verbal - Kemampuan motorik - Kemampuan aritmetik - Kehadiran di sekolah