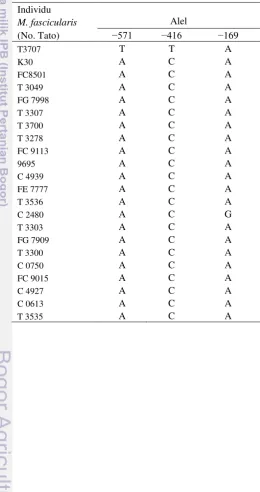
DASAR GENETIK SIFAT HIPER- DAN HIPO-RESPONS
MONYET EKOR PANJANG (
Macaca fascicularis)
TERHADAP DIET ATEROGENIK
ACHMAD TAHER
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI DISERTASI DAN
SUMBER INFORMASI SERTA PELIMPAHAN HAK CIPTA
Dengan ini saya menyatakan bahwa disertasi berjudul Dasar Genetik Sifat Hiper- dan Hipo-respons Monyet Ekor Panjang (Macaca fascicularis) terhadap Diet Aterogenik adalah benar karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apapun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir disertasi ini.
Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor.
Bogor, Juli 2016
RINGKASAN
ACHMAD TAHER. Dasar Genetik Sifat Hiper- dan Hipo-respons Monyet Ekor Panjang (Macaca fascicularis) terhadap Diet Aterogenik. Dibimbing oleh DEDY DURYADI SOLIHIN, SULISTIYANI, DONDIN SAJUTHI, dan DEWI APRI ASTUTI
Monyet ekor panjang (Macaca fascicularis) merupakan satu dari spesies satwa primata yang paling umum digunakan sebagai model dalam penelitian biomedis. Sensitivitas spesies ini terhadap lemak jenuh dan kolesterol diet menjadikannya sebagai model dalam mempelajari pengaruh diet terhadap profil lipid plasma dan etiologi penyakit aterosklerosis pada manusia. Walaupun secara umum bersifat sensitif (hiper-responder), namun terdapat pula individu monyet ekor panjang yang kurang atau tidak sensitif terhadap perubahan diet (hipo-responder). Selama ini seleksi monyet ekor panjang hipo- dari hiper-responder dilakukan dengan intervensi diet aterogenik selama 2 bulan. Cara ini tidak efisien karena membutuhkan volume darah hewan dalam jumlah banyak dan pengontrolan yang ketat terhadap diet. Penelitian ini dilakukan untuk mencari metode yang mampu mengidentifikasi secara cepat monyet ekor panjang hipo- dari hiper-responder sehingga seleksi hewan menjadi lebih efisien. Pendekatan yang digunakan adalah penanda genetik.
Penelitian ini menggunakan 22 ekor monyet ekor panjang hasil penangkaran di Pusat Studi Satwa Primata Institut Petanian Bogor (PSSP IPB) dan terdiri dari tiga tahapan, meliputi (1) Intervensi diet menggunakan diet aterogenik IPB-1 yang berbahan baku lokal dan analisis variasi respons kadar kolesterol plasma. Tahap ini bertujuan menyeleksi sensitivitas hewan berdasarkan status kolesterol plasma. (2) Identifikasi variasi genetik umum, berupa polimorfisme nukleotida tunggal (single nucleotide polymorphism, SNP) pada gen reseptor liporotein densitas rendah (low density lipoprotein receptor, LDLR). Tahap ini bertujuan mengelompokkan hewan berdasarkan polimorfisme umum. (3) Analisis ekspresi gen LDLR dalam sel darah tepi berinti tunggal (peripheral blood mononuclear cell, PBMC) dan membuat pustaka cDNA individu hipo-responder. Tahap ini bertujuan menjelaskan mekanisme molekuler yang mendasari keterkaitan antara variasi genetik dan variasi respons.
panjang ekstrem. Selain itu alel T pada posisi −416 dalam promotor adalah penanda genetik bagi monyet ekor panjang hipo-responder ekstrem dan alel C pada posisi *167 dalam 3’UTR adalah penanda genetik bagi monyet ekor panjang sangat ekstrem. Kelimpahan mRNA individu hipo-responder ekstrem yang lebih tinggi dan individu sangat ekstrem yang lebih rendah dibandingkan individu lain menunjukkan bagaimana mekanisme yang mendasari keterkaitan antara polimorfisme dan sensitivitas hewan. Penggunaan penanda genetik merupakan terobosan baru karena membuat seleksi hewan hipo- dan hiper-responder menjadi lebih cepat dan efisien.
SUMMARY
ACHMAD TAHER. Genetic Basis of the Hyper- and Hypo-Response of Long Tail Macaques (Macaca fascicularis) to the Atherogenic Diet. Supervised by DEDY DURYADI SOLIHIN, SULISTIYANI, DONDIN SAJUTHI and DEWI APRI ASTUTI
Long tail macaques or cynomolgus macaques (Macaca fascicularis) are one of the primate species, which are commonly used as models in biomedical researches. The sensitivity of this species to saturated lipids and cholesterol diets leads them to be as models in investigating the effect of diet to plasma lipids and the etiology of the atherosclerosis diseases in human. Generally, even though this species is sensitive (hyper-responder) to diet changes but some individuals may show less sensitive and even insensitive to the diet changes (Hypo-responder). The selections of the hypo-responder macaques from the hyper-responder ones are commonly performed by intervention the atherogenic diet within 2 months. This method is inefficient because it involves a large number of bloods and strict controls of the diet. This research was conducted to find a method that can identify promptly hypo- from the hyper-responder macaques so that selecting animal became more efficient. The approach used was a genetic markers.
The research used 22 long tail macaques from captivity in the Primate Research Center Bogor Agricultural University (PSSP IPB) and comprised three stages. The first stage was diet intervention using IPB-1 atherogenic diet which was local raw material contents, and response variation analysis of plasma cholesterol levels. This stage purposed to select animal sensitivity based on plasma cholesterol status. The second stage was identification of common genetic variation like single nucleotide polymorphism (SNP) on low density lipoprotein receptor gene (LDLR). This stage aimed to classify animals based on common polymorphism. The third stage was to analyze expression of LDLR gene in peripheral blood mononuclear cell (PBMC), and constructing of cDNA library of hypo-response individual. This stage aimed to explain molecular mechanisms underlying linkage between genetic variation and response variation.
hypo-responder and low abundance of the more extreme individual in compared to other individuals showed how mechanism underlying linkage between polymorphism and sensitivity of animal. The use of genetic markers is a new improvement method, which is quicker and more efficient, in the processes of selecting hypo- and hyper-responsive animals.
© Hak Cipta Milik IPB, Tahun 2016
Hak Cipta Dilindungi Undang-Undang
Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau menyebutkan sumbernya. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik, atau tinjauan suatu masalah; dan pengutipan tersebut tidak merugikan kepentingan IPB
DASAR GENETIK SIFAT HIPER- DAN HIPO-RESPONS
MONYET EKOR PANJANG (
Macaca fascicularis)
TERHADAP DIET ATEROGENIK
ACHMAD TAHER
Disertasi
sebagai salah satu syarat untuk memperoleh gelar Doktor
pada
Program Studi Primatologi
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
Penguji pada Ujian Tertutup : 1. Dr dr Irma Herawati Suparto, MS 2. Dr Ir R R Dyah Perwitasari, MSc
Judul Disertasi : Dasar Genetik Sifat Hiper- dan Hipo-respons Monyet Ekor Panjang (Macaca fascicularis) terhadap Diet Aterogenik
Nama : Achmad Taher
NIM : P063110011
Disetujui oleh
Komisi Pembimbing
Dr Ir Dedy Duryadi Solihin, DEA Ketua
Drh Sulistiyani, MSc, PhD Anggota
Prof drh Dondin Sajuthi, MT, PhD Anggota
Prof Dr Ir Dewi Apri Astuti, MS Anggota
Diketahui oleh
Ketua Program Studi Primatologi
Prof drh Dondin Sajuthi, MT, PhD
Dekan Sekolah Pascasarjana
Dr Ir Dahrul Syah, MScAgr
PRAKATA
Puji dan syukur penulis panjatkan kepada Allah subhanahu wa ta’ala atas segala karunia-Nya sehingga karya ilmiah ini berhasil diselesaikan. Tema yang dipilih dalam penelitian yang dilaksanakan sejak januari 2013 ini ialah genetik satwa primata dengan judul Dasar genetik sifat hiper- dan hipo-respons monyet ekor panjang (Macaca fascicularis) terhadap diet aterogenik. Penelitian ini merupakan bagian dari proyek penelitian pada Pusat Studi Satwa Primata IPB yang dibiayai oleh Direktorat Jenderal Pendidikan Tinggi (DIKTI) Kementrian Pendidikan dan Kebudayaan Republik Indonesia melalui dana Kerjasama Penelitian Internasional dan Publikasi Ilmiah atas nama Prof Dr Ir Dewi Apri Astuti MS dan dana BOPTN untuk Penelitian Unggulan Sesuai Mandat Pusat IPB atas nama Dr Ir Dedy Duryadi Solihin, DEA.
Terima kasih penulis ucapkan kepada Bapak Dr Ir Dedy Duryadi Solihin DEA selaku ketua komisi, Ibu drh Sulistiyani MSc PhD, Bapak Prof drh Dondin Sajuthi MT PhD, dan Ibu Prof Dr Ir Dewi Apri Astuti MS selaku anggota komisi yang telah banyak memberi saran. Penulis juga mengucapkan terima kasih kepada Ibu Dr dr Irma Herawati Suparto MS, Ibu Dr R R Dyah Perwitasari MSc, dan Bapak Prof Dr Ibnu Maryanto selaku penguji luar komisi pada ujian tertutup dan sidang promosi atas saran dan masukan yang diberikan. Tak lupa ucapan terima kasih penulis sampaikan kepada Bapak Dr drh Joko Pamungkas MSc, Ibu Dr drh Diah Iskandriati, dan Bapak Dr Uus Saepulloh, SSi Mbiomed, yang telah membantu selama penelitian. Ungkapan terima kasih juga disampaikan kepada ayah, ibu, serta seluruh keluarga, atas segala doa dan kasih sayangnya.
Semoga karya ilmiah ini bermanfaat.
Bogor, Juli 2016
DAFTAR ISI
DAFTAR TABEL ... xiv
DAFTAR GAMBAR ... xv
1 PENDAHULUAN ... 1
Latar Belakang ... 1
Perumusan Masalah ... 6
Tujuan Penelitian ... 7
Manfaat Penelitian ... 7
Hipotesis ... 7
Kebaharuan (Novelty) Penelitian... 7
Ruang Lingkup Penelitian ... 7
2 SELEKSI MONYET EKOR PANJANG (Macaca fascicularis) HIPER- DAN HIPO-RESPONDER BERDASARKAN STATUS KOLESTEROL PLASMA ... 10
Pendahuluan ... 10
Bahan dan Metode ... 11
Hasil dan Pembahasan... 13
Simpulan ... 19
3 VARIASI GENETIK PADA DAERAH PROMOTOR GEN LDLR DAN SIFAT RESPONS MONYET EKOR PANJANG (Macaca fascicularis) TERHADAP DIET ATEROGENIK ... 20
Pendahuluan ... 20
Bahan dan Metode ... 21
Hasil dan Pembahasan... 23
Simpulan ... 30
4 KERAGAMAN GENETIK DALAM 3’UTR GEN LDLR DAN SIFAT RESPONS MONYET EKOR PANJANG (Macaca fascicularis) TERHADAP DIET ATEROGENIK... 31
Pendahuluan ... 31
Bahan dan Metode ... 32
Hasil dan Pembahasan... 34
Simpulan ... 41
5 POLIMORFISME NUKLEOTIDA TUNGGAL PADA GEN LDLR DAN SIFAT RESPONS MONYET EKOR PANJANG (Macaca fascicularis) TERHADAP DIET ATEROGENIK ... 42
Pendahuluan ... 42
Bahan dan Metode ... 43
Hasil dan Pembahasan... 45
6 EKSPRESI GEN LDLR PADA MONYET EKOR PANJANG
YANG DIINDUKSI DIET ATEROGENIK ... 55
Pendahuluan ... 55
Bahan dan Metode ... 56
Hasil dan Pembahasan... 59
Simpulan ... 61
7 PEMBAHASAN UMUM ... 62
8 SIMPULAN DAN SARAN ... 69
DAFTAR PUSTAKA ... 70
DAFTAR TABEL
1 Komposisi diet aterogenik IPB-1 12
2 Bobot badan bulanan individual monyet ekor panjang 14 3 Rerata konsumsi diet bulanan individual monyet ekor panjang 15 4 Konsentrasi kolesterol plasma (TPC) bulanan individual
monyet ekor panjang 16
5 Konsumsi bahan kering, peningkatan bobot badan, dan konsentrasi kolesterol plasma monyet ekor panjang setelah tiga bulan intervensi diet aterogenik serta sifat responsnya berdasarkan status kolesterol
plasma ... 18
6 Komposisi nukleotida sekuen promotor ... 24
7 Matriks jumlah perbedaan nukleotida antar pasangan sekuen ... 25
8 Uji homogenitas pola substitusi antar pasangan sekuen ... 26
9 SNP dalam daerah promotor gen LDLR ... 27
10 Polimorfisme fungsional putatif yang ditemukan dalam daerah promotor gen LDLR ... 28
11 Haplotipe yang dihasilkan dari 3 situs polimorfik pada daerah Promotor dan disejajarkan dengan referensi (ref) monyet ekor Panjang di GenBank (nomor aksesi XM_005587996.2) ... 28
12 Komposisi nukleotida pada 3’UTR ... 35
13 Matriks jumlah perbedaan nukleotida antar pasangan sekuen ... 37
14 Uji homogenitas pola substitusi antar pasangan sekuen ... 38
15 Haplotipe yang dihasilkan dari 4 situs polimorfik pada daerah 3’UTR dan disejajarkan dengan referensi (ref) monyet ekor panjang di GenBank (nomor aksesi XM005587996.2) ... 39
16 Pasangan primer yang digunakan untuk mengamplifikasi daerah target dalam gen LDLR ... 45
17 Matriks jumlah perbedaan nukleotida antar pasangan sekuen ... 47
18 Uji homogenitas pola substitusi antar pasangan sekuen ... 48
19 Situs polimorfik yang diidentifikasi pada daerah intron 5 gen LDLR dan haplotipe yang dihasilkan, dan disejajarkan dengan referensi (ref) monyet rhesus di GenBank (nomor aksesi AY466854) ... 49
20 Situs polimorfik yang diidentifikasi pada daerah ekson 6 gen LDLR dan haplotipe yang dihasilkan, dan disejajarkan dengan referensi (ref) monyet ekor panjang di GenBank (nomor aksesi XM005587996.2) ... 51
21 Variasi genetik berupa SNP dalam ekson 12 ... 53
22 Monyet ekor panjang yang digunakan dalam penelitian, konsentrasi kolesterol plasma dan sifat responsnya terhadap diet aterogenik . 56 23 Primer yang digunakan untuk amplifikasi cDNA gen LDLR (http://primer3.wi.mit.edu/) 58 24 Tingkat ekspresi relatif gen LDLR ... 59
25 Polimorfisme nukleotida tunggal (SNP) pada gen LDLR ... 64
DAFTAR GAMBAR
1 Elemen pengatur transkripsi gen LDLR adalah yang terletak dalam 177 pb upstream dari kodon inisiasi (ATG), terutama dua boks TATA dan tiga pengulangan. R1 dan R3 mengikat Sp1 yang mengatur tingkat transkripsi basal, sedangkan R2 mengikat SREBP yang menjalankan pengaturan transkripsi termediasi kolesterol 2
2 3’UTR gen LDLR manusia. Kotak putih ekson 18 dengan
kodon stop diikuti sekuen ARE dan kaya Alu. Letak tiga sekuen ARE ditunjukkan oleh anak panah. Kotak hitam menunjukkan sekuen
Aludalam 2,5 kb 3’UTR 3
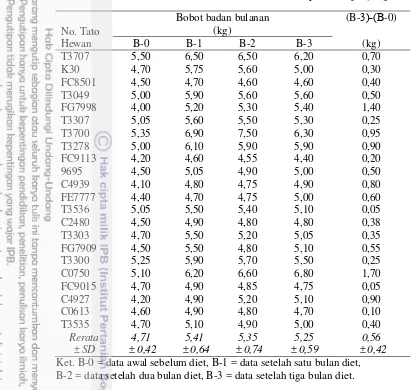
3 Struktur LDL-R manusia. Bagian kanan adalah ekson yan
Mengkode protein dan bagian kiri adalah domain protein matang 4 4 Bagan kerangka pikir penelitian... 9 5 Pita DNA berukuran 789 pb hasil amplifikasi PCR. 1 kb adalah
Marker DNA yang dgunakan, angka 1-6 adalah perwakilan
sampel hewan ... 23 6 Rekonstruksi pohon filogenetik monyet ekor panjang
berdasarkan sekuen daerah promotor yang dibuat dengan
metode Neighbor Joining dengan bootstrop 1000 kali ... 29 7 Pita DNA berukuran 750 pb hasil amplifikasi PCR. 1 kb adalah
marker DNA yang digunakan, angka 7-14 adalah perwakilan
sampel hewan 34
8 Rekonstruksi pohon filogenetik berdasarkan sekuen 3’UTR yang dibuat dengan metode Neighbor Joining dengan bootstrop
1000 kali. Angka yang terdapat pada cabang pohon
menunjukkan nilai bootstrop ... 40 9 Pita DNA berukuran 1010 pb hasil amplifikasi PCR 46 10 Rekonstruksi pohon filogenetik monyet ekor panjang
berdasarkan sekuen intron 5 yang dibuat dengan metode
Neighbor Joining dengan bootstrop 1000 kali. Angka yang
terdapat pada cabang menunjukkan nilai bootstrop 50 11 Pita DNA berukuran 184 pb hasil amplifikasi PCR
Keterangan: M=marker DNA 100 pb 51 12 Hasil elektroforesis SDS-PAGE terhadap RLFP yang menggunakan
enzim restriksi Tsp45I pada produk hasil amplifikasi. Sampel hipo-responder (T3707 dan K30) memiliki 3 pita, sedangkan
sampel lain 4 pita 51
13 Elektroferogram dari tiga pola haplotipe 51 14 Pita-pita DNA hasil amplifikasi PCR dengan pasangan primer
cDNA_1 (A), pasangan primer cDNA_2 (B), dan pasangan primer cDNA-3 dan cDNA_4 (C). Amplifikasi PCR dengan pasangan primer tersebut berturut-turut menghasilkan pita DNA berukuran
745,757, 621, dan 624 bp. Keterangan: M= Marker DNA 1 kb 60 15 Seleksi awal untuk memisahkan hewan hiper-responder dari
hipo-responder dan ekstrem berdasarkan SNP pada ekson 6 66 16 Seleksi lanjut untuk mendapatkan hewan murni hipo-respons dan
1
1 PENDAHULUAN
Latar Belakang
Monyet ekor panjang (Macaca fascicularis) memiliki sejarah panjang sebagai model satwa primata untuk mengkaji aterosklerosis pada manusia karena bersifat respons terhadap induksi lemak dan kolesterol diet. Spesies ini mengalami peningkatan kolesterol bila diberi diet tinggi lemak dan kolesterol dan sejalan dengan peningkatan kolesterol plasma dalam waktu lama mengalami aterosklerosis yang mirip dengan yang diamati pada manusia. Mulai dari lesi retensi makrofag kaya lipid (sel busa) dan sel-sel kekebalan lainnya di subendotelium, kemunculan garis-garis lemak di aorta dan arteri koroner, perkembangan dari garis-garis lemak menjadi ateroma berserat rumit dengan proliferasi sel-sel otot polos, hingga perkembangan menjadi lesi lebih kompleks yang ditandai dengan nekrosis intima, kalsifikasi, dan perdarahan. Selain itu, monyet ekor panjang yang diberi makan diet eksperimental juga menunjukkan perkembangan yang sesuai dengan tahapan penyakit secara klinik, termasuk iskemia dengan stenosis arteri koroner dan kematian mendadak yang dihasilkan dari trombosis oklusif dan infark miokard (Shelton et al. 2012).
Dalam kajian diet, peningkatan kolesterol plasma akibat intervensi diet aterogenik hanya dapat diprediksi pada tingkat populasi, tetapi tidak pada individual. Walaupun secara umum monyet ekor panjang bersifat hiper-respons (hiper-responder) dan rentan terhadap hiperkolesterolemia namun ada pula hewan dengan sifat hipo-respons (hipo-responder) yang kurang atau tidak rentan terhadap hiperkolesterolemia. Konsep sifat respons merujuk pada perbedaan yang besar dalam kadar kolesterol plasma yang ditemukan diantara individu yang diberi diet serupa, terutama diet yang mengandung lemak jenuh dan kolesterol dalam jumlah besar. Fenomena sifat respons menunjukkan perbedaan sensitivitas individual terhadap kolesterol diet dan merupakan sifat alamiah monyet ekor panjang karena kekonsistenannya dalam setiap pengulangan eksperimen. Secara teori 10% individu dalam populasi hipo-responder, 80% hiper-responder dan 10% sisanya adalah individu ekstrem (Beynen et al. 1987). Individu hiper-responder menunjukkan perkembangan aterosklerosis yang nyata, sementara individu hipo-responder tidak (Clarkson et al. 1988). Secara alami sulit untuk membedakan individu monyet ekor panjang hipo- dari hiper-responder karena fluktuasi diet di alam yang berpengaruh pada konsentrasi kolesterol plasma. Selama ini seleksi monyet ekor panjang hipo- dari hiper-responder dilakukan dengan intervensi diet aterogenik selama 2 bulan dan sensitivitas hewan ditentukan berdasarkan status kolesterol plasma setelah masa intervensi. Cara ini membutuhkan darah hewan dalam jumlah banyak dan berulang setiap interval waktu tertentu serta pengontrolan yang ketat terhadap diet (Clarkson et al. 1988; Turley et al. 1997).
2
Kandidat gen yang potensial menyebabkan variasi respons terhadap diet asam lemak jenuh dan tinggi kolesterol antara lain: klaster gen apolipoprotein A-I, C-III dan A-IV, gen apolipoprotein B, gen apolipoprotein E, gen pengkode enzim-enzim yang terlibat dalam metabolisme kolesterol (lipoprotein lipase, hepatik lipase, dan kolesterol 7α -hidroksilase), dan gen reseptor lipoprotein densitas rendah (low density
lipoprotein receptor, LDLR) serta gen-gen lain seperti gen protein transfer
ester kolesterol (cholesterol ester transfer protein, CETP), gen protein pengikat asam lemak usus (intestinal fatty acid-binding protein, FABP2) dan gen neuropeptida (Masson et al. 2003).
Hiperkolesterolemia turunan (familial hypercholesterolemia, FH) merupakan salah satu contoh keadaan hiperkolesterolemia akibat mutasi pada gen LDLR yang secara nyata menyebabkan tingginya kadar kolesterol LDL (LDL-C) plasma dan penyakit jantung koroner (PJK) dini (Hobbs et al. 1990). Gen LDLR manusia, terletak pada kromosom 19p13.2, terdiri dari 18 ekson dan 17 intron yang membentang sepanjang 45 kilo basa (kb) dan
3’-untranslated region (3‟UTR). 3‟UTR meliputi hampir setengah dari
keseluruhan mRNA. Dua daerah yang diketahui mengatur transkripsi gen
LDLR adalah daerah promotor dan downstream gen (Gambar 1). Elemen pengatur transkripsi pada daerah promotor terletak berkelompok dalam 280 pasang basa (pb) pada daerah upstream dari kodon awal. Elemen ini terdiri atas dua boks TATA (TATA box) sebagai sisi awal transkripsi dan tiga pengulangan tidak sempurna 16 pb kaya GC (Sudhof et al. 1987). Pengulangan 1 (repeat 1, R1) dan pengulangan 3 (repeat 3, R3) memiliki sisi pengikatan untuk faktor transkripsi specificity protein 1 (Sp1) dan bertanggung jawab terhadap tingkat transkripsi basal, sementara pengulangan 2 (repeat 2, R2) memiliki sisi elemen pengatur sterol-1 (sterol
regulatory element SRE-1) tempat protein pengatur sterol berikatan
sehingga meningkatkan transkripsi (Briggs et al. 1993).
Gambar 1 Elemen pengatur transkripsi gen LDLR adalah yang terletak dalam 288 pb upstream dari kodon inisiasi (ATG), terutama dua boks TATA dan tiga pengulangan. R1 dan R3 mengikat Sp1 yang mengatur tingkat transkripsi basal, sedangkan R2 mengikat SREBP yang menjalankan pengaturan transkripsi termediasi kolesterol
Transkripsi gen LDLR diatur oleh kadar kolesterol intraseluler (Smith
et al. 1990). Apabila kadar kolesterol intraseluler rendah, transkripsi
diinternalisasi semakin banyak. Sebaliknya, apabila kadar kolesterol dalam sel tinggi, transkripsi menurun sehingga pengambilan LDL-C ditekan (Dawson et al. 1988). Pengaturan ini bergantung pada protein pengikat elemen pengatur steroid (sterol regulatory element binding protein, SREBP) yang berikatan pada SRE-1 dalam R2 (Brigg et al. 1993). Penempatan SREBP inti diatur oleh protein lain yang disebut protein pengaktivasi pemecah protein pengikat elemen pengatur steroid (SREBP
cleavage-activating protein, SCAP). SCAP mempunyai domain peka sterol (sterol
sensong domain, SSD) sehingga apabila kandungan sterol intraseluler
rendah, SCAP mengaktifkan protease sisi-1 (site-1 protease, SIP) yang memecah SREBP pada sisi pertama. Produk pecahan selanjutnya dipecah oleh protease sisi-2, sehingga daerah domain-N aktif dari SREBP berpindah ke inti untuk menginisiasi transkripsi (Hua et al. 1993; Wang et al. 1994). Apabila kolesterol intraseluler tinggi, SCAP menginaktifkan SIP sehingga menghambat pemecahan domain terminal-N (Dawson et al. 1988).
Daerah downstream utama yang merupakan pengatur gen LDLR
adalah 3‟UTR. Sekuen 3‟UTR telah lama dikenal sebagai daerah pengatur penting ekspresi gen melalui stabilisasi mRNA-nya (Conne et al. 2000; Chen et al. 2006). Beberapa kajian menunjukkan bahwa 3‟UTR dari gen
LDLR merupakan sisi penting dari regulasi pascatranskripsi (Goto et al.
1997; Wilson et al. 1997). Daerah ini mengandung elemen-cis yang mempengaruhi stabilitas transkripsi, dan/atau mempengaruhi translasi melalui interaksi dengan runutan 5‟ dari transkrip, misalnya untaian elemen kaya AU (AU-rich element, ARE) yang mengandung motif penta-nukleotida AUUUA dan berfungsi sebagai sisi pengenal bagi protein spesifik yang meningkatkan laju pemendekan ekor poli A dan degradasi mRNA. 3‟UTR gen LDLR manusia mengandung tiga segmen yang masing-masing mengandung ARE. Selain itu daerah ini juga mengandung banyak sekuen
Alu (Gambar 2).
Gambar 2 3‟UTR gen LDLR manusia. Kotak putih ekson 18 dengan kodon stop diikuti sekuen ARE dan kaya Alu. Letak tiga sekuen ARE ditunjukkan oleh anak panah. Kotak hitam menunjukkan sekuen
Alu dalam 2,5 kb 3‟UTR
4
lisosom dan mengembalikan reseptor ke membran plasma (ekson 7-14), (iii) daerah terglikosilasi yang mengandung 58 asam amino (ekson 15), (iv) daerah transmembran (ekson 16,17), dan (v) daerah sitoplasma (ekson 17,18) (Sudhof et al. 1985). Struktur LDL-R manusia ditunjukkan pada Gambar 3. LDL-R berperan penting dalam dalam lintas metabolisme lipoprotein yang dimediasi reseptor. LDL-R memodulasi kadar LDL-C plasma dengan mengatur pengambilan partikel LDL oleh hati dan membawa kolesterol menuju kelenjar adrenal dan gonad untuk sintesis hormon steroid menuju hati untuk sintesis asam empedu (Goldstein et al. 2001).
Gambar 3 Struktur LDL-R manusia. Bagian kanan adalah ekson yang mengkode protein dan bagian kiri adalah domain protein matang
Mutasi pada gen LDLR menyebabkan sintesis LDL-R tidak terjadi atau fungsinya menjadi tidak normal (Hobbs et al. 1990). Analisis terhadap varian gen LDLR terkait FH diperkirakan ada 1066 mutasi atau penyusunan ulang pada gen LDLR, 65% (n=689) diantaranya adalah substitusi DNA, 24% (n=260) penyusunan ulang beberapa DNA (<100 pb), dan 11% (n-117) penyusunan ulang banyak DNA (>100 pb). Substitusi dan penyusunan ulang terjadi sepanjang gen, 839 dalam daerah ekson (93 nonsense, 499 missense, dan 247 penyusunan ulang beberapa DNA), 86 dalam daerah intron, dan 24 dalam daerah promotor. Proporsi terbanyak pada ekson terjadi dalam daerah pengikat ligan (ekson 2-6) dan daerah prekursor EGF (ekson 7-14) (Leigh et al. 2008).
Selain karena mutasi, adanya variasi genetik umum pada gen LDLR
(1773C>T) dalam ekson 12 terhadap kadar LDL-C menunjukkan bahwa pengaruh rerata (dari rerata sampel) dari alel 1773T terhadap LDL-C adalah +3.9 mg/dL, sementara pengaruh rerata dari alel 1773C adalah −6,2 mg/dL. Pengaruh kedua alel tersebut kecil tetapi nyata. Perubahan nukleotida dalam ekson 12 ini tidak mengubah asam amino, sehingga disimpulkan bahwa SNP ini berada dalam linkage disequilibrium dengan varian fungsional lainnya. Knoblauch et al. (2002) yang mengkaji pengaruh haplotipe SNP umum dari gen LDLR menunjukkan keberadaan SNP pada rs5930 (26462G>A dalam ekson 10), rs5925 (33078A>G dalam ekson 13), dan rs5927 (36138C>T alam ekson 15) yang dikelompokkan ke dalam 7 haplotipe: GTG, GTA, GCG, GCA, ATG, ATA, dan ACG. Haplotipe GTG adalah haplotipe yang terkait dengan profil lipid karena secara nyata menurunkan total kolesterol sebesar 0,32 mg/dl dan LDL-C sebesar 0,41 mg/dl. Kajian lebih luas yang meliputi SNP, rs2228671 (13109C>T dalam ekson 2), rs885765 (18896A>C dalam intron 4), rs5930 (26462G>A dalam ekson 10), rs5925 (33078A>G dalam ekson 13), rs5927 (36138C>T dalam ekson 15), Pvu II intron 15, C/T dan rs1433099 (44857C>T dalam 3‟UTR) menunjukkan bahwa kontribusi haplotipe gen LDLR terhadap varian LDL-C adalah 5%, HDL-C 6% dan LDL/HDL 2% dan tidak ada dari polimorfisme yang dilaporkan memiliki pengaruh fungsional sehingga dianggap berada dalam linkage disequilibrium dengan polimorfisme penyebab variasi (Knoblauch et al. 2004).
SNP rs688 (1773C>T dalam ekson 12) yang potensial terkait dengan perubahan ekspresi gen LDLR telah dilaporkan oleh Zhu et al. (2007). Wanita homozigot dengan alel 1773T mempunyai efisiensi penyambungan ekson 12 yang menurun sekitar 8,6% dibandingkan wanita homozigot dengan alel 1773C. Alel 1773T mengarah pada peningkatan jumlah transkrip LDLR tanpa ekson 12 sehingga menghasilkan perubahan kerangka baca dan protein terminasi dini. Pada kajian ini alel 1773T terkait dengan kenaikan 10% dalam total kolesterol dan LDL-C pada wanita pramenopause. Di sisi lain, penurunan efisiensi penyambungan tidak nyata pada pria. Perbedaan ini disebabkan pengaruh modulasi estrogen pada SRp40, faktor penyambungan prediksi yang mengikat pada enhancer
splising ekson (ESE). SNP 1773C>T tidak mengubah runutan asam amino,
tetapi berada di dalam daerah ESE. Ini adalah SNP umum fungsional potensial pertama dalam gen LDLR manusia yang dilaporkan. Beberapa kajian terkait genom secara luas (genome wide association studies, GWAS) yang dilakukan selama dekade terakhir menunjukkan bahwa variabilitas pada gen LDLR terkait dengan kadar LDL-C (Sandu et al. 2008; Kathiresan
et al. 2008; Willer et al. 2008). Saat inigen LDLR merupakan salah satu gen
kandidat penyebab hiperkolesterolemia poligenik (Teslovich et al. 2010; De Castro-Oros et al. 2013) dan termasuk dalam skor gen LDL-C, walaupun mekanismenya masih belum diketahui (Talmud et al. 2013).
6
ekspresi messenger RNA (mRNA), akan berdampak penting pada pemahaman mengenai kerentanan terhadap kejadian dan perkembangan penyakit dalam organisme model tersebut.
Informasi mengenai variasi genetik pada spesies dalam genus macaca yang banyak digunakan sebagai organisme model dalam penelitian biomedis telah banyak dilaporkan. Sebagian besar spesies model ini menunjukkan variabilitas genetik terkait asal geografis (Tosi dan Coke 2007; Zinner et al. 2009; Haus et al. 2013). Data sekuen lima daerah genomik (150 kb) pada 9 monyet rhesus (M. mulatta) asal Cina dan 38 asal india menunjukkan bahwa densitas SNP 7,25 per kb dalam rhesus asal Cina dan 5,8 per kb dalam rhesus asal India (Hernandez et al. 2007). Kajian terhadap sekuen genom utuh 3 monyet rhesus India menunjukkan keberadaan lebih dari 3 juta SNP (Fawcett 2011). Dalam subspesies Pan
troglodytes verus, simpanse Afrika Barat yang paling umum digunakan di
laboratorium penelitian biomedis, rerata heterosigositas diperkirakan 0,0008, sedangkan subspesies P. t troglodytes dari Afrika tengah diperkirakan dua kali lebih tinggi (Chimpanzee Sequencing and Analysis Consortium 2005). Tanpa memperhitungkan tambahan variasi pada subspesies Timur (P. t schweinfurthi), kedua subspesies memiliki rerata heterosigositas 0,00019. Scally et al. (2012) menemukan bahwa dua gorila dataran rendah barat memiliki tingkat heterosigositas minimal 1,8 per kb, sedangkan gorila dataran rendah timur menunjukkan tingkat heterosigositas setengahnya. Semua perkiraan tingkat heterosigositas pada kera dan macaca menunjukkan keragaman lebih tinggi daripada yang diamati pada manusia (Abecasis et al. 2012; Yuan et al. 2012; Rogers dan Gibbs 2014).
Sebagai spesies out-bred monyet ekor panjang juga menunjukkan variasi genetik yang cukup besar (Yan et al. 2011; Higashino et al. 2012; Ogawa dan Vallender 2014). Beberapa diantaranya adalah polimorfisme fungsional dalam gen yang terlibat lintas metabolik dan inflamasi (Flynn et al. 2009; Uno et al. 2010; Blancher et al. 2012; Wu dan Adkins 2012). Walaupun demikian belum ada data yang menunjukkan variasi genetik pada
gen LDLR dan keterkaitannya dengan sifat respons monyet ekor panjang
terhadap diet aterogenik.
Perumusan Masalah
kesamaan peran LDL-R dalam mengatur homeostasis kolesterol antara manusia dan monyet ekor panjang. Untuk itu pada penelitian ini dilakukan analisis variasi genetik umum pada gen LDLR monyet ekor dan keterkaitannya dengan sifat respons hewan terhadap diet aterogenik.
Tujuan Penelitian
Tujuan utama penelitian ini adalah mendapatkan penanda genetik sifat hiper- dan hipo-respons monyet ekor panjang terhadap diet aterogenik. Untuk mencapai tujuan utama tersebut, penelitian ini memiliki beberapa beberapa tujuan khusus, yaitu
1. Menyeleksi hewan sesuai sifat responsnya berdasarkan status kolesterol plasma setelah diintervensi diet aterogenik selama tiga bulan.
2. Mengelompokkan hewan berdasarkan polimorfisme nukleotida tunggal (SNP) dalam gen LDLR.
3. Menjelaskan mekanisme molekuler yang mendasari keterkaitan antara variasi genetik dan variasi respons.
Manfaat Penelitian
Penelitian ini bermanfaat dalam seleksi monyet ekor panjang sebagai hewan model dalam penelitian aterosklerosis. Penggunaan penanda genetik membuat seleksi hewan hipo- dari hiper-responder menjadi lebih cepat dan efisien.
Hipotesis
Variasi genetik umum pada gen LDLR berkaitan dengan sifat hiper- atau hipo-respons monyet ekor panjang terhadap diet aterogenik
Kebaharuan (Novelty) Penelitian
Berdasarkan kajian literatur, hingga saat ini belum ada data genetik mengenai variasi umum pada gen LDLR monyet ekor panjang dan kaitannya dengan sifat hiper- atau hipo-respons terhadap diet tinggi kolesterol. Penelitian ini menghasilkan informasi baru mengenai SNP pada gen LDLR
monyet ekor panjang yang berpotensi sebagai penanda genetik untuk menyeleksi sensitivitas hewan terhadap diet aterogenik.
Ruang Lingkup Penelitian
Penelitian ini difokuskan pada analisis terhadap gen LDLR untuk menunjukkan bahwa sifat hiper- atau hipo-respon monyet ekor panjang terhadap diet aterogenik berkaitan dengan variasi genetik berupa SNP pada gen tersebut. Tahapan penelitian yang dilakukan meliputi:
8
analisis variasi respons kadar kolesterol plasma untuk menyeleksi sensitivitas hewan berdasarkan status kolesterol plasma. Tahapan ini dibahas dalam Bab II.
2. Tahap kedua adalah identifikasi variasi genetik umum pada gen LDLR. Identifikasi dilakukan pada daerah pengatur yaitu promotor dan 3‟UTR, ekson dan intron gen LDLR. Analisis genetik dilakukan untuk mengelompokkan hewan berdasarkan polimorfisme umum. Tahapan ini dibahas dalam Bab III, IV, dan V.
3. Tahap ketiga adalah analisis ekspresi gen LDLR dan membuat pustaka cDNA individu hipo-responder. Analisis ekspresi gen dilakukan dengan mengukur kelimpahan mRNA dalam sel darah tepi berinti tunggal
(peripheral blood mononuclear cell, PBMC). Analisis ini dilakukan
untuk menjelaskan mekanisme molekuler yang mendasari keterkaitan antara variasi genetik dan variasi respons. Tahapan ini dibahas dalam Bab VI.
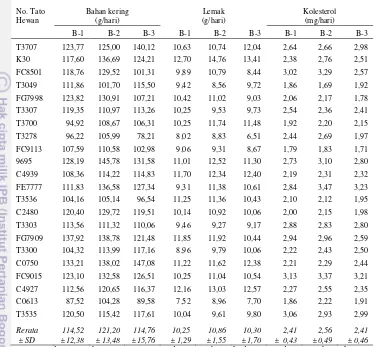
Gambar 4 Bagan kerangka pikir penelitian
Penanda genetik Intervensi diet aterogenik
Identifikasi variasi genetik umum
Analisis variasi respons kolesterol
plasma
Analisis ekspresi gen
Dasar seleksi hipo- dari hiper-responder
Hewan model dalam penelitian biomedis terkait aterosklerosis Polimorfisme
nukleotida tunggal (SNP)
Individu hipo-responder
Individu hiper-responder
Kadar kolesterol total plasma
(mg/dL)
Profil mRNA dan sekuensing
cDNA
Ekson Promotor
dan 3‟UTR
10
2 SELEKSI MONYET EKOR PANJANG (
Macaca
fascicularis
) HIPER- DAN HIPO-RESPONDER
BERDASARKAN STATUS KOLESTEROL PLASMA
[Selection of Hyper- and Hyporesponder Cynomolgus
Macaque (Macaca fascicularis) Based on the Status of Plasma
Cholesterol]
Abstract
The effectiveness of atherogenic diet in raising plasma cholesterol level of cynomolgus macaques (Macaca fascicularis) can be predicted for population, but not for individuals. This study aimed to evaluate the individual plasma cholesterol of cynomolgus macaques in response to IPB-1 atherogenic diet and to select the animals according their responsiveness based on the status of plasma cholesterol after intervention of atherogenic diet. The animals under study were 22 adult male monkeys from the animal facility of Primate Research Center Bogor Agricultural University (PSSP IPB). All animals were intervened with the IPB-1 atherogenic diet for three months and individual plasma cholesterol was evaluated in a monthly basis. The results showed that the macaques‟ plasma cholesterol had increased significantly (P <0,05) after one month of intervention period and the increases were very significantly different (P<0,01) after three months. Individually, increases in plasma cholesterol varied among animals. Based on these variations, 2 animals were categorised as hypo-response, 18 animals as hyper-response and 2 animals as extreme.
Keywords: IPB-1 atherogenic diet, Macaca fascicularis, responsiveness
PENDAHULUAN
stenosis arteri koroner dan kematian mendadak yang dihasilkan dari trombosis oklusif dan infark miokard (Shelton et al. 2012).
Walaupun efek kuantitatif dari komponen diet aterogenik dapat diprediksi meggunakan rumus empiris, namun prediksi perubahan kolesterol plasma hanya berlaku untuk rataan kelompok dan tidak untuk individual. Fakta menunjukkan adanya individu hipo-responder dengan kadar kolesterol plasma yang tidak atau kurang sensitif terhadap perubahan diet selain individu hiper-responder yang sensitif. Konsep sifat hiper- dan hipo-respons merujuk pada perbedaan yang besar dalam kadar kolesterol plasma yang ditemukan diantara individu yang diberi diet serupa, terutama diet yang mengandung lemak jenuh dan kolesterol dalam jumlah besar (Beynen et al. 1987).
Selama ini seleksi monyet ekor panjang hiper- atau hipo-responder dilakukan berdasarkan status kolesterol plasma hewan setelah di intervensi diet aterogenik selama 2 bulan (Clarkson et al. 1988; Turley et al. 1997). Oleh karena itu pengembangan diet aterogenik yang mampu meningkatkan konsentrasi kolesterol plasma secara efektif perlu dilakukan. Sejalan dengan hal tersebut, peneliti di Pusat Studi Satwa Primata Institut Pertanian Bogor (PSSP IPB) telah melakukan formulasi diet aterogenik. Diawali dengan formulasi diet tinggi karbohidrat untuk obesitas (Astuti et al. 2009) dan diet tinggi lemak untuk meningkatkan profil lipid darah monyet ekor panjang (Suparto et al. 2010), pengembangan selanjutnya berhasil diformulasi diet baru berbasis bahan baku lokal yang diberi nama diet aterogenik IPB-1 (Astuti et al. 2014). Diet ini diharapkan mampu meningkatkan kolesterol plasma monyet ekor panjang secara efektif. Penelitian ini bertujuan mengevaluasi kolesterol plasma individual monyet ekor panjang sebagai respons terhadap intervensi diet aterogenik IPB-1 dan menyeleksi hewan sesuai sifat responsnya berdasarkan status kolesterol plasma setelah diintervensi diet aterogenik IPB-1 selama tiga bulan.
BAHAN DAN METODE
Hewan
Hewan yang digunakan dalam penelitian ini 22 ekor monyet ekor panjang (M. fascicularis) jantan dewasa (ditentukan berdasarkan dentisi) hasil penangkaran PSSP IPB dengan umur berkisar 6-8 tahun dan bobot badan antara 4 – 5 kg. Identifikasi individual dilakukan dengan penomoran tato di bagian dada hewan. Hewan dikandangkan dalam kandang individual yang ditempatkan pada posisi agar antar individu berinteraksi secara audiovisual. Semua prosedur yang dilakukan pada hewan telah disetujui Komisi Kesejahteraan dan Penggunaan Hewan Laboratorium dengan nomor protokol 12-B009-IR.
Diet
12
2014). Sebelum pemberian diet, hewan diberikan pakan standar selama dua minggu untuk adaptasi. Setelah masa adaptasi, hewan diberi diet aterogenik IPB-1 selama 3 bulan. Makanan diberikan 100-180 g per hewan dua kali sehari (pukul 08.00 pagi dan 14.00 siang) dan minuman diberikan secara ad
libitum. Sebagai tambahan diberikan pisang 70 g per hari (pukul 12.00
siang). Komposisi diet aterogenik IPB-1 ditunjukkan pada Tabel 1 (Astuti et al. 2014).
Tabel 1 Komposisi diet aterogenik IPB-1
Bahan % bahan kering
Tepung terigu 42
Gula pasir 9
Kuning telur segar 10 Lemak daging sapi 5
Minyak kelapa 10
Tepung jagung 8
Dedak 3
Tepung kedelai 4
Tepung ikan 5
Mineral mix 1
Selulosa 1
Vitamin mix 1
Agar 1
Total 100
Prosedur Penelitian
Bobot Badan dan Koleksi Darah
Hewan ditimbang bobot badannya dan diambil darahnya sebelum pemberian diet aterogenik dan setiap bulan setelah pemberian diet. Sebelum ditimbang dan diambil darahnya, hewan disedasi dengan ketamin HCl (10 mg/kg bobot tubuh) secara intramuskuler. Penimbangan menggunakan timbangan dengan skala terkecil gram, sedangkan darah diambil dari vena femoralis sebanyak 3 mL dengan tabung berisi antikoagulan
ethylenediaminetetraacetic (EDTA). Sampel darah digunakan untuk analisis
kolesterol plasma
Konsumsi Diet
Total Kolesterol Plasma
Pengukuran total kolesterol plasma (TPC) dilakukan berdasarkan uji enzimatik kolorimetrik (metode Cholesterol Oxidase-Peroxidase
Aminoantipyrine Phenol/CHOD-PAP, menggunakan kit Cholesterol dengan
No Cat:101598 sesuai dengan petunjuk perusahaan) dengan mesin fotometer seri 5010.
Analisis Data
Data konsumsi, bobot badan dan konsentrasi total kolesterol plasma disajikan sebagai nilai individual dan nilai rerata serta diolah menggunakan analisis ragam (ANOVA). Sifat hiper- atau hipo-respons didasarkan pada konsentrasi kolesterol plasma setelah diintervensi diet aterogenik. Hewan dengan sifat hiper-respons memiliki konsentrasi kolesterol plasma dalam kisaran 1,5 SD dari rerata, sedangkan hewan dengan sifat hipo-respons memiliki konsentrasi kolesterol di bawah kisaran tersebut. Selain itu hewan dengan konsentrasi kolesterol di atas kisaran dikategorikan sebagai hewan dengan sifat ekstrem (Beynen et al. 1987).
HASIL DAN PEMBAHASAN
Bobot Badan
Pengamatan terhadap rataan bobot badan menunjukkan mulai terjadinya peningkatan yang berbeda nyata (P<0,05) pada bulan pertama dan tetap stabil pada bulan kedua dan ketiga (P>0,05). Data peningkatan bobot badan individual monyet ekor panjang ditunjukkan pada Tabel 2. Intervensi diet selama bulan pertama meningkatkan rerata bobot hewan 0,70 kg, yaitu dari 4,71 kg menjadi 5,41 kg. Lima hewan, yaitu T3700, FG7998, T3278, C0750, dan K30 mengalami peningkatan bobot badan lebih dari 1,00 kg, sementara 4 hewan, yaitu FC9015, FC8501, C0613, dan FE7777 mengalami peningkatan bobot badan kurang dari 0,35 kg. Setelah tiga bulan hewan C0750 dan FG7998 mengalami peningkatan bobot badan lebih dari 1,00 kg, sedangkan hewan T3536, FC9015, dan C0613 mengalami peningkatan kurang dari 0,20 kg. Secara individual terdapat 3 hewan yang setiap bulan mengalami peningkatan bobot badan, yaitu FG7998, FE7777, dan C0750.
Peningkatan bobot badan yang berbeda nyata pada bulan pertama berkaitan dengan penambahan kuning telur sebagai sumber kolesterol dalam diet aterogenik. Penelitian sebelumnya yang dilakukan para peneliti di PSSP IPB menunjukkan bahwa kuning telur terbukti memperbaiki palatabilitas sehingga mempercepat terjadinya peningkatan bobot badan (Suparto et al.
14
Tabel 2 Bobot badan bulanan individual monyet ekor panjang
No. Tato Hewan
Bobot badan bulanan (kg)
(B-3)˗(B-0)
B-0 B-1 B-2 B-3 (kg)
T3707 5,50 6,50 6,50 6,20 0,70
K30 4,70 5,75 5,60 5,00 0,30
FC8501 4,50 4,70 4,60 4,60 0,40
T3049 5,00 5,90 5,60 5,60 0,50
FG7998 4,00 5,20 5,30 5,40 1,40
T3307 5,05 5,60 5,50 5,30 0,25
T3700 5,35 6,90 7,50 6,30 0,95
T3278 5,00 6,10 5,90 5,90 0,90
FC9113 4,20 4,60 4,55 4,40 0,20
9695 4,50 5,05 4,90 5,00 0,50
C4939 4,10 4,80 4,75 4,90 0,80
FE7777 4,40 4,70 4,75 5,00 0,60
T3536 5,05 5,50 5,40 5,10 0,05
C2480 4,50 4,90 4,80 4,80 0,38
T3303 4,70 5,50 5,20 5,05 0,35
FG7909 4,50 5,50 4,80 5,10 0,55
T3300 5,25 5,90 5,70 5,50 0,25
C0750 5,10 6,20 6,60 6,80 1,70
FC9015 4,70 4,90 4,85 4,75 0,05
C4927 4,20 4,90 5,20 5,10 0,90
C0613 4,60 4,90 4,80 4,70 0,10
T3535 4,70 5,10 4,90 5,00 0,40
Rerata ± SD 4,71 ± 0,42 5,41 ± 0,64 5,35 ± 0,74 5,25 ± 0,59 0,56 ± 0,42
Ket. B-0 = data awal sebelum diet, B-1 = data setelah satu bulan diet, B-2 = data setelah dua bulan diet, B-3 = data setelah tiga bulan diet.
Konsumsi Diet
Rerata konsumsi diet bulanan disajikan pada Tabel 3. Hasil analisis terhadap konsumsi diet menunjukkan bahwa rerata konsumsi diet selama bulan pertama, kedua dan ketiga tidak berbeda nyata (P>0,05). Hal ini berarti konsumsi diet oleh hewan adalah stabil selama penelitian. Dari Tabel 3 terlihat bahwa selama bulan pertama hewan K30 dan C4927 mengkonsumsi lemak paling tinggi, sedangkan hewan C0613, dan T3278 paling rendah. Selain itu, terlihat pula bahwa hewan FC9015, T3535 dan FC8501 mengkonsumsi kolesterol paling tinggi, sementara FC9113, C0613 dan T3049 paling rendah. Pada bulan ketiga hewan K30 dan C4927 tetap merupakan hewan dengan konsumsi lemak tinggi, sementara hewan T3278, C0613 dan FC8501 rendah. Hewan FE7777 dan FC9015 mengkonsumsi kolesterol paling tinggi, sementara FC9113, FG7998, dan C0613 paling rendah.
dengan kesukaan hewan pada rasa gurih dari kuning telur yang terdapat dalam diet (Suparto et al. 2010).
Tabel 3 Rerata konsumsi diet bulanan individual monyet ekor panjang
No. Tato Hewan Bahan kering (g/hari) Lemak (g/hari) Kolesterol (mg/hari) B-1 B-2 B-3 B-1 B-2 B-3 B-1 B-2 B-3 T3707 123,77 125,00 140,12 10,63 10,74 12,04 2,64 2,66 2,98 K30 117,60 136,69 124,21 12,70 14,76 13,41 2,38 2,76 2,51 FC8501 118,76 129,52 101,31 9,89 10,79 8,44 3,02 3,29 2,57 T3049 111,86 101,70 115,50 9,42 8,56 9,72 1,86 1,69 1,92 FG7998 123,82 130,91 107,21 10,42 11,02 9,03 2,06 2,17 1,78 T3307 119,35 110,97 113,26 10,25 9,53 9,73 2,54 2,36 2,41 T3700 94,92 108,67 106,31 10,25 11,74 11,48 1,92 2,20 2,15 T3278 96,22 105,99 78,21 8,02 8,83 6,51 2,44 2,69 1,97 FC9113 107,59 110,58 102,98 9,06 9,31 8,67 1,79 1,83 1,71 9695 128,19 145,78 131,58 11,01 12,52 11,30 2,73 3,10 2,80 C4939 108,36 114,22 114,83 11,70 12,34 12,40 2,19 2,31 2,32 FE7777 111,83 136,58 127,34 9,31 11,38 10,61 2,84 3,47 3,23 T3536 104,16 105,14 96,54 11,25 11,36 10,43 2,10 2,12 1,95 C2480 120,40 129,72 119,51 10,14 10,92 10,06 2,00 2,15 1,98 T3303 113,56 111,32 110,06 9,46 9,27 9,17 2,88 2,83 2,80 FG7909 137,92 138,78 121,48 11,85 11,92 10,44 2,94 2,96 2,59 T3300 104,32 113,99 117,16 8,96 9,79 10,06 2,22 2,43 2,50 C0750 133,21 138,02 147,08 11,22 11,62 12,38 2,21 2,29 2,44 FC9015 123,10 132,58 126,51 10,25 11,04 10,54 3,13 3,37 3,21 C4927 112,56 120,65 116,37 12,16 13,03 12,57 2,27 2,55 2,35 C0613 87,52 104,28 89,58 7,52 8,96 7,70 1,86 2,22 1,91 T3535 120,50 115,42 117,61 10,04 9,61 9,80 3,06 2,93 2,99
Rerata ± SD 114,52 ± 12,38 121,20 ± 13,48 114,76 ± 15,76 10,25 ± 1,29 10,86 ± 1,55 10,30 ± 1,70 2,41 ± 0,43
2,56 ± 0,49
2,41 ± 0,46 Ket. B-1 = data rerata bulan pertama, B-2 = data rerata bulan kedua, B-3 = data rerata bulan ketiga.
Total Kolesterol Plasma
16
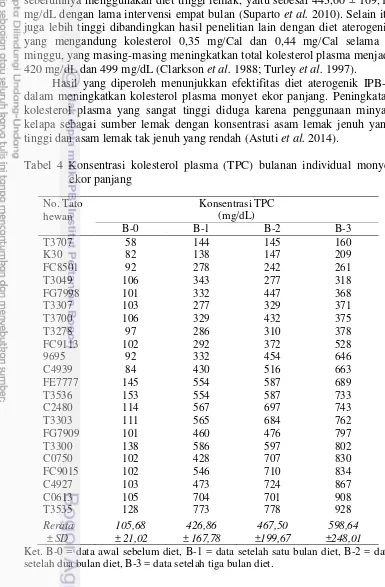
Pada saat ini hewan C0613 dan T3535 memiliki konsentrasi yang sangat tinggi (lebih dari 900 mg/dL), sementara hewan T3707 dan K30 tetap tidak mengalami hiperkolesterolemia karena konsentrasi kolesterol plasmanya masih mendekati nilai normal. Peningkatan rerata konsentrasi total kolesterol pada bulan ketiga lebih tinggi dibandingkan penelitian sebelumnya menggunakan diet tinggi lemak, yaitu sebesar 443,60 ± 169,10 mg/dL dengan lama intervensi empat bulan (Suparto et al. 2010). Selain itu juga lebih tinggi dibandingkan hasil penelitian lain dengan diet aterogenik yang mengandung kolesterol 0,35 mg/Cal dan 0,44 mg/Cal selama 8 minggu, yang masing-masing meningkatkan total kolesterol plasma menjadi 420 mg/dL dan 499 mg/dL (Clarkson et al. 1988; Turley et al. 1997).
Hasil yang diperoleh menunjukkan efektifitas diet aterogenik IPB-1 dalam meningkatkan kolesterol plasma monyet ekor panjang. Peningkatan kolesterol plasma yang sangat tinggi diduga karena penggunaan minyak kelapa sebagai sumber lemak dengan konsentrasi asam lemak jenuh yang tinggi dan asam lemak tak jenuh yang rendah (Astuti et al. 2014).
Tabel 4 Konsentrasi kolesterol plasma (TPC) bulanan individual monyet ekor panjang
No. Tato hewan
Konsentrasi TPC (mg/dL)
B-0 B-1 B-2 B-3
T3707 58 144 145 160
K30 82 138 147 209
FC8501 92 278 242 261
T3049 106 343 277 318
FG7998 101 332 447 368
T3307 103 277 329 371
T3700 106 329 432 375
T3278 97 286 310 378
FC9113 102 292 372 528
9695 92 332 454 646
C4939 84 430 516 663
FE7777 145 554 587 689
T3536 153 554 587 733
C2480 114 567 697 743
T3303 111 565 684 762
FG7909 101 460 476 797
T3300 138 586 597 802
C0750 102 428 707 830
FC9015 102 546 710 834
C4927 103 473 724 867
C0613 105 704 701 908
T3535 128 773 778 928
Rerata ± SD 105,68 ± 21,02 426,86 ± 167,78 467,50 ±199,67 598,64 ±248,01
[image:32.595.61.446.161.748.2]Sifat Hiper- dan Hipo-respons
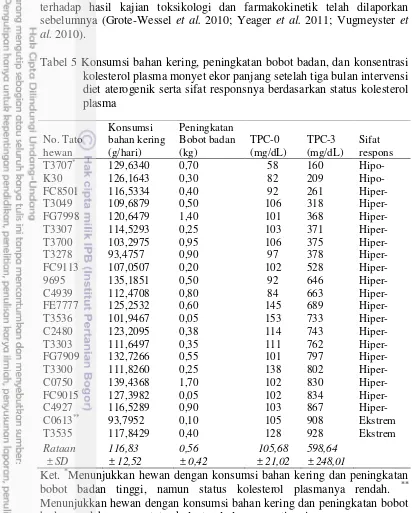
Variasi peningkatan konsentrasi kolesterol plasma menunjukkan perbedaan sensitivitas (sifat respons) antar individu. Hewan dengan konsentrasi kolesterol plasma setelah tiga bulan intervensi diet aterogenik berkisar 1,5 x SD dikelompokkan sebagai hewan dengan sifat hiper-respons, kurang dari ,5 x SD bersifat hipo-respons, dan lebih dari 1,5 x SD bersifat ekstrem (Beynen et al. 1987). Tabel 5 merangkum data konsumsi bahan kering, peningkatan bobot tubuh, dan konsentrasi kolesterol plasma individual monyet ekor panjang setelah bulan ketiga dan pengelompokkan sifat responsnya berdasarkan status kolesterol plasma. Berdasarkan status kolesterol plasma setelah bulan ketiga 2 hewan (T3707 dan K30) dengan konsentrasi kolesterol plasma kurang dari 221 mg/dL) dikelompokkan sebagai hipo-responder, 18 hewan dengan konsentrasi kolesterol plasma antara 221 hingga 900 mg/dL dikelompokkan sebagai hewan hiper-responder, dan 2 hewan dengan konsentrasi kolesterol plasma lebih dari 900 mg/dL dikelompokkan sebagai hewan ekstrem. Pengelompokkan dengan hasil yang sama juga diperoleh bila didasarkan pada status kolesterol plasma bulan pertama, yaitu 2 hewan hipo-responder, 18 hewan hiper-responder, dan 2 hewan ekstrem. Hewan hipo-responder, hiper-responder, dan ekstrem masing masing memiliki kolesterol plasma kurang dari 175 mg/dL, 175 hingga 677 mg/dL, dan lebih dari >677 mg/dL. Keberadaan sekitar 10% individu yang bersifat hipo-respons dan 10% lainnya yang bersifat ekstrem terhadap diet aterogenik dalam penelitian ini sejalan dengan laporan Beynen
et al. (1987) mengenai distribusi individu berdasarkan sensitivitasnya dalam
populasi.
Efektivitas diet aterogenik IPB-1 dalam meningkatkan konsentrasi kolesterol plasma monyet ekor panjang dalam waktu 1 bulan membuat seleksi sensitivitas hewan berdasarkan status kolesterol plasma menjadi semakin cepat. Hal ini akan menekan tingginya biaya pemeliharaan hewan selama masa seleksi di pusat-pusat penelitian satwa primata. Selain itu penggunaan diet aterogenik IPB-1 yang berbahan baku lokal juga akan mengurangi ketergantungan terhadap diet aterogenik komersil yang semakin mahal.
18
[image:34.595.45.457.99.612.2]mempengaruhi perbedaan individu monyet ekor panjang dalam respons terhadap hasil kajian toksikologi dan farmakokinetik telah dilaporkan sebelumnya (Grote-Wessel et al. 2010; Yeager et al. 2011; Vugmeyster et al. 2010).
Tabel 5 Konsumsi bahan kering, peningkatan bobot badan, dan konsentrasi kolesterol plasma monyet ekor panjang setelah tiga bulan intervensi diet aterogenik serta sifat responsnya berdasarkan status kolesterol plasma No. Tato hewan Konsumsi bahan kering (g/hari) Peningkatan Bobot badan (kg) TPC-0 (mg/dL) TPC-3 (mg/dL) Sifat respons
T3707* 129,6340 0,70 58 160 Hipo-
K30 126,1643 0,30 82 209 Hipo-
FC8501 116,5334 0,40 92 261 Hiper-
T3049 109,6879 0,50 106 318 Hiper-
FG7998 120,6479 1,40 101 368 Hiper-
T3307 114,5293 0,25 103 371 Hiper-
T3700 103,2975 0,95 106 375 Hiper-
T3278 93,4757 0,90 97 378 Hiper-
FC9113 107,0507 0,20 102 528 Hiper-
9695 135,1851 0,50 92 646 Hiper-
C4939 112,4708 0,80 84 663 Hiper-
FE7777 125,2532 0,60 145 689 Hiper-
T3536 101,9467 0,05 153 733 Hiper-
C2480 123,2095 0,38 114 743 Hiper-
T3303 111,6497 0,35 111 762 Hiper-
FG7909 132,7266 0,55 101 797 Hiper-
T3300 111,8260 0,25 138 802 Hiper-
C0750 139,4368 1,70 102 830 Hiper-
FC9015 127,3982 0,05 102 834 Hiper-
C4927 116,5289 0,90 103 867 Hiper-
C0613** 93,7952 0,10 105 908 Ekstrem
T3535 117,8429 0,40 128 928 Ekstrem
Rataan ± SD 116,83 ± 12,52 0,56 ± 0,42 105,68 ± 21,02 598,64 ± 248,01
Ket. *Menunjukkan hewan dengan konsumsi bahan kering dan peningkatan bobot badan tinggi, namun status kolesterol plasmanya rendah. ** Menunjukkan hewan dengan konsumsi bahan kering dan peningkatan bobot badan rendah, namun status kolesterol plasmanya tinggi.
gen apolipoprotein B, gen apolipoprotein E, gen pengkode enzim-enzim yang terlibat dalam metabolisme kolesterol (lipoprotein lipase, hepatik lipase, dan kolesterol 7α-hidroksilase) dan gen LDLR serta gen-gen lain seperti gen protein transfer ester kolesterol (cholesterol ester transfer
protein, CETP), gen protein pengikat asam lemak usus (intestinal fatty
acid-binding protein, FABP2) dan gen neuropeptida (Masson et al. 2003).
Keberadaan gen yang berpotensi menyebabkan variasi respons terhadap perubahan intervensi diet pada manusia penting juga dikaji pada hewan, terutama kemungkinan keterkaitan antara variasi genetik dan variasi respons. Dengan demikian variasi genetik dapat dijadikan sebagai penanda genetik bagi sifat respons tertentu.
SIMPULAN
20
3 VARIASI GENETIK PADA DAERAH PROMOTOR GEN
LDLR
DAN SIFAT RESPONS MONYET EKOR PANJANG
(
Macaca fascicularis
) TERHADAP DIET ATEROGENIK
[Genetic Variation at the Promoter Region of
LDLR
Gene
and Responsiveness of Cynomolgus Macaque (
Macaca
fascicularis
) to Atherogenic Diet]
Abstract
Common genetic polymorphism at the human LDLR gene can potential affect normal variation of plasma lipid profile. Although cynomolgus macaques (Macaca fascicularis) are widely used animals as models for response of plasma cholesterol to dietary cholesterol, little is known about genetic variation in its LDLR gene. In this research, genetic variation at the promoter region of LDLR gene was studied using isolated DNAs of 22 cynomolgus macaques which have differences in responsiveness to atherogenic diets. The objective of study was identify genetic variation at the promoter region of the LDLR gene and evaluate the kind of haplotype related to the responsiveness of cynomolgus macaque (Macaca fascicularis) to atherogenic diet. The result showed that promoter sequence of LDLR
gene had lower genetic diversity (nucleotide composition, number of nucleotide difference, nucleotide diversity, genetic distance, and substitution pattern) than human. There are 3 single nucleotide polymorphisms (SNPs), i.e. g.−571A>T, g.−416C>T and g.−169A>G, and distributed in 3 haplotipes, i.e. haplotype I (ACA), II (TTA) and III (ACG) with haplotype diversity 0.177±0.01128. Haplotype II (TTA) showed linkages with the hyporesponsiveness of cynomolgus macaque to atherogenic diet and SNP g.−571A>T and g.−416C>T which were potential genetic marker for hyporesponder.
Keywords: SNP, LDLR gene, Macaca fascicularis, promoter, responsiveness
PENDAHULUAN
Pada manusia hiperkolesterolemia memiliki dasar yang kompleks karena fenotip tersebut dihasilkan dari interaksi antara pengaruh lingkungan dan genetik. Hiperkolesterolemia turunan (familial hypercholesterolemia,
FH) merupakan salah satu contoh keadaan hiperkolesterolemia akibat variasi genetik langka berupa mutasi pada gen LDLR yang secara nyata menyebabkan tingginya kadar kolesterol LDL (LDL-C) plasma dan penyakit jantung koroner (PJK) dini. Mutasi pada gen LDLR menyebabkan sintesis reseptor LDL tidak terjadi atau fungsinya menjadi tidak normal (Hobbs et al. 1990). Selain karena mutasi, adanya variasi genetik umum berupa polimorfisme nukleotida tunggal (single nucleotide polymorphism, SNP) pada gen LDLR juga telah dilaporkan mempengaruhi variasi normal dalam profil lipid plasma. Saat ini gen LDLR merupakan salah satu gen kandidat penyebab hiperkolesterolemia poligenik (Teslovich et al. 2010; De Castro-Oros et al. 2013) dan termasuk dalam skor gen LDL-C, walaupun mekanismenya masih belum diketahui (Talmud et al. 2013). Mengingat kemiripan metabolisme homeostasis kolesterol antara manusia dan monyet ekor panjang (Turley et al. 1995), maka keberadaan variasi genetik pada gen
LDLR kemungkinan dapat digunakan sebagai dasar seleksi kerentanan monyet ekor panjang terhadap hiperkolesterolemia.
Pada penelitian ini dilakukan sekuensing terhadap daerah promotor gen LDLR monyet ekor panjang. Promotor dipilih karena merupakan pengatur transkripsi gen LDLR. Elemen pengatur transkripsi pada promotor
LDLR terletak berkelompok dalam 280 pb pada daerah upstream dari kodon awal, terdiri dari dua boks TATA (sisi awal transkripsi) dan tiga pengulangan tidak sempurna 16 pb kaya GC (R1-R3) (Dawson et al. 1988; Sudhof et al. 1987). R1 dan R3 mengandung sisi pengikatan untuk faktor transkripsi SP1 dan bertanggung jawab terhadap tingkat transkripsi basal dari gen LDLR, sementara R2 memiliki sisi elemen pengatur sterol (SRE-1) tempat protein pengatur sterol (SREBP) berikatan sehingga meningkatkan transkripsi (Briggs et al. 1993). 5‟UTR meliputi mRNA antara sisi awal
transkripsi dan kodon AUG. Selain itu, terdapat pengatur penting lain seperti elemen FP1 dan FP2, dan element respons kaya CT dalam sekuen R3 (Li dan Liu 2010, Liu et al. 2000, Mehta et al. 1996). Tujuan penelitian adalah mengidentifikasi variasi genetik pada daerah promotor gen LDLR
dan mengevaluasi jenis haplotipe yang terkait sifat respons terhadap diet aterogenik.
BAHAN DAN METODE
Hewan Laboratorium
Hewan yang digunakan adalah 22 monyet ekor panjang (M.
fascicularis) jantan dewasa yang telah dikelompokkan sesuai sifat
22
Prosedur Penelitian
Koleksi Darah Sampel dan Ekstraksi DNA Genomik
Hewan disedasi dengan ketamin HCl (10 mg/kg bobot badan) secara intramuskuler untuk tujuan pengambilan darah. Darah diambil dari vena femoralis sebanyak 3 ml dan dimasukkan ke dalam tabung yang berisi antikoagulan EDTA. DNA genomik diekstrak dari darah sampel menggunakan QiaAmp™ DNA blood minikit (Qiagen, Hilden, Jerman) sesuai dengan petunjuk perusahaan.
Desain primer, Amplifikasi dan Sekuensing
Primer didesain berdasarkan sekuen gen LDLR monyet rhesus
(http://genome.ucsc.edu, dengan nomor aksesi GenBank AY466854)
menggunakan program Primer3 (http://primer3.wi.mit.edu/). Primer yang digunakan adalah F: 5‟-TCATCCAAAGGCAGGATCTC-3‟ dan R: 5‟- CCTGGAGCAAGCCTTACCT-3‟. Ukuran produk amplifikasi adalah 789 pb. Amplifikasi dilakukan dengan mesin Gene Amp® PCR System 9700
(Applied Biosystem). Komponen reaksi untuk amplifikasi promotor terdiri
atas: 5 μl cetakan DNA, 1 μl primer forward dan 1 μl primer reverse dengan konsentrasi 10 pmol/μl, 12,5 μl KAPA Taq Extra HotStart readymix
with dye (buffer, dNTP, dan Taq polimerase) dan 5,5 μl nuclease free water.
PCR terdiri dari denaturasi awal pada suhu 94oC selama 5 menit lalu tahapan 40 siklus. Setiap siklus dilakukan dengan tahapan reaksi sebagai berikut: sampel didenaturasi pada suhu 94oC selama 30 detik, dilanjutkan
annealing pada suhu 56oC selama 30 detik, dan extension pada suhu 72oC
selama 30 detik. Setelah itu proses PCR dilanjutkan dengan post extension
pada suhu 72oC selama 7 menit, dan diakhiri pada suhu 25oC selama 4 menit. Konfirmasi produk PCR dilakukan menggunakan elektroforesis gel agarosa 1,8% yang mengandung 10 μg/ ml etidium bromida. Purifikasi produk amplifikasi dilakukan berdasarkan metode MinElute dari Qiagen (Qiagen, Hilden, Jerman). Hasil purifikasi ditentukan runutan basanya dengan teknik sekuensing di First BASE Laboratories Sdh Bhd (Malaysia).
Analisis Data
Runutan basa-basa nukleotida yang diperoleh diedit secara manual berdasarkan kromatogram menggunakan Geneious 7.0.2 (http://geneious.en.
softonic.com, versi coba 30-hari). Pensejajaran runutan basa-basa
nukleotida dan analisis komposisi nukleotida, perbedaan nukleotida, keragaman nukleotida (π), jarak genetik dan pohon filogenetik dilakukan menggunakan program Mega-6 (Tamura et al. 2013). Pensejajaran menggunakan Clustal W, jumlah perbedaan nukleotida menggunakan opsi
number of differences, penghitungan jarak genetik berdasarkan Kimura
2-parameter dan pohon filogenetik dibentuk berdasarkan Neibourjoining
dengan melakukan bootstraps sebanyak 1000 pengulangan. Analisis haplotipe dilakukan menggunakan program DnaSP (Rozas et al. 2003). Prediksi in siliko situs pengikatan faktor transkripsi pada daerah polimorfik menggunakan TFSEARCH (http://www.cbrc.jp/research/db/TFSEARCH.
1000 pb 750 pb 500 pb 250 pb
HASIL DAN PEMBAHASAN
Amplifikasi dan Sekuensing Daerah Promotor
Sebanyak 22 sampel DNA monyet ekor panjang berhasil diamplifikasi daerah promotornya menggunakan primer forward dan reverse yang didesain menggunakan program Primer3. Produk PCR yang dihasilkan sesuai dengan yang diharapkan, yaitu berukuran 789 pb (Gambar 5). Pensejajaran hasil sekuensing dengan referensi monyet ekor panjang di
GenBank (nomor aksesi XM_005587996.2) menunjukkan bahwa produk
amplifikasi terdiri atas 705 pb yang merupakan bagian dari daerah promotor (terletak pada posisi −705 hingga −1), 67 pb merupakan ekson 1 dan 17 pb merupakan bagian dari intron 1.
Gambar 5 Pita DNA berukuran 789 pb hasil amplifikasi PCR. 1 kb adalah marker DNA yang digunakan, angka 1-6 adalah perwakilan sampel hewan
Variasi Nukleotida Antar Sekuen Promotor
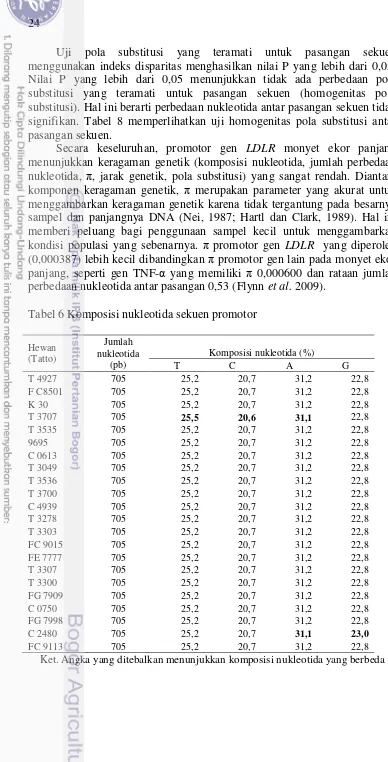
Komposisi nukleotida Timin (T), Sitosin (C), Adenin (A) dan Guanin (G) pada semua hewan sama, kecuali pada hewan T3707 dan C2480. Hewan T3707 memiliki perbedaan komposisi pada nukleotida T, C dan A, sedangkan hewan C2480 pada nukleotida A dan G. Tabel 6 memperlihatkan komposisi nukleotida dari ke 22 hewan.
Analisis pairwise distance dengan opsi number of differences
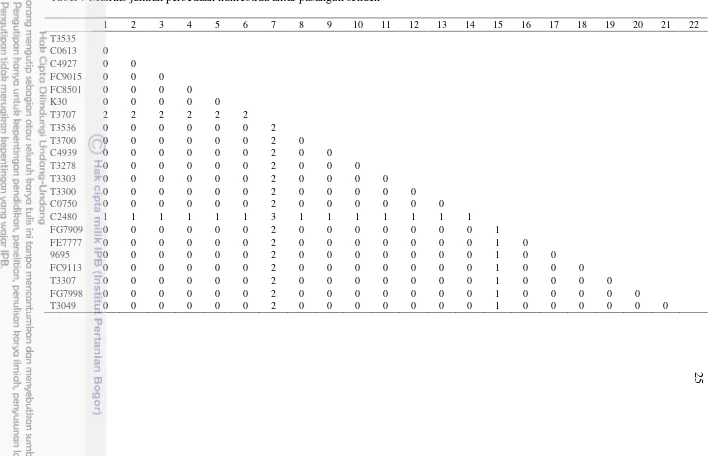
menunjukkan jumlah perbedaan nukleotida antar pasangan sekuen promotor berkisar 0 hingga 3 nukleotida dengan rataan 0,273 nukleotida dan keragaman nukleotida (π) 0,000387. Sekuen dengan perbedaan nukleotida paling banyak adalah yang dimiliki hewan T3707 dan C2480. Sekuen C3707 berbeda 3 nukleotida dengan sekuen C2480 dan berbeda 2 nukleotida dengan sekuen lainnya. Pasangan sekuen dengan perbedaan nukleotida 0 menunjukkan bahwa kedua sekuen tersebut identik. Tabel 7 memperlihatkan perbedaan nukleotida antar pasangan sekuen. Jarak genetik yang diperoleh berdasarkan analisis pairwise distance menggunakan model Kimura 2 Parameter berkisar 0,000 (0%) hingga 0,004 (0,4%). Pasangan sekuen identik memiliki jarak genetik 0,0%, sedangkan pasangan sekuen dengan 3 perbedaan nukleotida memiliki jarak genetik 0,4%.
24
Uji pola substitusi yang teramati untuk pasangan sekuen menggunakan indeks disparitas menghasilkan nilai P yang lebih dari 0,05. Nilai P yang lebih dari 0,05 menunjukkan tidak ada perbedaan pola substitusi yang teramati untuk pasangan sekuen (homogenitas pola substitusi). Hal ini berarti perbedaan nukleotida antar pasangan sekuen tidak signifikan. Tabel 8 memperlihatkan uji homogenitas pola substitusi antar pasangan sekuen.
[image:40.595.57.445.40.802.2]Secara keseluruhan, promotor gen LDLR monyet ekor panjang menunjukkan keragaman genetik (komposisi nukleotida, jumlah perbedaan nukleotida, π, jarak genetik, pola substitusi) yang sangat rendah. Diantara komponen keragaman genetik, π merupakan parameter yang akurat untuk menggambarkan keragaman genetik karena tidak tergantung pada besarnya sampel dan panjangnya DNA (Nei, 1987; Hartl dan Clark, 1989). Hal ini memberi peluang bagi penggunaan sampel kecil untuk menggambarkan kondisi populasi yang sebenarnya. π promotor gen LDLR yang diperoleh (0,000387) lebih kecil dibandingkan π promotor gen lain pada monyet ekor panjang, seperti gen TNF-α yang memiliki π 0,000600 dan rataan jumlah perbedaan nukleotida antar pasangan 0,53 (Flynn et al. 2009).
Tabel 6 Komposisi nukleotida sekuen promotor
Hewan (Tatto)
Jumlah nukleotida
(pb)
Komposisi nukleotida (%)
T C A G
T 4927 705 25,2 20,7 31,2 22,8 F C8501 705 25,2 20,7 31,2 22,8
K 30 705 25,2 20,7 31,2 22,8
T 3707 705 25,5 20,6 31,1 22,8 T 3535 705 25,2 20,7 31,2 22,8
9695 705 25,2 20,7 31,2 22,8
C 0613 705 25,2 20,7 31,2 22,8 T 3049 705 25,2 20,7 31,2 22,8 T 3536 705 25,2 20,7 31,2 22,8 T 3700 705 25,2 20,7 31,2 22,8 C 4939 705 25,2 20,7 31,2 22,8 T 3278 705 25,2 20,7 31,2 22,8 T 3303 705 25,2 20,7 31,2 22,8 FC 9015 705 25,2 20,7 31,2 22,8 FE 7777 705 25,2 20,7 31,2 22,8 T 3307 705 25,2 20,7 31,2 22,8 T 3300 705 25,2 20,7 31,2 22,8 FG 7909 705 25,2 20,7 31,2 22,8 C 0750 705 25,2 20,7 31,2 22,8 FG 7998 705 25,2 20,7 31,2 22,8 C 2480 705 25,2 20,7 31,1 23,0
FC 9113 705 25,2 20,7 31,2 22,8
25
Tabel 7 Matriks jumlah perbedaan nukleotida antar pasangan sekuen
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 T3535
C0613 0 C4927 0 0 FC9015 0 0 0 FC8501 0 0 0 0 K30 0 0 0 0 0 T3707 2 2 2 2 2 2 T3536 0 0 0 0 0 0 2 T3700 0 0 0 0 0 0 2 0 C4939 0 0 0 0 0 0 2 0 0 T3278 0 0 0 0 0 0 2 0 0 0 T3303 0 0 0 0 0 0 2 0 0 0 0 T3300 0 0 0 0 0 0 2 0 0 0 0 0 C0750 0 0 0 0 0 0 2 0 0 0 0 0 0 C2480 1 1 1 1 1 1 3 1 1 1 1 1 1 1 FG7909 0 0 0 0 0 0 2 0 0 0 0 0 0 0 1 FE7777 0 0 0 0 0 0 2 0 0 0 0 0 0 0 1 0 9695 0 0 0 0 0 0 2 0 0 0 0 0 0 0 1 0 0 FC9113 0 0 0 0 0 0 2 0 0 0 0 0 0 0 1 0 0 0 T3307 0 0 0 0 0 0 2 0 0 0 0 0 0 0 1 0 0 0 0 FG7998 0 0 0 0 0 0 2 0 0 0 0 0 0 0 1 0 0 0 0 0 T3049 0 0 0 0 0 0 2 0 0 0 0 0 0 0 1 0 0 0 0 0 0
26
Tabel 8Uji homogenitas pola substitusi antar pasangan sekuen
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 T3535
C0613 1,000 C4927 1,000 1,000 FC9015 1,000 1,000 1,000 FC8501 1,000 1,000 1,000 1,000 K30 1,000 1,000 1,000 1,000 1,000 T3707 0,444 0,430 0,380 0,414 0,432 0,448 T3536 1,000 1,000 1,000 1,000 1,000 1,000 0,386 T3700 1,000 1,000 1,000 1,000 1,000 1,000 0,466 1,000 C4939 1,000 1,000 1,000 1,000 1,000 1,000 0,424 1,000 1,000 T3278 1,000 1,000 1,000 1,000 1,000 1,000 0,410 1,000 1,000 1,000 T3303 1,000 1,000 1,000 1,000 1,000 1,000 0,408 1,000 1,000 1,000 1,000 T3