ANALISIS KOMPOSISI ASAM LEMAK DAN IDENTIFIKASI
POSISI ASAM LAURAT DALAM MINYAK KELAPA MURNI
DAN MINYAK INTI SAWIT
SKRIPSI
OLEH:
LIDA JAYANTI KARO KARO NIM 081501028
PROGRAM STUDI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
ANALISIS KOMPOSISI ASAM LEMAK DAN IDENTIFIKASI
POSISI ASAM LAURAT DALAM MINYAK KELAPA MURNI
DAN MINYAK INTI SAWIT
SKRIPSI
Diajukan untuk melengkapi salah satu syarat untuk memperoleh gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara OLEH:
LIDA JAYANTI KARO KARO NIM 081501028
PROGRAM STUDI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PENGESAHAN SKRIPSI
ANALISIS KOMPOSISI ASAM LEMAK DAN IDENTIFIKASI
POSISI ASAM LAURAT DALAM MINYAK KELAPA MURNI
DAN MINYAK INTI SAWIT
OLEH :
LIDA JAYANTI KARO KARO NIM 081501028
Dipertahankan di hadapan Panitia Penguji Skripsi Fakultas Farmasi Universitas Sumatera Utara
Pada Tanggal : Agustus 2012
Pembimbing I, Panitia Penguji,
Prof. Dr. Jansen Silalahi, M.App.Sc., Apt. Dr. Ginda Haro, M.Sc., Apt. NIP 195006071979031001 NIP 195108161980031002
Pembimbing II, Prof. Dr. Jansen Silalahi, M.App.Sc., Apt. NIP 195006071979031001
Prof. Dr. Siti Morin Sinaga, M.Sc., Apt. Drs. Immanuel S. Meliala, M.Si., Apt. NIP 1950082819760320021 NIP 195001261983031002
Dra. Saleha Salbi, M.Si., Apt. NIP 194909061980032001
Medan, Agustus 2012 Fakultas Farmasi
Universitas Sumatera Utara Dekan,
KATA PENGANTAR
Puji dan syukur kehadirat Tuhan Yang Maha Esa, karena limpahan
rahmat, kasih dan karunianNya, sehingga penulis dapat menyelesaikan skripsi ini.
Penelitian ini bertujuan untuk melakukan analisis komposisi asam lemak dan
identifikasi posisi asam laurat dalam minyak kelapa murni dan minyak inti sawit.
Skripsi ini diajukan sebagai salah satu syarat untuk memperoleh gelar sarjana
farmasi pada Fakultas Farmasi Universitas Sumatera Utara.
Pada kesempatan ini penulis mengucapkan terima kasih yang tulus dan ikhlas
kepada Bapak Prof. Dr. Sumadio Hadisahputra., Apt., selaku Dekan Fakultas
Farmasi USU Medan yang telah memberikan fasilitas sehingga penulis dapat
menyelesaikan pendidikan. Ibu Dra. Masfria, M.S., Apt., selaku penasehat
akademis yang telah memberikan bimbingan kepada penulis. Bapak Prof. Dr.
Jansen Silalahi, M.App.Sc., Apt., dan Ibu Prof. Dr. Siti Morin Sinaga, M.Sc.,
Apt., selaku pembimbing yang telah memberikan waktu, bimbingan dan nasehat
selama penelitian hingga selesainya penyusunan skripsi ini. Bapak Dr. Ginda
Haro, M.Sc., Apt., Bapak Drs. Immanuel S. Meliala, M.Si., Apt., dan Ibu Dra.
Saleha Salbi, M.Si., Apt., selaku dosen penguji yang telah memberikan kritik,
saran dan arahan kepada penulis dalam menyelesaikan skripsi ini. Bapak dan Ibu
staf pengajar Fakultas Farmasi USU Medan yang telah mendidik selama
perkuliahan. Bapak kepala Laboratorium Penelitian yang telah memberikan
bantuan dan fasilitas selama penulis melakukan penelitian.
Penulis juga mengucapkan terima kasih dan penghargaan yang tiada terhingga
kepada Ayahanda dan Ibunda tercinta, Tahan Karo Karo Kacaribu dan Ibunda
kesuksesan penulis, juga kepada kakak dan adikku yang selalu setia memberi
doa, dorongan, dan motivasi selama penulis melakukan penelitian.
Penulis menyadari bahwa penulisan skripsi ini masih belum sempurna, sehingga
penulis mengharapkan kritik dan saran yang membangun untuk
penyempurnaannya. Harapan saya semoga skripsi ini dapat bermanfaat bagi ilmu
pengetahuan kefarmasian.
Medan, Agustus 2012 Penulis
ANALISIS KOMPOSISI ASAM LEMAK DAN IDENTIFIKASI POSISI ASAM LAURAT DALAM MINYAK KELAPA MURNI
DAN MINYAK INTI SAWIT. ABSTRAK
Nilai gizi dan sifat biokimia suatu minyak ditentukan berdasarkan komposisi asam lemak pada minyak dan posisi asam lemak pada molekul triasilgliserol (TAG). Tujuan penelitian ini adalah untuk mengevaluasi komposisi minyak kelapa murni (virgin coconut oil = VCO) dan minyak inti sawit (palm kernel oil = PKO) berdasarkan komposisi asam lemak jenuh (saturated fatty acid
= SFA), asam lemak tak jenuh tunggal (monounsaturated fatty acid = MUFA) dan asam lemak tak jenuh jamak (polyunsaturated fatty acid = PUFA) serta untuk mengkaji kandungan asam laurat pada posisi sn-2 dalam VCO dan PKO.
VCO yang digunakan dalam penelitian ini adalah VCO yang di produksi oleh Noery ViCO Lhokseumawe dan PKO oleh PT. Multimas Nabati Asahan. Komposisi asam lemak total dianalisis dengan Kromatografi Gas. Nilai gizi dari lemak ditentukan dengan menghitung persen penyimpangan dari 33,33% dari SFA, MUFA, PUFA. Distribusi asam laurat pada TAG dilakukan dengan menghidrolisis VCO dan PKO menggunakan enzim lipase yang spesifik pada posisi sn-1,3 sehingga dihasilkan asam lemak bebas dan 2-monoasilgliserol. Kemudian asam lemak bebas dianalisis dengan Kromatografi Gas. Nilai distribusi asam laurat pada posisi sn-2 adalah pengurangan total asam laurat pada TAG dengan komposisi asam laurat bebas dari posisi sn-1,3.
Hasil analisis menunjukkan adanya penyimpangan dari nilai nilai gizi dari komposisi asam lemak pada VCO dan PKO berturut-turut yaitu 118,55% dan 95,29%. Analisis posisi asam laurat pada sn-2 dari VCO dan PKO menunjukkan distribusi asam laurat pada posisi sn-2 yaitu 48,33% dan 48,59%.
ANALYSIS OF FATTY ACID COMPOSITION AND IDENTIFICATION OF LAURIC ACID POSITION ON VIRGIN COCONUT OIL
AND PALM KERNEL OIL
ABSTRACT
Nutritional value and biochemical properties of oil are influenced by fatty acid composition of oil and fatty acid position on the triacylglycerol (TAG). The purpose of this study was to evaluate the nutritional value of virgin coconut oil (VCO) and palm kernel oil (PKO) based on the ratio of saturated fatty acid (SFA), monounsaturated fatty acid (MUFA) and polyunsaturated fatty acid (PUFA) and to assess lauric acid distribution in sn-2 position on VCO and PKO.
VCO that was used in this study was produced by the Noery ViCO Lhokseumawe and PKO by PT. Multimas Nabati Asahan.The nutritional value of fat was determine by the deviation percentage from 33,33% of each group SFA, MUFA, PUFA. Composition of total fatty acid was analyzed by Gas Chromatography. Distribution of lauric acid in TAG was determined by hydrolyzing the VCO and PKO with specific lipase enzyme active at position sn -1,3 generating freed fatty acid and 2-monoacylglycerol. Then the free fatty acid was analyzed by Gas Chromatography and the distribution of lauric acid at the sn -2 position was the difference between total lauric acids in TAG and free lauric acid composition of sn-1,3 position.
The result showed that the nutritional value of VCO and PKO were 118.55% and 95.29% deviated from 33.33%. The distribution of lauric acid in sn -2 position on VCO and PKO showed 48.33% and 48.59%.
DAFTAR ISI
Halaman
JUDUL ... ... i
HALAMAN JUDUL ... ... ii
PENGESAHAN SKRIPSI ... ... iii
KATA PENGANTAR ... iv
ABSTRAK ... ... vi
ABSTRACT ... ... vii
DAFTAR ISI ... viii
DAFTAR GAMBAR ... x
DAFTAR TABEL ... xi
DAFTAR LAMPIRAN ... xii
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 3
1.3 Hipotesis ... ... 3
1.4 Tujuan Penelitian ... 3
1.5 Manfaat Penelitian ... 3
BAB II TINJAUAN PUSTAKA ... 4
2.1 Minyak Kelapa Murni dan Minyak Inti Sawit ... 4
2.2 Asam Lemak ... 6
2.3 Lemak ... 7
2.4 Metabolisme Lemak ... 8
2.6 Aktivitas Antibakteri Asam Laurat dan Monolaurin ... 13
2.7 Analisis Asam Lemak ... 15
BAB III METODE PENELITIAN ... 17
3.1 Alat ... 17
3.2 Bahan ... 17
3.3 Pembuatan Pereaksi ... 17
3.3.1 Pembuatan Na Metanolik 0,5N ... 17
3.3.2 Pembuatan larutan NaCl Jenuh ... 18
3.3.3 Pembuatan Larutan Standar Metil Ester ... 18
3.4 Prosedur Penelitian ... 18
3.4.1 Pengambilan Sampel ... 18
3.4.2 Analisis Komposisi Asam Lemak pada Sampel ... 18
3.4.3 Cara Evaluasi Nilai gizi ... 19
3.4.4 Penetuan Distribusi Asam Laurat pada Posisi sn-2 .... 19
BAB IV HASIL DAN PEMBAHASAN ... 21
4.1 Sampel ... 21
4.2 Komposisi Asam Lemak Pada VCO dan PKO ... 21
4.3 Nilai Gizi VCO dan PKO ... 23
4.4 Distribusi Asam Laurat pada VCO dan PKO ... 25
BAB V KESIMPULAN DAN SARAN ... 27
5.1 Kesimpulan ... 27
5.1 Saran ... 27
DAFTAR PUSTAKA ... 28
DAFTAR GAMBAR
Halaman Gambar 2.1 Struktur Kimia Lemak trigliserida ... 7
Gambar 2.2 Metabolisme Dan Transportasi Triasilgliserol Pada
Manusia ... 8
Gambar 2.3 Reaksi Hidrolisis Enzimatik Triasilgliserol ... 11
DAFTAR TABEL
Halaman
Tabel 2.1 Komposisi Asam Lemak VCO dan PKO ... 5
Tabel 2.2 Klasifikasi Enzim Lipase Berdasarkan Spesifikasinya ... 11
Tabel 2.3 Distribusi Asam Palmitat pada Posisi sn-2 ... 12
Tabel 4.1 Komposisi Asam Lemak VCO dan PKO ... 22
Tabel 4.2 Nilai Gizi VCO dan PKO ... 24
DAFTAR LAMPIRAN
Halaman Lampiran 1. Bagan Alir Pembuatan Metil Ester Asam Lemak Sebelum
Hidrolisis ... 30
Lampiran 2. Kondisi Alat Kromatografi Gas ... 31
Lampiran 3. Bagan Alir Hidrolisis VCO dan PKO ... 32
Lampiran 4. Bagan Alir Pembuatan Metil Ester Asam Lemak Sesudah Hidrolisis ... 33
Lampiran 5. Karakteristik Kromatogram Standar Metil Ester Asam Lemak Sebelum Hidrolisis ... 34
Lampiran 6. Kromatogram I VCO Sebelum Hidrolisis ... 35
Lampiran 7. Kromatogram II VCO Sebelum Hidrolisis ... 36
Lampiran 8. Kromatogram III VCO Sebelum Hidrolisis ... 37
Lampiran 9. Kromatogram I PKO Sebelum Hidrolisis ... 38
Lampiran 10. Kromatogram II PKO Sebelum Hidrolisis ... 39
Lampiran 11. Kromatogram III PKO Sebelum Hidrolisis ... 40
Lampiran 12. Perhitungan Nilai Gizi VCO dan PKO ... 41
Lampiran 13. Daftar Spesifikasi Enzim Lipase ... 42
Lampiran 14. Kromatogram I VCO Sesudah Hidrolisis ... 43
Lampiran 15. Kromatogram II VCO Sesudah Hidrolisis ... 44
Lampiran 16. Kromatogram III VCO Sesudah Hidrolisis ... 45
Lampiran 17. Kromatogram I PKO Sesudah Hidrolisis ... 46
Lampiran 18. Kromatogram II PKO Sesudah Hidrolisis ... 47
Lampiran 20. Perhitungan Asam Laurat pada Posisi Sn-2 ... 49
Lampiran 21. Hasil Perhitungan Berat Asam Laurat Sebelum Hidrolisis ... 50
Lampiran 22. Hasil Perhitungan Berat Asam Laurat Sesudah Hidrolisis ... 51
Lampiran 23. Perhitungan Distribusi Asam Laurat pada Posisi Sn-2 ... 52
Lampiran 24. Perhitungan Statistik Berat Asam Laurat ... 53
Lampiran 25. Gambar Sampel Minyak ... 58
Lampiran 26. Gambar Kromatografi Gas ... 59
ANALISIS KOMPOSISI ASAM LEMAK DAN IDENTIFIKASI POSISI ASAM LAURAT DALAM MINYAK KELAPA MURNI
DAN MINYAK INTI SAWIT. ABSTRAK
Nilai gizi dan sifat biokimia suatu minyak ditentukan berdasarkan komposisi asam lemak pada minyak dan posisi asam lemak pada molekul triasilgliserol (TAG). Tujuan penelitian ini adalah untuk mengevaluasi komposisi minyak kelapa murni (virgin coconut oil = VCO) dan minyak inti sawit (palm kernel oil = PKO) berdasarkan komposisi asam lemak jenuh (saturated fatty acid
= SFA), asam lemak tak jenuh tunggal (monounsaturated fatty acid = MUFA) dan asam lemak tak jenuh jamak (polyunsaturated fatty acid = PUFA) serta untuk mengkaji kandungan asam laurat pada posisi sn-2 dalam VCO dan PKO.
VCO yang digunakan dalam penelitian ini adalah VCO yang di produksi oleh Noery ViCO Lhokseumawe dan PKO oleh PT. Multimas Nabati Asahan. Komposisi asam lemak total dianalisis dengan Kromatografi Gas. Nilai gizi dari lemak ditentukan dengan menghitung persen penyimpangan dari 33,33% dari SFA, MUFA, PUFA. Distribusi asam laurat pada TAG dilakukan dengan menghidrolisis VCO dan PKO menggunakan enzim lipase yang spesifik pada posisi sn-1,3 sehingga dihasilkan asam lemak bebas dan 2-monoasilgliserol. Kemudian asam lemak bebas dianalisis dengan Kromatografi Gas. Nilai distribusi asam laurat pada posisi sn-2 adalah pengurangan total asam laurat pada TAG dengan komposisi asam laurat bebas dari posisi sn-1,3.
Hasil analisis menunjukkan adanya penyimpangan dari nilai nilai gizi dari komposisi asam lemak pada VCO dan PKO berturut-turut yaitu 118,55% dan 95,29%. Analisis posisi asam laurat pada sn-2 dari VCO dan PKO menunjukkan distribusi asam laurat pada posisi sn-2 yaitu 48,33% dan 48,59%.
ANALYSIS OF FATTY ACID COMPOSITION AND IDENTIFICATION OF LAURIC ACID POSITION ON VIRGIN COCONUT OIL
AND PALM KERNEL OIL
ABSTRACT
Nutritional value and biochemical properties of oil are influenced by fatty acid composition of oil and fatty acid position on the triacylglycerol (TAG). The purpose of this study was to evaluate the nutritional value of virgin coconut oil (VCO) and palm kernel oil (PKO) based on the ratio of saturated fatty acid (SFA), monounsaturated fatty acid (MUFA) and polyunsaturated fatty acid (PUFA) and to assess lauric acid distribution in sn-2 position on VCO and PKO.
VCO that was used in this study was produced by the Noery ViCO Lhokseumawe and PKO by PT. Multimas Nabati Asahan.The nutritional value of fat was determine by the deviation percentage from 33,33% of each group SFA, MUFA, PUFA. Composition of total fatty acid was analyzed by Gas Chromatography. Distribution of lauric acid in TAG was determined by hydrolyzing the VCO and PKO with specific lipase enzyme active at position sn -1,3 generating freed fatty acid and 2-monoacylglycerol. Then the free fatty acid was analyzed by Gas Chromatography and the distribution of lauric acid at the sn -2 position was the difference between total lauric acids in TAG and free lauric acid composition of sn-1,3 position.
The result showed that the nutritional value of VCO and PKO were 118.55% and 95.29% deviated from 33.33%. The distribution of lauric acid in sn -2 position on VCO and PKO showed 48.33% and 48.59%.
BAB I PENDAHULUAN
1.1Latar Belakang
Nilai gizi suatu minyak atau lemak dapat ditentukan berdasarkan dua
aspek yaitu komposisi asam lemak pada minyak atau lemak dan posisi asam
lemak pada molekulnya. Komposisi asam lemak yang ideal dari pangan,
sebaiknya mempunyai perbandingan asam lemak jenuh (saturated fatty acid = SFA), asam lemak tak jenuh tunggal (monounsaturated fatty acid = MUFA), dan asam lemak tak jenuh jamak (polyunsaturated fatty acid = PUFA) adalah 1:1:1 (Silalahi, 2011).
Potensi medis dari produk-produk kelapa pertama kali diidentifikasi oleh
Jon Kabara di tahun 70-an, yaitu aktivitas antibakteri, antivirus dan antijamur dari
asam lemak rantai sedang (Medium Chain Fatty Acid, MCFA), khususnya asam laurat (C12:0) dalam bentuk monogliserida (monolaurin atau ML) (Kabara, et al.,
1972; Conrado, 2000). Produk olahan kelapa seperti Minyak Kelapa Murni
(Virgin Coconut Oil, VCO) dan Minyak inti sawit (Palm kernel Oil, PKO) aman dikonsumsi oleh masyarakat. Mutu VCO dan PKO ditentukan dari MCFA dan
asam laurat yang terkandung didalamnya. Kandungan MCFA dan kadar asam
laurat dipengaruhi oleh varietas kelapa, tinggi tempat tumbuh, dan teknologi
proses pembuatannya. MCFA mudah diserap ke dalam sel kemudian ke dalam
mitokondria, sehingga metabolisme meningkat. Dengan peningkatan metabolisme
maka sel-sel bekerja lebih efisien membentuk sel-sel baru serta mengganti sel-sel
Aktivitas antibakteri MCFA terbaik adalah dalam bentuk bebas dan
monogliserida. Dari semua asam lemak jenuh, asam laurat memiliki aktivitas
antimikroba lebih baik dibandingkan dengan asam kaprilat (C8:0), asam kaprat
(C10:0), dan asam miristat (C14:0). Secara umum dilaporkan bahwa asam lemak
dan monogliserida menginaktivasi bakteri dengan cara merusak membran plasma
(lipid bilayer) dari bakteri tersebut (Enig, 1996; Kabara, et al., 1972).
Menurut Permata (2012), aktivitas antibakteri dari trigliserida yang
dihidrolisis dengan bantuan enzim lebih efektif dibandingkan dengan hidrolisis
dengan penyabunan. Hasil hidrolisis dengan penyabunan dapat berupa
monogliserida, digliserida atau bahkan trigliserida sama sekali tidak pecah karena
jumlah alkali tidak mencukupi untuk menyabunkan semua trigliserida, sehingga
dapat disebut hidrolisis parsial.
Untuk memperoleh monogliserida dari trigliserida yang terkandung dalam
VCO dan PKO adalah dengan melakukan hidrolisis menggunakan enzim yang
spesifik bekerja hanya untuk menghidrolisis secara parsial yaitu menghidrolisis
trigliserida pada posisi sn-1 dan 3. Enzim yang spesifik bekerja pada posisi sn-1 dan 3 adalah ensim lipase tetapi tidak menghidrolisis asil pada posisi sn-2, sehingga menghasilkan 2-monoasilgliserol (2-MAG) dan asam lemak bebas.
Asam lemak bebas kemudian diubah dalam bentuk metil ester dan diinjeksikan ke
Kromatografi Gas sehingga dapat diketahui persentase asam laurat pada posisi sn -2 dengan cara pengurangan asam lemak total laurat didalam triasilgliserol dan
asam lemak bebas dari posisi sn-1,3(Silalahi, 2011).
Tujuan penelitian ini adalah untuk mengevaluasi komposisi VCO dan
1.2Perumusan Masalah
Berdasarkan uraian dari latar belakang di atas, maka perumusan masalah
adalah:
a. Apakah VCO dan PKO mempunyai komposisi SFA, MUFA, PUFA yang tidak
ideal?
b. Bagaimanakah distribusi asam laurat pada posisi sn-2 dalam VCO dan PKO?
1.3Hipotesis
Hipotesis dari penelitian ini adalah sebagai berikut:
a. VCO dan PKO mempunyai komposisi SFA, MUFA, PUFA yang tidak ideal.
b. Distribusi asam laurat pada molekul lemak VCO dan PKO paling banyak pada
posisi sn-2.
1.4Tujuan Penelitian
Tujuan penelitian ini adalah untuk:
a. Mengevaluasi komposisi VCO dan PKO berdasarkan komposisi SFA, MUFA,
PUFA.
b. Mengkaji kandungan asam laurat pada posisi sn-2 dalam VCO dan PKO. 1.5Manfaat Penelitian
Diharapkan penelitian ini dapat:
a. Memberikan informasi tentang komposisi SFA, MUFA, PUFA dari VCO dan
PKO.
BAB II
TINJAUAN PUSTAKA
2.1 Minyak Kelapa Murni dan Minyak Inti Sawit
Kelapa merupakan tanaman perkebunan yang mampu tumbuh dan
berproduksi dengan baik bila ditanam pada ketinggian 0-600 m dari permukaan
laut dengan suhu rata-rata 25o
Proses produksi VCO yang tidak menggunakan pemanasan yang tinggi
bukan hanya menghasilkan MCFA yang tinggi, tetapi juga dapat mempertahankan
keberadaan vitamin E dan enzim-enzim yang terkandung dalan daging buah
kelapa. VCO yang dibuat dari kelapa segar berwarna putih murni ketika
minyaknya dipadatkan dan jernih kristal seperti air ketika dicairkan (Syah, 2005). C dan kelembapan udara 80-90%. Daerah ini
umumnya dilewati garis katulistiwa sehingga beriklim tropis (Setiaji dan Surip,
2002). Minyak kelapa murni (Virgin Coconut Oil, VCO) merupakan produk olahan buah kelapa. Minyak kelapa murni adalah minyak yang diperoleh dari
daging buah kelapa (Cocos nucifera L) tua yang segar dan diproses dengan diperas dengan atau tanpa penambahan air, tanpa pemanasan atau pemanasan
tidak lebih dari 60°C dan aman dikonsumsi manusia (Badan Standardisasi
Nasional, 2008).
VCO berbeda dengan lemak dan minyak pada umumnya karena
mempunyai kandungan asam lemak jenuh yang tinggi yaitu sekitar 90% asam
lemak jenuh yang terdiri dari asam laurat, miristat, dan palmitat. Kandungan asam
lemak jenuh dalam VCO didominasi oleh asam laurat dan asam miristat.
Tingginya asam lemak jenuh yang dikandungnya menyebabkan VCO tahan
Kelapa sawit (Elaeis guineensis Jacq.) pada bagian buahnya terdiri dari eksokarp (kulit paling luar), mesokarp (serabut, mirip serabut kelapa), endokarp
(tempurung), dan kernel (inti sawit). Pengolahan bagian serabutnya (mesokarp)
dengan cara ekstraksi dapat menghasilkan minyak sawit (crude palm oil), sedangkan pengolahan bagian kernel (inti) dapat menghasilkan minyak inti sawit
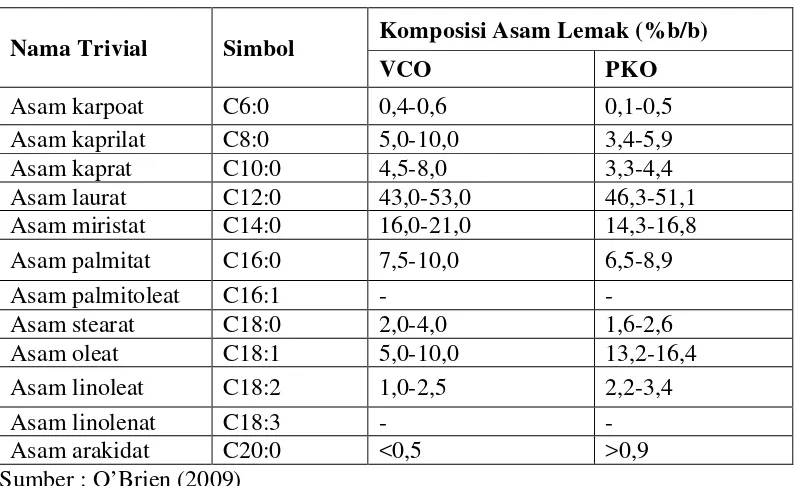
(palm kernel oil,PKO) (Haryati, 1999). Komposisi asam lemak pada VCO dan PKO dapat dilihat pada Tabel 2.1.
Tabel 2.1 Komposisi Asam Lemak Dari VCO dan PKO
Nama Trivial Simbol Komposisi Asam Lemak (%b/b)
VCO PKO
Asam karpoat C6:0 0,4-0,6 0,1-0,5 Asam kaprilat C8:0 5,0-10,0 3,4-5,9 Asam kaprat C10:0 4,5-8,0 3,3-4,4 Asam laurat C12:0 43,0-53,0 46,3-51,1 Asam miristat C14:0 16,0-21,0 14,3-16,8 Asam palmitat C16:0 7,5-10,0 6,5-8,9 Sumber : O’Brien (2009)
VCO dan PKO berbeda dengan lemak dan minyak pada umumnya karena
mempunyai kandungan asam lemak jenuh yang tinggi. VCO dan PKO
mengandung sekitar 90% asam lemak jenuh yang terdiri dari asam laurat,
miristat., dengan kandungan SFA sehingga VCO dan PKO memadat dan memutih
pada suhu 26°C dan kembali mencair pada suhu 29°C (Syah, 2005; O’Brien,
2009).
Asam lemak adalah asam monokarboksilat rantai lurus tanpa cabang yang
mengandung atom karbon genap mulai dari C-4, tetapi yang paling banyak adalah
C-16 dan C-18.Asam lemak digolongkan menjadi tiga yaitu berdasarkan panjang
rantai asam lemak, tingkat kejenuhan, dan bentuk isomer geometrisnya.
Berdasarkan panjang rantai asam lemak dibagi atas; asam lemak rantai pendek
(short chain fatty acids, SCFA) mempunyai atom karbon lebih rendah dari 8, asam lemak rantai sedang mempunyai atom karbon 8 sampai 12 (medium chain fatty acids, MCFA) dan asam lemak rantai panjang mempunyai atom karbon 14 atau lebih (long chain fatty acids, LCFA). Semakin panjang rantai C yang dimiliki asam lemak, maka titik lelehnya akan semakin tinggi (Silalahi, 2000; Silalahi dan
Tampubolon, 2002).
Berdasarkan tingkat kejenuhan asam lemak dibagi atas; asam lemak jenuh
(SFA) karena tidak mempunyai ikatan rangkap, asam lemak tak jenuh tunggal
(MUFA) hanya memiliki satu ikatan rangkap dan asam lemak tak jenuh jamak
(PUFA) memiliki lebih dari satu ikatan rangkap. Semakin banyak ikatan rangkap
yang dimiliki asam lemak, maka semakin rendah titik lelehnya (Silalahi, 2000;
Silalahi dan Tampubolon, 2002).
Berdasarkan bentuk isomer geometrisnya asam lemak dibagi atas asam
lemak tak jenuh bentuk cis dan trans. Pada isomer geometris, rantai karbon
melengkung ke arah tertentu pada setiap ikatan rangkap. Bagian rantai karbon
akan saling mendekat atau saling menjauh. Jika saling mendekat disebut isomer
cis (berarti berdampingan), dan apabila saling menjauh disebut trans (berarti
berseberangan). Asam lemak alami biasanya dalam bentuk cis. Isomer trans
biasanya terbentuk selama reaksi kimia seperti hidrogenasi atau oksidasi. Titik
O
tak jenuh bentuk cis karena orientasi antar molekul dengan bentuk cis yang
membengkok tidak sempurna sedangkan asam lemak tak jenuh trans lurus sama
seperti bentuk asam lemak jenuh (Silalahi, 2000; Silalahi dan Tampubolon, 2002).
2.3 Lemak
Lipida adalah senyawa organik yang terdapat di dalam mahluk hidup yang
tidak larut di dalam air tetapi larut di dalam pelarut nonpolar seperti heksan,
dietileter. Komponen utama lipida adalah lemak, lebih 95% lipida adalah lemak.
Lemak adalah triester asam lemak dan gliserol. Nama kimia dari lemak adalah
triasilgliserol (TAG) dan nama lain yang sering digunakan adalah trigliserida
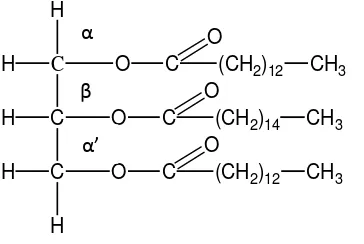
(McKee dan McKee, 2003).Struktur kimia trigliserida dapat dilihat pada Gambar
2.1 (Darmoyuwono, 2006; McKee dan McKee, 2003).
Gambar 2.1 Struktur Kimia trigliserida
Keterangan: R – C – disebut dengan gugus asil, yang terikat pada molekul
gliserol.
Setiap molekul triasilgliserol (TAG) atau trigliserida (TG) dapat
mengandung campuran dari tiga asam lemak yang berbeda atau semuanya sama.
Ketiga asam lemak ini teresterkan pada tiga posisi yang berbeda di dalam molekul
lemaknya. Distribusi atau posisi asam lemak dalam molekul lemak dapat
digolongkan berdasarkan stereospecific numbering (sn) atau atom karbon dalam molekul gliserol yakni sn-1, sn-2 dan sn-3 (McKee dan McKee, 2003).
2.4 Metabolisme Lemak
Metabolisme lemak dipengaruhi oleh panjang rantai asam lemak dan
posisi asam lemak didalam molekul TAG. Enzim lipase adalah sekelompok enzim
yang bertanggung jawab pada metabolisme lemak dalam pencernaan manusia.
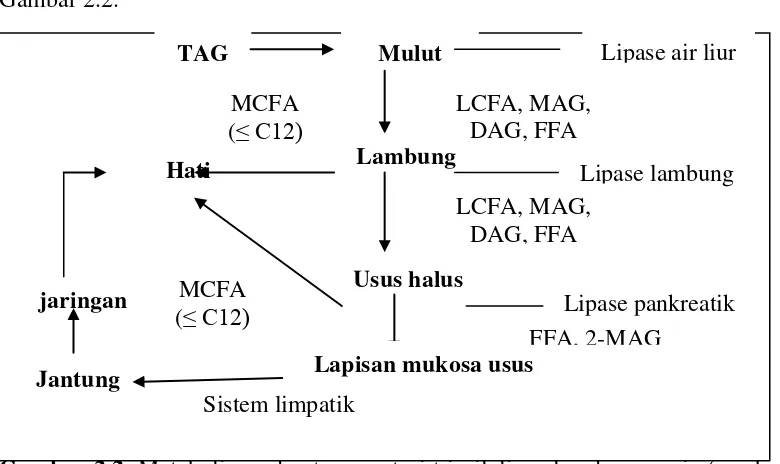
Metabolisme dan transportasi triasilgliserol pada manusia dapat dilihat pada
Gambar 2.2.
Gambar 2.2 Metabolisme dan transportasi triasilgliserol pada manusia (sumber: Willis et al., 1998)
Keterangan:
TAG (Triasilgliserol), DAG (Diasilgliserol) , MAG (Monoasilgliserol), MCFA (Medium chain fatty acid /asam lemak rantai sedang), LCFA (Long chain fatty acid/asam lemak rantai panjang), FFA (Free Fatty Acid /asam lemak bebas).
Ada tiga sumber lipase yang aktif menghidrolisa lemak sebelum
diabsorpsi. Enzim lipase pada manusia bekerja secara spesifik pada posisi sn-1 dan sn-3, dan tidak menghidrolisa asil pada posisi sn-2 atau pada atom karbon nomor 2. Pada dasarnya hidrolisa lemak dimulai oleh lingual lipase dalam mulut
TAG Mulut
Lambung
Usus halus
Lapisan mukosa usus Jantung
Sistem limpatik
Lipase air liur
terutama pada bayi tetapi aktivtas ini rendah pada orang dewasa. Enzim ini aktif
dalam bagian atas pencernaan, menghidrolisa lemak (TAG) menjadi
monoasilgliserol (MAG), diasilgliserol (DAG), dan asam lemak bebas. Selain
daripada itu lingual lipase cendrung akan menghidrolisa asam lemak rantai pendek dan sedang saja (Decker, 1996; Willis, et al., 1998).
Asam lemak rantai pendek dan sedang akan mudah berinteraksi dengan
medium berair sehingga dapat langsung diserap melalui lambung ke sirkulasi via
vena porta ke hati, dimana akan terjadi oksidasi dan menghasilkan kalori sehingga
tidak bersifat aterogenik seperti yang terjadi terhadap minyak kelapa (Willis, et
al., 1988; Willis dan Marangoni, 1999; Enig, 1996; Enig, 2010). Hal ini terutama penting pada pasien yang penyerapan lemak yang tidak baik (fat malabsorption) dan juga untuk menghasilkan energi yang cepat untuk bayi yang premature. Asam
lemak rantai pendek dan sedang juga dapat dimanfaatkan untuk mensuplai energi
yang cepat dalam otot karena transportasi ke mitokondria tidak memerlukan
carnitine (Willis dan Marangoni, 1999). Di dalam lambung lemak akan dihidrolisa
oleh lipase lambung (gastric lipase) yang juga aktif terhadap asam lemak rantai pendek dan sedang, kemudian dapat memasuki sirkulasi via vena porta juga
langsung ke hati. Lipase pankreas (pancreatic lipase) yang berada di dalam usus halus akan mengkataliser hidrolisa tahap terakhir dari lemak yang sedikit lebih
aktif terhadap asam lemak pada posisi sn-1. Lipase pankreas walaupun lebih cendrung terhadap asam lemak pendek dan sedang tetapi dapat juga
menghidrolisa asam lemak panjang yang berada pada posisi sn-1,3 (Silalahi, 2006).
Setelah hidrolisa asam lemak dan 2-MAG dalam bentuk misel bersama
sedang dalam bentuk 2-MAG diserap, bercampur dengan kilomikron, dan
diangkut melalui saluran limpha. Asam lemak jenuh rantai panjang dalam bentuk
bebasnya tidak atau sedikit saja diserap, karena titik leleh yang tinggi akan berupa
zat padat dan dapat bereaksi dengan kalsium dan magnesium membentuk garam
atau sabun yang tak larut dalam air. Oleh karena itu, diupayakan untuk
menempatkan asam lemak yang bermanfaat bagi kesehatan pada posisi sn-2 agar
absorbsinya lebih baik (Willis, et al., 1988; Willis dan Marangoni, 1999).
2.5 Penentuan Jenis Asam Lemak pada Posisi sn-2 pada Triasilgliserol
Enzim lipase sangat penting dalam metabolisme lemak dalam tubuh.
Proses pemecahan lemak (fat splitting) melepaskan asam lemak dari struktur triasilgliserol yang dapat terjadi dengan enzim lipase spesifik pada posisi sn
tertentu (Aehle, 2004). Reaksi hidrolisis dengan menggunakan enzim lipase lebih
efisien dan mudah dikontrol karena dan enzim lipase spesifik pada posisi tertentu
sehingga dapat mengubah produk lemak dan distribusi asam lemak sesuai dengan
yang diinginkan.
Apabila reaksi hidrolisis dilakukan dengan penggunaan zat kimia maka
akan menghasilkan produk lemak dengan distribusi asam lemak yang acak yaitu
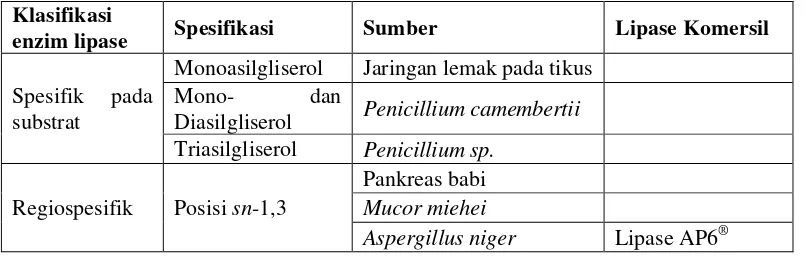
akan menghidrolisis pada semua posisi sn dalam produk lemak. Klasifikasi enzim lipase berdasarkan spesifikasinya dapat dilihat pada Tabel 2.2
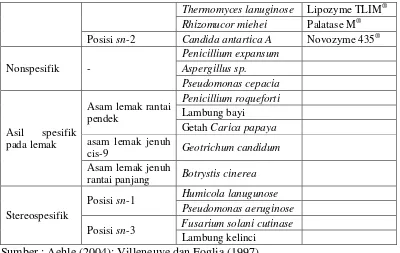
Tabel 2.2 Klasifikasi Enzim Lipase Berdasarkan Spesifikasinya
Klasifikasi
enzim lipase Spesifikasi Sumber Lipase Komersil
Spesifik pada substrat
Monoasilgliserol Jaringan lemak pada tikus
Mono- dan
Diasilgliserol Penicillium camembertii Triasilgliserol Penicillium sp.
Regiospesifik Posisi sn-1,3
Pankreas babi
Mucor miehei
Thermomyces lanuginose Lipozyme TLIM®
Rhizomucor miehei Palatase M® Posisi sn-2 Candida antartica A Novozyme 435®
Nonspesifik -
Asam lemak rantai pendek
Penicillium roqueforti
Lambung bayi Getah Carica papaya
asam lemak jenuh
cis-9 Geotrichum candidum
Asam lemak jenuh
rantai panjang Botrystis cinerea
Stereospesifik
Posisi sn-1 Humicola lanugunose
Pseudomonas aeruginose
Posisi sn-3 Fusarium solani cutinase Lambung kelinci
Sumber : Aehle (2004); Villeneuve dan Foglia (1997)
Prinsip dilakukan proses hidrolisis enzimatik bertujuan untuk
menghasilkan produk monogliserida, digliserida atau gliserol dan asam lemak
bebas dari posisi sn yang diinginkan dengan penambahan enzim lipase (Aehle, 2004). Reaksi hidrolisis enzimatik triasilgliserol dapat dilihat pada Gambar 2.3.
Gambar 2.3 Reaksi Hidrolisis Enzimatik Triasilgliserol (Sumber: Aehle, 2004) Menurut Silalahi (2011), penentuan asam palmitat pada posisi sn-2 dapat
dilakukan dengan menghidrolisis triasilgliserol secara enzimatik dengan enzim
lipase yang spesifik pada posisi sn-1,3 adalah dengan menghidrolisis triasilgliserol pada posisi sn-1,3 sehingga akan menghasilkan produk 2-MAG dan asam lemak bebas dari asam lemak pada posisi sn-1,3. Kemudian dipisahkan dengan larutan polar yang mengikat 2-MAG, ataupun disentrifugasi pada kecepatan dan waktu
posisi sn-1,3. Setelah terpisah, asam lemak bebas pada posisi sn-1,3 dimetilesterkan untuk diinjeksikan ke Kromatografi Gas. Hasil pengurangan total
asam lemak dan asam lemak bebas adalah nilai produk 2-MAG. Distribusi asam
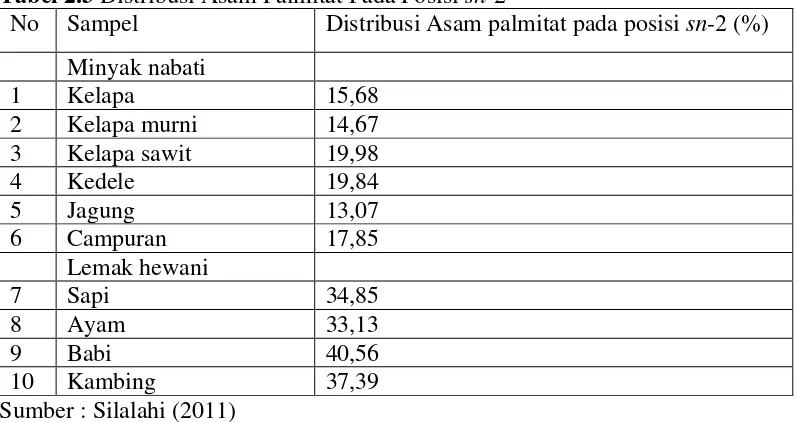
palmitat pada posisi sn-2 dapat dilihat pada Tabel 2.3. Tabel 2.3 Distribusi Asam Palmitat Pada Posisi sn-2
No Sampel Distribusi Asam palmitat pada posisi sn-2 (%) Minyak nabati Sumber : Silalahi (2011)
Berdasarkan perhitungan distribusi asam palmitat, maka dapat diperoleh
persentase nilai sn-2. Persentase asam palmitat pada minyak nabati yang terdistribusi pada posisi sn-2 lebih sedikit dibandingkan dengan lemak hewani. Asam lemak palmitat yang terdapat pada minyak nabati, dalam jumlah yang
terbanyak terdapat pada minyak kelapa sawit dan dalam jumlah terkecil terdapat
pada minyak jagung (Silalahi, 2011).
2.6 Aktivitas Antibakteri Asam Laurat dan Monolaurin
Monolaurin merupakan monoester yang terbentuk dari asam laurat yang
telah diteliti memiliki aktivitas antivirus, antibakteri dan antijamur. Asam laurat
merupakan komponen utama VCO dan PKO. Asam laurat juga banyak terdapat
dalam air susu ibu dan meningkatkan kekebalan tubuh bayi, itulah sebabnya bayi
kebal berbagai macam penyakit. Aktivitas antimikroba dari asam lemak
dipengaruhi oleh pH yang merupakan faktor penentu bakteri dapat mati atau
hanya terinaktivasi pH dari asam lemak rantai pendek (kaproat, kaprilat dan
kaprat) yang berfungsi baik sebagai antimikroba adalah 6,5 - 7,5, namun untuk
asam lemak rantai sedang (laurat dan miristat), pH minimum 6,5 sudah mampu
membunuh bakteri (Syah, 2005).
Menurut Permata (2012), VCO tidak memilki aktivitas antibakteri dan
hidrolisis parsial dapat meningkatkan daya hambat pertumbahan bakteri VCO,
baik itu hidrolisis dengan enzim (lipozim) maupun dengan NaOH (penyabunan).
Hasil yang paling baik ditunjukkan oleh hidrolisis dengan metode enzimatik
dengan lama inkubasi 12 jam. Peningkatan waktu inkubasi enzimatik sebanding
dengan peningkatan kandungan asam lemak bebas dalam VCO dan peningkatan
aktivitas antibakterinya. Semakin lama inkubasi maka semakin banyak asam
laurat dan monolaurin yang dihasilkan, sehingga aktivitas antibakteri semakin
meningkat. Hidrolisis menggunakan NaOH (penyabunan) meningkatkan
kandungan asam lemak bebas sebanding dengan peningkatan NaOH yang
digunakan dalam hidrolisis. Semakin banyak NaOH yang ditambahkan dalam
reaksi penyabunan, maka semakin banyak trigliserida yang tersabunkan. Sehingga
semakin tinggi kandungan asam lemak dalam VCO dan meningkatkan aktivitas
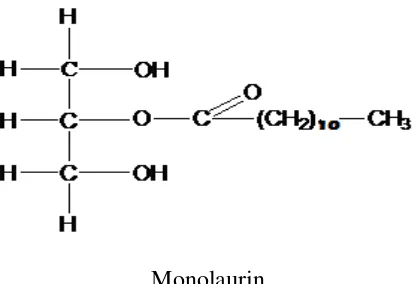
antibakteri dari VCO. Rumus struktur kimia asam laurat dan monolaurin dapat
dilihat pada Gambar 2.4.
C O
OH
Monolaurin
Gambar 2.4 Struktur Kimia Asam Laurat Dan Monolaurin
Lemak jenuh dalam minyak kelapa, seperti asam kaprat, dan asam laurat,
terbukti dapat meningkatkan sistem kekebalan tubuh karena minyak kelapa
berfungsi sebagai antivirus, antibakteri, antijamur, dan antiprotozoa. Asam laurat
dan monogliserida yang disebut monolaurin telah terbukti berperan sebagai
antivirus, khususnya virus yang berselubung lemak. Baik asam kaprat maupun
asam laurat di dalam minyak kelapa dapat mengatasi Candida albicans
(Darmoyuwono, 2006).
2.7 Analisis Asam Lemak
Asam lemak yang terdapat di dalam makanan dapat dianalisa
menggunakan kromatografi gas cair dengan menggunakan kolom kapiler, dalam
hal ini dapat dipisahkan isomer cis dan isomernya. Penelitian yang telah dilakukan terhadap berbagai jenis makanan untuk mengetahui jumlah asam lemak yaitu,
Satchithanandam, et al (2004) menganalisis 117 produk makanan berupa
margarin, kue dan crakers, produk kentang goreng, minyak nabati dan
shorthening, cereals, dan mayonnaise yang ada di Amerika dengan menggunakan kromatografi gas dan diperoleh hasil 30% produk makanan berupa roti dan kue
Kromatografi gas telah luas digunakan dalam metode analisa metil ester
asam lemak (fatty acid methyl ester/FAME). Kesuksesan pemisahan komposisi asam lemak dalam bentuk FAME dengan kromatografi gas bergantung pada
kondisi percobaan dari metode yang digunakan. Kebanyakan metode
kromatografi gas untuk mendeteksi asam lemakmenggunakan kolom kapiler yang
panjang dengan fase diam berupa senyawa yang kepolarannya tinggi. Pada
kondisi ini, pemisahan berdasarkan pada panjang rantai dari asam lemak, derajat
ketidakjenuhan, dan geometri serta posisi ikatan rangkapnya. Deretan elusi yang
diharapkan untuk asam lemak yang spesifik dengan panjang rantai yang sama
pada kolom yang kepolarannya tinggi yaitu sebagai berikut: bentuk jenuh
(saturated), bentuk tidak jenuh dengan satu ikatan rangkap (monounsaturated), bentuk tidak jenuh dengan dua ikatan rangkap (diunsaturated) (Moss dan Wilkening, 2005).
Berdasarkan (American Oil Chemists’ Society (AOCS), 1997), penentuan
kualitatif dan kuantitatif untuk saturated fatty acid (SFA), monounsaturated fatty acid (MUFA), dan polyunsaturated acid (PUFA) secara kromatografi gas dapat menggunakan kolom kapiler. AOCS Ce Ie-91 juga menetapkan bahwa kolom
yang dapat digunakan bisa pendek (50-60 m) atau panjang (100-120 m) dengan
fase diam yang kepolarannnya tinggi. Selain itu, detektor yang dapat digunakan
yaitu flame ionization detector (FID) dengan suhu pengoperasian 250 °C. Gas pembawa yang dapat digunakan yaitu helium, nitrogen, atau hidrogen. Metode
boron triflorida merupakan metode yang dapat digunakan untuk menghasilkan
asam lemak metil ester dari trigliserol minyak atau lemak (Moss dan Wilkening,
Metil ester asam lemak dari VCO dan PKO dibuat terlebih dahulu dengan
mereaksikan minyak dengan NaOH yang akan membentuk garam natrium asam
lemak, reaksi akan terus berlangsung hingga seluruh asam lemak lepas dari lemak.
Kemudian ke dalam garam natrium asam lemak ditambahkan BF3 14% dalam
metanol maka akan terbentuk metil ester asam lemak. Pembuatan metil ester asam
lemak menggunakan NaOH gunanya untuk membentuk metoksida yang bersifat
basa kuat sehingga pembentukan metil ester menjadi lebih baik. BF3 adalah asam
Lewis sebagai katalisator yang dapat menerima sepasang elektron sehingga
pembentukan metanoat lebih cepat dan sempurna (Solomons, 1994). NaCl jenuh
berguna untuk memisahkan koloid berwarna putih yang tersebar dalam larutan
BAB III
METODE PENELITIAN
Metode penelitian yang dilakukan adalah metode deskriptif yang bertujuan
untuk menganalisis komposisi asam lemak dan menetukan persentase asam laurat
pada posisi sn-2 yang terkandung dalam VCO dan PKO.
3.1 Alat
Alat yang digunakan dalam penelitian ini adalah satu unit Kromatografi
Gas Shimadzu GC-14B (Gambar 3 Lampiran 26, halaman 60), hot magnetic stirrer, penangas air (Memmert), neraca analitik, vortex, bola karet, oven, dan alat-alat gelas yaitu maat pipet (Pyrex), tabung reaksi bertutup (Pyrex), beaker
glass (Pyrex), Erlenmeyer (Pyrex).
3.2 Bahan
Bahan-bahan kimia yang digunakan dalam penelitian ini jika tidak
dinyatakan lain, berkualitas pro analis produksi E. Merck (Jerman) yaitu boron
trifluorida, natrium hidroksida, Tris- hidroksimetilaminometan, n-heksan, etanol,
metanol, natrium klorida, natrium sulfat anhidrat, kalsium klorida, lipase spesifik
pada posisi sn – 1,3 (Lipozyme® TL IM), standar asam lemak F.A.M.E C8-C22.
3.3 Pembuatan Pereaksi
3.3.1 Pembuatan Na Metanolik 0,5 N
Na metanolik 0,5 N dibuat dengan melarutkan 2 gram NaOH dalam 100
3.3.2 Pembuatan Larutan NaCl jenuh
Larutan NaCl jenuh dibuat dengan cara melarutkan 36 gram NaCl dalam
100 ml akuades.
3.3.3 Pembuatan Larutan Standat Metil Ester Larutan standar metil ester campuran C8-C22
3.4 Prosedur Penelitian
dibuat dengan cara
melarutkan 100 mg standar dalam 5 ml heksan (American Oil Chemists’ Society
(AOCS), 1997).
3.4.1 Pengambilan sampel
Metode pengambilan sampel yang digunakan secara purposif, dimana
sampel yang diambil dari satu tempat dianggap dapat mewakili sampel secara
keseluruhan. Dalam hal ini sampel VCO diperoleh di apotek kota Medan, dan
PKO diperoleh dari PT. Multimas Nabati Asahan.
3.4.2 Analisis komposisi asam lemak pada sampel
Minyak ditimbang sebanyak 250 mg didalam tabung reaksi bertutup
ditambahkan 5 ml Na metanolik 0,5 N, lalu dikocok 1menit. Tabung ditutup rapat
dan dipanaskan di dalam penangas air 100°C selama 5 menit, kemudian
didinginkan hingga suhu berkisar antara 30-40°C. Ditambahkan 6 ml BF3 dalam
metanol dan tutup rapat kembali tabung, lalu dipanaskan di dalam penangas air
100°C selama 5 menit. Kemudian didinginkan hingga 30-40°C lalu ditambahkan
10 ml n-heksan dan dikocok kuat selama 30 detik. Ditambahkan 15 ml larutan
NaCl jenuh sehingga terbentuk dua lapisan yaitu lapisan air dan lapisan n-heksan.
Lapisan n-heksan yang terbentuk dipisahkan sehingga yang tersisa hanya lapisan
air. Lapisan air diekstraksi kembali dengan 5 ml n-heksan. Lapisann-heksan yang
n-heksan ditambahkan 500 mg Na2SO4
Analisis sampel dilakukan sebanyak tiga kali lalu penentuan asam lemak
secara kualitatif dilihat dari waktu tambatnya (retention time) yang dibandingkan dengan penginjeksian baku standar asam lemak pada kondisi yang sama dengan
sampel sedangkan penentuan kuantitatif dihitung peak area dari salah satu asam lemak tersebut dibagi total peak area dikali 100% sehingga dapat diperoleh komposisi asam lemak pada sampel (American Oil Chemists’ Society (AOCS),
1997).
anhidrat dan biarkan selama 15 menit. Fase
cair bebas air diinjeksikan sebanyak 1 µL untuk dianalisis dengan menggunakan
alat kromatografi gas.Bagan alir pembuatan metil ester asam lemak dan kondisi
alat kromatografi gas dapat dilihat pada Lampiran 1 dan 2, halaman 30 dan 31.
3.4.3 Evaluasi Nilai Gizi
Rumus mencari nilai penyimpangan adalah jumlah nilai mutlak (Δ) dari
selisih antara persentase setiap golongan asam lemak dengan nilai ideal (33,33%).
Δ = │33,33% - %SFA│+│33,33% - % MUFA │+│33,33% - %PUFA│
Jika nilai Δ adalah 0 maka minyak tersebut bernilai gizi baik, makin besar
penyimpangan makin jelek nilai gizinya (Silalahi, dkk., 2011).
3.4.4 Penentuan distribusi asam laurat pada posisi sn-2
Dilakukan hidrolisis terhadap VCO dan PKO yaitu dengan cara 6 gram
minyak ditimbang dalam erlenmeyer 125 ml. Tambahkan 10 ml aquades, 2,5 ml
CaCl2 0,063 M, 5ml larutan buffer tris-HCl, 100 mg lipase, lalu di inkubasi pada
suhu 37 ± 0,5°C dengan variasi waktu inkubasi 8 jam dengan pengocokan yang
dilakukan tiap selang 1 jam, selama 10 menit. Lalu diinaktifkan dengan etanol
sebanyak 50 ml. Kemudian campuran dipindahkan ke corong pisah, dikocok dan
ditambahkan dengan etanol sebanyak 50 ml dan diambil lapisan atas. Lalu
diuapkan diatas penagas air dalam cawan penguap yang sudah diketahui beratnya
(Satiawihardja, 2001).Bagan alir proses hidrolisis dapat dilihat pada Lampiran 3,
halaman 32. Lapisan asam lemak hasil hidrolisis minyak dengan enzim lipase
dilakukan preparasi yaitu ditimbang sebanyak 250 mg. Ditambahkan 6 ml BF3
dan tutup rapat kembali tabung, lalu dipanaskan di dalam penangas air 100°C
selama 5 menit.Kemudian didnginkan hingga suhu 30-40°C lalu ditambahkan 10
ml n-heksan dan dikocok kuat selama 30 detik. Ditambahkan 15 ml larutan NaCl
jenuh sehingga terbentuk dua lapisan yaitu lapisan air dan lapisan n-heksan.
Lapisan n-heksan yang terbentuk dipisahkan sehingga yang tersisa hanya lapisan
air. Lapisan air diekstraksi kembali dengan 5 ml n-heksan. Lapisan n-heksan yang
terbentuk diambil dan disatukandengan lapisan heksan yang pertama. Ekstrak
n-heksan ditambahkan 500 mg Na2SO4
Bobot asam Laurat pada sampel dapat ditentukan dengan rumus :
anhidrat dan biarkan selama 15 menit. Fase
cair bebas air diinjeksikan sebanyak 1 µL untuk dianalis dengan menggunakan
alat kromatografi gas.Bagan alir pembuatan metil ester asam lemak dapat dilihat
pada Lampiran 4, halaman 33. Hasil analisis Kromatografi Gas pada asam Laurat
sebelum dan sesudah hidrolisis kemudian dikonversikan dalam satuan berat.
Bobot pengurangan sebelum dan sesudah hidrolisis adalah bobot asam laurat pada
posisi sn-2 (American Oil Chemists’ Society (AOCS), 1997).
Bobot asam laurat (mg/mg sampel) = Faktor koreksi × Luas area asam laurat
Keterangan:
Faktor koreksi : Hasil bagi berat asam laurat standar dengan luas area asam
BAB IV
HASIL DAN PEMBAHASAN
4.1 Sampel
VCO yang digunakan dalam penelitian ini adalah VCO yang di produksi
oleh Noery ViCO Lhokseumawe dan PKO oleh PT.Multimas Nabati Asahan.
VCO berwarna bening dan PKO berwarna kuning jernih.
4.2 Komposisi Asam Lemak pada VCO dan PKO
Metil ester asam lemak yang diperoleh dari esterifikasi minyak nabati
kemudian dianalisis dengan alat Kromatografi Gas. Analisis metil ester asam
lemak adalah berdasarkan waktu retensi metil ester asam lemak yang tertahan di
dalam kolom. Waktu retensi metil ester asam lemak kromatogram standar dan
sampel relatif sama, sehingga detektor dapat menganalisis puncak-puncak asam
lemak pada sampel. Metil ester asam lemak jenuh yang lebih pendek dan asam
lemak tak jenuh trans akan lebih mudah menguap dibandingkan metil ester asam lemak jenuh yang lebih panjang dan asam lemak tak jenuh cis lalu masuk ke detektor untuk dideteksi tinggi puncak asam lemaknya. Komposisi asam lemak
dari VCO dan PKO dapat dilihat pada Tabel 4.1. Kromatogram metil ester asam
lemak standar dapat dilihat pada Lampiran 5, halaman 34. Kromatogram metil
ester asam lemak VCO dan PKO sebelum dihidrolisis dapat dilihat pada Lampiran
6-11, halaman 35-40.
Pada VCO dan PKO, kandungan SFA tinggi yaitu asam laurat dengan
mencair pada suhu 29°C. Komposisi asam lemak pada VCO dan PKO dapat
dilihat pada Tabel 4.1.
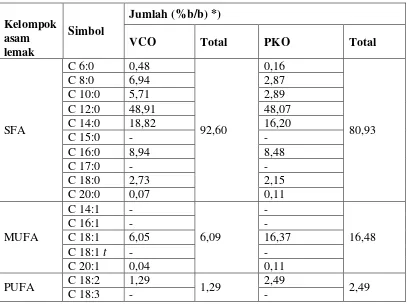
Tabel 4.1 Komposisi Asam Lemak VCO dan PKO
Kelompok
*) : Hasil merupakan rata-rata dari 3 kali pengulangan penyuntikan sampel.
SFA : saturated fatty acid, MUFA : monounsaturated fatty acid, PUFA : polyunsaturated fatty acid.
Pada PKO, kandungan SFA yaitu asam kaprat (C 10:0) 2,89% lebih kecil
dari kisaran 3,3-4,4%. Pada umumnya, perbedaan komposisi asam lemak yang
hilang atau munculnya asam lemak dipengaruhi oleh proses pembuatannya.
Misalnya pada produk VCO secara teknik dibuat dengan proses dingin tanpa ada
pemanasan yang tinggi. Pada produk PKO proses pembuatannya melalui proses
pemisahan, pemecahan, pengeringan dan proses ekstraksi menjadi minyak. Proses
pembuatan ini menimbulkan adanya perbedaan, tetapi menghasilkan komposisi
4.3 Nilai Gizi VCO dan PKO
Salah satu metode yang dilakukan untuk menentukan nilai gizi suatu
minyak adalah berdasarkan komposisi asam lemaknya yaitu dengan menghitung
nilai penyimpangan minyak dari perbandingan golongan asam lemak ideal dengan
persentase SFA : MUFA : PUFA yaitu 33,33% : 33,33% : 33,33%. Nilai gizi
VCO dan PKO dihitung berdasarkan penyimpangan nilai mutlak atau selisih dari
persentase golongan asam lemak dalam minyak kelapa murni dan minyak inti
sawit dengan nilai komposisi ideal yaitu 33,33% untuk masing-masing kelompok
ideal asam lemak. Contoh perhitungan nilai gizi minyak nabati dapat dilihat pada
Lampiran12, halaman 41.
Penentuan nilai gizi dari masing-masing minyak kelapa murni dan minyak
inti sawit adalah berdasarkan persentase penyimpangan golongan asam lemak.
Nilai gizi minyak kelapa murni dan minyak inti sawit yang ideal adalah yang
mempunyai total penyimpangan sebesar 0 (nol) (Silalahi, 2011). Makin besar nilai
penyimpangan maka nilai gizi minyak kelapa murni dan minyak inti sawit
tersebut makin rendah. Berdasarkan data nilai penyimpangan, minyak kelapa
murni dengan penyimpangan 118,55% dan minyak inti sawit dengan
penyimpangan 95,29%. VCO dan PKO memiliki penyimpangan yang besar
karena banyak mengandung asam lemak jenuh. Kandungan SFA yang tinggi
92,60% dan 80,93% dengan persentase asam laurat (C 12:0) yang dominan yaitu
48,91% dan 48,07% sehingga VCO dan PKO dikatakam minyak laurat. Asam
lemak rantai pendek, dan sedang pada sn-1,3, yang melewati sistem pencernaan yaitu dari mulut, lambung dan usus halus, dimetabolisme dengan bantuan enzim
sedang dan asam laurat (C 12:0) yang paling dominan di VCO dan PKO, tidak
memasuki aliran darah sehingga tidak menyebabkan aterosklerosis pada
pembuluh darah menuju jantung. Jadi, walaupun VCO dan PKO merupakan
minyak yang mempunyai penyimpangan yang dan dari segi nilai gizi kurang baik.
Akan tetapi VCO dan PKO bukan pemicu penyakit jantung koroner (Silalahi,
2011). Dengan persentase komposisi golongan asam lemak (SFA, MUFA, PUFA)
VCO dan PKO yang dianalisis maka dapat diperoleh nilai gizinya berdasarkan
penyimpangan dari yang ideal. Nilai gizi VCO dan PKO dapat dilihat dari Tabel
4.2.
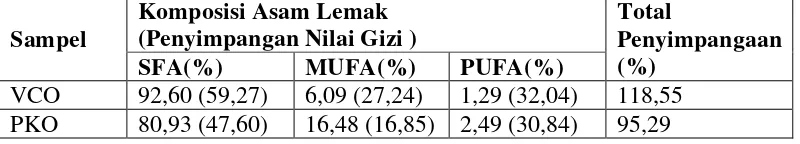
Tabel 4.2 Nilai gizi VCO dan PKO
Sampel
Komposisi Asam Lemak (Penyimpangan Nilai Gizi )
Total
Selain berdasarkan komposisi asam lemak, nilai gizi juga ditentukan oleh
jenis asam lemak pada posisi TAG, karena berkaitan dengan mekanisme
metabolisme di dalam tubuh. Misalnya, asam lemak jenuh rantai panjang terutama
asam palmitat dan miristat yang berada pada posisi sn-2 lebih bersifat aterogenik dibandingkan dengan jika berada pada posisi sn-1,3. Sehingga untuk mengkaji nilai gizi VCO dan PKO penting juga dievaluasi distribusi jenis asam lemak pada
posisi triasilgliserol.
4.4 Distribusi Asam Laurat pada Posisi sn-2
VCO dan PKO dihidrolisis dengan enzim lipase yang kondisinya
disesuaikan dengan metabolisme tubuh menghidrolisis minyak. Setelah
diperoleh kemudian dianalisis dengan alat Kromatografi Gas. Kromatogram asam
lemak pada sampel VCO dan PKO pada posisi sn-1,3 dapat dilihat pada Lampiran 14-19, halaman 43-48. Contoh perhitungan distribusi asam palmitat pada posisi
sn-2 dapat dilihat pada Lampiran 23, halaman 52. Persentase distribusi asam laurat pada VCO dan PKO yang dapat dilihat pada Tabel 4.3.
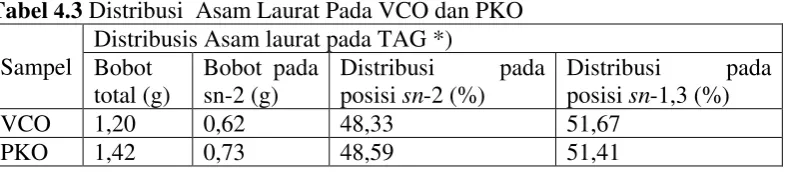
Tabel 4.3 Distribusi Asam Laurat Pada VCO dan PKO Sampel
Distribusis Asam laurat pada TAG *) Bobot *) : Hasil merupakan rata-rata dari 3 kali pengulangan penyuntikan sampel. Berat sampel : 6 gram minyak.
Berdasarkan Tabel 4.3, bobot asam laurat pada VCO pada posisi sn-2 lebih sedikit dibandingkan dengan PKO. Tetapi perbedaan bobot asam laurat ini
tidak memiliki perbedaan yang jauh. Asam lemak rantai pendek yang banyak
terdapat pada posisi sn-1,3 dapat langsung dimetabolisme oleh hati dan langsung menjadi energi. Sedangkan asam lemak rantai panjang yang berada pada posisi
sn-1,3 tidak semua dapat diserap karena bereaksi dengan kalsium dan magnesium membentuk garam yang tidak larut dalam air dan diekskresikan dari tubuh melalui
feses.
Hasil penelitian Permata (2012), penggunaan metode hidrolisis dapat
meningkatkan aktivitas antibakteri, dan metode enzimatik lebih baik
dibandingkan metode penyabunan, dimana hasil hidrolisis enzimatik adalah asam
laurat dan monolaurin, sedangkan pada hidrolisis penyabunan yang dihasilkan
adalah asam laurat, monolaurin atau dilaurin atau tetap dalam bentuk trigliserida.
Aktivitas antibakteri MCFA terbaik adalah dalam bentuk bebas dan
semua asam lemak jenuh, asam laurat memiliki aktivitas antimikroba lebih baik
dibandingkan dengan asam kaprilat (C8:0), asam kaprat (C10:0), dan asam
miristat (C14:0). Secara umum dilaporkan bahwa asam lemak dan monogliserida
menginaktivasi bakteri dengan cara merusak membran plasma (lipid bilayer) dari bakteri tersebut (Enig, 1996; Kabara, et al., 1972; Widiyarti, dkk., 2009).
Monolaurin mempunyai keunggulan dibandingkan dengan antibakteri
lainnya, dimana monolaurin hanya efektif terhadap bakteri patogen tetapi tidak
untuk bakteri probiotik. Monolaurin menunjukkan sifat antibakteri terhadap
BAB V
KESIMPULAN DAN SARAN
5.1Kesimpulan
Komposisi asam laurat pada VCO dan PKO didominasi oleh SFA dengan
penyimpangan nilai gizi berturut-turut sebesar 118,55% dan 95,29%.
Analisis posisi asam laurat pada posisi sn-2 pada VCO dan PKO menunjukkan distribusi asam laurat pada posisi sn-2 yaitu berturut-turut sebesar 48,33% dan 48,59%.
5.2 Saran
Dari hasil penelitian ini disarankan:
1. Melakukan penelitian lanjutan tentang kandungan asam laurat dan monolaurin
pada sampel minyak lain.
2. Melakukan penelitian dan pengembangan dari monolaurin menjadi Sedian
Farmasi.
DAFTAR PUSTAKA
Aehle, W. (2004). Enzyme in Industry. Weinheim: Wiley-VCH. Hal. 149-155. American Oil Chemists’ Society (AOCS). (1997). Official methods and
recommended practices of the American Oil Chemists’ Society. AOCS: Preparation of Methyl Esters of Fatty Acids. Champaign: AOCS Press. Method Ce 2-66.
Badan Standardisasi Nasional. (2008). SNI 7381:2008, Minyak Kelapa Virgin (VCO). Jakarta : Badan Standardisasi Nasional.
Berry, S.E.E. (2009). Triacylglycerol Structure and Interesterification of Palmitic and Stearic Acid-Rich Fats: An Overview and Implications for Cardiovascular Disease. Nutrition Research Reviews. 22(1): 3-17.
Conrado, S.D. (2000). Coconut Oil In Health And Disease: Its And Monolaurin’s Potential As Cure For HIV/AIDS. Cocotech Meeting Chennai. XXXVII. Darmoyuwono, W. (2006). Gaya Hidup Sehat dengan Virgin Coconut Oil.
Jakarta: Penerbit PT Indeks Kelompok Gramedia. Hal. 1-10, 15-20.
Decker, E.A. (1996). The Role of Stereospesific Saturated Fatty Acid Positions on Lipid Nutrition. Nutrition Reviews. 54(4): 108-110.
Enig, M.G. (1996). Health and Nutritional Benefits from Coconut Oil: An Important Functional Food for the 21st Century. Presented at the AVOC Lauric Oil Symposium. Ho Chi Min City. Vietnam.
Enig, M.G. (2010). Health and Nutrition Benefits from Coconut Oil and Its Advantages Over Competing Oils. Indian Coconut Jurnal. 2(3): 9-15. Haryati. T. (1999). Development and Application of Differential Scanning
Calorimetric Methods for Physical and Chemical Analysis of Palm Oil.
Disertation of PhD. Malaysia: University Putra Malaysia.
Kabara, J.J., Swieczkowski, D.M., Conley, A.J., dan Truant, J.P. (1972). Fatty Acids and Derivatives as Antimicrobial Agents. Antimicrobial Agents Chemotheraphy. 2(1): 23-28.
Lieberman, S., Enig, M.G., dan Preuss, H.G. (2006). A Review of Monolaurin and Lauric Acid: Natural Virucidal and Bactericidal Agents. Alternative and Complementary Therapies. 55(1): 310-314.
McKee, T., dan McKee, J.R. (2003). Biochemistry: The Molecular Basis Of Life. Edisi III. Boston: The McGraw-Hill. Hal. 68-71.
O’Brien, R.D. (2009). Fats and Oils: Formulating and Prossesing for Applications. Edisi Ketiga. London: CRC Press. Hal. 43-47, 273.
Permata, Y.M. (2012). Pengaruh Hidrolisis Parsial Minyak Kelapa Murni Terhadap Aktivitas Antibakteri. Tesis. Medan: Fakultas Farmasi. Universitas Sumatera Utara.
Sari, N. (2009). Efek Pemberian Virgin Coconut Oil (VCO) Terhadap Profil Imunohistokimia Antioksidan Superoxide Dismutase (SOD) Pada Jaringan Ginjal Tikus Diabetes Mellitus. Skripsi. Bogor: Fakultas Kedokteran Hewan. Institut Pertanian Bogor.
Satchithanandam, S., Carolyn, J. O., Carol, J.S. dan Mary, M.B. (2004). Trans Saturated, and Unsaturated Fat in Foods in the United States Prior to Mandatory Trans Fat Labeling. Journal of Lipids. 39(1): 11-18.
Satiawihardja, B. (2001). Studi Pembuatan Mentega Coklat Tiruan dari Minyak Sawit dengan Proses Interesterifikasi Enzimatik. Jurnal Teknologi Indonesia Pertanian. 10(3): 129-138.
Setiaji, B., dan Surip, P. (2006). Membuat VCO Berkualitas Tinggi. Jakarta: Penerbit Penebar Swadaya. Hal. 3-9, 67-71.
Silalahi, J. (2000). Hypocholesterolemic Factors in Foods. A Review. Indonesian Food Nutrition Progress. 7(1):26-36.
Silalahi, J. (2006). Fats and Oils: Modification and Substitution. Lecture Notes. Postgraduate Section. Medan: University Sumatera Utara. Hal. 17-25, 63-68.
Silalahi, J., dan Tampubolon, S.D.R. (2002). Asam Lemak Trans dalam Makanan dan Pengaruhnya Terhadap Kesehatan. Jurnal Teknloogi dan Industri Pangan. 8(2): 184-188.
Silalahi, Y.C.E. (2011). Komposisi Asam Lemak dan Identifikasi Posisi Asam Palmitat pada Beberapa Minyak Nabati dan Lemak Hewani. Tesis. Medan: Fakultas Farmasi. Universitas Sumatera Utara.
Solomon, G. (1994). Fundamental Organic Chemistry. Edisi Keempat. New York: John Wiley and Sons Inc. Hal. 74-75.
Syah, A.N.A. (2005). Perpaduan Sang Penakluk Penyakit. Jakarta: Penerbit Agro Media Pustaka. Hal. 5-6, 14-18, 22-23.
Villeneuve, P. dan Foglia, FA. (1997). Lipase Specificities : Potential Application in Lipid Bioconversion. Inform. 8(6): 640-650.
White, B. (2009). Dietary Fatty Acids. American Family Physician. 80(4):345-350.
Willis, W.M., Lencki, R.W., dan Marangoni, A.G. (1998). Lipid Modification Strategies in The Production Of Nutritionally Functional Fats and Oil.
Critical Reviews in Food Science and Nutrition. 38(8): 638-674.
Willis, W.M., dan Marangoni, A.G. (1999). Biotechnological Strategies for the Modification of Food Lipids. Biotech. Genetic Eng. Rev. 16(5): 141-175.
Lampiran 1. Bagan Alir Pembuatan Metil Ester Asam Lemak Sebelum Hidrolisis
Ditambah 5 ml Na metanolik 0,5 N
Dipanaskan pada suhu 100°C selama 5 menit Didinginkan hingga 30-40°C
Ditambah 6 ml BF3
Dipanaskan 100°C selama 5 menit tabung di tutup
Didinginkan
Ditambah 10 ml n-heksan,dikocok kuat 30 detik Ditambah 15 ml NaCl jenuh, terbentuk 2 lapisan Dipisahkan dua lapisan tersebut
Diekstraksi lagi dengan 5 ml n-heksan Dipisahkan 2 lapisan yang terbentuk
Disatukan dengan lapisan n-heksan pertama
Ditambah 500 mg Na2SO4
Didiamkan selama 25 menit
anhidrat
Disaring
Diambil 1 µL untuk diinjeksikan kea lat Kromatografi Gas
Lampiran 2. Kondisi Alat Kromatografi Gas Kondisi alat Kromatografi Gas sebagai berikut:
1. Jenis GC : shimadzu, GC – 14B dari jepang
2. Jenis detector : FID (Flame Ionization Detector)
3. Jenis kolom : kapiler DB-23
4. Kondisi operasi alat Kromatografi Gas
a. Suhu detector : 260°C Lapisan n heksan
Lapisan air
Lapisan air Lapisan n-heksan
Lapisan n-heksan
Na2SO4 anhidrat
b. Suhu injector : 260°C
c. Gas pembawa : N2
5. Temperatur kolom terprogram :
dengan tekanan 100 kPa
a.Suhu pertama : 200°C dipertahankan selama 5 menit naik 7°C/menit
b.Suhu kedua : 220°C dipertahankan selama 10 menit
6. Split : 40 menit/5 ml
7. Waktu retensi : 30 menit
8. Volume injeksi : 1 µL
9. Kecepatan alir : 3,0 ml/menit
Lampiran 3. Bagan Alir Hidrolisis VCO dan PKO
Ditambahkan 10 ml akuades Ditambahkan 2,5 ml CaCl2
Ditambahkan suspense 5ml buffer tris-HCl dan 100 mg enzim lipase
0,063 M
Diinkubasi pada suhu 37°C selama 8 jam Dikocok selama 10 menit tiap selang 1 jam VCO/PKO (6 g)
Ditambahkan 50 ml etanol
Lampiran 4. Bagan Alir Pembuatan Metil Ester Asam Lemak Sesudah Hidrolisis
Ditambah 6 ml BF3
Dipanaskan 100°C selama 5 menit tabung ditutup
Didinginkan
Ditambah 10 ml n-heksan, dikocok kuat 30 detik
Ditambah 15 ml NaCl jenuh, terbentuk 2 lapisan
Dipisahkan dua lapisan tersebut Lapisan atas : asam lemak Lapisan bawah
250 ml VCO atau PKO
Diekstraksi lagi dengan 5 ml n-heksan Dipisahkan 2 lapisan yang terbentuk
Disatukan dengan lapisan n-heksan pertama
Ditambahkan 500 mg Na2SO4
Didiamkan selama 15 menit
anhidrat
Disaring
Diambil 1 µL untuk diinjeksikan ke alat Kromatografi Gas
Lampiran 5. Karakteristik Kromatogram Standar Metil Ester Asam Lemak Sebelum Hidrolisis
Lapisan n-heksan
Lapisan air Lapisan n-heksan
Lapisan n-heksan
Lampiran 12. Perhitungan Nilai Gizi VCO dan PKO
Contoh perhitungan evaluasi nilai gizi VCO. Perbandingan persentase dari tiap
golongan asam lemak dari hasil analisi Kromatografi Gas adalah sebagai berikut :
%SFA:%MUFA :%PUFA
(0,48 + 6,94 + 5,71+ 48,91 + 18,82 + 8,94 + 2,73 + 0,07)%:( 6,05 + 0,04)% : 1,29%
71,06% :6,09% : 1,29%
Δ = | 33,33% - %SFA| + | 33,33% - %MUFA| + | 33,33% - %PUFA| = | 33,33% - 92,60%| + | 33,33% - 6,09%| + | 33,33% - 1,29%| = 59,27% + 27,24% + 32,04%
= 118,55 %
Nilai penyimpangan VCO dan PKO
Sampel
Komposisi asam lemak (penyimpangan) Total
Penyimpangaan (%)
SFA(%) MUFA (%) PUFA(%)
Ideal 0 0 0 0
VCO 59,27 27,24 32,04 118,55 PKO 47,60 16,85 30,84 95,29
Lampiran 13. Daftar Spesifikasi Enzim Lipase Prodek enzim lipase : Lipozyme®
Produksi : Novo Nordisk Bioindustry Ltd. Denmark TL IM
Asal : Thermomyces lanuginosus diproduksi oleh permentasi medis cair dari suatu rekayasa
genetika dari Aspergillus oryzae.
Ukuran partikel (mm) : 0,3-1,0
Spesifikasi posisi : sn - 1,3
Aplikasi : Interistefikasi lemak, mentega, margarine
Pengelompokkan penggunaan : makanan
Lampiran 20. Perhitungan Asam Laurat pada Posisi Sn-2 Berat total minyak VCO = 6000 mg
Berat standar FAME campuran = 100 mg
Persentase asam laurat standar = 6,4537%
mg
Berat sampel yang dipreparasi = 246 mg
000013853
Maka bobot asam laurat (mg/mg sampel) = Faktor koreksi x luas area asam laurat
sampel
= 0,00001383 x 3538600
= 49,0096 mg /246 mg
Lampiran 22. Hasil Perhitungan Berat Asam Laurat Setelah Hidrolisis
Luas area laurat
Faktor Standar Sampel
VCO
6000 246 6,4537 466475 3538600 0,00001385 49,0096 1193,6302
1194,0500 6000 252 6,4537 466475 3611856 0,00001385 50,0242 1189,3333
6000 250 6,4537 466475 3612879 0,00001385 50,0383 1199,2864
PKO
6000 258 6,4537 466475 4359508 0,00001385 60,3791 1402,1395
1422,7684 6000 262 6,4537 466475 4463555 0,00001385 61,8202 1413,6870
6000 252 6,4537 466475 441100 0,00001385 61,0923 1452,4786
Lampiran 23. Perhitungan Distribusi Asam Laurat pada Posisi Sn-2 Bobot asam laurat posisi sn-2
Bobot asam laurat pada posisi sn-2 dapat dihitung dengan mengurangkan bobot asam laurat sebelum dan sesudah hidrolisis
Bobot pada posisi sn-2 = Bobot total – Bobot pada posisi sn-1,3 Standar Sampel
VCO
3655,8 248 6,4537 466475 3130375 0,00001385 43,3556 638,1892
620,7986 3655,8 254 6,4537 466475 2982254 0,00001385 41,3042 593,6299
3655,8 254 6,4537 466475 3167864 0,00001385 43,8749 630,5766
PKO
3686,2 254 6,4537 466475 3711698 0,00001385 51,4070 744,9723
735,3693 3686,2 258 6,4537 466475 3753783 0,00001385 51,9898 741,7377
= 1,20 g – 0,62 g
= 0,58 g
Persentase distribusi asam laurat pada posisi sn-2 = X100% total
Asam laurat dalam 6 gram sampel minyak
Bobot total (g)
Bobot total pada
sn-1,3(g) laurat pada posisi
sn-1,3 (%) VCO 1,20 0,62 0,58 48,33 51,67 PKO 1,42 073 0,69 48,59 51,41
Lampiran 24. Perhitungan Statistik Berat Asam Laurat dalam VCO dan PKO 1. Perhitungan Statistik Berat Asam Laurat pada VCO Sebelum Hidrolisis
No. Xi
Berat as. Laurat/ total asam lemak sampel (mg)
(Xi-X ) (Xi-X )2
∑ 3582,1499
Data diterima jika t
= 9,9250.
2. Perhitungan Statistik Berat Asam Laurat pada PKO Sebelum Hidrolisis
No. Xi
Berat as. Laurat/ total asam lemak sampel (mg)
=
Data diterima jika t
= 9,9250.
3. Perhitungan Statistik Berat Asam Laurat pada VCO Sesudah Hidrolisis
No. Xi
Berat as. Laurat/ total asam lemak sampel (mg)
(Xi-X ) (Xi-X )2
Pada interval kepercayaan 99% dengan nilai α = 0.01, dk = n-1 = 3-1 =2 diperoleh
nilai t tabel (α /2, dk)
Data diterima jika t
= 9,9250.
4. Perhitungan Statistik Berat Asam Laurat pada PKO Sesudah Hidrolisis
No. Xi
Berat as. Laurat/ total asam lemak sampel (mg)
(Xi-X ) (Xi-X )2
1. 744,9723 9,6030 92,2176 2. 741,7377 6,3684 40,5565 3. 719,3981 -15,9712 255,0792294
∑ 2206,1081
Data diterima jika t
= 9,9250.
t hitung
Gambar 1. VCO
Gambar 2. PKO
Lampiran 26. Gambar