MIKROENKAPSULASI MINYAK KELAPA MURNI
MENGGUNAKAN PENYALUT KITOSAN
NUR AMALIA USMAYANTI
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
ABSTRAK
NUR AMALIA USMAYANTI. Mikroenkapsulasi Minyak Kelapa Murni Menggunakan Penyalut Kitosan. Dibimbing oleh GUSTINI SYAHBIRIN dan BAMBANG SRIJANTO.
Kelapa merupakan suatu komoditas perkebunan yang bisa diolah menjadi minyak kelapa murni (VCO). Kelebihan VCO dibanding minyak lainnya adalah VCO mengandung asam lemak jenuh rantai sedang sekitar 64% yang didominasi oleh asam laurat dengan kandungan sekitar 44–52%. Asam laurat di dalam tubuh diubah menjadi monolaurin yang dapat mencegah serangan virus dan bakteri seperti HIV, HSV-1, dan influenza. VCO yang berwujud cair dan berbau khas dibuat menjadi sediaan obat berbentuk mikrokapsul. Bahan penyalut yang digunakan pada penelitian ini adalah kitosan. Kitosan dilarutkan dalam asam asetat 1%, kemudian ditambah gom guar 0.33%, glutaraldehida 4.86%, VCO, dan tween 80. Mikrokapsul dibuat dengan mengeringkan campuran tersebut menggunakan pengering semprot. Mikrokapsul yang diperoleh dilihat morfologinya dengan mikroskop elektron payaran (SEM), diukur kadar air, kadar abu, dan kadar asam laurat dalam VCO. Hasil SEM menunjukkan morfologi mikrokapsul kosong (tanpa VCO) terlihat kisut dan berlubang, sedang mikrokapsul yang terisi VCO tampak bulat dan halus. Kandungan VCO dalam mikrokapsul dengan glutaraldehida dan tanpa glutaraldehida sebesar 21.08 dan 3.37%.Analisis asam laurat dalam VCO sebelum perlakuan, VCO dari mikrokapsul dengan dan tanpa penambahan glutaraldehida berturut-turut sebesar 42.62, 35.12, dan 31.94%.
ABSTRACT
NUR AMALIA USMAYANTI. Microencapsulation of Virgin Coconut Oil Using Chitosan as a Coating Agent. Supervised by GUSTINI SYAHBIRIN and BAMBANG SRIJANTO.
MIKROENKAPSULASI MINYAK KELAPA MURNI
MENGGUNAKAN PENYALUT KITOSAN
NUR AMALIA USMAYANTI
Skripsi
Sebagai salah satu syarat memperoleh gelar Sarjana Sains pada
Departemen Kimia
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
Judul : Mikroenkapsulasi Minyak Kelapa Murni Menggunakan Penyalut Kitosan
Nama : Nur Amalia Usmayanti
NIM : G44201036
Menyetujui:
Pembimbing I, Pembimbing II,
Dra. Gustini Syahbirin, MS Ir. Bambang Srijanto
NIP 131 842 414 NIP 680 0003 303
Mengetahui:
Dekan Fakultas Matematika dan Ilmu pengetahuan Alam
Institut Pertanian Bogor
Prof. Dr. Ir. Yonny Koesmaryono, MS
NIP 131 473 999
PRAKATA
Puji syukur penulis panjatkan ke hadirat Allah SWT atas berkah dan rahmat-Nya karya ilmiah ini dapat diselesaikan. Penelitian ini telah dilakukan dari bulan Maret 2006 sampai Januari 2007, di Laboratorium Kimia Organik, FMIPA IPB dan Laboratorium BPPT Serpong. Judul yang dipilih adalah Mikroenkapsulasi Minyak Kelapa Murni
Menggunakan Penyalut Kitosan.
Secara tulus dan kerendahan hati, penulis ingin menyampaikan terimakasih kepada Ibu Dra. Gustini Syahbirin, MS. dan Bapak Ir. Bambang Srijanto, selaku pembimbing I dan II yang telah berkenan memberikan bimbingan, masukan, saran, arahan, dan perhatian selama penelitian dan penulisan skripsi ini. Terima kasih juga penulis ucapkan kepada Budi Arifin S.Si, dan Ibu Idah yang telah banyak memberi saran dan arahan. Di samping itu, penghargaan penulis sampaikan kepada seluruh staf dan laboran Kimia Organik (Bapak Sabur, Ibu Yeni, dan Ibu Aah), dan Mas Heri. Penulis juga mengucapkan
terima kasih kepada kedua orang tuaku (Usman dan Nuryati), Kak Rahma, Kak Mulky, Bang Udin, Teh Santi, Rika, Niar, Kayla, dan keluargaku di Manggarai atas doa, cinta
dan semangat yang senantiasa diberikan. Terima kasih penulis haturkan untuk sahabat-sahabatku tercinta (Aditya, Rahma, Dyah, Dian, Eka, Atik, Soele, Budhi, dan Kdut) atas semangat, bantuan, doa, dan persahabatan yang indah, anak kimia 38, warga kosan Cr4, dan C8, terima kasih untuk kebersamaannya.
Semoga karya ilmiah ini bermanfaat.
Bogor, Februari 2007
RIWAYAT HIDUP
Penulis dilahirkan di Jakarta pada tanggal 6 Agustus 1982 sebagai anak ketiga dari lima bersaudara, dari pasangan Usman dan Nuryati.
DAFTAR ISI
Halaman
DAFTAR TABEL... viii
DAFTAR GAMBAR ... viii
DAFTAR LAMPIRAN... x
PENDAHULUAN ... 1
TINJAUAN PUSTAKA Minyak Kelapa Murni ... 1
Mikroenkapsulasi ... 2
Kitosan ... 3
Gom guar ... 3
Glutaraldehida ... 4
Pengering semprot ... 4
SEM ... 5
BAHAN DAN METODE Bahan dan Alat ... 5
Metode Penelitian ... 5
HASIL DAN PEMBAHASAN Pencirian kitosan ... 6
Pencirian Minyak Kelapa Murni ... 7
Rendemen Mikrokapsul ... 7
Pencirian Mikrokapsul ... 8
Hasil Analisa kandungan asam laurat ... 11
SIMPULAN DAN SARAN... 14
DAFTAR PUSTAKA ... 15
DAFTAR TABEL
Halaman
1 Spesifikasi kitosan niaga ... 3
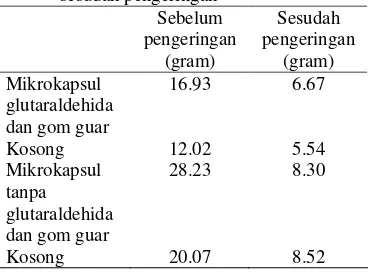
2 Bobot mikrokapsul sebelum dan sesudah pengeringan ... 8
3 Kandungan VCO dalam mikrokapsul ... 11
4 Hasil kromatografi gas dari VCO sebelum dibuat mikrokapsul ... 12
5 Hasil kromatografi gas dari VCO pada mikrokapsul dengan penambahan glutaraldehida dan gom guar ... 13
6 Hasil kromatografi gas dari VCO pada mikrokapsul tanpa penambahan glutaraldehida dan gom guar ... 13
7 Hasil kromatografi gas dari asam lemak standar ... 14
8 Kandungan asam lemak dalam VCO hasil analisa kromatografi gas ... 14
DAFTAR GAMBAR
Halaman 1 Struktur asam laurat, asam kaprat, asam kaprilat ... 22 Klasifikasi mikrokapsul menurut morfologi ... 3
3 Struktur unit ulangan selulosa (R = -OH), kitin (R = -NHCOCH3), dan kitosan (R = -NH2)... 3
4 Struktur gom guar... 4
5 Struktur glutaraldehida ... 4
6 Alat pengering semprot ... 5
7 Kitosan yang digunakan ... 6
8 Hasil spektrum FTIR kitosan ... 7
9 VCO yang digunakan ... 7
10 Mikrokapsul VCO dengan penambahan glutaraldehida dan gom guar ... 8
11 Mikrokapsul kosong (tanpa VCO) dengan penambahan glutaraldehida dan gom guar ... 8
12 Mikrokapsul VCO tanpa penambahan glutaraldehida dan gom guar ... 8
13 Mikrokapsul kosong (tanpa VCO) dan tanpa penambahan glutaraldehida dan gom guar... 9
Halaman 15 Struktur permukaan mikrokapsul VCO dengan penambahan glutaraldehida dan
gom guar... 10 16 Struktur permukaan mikrokapsul kosong tanpa penambahan glutaraldehida dan
gom guar... 10 17 Struktur permukaan mikrokapsul VCO tanpa penambahan glutaraldehida dan gom
guar... 10 18 Kromatogram VCO sebelum dibuat mikrokapsul ... 12 19 Kromatogram VCO pada mikrokapsul dengan penambahan glutaraldehida dan
gom guar... 12 20 Kromatogram VCO pada mikrokapsul tanpa penambahan glutaraldehida dan gom
DAFTAR LAMPIRAN
Halaman
1. Diagram alir penelitian ... 18
2. Metode pembuatan pereaksi ... 19
3. Data hasil pengukuran kadar air dan abu kitosan ... 20
4. Data hasil pengukuran kadar air dan abu mikrokapsul ... 20
5. Kadar air VCO ... 20
6. Perhitungan derajat deasetilasi kitosan ... 21
MIKROENKAPSULASI MINYAK KELAPA MURNI
MENGGUNAKAN PENYALUT KITOSAN
NUR AMALIA USMAYANTI
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
ABSTRAK
NUR AMALIA USMAYANTI. Mikroenkapsulasi Minyak Kelapa Murni Menggunakan Penyalut Kitosan. Dibimbing oleh GUSTINI SYAHBIRIN dan BAMBANG SRIJANTO.
Kelapa merupakan suatu komoditas perkebunan yang bisa diolah menjadi minyak kelapa murni (VCO). Kelebihan VCO dibanding minyak lainnya adalah VCO mengandung asam lemak jenuh rantai sedang sekitar 64% yang didominasi oleh asam laurat dengan kandungan sekitar 44–52%. Asam laurat di dalam tubuh diubah menjadi monolaurin yang dapat mencegah serangan virus dan bakteri seperti HIV, HSV-1, dan influenza. VCO yang berwujud cair dan berbau khas dibuat menjadi sediaan obat berbentuk mikrokapsul. Bahan penyalut yang digunakan pada penelitian ini adalah kitosan. Kitosan dilarutkan dalam asam asetat 1%, kemudian ditambah gom guar 0.33%, glutaraldehida 4.86%, VCO, dan tween 80. Mikrokapsul dibuat dengan mengeringkan campuran tersebut menggunakan pengering semprot. Mikrokapsul yang diperoleh dilihat morfologinya dengan mikroskop elektron payaran (SEM), diukur kadar air, kadar abu, dan kadar asam laurat dalam VCO. Hasil SEM menunjukkan morfologi mikrokapsul kosong (tanpa VCO) terlihat kisut dan berlubang, sedang mikrokapsul yang terisi VCO tampak bulat dan halus. Kandungan VCO dalam mikrokapsul dengan glutaraldehida dan tanpa glutaraldehida sebesar 21.08 dan 3.37%.Analisis asam laurat dalam VCO sebelum perlakuan, VCO dari mikrokapsul dengan dan tanpa penambahan glutaraldehida berturut-turut sebesar 42.62, 35.12, dan 31.94%.
ABSTRACT
NUR AMALIA USMAYANTI. Microencapsulation of Virgin Coconut Oil Using Chitosan as a Coating Agent. Supervised by GUSTINI SYAHBIRIN and BAMBANG SRIJANTO.
MIKROENKAPSULASI MINYAK KELAPA MURNI
MENGGUNAKAN PENYALUT KITOSAN
NUR AMALIA USMAYANTI
Skripsi
Sebagai salah satu syarat memperoleh gelar Sarjana Sains pada
Departemen Kimia
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
Judul : Mikroenkapsulasi Minyak Kelapa Murni Menggunakan Penyalut Kitosan
Nama : Nur Amalia Usmayanti
NIM : G44201036
Menyetujui:
Pembimbing I, Pembimbing II,
Dra. Gustini Syahbirin, MS Ir. Bambang Srijanto
NIP 131 842 414 NIP 680 0003 303
Mengetahui:
Dekan Fakultas Matematika dan Ilmu pengetahuan Alam
Institut Pertanian Bogor
Prof. Dr. Ir. Yonny Koesmaryono, MS
NIP 131 473 999
PRAKATA
Puji syukur penulis panjatkan ke hadirat Allah SWT atas berkah dan rahmat-Nya karya ilmiah ini dapat diselesaikan. Penelitian ini telah dilakukan dari bulan Maret 2006 sampai Januari 2007, di Laboratorium Kimia Organik, FMIPA IPB dan Laboratorium BPPT Serpong. Judul yang dipilih adalah Mikroenkapsulasi Minyak Kelapa Murni
Menggunakan Penyalut Kitosan.
Secara tulus dan kerendahan hati, penulis ingin menyampaikan terimakasih kepada Ibu Dra. Gustini Syahbirin, MS. dan Bapak Ir. Bambang Srijanto, selaku pembimbing I dan II yang telah berkenan memberikan bimbingan, masukan, saran, arahan, dan perhatian selama penelitian dan penulisan skripsi ini. Terima kasih juga penulis ucapkan kepada Budi Arifin S.Si, dan Ibu Idah yang telah banyak memberi saran dan arahan. Di samping itu, penghargaan penulis sampaikan kepada seluruh staf dan laboran Kimia Organik (Bapak Sabur, Ibu Yeni, dan Ibu Aah), dan Mas Heri. Penulis juga mengucapkan
terima kasih kepada kedua orang tuaku (Usman dan Nuryati), Kak Rahma, Kak Mulky, Bang Udin, Teh Santi, Rika, Niar, Kayla, dan keluargaku di Manggarai atas doa, cinta
dan semangat yang senantiasa diberikan. Terima kasih penulis haturkan untuk sahabat-sahabatku tercinta (Aditya, Rahma, Dyah, Dian, Eka, Atik, Soele, Budhi, dan Kdut) atas semangat, bantuan, doa, dan persahabatan yang indah, anak kimia 38, warga kosan Cr4, dan C8, terima kasih untuk kebersamaannya.
Semoga karya ilmiah ini bermanfaat.
Bogor, Februari 2007
RIWAYAT HIDUP
Penulis dilahirkan di Jakarta pada tanggal 6 Agustus 1982 sebagai anak ketiga dari lima bersaudara, dari pasangan Usman dan Nuryati.
DAFTAR ISI
Halaman
DAFTAR TABEL... viii
DAFTAR GAMBAR ... viii
DAFTAR LAMPIRAN... x
PENDAHULUAN ... 1
TINJAUAN PUSTAKA Minyak Kelapa Murni ... 1
Mikroenkapsulasi ... 2
Kitosan ... 3
Gom guar ... 3
Glutaraldehida ... 4
Pengering semprot ... 4
SEM ... 5
BAHAN DAN METODE Bahan dan Alat ... 5
Metode Penelitian ... 5
HASIL DAN PEMBAHASAN Pencirian kitosan ... 6
Pencirian Minyak Kelapa Murni ... 7
Rendemen Mikrokapsul ... 7
Pencirian Mikrokapsul ... 8
Hasil Analisa kandungan asam laurat ... 11
SIMPULAN DAN SARAN... 14
DAFTAR PUSTAKA ... 15
DAFTAR TABEL
Halaman
1 Spesifikasi kitosan niaga ... 3
2 Bobot mikrokapsul sebelum dan sesudah pengeringan ... 8
3 Kandungan VCO dalam mikrokapsul ... 11
4 Hasil kromatografi gas dari VCO sebelum dibuat mikrokapsul ... 12
5 Hasil kromatografi gas dari VCO pada mikrokapsul dengan penambahan glutaraldehida dan gom guar ... 13
6 Hasil kromatografi gas dari VCO pada mikrokapsul tanpa penambahan glutaraldehida dan gom guar ... 13
7 Hasil kromatografi gas dari asam lemak standar ... 14
8 Kandungan asam lemak dalam VCO hasil analisa kromatografi gas ... 14
DAFTAR GAMBAR
Halaman 1 Struktur asam laurat, asam kaprat, asam kaprilat ... 22 Klasifikasi mikrokapsul menurut morfologi ... 3
3 Struktur unit ulangan selulosa (R = -OH), kitin (R = -NHCOCH3), dan kitosan (R = -NH2)... 3
4 Struktur gom guar... 4
5 Struktur glutaraldehida ... 4
6 Alat pengering semprot ... 5
7 Kitosan yang digunakan ... 6
8 Hasil spektrum FTIR kitosan ... 7
9 VCO yang digunakan ... 7
10 Mikrokapsul VCO dengan penambahan glutaraldehida dan gom guar ... 8
11 Mikrokapsul kosong (tanpa VCO) dengan penambahan glutaraldehida dan gom guar ... 8
12 Mikrokapsul VCO tanpa penambahan glutaraldehida dan gom guar ... 8
13 Mikrokapsul kosong (tanpa VCO) dan tanpa penambahan glutaraldehida dan gom guar... 9
Halaman 15 Struktur permukaan mikrokapsul VCO dengan penambahan glutaraldehida dan
gom guar... 10 16 Struktur permukaan mikrokapsul kosong tanpa penambahan glutaraldehida dan
gom guar... 10 17 Struktur permukaan mikrokapsul VCO tanpa penambahan glutaraldehida dan gom
guar... 10 18 Kromatogram VCO sebelum dibuat mikrokapsul ... 12 19 Kromatogram VCO pada mikrokapsul dengan penambahan glutaraldehida dan
gom guar... 12 20 Kromatogram VCO pada mikrokapsul tanpa penambahan glutaraldehida dan gom
DAFTAR LAMPIRAN
Halaman
1. Diagram alir penelitian ... 18
2. Metode pembuatan pereaksi ... 19
3. Data hasil pengukuran kadar air dan abu kitosan ... 20
4. Data hasil pengukuran kadar air dan abu mikrokapsul ... 20
5. Kadar air VCO ... 20
6. Perhitungan derajat deasetilasi kitosan ... 21
PENDAHULUAN
Latar Belakang
Kelapa banyak terdapat di daerah tropis, terutama pada sekitar daerah katulistiwa. Indonesia merupakan salah satu penghasil tumbuhan kelapa terbesar. Luas lahan perkebunan kelapa yang tersebar di Indonesia mencapai 3.712 juta hektar yang hampir seluruhnya adalah perkebunan rakyat (Syah 2005).
Sebagai komoditi hasil perkebunan, buah kelapa telah banyak diolah menjadi berbagai macam produk pangan, seperti santan, nata de coco, kopra, dan lain-lain. Saat ini kelapa juga
diolah menjadi minyak kelapa murni atau
virgin coconut oil (VCO) yang dapat
meningkatkan nilai mutu buah kelapa. VCO oleh tubuh diubah menjadi monolaurin. Asam lemak ini dikenal sebagai anti virus yang bermanfaat dalam penyembuhan berbagai penyakit, dari influenza hingga acquired immuno deficiency syndrome (AIDS). Berdasarkan hasil
penelitian sebelumnya, VCO mempunyai banyak manfaat bagi manusia, terutama untuk bidang medis, antara lain dapat mengurangi resiko kanker, mengurangi kadar kolesterol darah, memperbaiki sistem pencernaan, dan lain-lain. Selain dapat digunakan dalam industri farmasi, VCO juga dapat dimanfaatkan dalam industri kosmetik, susu formula, maupun sebagai minyak goreng bermutu tinggi (Rindengan & Novarianto 2005).
Saat ini VCO sudah banyak diproduksi dalam bentuk cair dalam kemasan botol. Tetapi karena bentuk VCO adalah minyak cair dan berbau khas sehingga untuk sebagian orang tidak cocok digunakan sebagai pengobatan secara oral. Untuk mengatasi masalah ini maka dicoba untuk membuat VCO tidak dalam bentuk cair atau diubah menjadi bentuk padatan sehingga VCO mudah dikonsumsi oleh masyarakat. Salah satu bentuk padatan yang bisa dibuat adalah mikrokapsul.
Mikroenkapsulasi adalah suatu proses penyalutan bahan-bahan inti yang berbentuk cair atau padat dengan menggunakan suatu bahan penyalut khusus yang membuat partikel-partikel inti mempunyai sifat fisika dan kimia seperti yang dikehendaki. Bahan penyalut yang berfungsi sebagai dinding pembungkus bahan inti tersebut dirancang untuk melindungi bahan-bahan terbungkus dari faktor-faktor yang dapat menurunkan
kualitas bahan tersebut (Rosenberg et al.
1990)
Sebelumnya Kristiani (1997) telah melakukan penelitian tentang pembuatan mikrokapsul minyak kaya asam lemak gamma linolenat. Pada penelitian ini akan dicoba untuk melakukan mikroenkapsulasi VCO yang kaya akan asam lemak jenuh rantai sedang, yaitu asam laurat.
Ariati (1998) telah melakukan penelitian tentang mikroenkapsulasi konsentrat asam lemak omega-3 dengan metode spray drying.
Pada penelitian ini juga akan dilakukan proses mikroenkapsulasi VCO menggunakan penyalut kitosan dengan metode spray drying.
VCO sebelum dibuat mikrokapsul dianalisa kandungan asam laurat menggunakan alat kromatografi gas (GC). Kitosan dilarutkan dalam asam asetat encer, kemudian dicampur dengan VCO hingga homogen. Larutan tadi dibuat mikrokapsul menggunakan alat pengering semprot.
Penelitian ini diharapkan dapat men-jelaskan morfologi mikrokapsul dan menentukan jumlah asam laurat dari VCO yang dapat dikungkung oleh kitosan sebagai bahan penyalut.
TINJAUAN PUSTAKA
Minyak Kelapa Murni
Virgin Coconut Oil (VCO) atau minyak
kelapa murni merupakan salah satu produk olahan dari daging buah kelapa. VCO adalah minyak yang mengandung asam lemak jenuh rantai sedang sekitar 64% dengan perincian bahwa lebih dari 50% merupakan asam laurat (C12), 6-7% asam kaprat (C10), dan 8% asam kaprilat (C8). Kandungan VCO sendiri sebagian besar terdiri atas asam lemak jenuh (92% dari kandungan total), 6% asam lemak tak jenuh tunggal, dan 2% asam lemak tak jenuh jamak (Wibowo 2005).
VCO merupakan minyak jenuh, maka minyak ini sangat stabil dan tahan oksidasi sehingga sulit untuk menjadi tengik (rancid),
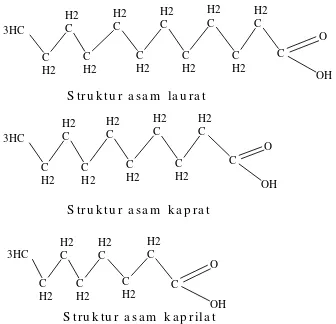
3HC C H2 H2 C C H2 H2 C C H2 H2 C C H2 H2 C C H2
S tru k tu r a s a m la u ra t H2 C C O OH 3HC C H2 H2 C C H2 H2 C C H2 H2 C C H2 H2 C C O OH
S tru k tu r a s a m k a p ra t
3HC C H2 H2 C C H2 H2 C C H2 H2 C C O OH S tru k tu r a s a m k a p rila t
Gambar 1 Struktur asam laurat, asam kaprat, asam kaprilat
Proses pembuatan VCO dari daging buah kelapa ada beberapa macam, diantaranya yaitu dengan proses pemanasan dan tanpa pemanasan. Pembuatan VCO dengan pemanasan diawali dengan penghalusan daging buah kelapa, kemudian dibuat santan dengan perbandingan air 1:2, lalu airnya diperas dan didiamkan selama 3 jam. Air santan ini akan membuat tiga lapisan, lapisan atas yang disebut krim ini kaya akan minyak, lapisan tengah disebut skim yang kaya akan protein, dan lapisan bawah berupa endapan. Lapisan yang akan dibuat VCO adalah lapisan krim yang kemudian dipanaskan pada suhu 100-110oC selama 3 jam atau setelah terlihat
adanya pemisahan blondo. Setelah minyak didinginkan kemudian disaring. Untuk mendapatkan minyak murni, minyak yang belum matang ini dipanaskan lagi pada suhu 100-110oC sampai diperoleh minyak yang
jernih, lalu disaring agar minyak ini benar-benar bersih (Rindengan & Novarianto 2005). Pembuatan VCO tanpa pemanasan prosesnya tidak jauh berbeda dengan pembuatan yang dengan pemanasan. Pada pembuatan VCO tanpa pemanasan, krim yang diperoleh dicampur dengan minyak pancing dengan nisbah krim dan minyak pancing 3:1. setelah dicampur rata kemudian difermentasi selama 10-12 jam. Setelah itu lapisan minyak dipisahkan dan disaring menggunakan penyaring minyak (Rindengan & Novarianto 2005).
VCO sangat berguna bagi kesehatan tubuh manusia, diantaranya ialah mengurangi resiko astroklerosis dan penyakit terkait, menurunkan resiko kanker dan penyakit degeneratif lainnya, membantu mencegah infeksi virus, mendukung sistem kekebalan
tubuh, mencegah osteoporosis, mengontrol diabetes, memperbaiki sistem pencernaan dan penyerapan nutrisi, mencegah kanker kulit, tidak mengandung kolesterol, dan lain-lain (Rindengan & Novarianto 2005). Melihat banyaknya manfaat yang diperoleh dari VCO maka sudah banyak masyarakat yang mulai mengkonsumsinya.
Kendala yang dihadapi oleh para konsumen karena bentuk VCO adalah minyak cair dan berbau khas sehingga untuk sebagian orang tidak cocok digunakan sebagai pengobatan secara oral. Untuk mengatasi masalah ini maka dicoba untuk membuat VCO tidak dalam bentuk cair atau diubah menjadi bentuk padatan sehingga VCO mudah dikonsumsi oleh masyarakat. Salah satu bentuk padatan yang bisa dibuat adalah mikrokapsul, dimana VCO akan terselimuti oleh bahan penyalut yang aman dikonsumsi dan diproses sehingga terbentuk serbuk dengan ukuran sangat kecil hanya beberapa mikron.
Mikroenkapsulasi
Mikroenkapsulasi adalah teknik yang digunakan untuk mengungkung suatu senyawa dengan menggunakan bahan penyalut dengan ukuran yang sangat kecil dengan diameter rata-rata 15-20 mikron atau kurang dari setengah diameter rambut manusia (Yoshizawa 2002). Terdapat lebih dari 400 miliar kapsul kecil dalam setiap galon material yang termikrokapsul (Sutriyo
et al. 2004).
Kegunaan dari menggunakan teknik ini antara lain untuk mengendalikan pelepasan senyawa, membuat senyawa aktif lebih mudah dan aman untuk dipegang, melindungi material peka dari lingkungan, dan mengubah wujud material dari cair menjadi padat (Yoshizawa 2002).
Secara umum ada dua metode untuk mengkapsulasi suatu senyawa, yaitu metode fisika dan metode kimia. Metode fisika antara lain dengan pengeringan semprot (spray drying), piringan pemutar, stationer extrusion nozzle, dan suspensi udara. Sedangkan
pengering semprot dengan serbuk mikrokapsul sebagai produk (Durant 2001).
Secara garis besar, mikrokapsul dapat dibagi menjadi tiga kelompok dasar menurut morfologinya yaitu tipe berinti tunggal, berinti jamak, dan tipe matriks. Pembagian kelompok secara lebih jelas dapat diamati pada Gambar 2.
Gambar 2 Klasifikasi mikrokapsul menurut morfologi (Yoshizawa 2004)
Kitosan
Kitin dan kitosan merupakan biopolimer polisakarida alami yang menarik, karena sumbernya melimpah di alam serta selalu terbaharui, dapat terdegradasi secara alami, tidak beracun, biokompatibel, tidak menimbulkan efek alergi, karakteristik bahannya yang unik dan sifat fungsionalnya yang beragam. Kitosan merupakan kitin yang terdeasetilasi, yaitu modifikasi struktur kitin melalui hidrolisis menggunakan larutan alkali maupun secara biokimiawi. Kitin dan kitosan bernilai komersial tinggi dan mengandung kadar nitrogen yang tinggi (6.89%), yang pertama dieksploitasi sebagai agen pengkelat. Kemampuan kitosan dalam mengikat logam lebih efektif dibandingkan selulosa. Disamping itu, kegunaan kitin dan kitosan amat luas, meliputi bidang industri, kedokteran, farmasi, kosmetika, pertanian, pangan, dan bioteknologi (Sugita 2005).
Teknologi proses produksi untuk memperoleh kitin dilakukan melalui proses deproteinasi, delipidasi, dan demineralisasi dari kulit atau cangkang udang sehingga diperoleh kitin. Secara alami kitin terdapat pada kulit udang dengan kadar sekitar 17%. Selanjutnya dilakukan proses deasetilasi basa sehingga didapat kitosan yang memenuhi syarat-syarat industri. Perbedaan antara
kitosan dengan selulosa adalah gugus 2-hidroksi dari selulosa digantikan oleh gugus asetamida dan menghasilkan -(1-4)-2-asetomido-2-deoksi-D-glukopiranosa
(Shepherd et al. 1999). Perbedaan struktur
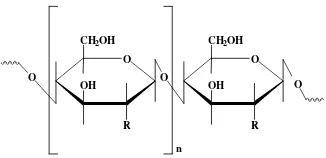
senyawa kitin, kitosan, dan selulosa dapat dilihat pada Gambar 3.
O
R OH CH2OH
O
R OH CH2OH
O
O O
n
Gambar 3 Struktur unit ulangan selulosa (R = -OH), kitin (R = -NHCOCH3) dan
kitosan (R = -NH2).
Tabel 1 Spesifikasi kitosan niaga* Parameter Ciri Ukuran partikel Serpihan sampai
bubuk Kadar air ≤ 10% Kadar abu ≤ 2%
Derajat
deasetilasi ≥ 70% Warna larutan tidak berwarna Viskositas (cps):
Rendah < 200 Medium 200−799 Tinggi 800−2000 Sangat tinggi >2000
* Sumber: Anonim 1987 dalam Jamaludin 1994
Karakteristik kitosan bergantung pada sumber (asal), derajat deasetilasi (DDs), distribusi gugus asetil, gugus amina, panjang rantai dan distribusi bobot molekul. Di samping itu, kitosan terdeasetilasi sebagian kira-kira tersusun 50% unit D-glukosamin dapat larut dalam air. Kelenturan rantai molekul kitosan dalam larutan dapat dimanipulasi menggunakan kitosan yang berbeda DDs atau larutan berbeda pH dan atau kekuatan ionik untuk mengendalikan ukuran pori, kekuatan mekanik atau permeabilitas membran (Khan 2002).
Gom Guar
Gom adalah molekul berbobot molekul tinggi yang bersifat koloid (berukuran 10– 1000 Å) dan dalam bahan pengembang yang sesuai dapat membentuk gel, larutan ataupun suspensi kental pada konsentrasi yang sangat rendah. Selain sebagai bahan pengental dan
Inti tunggal Inti jamak Matriks mikropartikel
pembentuk gel, gom mempunyai banyak sifat fungsional sekunder yang berguna bagi produk pangan. Sifat-sifat fungsional tersebut diantaranya adalah sebagai perekat, pengikat, penghambat kristalisasi es, penjernih, pengeruh, pelapis, pengemulsi, pembentuk film, pemantap buih, pensuspensi, dan penghambat pengerutan (Fardiaz 1989).
Gom guar merupakan gom biji yang diperoleh dengan cara pemisahan secara mekanik dari biji tanaman Cyamopsis tetragonolobus yang ditemukan di barat laut
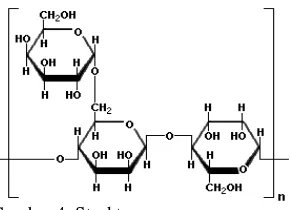
India dan Pakistan (Nussinovitch 1997). Dilihat dari strukturnya (Gambar 4), gom guar adalah galaktomanan yang terdiri atas D-galaktosa yang berikatan α(1,6) dengan rantai tulang punggung 1,4-β-D-manopiranosa (Chaplin 2005).
Gom ini tidak bermuatan, maka gom guar tidak dipengaruhi secara nyata pada pH rendah dan sangat efektif digunakan dalam produk-produk asam. Interaksi gom guar tidak menghasilkan gel, tetapi hanya meningkatkan kekentalan. Hal ini disebabkan karena derajat substitusi rantai molekulnya yang tinggi mengurangi interaksi (Fardiaz 1989). Gom guar juga telah dimanfaatkan sebagai pembawa (carrier) untuk memperbaiki sistem
penghantaran obat ke dalam usus besar untuk mengobati radang usus besar dan kanker usus besar (Kshirsagar 2000).
Gambar 4 Struktur gom guar.
Glutaraldehida
Glutaraldehida merupakan senyawa dwifungsi yang umumnya digunakan untuk modifikasi protein dan polimer. Glutaraldehida mempunyai rumus molekul C5H8O2 (Gambar 5) dengan bobot molekul
sebesar 100.1 g mol-1, titik didih sebesar
100oC, titik lebur -15oC, pH antara 3.2-4.2,
berupa larutan yang berwarna kuning, larut dalam air, alkohol, dan benzena (BASF 1999 dalam Aisyah 2005).
Glutaraldehida dapat digunakan sebagai senyawa pengikat silang dalam polipeptida dan ikatan silang dari protein. Hal ini
disebabkan adanya aktivitas gugus aldehida yang tinggi dalam bentuk basa Schiff dengan gugus amino dari protein. Glutaraldehida berfungsi sebagai perantara ikatan silang untuk PVA dan beberapa polisakarida (Wang
et al. 2004). Glutaraldehida komersial
umumnya berbentuk larutan dalam air dengan konsentrasi 2%, 20%, dan 25%.
Gambar 5 Struktur glutaraldehida
Pengering Semprot
Spray Dryer atau alat pengering semprot
adalah alat yang digunakan untuk membuat suatu larutan atau suspensi menjadi suatu padatan serbuk yang kering. Ada dua jenis pengering semprot yang biasa digunakan, yaitu dengan sistem sirkulasi terbuka dan sistem sirkulasi tertutup. Pada sistem sirkulasi terbuka, udara dengan suhu yang tinggi akan masuk ke dalam sistem dan kemudian akan keluar dari sistem sebagai hasil sisa atau limbah. Pada sistem sirkulasi tertutup, udara yang dialirkan ke dalam sistem tidak dikeluarkan dari sistem, melainkan akan digunakan kembali (Deymonaz et al. 1998).
Kelebihan dari alat ini adalah sistem operasinya sederhana dan biaya perawatan yang rendah, dapat memproduksi dengan kapasitas yang tinggi. (Deymonaz et al. 1998).
Kemurnian bahan dapat terjaga, Kelebihannya juga dapat mengatasi banyak bahan yang tidak tahan panas atau titik didihnya rendah.
Kekurangan dari alat ini yaitu ada beberapa senyawa aromatik yang mempunyai titik didih rendah dapat hilang selama proses pengeringan berlangsung, dan bahan inti dari mikrokapsul bisa juga terdapat di permukaan kapsul yang dapat terjadi oksidasi dan terjadi perubahan cita rasa pada produk kapsul (Dziezak 1988). Masalah lainnya dalam proses pengeringan mikroenkapsulasi, pada saat bahan dimasukkan ke dalam tabung suhu
inlet yang digunakan tidak cukup tinggi,
sehingga pengeringannya tidak sempurna dan terjadi pelengketan pada dinding tabung. Partikel yang tidak stabil juga dapat terjadi bila kondisi operasi tidak ideal, sehingga pada suhu yang rendah partikel akan mengembang dan merusak permukaan kapsul. Kerusakan ini akan menyebabkan hilangnya senyawa volatil dan menjadikan produk bermutu rendah (Bhandari et al. 1985).
O C
H (CH2)3 C
Gambar 6 Alat pengering semprot
Mikroskop Elektron Payaran (SEM)
SEM merupakan alat untuk melihat benda yang sangat kecil dalam bentuk stereo dengan skala perbesaran tinggi (Rachman 2001). Gambar yang dihasilkan merupakan gambar topografi dengan segala tonjolan, lekukan, dan lubang pada permukaan. Gambar topografi diperoleh dari penangkapan elektron sekunder yang dipancarkan oleh spesimen atau bahan. Sinyal elektron sekunder yang dihasilkan ditangkap oleh detektor kemudian diteruskan ke monitor, selanjutnya monitor akan menampilkan gambar khas yang menggambarkan struktur permukaan bahan.
Prinsip kerja SEM adalah deteksi elektron yang dihamburkan oleh suatu sampel padatan ketika ditembakkan oleh berkas elektron berenergi tinggi secara kontinu yang dipercepat di dalam electromagnetic coil yang
dihubungkan dengan CRT (chatode ray tube)
sehingga dihasilkan suatu informasi mengenai keadaan permukaan suatu sampel senyawa. (Noor 2001).
Sebelum dianalisa dengan SEM, sampel harus dipreparasi terlebih dahulu. Hal-hal yang harus dipenuhi untuk menyiapkan sampel yaitu menghilangkan seluruh pelarut air, atau bahan lain yang dapat menguap ketika di dalam vakum dan menipiskan sampel yang dianalisis. Jika spesimen merupakan suatu isolator, seperti tanaman, kuku jari, dan keramik, maka bahan tersebut perlu dilapisi dengan bahan konduktor. Bahan konduktor yang biasa digunakan ialah emas, perak, dan aliansi emas dan paladium. Pelapisan dilakukan dalam ruang penguapan vakum (Sutiani 1997).
BAHAN DAN METODE
Bahan dan Alat
Bahan-bahan yang diperlukan dalam penelitian ini ialah VCO dan serbuk kitosan
yang diperoleh dari BPPT, Tween 80 1% (v/v), asam asetat 1% (v/v), gom guar 0.33%, glutaraldehida 4.86%, n-heksana, dan
akuades.
Alat-alat yang digunakan dalam penelitian ini adalah, kromatografi gas (GC), mikroskop elektron payaran (SEM), spektrofotometer inframerah transformasi fourier (FTIR), alat
pengering semprot LABPLANT SD-06, dan alat-alat gelas.
Metode
Sebelum dibuat mikrokapsul dilakukan pencirian kitosan dan VCO sebagai bahan bakunya. Pencirian kitosan meliputi pengukuran kadar air dan abu, dan penentuan derajat deasetilasi (DDs) menggunakan FTIR, sedang pencirian VCO meliputi pengukuran kadar air, titik didih, dan analisa kandungan asam lemak dalam VCO menggunakan GC.
Pembuatan mikrokapsul yang dilakukan dalam penelitian ini menggunakan metode
spray drying. Mikrokapsul VCO dibuat
menjadi 2 macam, yaitu mikrokapsul dengan penambahan glutaraldehida dan gom guar, dan tanpa penambahan glutaraldehida dan gom guar. Dibuat juga dari tiap macam mikrokapsul itu mikrokapsul kosong, yaitu mikrokapsul tanpa isi atau tanpa VCO. Mikrokapsul yang terbentuk kemudian diuji kadar air dan abu, dilihat morfologinya dengan SEM, dan dianalisa kandungan VCO nya dengan kromatografi gas. Diagram alir penelitian ini dapat diamati pada Lampiran 1.
Penentuan Derajat Deasetilasi
(Domzsy dan Roberts 1985 dalam Khan et al.
2002)
Penentuan derajat deasetilasi (DD) kitin dan kitosan diukur dengan menggunakan FTIR. Puncak tertinggi dicatat dan diukur dari garis dasar yang dipilih. Nilai absorbansi dapat dihitung dengan menggunakan rumus:
A = log P Po
dengan Po = % transmitans pada garis dasar P = % transmitans pada puncak
minimum
A = absorbans
Kitin yang terdeasetilasi sempurna (100%) menghasilkan nilai A1655 = 1.33. Perbandingan absorbans antara bilangan gelombang1655 cm-1 (serapan pita amida I) dan 3450 cm-1
% DD = 1 – 100% 33 . 1 1 A A 3450
1655 × ×
Penentuan Kadar Air (AOAC 1999)
Penentuan kadar air mikrokapsul dilakukan dengan metode gravimetri. Sebanyak ± 1.0000 g contoh dimasukkan ke dalam cawan petri yang telah diketahui bobotnya, kemudian cawan beserta isinya dimasukkan ke dalam oven dengan suhu 105°C selama 3 jam atau sampai bobotnya konstan. Setelah itu, dimasukkan ke dalam desikator dan ditimbang. Kadar air contoh dihitung dengan persamaan:
Kadar air =
X
Y
X
)
(
−
x 100%
dimana: X = berat cuplikan mula-mula (g) Y = berat cuplikan kering (g)
Penentuan Kadar Abu (AOAC 1999)
Cawan porselin yang telah disiapkan dimasukkan ke dalam tanur, didinginkan dalam desikator, dan ditimbang beratnya. Sebanyak 0.5 g contoh dimasukkan ke dalam cawan tersebut, selanjutnya dibakar sampai asapnya habis kemudian dimasukkan ke dalam tanur pengabuan dengan suhu 600 oC
sampai diperoleh abu berwarna putih. Cawan beserta isinya didinginkan dalam desikator dan ditimbang. Kadar abu dihitung dengan persamaan sebagai berikut:
Kadar abu =
(g) cuplikan Bobot (g) abu Bobot × 100% Pembuatan Mikrokapsul
Larutan asam asetat 1% dibuat dengan melarutkan asam asetat glasial ke dalam akuades. Kitosan dalam bentuk padatan sebanyak 40g dilarutkan dalam larutan asam asetat 1% dan diaduk hingga homogen menggunakan pengaduk magnet sehingga diperoleh larutan kitosan 4% b/v sebanyak 1000 mL. Kemudian ditambahkan larutan gom guar 0.33% sebanyak 166.67 mL setetes demi tetes sambil diaduk diatas pengaduk magnet, dan ditambah larutan glutaraldehida 4.86% sebanyak 33.34 mL baru kemudian dicampur dengan VCO sebanyak 20 mL dan 10 mL Tween 80 untuk membuat suatu larutan kitosan-VCO dengan nisbah 2:1. Untuk mikrokapsul VCO tanpa penambahan gom guar dan glutaraldehida dibuatnya juga
sama, hanya tidak ditambahkan gom guar dan glutaraldehida. Metode pembuatan pereaksi dijelaskan pada Lampiran 2.
Larutan kemudian dibuat mikrokapsul menggunakan pengering semprot hingga diperoleh mikrokapsul kitosan-VCO. Alat pengering semprot diatur pada suhu 180oC, fan pada skala 20, pump pada skala 7 yang
setara dengan 339.5 mL/jam, dan deblocker
pada skala medium.
Pencirian Mikrokapsul
Pencirian mikrokapsul yang dilakukan pada penelitian ini menggunakan SEM untuk melihat struktur morfologi mikrokapsul, kadar air dan abu mikrokapsul, dan analisis kandungan asam lemak dalam VCO yang dibuat mikrokapsul menggunakan GC.
HASIL DAN PEMBAHASAN
Pencirian Kitosan
Kitosan yang digunakan berbentuk serpihan kecil berwarna kuning. Gambar 7 memperlihatkan contoh kitosan yang digunakan. Kadar air kitosan diperoleh sebesar 7.72% dan kadar abu sebesar 0.52% (Lampiran 3). Nilai ini mememenuhi persyaratan spesifikasi kitosan niaga seperti yang tertera dalam Tabel 1. Kadar air menunjukkan jumlah air yang terkandung dalam kitosan, pada kondisi ini air yang terikat dalam kitosan, yaitu air tipe II (kadar air bahan berkisar 3–10%) telah dihilangkan sehingga pertumbuhan mikroorganisme dan reaksi kimia yang bersifat merusak seperti pencokelatan (browning), hidrolisis, atau
oksidasi lemak dapat dikurangi (Winarno 1997). Kadar abu menunjukkan jumlah unsur anorganik atau mineral dari suatu bahan. Nilai kadar abu yang diperoleh menunjukkan bahwa kitosan yang digunakan tidak mengandung unsur anorganik atau mineral, karena semakin kecil kadar abu suatu bahan, maka mineral yang terkandung dalam suatu bahan juga kecil.
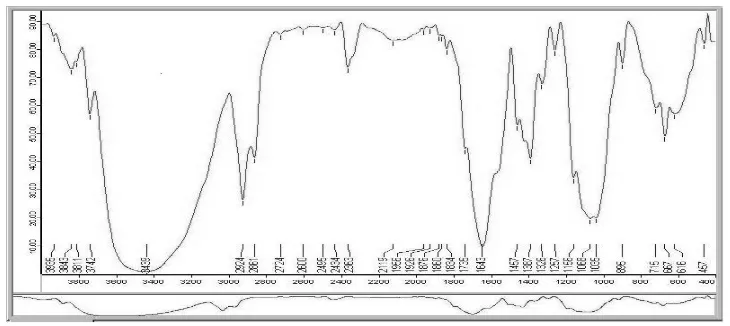
Gambar 8 Hasil spektrum FTIR kitosan
Deasetilasi kitosan merupakan proses penghilangan gugus asetil pada kitin menjadi gugus amino bebas kitosan menggunakan basa kuat. Salah satu metode yang dapat digunakan untuk menentukan derajat deasetilasi kitosan adalah spektroskopi inframerah (IR). Pada penelitian ini dilakukan pengukuran derajat deasetilasi menggunakan FTIR. Gambar 8 menunjukkan hasil spetrum FTIR kitosan.
Penentuan derajat deasetilasi kitosan dari hasil spektrum FTIR menggunakan metode
baseline dipengaruhi oleh gugus hidroksi dan
gugus amida. Serapan gugus hidroksi terdapat pada bilangan gelombang 3700 - 3000 cm-1,
sedang gugus C=O dari amida terletak pada bilangan gelombang 1680 – 1630 cm-1. dari
hasil spektrum (Gambar 8) terlihat bahwa puncak serapan gugus hidroksi terletak pada bilangan gelombang 3439 cm-1, dan puncak
serapan amida terletak pada bilangan gelombang 1643 cm-1.
Derajat deasetilasi kitosan diperoleh sebesar 65.07% (Lampiran 6). Nilai derajat deasetilasi ini menunjukkan bahwa kitin telah mengalami penghilangan gugus asetil selama proses isolasinya. Sementara itu, kitosan tidak seluruhnya terdeasetilasi, masih ada sekitar 34.93% gugus asetil. Semakin tinggi nilai derajat deasetilasi kitosan semakin berkurang gugus asetil dalam kitosan.
Pencirian Minyak Kelapa Murni
VCO yang digunakan berupa minyak tak berwarna yang jernih dan berbau harum khas minyak kelapa (Gambar 9). VCO ini mempunyai kadar air sebesar 0.48% (Lampiran 5). Penentuan kadar air berguna untuk mengetahui ketahanan suatu bahan yang
akan disimpan agak lama, karena kandungan air di dalam suatu bahan merupakan media tumbuh bakteri dan mikroorganisme.
Nilai ini cukup kecil, sehingga mutu VCO yang digunakan juga cukup baik karena dengan sedikitnya kandungan air maka VCO ini tidak mudah rusak oleh pertumbuhan mikroba.
Gambar 9 VCO yang digunakan
Titik didih VCO yang digunakan sekitar 330oC. Suhu titik didih VCO ini cukup tinggi,
sehingga tidak khawatir hilang karena ikut menguap saat proses pengeringan pada alat pengering semprot yang menggunakan suhu 180oC, yang akan mengurangi jumlah VCO
yang terkungkung dalam mikrokapsul yang diperoleh.
Rendemen Mikrokapsul
penampung akhir, pada alat pengering semprot terdapat dua tabung lagi, yaitu tabung pengering dan tabung vakum. Tabung pengering adalah tabung pertama tempat mikrokapsul ditampung setelah disemprotkan melalui nozzle pada suhu tinggi dan kemudian
dikeringkan. Setelah kering mikrokapsul itu akan dialirkan ke dalam tabung vakum dan akhirnya dialirkan ke botol penampung.
Tabel 2 Bobot mikrokapsul sebelum dan sesudah pengeringan Sebelum pengeringan (gram) Sesudah pengeringan (gram) Mikrokapsul glutaraldehida dan gom guar
16.93 6.67
Kosong 12.02 5.54 Mikrokapsul
tanpa glutaraldehida dan gom guar
28.23 8.30
Kosong 20.07 8.52
Kelemahan alat ini menurut Dziezak (1988) bisa terjadi pelengketan pada dinding tabung pengering yang disebabkan karena suhu yang kurang cukup tinggi, maka bahan yang masuk ke dalam alat ini tidak seluruhnya mengering, sehingga bahan itu menempel pada dinding tabung pengering. Bahan yang menempel pada dinding tabung itu cukup banyak sehingga mengurangi jumlah mikrokapsul yang diperoleh pada botol penampung.
Pencirian Mikrokapsul
Mikrokapsul VCO dengan penambahan glutaraldehida dan gom guar yang dihasilkan berbentuk serbuk halus berwarna kuning kecokelatan (Gambar 10). Begitu juga dengan mikrokapsul kosong yang berwarna kuning kecoklatan (Gambar 11). Warna ini dihasilkan karena selain warna larutan kitosan yang digunakan berwarna kuning, juga ditambah dengan larutan glutaraldehida yang berwarna kuning. Akibatnya setelah penambahan glutaraldehida ke dalam larutan kitosan, warna campuran menjadi semakin tua, sehingga mempengaruhi warna larutan sebelum dan sesudah dikeringkan dengan pengering semprot.
Gambar 10 Mikrokapsul VCO dengan penambahan glutaraldehida dan gom guar
Gambar 11 Mikrokapsul kosong (tanpa VCO) dengan penambahan glutaral dehida dan gom guar
Mikrokapsul VCO yang dibuat tanpa penambahan glutaraldehida dan gom guar berbentuk serbuk halus berwarna kuning lebih terang jika dibandingkan dengan mikrokapsul yang menggunakan glutaraldehida (Gambar 12). Begitu juga dengan mikrokapsul kosongnya yang berwarna kuning (Gambar 13). Hal ini disebabkan karena warna yang timbul pada mikrokapsul ini hanya dipengaruhi oleh warna larutan kitosan yang digunakan.
Gambar 13 Mikrokapsul kosong
(tanpa VCO) tanpa penambahan
glutaraldehida dan gom guar
Mikrokapsul VCO dengan penambahan glutaraldehida dan gom guar memiliki kadar air sebesar 13.04%, lebih rendah dari mikrokapsul kosongnya yang memiliki kadar air sebesar 17.64%. Untuk mikrokapsul VCO tanpa penambahan glutaraldehida dan gom guar memiliki kadar air sebesar 17.78%, juga lebih rendah dari mikrokapsul kosongnya yang memiliki kadar air sebesar 20.46% (Lampiran 4).
Kadar air mikrokapsul VCO dengan glutaraldehida dan gom guar lebih rendah dari kadar air mikrokapsul VCO tanpa glutaraldehida dan gom guar. Hal ini diduga disebabkan karena peran glutaraldehida sebagai pengikat silang antara kitosan membuat reaksi yang mengeluarkan air, sehingga air mudah keluar dengan penguapan akibat pemanasan pada pengering semprot. Pelepasan air juga dibantu dengan adanya gugus –NH2 dalam kitosan yang tidak
bereaksi dengan glutaraldehida dapat membentuk ikatan hidrogen antar molekulnya mengakibatkan struktur mikrokapsul semakin rapat sehingga air mudah keluar dari mikrokapsul. Selain itu, adanya gugus –OH dalam kitosan dan gom guar juga dapat mengeluarkan air berupa air konstitusi, yaitu air terikat secara kimia yang merupakan bagian dari molekul senyawa tertentu dan bukan dalam bentuk H2O (Syarief & Halid
1991).
Kadar air mikrokapsul menunjukkan tingkat kelembaban dari mikrokapsul tersebut. Besarnya kadar air menentukan daya tahan simpan mikrokapsul, jika suatu mikrokapsul memiliki kadar air yang rendah, berarti mikrokapsul itu bersifat kering dan mempunyai daya tahan simpan yang lama. Sebaliknya, jika kadar air suatu mikrokapsul tinggi, berarti mikrokapsul itu masih basah
dan mempunyai daya tahan simpan yang tidak lama, karena dalam kondisi mikrokapsul yang lembab kemungkinan suatu mikroba untuk hidup lebih besar dan dapat mempengaruhi sifat fisika dan kimia mikrokapsul, sehingga mudah terjadi kerusakan pada mikrokapsul tersebut.
Secara keseluruhan kadar air pada mikrokapsul yang diperoleh dengan metode
spray drying nilainya cukup besar. Hal ini
diduga disebabkan oleh metode spray drying
yang digunakan, karena pada metode ini untuk menghilangkan air pada campuran digunakan suhu yang tinggi dalam tabung pengering pada alat pengering semprot, dan langsung dialirkan ke tabung vakum dan botol penampung yang suhunya rendah. Hal ini dapat membuat bahan yang diperoleh menjadi bersifat higroskopis, sehingga air mudah masuk lagi ke dalam mikrokapsul.
Kandungan mineral ditentukan dari kadar abu. Kadar abu menunjukkan banyaknya bahan anorganik yang terkandung di dalam contoh. Kadar abu yang tinggi berarti tingginya kandungan bahan anorganik yang terkandung di dalam contoh, sebaliknya kadar abu yang rendah memiliki kandungan bahan anorganik yang rendah.
Kadar abu untuk mikrokapsul VCO dengan glutaraldehida dan gom guar, dan mikrokapsul kosongnya sebesar 0.27% dan 0.26%. Kadar abu untuk mikrokapsul VCO tanpa penambahan glutaraldehida dan gom guar, dan mikrokapsul kosongnya sebesar 0.51% dan 0.38%. Kadar abu mikrokapsul VCO dengan glutaraldehida dan tanpa glutaraldehida tidak jauh berbeda, hal ini dikarenakan glutaraldehida dan gom guar tidak mengandung unsur anorganik, jadi abu yang dihasilkan kecil. Secara umum mikrokapsul yang dihasilkan mempunyai kadar abu yang kecil.
Hasil SEM Mikrokapsul
.
Mikrokapsul kosong dengan penambahan glutaraldehida dan gom guar jika diamati dari hasil SEM (Gambar 14) mempunyai ukuran sekitar 1-9µm. Mikrokapsulnya terlihat kisut dan berlubang yang disebabkan karena VCO sebagai bahan pengisi tidak ditambahkan ke dalam larutannya.
Hasil SEM mikrokapsul VCO dengan penambahan glutaraldehida dan gom guar (Gambar 15) memperlihatkan ukuran mikrokapsul dari sekitar 2-14µm. Jika dibandingkan dengan ukuran mikrokapsul kosongnya, mikrokapsul ini berukuran lebih besar, karena mikrokapsul ini sudah diisi dengan bahan pengisinya, yaitu VCO. VCO yang ditambahkan ke dalam larutan akan mengisi ruang kosong di dalam mikrokapsul, sehingga membuat mikrokapsul menjadi bertambah ukurannya.
Hasil SEM juga memperlihatkan bentuk mikrokapsul yang halus, tidak kisut, dan tidak berlubang. Tetapi mikrokapsul ini terlihat tidak terpisah sempurna antara tiap butirannya. Hal ini diduga disebabkan karena VCO yang bersifat non polar akan berinteraksi dengan sisi non polar pada kitosan, dan sisi polar pada kitosan dan glutaraldehida akan berinteraksi dengan sisi polar antar kitosan, sehingga terjadi hubungan antara tiap kulit mikrokapsul yang merupakan sisi-sisi polar pada kitosan.
Gambar 15 memperlihatkan morfologi mikrokapsul dari hasil SEM yang memperlihatkan bahwa pada tiap mikrokapsul VCO dengan penambahan glutaraldehida dan gom guar tidak memisah sempurna menjadi satu butiran yang utuh, tetapi saling berikatan antara mikrokapsul yang satu dengan mikrokapsul lainnya.
Gambar 15 Struktur permukaan mikrokapsul VCO dengan penambahan glutaraldehida dan gom guar
Mikrokapsul kosong tanpa penambahan glutaraldehida dan gom guar mempunyai ukuran antara 0,5-10 m (Gambar 16). Secara
umum morfologi mikrokapsul berbentuk kisut dan terlipat ke dalam yang menandakan ada rongga kosong di dalamnya. Lipatan ke dalam tersebut akibat keadaan vakum ketika pengambilan gambar oleh alat SEM. Menurut Wawensyah (2006), jika tidak dalam keadaan vakum, diperkirakan rongga tersebut berisi udara dengan rongga tunggal (monocore). Keadaan vakum ini juga yang
mengakibatkan semua mikrokapsul memiliki struktur permukaan kisut karena kulit mikrokapsul tertarik ke dalam akibat udara dalam rongga yang dikeluarkan.
Gambar 16 Struktur permukaan mikrokapsul kosong tanpa penambahan glutaraldehida dan gom guar (insert: mikrokapsul yang terlipat ke dalam
Mikrokapsul VCO tanpa penambahan glutaraldehida dan gom guar memiliki ukuran antara 1-10 m. Dari hasil SEM (Gambar 17) terlihat kalau mikrokapsul yang dihasilkan tidak semua berbentuk bulat, ada yang kisut dan bolong-bolong. Hal ini menunjukkan bahwa VCO tidak terkungkung sempurna, yang berarti tidak semua mikrokapsul ini berisi VCO.
Gambar 17 Struktur permukaan mikrokapsul VCO tanpa penambahan glutaraldehida dan gom guar
[image:30.612.352.495.227.333.2] [image:30.612.342.493.510.622.2] [image:30.612.149.297.522.622.2]dengan baik sebelum dimasukkan ke dalam alat pengering semprot sehingga pada saat pengeringan, mikrokapsul yang dihasilkan bentuknya tidak seragam.
Ukuran mikrokapsul ini juga bergantung pada ukuran nozzle dari alat pengering
semprot. Semakin kecil lubang nozzle,
diameter mikrokapsul semakin kecil. Demikian halnya jika semakin besar ukuran
nozzle, maka diameter mikrokapsul yang
terbentuk semakin besar. Alat pengering semprot yang digunakan pada penelitian ini mempunyai ukuran diameter nozzle sebesar
0.5 mm.
Kandungan VCO dalam Mikrokapsul
Kandungan VCO dalam mikrokapsul diperoleh setelah mikrokapsul tersebut diekstrak VCO nya dengan pelarut yang sesuai. Dalam penelitian ini digunakan n
[image:31.612.127.316.374.440.2]-heksana sebagai pelarut yang bersifat non polar, sesuai dengan sifat VCO yang non polar pula. Ekstraksi dilakukan dengan cara maserasi.
Tabel 3 Kandungan VCO dalam mikrokapsul Mikrokapsul Kandungan VCO
(%) VCO Dengan glutaral
dehida dan gom guar 21.08 VCO Tanpa glutaral
dehida dan gom guar 3.37
Kandungan VCO dalam mikrokapsul dengan penambahan glutaraldehida dan gom guar sebesar 21.08% (Tabel 3). Pada saat pembuatannya nisbah kitosan:VCO yang digunakan adalah 2:1, berarti pada mikrokapsul yang dihasilkan terdapat pengurangan kandungan VCO. Hal ini bisa disebabkan karena pada saat pencampuran VCO ke dalam kitosan belum tercampur sempurna atau belum terbentuk emulsi yang baik, sehingga pada saat pengeringan, VCO yang belum teremulsi itu hanya menempel pada dinding mikrokapsul, sehingga VCO itu mudah lepas dari mikrokapsul. Untuk kandungan VCO dalam mikrokapsul tanpa penambahan glutaraldehida dan gom guar diperoleh VCO sebesar 3.37% (Tabel 3). Hasil yang diperoleh ini jauh lebih kecil daripada mikrokapsul VCO yang menggunakan glutaraldehida dan gom guar. Jika diasumsikan jumlah pengemulsi yang digunakan dan pengadukan sebelum
dikeringkan pada dua variasi tersebut sama, maka hal ini mungkin disebabkan tidak adanya pengikat silang dalam campuran yang dapat membuat VCO terkungkung kuat di dalam kitosan, akibatnya VCO dalam campuran yang tidak menggunakan glutaraldehida dan gom guar lebih mudah keluar karena tidak terkungkung baik dalam kitosan.
Penambahan pengikat silang seperti glutaraldehida pada kitosan juga dapat membuat ukuran pori kitosan semakin kecil, dan membuat struktur kitosan menjadi lebih rapat dan kuat. Pada mikrokapsul VCO yang menggunakan glutaraldehida, VCO yang sudah terkungkung dalam kitosan akan lebih sukar kembali keluar karena pori-pori kitosannya lebih kecil, sedang pada mikrokapsul tanpa penambahan glutaral dehida, VCO yang sudah terkungkung dalam kitosan lebih mudah kembali keluar dari kitosan karena ukuran porinya lebih besar daripada ukuran pori kitosan dengan penambahan glutaraldehida. Hal ini bisa dilihat dari hasil SEM mikrokapsul VCO tanpa glutaraldehida (Gambar 16) yang bentuknya tidak seragam, ada yang bulat halus menandakan mikrokapsul itu terisi VCO, dan ada juga yang kisut dan bolong-bolong yang menandakan VCO tidak mengisi ruang kosong dalam kitosan tersebut.
Hasil Analisis Kandungan Asam Laurat
Asam laurat dalam VCO dianalisa kandungannya menggunakan alat kromatografi gas. Hasil dari kromatografi gas berupa kromatogram yang menunjukkan area, tinggi puncak, dan waktu retensi dari suatu senyawa yang dianalisis. Penentuan kadar suatu senyawa diperoleh dengan membandingkan kromatogram suatu senyawa itu dengan kromatogram standar senyawa tersebut.
Kondisi operasional kromatografi gas untuk VCO menggunakan kolom sianopropil metil sil yang merupakan kolom kapiler dengan panjang 60m, diameter 0.25mm, dan ketebalan film 25 m. Laju alir gas N2, H2, dan
udara berturut-turut 20mL/menit, 30 mL/menit, dan 200-250mL/menit. Suhu injektor dan detektor yang digunakan sebesar 200oC dan 230oC. Volume injeksi sebesar
Gambar 18 Kromatogram VCO sebelum dibuat mikrokapsul
Tabel 4 Hasil kromatografi gas dari VCO sebelum dibuat mikrokapsul Asam lemak Waktu retensi
(menit) Luas area Asam laurat 7.635 1893630 Asam kaprat 6.852 268024 Asam kaprilat 6.405 327961
[image:32.612.132.503.336.623.2]Tabel 5 Hasil GC dari VCO pada mikrokapsul dengan penambahan glutaraldehida dan gom guar
Asam lemak Waktu retensi
(menit) Luas area Asam laurat 7.630 1389891 Asam kaprat 6.849 200576 Asam kaprilat 6.401 250596
Gambar 20 Kromatogram VCO pada mikrokapsul tanpa penambahan glutaraldehida dan gom guar
Tabel 6 Hasil GC dari VCO pada mikrokapsul tanpa penambahan glutaraldehida dan gom guar
Asam lemak Waktu retensi (menit)
Luas area
[image:33.612.130.506.440.700.2]Asam laurat 7.665 1426259 Asam kaprat 6.875 220529 Asam kaprilat 6.422 317052
Tabel 7 Hasil kromatografi gas dari asam lemak standar
Asam lemak Waktu retensi
(menit) Luas area Asam laurat 7.639 925588 Asam kaprat 6.854 898948 Asam kaprilat 6.401 810853
Hasil dari kromatografi gas berupa waktu retensi dan puncak dari masing-masing komponen. Jika recorder dilengkapi dengan integrator maka waktu retensi dan luas
puncak langsung diperoleh dari integrator. Waktu retensi itu lalu dibandingkan dengan waktu retensi standarnya untuk mendapatkan informasi mengenai jenis dari komponen-komponen dalam contoh. Waktu retensi merupakan waktu yang dibutuhkan suatu senyawa selama injeksi sampai keluar puncak maksimum (Grob & Barry 2004).
Waktu retensi digunakan untuk uji kualitatif suatu bahan. Kromatogram menunjukkan puncak-puncak dari tiap senyawa yang dikandungnya, juga waktu retensi dari tiap senyawa itu. Waktu retensi suatu senyawa berbeda dengan waktu retensi senyawa lainnya. Kromatogram dari bahan yang diuji kemudian dibandingkan dengan kromatogram senyawa standarnya. Jika waktu retensi dari suatu bahan adalah sama atau mendekati waktu retensi senyawa standarnya, maka bahan itu mengandung senyawa yang sama dengan senyawa standarnya.
Luas area bisa digunakan untuk uji kuantitatif. Luas area dari suatu senyawa itu dibandingkan dengan luas area standarnya untuk mengetahui konsentrasi senyawa tersebut.
Tabel 8 Kandungan asam lemak dalam VCO hasil analisa kromatografi gas Asam
lemak VCO 1 (%b/b) VCO 2 (%b/b) VCO 3 (%b/b) As. Laurat 42.62 35.12 31.94 As. Kaprat 6.21 5.22 5.08 As. kaprilat 8.43 7.23 8.10 Keterangan :
VCO1: VCO sebelum dibuat mikrokapsul VCO2: VCO pada mikrokapsul dengan
penambahan glutaraldehida dan gom guar
VCO3: VCO pada mikrokapsul tanpa penambahan glutaraldehida dan gom guar
Tabel 8 memperlihatkan kandungan asam lemak dalam VCO yang dianalisis dengan kromatografi gas. Dari tabel terlihat bahwa
kandungan asam laurat tertinggi terdapat pada VCO yang belum dibuat mikrokapsul, yaitu 42.62% (Lampiran 7), sedang pada VCO yang dibuat mikrokapsul dengan penambahan glutaraldehida dan gom guar asam lauratnya sebesar 35.12%. Nilai asam laurat paling kecil adalah pada VCO yang dibuat mikrokapsul tanpa penambahan glutaraldehida dan gom guar, yaitu 31.94%. Kadar asam laurat pada kedua mikrokapsul mengalami penurunan jika dibandingkan dengan kadar asam laurat pada VCO tanpa perlakuan, hal ini diduga disebabkan karena adanya pemanasan suhu tinggi saat pengeringan pada alat pengering semprot. Suhu pengeringan yang digunakan sebesar 180oC, sedang titik didih asam laurat
sebesar 131oC, sehingga diduga terjadi
kehilangan asam laurat selama pengeringan berlangsung.
Kadar asam laurat pada mikrokapsul dengan penambahan glutaraldehida dan gom guar lebih besar dari mikrokapsul tanpa glutaraldehida dan gom guar diduga disebabkan karena pengaruh pengekstrakan VCO dari mikrokapsulnya yang kurang sempurna. Juga penambahan glutaraldehida membuat pori-pori kitosan menjadi lebih kecil sehingga VCO yang terkungkung tidak mudah keluar dari mikrokapsul, juga bahan-bahan lain pun tidak mudah masuk ke dalam mikrokapsul yang dapat mempengaruhi kadar asam lauratnya.
Asam laurat digunakan sebagai senyawa acuan dalam penentuan kandungan asam lemak pada VCO karena memiliki konsentrasi paling tinggi diantara asam lemak lainnya dalam VCO, juga merupakan asam lemak yang paling berperan dalam penggunaan VCO bagi kesehatan manusia.
SIMPULAN DAN SARAN
Simpulan
[image:34.612.128.308.100.158.2] [image:34.612.128.309.526.584.2]dan gom guar berturut-turut sebesar 42.62%, 35.12%, dan 31.94%.
Saran
Perlu dilakukan penelitian lebih lanjut untuk mengetahui kondisi optimum pada alat
spray dryer untuk pembuatan mikrokapsul
dengan metode spray dry, juga perlu
dilakukan penelitian lebih lanjut untuk mengetahui kondisi optimum untuk konsentrasi kitosan, VCO, glutaraldehida, dan pengemulsi agar diperoleh mikrokapsul yang cukup kering dan tersalut sempurna. Sebaiknya digunakan senyawa pengikat silang lain yang lebih aman untuk tubuh karena glutaraldehida bersifat neurotoksik.
DAFTAR PUSTAKA
Aisyah IN. 2005. Pembengkakan hidrogel kitosan-polivinil alkohol [skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
AOAC, Cunnif P, editor. 1999. Official Methods of Analysis of AOAC International. 5th Revision. Volume 2.
Maryland: AOAC International.
Ariati F. 1998. Pengaruh penambahan bahan penyalut dan jumlah fraksi minyak terhadap mikroenkapsulasi konsentrat asam lemak omega-3 dengan metode
spray drying [skripsi]. Bogor: Fakultas
Teknologi Pertanian, Institut Pertanian Bogor.
Bhandari BR, Dumoulin ED, Richard HMJ, Noleau I, Lebert AM. 1992. Flavorencapsulation by spray drying: application to citral and linalyl acetate.http://www.wsu.edu/gmhyde/433 _web_pages/drying-webpages98/ spraydry/microencapsulation.htm [10 Jan 2006].
Chaplin M. 2005. Guar gum. London: South Bank University. http://chem.skku.ac. kr/~wkpark/tutor/mirror/www.martin.cha plin.btinternet.co.uk/hygua.html [1 Desember 2005].
Deymonaz C, Hobson M, Diaz D, Guidinger N. 1998. Spray drying. http:// www.wsu.edu/ gmhyde/43_web_pages/
drying-web-pages98/spray-dry/ spray-drying-intro. htm [9 Jan 2006].
Durant YG. 2002. Microcapsule morphology in microencapsulation processes, fundamental chemical differences http://www.unh.edu/apl/communications/ CRSO2. pdf [15 Nov 2005].
Dziezak JD. 1988. Microencapsulation and encapsulatedingredients.http://wsu.edu/- gmhyde/433_web_pages/drying-web-pages98/spray-dry/ microencapsulation. htm [10 Jan 2006].
Fardiaz D. 1989. Hidrokoloid. Bogor: Pusat
Antar Universitas Pangan dan Gizi, Institut Pertanian Bogor.
Khan TA, Peh KK, Ch’ng HS. 2002. Reporting degree of deacetylation values of chitosan: the influence of analytical methods. J Pharm Pharmacet Sci
5:205-212.
Kristiani S. 1997. Studi mikroenkapsulasi dan stabilitas minyak kaya asam lemak gamma linolenat dari kapang Mortiriella Isabellina [skripsi]. Bogor: Fakultas
Teknologi Pertanian, Institut Pertanian Bogor.
Kshirsagar NA. 2000. Drug Delivery System.
Indian J Pharmacol 32: 54-61.
Noor RR. 2001. Scanning Electron Microscope. Bogor: Fakultas Peternakan,
Institut Pertanian Bogor.
Nussinovitch A. 1997. Hydrocolloid Applications. Israel: Chapman & Hall.
Rachman R. 2001. Scanning Electron Microscope. Bogor: Institut Pertanian
Bogor.
Rindengan B, Novarianto H. 2005.
Pembuatan dan Pemanfaatan Minyak Kelapa Murni. Jakarta: Penebar Swadaya.
Fakultas Teknologi Pertanian, Institut Pertanian Bogor.
Shepherd R, Reader S, Flshow A. 1999. Chitosan functional properties [editorial]. Glycoconjugate Journal 14:535-542.
Sugita P. 2005. Sintesis dan modifikasi kitosan sebagai adsorben ramah lingkungan. Usulan Hibah Penelitian Kompetisi A2. Bogor: Departemen Kimia, Institut Pertanian Bogor.
Sutiani A. 1997. Biodegradasi poliblend polistirena-pati [tesis]. Bandung: Program Pascasarjana, Institut Teknologi Bandung.
Sutriyo, Djajadisastra J, Novitasari A. 2004. Mikroenkapsulasi propanolol hidro-klorida dengan penyalut etil selulosa menggunakan metode penguapan pelarut.
Majalah Ilmu Kefarmasian 1:93-200.
Syah A N A. 2005. Mengenal Lebih Dekat Virgin Coconut Oil, Minyak Penakluk Aneka Penyakit. Jakarta: Agromedia
Pustaka.
Syarief R, Halid H. 1991. Teknologi Penyimpanan Pangan. Jakarta: Arcan.
Wang Tao, Turhan M, Gunasekaram S. 2004. Selected properties of pH-sensitive, biodegradable chitosan-poly(vinyl alcohol) hydrogel. Society of Chemical Industry. Polym Int. 53: 911-918.
Wawensyah J A. 2006. Mikroenkapsulasi minyak atsiri jahe merah dengan penyalut kitosan [skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Wibowo S. 2005. VCO: Pencegahan Komplikasi Diabetes. Jakarta: Pawon.
Winarno FG. 1997. Kimia Pangan dan Gizi.
Jakarta: Gramedia.
Lampiran 1 Diagram alir penelitian
Pencirian Kitosan
+ Asam asetat 1%
+ Gom guar
+ Glutaraldehida GC
Tween 80 + + Tween 80 Kadar air
Kitosan
Larutan kitosan 4%
VCO
VCO
Pengering Semprot
Mikrokapsul VCO-Glu
Mikrokapsul VCO
GC
Pencirian mikrokapsul
SEM
Kadar abu
Kadar air
GC
Pencirian mikrokapsul
Lampiran 2 Metode pembuatan pereaksi
Pembuatan larutan asam asetat 1% (v/v)
Sebanyak 1 ml asam asetat glasial dimasukan ke dalam labu takar 100 ml, kemudian ditera dengan akuades sampai tanda tera.
Pembuatan larutan kitosan 4% (b/v)
Sebanyak 4 gram kitosan larutkan ke dalam 100 ml asam asetat 1%
Pembuatan larutan gom guar 0,33% (b/v)
Sebanyak 0,33 gram gom guar dilarutkan dengan akuades sampai mencapai volume total 100 ml.
Pembuatan larutan glutaraldehida 4,86%
Lampiran 3 Data hasil pengukuran kadar air dan abu kitosan.
Kadar air dan abu kitosan
Ulangan ke- Sampel Kadar air (%) Kadar abu (%)
1 Kitosan 8.27 0.59
2 Kitosan 6.63 0.42
3 Kitosan 8.26 0.54
Rerata 7.72 0.52
Lampiran 4 Data hasil pengukuran kadar air dan abu mikrokapsul
Kadar air dan abu mikrokapsul
mikrokapsul Ulangan ke- Kadar air (%) Kadar abu (%) VCO - glutaraldehida 1 13.19 0.27
2 12.87 0.21
3 13.07 0.33
Rerata 13.04 0.27
Kosong 1 17.95 0.35
2 17.23 0.19
3 17.76 0.25
Rerata 17.64 0.26 VCO – tanpa glutaraldehida 1 17.17 0.55
2 18.36 0.47
3 17.83 0.52
Rerata 17.78 0.51
Kosong 1 20.67 0.38
2 20.15 0.34
3 20.56 0.43
Rerata 20.46 0.38
Lampiran 5 Kadar air VCO
Ulangan Kadar air (%)
1 0.39
2 0.53
3 0.54
Lampiran 6 Perhitungan derajat deasetilasi kitosan
Spektrum FTIR Kitosan
Perhitungan derajat deasetilasi:
C
F
Lampiran 7 Perhitungan kadar senyawa dalam VCO
Penentuan kadar senyawa:
Dimana :
Cx = konsentrasi komponen x Cs = konsentrasi standar Ax = luas area komponen x As = luas area standar
Contoh senyawa: asam laurat
C asam laurat = 42.62% X Cs X
100
Vcontoh
X 100%As
Ax
Cx =
Bobot contoh
100
1
mL
19.2 mg
925588
1893630
X 0.4% X X 100%