54
LAMPIRAN 1
DATA PERCOBAAN
L1.1 DATA RENDEMEN Virgin Coconut Oil (VCO)
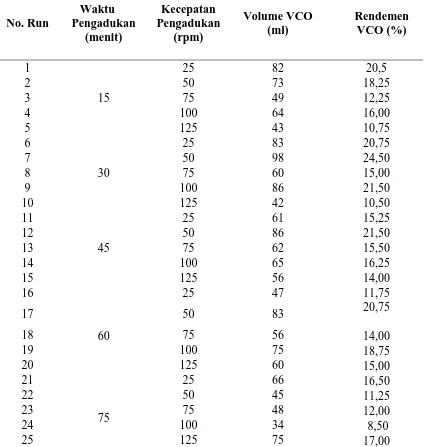
Dari hasil percobaan diperoleh data rendemen VCO sebagai berikut: Tabel L1.1 Data Rendemen VCO
No. Run Waktu Pengadukan (menit) Kecepatan Pengadukan (rpm) Volume VCO (ml) Rendemen VCO (%) 1 15
25 82 20,5
2 50 73 18,25
3 75 49 12,25
4 100 64 16,00
5 125 43 10,75
6
30
25 83 20,75
7 50 98 24,50
8 75 60 15,00
9 100 86 21,50
10 125 42 10,50
11
45
25 61 15,25
12 50 86 21,50
13 75 62 15,50
14 100 65 16,25
15 125 56 14,00
16
60
25 47 11,75
17 50 83 20,75
18 75 56 14,00
19 100 75 18,75
20 125 60 15,00
21 25 66 16,50
22
75
50 45 11,25
23 75 48 12,00
24 100 34 8,50
55
Pada Tabel L1.1 di atas terlihat besar rendemen virgin coconut oil (VCO) dari 25 run, yang dinyatakan dalam satuan %. Besar rendemen VCO didapat dengan membandingkan volume VCO yang didapat dari setiap run dengan volume bahan baku yaitu santan kelapa (yang volumenya 400 ml). Metode perhitungannya dapat dilihat pada Lampiran 3.
L1.2 DATA KADAR VCO
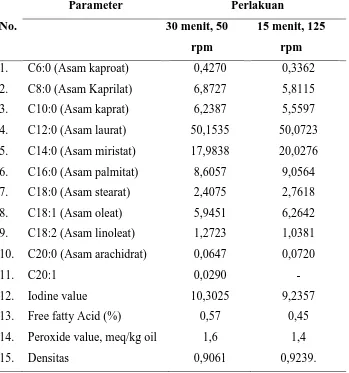
Dari hasil percobaan diperoleh data kadar virgin coconut oil (VCO) sebagai berikut dimana untuk analisa GC, bilangan peroksida, bilangan iod dan densitas hanya dilakukan pada rendemen VCO tertinggi yaitu pada perlakuan waktu pengadukan 30 menit dan kecepatan pengadukan 50 rpm dan terendah pada waktu pengadukan 15 menit dan kecepatan pengadukan 125 rpm seperti terlihat pada tabel berikut:
Tabel L1.2 Data Kadar VCO
No.
Parameter Perlakuan
30 menit, 50
rpm
15 menit, 125
rpm
1. C6:0 (Asam kaproat) 0,4270 0,3362
2. C8:0 (Asam Kaprilat) 6,8727 5,8115
3. C10:0 (Asam kaprat) 6,2387 5,5597
4. C12:0 (Asam laurat) 50,1535 50,0723
5. C14:0 (Asam miristat) 17,9838 20,0276 6. C16:0 (Asam palmitat) 8,6057 9,0564
7. C18:0 (Asam stearat) 2,4075 2,7618
8. C18:1 (Asam oleat) 5,9451 6,2642
9. C18:2 (Asam linoleat) 1,2723 1,0381 10. C20:0 (Asam arachidrat) 0,0647 0,0720
11. C20:1 0,0290 -
12. Iodine value 10,3025 9,2357
13. Free fatty Acid (%) 0,57 0,45
14. Peroxide value, meq/kg oil 1,6 1,4
56
57
LAMPIRAN 2
HASIL ANALISA MINYAK KELAPA MURNI
L2.1 HASIL ANALISA MINYAK KELAPA MURNI SAMPEL 50 RPM 30
MENIT
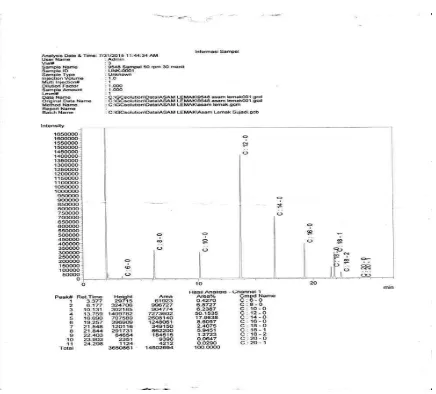
Gambar L.2.1 Hasil Analisa Gas Kromatografi pada Kecepatan Pengadukan 50 rpm dan Waktu Pengadukan 30 menit
58
L2.1 HASIL ANALISA MINYAK KELAPA MURNI SAMPEL 125 RPM 15
MENIT
Gambar L.2.1 Hasil Analisa Gas Kromatografi pada Kecepatan Pengadukan 125 rpm dan Waktu Pengadukan 15 menit
59
LAMPIRAN 3
CONTOH PERHITUNGAN
L3.1 PERHITUNGAN BAHAN BAKU
Volume santan : 400 ml
Untuk perlakuan run 1 : 10 % penambahan inokulum (v/v)
Maka volume inokulum yang ditambahkan untuk semua run: 10010 x 400
L3.2 PERHITUNGAN RENDEMEN MINYAK KELAPA MURNI
Perhitungan rendemen dilakukan dengan cara membandingkan antara volume produk yang dihasilkan dengan volume bahan baku awal, dengan rumus :
volume santan awalvolume VCO jadi x 100
Misal, untuk Run 12 diperoleh volume VCO (produk jadi) sebesar 86 ml dari volume awal 400 ml santan kelapa, maka perhitungannya adalah :
40086 x 100
60
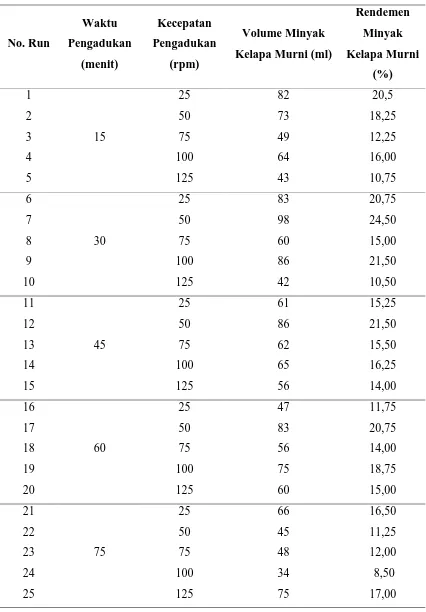
Tabel L3.1Rendemen Minyak Kelapa Murni untuk Masing-masing Run
No. Run Waktu Pengadukan (menit) Kecepatan Pengadukan (rpm) Volume Minyak
Kelapa Murni (ml)
Rendemen Minyak Kelapa Murni (%) 1 15
25 82 20,5
2 50 73 18,25
3 75 49 12,25
4 100 64 16,00
5 125 43 10,75
6
30
25 83 20,75
7 50 98 24,50
8 75 60 15,00
9 100 86 21,50
10 125 42 10,50
11
45
25 61 15,25
12 50 86 21,50
13 75 62 15,50
14 100 65 16,25
15 125 56 14,00
16
60
25 47 11,75
17 50 83 20,75
18 75 56 14,00
19 100 75 18,75
20 125 60 15,00
21
75
25 66 16,50
22 50 45 11,25
23 75 48 12,00
24 100 34 8,50
61
L3.3 PERHITUNGAN ANALISA MINYAK KELAPA MURNI
Analisa data yang dilakukan antara lain analisa bilangan peroksida, analisa bilangan iodin, analisa FFA dan analisa densitas dimana pada penelitian ini analisa hanya dilakukan pada rendemen minyak kelapa murni tertinggi yaitu pada perlakuan kecepatan pengadukan 50 rpm, 30 menit waktu pengadukan dan rendemen terendah yaitu pada perlakuan kecepatan pengadukan 125 rpm, 15 menit waktu pengadukan.
L3.3.1 Analisa Kadar Air
Untuk perlakuan 50 rpm, 30 menit Berat Awal = 2,160 gram
Berat Akhir = 2,135 gram
% kadar air =
= 1,157 %
L3.3.2 Analisa Bilangan Peroksida
Untuk perlakuan 50 rpm, 30 menit: w
Dimana:
Vs: volume Na2S2O3
N : normalitas larutan Na2S2O3 W : berat cuplikan
PV: peroxide value Pada perlakuan ini: Vs = 0,82 ml N = 0,01 W = 5 gram Maka:
5
L3.3.3 Analisa Bilangan iodin
62 w
A: volume blanko B: volume pentiter N : normalitas pentiter W : berat cuplikan IV: iodine value
Dimana pada perlakuan ini A= 50 ml
B = 42,5 ml N = 0,1 W = 1,0025 Maka:
1,0025
L3.3.4 Analisa Densitas
Untuk perlakuan 125 rpm, 15 menit
Mpikno = 28,4 gr Maka:
L3.3.5 Analisa FFA
Analisa FFA dilakukan pada semua run berikut contoh perhitungan analisa FFA. Untuk perlakuan 50 rpm, 30 menit:
63 V = volume NaOH dalam peniteran (ml) N = Normalitas NaOH
M = Bobot contoh (gr)
200 = Bobot molekul asam laurat
=
64
LAMPIRAN 4
DOKUMENTASI PENELITIAN
L4.1 FOTO PEMBUATAN VCO
Gambar L4.1 Foto Pemisahan skim dan krim
65
Gambar L.4.3 Foto terbentuk 3 lapisan yaitu air, blondo dan VCO
L4.2 FOTO PROSES ANALISA VCO
Gambar L4.4 Foto Hasil Titrasi Analisa FFA
L4.3 FOTO ANALISA DENSITAS
66 L4.3 FOTO HASIL VCO
50
DAFTAR PUSTAKA
[1] Ahmad Alreza,. Pengaruh Bahan Pelapis Terhadap Karakteristik Kelapa Muda Siap Saji Selama Penyimpanan. Fakultas Teknologi Pertanian Institutut Pertanian Bogor. Bogor. 2012
[2] Bregas S.T .Sembodo, Ardiena Noorlyta, Nur Erika Laila M. Pengaruh Kecepatan Putar Pengaduk Proses Pemecahan Emulsi Santan Buah Kelapa Menjadi Virgin Coconut Oil (VC0). Ekuilibrium Vol. 9. No. 1. Halaman:17-22. ISSN:1412-9124. 2010
[3] Anita Dewi. Evaluasi Metode Ekstraksi Minyak Kelapa Murni Ditinjau Dari Total Rendemen Dan Sifat Fisikomia Selama Penyimpanan. Skripsi. Program Studi Teknologi Pangan Fakultas Pertanian Universitas Katolik Soegijapranata. Semarang. 2006
[4] Cahyono Dan Lia Untari. Proses Pembuatan Virgin Coconut Oil (VCO) Dengan Menggunakan Starter Ragi Tempe. Jurusan Teknik Kimia. Fakultas Teknik. Universitas Diponegoro. 2012
[5] Fachry, A. Rasyidi dkk. Pembuatan Virgin Coconut Oil Dengan Metode Sentrifugasi. Seminar Nasional Teknik Kimia Indonesia BBTP Vol. 20, No. 1, 2006
[6] Firman Budiman, Obrin Ambari dan Azhary H. Surest. Pengaruh Waktu Fermentasi Dan Perbandingan Volume Santan Dan Sari Nanas Pada Pembuatan Virgin Coconut Oil (VCO). Jurnal Teknik Kimia Jurusan Teknik Kimia Fakultas
Teknik Universitas Sriwijaya No. 2, Vol. 18, 2012
[7] Farida, Rahim. 2011. Pemanfaatan Zat Warna Dari Ekstrak Cyphomandra Betacea Dan Minyak Kelapa Murni Dalam Formulasi Lipstik. Scientia STIFI
Perintis Padang,Vol.1 No. 2. ISSN : 2087 – 5045. 2011
[8] Didik Purwanto. Pengaruh Desain Impeller, Baffel, Dan Kecepatan Putar Pada Proses Isolasi Minyak Kelapa Murni Dengan Metode Pengadukan. Seminar
Nasional Aplikasi Sains dan Teknologi 2008 – IST AKPRIND Yogyakarta. Jurusan Teknik Kimia Institut Teknologi Adhi Tama Surabaya (ITATS). 2008
[9] Ngatemin, Nurrahman, Joko Teguh Isworo.. Pengaruh Lama Fermentasi Pada Produksi Minyak Kelapa Murni (Virgin Coconut Oil) Terhadap Sifat Fisik, Kimia, Dan Organoleptik. Jurnal Pangan dan Gizi Vol. 04 No. 08. 2013
51
[11] Heny Kusumayanti, Margaretha Tuti Susanti. Mohamad Endvyulianto. Apilkasi Rhizopus oligosporus, Rhizopus oryzae, Isi Tubuh Kepiting dan Enzim Bromelin pada Bioekstraksi Krim Santan Kelapa menjadi Virgin Coconut Oil. JurusanTeknik Kimia PSD III Fakultas Teknik Universitas Diponegoro. 2012 [12] Y.C.Wong and H. Hartina. Virgin Coconut Oil Production by Centrifugation Method. Oriental Journal Of Chemistry Faculty of Agro Based Industry,
Universiti Malaysia Kelantan, Malaysia. Vol. 30(1), 237-245. 2014
[13] Panpanya, Supamas Siwalak Pathaveerat. Study and design manufacture of virgin coconut oil by centrifuge method. Department of agricultural Engineering, Faculty of Engineering, Kasetsart University. The International conference of the
Thai Society of Agricultural Engineering Chiangmai, Thailand. 2012
[14] Nely R Fatwatun,Kaunaini Chusna dan Bambang Pramudono. Pembuatan Virgin Coconut Oil (VCO) Dengan Pemecahan Emulsi Dengan Metode Ultrasonik. Jurnal Teknologi Kimia dan Industri, Jurusan Teknik Kimia, Fakultas
Teknik, Universitas Diponegoro.Vol. 2, No. 4, Tahun 2013, Halaman 184 –
188.2013
[15] LarasCristiatidan Adi Hendra Prakoso. Pembuatan Minyak Kelapa Murni (Virgin Coconut Oil) Menggunakan Fermentasi Ragi Tempe. Laporan Tugas Akhir Program Studi DIII Teknik Kimia Jurusan Teknik Kimia Fakultas Teknik. Universitas Sebelas Maret. Surakarta. 2009
[16] Kumalla M, Larose, Sumardi H.S, M. Bagus Hermanto. Uji Performansi Pengering Semprot Tipe Buchi B-290 Pada Proses Pembuatan Tepung Santan.
Jurnal Bioproses Komoditas Tropis, Jurusan Keteknikan Pertanian Fakultas Teknologi Pertanian. Universitas Brawijaya, Vol. 1 No. 1, 2013
[17] Muhammad Hairi. Pengaruh Umur Buah Nanas Dan Konsentrasi Ekstrak Kasar Enzim Bromelin Pada Pembuatan Virgin Coconut Oil Dari Buah Kelapa Typical (Cocos nucifera L.). Laporan Skripsi Jurusan Kimia. Fakultas Sains Dan Teknologi. Universitas Islam Negeri Maulana Malik Ibrahim. Malang. 2010 [18] Tri Widiandani, Purwanto, Suko Hardjono, Bambang Tri P, Rully Susilowati dan Nuzul W Diyah. 2010. Upaya Peningkatan Kualitas Minyak Kelapa Yang Dibuat Dari Cocos Nucifera L Dengan Berbagai Metode Kimiawi Dan Fisik. Departemen Kimia Farmasi, Fakultas Farmasi Universitas Airlangga, Surabaya [19] Sasniwati Sari Hasibuan. Pengggunaan Minyak Kelapa Murni (VCO) Sebagai Pelembab Dalam Sediaan Krim. Skripsi.Fakultas Farmasi Universitas Sumatera Utara Medan. 2011
[20] Mansor, T. S. T., Che Man, Y. B., Shuhaimi ,M, Abdul Afiq ,M. J. and Ku Nurul, F. K. M. Physicochemical properties of virgin coconut oil extracted from different processing methods. International Food Research Journal Universiti
52
[21] Sari Nilam dan Lien Damayanti. Analisis Titik Impas (BEP) Virgin Coconut Oil Pada Kub ”Yevo Mulia” Desa Lalombi Kecamatan Banawa Selatan Kabupaten Donggala. J. Agroland Jurusan Sosial Ekonomi Pertanian Fakultas
Pertanian Universitas Tadulako, Palu 15 (2) : 129 - 134, ISSN : 0854 –
641X.2008
[22] HanafiahWs, Eva Maria Widyasari, Nanny Kartini Oekar. Virgin Coconut Oil (VCO) Bertanda Radioiodium-131 .Jurnal Sains dan Teknologi Nuklir
Indonesia Indonesian Pusat Teknologi Nuklir Bahan dan Radiometri – BATAN,
vol. XII, No.2, hal 75-84. ISSN 1411 – 3481. 2011
[23] APCC. Asian and Pacific Coconut Community StandartFor Virgin Coconut Oil. http://www. apccsec.org. 2004
[24] Julius Pontoh, Mariana Br. Surbakti dan Mayz Papilaya. Kualitas Virgin Coconut Oil Dari Beberapa Metode Pembuatan. Jurnal Chem. Prog. Jurusan
Kimia Fakultas MIPA UNSRAT Manado, vol. 1, No. 1, 2008
[25] Nour, A. H. Demulsification of virgin coconut oil by centrifugation methods : A Feasibility Study. International Jurnal of Chemical Techonology, 2, hal 59-64. 2009
[26] Winarno, F.G. Kimia PangandanGizi. Jakarta: PT Gramedia. 1997.
[27] Rommel Doloksaribu. Pengaruh Konsentrasi Starter Saccharomyces cereviceae Dan Waktu Fermentasi Terhadap Hasil Dan Mutu Minyak Kelapa Virgin Coconut Oil. Tesis Program Magister Biologi Program Magister Biologi Fakultas Matematika Dan Ilmu Pengetahuan Alam. Universitas Sumatera Utara. 2010
[28] Nuraini, Rahayu Endah. Pengaruh Waktu Fermentasi Saccharomyces cereviceae Terhadap Ketengikan Dan Kejenuhan Virgin Coconut Oil (VCO). Skripsi IKIP PGRI Semarang. Fakultas Matematika Dan Ilmu Pengetahuan Alam. Program Studi Pendidikan Biologi. Semarang. 2013
[29] Ahmad, Riza Zainuddin. Pemanfaatan Khamir Saccharomyces cereviseae Untuk Ternak. Balai Penelitian Veteriner. Wartazoa Vol. 15, No. 1. Hal:49-51. Bogor. 2005
[30] Idral De Daniel, Marniati Salim, dan Elida Mardiah. Pembuatan Bioetanol Dari Ampas Sagu Dengan Proses Hidrolisis Asam Dan Menggunakan Saccharomyces cerevisiae. Laboratorium Bioteknologi Jurusan Kimia FMIPA, Universitas Andalas. 2012
[31] Raudah, Ernawati. Pemanfaatan Kulit Kopi Arabika Dari Proses Pulping Untuk Pembuatan Bioetanol. Jurnal Kimia Unand JurusanTeknik Kimia
53
[32] Arinda Kusuma Dewi, Cahya Setya Utamadan Sri Mukodiningsih. Kandungan Total Fungi Serta Jenis Kapang dan Khamir pada Limbah Pabrik Pakan yang Difermentasi dengan Berbagai Aras Starter Starfung. Agripet
Fakultas Peternakan dan Pertanian Universitas Diponegoro, Semarang.Vol 14,
No. 2, Oktober 2014
[33] Lucky IndratiUtami. Pengambilan minyak kelapa dengan proses fermentasi Menggunakan sacharomyces cereviceae amobil. Jurnal Penelitian Ilmu Teknik Vol.8, No.2: 86-95. 2008
[33] Mukhammad Asy’ari dan Bambang Cahyono. Pra-Standarisasi: Produksi dan Analisis Minyak Virgin Coconut Oil (VCO). JSKA .Laboratorium Biokimia
Jurusan Kimia FMIPA Universitas Diponegoro Semarang dan Pusat Pengembangan Obat dari Bahan Alam Universitas Diponegoro Semarang,Vol.IX.No.3.Tahun.2006
[34] Ria Rizqi Rachmawati, Yuni Sri Rahayu, Evie Ratnasari. Pengaruh Penambahan Buah Naga Merah (Hylocereusundatus) terhadap Kualitas Virgin Coconut Oil. Lentera Bio, Jurusan Biologi, Fakultas Matematika dan Ilmu
Pengetahuan Alam, Universitas Negeri Surabaya, Vol. 4 No. 1, Januari 2015, hal
101.
[35] Nodjeng MF, Feti J, Rorong A. Kualitas Virgin Coconut Oil yang Di buat Pada Metode Pemanasan Bertahap Sebagai Minyak Goreng dengan PenambahanWortel (Daucuscarrota L.). Jurnal Ilmiah Sains, Program Studi
Kimia FMIPA Universitas Sam Ratulangi, Vol. 13 (2): hal 102-109. 2013
[36] Riliani P.Maradesaa, Feti Fatimaha, Meiske S. Sangia. Kualitas Virgin Coconut Oil (VCO) Sebagai Minyak Goreng Yang Dibuat Dengan Metode Pengadukan Dengan Adanya Penambahan Kemangi (Ocimum sanctum). Jurnal
Mipa Unsrat Jurusan Kimia, FMIPA, Unsrat, Manado. Online 3 (1),2014
26
BAB III
METODOLOGI PENELITIAN
3.1Tempat dan Waktu Penelitian
Penelitian ini dilaksanakan di Laboratorium Proses Industri Kimia dan Laboratorium Mikrobiologi Industri Departemen Teknik Kimia, Fakultas Teknik, Universitas Sumatera Utara, Medan. Penelitian ini dilakukan selama kurang lebih 3 bulan.
3.2Alat Dan Bahan Penelitian
3.2.1 Alat
Alat yang diperlukan untuk pembuatan minyak kelapa murni sebagai berikut: 1. Wadah plastik transparan
2. Kertas saring 3. Termometer 4. Gelas ukur 5. Beaker gelas 6. Erlenmeyer 7. Pipet volume 8. Pipet tetes 9. Corong kaca 10.Pengaduk kaca 11.Botol kaca 12.Piknometer 13.Shaker
3.2.2 Bahan
3.1.2.1 Bahan Baku
1. Kelapa 2. Aquadest
27 3.1.2.2. Bahan Analisa
1. Aquadest 2. Alkohol 96 % 3. KOH
4. Indikator larutan Phenolphtalein 5. HCL
6. Asam asetat glasial 7. Kloroform
8. Kalium Iodida 9. Natrium Thiosulfat
3.3Prosedur Penelitian
Teknik Pembuatan minyak kelapa murni menggunakan fermentasi dengan khamir saccharomyces cereviseae sebagai berikut:
3.3.1 Pembuatan Krim/ Kanil.
1. Menyiapkan dan memilih daging kelapa yang sudah tua.
2. Memarut daging kelapa kemudian memeras daging kelapa parut hingga diperoleh santan.
3. Menambahkan air kedalam parutan kelapa dengan perbandingan 1,5 liter air untuk 1 kg kelapa lalu mengambil santannya.
4. Menyaring semua santan yang dihasilkan.
5. Mengendapkan santan yang telah disaring selama 30 menit, sehingga terbentuk dua lapisan yaitu: lapisan bawah berupa air dan lapisan atas berupa krim (kanil).
6. Memisahkan krim dan air dan membuang air yang tidak diperlukan.
3.3.2. Persiapan Starter
1. Skim yang diperoleh dari pembuatan santan dijadikan sebagai medium untuk pembuatan starter
2. Skim dimasukkan ke dalam botol sebanyak 1 liter
28
5. Mendinginkan skim yang sudah steril hingga suhu kamar
6. Sebanyak 2 (dua) ose khamir Saccharomyces cerevisiae diinokulasikan ke dalam medium skim
7. Diaduk selama 24 jam dengan menggunakan shaker 8. Dimasukkan ke dalam kulkas
3.3.3. Pembuatan Minyak VCO
1. Menampung krim/kanil yang terbentuk ke dalam toples transparan. 2. Menambahkan larutan bakteri dengan konsentrasi inokulum 10 %.
3. Kemudian krim dimasukkan kedalam aqua lalu larutan diaduk menggunakan shaker dengan kecepatan sesuai dengan variabel penelitian. 4. Mendiamkan campuran tersebut selama 24 jam, hingga terbentuk 3
lapisan. Lapisan paling atas merupakan minyak kelapa murni, lapisan tengah adalah blondo (ampas kanil) dan lapisan paling bawah adalah air. 5. Memisahkan minyak kelapa murni tersebut dari air dan blondo dan
melakukan penyaringan pada minyak.
6. Mengulang langkah diatas sesuai dengan variabel penelitian. 7. Perhitungan rendemen
Rendemen =Volume minyak VCO Volume kanil x 100 %
3.4. Karakteristik Minyak Kelapa Murni (VCO)
3.4.1 Analisa Bilangan Asam Lemak Bebas (FFA)
1. Menimbang 30 gram contoh minyak atau lemak dan memasukkan kedalam erlenmeyer 250 ml.
2. Menambahkan 50 ml etanol 95%. 3. Tambahkan 3 tetes -5 tetes indikator PP.
4. Titrasi dengan larutan standar NaOH 0,1 N hingga warna merah muda (tidak berubah selama 15 detik).
5. Lakukan penetapan duplo.
29 V = volume NaOH dalam peniteran (ml) N = Normalitas NaOH
M = Bobot contoh (gr)
200 = Bobot molekul asam laurat
3.4.2 Analisa Kadar Air
1. Menimbang sampel sebanyak 5 gram 2. Mencatat berat sampel (berat awal)
3. Dipanaskan dalam oven pada suhu 105 0C selama satu jam 4. Didinginkan dalam desikator selama ½ jam
5. Menimbang botol yang berisi sampel tersebut
6. Diulangi pemanasan dan penimbangan sampai diperoleh berat yang tetap 7. Mencatat berat sampel (berat akhir)
3.4.3 Analisa Bilangan Peroksida
1. Menimbang minyak seberat 5 gram, kemudian dimasukkan ke dalam Erlenmeyer 250 ml.
2. Ditambahkan 10 ml kloroform dan dilarutkan contoh dengan cara menggoyangkan erlenmeyer dengan kuat.
3. Ditambahkan 15 ml asam asetat glasial dan 1 ml larutan kalium iodida jenuh.
4. Ditutup erlenmeyer dan dikocok kira-kira 5 menit ditempat gelap pada suhu 15oC – 25 oC.
5. Tambahkan 75 ml air suling dan kocok dengan kuat
6. Dititrasi dengan larutan standar natrium thiosulfat 0,02 N dengan larutan kanji sebagai indikator
7. Dilakukan penetapan blanko 8. Dilakukan penetapan duplo
9. Hitung bilangan peroksida dalam contoh
Vo = Volume dari natrium thiosulfat untuk titrasi blanko (ml)
30
N = Normalitas larutan standar natrium thiosulfat yang digunakan M = berat contoh
3.4.4 Bilangan Iodin
1. Menimbang dengan teliti sejumlah contoh berdasarkan bilangan iod dari contoh kemudian dimasukkan ke dalam erlenmeyer bertutup asah.
2. Ditambahkan 15 ml pelarut (sikloheksan:asam asetat, 1:1) dengan menggunakan gelas ukur untuk melarutkan lemak.
3. Ditambahkan 25 ml larutan wijs dengan menggunakan pipet gondok kemudian erlenmeyer ditutup
4. Simpan selama 1-2 jam dalam ruangan gelap selama 1 jam.
5. Ditambahkan 10 ml larutan KI 20% dan 100 ml air suling. Erlenmeyer ditutup segera, kocok dan titrasi dengan larutan natrium tiosulfat 0,1 N dan larutan kanji sebagai indikator.
6. Dilakukan penetapan duplo. 7. Dilakukan peetapan blanko.
8. Dihitung bilangan iod dalam sampel.
3.4.5 Analisa Berat Jenis
1. Menimbang piknometer kosong
2. Mengisi picnimeter dengan aquadest sampai meluap dan tidak terbentuk gelembung udara kemudian menutupnya.
3. Menimbang piknometer dan isinya. 4. Mengukur suhu aquadest.
5. Melakukan hal yang sama pada contoh minyak. 3.4.6 Analisa Asam Lemak
31 3.5 FLOWCHART PENELITIAN
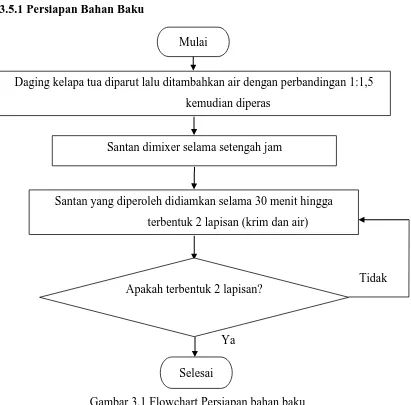
3.5.1 Persiapan Bahan Baku
Tidak
Ya
Gambar 3.1 Flowchart Persiapan bahan baku
Daging kelapa tua diparut lalu ditambahkan air dengan perbandingan 1:1,5 kemudian diperas
Santan yang diperoleh didiamkan selama 30 menit hingga terbentuk 2 lapisan (krim dan air)
Mulai
Apakah terbentuk 2 lapisan?
Selesai
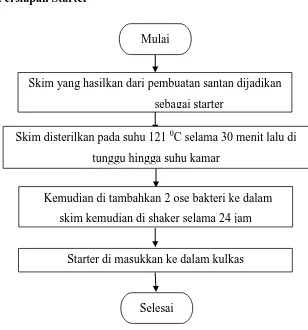
32 3.5. 2 Persiapan Starter
Gambar 3.2 Flowchart Pembuatan Starter Skim yang hasilkan dari pembuatan santan dijadikan
sebagai starter Mulai
Skim disterilkan pada suhu 121 0C selama 30 menit lalu di tunggu hingga suhu kamar
Starter di masukkan ke dalam kulkas
Selesai
33
3.5.3 Pembuatan Minyak Kelapa Murni (VCO)
Gambar 3.3 Flowchart Pembuatan Minyak Kelapa Murni (VCO) Ditampung krim/kanil yang terbentuk ke dalam beaker gelas.
Mulai
Didiamkan campuran tersebut selama 24 jam, hingga terbentuk 3 lapisan (minyak kelapa murni, blondo dan air)
Dipisahkan minyak kelapa murni tersebut dari air dan blondo dan melakukan penyaringan pada minyak.
Selesai
Kemudian krim dimasukkan kedalam botol aqua
Kenudian krim diaduk dengan shaker kecepatan pengadukan 25, 50, 75, 100 dan 125 rpm dan variasi waktu pengadukan
15, 30, 45, 60 dan 75 menit.
34
3.5.4 Flowchart Karakterisasi Minyak Kalapa Murni (VCO)
3.5.4.1 Analisa Bilangan Asam Lemak Bebas (FFA)
Gambar 3.4 Flowchart Analisa Bilangan Asam Dititrasi dengan menggunakan KOH 0,1 N dengan
indikator larutan phenolphtalein.
Diakhiri jika terbentuk atau terlihat warna merah jambu
Dihitung volume KOH yang terpakai Mulai
Ditimbang 20 gram sampel minyak atau lemak dan memasukkan kedalam erlenmeyer 250 ml.
Ditambahkan 50 ml alkohol netral 96% kemudian dipanaskan selama 10 menit.
35 3.5.4.2Analisa Kadar Air
Gambar 3.5 Flowchart Analisa Kadar Air Mulai
Ditimbang sampel sebanyak 5 gram
Mencatat berat sampel (berat awal)
Memanaskan sampel dalam oven pada suhu 105 0C
Menimbang botol yang berisi sampel tersebut
Selesai
Mencatat berat sampel (berat akhir) Diulangi pemanasan dan penimbangan sampai
36 3.5.4.3Analisa Bilangan iod
Gambar 3.5 Flowchart Analisa Bilangan Iodin Mulai
Ditimbang sejumlah contoh dalam penelitian ini sebanyak 1,0025 gram
Sampel dimasukkan ke dalam erlenmeyer dan ditutup
Simpan selama 1 jam dalam ruangan gelap
Dititrasi dengan menggunakan larutan natrium tiosulfat 0,1 N dan larutan kanji sebagai indikator
Selesai
Ditambahkan 25 ml larutan wijs dengan menggunakan pipet gondok
lalu ditutup
Dilakukan penetapan blanko Ditambahkan 10 ml larutan KI 20% dan 100 ml air suling,
ditutup lalu dikocok
Dilakukan penetapan duplo
37 3.5.4.4Analisa Bilangan Peroksida
Gambar 3.6 Flowchart Analisa Bilangan Peroksida Mulai
Ditimbang contoh sebanyak 0,3 gram -5 gram
Sampel dimasukkan ke dalam erlenmeyer
Dititrasi dengan larutan natrium thiosulfat 0,02 N dengan larutan kanji sebagai indikator
Selesai
Ditambahkan 15 ml asam asetat glasial dan 1 ml larutan kalium iodida
Ditambahkan aquadest sebanyak 75 ml
Hitung bilangan peroksida pada contoh Ditutup erlenmeyer dan dikocok kira-kira 5
menit pada suhu 15 oC-25 oC
38 3.5.4.5Analisa Densitas
Ya
Tidak
[image:30.595.136.524.93.452.2]
Gambar 3.7 Flowchart Analisa Berat Jenis Ditimbang piknometer kosong
Apakah ada sampel lain?
Kemudian diisi piknometer dengan aquadest sampai penuh kemudian ditutup
Mulai
Kemudian ditimbang piknometer dan isinya lalu diukur suhu aquadest
39
BAB IV
HASIL DAN PEMBAHASAN
Analisa yang dilakukan dalam penelitian ini adalah analisa kualitatif dan kuantitatif. Analisa kualitatif meliputi beberapa karakteristik seperti penampilan, warna dan bau yang mengidentifikasikan sifat-sifat dari minyak kelapa murni. Selain itu, juga dilakukan analisa kuantitatif berupa analisa rendemen dan kadar minyak kelapa murni yang diperoleh.
4.1 ANALISA KUALITATIF
[image:31.595.131.491.351.459.2]Berikut ini merupakan data hasil analisa kualitatif minyak kelapa murni: Tabel 4.1 Hasil Analisa Kualitatif Minyak Kelapa Murni
No Karakteristik Pengamatan
1 Penampilan cairan
2 Warna Jernih (tidak berwarna)
3 Bau Beraroma kelapa segar
Dari pengamatan yang dilakukan pada penelitian ini, hasil yang diperoleh yaitu penampilan berupa cairan jernih dengan bau beraroma kelapa segar seperti yang dapat dilihat pada table 4.1.
40
Hasil penelitian analisa kualitatif yang diperoleh pada penelitian ini juga sama dengan hasil penelitian yang dilakukan Firman [6] yaitu minyak kelapa murni yang jernih (tidak berwarna).
4.2 ANALISA KUANTITATIF
4.2.1 Pengaruh WaktuPengadukan Terhadap Rendemen Minyak Kelapa
Murni
[image:32.595.129.516.284.473.2]Berikut pengaruh waktu pengadukan terhadap rendemen minyak kelapa murni dapat di lihat pada gambar 4.1 berikut:
Gambar 4.1 Pengaruh waktu pengadukan terhadap Rendemen Minyak Kelapa Murni
Pada Gambar 4.1 dapat dilihat bahwa rendemen minyak kelapa murni yang dihasilkan untuk berbagai macam kecepatan pengadukan yang cenderung menurun dengan peningkatan waktu pengadukan kecuali pada 125 rpm. Rendemen minyak kelapa murni cenderung meningkat dengan peningkatan waktu pengadukan.
Hasil penelitian yang diperoleh memperlihatkan bahwa waktu pengadukan selama 15 menit menghasilkan rendemen minyak kelapa murni (10,75-20,5%), sementara 30 menit pengadukan menghasilkan rendemen minyak kelapa murni (10,5-24,5%), 45 menit (14-21,5%), 60 menit (11,75-20,75%) dan 75 menit
0% 5% 10% 15% 20% 25% 30%
15 30 45 60 75
Re n d em en VC O (% )
Waktu Pengadukan (menit)
41
memberikan rendemen minyak kelapa murni (8,5-17%). Penurunan rendemen minyak kelapa murni bisa disebabkan oleh penggunaan bakteri pada proses fermentasi. Dimana faktor-faktor yang mempengaruhi fermentasi antara lain suhu, waku dan pH [33].
Waktu pengadukan yang berbeda mempengaruhi kualitas minyak kelapa murni yang dihasilkan yaitu dengan bertambahnya waktu pengadukan maka kadar air semakin besar, berat jenis semakin besar, angka asam semakin besar, angka penyabunan semakin kecil. Pada proses pengadukan, lamanya pengadukan tentu berbanding lurus dengan efek pengadukan yang diharapkan. Namun untuk skala industri yang komersial, semakin lama proses pengadukan dilakukan akan menyebabkan biaya operasional semakin tinggi karena energi pengadukan akan semakin banyak dibutuhkan [8].
Dari data tersebut dapat dilihat bahwa semakin lama waktu pengadukan yang dilakukan maka rendemen minyak kelapa murni cenderung semakin menurun. Rendemen tertinggi diperoleh saat pengadukan dilakukan selama 30 menit.
4.2.2 Pengaruh Kecepatan Pengadukan Terhadap Rendemen Minyak Kelapa
Murni
[image:33.595.136.500.532.691.2]Berikut pengaruh kecepatan pengadukan terhadap rendemen minyak kelapa murni pada masing – massing perlakuan dapat di lihat pada gambar 4.2
Gambar 4.2 Pengaruh Kecepatan Pengadukan Terhadap Rendemen Minyak Kelapa Murni 0% 5% 10% 15% 20% 25% 30%
25 50 75 100 125
Re n d em en VC O (% )
Kecepatan Pengadukan rpm)
42
Pada gambar 4.2 dapat dilihat bahwa rendemen minyak kelapa murni yang dihasilkan untuk berbagai macam waktu pengadukan yang cenderung menurun dengan peningkatan kecepatan pengadukan.
Hasil penelitian yang diperoleh memperlihatkan bahwa kecepatan pengadukan selama 25 rpm menghasilkan rendemen minyak kelapa murni (11,75-20,75%), sementara 50 rpm menghasilkan rendemen minyak kelapa murni (11,25-24,5%), 75 rpm (12-15,5%), 100 rpm (8,5-21,5%) dan 125 rpm memberikan rendemen minyak kelapa murni (10,5-17%). Penurunan rendemen minyak kelapa murni bisa disebabkan oleh penggunaan bakteri pada proses fermentasi. Faktor-faktor yang mempengaruhi fermentasi antara lain suhu, waktu dan pH [33].
Kecepatan pengadukan yang berbeda mempengaruhi rendemenminyak kelapa murni dimana pada proses pengadukan, kecepatan pengadukan pada umumnya akan mempercepat homogenitas campuran. Ketika pengadukan diaplikasikan untuk memecahkan emulsi antara minyak dengan protein pada cairan santan, semakin cepat pengadukan maka molekul-molekul minyak akan semakin cepat dan banyak terpecah menjadi ukuran yang lebih kecil sehingga lebih mudah terpisah [8].
Dari data tersebut dapat dilihat bahwa semakin cepat pengadukan yang dilakukan maka rendemen minyak kelapa murni cenderung menurun. Rendemen tertinggi diperoleh saat kecepatan pengadukan dilakukan selama 50 rpm.
4.2.3 Pengaruh Waktu Pengadukan dan Kecepatan Pengadukan Terhadap
Kadar FFA Minyak Kelapa Murni
43
Gambar 4.3 Pengaruh Waktu Pengadukan Terhadap Kadar FFA Minyak Kelapa Murni
Gambar 4.4 Pengaruh Kecepatan Pengadukan Terhadap Kadar FFA Minyak Kelapa Murni
Pada Gambar 4.3 dapat dilihat bahwa FFA minyak kelapa murni yang dihasilkan untuk berbagai macam kecepatan pengadukan yang cenderung menurun dengan peningkatan waktu pengadukan. Sedangkan pada Gambar 4.4 dapat dilihat bahwa FFA minyak kelapa murni yang dihasilkan untuk berbagai macam waktu pengadukan yang cenderung meningkat dengan peningkatan kecepatan pengadukan. 0 0.1 0.2 0.3 0.4 0.5 0.6 0.7
25 50 75 100 125
K ad ar F F A (% )
Kecepatan Pengadukan (rpm)
15 menit 30 menit 45 menit 60 menit 75 menit 0.1 0.2 0.3 0.4 0.5 0.6 0.7
15 30 45 60 75
K adar F F A ( % )
Waktu Pengadukan (menit)
[image:35.595.137.511.341.523.2]44
Asam lemak bebas merupakan salah satu komponen yang terdapat dalam minyak, tinggi rendahnya asam lemak bebas pada minyak akan mempengaruhi kualitas minyak kelapa yang dihasilkan karena komponen ini merupakan penyebab ketengikan [34]. Nilai asam lemak bebas yang tinggi inilah yang dapat menyebabkan bau tengik pada minyak yang mana menandakan bahwa minyak tersebut sudah tak layak pakai atau rusak [35].
Meningkatnya asam lemak bebas disebabkan adanya kandungan air pada substrat yaitu santan yang akan dijadikan sebagi sumber minyak kelapa. Adanya air pada substrat menyebabkan terjadinya proses hidrolisis pada minyak kelapa pada saat proses pencampuran yang memicu terbentuknya asam lemak bebas [35]. Menurut [37] kadar FFA maksimal yang terkandung dalam minyak kelapa murni yaitu 0,2 % sedangkan menurut [23] kadar FFA maksimal yang terkandung dalam minyak kelapa murni yaitu 0,5 %. Dari hasil penelitian terlihat bahwa kadar FFA masih sesuai standart menurut [23].
Tingginya kadar FFA disebabkan oleh adanya kandungan air didalam minyak, proses pemisahan minyak yang tidak baik dan selain itu proses pengadukan dilakukan di ruang terbuka dengansuhu ruang. Hal tersebut menyebabkan santan terkena kontak langsung dengan oksigen sehingga selama penyimpanan reaksi oksidasi yang terjadi lebih besar. Dengan adanya reaksi oksidasi dihasilkan senyawa-senyawa lain seperti karbonrantai pendek, asam lemak bebas, sejumlah kecil aldehida dan metil keton yang mengurangi kemurnian minyak kelapa murni. Ketengikan yang terjadi terutama disebabkan oleh aldehid dan keton.
4.2.4 Kadar Air Minyak Kelapa Murni
45
Kadar air yang diperoleh pada rendemen minyak kelapa murni tertinggi yaitu sebesar 1,157 % dan pada rendemen minyak kelapa murni terendah diperoleh kadar air sebesar 0,719 %.
Menurut standar APCC (Asian and Pacific Coconut Community) [23] untuk
virgin coconut oil, kadar airminyak kelapa murni yang diperbolehkan adalah
0,1-0,5. Dari hasil penelitian diperoleh bahwa kadar air tidak sesuai dengan standar yang ada.
Kadar air yang tinggi bisa dikarenakan bercampurnya air pada saat pembuatan dan tidak bisa dipisahkan dengan metode pemisahan biasa. Kadar air yang tinggi dalam minyak minyak kelapa murniakan menjadi media yang baik untuk reaksi-reaksi kimia, seperti reaksi redoks dan enzimatis maupun aktivitas mikroorganisme yang cenderung merusak minyak minyak kelapa murniitu sendiri [33].
4.2.5 Peroxide Value (Angka Peroksida) Minyak Kelapa Murni
Bilangan peroksida adalah nilai terpenting untuk menentukan derajat kerusakan pada minyakatau lemak. Asam lemak tidak jenuh dapat mengikat oksigen pada ikatan rangkapnya sehingga membentuk peroksida [36]. Angka peroksida sangat penting untuk menentukan derajat kerusakan minyak. Asam lemak tak jenuh dapat mengikat oksigen pada ikatan rangkapnya sehingga membentuk peroksida. Semakin kecil angka peroksida maka kualitas minyak semakin baik [10]. Adanya peroksida akan meyebabkan terjadinya reaksi oksidasi danradikal bebas sehingga akan menurunkan kualitas minyak minyak kelapa murni [34].
46
Bilangan peroksida yang diperoleh pada rendemen minyak kelapa murni tertinggi yaitu sebesar 1,6 meq/kg dan pada rendemen minyak kelapa murni terendah diperoleh bilangan peroksida sebesar 1,4 meq/kg.
Menurut standar APCC (Asian and Pacific Coconut Community) [23] untuk
virgin coconut oil, bilangan peroksida minyak kelapa murniyang diperbolehkan
adalah maksimal 3 meq/kg.
Jika dilihat dari SNI [37] dan standar APCC [23] di atas maka bilangan peroksida yang diperoleh pada penelitian ini masih sesuai dengan standar yang diperbolehkan.
4.2.6 Iodine Value (Angka Iodin) Minyak Kelapa Murni
Angka iod menjelaskan ketidakjenuhan asam lemak penyusunminyak dan lemak. Asam lemak tidak jenuh mampu mengikat iod danmembentuk senyawaan yang jenuh. Banyaknya iod yang diikat menunjukkan banyaknya ikatan rangkap. oleh 100 gram minyak atau lemak. Penentuan angka iod dapat dilakukan dengan cara Hanus atau cara Kaufmaun dan cara Von Hubl atau cara Wijs[10].
Pada penelitian ini bilangan iod hanya diuji pada perolehan rendemen minyak kelapa murni tertinggi dan terendah. Dimana perolehan minyak kelapa murni tertinggi diperoleh pada kecepatan pengadukan 50 rpm dengan waktu pengadukan 30 menit yaitu sebanyak 98 ml (rendemen 24,5%) dan terendah diperoleh pada kecepatan pengadukan 100 rpm dengan waktu pengadukan 75 menit yaitu sebanyak 34 ml VC0 (rendemen 8,5%).
Bilangan iod yang diperoleh pada rendemen minyak kelapa murni tertinggi yaitu sebesar 10,3025 dan pada rendemen minyak kelapa murni terendah diperoleh bilangan iod sebesar 9,4937.
Menurut standar APCC (Asian and Pacific Coconut Community) [23] untuk
virgin coconut oil, bilangan iod minyak kelapa murniyang diperbolehkan adalah
4,1-11.
47
4.2.7 Densitas (Berat Jenis) Minyak Kelapa Murni
Massa jenis merupakan salah satu parameter yang digunakan untuk menentukan kualitas suatu minyak, semakin tinggi nilai massa jenis maka kualitas minyak tersebut rendah, hal ini dikarenakan kenaikan massa jenis dipengaruhi asam lemak bebas [34]. Menurut Asian and Pacific Coconut Community (APCC) (2012) [23] untuk virgin coconut oil, menyebutkan bahwa relative densitiy dari minyak kelapa murni yang diperbolehkan adalah 0,915-0,920.
Pada penelitian ini analisa densitas hanya dilakukan pada perolehan rendemen minyak kelapa murnitertinggi dan terendah. Untuk rendemen minyak kelapa murni tertinggi diperoleh densitas minyak kelapa murni sebesar 0,918 dan densitas untuk rendemen minyak kelapa murni terendah sebesar 0,906.
Maka dari hasil yang diperoleh pada penelitian ini, maka disimpulkan bahwa densitas minyak kelapa murni yang didapat masih sesuai dengan standar yang ada.
4.2.8 Analisa kadar Asam Laurat
Hasil analisis GC terhadap sampel minyak minyak kelapa murnihasil penelitian ini menunjukkan adanya 9 jenis asam lemak yang terkandung di dalam minyak kelapa murni. Kandungan asam lemak tertinggi adalah asam laurat yaitu sebesar 50,15 % pada 50 rpm 30 menit dan pada 125 rpm 15 menit kandungan asam laurat sebesar 50,07 %.
48
BAB V
KESIMPULAN DAN SARAN
5.1 KESIMPULAN
Adapun kesimpulan yang di peroleh dari penelitian yang ini adalah : 1. Pengaruh waktu pengadukan
- Rendemen VCO yang diperoleh cenderung semakin menurun seiring dengan bertambahnya kecepatan pengadukan
- Rendemen VCO tertinggi yang diperoleh yaitu 24,5% pada penambahan waktu pengadukan 30 menit. Sedangkan rendemen terendah yang diperoleh sebesar 8,5% pada waktu pengadukan 75 menit
- Kadar free fatty acid (FFA) semakin menurun seiring bertambahnya waktu pengadukan.
2. Pengaruh kecepatan pengadukan
- Rendemen VCO yang diperoleh cenderung semakin menurun seiring dengan bertambahnya kecepatan pengadukan
- Rendemen VCO tertinggi yang diperoleh yaitu 24,5% pada penambahan kecepatan pengadukan 50 rpm. Sedangkan rendemen terendah yang diperoleh sebesar 8,5% pada kecepatan pengadukan 100 rpm
- Kadar free fatty acid (FFA) semakin meningkat seiring bertambahnya kecepatan pengadukan.
3. Karakteristik virgin coconut oil (VCO)
- Analisa kualitatif virgin coconut oil (VCO) yang difermentasi dari santan kelapa menunjukkan beberapa karakteristik yaitu penampilan berupa cairan jernih dengan bau yang khas kelapa segar.
49
- Kandungan asam-asam lemak pada analisa gas kromatografi sesuai dengan standar yang ada.
5.2 SARAN
Adapun saran yang dapat diberikan adalah :
1. Penelitian selanjutnya disarankan agar mengutamakan kebersihan selama mulai persiapan bahan baku hingga proses pengerjaan penelitian selesai karena sangat mempengaruhi jumlah dan kualitas minyak yang diperoleh. 2. Penelitian selanjutnya disarankan agar proses penyaringan minyak
dilakukan di dalam ruangan tertutup dan menyimpan minyak didalam bootol kaca gelap agar tidak terkena kontak langsung dengan udara sehingga mempercepat terjadi proses oksidasi.
3. Penelitian selanjutnya disarankan agar menggunakan bakteri yang sama untuk setiap run supaya dapat mengetahui kinerja dari bakteri dan melihat hasil minyak yang dihasilkan.
4. Penelitian selanjutnya disarankan untuk langsung menyaring VCO yang dihasilkan agar VCO yang di hasilkan lebih baik dengan kadar air yang rendah dan tidak terbentuk kotoran didalam minyak.
6
BAB II
TINJAUAN PUSTAKA
2.1 Kelapa
Kelapa (Cocos nucifera L) merupakan tanaman perkebunan berupa pohon batang lurus dari famili Palmae. Selain sebagai salah satu komoditas strategis, tanaman kelapa memiliki banyak manfaat mulai dari akar, batang, daging, buah hingga pelepahnya [14]. Banyak kegunaan yang dapat diperoleh dari kelapa misalnya mengolahnya menjadi minyak makan atau minyak goreng. Produk kelapa yang paling berharga adalah minyak kelapa yang dapat diperoleh dari daging buah kelapa segar atau dari kopra [15].
Buah kelapa terdiri dari bagian – bagian seperti:
1. Epicarp (Kulit Luar) adalah kulit bagian luar yang berwarna hijau, kuning, atau jingga permukaannya licin, agak keras dan tebalnya 0,14 mm.
2. Mesocarp (Sabut) adalah kulit bagian tengah yang disebut serabut terdiri dari bagian berserat tebalnya berkisar 3 - 5 mm.
3. Endocarp (Tempurung) adalah bagian tempurung kelapa yang keras dan tebalnya berkisar antara 3 - 5 mm.
4. Testa (Kulit Daging Buah) adalah bagian luar daging buah berwarna kuning sampai coklat
5. Endosperm (Daging Buah) adalah bagian yang berwarna putih dan lunak, sering disebut daging kelapa yang tebalnya berkisar 8 – 10 mm.
6. Air Kelapa adalah air yang terkandung dalam buah kelapa yang mengandung mineral 4%, dan gula 2%.
7
Gambar 2.1 Bagian – Bagian Tanaman Kelapa
[image:43.595.225.452.94.254.2]Daging buah kelapa mempunyai kandungan gizi yang cukup tinggi dimana komposisi zat gizi daging buah kelapa dapat dilihat pada Tabel 2.1.
Tabel 2.1 Komposisi zat gizi daging buah kelapa per 100 gram zat gizi [16]
Zat Gizi Muda Setengah Tua Tua
Kalori (K) 68 180 359
Protein (g) 1 4 3,4
Lemak (g) 0,9 13 34,7
Karbohidrat (g) 14 10 14
Kalsium (mg) 17 8 21
Fosfor (mg) 30 35 21
Besi (mg) 1 1,3 2
Vitamin A (SI) 0 10 0
Vitamin B1 (mg) 0 0,5 0,1
Vitamin C (mg) 4 4 2
Air (g) 83,3 70 46,9
2.1.1 Varietas Kelapa
Tanaman kelapa ada dua varitas yaitu varietas typical (tall variety) dan varietas genjah (dwarf variety).
a. Typical (Cocos nucefera L.)
8
berbuah pada umur 6-8 tahun dan umur pohon mencapai 110 tahun. Batangnya tinggi sampai mencapai 35 m apabila tanaman rapat, pada umumnya tingginya 30 m. Buahnya berukuran besar, yaitu rata-rata beratnya 2 kg dengan daging buah ½ kg dan air ½ liter. Sebutir kelapa dapat menghasilkan kopra 200 - 300 gram dan kelapa ini menghasilkan minyak sebanyak 132 gram. Warna buah kelapa ini adalah hijau dan merah.
b. Kelapa Genjah
Kelapa genjah disebut kelapa kerdil atau kelapa puyuh. Kelapa ini mulai berbuah pada umur 3 - 4 tahun. Buahnya kecil - kecil, beratnya rata-rata 1 kg dan daging buahnya 400 gram. Batang kelapa ini berukuran kecil dan pangkal batangnya tidak besar. Umur kelapa genjah rata-rata 50 tahun [17].
Gambar 2.2 Tanaman Kelapa
2.2 Minyak Kelapa
Minyak kelapa digunakan sebagai minyak goreng, bahan margarin dan mentega putih, komponen dalam pembuatan sabun serta formulasi kosmetika. Selain digunakan untuk menggoreng, pada masyarakat pedesaan minyak kelapa juga digunakan sebagai minyak pijat, kerik, dan untuk minyak cem-ceman [18].
9
minyak kelapa dapat dimasukkan ke dalam golongan non drying oils, karena bilangan iod minyak tersebut berkisar antara 7,5 - 10,5 [15].
[image:45.595.110.517.189.482.2]Berikut komposisi Asam Lemak Minyak Kelapa dapat di lihat pada Tabel 2.2 berikut:
Tabel 2.2. Komposisi Asam Lemak Minyak Kelapa (%) [15].
Asam Lemak Rumus Kimia Jumlah (%)
Asam Lemak Jenuh
Asam Kaproat C5H11COOH 0,0 – 0,8
Asam Kaprilat C7H17COOH 5,5 – 9,5
Asam Laurat C11H23COOH 44,0 – 52,0
Asam Miristat C13H27COOH 13,0 – 19,0
Asam Palmitat C15H31COOH 7,5 – 10,5
Asam Stearat C17H35COOH 1,0 – 3,0
Asam Arachidat C19H39COOH 0,0 – 0,4
Asam Lemak Tidak Jenuh
Asam Palmitit C15H29COOH 0,0 – 1,3
Asam Oleat C17H33COOH 5,0 – 8,0
Asam Linoleat C17H31COOH 1,5 - 2,5
2.3 Minyak kelapa murni
Minyak kelapa murni didefinisikan sebagai minyak yang dihasilkan dari kelapa segar ( Cocos nucifera L. ) melalui cara mekanik dan alami, baik dengan penggunaan panas atau tidak menyebabkan perubahan atau transformasi minyak [19].
Minyak kelapa murni mengandung asam lemak rantai sedang yang mudah dicerna dan dioksidasi oleh tubuh sehingga tidak terjadi penimbunan di dalam tubuh. Selain itu kandungan antioksidan di dalam juga sangat tinggi seperti tokoferol dan betakaroten. Antioksidan ini berfungsi untuk mencegah penuaan dini dan menjaga vitalitas tubuh [20].
10
digunakan sebagai bahan konsumsi pangan masyarakat. minyak kelapa murni mengandung 93% asam lemak jenuh, tetapi 47-53 % berupa minyak jenuh berantai medium yang tidak ditimbun dalam tubuh, mudah dicerna dan terbakar [21].
Minyak kelapa murni mengandung berbagai macam MCT (medium chain
trigliserida) seperti asam kaproat (0,7 %), asam kaprilat (4,6 – 10%), asam kaprat (5,0 – 8,0%), asam laurat (45,1– 53,2%) dan asam miristat (16,8 – 21%). Asam laurat dari minyak kelapa murni di dalam tubuh akan dikonversi menjadi monogliserida yang disebut monolaurin dimana senyawa ini sangat kuat melawan berbagai macam virus, bakteri dan protozoa. Efek fungisida dari minyak kelapa murni juga telah diteliti bahkan dibandingkan dengan obat antifungi sintetis yang mempunyai efek menghambat biosíntesis ergosterol yang sangat diperlukan untuk pembentukan membran fungi [22].
Minyak kelapa murni memiliki sifat kimia-fisika antara lain [17]: 1. Aroma : sedikit berbau asam
2. Kelarutan : tidak larut dalam air 3. pH : di bawah 7
4. Titik didih : 225 ⁰C
[image:46.595.108.516.499.753.2]Standar mutu minyak kelapa menurut APCC [23] disajikan pada tabel 2.3.
Tabel 2.3 Standar mutu Minyak kelapa murni menurut APCC
Mutu Minyak Syarat standar AFCC
Indeks bias 1,4480-1,4492
Berat jenis 0,915-0,920
Kadar air (%) 0,1 – 0,5
Bilangan penyabunan 250 – 260
Bilangan iodine 4,1 – 11
Komposisi asam lemak jenuh
Asam kaproat (%) 0,4 – 0,6
Asam kaprilat (%) 5,0 – 10,0
Asam kaprat (%) 4,5 – 8,0
11
Asam miristat (%) 16,0 - 21,0
Asam palmitat (%) 7,5 - 10,0
Asam palmitoletik (%) 2,0 - 4,0
Asam stearat (%) 5,0 – 10,0
Asam oleat (%) 1,0 – 2,5
Mutu Minyak
Warna Jernih
Asam lemak bebas (%) 0,5
Bilangan peroksida (meq/kg) 3
Bau dan rasa Normal
2.4 Proses Pembuatan Minyak kelapa murni
Kandungan kimia yang paling utama (tinggi) dalam sebutir kelapa yaitu air, protein, dan lemak. Ketiga senyawa tersebut merupakan jenis emulsi dengan protein sebagai emulgatornya. Emulsi adalah cairan yang terbentuk dari campuran dua zat atau lebih yang sama, di mana zat yang satu terdapat dalam keadaan terpisah secara halus atau merata di dalam zat yang lain. Sementara yang dimaksud dengan emulgator adalah zat yang berfungsi untuk mempererat (memperkuat) emulsi tersebut. Dari ikatan tersebut protein akan mengikat butir - butir minyak kelapa dengan suatu lapisan tipis sehingga butir – butir minyak tidak akan bisa bergabung dengan air. Emulsi tersebut tidak pecah karena masih ada tegangan permukaan antara protein dan air yang lebih kecil dibandingkan protein dan minyak. Minyak kelapa terbentuk jika ikatan emulsi tersebut dirusak [15].
Minyak kelapa murni diolah dari daging buah kelapa segar dan proses pembuatannya dilakukan pada suhu yang relatif rendah. Beberapa metode yang saat ini banyak digunakan dalam pembuatan minyak kelapa murni adalah metode pemanasan bertahap, metode pemancingan minyak dan metode fermentasi.
Proses pembuatan minyak kelapa murni secara umum yaitu : 1. Metode Pemanasan Bertahap
12
rendah (< 65 ºC). Proses tradisional melalui cara fisika (pemanasan) menghasilkan minyak dengan kualitas rendah karena kandungan airnya tinggi dan menyebabkan ketengikan. Metode Pemanasan bertahap misalnya dapat menghasilkan minyak dengan kadar air yang rendah karena air akan menguap pada saat dilakukan pemanasan. Pemanasan juga dapat menyebabkan inaktifnya enzim – enzim seperti lipase sehingga proses hidrolisis dapat diminimalkan [24].
2. Metode Fermentasi
Pembuatan minyak kelapa murni secara fermentasi dilakukan menggunakan
Saccharomyces cerevisiae yang menghasilkan enzim secara langsung atau melalui
mikroba penghasil enzim protease yang dapat memecah ikatan protein dengan minyak pada emulsi santan. Enzim amilolitik akan memecah karbohidrat sehingga menghasilkan asam. Adanya asam akan menurunkan pH santan sampai mencapai titik isoelektrik protein sehingga protein akan terkoagulasi. Kemudian enzim proteolitik akan memecah protein terkoagulasi, akhirnya mudah dipisahkan dari minyak [9].
Minyak kelapa fermentasi (fermikel) memiliki banyak kelebihan, diantaranya hampir tanpa kandungan kolesterol, hemat bahan bakar, tingkat ketengikan rendah dengan daya simpan lebih lama, aroma lebih harum, dan bebas senyawa penginduksi kolesterol [24].
3. Metode Pengasaman
Pengasaman merupakan salah satu upaya pembuatan minyak kelapa murni dengan cara membuat suasana emulsi (santan) dalam keadaan asam. Asam memiliki kemampuan untuk memutus ikatan lemak protein dengan cara mengikat senyawa yang berikatan dengan lemak. Namun asam yang dicampurkan kedalam santan hanya bisa bekerja dengan maksimal bila kondisi pH (derajat keasamannya) sesuai. Pada proses pembuatan minyak kelapa murni, pH yang paling optimal yaitu 4,3. Pengukuran pH tersebut dilakukan dengan pH meter atau kertas lakmus [15].
13
a. Warna lebih bening dibandingkan dengan minyak kelapa murni yang dibuat secara tradisional.
b. Kandungan asam lemak dan antioksidannya tidak banyak berubah karena proses hanya memutuskan ikatan protein lemak saja.
c. Daya simpan sangat lama, bisa sampai 10 tahun karena selama proses pembuatan tidak terjadi denaturasi komposisi gizinya.
d. Proses pembuatan tidak membutuhkan tenaga tambahan.
e. Tidak membutuhkan biaya terlalu mahal karena harga asam cuka sebagai bahan tambahan cukup murah.
Sementara kekurangan pembuatan minyak kelapa murni dengan metode pengasaman [17]:
a. Tidak bisa diformulasikan secara pasti karena untuk mendapatkan pH 4,3 banyak faktor yang berpengaruh sehingga harus dilakukan pencampuran (santan dan asam) berulang - ulang.
b. pH campuran santan dan asam harus pas, yaitu 4,3. Apabila pH nya kurang atau lebih kemungkinan kegagalan dalam pembuatan sangat tinggi.
c. Waktu yang dibutuhkan untuk proses pembuatan minyak kelapa murni cukup lama, sekitar 10 jam.
4. Metode Sentrifugasi
Sentrifugasi merupakan salah satu cara untuk pembuatan minyak kelapa murni dengan cara mekanik. Pemutaran (pemusingan) dari sentrifuse akan memutuskan ikatan lemak dan protein pada santan dengan adanya gaya sentrifugal karena berat jenis minyak dan air berbeda maka setelah dilakukan sentrifugasi keduanya akan terpisah dengan sendirinya. Berat jenis minyak yang lebih ringan dibanding air akan menyebabkan minyak terkumpul pada lapisan atas [15].
14
zeta potensial sehingga menurunkan viskositas larutan. Zeta potensial adalah gaya yang menjaga agar droplet- droplet emulsi tetap alam keadaan stabil [25].
Penyebab hilangnya stabilitas protein dalam santan karena adanya pengadukan. Hal ini berarti protein mengalami denaturasi sehingga kelarutan nya berkurang. Lapisan molekul protein bagian dalam yang bersifat hidrofobik berbalik keluar sedangkan bagian luar yang bersifat hidrofilik terlipat kedalam. Hal ini menyebabkan protein mengalami koagulasi dan mengalami pengendapan sehingga lapisan minyak dan air terpisah [26].
Waktu pengadukan yang berbeda mempengaruhi kualitas minyak kelapa murni yang dihasilkan yaitu dengan bertambahnya waktu pengadukan maka kadar air semakin besar, berat jenis semakin besar, angka penyabunan semakin kecil [2]. Kelebihan pembuatan minyak kelapa murni dengan metode sentrifugasi [15]:
a. Berwarna jernih dan berbau khas minyak kelapa. b. Daya simpan lama, sekitar 10 tahun.
c. Proses pambuatannya sangat cepat, hanya membutuhkan waktu sekitar 15 menit.
d. Kandungan asam lemak rantai sedang tidak mengalami denaturas, demikian juga dengan kandungan antioksidannya.
Sementara kekurangan pembuatan minyak kelapa murni dengan metode sentrifugasi yaitu [17]:
a. Membutuhkan biaya yang relatif mahal untuk alat sentrifiusnya.
b. Membutuhkan tenaga listrik yang cukup tinggi sehingga bisa menambah biaya produksi.
2.5 Faktor Penyebab Kerusakan Pada Minyak Kelapa Murni
15
terhadap kerusakan sangat tergantung pada komponen penyusunnya, terutama kandungan asam lemak. Minyak yang mengandung asam lemak tidak jenuh cenderung mudah teroksidasi, sedangkan yang banyak mengandung asam lemak jenuh lebih mudah terhidrolisis. Asam lemak pada umumnya bersifat reaktif terhadap oksigen [27].
Ketengikan adalah proses kerusakan lemak yang menimbulkan timbulnya bau dan rasa tengik. Tiga penyebab ketengikan dalam lemak yaitu ketengikan oleh oksidasi, ketengikan oleh enzim dan ketengikan oleh proses hidrolisa.
a. Ketengikan oleh oksidasi
Ketengikan ini terjadi karena proses oksidasi oleh oksigen udara terhadap asam lemak tidak jenuh dalam lemak. Proses oksidasi dapat terjadi pada suhu kamar, dan selama proses pengolahan menggunakan suhu tinggi. Beberapa jenis logam atau garam yang terdapat dalam minyak merupakan katalisator dalam proses oksidasi, misalnya logam tembaga, besi, kobalt, vanadium, mangan, nikel, khromium, sedangkan aluminium kecil pengaruhnya terhadap proses oksidasi.
b. Ketengikan oleh enzim
Bahan pangan berlemak dengan kadar air dan kelembaban udara tertentu merupakan medium yang baik bagi pertumbuhan jamur. Jamur tersebut mengeluarkan enzim, misalnya enzim lipo clastic dapat menguraikan trigliserida menjadi asam lemak bebas dan gliserol. Enzim peroksida dapat mengoksidasi asam lemak tidak jenuh sehingga terbentuk peroksida.
c. Ketengikan hidrolisis
Komponen zat berbau tengik dalam minyak selain dihasilkan dari proses oksidasi dan enzimatis, juga disebabkan oleh hidrolisa lemak yang mengandung asam lemak tidak jenuh berantai pendek. Asam lemak tersebut mudah menguap dan berbau tidak enak misalnya asam butirat, asam valerat, asam kaproat dan ester alifatis yaitu metil nonil keton.
16
lemak tidak jenuh dapat mengikat oksigen pada ikatan rangkapnya sehingga membentuk peroksida. Peroksida ini dapat ditentukan dengan metode iodometri.
Cara yang sering digunakan untuk menentukan bilangan peroksida berdasarkan pada reaksi antara alkali iodida dalam larutan asam dengan ikatan peroksida [28].
2.6 Bakteri Saccharomyces cereviseae
Saccharomyces cervisae merupakan khamir yang paling populer dalam
pengolahan makanan. Dalam bidang pangan, khamir digunakan dalam pengembangan adonan roti dan dikenal sebagai ragi roti [28].
Saccharomyces cervisae berkembang biak dengan membelah diri melalui
"budding cell". Reproduksinya dapat dipengaruhi oleh keadaan lingkungan serta jumlah nutrisi yang tersedia bagi pertumbuhan sel [29].
Taksonomi Saccharomyces cereviseae sebagai berikut :
Saccharomyces cerevisiae
Kingdom: Fungi Phylum: Ascomycota
Sub Phylum: Saccharomycolina Class: Saccharomycetes
Order: Saccharomycetales Family: Saccharomycetaceae Genus: Saccharomyces Species: S. cerevisiae
Binominal name: Saccharomyces cerevisiae
Dalam pertumbuhannya mikroorganisme memerlukan faktor-faktor pertumbuhan antara lain unsur C, H, O, N, S dan P yang diperolehnya dengan mengubah protein, karbohidrat, dan zat-zat lain dalam media pertumbuhannya, sehingga zat-zat dalam media tersebut berkurang dibebaskan oleh sel-sel mikroorganisme [27].
17
Perubahan pH dalam fermentasi disebabkan karena dalam aktivitasnya sel khamir selain menghasilkan etanol sebagai metabolit primer juga menghasilkan asam-asam organik seperti asam malat, asam tartarat, asam sitrat, asam laktat, asam asetat, asam butirat dan asam propionat sebagai hasil sampingan. Asam - asam ini menurunkan pH medium [30].
Komposisi kimia Saccharomyces cerevisiae terdiri atas protein 50-52%, karbohidrat 30-37%, lemase 4-5%, dan mineral 7-8% [29]. Temperatur pertumbuhan yang optimum untuk Saccharomyces cereviseae adalah 28 – 36 oC dan pH optimum pertumbuhan sel khamir 4,5 - 5,5. Sacharomyces cerevisieae dapat tumbuh secara anaerob, fakultatif dan mempunyai toleransi suhu yang tinggi, mempunyai kemampuan untuk mencapai konversi yang lebih tinggi, dan pH yang rendah [31].
[image:53.595.228.403.430.555.2]Berdasarkan hasil pengamatan diperoleh bahwa Saccharomyces sp memiliki ciri-ciri yaitu koloni berbentuk bulat, warna kekuning-kuningan, permukaan licin dan berkilau [32].
Gambar 2.3 Khamir Saccharomyces cereviseae [32]
2.7 Analisa Ekonomi
Analisa Ekonomi dapat dilihat pada tabel 2.4 berikut. Tabel 2.4 Analisa Ekonomi
Modal Investasi Tetap (MIT) Harga
Bangunan
Alat
Rp Rp
18 Modal Kerja (MK) / 3 bulan
Bahan Baku
Kas (Gaji, adm, pemasaran)
Piutang Dagang
Rp Rp Rp 294.000.000,00 69.300.000,00 40.000.000,00 Total Modal Kerja (TMK) Rp 403.300.000,00
Total Modal Investasi Rp 578.340.000,00
Biaya Tetap (BT) / 3 bulan
Gaji Karyawan
Bunga Pinjaman Bank
Depresiasi
Rp Rp Rp 49.500.000,00 10.843.875,00 2.491.796,00 Total Biaya Tetap (TBT) Rp 95.162.218,00 Biaya Variabel (BV) / 3 bulan
Bahan Baku
Biaya Variabel Tambahan
Rp Rp
294.000.000,00 58.800.000,00 Total Biaya Variabel (TBV) Rp 352.800.000,00 Total Biaya Produksi (TBP) / 3 bulan Rp 447.962.218,00 Total Biaya Produksi (TBP) / tahun Rp 1.791.848.872,00
Total Penjualan / tahun Rp 1.920.000.000,00
Laba sebelum pajak / tahun Rp 128.151.128,00
Pajak Rp 38.445.338,00
Laba setelah pajak / tahun Rp 89.705.789,00
Adapun analisa ekonominya akan dijabarkan sebagai berikut :
2.7.1 Modal Investasi Tetap (MIT)
A. Modal Biaya Tanah dan Bangunan
Bangunan kerja menggunakan rumah seharga = Rp 100.000.000
B. Perincian Harga Alat
19
No Jenis alat jumlah Harga (Rp) Harga total (Rp) 1 HZ-300 digital orbital shaker 1 7.840.000 7.840.000 2 Coconut milk press machine 1 67.200.000 67.200.000
total Rp 75.040.000
Total MIT = Rp 100.000.000 + Rp 75.040.000 = Rp 175.040.000
2.7.2 Modal Kerja
Modal kerja dihitung untuk pengoperasian selama 3 bulan 1 minggu = 5 hari kerja
1 bulan = 20 hari 3 bulan = 60 hari
A. Kelapa
1 shaker = 20 botol santan Waktu shaker = 30 menit
1 kg kelapa = 3 buah kelapa 1 buah kelapa = Rp. 8000
Harga 1 kg buah kelapa = 3x Rp 8000 = Rp 24.000/kg Asumsi target produksi = 200 botol/hari
⁄ ⁄
B. Khamir Saccharomyces cerevisiae
1 cawan petri = 10 liter khamir 1 liter = 1000 ml khamir
20
Kebutuhan khamir
Pada penelitian ini rendemen tertinggi diperoleh pada penambahan 10 % khamir. Volume khamir = 10% x volume santan
1 botol = 500 ml santan
Maka khamir yang dibutuhkan = 10.000 ml/hari = 1 cawan petri/hari
Harga 1 cawan khamir = Rp. 100.000
Harga khamir untuk 3 bulan = 60 x Rp. 100.000 = Rp. 6.000.000
Total biaya bahan baku selama 3 bulan = Rp. 6.000.000 + Rp 288.000.000
= Rp. 294.000.000
2.7.3 Kas
A. Gaji Pegawai
Tabel 2.6 Daftar Gaji Pegawai
Jabatan Jumlah Gaji/Orang
(Rp)
Total Gaji
(Rp)
Manajer 1 4.000.000 4.000.000
Karyawan Produksi 7 1.500.000 10.500.000
Karyawan Keuangan dan Administrasi 1 2.000.000 2.000.000
Total 16.500.000
Total gaji karyawan 1 bulan = Rp 16.500.000 Total gaji karyawan 3 bulan = Rp 49.500.000
B. Biaya Administrasi Umum
21 C. Biaya Pemasaran
[image:57.595.111.401.167.295.2]Diperkirakan sebesar 20 % dari gaji 3 bulan = 0,2 x Rp 49.500.000 = Rp. 9.900.000 Tabel 2.7 Perincian Biaya Kas
No Jenis Biaya Jumlah (Rp)
1 Gaji
karyawan 49.500.000 2 Administrasi umum 9.900.000
3 Pemasaran 9.900.000
Total 69.300.000
Maka Total biaya kas = Rp 69.300.000 / 3 bulan
2.7.4 Piutang Dagang
Dimana
PD : Piutang dagang
IP : Jangka waktu yang diberikan (1 bulan) HPT : Hasil penjualan 1 tahun
Produksi VCO = 200 botol/hari
Pada penelitian ini, rendemen VCO tertinggi yang diperoleh sebesar 24,5%. 1 botol = 500 ml santan
Maka VCO yang diperoleh per botol = 24,5% x 500 = 122,5 ml Harga produk VCO = Rp. 40.000/botol
22
Harga Penjualan Tahunan (HPT) = Rp 1.920.000.000
[image:58.595.110.427.213.322.2]
Tabel 2.8 Perincian Modal Kerja
No Modal Kerja Jumlah (Rp)
1 Bahan Baku 294.000.000
2 Kas 69.300.000
3 Piutang Dagang
Total 403.300.000
Total Modal Investasi = MIT + Modal Kerja
= Rp. 175.040.000 + Rp 403.300.000 = Rp. 578.340.000
Modal berasal dari :
Modal sendiri = 50% dari total modal investasi = 0,5 x Rp 592.340.000
= Rp 289.170.000
Modal pinjaman bank = 50% dari total modal investasi = 0,5 x Rp 592.340.000
= Rp 289.170.000
2.7.5 Biaya Produksi Total
A. Biaya Tetap (Fixed Cost)
Biaya tetap yaitu biaya yang tidak tergantung dari jumlah produksi, yakni :
Gaji Tetap Karyawan
Gaji tetap karyawan = 49.500.000 / 3 bulan
Bunga Pinjaman Bank
Diperkirakan 15% per tahun dari modal pinjaman bank = 0,15 x Rp 289.170.000
23
Bunga pinjaman bank selama 3 bulan = Rp 10.843.875 / 3 bulan
Depresiasi
[image:59.595.114.535.272.461.2]Pengeluaran untuk memperoleh harta berwujud yang mempunyai masa manfaat lebih dari 1 (satu) tahun harus dibebankan sebagai biaya untuk mendapatkan, menagih, dan memelihara penghasilan melalui penyusutan. Dasar penyusutan menggunakan masa manfaat dan tarif penyusutan sesuai dengan Undang-undang Republik Indonesia No. 17 Tahun 2000 Pasal 11 ayat 6 dapat dilihat pada tabel LE.8.
Tabel 2.9 Aturan Depresiasi Sesuai UU Republik Indonesia No. 17 Tahun 2000 Kelompok Harta
Berwujud
Umur
(Tahun)
Tarif
(%) Beberapa Jenis Harta
I. Bukan Bangunan
1. Kelompok 1 4 25 Mesin kantor, perlengkapan, alat perangkat/tools industry
2. Kelompok 2 8 12,5 Mobil, truk kerja
3. Kelompok 3 16 6,25 Mesin industri kimia, mesin industri mesin
II.Bangunan Permanen 20 5 Bangunan sarana dan penunjang
Depresiasi dihitung dengan metode garis lurus
D ( P L )n
Dimana :
D : Depresiasi per tahun P : Harga awal peralatan L : Harga akhir peralatan N : Umur peralatan (tahun) Depresiasi Bangunan
D = ( 100 000 000 - (5 x 100 000 000) )
24 Depresiasi Peralatan Mesin
D = ( 75 040 000 - (6,25 x 75 040 000) ) 16
= Rp 4.396.875
Total Depresiasi = Rp. 4.750.000 + Rp. 4.396.875 = Rp. 9.146.875/tahun Total Depresiasi per 3 bulan = Rp. 2.286.718 / 3 bulan
Total Biaya Tetap = Gaji Tetap Karyawan + Bunga Pinjaman Bank + Depresiasi = Rp 49.500.000 + Rp 43.375.500 + Rp 2.286.718
= Rp 95.162.218 / 3 bulan
- Biaya Variabel (Variabel Cost)
Biaya Variabel Bahan Baku per 3 bulan
Biaya persediaan bahan baku selama 3 bulan adalah = Rp. 294.000.000
Biaya Variabel Tambahan per 3 bulan
Diperkirakan sebesar 20 % dari biaya variabel bahan baku = 0,2 x Rp. 294.000.000 = Rp. 58.800.000
Total Biaya Variabel = Rp. 294.000.000 + Rp 58.800.000 = Rp. 352.800.000
Total Biaya Produksi per 3 bulan = Fixed Cost + Variabel Cost = Rp 95.162.218+ Rp 352.800.000 = Rp 447 .962.218 / 3 bulan
2.7.6 Perhitungan Rugi / Laba Usaha
A. Laba Sebelum Pajak
Total Penjualan / tahun = Rp 1.920.000.000 / tahun
Total Biaya Produksi / 3 bulan = Rp 447.962.218 / 3 bulan, maka Total Biaya Produksi / tahun = 1.791.848.872 / tahun
Laba atas penjualan = Total Penjualan – Total Biaya Produksi
25 = Rp 128.151.128/tahun B. Pajak Penghasilan
Berdasarkan Kep. Menkeu RI tahun 2000, pasal 17 tarif pajak penghasilan adalah :
Penghasilan 0 – 50.000.000 dikenakan pajak sebesar 10 %
Penghasilan 50.000.000 – 100.000.000 dikenakan pajak sebesar 15%
Penghasilan diatas 100.000.000 dikenakan pajak sebesar 30 % Maka perincian pajak penghasilan (PPh) :
= 0,3 x Rp. 128.151.128 = Rp. 38.445.338
Maka, Laba Setelah Pajak = Laba Sebelum Pajak - PPh = Rp 128.151.128– Rp 38.445.338
= Rp 89. 705.789
2.7.7 Analisa Aspek Ekonomi
Break Even Point (BEP)
BEP (Harga Jual per Unit Biaya Variabel per Unit)(Biaya Tetap)
Biaya Tetap = Rp 95.162.218/3 bulan
Biaya Variabel per unit = p 352 800 000 3 bulan 12000 botol 3 bulan = Rp 29.400/botol Harga Jual per unit = Rp 40.000/botol
BEP = ( p 95 162 218 3 bulan)
( p 10 600 botol)
= 8977 botol/ 3 bulan
1
BAB I
PENDAHULUAN
1.1 Latar Belakang
Indonesia adalah negara agraris yang memiliki lahan yang luas yang berdampak positif pada pertanian Indonesia yang melimpah. Keragaman Indonesia akan berbagai varietas tanaman sudah tersohor di dunia. Oleh karena itu berbagai produk pertanian Indonesia cukup terkenal di kawas