EFIKASI GABUNGAN ARTEMETER-LUMEFANTRIN DAN ARTESUNAT-AMODIAKUIN SEBAGAI PENGOBATAN MALARIA FALSIPARUM TANPA
KOMPLIKASI PADA ANAK
TESIS
TRI FARANITA 077103006/IKA
PROGRAM MAGISTER KLINIK-SPESIALIS ILMU KESEHATAN ANAK FAKULTAS KEDOKTERAN UNIVERSITAS SUMATERA UTARA
EFIKASI GABUNGAN ARTEMETER-LUMEFANTRIN DAN ARTESUNAT-AMODIAKUIN SEBAGAI PENGOBATAN MALARIA FALSIPARUM TANPA
KOMPLIKASI PADA ANAK
TESIS
Untuk memperoleh gelar Magister Kedokteran Klinik di Bidang Ilmu Kesehatan Anak / M.Ked (Ped) pada Fakultas Kedokteran
Universitas Sumatera Utara
TRI FARANITA 077103006/IKA
PROGRAM MAGISTER KLINIK-SPESIALIS ILMU KESEHATAN ANAK FAKULTAS KEDOKTERAN UNIVERSITAS SUMATERA UTARA
Judul Penelitian : Efikasi Gabungan Artemeter-Lumefantrin dan
Artesunat-Amodiakuin sebagai Pengobatan Malaria
Falsiparum Tanpa Komplikasi pada Anak
Nama Mahasiswa : Tri Faranita
Nomor Induk Mahasiswa : 077103006
Program Magister : Magister Kedokteran Klinik
Konsentrasi : Kesehatan Anak
Menyetujui
Komisi Pembimbing :
Prof. DR. dr H. Syahril Pasaribu, DTM&H, MSc(CTM), SpA(K)
Ketua
Dr. Muhammad Ali, SpA(K)
Anggota
Ketua Program Magister Ketua TKP-PPDS
Telah diuji pada
Tanggal : 7 November 2011
PANITIA PENGUJI TESIS
Ketua : Prof. DR. dr. Syahril Pasaribu, DTM&H, ...
MSc(CTM), SpA(K)
Anggota : 1. Dr. Muhammad Ali, SpA(K) ...
2. Dr. Endang H. Ganie, DTM&H, SpPar(K) ...
3. Dr. Hj. Melda Deliana, SpA(K) ...
UCAPAN TERIMA KASIH
Assalamualaikum Wr. Wb.
Puji dan syukur kehadirat Allah SWT yang telah melimpahkan rahmat dan hidayah-Nya serta telah memberikan kesempatan kepada penulis sehingga dapat menyelesaikan penulisan tesis ini.
Tesis ini dibuat untuk memenuhi persyaratan dan merupakan tugas akhir pendidikan magister Kedokteran Klinik Konsentrasi Ilmu Kesehatan Anak di FK-USU / RSUP H. Adam Malik Medan.
Pada kesempatan ini perkenankanlah penulis menyatakan penghargaan dan ucapan terima kasih yang sebesar-besarnya kepada :
1. Pembimbing utama Prof. DR. dr. Syahril Pasaribu, DTM&H, Msc(CTM), SpA(K), dan dr. Muhammad Ali, SpA(K), yang telah memberikan bimbingan, bantuan serta saran-saran yang sangat berharga dalam pelaksanaan penelitian dan penyelesaian tesis ini.
2. Prof. dr. H. Munar Lubis, SpA(K), selaku Ketua Program Studi Pendidikan Dokter Spesialis Anak FK-USU periode 2007 – 2010 dan Ketua Departemen Ilmu Kesehatan Anak sejak tahun 2011, yang telah banyak memberi waktu, tenaga dan pikiran dalam mewujudkan penelitian hingga selesai penyusunan tesis ini.
3. Dr. H. Ridwan M. Daulay, SpA(K), selaku Ketua Departemen Ilmu Kesehatan Anak Fakultas Kedokteran USU/RSUP H. Adam Malik Medan periode 2007 – 2010 dan Dr. Hj. Melda Deliana, SpA(K), sebagai Ketua Program Studi sejak tahun 2011 hingga saat ini yang telah banyak membantu dalam menyelesaikan tesis ini.
4. Seluruh staf pengajar di Departemen Ilmu Kesehatan Anak FK USU / RSUP H. Adam Malik Medan dan RS. dr. Pirngadi Medan, terutama dr. Ayodhia Pitaloka Pasaribu, MKed(Ped), SpA dan dr. Hj. Bugis Mardina Lubis, SpA yang telah memberikan sumbangan pikiran dalam pelaksanaan penelitian dan penulisan tesis ini.
6. Drg. Bidasari Lubis sebagai direktur Rumah Sakit Umum Panyabungan saat penelitian ini berlangsung serta para perawat yang telah memberi kerja sama yang baik dalam mewujudkan penelitian ini.
7. Kepala Balai Pusat Penanggulangan Malaria pada saat penelitian ini berlangsung, Bapak Arifin Fauzi Lubis,S.Si,Apt,MM dan para kader malaria yang sudah dengan tangan terbuka menerima kami dan bekerjasama dalam kelancaran penelitian ini.
8. Kepala Sekolah beserta guru-guru dimana penelitian ini dilakukan, yang telah baik menerima dan membantu selama penelitian.
9. Dr. Athos Daulay, SpA dan istri, serta Dr. Nuraidah,SpA yang dengan berbaik hati menerima kami sehingga penelitian ini dapat diselesaikan, semoga Allah SWT senantiasa melimpahkan rahmatNya.
10. Teman-teman yang tidak mungkin bisa saya lupakan yang telah membantu saya dalam keseluruhan penelitian maupun penyelesaian tesis ini, dr. Mahrani Lubis, dr. Washli Zakiah, dr. Fadli Syahputra, dr. Kholidah Nasution, dr. Sevina Marisya, dr. Suratmin, dr. Vivianna, dr. Erika, dan teman-teman yang lain yang tidak dapat disebutkan satu persatu, terimakasih untuk ketulusan dan mohon maaf atas kesalahan selama penelitian maupun masa pendidikan.
Teristimewa untuk suami tercinta Prima Septanto, ST dan ananda tersayang Nadaura Kayyisah, terima kasih atas doa, pengertian, dukungan dan pengorbanan hingga penulis mampu menyelesaikan penelitian dan tesis ini. Mudah-mudahan Allah SWT senantiasa melimpahkan rahmat dan perlindunganNya buat kita semua.
Kepada yang sangat saya cintai dan hormati, orangtua saya Prof. dr. M. Fauzie Sahil, SpOG.K (Onk) dan dr. Hj. RA. Anggraini Erma, SpA atas pengertian serta dukungan yang sangat besar, terima kasih karena selalu mendo’akan saya dan memberikan bantuan moril dan materil. Begitu juga Ayuk Sum, Kak Rinny, Kak Dina, Arrie, Icut, En, Sonya dan Beby yang selalu mendo’akan dan memberikan dorongan selama mengikuti pendidikan ini. Semoga budi baik yang telah diberikan mendapat imbalan dari Allah SWT.
Akhirnya penulis mengharapkan semoga penelitian dan tulisan ini dapat bermanfaat bagi kita semua, Amin.
Wassalamualaikum Wr. Wb.
DAFTAR ISI
Lembar Persetujuan Pembimbing ii
Ucapan Terima Kasih iv
Daftar Isi vi
Daftar Tabel vii
Daftar Gambar viii
Daftar Singkatan dan Tanda ix
Abstrak x
Bab 1. Pendahuluan 1
1.1. Latar Belakang 1
1.2. Rumusan Masalah 2
1.3. Hipotesis 3
1.4. Tujuan Penelitian 3
1.5. Manfaat Penelitian 3
Bab 2. Tinjauan Pustaka 5
2.1. Penyebab Malaria 5
2.2. Diagnosis Malaria Falsiparum 5
2.3. Pengobatan Malaria Falsiparum Tanpa Komplikasi 6
2.4. Gabungan Artesunat-Amodiakuin 7
2.5. Gabungan Artemether-Lumefantrin 10
2.6. Kerangka Konseptual 12
Bab 3. Metode Penelitian 13
3.1. Desain Penelitian 13
3.2. Tempat dan Waktu Penelitian 13
3.3. Populasi Penelitian 13
3.4. Estimasi Besar Sampel 14
3.5. Kriteria Inklusi dan Eksklusi 15
3.6. Persetujuan/Informed Consent 15
3.7. Etika Penelitian 16
3.8. Cara Kerja dan Alur Penelitian 16
3.9. Identifikasi Variabel 19
3.10. Definisi Operasional 19
3.11. Analisis dan Penyajian Data 22
Bab 5. Pembahasan 28
Bab 6. Kesimpulan dan Saran
6.1. Kesimpulan 34
6.2. Saran 34
Bab 7. Ringkasan 35
Daftar Pustaka 39
Lampiran
1. Personil Penelitian 44
2. Biaya Penelitian 45
3. Jadwal Penelitian 45
4. Penjelasan dan Persetujuan kepada Orang Tua 46
5. Kuisioner Penelitian 49
6. Lembar Pemantauan Pasien 51
7. Persetujuan Komite Etik 55
DAFTAR TABEL
Tabel 4.1. Karakteristik dasar subjek penelitian 25
Tabel 4.2. Respon pengobatan 26
DAFTAR GAMBAR
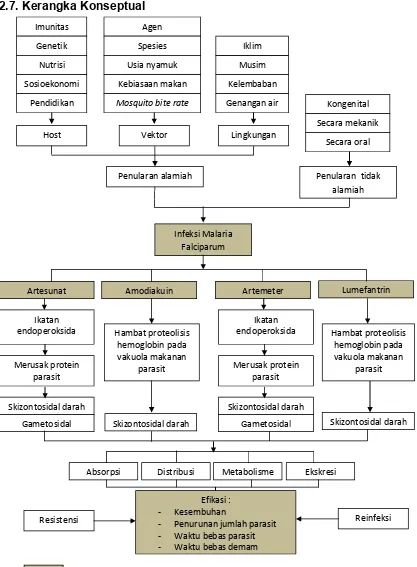
Gambar 2.1. Kerangka konsep penelitian 12
DAFTAR LAMBANG DAN SINGKATAN
ACTs : Artemisinin combination therapies
ACPR : Adequate clinical and parasitology response
AL : Artemeter lumefantrin
An. kochi : Anopheles kochi An. nigerrimus : Anopheles nigerrimus An. sundaicus : Anopheles sundaicus An. tesselatus : Anopheles tesselatus
ASAQ : Artesunat amodiakuin
CDC : Centers for Disease Control
ETF : Early treatment failure
LTF : Late treatment failure
PCR : Polymerase Chain reaction
P. falciparum : Plasmodium falciparum P. knowlesi : Plasmodium knowlesi P. malariae : Plasmodium malariae
P. ovale : Plasmodium ovale
P. vivax : Plasmodium vivax
PF : Parasitological failure
WHO : World Health Organization
% : Persen
cm : centimeter
mg : miligram
kgbb : kilogram berat badan
z : Deviat baku normal untuk
zβ : Deviat baku normal untuk β
n : Jumlah subjek / sampel
> : Lebih besar dari
< : Lebih kecil dari
α : Kesalahan tipe I
β : Kesalahan tipe II
P : Besarnya peluang untuk hasil yang diobservasi bila hipotesis nol benar
Abstrak
Latar Belakang.Gabungan artesunat-amodiakuin (ASAQ) telah digunakan sebagai obat lini pertama untuk anak Malaria Falsiparum tanpa komplikasi di Indonesia
sejak tahun 2004. Efikasi obat ini tergantung pada resistensi terhadap amodiakuin. Artemeter-lumefantrin (AL) memiliki efikasi yang tinggi dalam mengobati Malaria
Falsiparum tanpa komplikasi di beberapa negara. Namun informasi tentang gabungan obat ini sangat terbatas di Indonesia.
Tujuan. Untuk membandingkan efikasi AL dengan ASAQ dalam mengobati anak Malaria Falsiparum tanpa komplikasi.
Metode. Penelitian terbuka dilakukan pada anak usia sekolah di Kabupaten Mandailing Natal, Propinsi Sumatera Utara, Indonesia mulai Oktober hingga Desember 2010. Secara acak 280 anak Malaria Falsiparum tanpa komplikasi diberi
pengobatan dengan AL atau ASAQ selama 3 hari. Partisipan dipantau pada hari 1, 2, 3, 7, 14, 28 dan 42. Hasil yang dinilai berupa Adequate Clinical and Parasitological Response (ACPR), waktu bebas demam, waktu bebas parasit, penurunan jumlah parasit dan efek samping. Analisis penelitian ini berbasis
intention to treat.
Hasil. Pada penelitian ini didapatkan ACPR hari ke 42 pada kedua kelompok pada kelompok ASAQ 86.4% dan kelompok AL 90.7% (P=0.260). Angka kesembuhan
hari ke 7 dan 14 lebih tinggi pada kelompok AL dibandingkan kelompok ASAQ. ETF, LTF dan PF pada kedua kelompok tidak berbeda bermakna. Dijumpai waktu
bebas parasit yang lebih cepat dan penurunan parasit yang lebih tinggi pada kelompok AL dibandingkan kelompok ASAQ. Sedangkan waktu bebas demam lebih
cepat dijumpai pada kelompok ASAQ. Insiden efek samping seperti mual, muntah, malaise dan pruritus tidak berbeda pada kedua kelompok (P=0.441).
Abstract
Background. Artesunate-amodiaquine (ASAQ) has been used as first line treatment for uncomplicated falciparum malaria in Indonesia since 2004. Its efficacy
depends on amodiaquine resistance. Artemether-lumefantrine (AL) has high efficacy
in treating uncomplicated falciparum malaria in several countries. However, there is
little information on this combination in Indonesia.
Objective. To compare the efficacy of AL and ASAQ for treating uncomplicated falciparum malaria in children.
Methods. An open randomized controlled trial was conducted in school aged children in Mandailing Natal Regency, North Sumatera Province, Indonesia, from
October to December 2010. A total of 280 uncomplicated falciparum malaria
children were randomly assigned for AL or ASAQ for 3 days. Participants were
followed-up on day 1, 2, 3, 7, 14, 28 and 42. The outcomes were adequate clinical
and parasitological response (ACPR), parasite reduction, parasite clearance time,
fever clearance time and adverse events. Analysis was based on intention to treat.
Results. In this study, ACPR on day 42 were 86.4% and 90.7% on ASAQ and AL group, respectively (P=0.260). On day 7 and 14, AL group has higher cure rate than
ASAQ group (P<0.05). ETF, LTF and PF on both groups were similar. We also
found faster parasite clearance time and higher parasite reduction on AL group
compared to ASAQ group. But fever clearance time were shorter in ASAQ group.
The incidence of adverse events such as nausea, vomit, malaise and pruritus were
similar between two groups (P=0.441).
Conclusion. AL has higher efficacy than ASAQ for the treatment of uncomplicated falciparum malaria in children
Abstrak
Latar Belakang.Gabungan artesunat-amodiakuin (ASAQ) telah digunakan sebagai obat lini pertama untuk anak Malaria Falsiparum tanpa komplikasi di Indonesia
sejak tahun 2004. Efikasi obat ini tergantung pada resistensi terhadap amodiakuin. Artemeter-lumefantrin (AL) memiliki efikasi yang tinggi dalam mengobati Malaria
Falsiparum tanpa komplikasi di beberapa negara. Namun informasi tentang gabungan obat ini sangat terbatas di Indonesia.
Tujuan. Untuk membandingkan efikasi AL dengan ASAQ dalam mengobati anak Malaria Falsiparum tanpa komplikasi.
Metode. Penelitian terbuka dilakukan pada anak usia sekolah di Kabupaten Mandailing Natal, Propinsi Sumatera Utara, Indonesia mulai Oktober hingga Desember 2010. Secara acak 280 anak Malaria Falsiparum tanpa komplikasi diberi
pengobatan dengan AL atau ASAQ selama 3 hari. Partisipan dipantau pada hari 1, 2, 3, 7, 14, 28 dan 42. Hasil yang dinilai berupa Adequate Clinical and Parasitological Response (ACPR), waktu bebas demam, waktu bebas parasit, penurunan jumlah parasit dan efek samping. Analisis penelitian ini berbasis
intention to treat.
Hasil. Pada penelitian ini didapatkan ACPR hari ke 42 pada kedua kelompok pada kelompok ASAQ 86.4% dan kelompok AL 90.7% (P=0.260). Angka kesembuhan
hari ke 7 dan 14 lebih tinggi pada kelompok AL dibandingkan kelompok ASAQ. ETF, LTF dan PF pada kedua kelompok tidak berbeda bermakna. Dijumpai waktu
bebas parasit yang lebih cepat dan penurunan parasit yang lebih tinggi pada kelompok AL dibandingkan kelompok ASAQ. Sedangkan waktu bebas demam lebih
cepat dijumpai pada kelompok ASAQ. Insiden efek samping seperti mual, muntah, malaise dan pruritus tidak berbeda pada kedua kelompok (P=0.441).
Abstract
Background. Artesunate-amodiaquine (ASAQ) has been used as first line treatment for uncomplicated falciparum malaria in Indonesia since 2004. Its efficacy
depends on amodiaquine resistance. Artemether-lumefantrine (AL) has high efficacy
in treating uncomplicated falciparum malaria in several countries. However, there is
little information on this combination in Indonesia.
Objective. To compare the efficacy of AL and ASAQ for treating uncomplicated falciparum malaria in children.
Methods. An open randomized controlled trial was conducted in school aged children in Mandailing Natal Regency, North Sumatera Province, Indonesia, from
October to December 2010. A total of 280 uncomplicated falciparum malaria
children were randomly assigned for AL or ASAQ for 3 days. Participants were
followed-up on day 1, 2, 3, 7, 14, 28 and 42. The outcomes were adequate clinical
and parasitological response (ACPR), parasite reduction, parasite clearance time,
fever clearance time and adverse events. Analysis was based on intention to treat.
Results. In this study, ACPR on day 42 were 86.4% and 90.7% on ASAQ and AL group, respectively (P=0.260). On day 7 and 14, AL group has higher cure rate than
ASAQ group (P<0.05). ETF, LTF and PF on both groups were similar. We also
found faster parasite clearance time and higher parasite reduction on AL group
compared to ASAQ group. But fever clearance time were shorter in ASAQ group.
The incidence of adverse events such as nausea, vomit, malaise and pruritus were
similar between two groups (P=0.441).
Conclusion. AL has higher efficacy than ASAQ for the treatment of uncomplicated falciparum malaria in children
BAB 1. PENDAHULUAN
1.1. Latar Belakang
Malaria merupakan penyakit infeksi yang menjadi masalah kesehatan pada
anak-anak dan orang dewasa di daerah tropis.1,2 Diperkirakan penyakit ini
menyebabkan 1 juta kematian tiap tahunnya atau 3 ribu kematian tiap hari
terutama pada anak dan ibu hamil.2,3 Di Indonesia, pada tahun 2008
dilaporkan sebanyak 411 ribu orang menderita malaria dengan kematian
sebesar 788 kasus, 46% diantaranya disebabkan oleh infeksi Plasmodium
falciparum.4
Malaria yang disebabkan Plasmodium falciparum paling banyak
menyebabkan kematian dan sakit berat.5 Untuk mencegah peningkatan
angka kesakitan malaria dibutuhkan pengobatan yang efektif pada Malaria
Falsiparum tanpa komplikasi.6,7
Resisten obat merupakan masalah utama di Afrika dan kebanyakan
negara lain sehingga tiap negara harus mengubah kebijakan obat
antimalaria untuk memastikan penatalaksanaan yang efektif.7 Gabungan
artesunat-amodiakuin telah digunakan sebagai obat lini pertama Malaria
Falsiparum tanpa komplikasi di Indonesia sejak tahun 2004.3 Penelitian yang
gabungan artesunat-amodiakuin efektif dalam mengobati Malaria Falsiparum
tanpa komplikasi.8
Resistensi terhadap amodiakuin telah dilaporkan di Afrika maupun
Papua Nugini.9,10 Efek samping amodiakuin yang berat pada penggunaan
profilaksis membuat obat ini hanya digunakan sebagai terapi. Efek samping
berupa bradikardi persisten telah dilaporkan pada anak yang diobati dengan
amodiakuin.11
Artemeter-lumefantrin merupakan salah satu Artemisinin-based
combination therapies (ACTs) yang menjadi obat lini pertama untuk malaria
tanpa komplikasi di Caala, Angola.12 Gabungan artemeter- lumefantrin
terbukti memiliki efektivitas yang tinggi dan ditoleransi baik pada beberapa
studi di Afrika.12,13 Informasi mengenai efektivitas obat ini di Indonesia masih
terbatas. Hasil penelitian di Papua, Indonesia terhadap artemeter-lumefantrin
sebagai pengobatan Malaria Falsiparum, Malaria Vivax ataupun infeksi
campuran falsiparum dan vivax didapatkan bahwa gabungan obat ini
memiliki efektivitas yang tinggi pada anak dan dewasa.14
1.2. Rumusan Masalah
Berdasarkan latar belakang masalah di atas, dapat dirumuskan masalah
Apakah gabungan artemeter-lumefantrin memiliki efikasi yang sama dengan
artesunat-amodiakuin sebagai terapi Malaria Falsiparum tanpa komplikasi
pada anak?
1.3. Hipotesis
Gabungan artemeter-lumefantrin memiliki efikasi yang sama dengan
artesunat-amodiakuin pada anak dengan Malaria Falsiparum tanpa
komplikasi.
1.4. Tujuan Penelitian
Membandingkan efikasi gabungan artemeter-lumefantrin dengan
artesunat-amodiakuin sebagai pengobatan Malaria Falsiparum tanpa komplikasi pada
anak.
1.5. Manfaat Penelitian
1.5.1. Di bidang akademis/ilmiah: meningkatkan pengetahuan peneliti
terhadap efikasi gabungan artemeter-lumefantrin dengan
artesunat-amodiakuin sebagai pengobatan Malaria Falsiparum tanpa komplikasi
1.5.2. Di bidang pelayanan masyarakat: meningkatkan kualitas pelayanan
kesehatan anak, khususnya terhadap pilihan terapi kombinasi
artemisinin pada anak dengan Malaria Falsiparum tanpa komplikasi.
1.5.3. Di bidang pengembangan penelitian: memberi data awal terhadap
Divisi Infeksi dan Penyakit Tropik khususnya mengenai efikasi
gabungan artemeter-lumefantrin sebagai pengobatan Malaria
BAB 2. TINJAUAN PUSTAKA
2.1. Penyebab Malaria
Malaria adalah penyakit yang disebabkan oleh protozoa genus Plasmodium
yang ditransmisikan ke manusia melalui nyamuk anopheles betina.5,15 Ada
lima spesies Plasmodium yang dapat menginfeksi manusia, yaitu P.
malariae, P. vivax, P. falciparum, P. ovaledan P. knowlesi.16,17
Plasmodium falciparum merupakan spesies yang banyak dijumpai di
daerah tropis.1,6 Empat puluh persen populasi dunia menderita penyakit
malaria akibat spesies ini. 6,9 Plasmodium falciparum juga menyebabkan
malaria berat dan kematian.2,7,15
2.2. Diagnosis Malaria Falsiparum
Diagnosis malaria ditegakkan berdasarkan gejala klinis disertai dengan
adanya parasit di darah.7 Masa inkubasi P. falciparum biasanya 10 sampai
14 hari dengan gejala berupa demam paroksismal timbul saat pecahnya
eritrosit yang mengandung parasit.18 Namun gejala klasik ini sering tidak
terjadi terutama pada infeksi P. falciparum.1,15 Gejala yang mungkin timbul
akibat infeksi spesies ini berupa demam terus menerus, gangguan
nyeri sendi, sesak napas dan pucat.1,5,6,15 Pada pemeriksaan fisis dapat
dijumpai pucat serta hepatosplenomegali.1,18
Dua metode yang digunakan untuk pemeriksaan parasit dalam darah
yaitu melalui mikroskop dan tes diagnostik cepat.6,19 Pemeriksaan apusan
darah tepi tipis dan tebal dengan menggunakan pewarnaan Field maupun
Giemsa masih menjadi baku emas diagnosis malaria dengan sensitivitas
dan spesifisitas yang tinggi jika diperiksa oleh para ahli.1,3,6,19 Penelitian yang
membandingkan lima metode untuk mendeteksi malaria didapati bahwa
pewarnaan Field memiliki sensitivitas, spesifisitas, kemudahan dan cost
effectiveyang lebih baik sebagai penunjang diagnosis malaria.19
Pada pemeriksaan apusan darah tepi Malaria Falsiparum akan terlihat
parasit stadium tropozoit muda (bentuk cincin) tanpa atau dengan stadium
gametosit yang berbentuk pisang.20
2.3. Pengobatan Malaria Falsiparum Tanpa Komplikasi
Untuk mengatasi ancaman resistensi P. falciparum terhadap monoterapi,
saat ini WHO merekomendasikan kombinasi obat antimalaria sebagai
pengobatan lini pertama terhadap malaria tanpa komplikasi yang terdiri dari
Artemisinin-based combinations therapies (ACTs) dan Non
Tujuan terapi kombinasi obat antimalaria adalah untuk memperlambat
timbulnya resistensi dengan menggunakan dua jenis obat blood
schizontocidal atau lebih yang memiliki kerja yang berbeda dengan target
biokimiawi parasit yang berbeda pula.6,21
Artemisinin dan derivatnya dapat menurunkan parasitemia dan gejala
dengan cepat.6,21 Artemisinin-based combination therapies (ACTs) yang
direkomendasikan yaitu antara lain gabungan artemeter-lumefantrin,
artesunat-amodiakuin, artesunat-meflokuin, artesunat dan
sulfadoksin-pirimetamin, serta dihidroartemisinin-piperakuin.6
Sebuah uji klinis terbuka di Ghana yang membandingkan gabungan
artemeter-lumefantrin dengan gabungan artesunat-amodiakuin didapati
bahwa kedua gabungan obat tersebut memiliki efektivitas yang tinggi dan
baik ditoleransi pada populasi.22 Hasil yang sama didapati dari penelitian
yang dilakukan di Uganda.23
2.4. Gabungan Artesunat-Amodiakuin
Artesunat merupakan derivat artemisinin yang larut dalam air dan paling luas
digunakan sebagai terapi.6,15Obat ini cepat diabsorpsi dengan masa paruh <
10 menit dengan metabolit berupa dihidroartemisinin yang memiliki waktu
Artesunat memiliki bioavaibilitas yang baik pada Malaria Falsiparum yang
akut.25
Cara kerja artesunat sama dengan derivat artemisinin lainnya yaitu
dengan mengikat besi pada pigmen malaria untuk menghasilkan radikal
bebas yang akan berinteraksi dan merusak protein parasit mulai dari bentuk
cincin, tropozoit, skizon dan mampu menghambat gametosit.15,24 Efek
samping obat ini dapat berupa gangguan gastrointestinal ringan, pusing,
tinitus, retikulositopenia, netropenia, peningkatan enzim hati dan
abnormalitas ekokardiografi.6
Amodiakuin merupakan 4-aminokuinolon yang mirip secara struktur
dan aktivitas dengan klorokuin dengan efikasi yang lebih tinggi.5,6 Secara
oral absorpsi amodiakuin sangat cepat dan diubah menjadi metabolit aktif di
hati.6,21 Belum ada data waktu paruh eliminasi plasma dari
desethylamodiaquine, baik amodiakuin maupun metabolit aktifnya dapat
dideteksi pada urin setelah beberapa bulan dari pemberian obat.6
Amodiakuin bekerja dengan cara menghambat proteolisis hemoglobin
pada vakuola makanan parasit.15 Amodiakuin memiliki efek samping
netropenia bila diberikan sebagai obat profilaksis.11 Efek samping yang
mungkin dapat timbul pada penggunaan amodiakuin sebagai terapi adalah
Di Indonesia gabungan obat artesunat dengan amodiakuin
merupakan lini pertama untuk pengobatan Malaria Falsiparum tanpa
komplikasi.3 Efikasi dan keamanan gabungan artesunat dan amodiakuin
telah dievaluasi dan didapati bahwa gabungan obat ini sangat baik
ditoleransi.8,23,26 Derajat efikasi gabungan obat ini berhubungan dengan
rendahnya resistensi amodiakuin di daerah penelitian.10,26
Gabungan artesunat-amodiakuin tampaknya menjadi pilihan yang
baik di tempat yang resistensi terhadap klorokuin. Namun pemantauan
berkelanjutan terhadap resistensi amodiakuin perlu dilakukan.26
Dari uji klinis yang membandingkan tiga gabungan obat di Uganda
didapatkan bahwa gabungan artesunat amodiakuin sedikit menimbulkan efek
samping anoreksia dan tubuh lemah dibandingkan dengan gabungan
amodiakuin dan sulfadoksin-pirimetamin.13 Efek samping lain yang mungkin
dapat timbul dari gabungan kedua obat ini adalah batuk, nyeri perut, muntah,
sakit kepala dan tinitus.8,23,27
Saat ini sediaan artesunat-amodiakuin yang tersedia terdiri dari 50
mg artesunat dan 153 mg basa amodiakuin dengan dosis pemberian
2.5. Gabungan Artemeter-Lumefantrin
Gabungan artemeter dan lumefantrin dengan perbandingan 1:6 merupakan
obat antimalaria derivat artemisinin fixed-dose pertama. Kedua obat ini
merupakan blood schinzoticides dengan farmakokinetik tidak sama dan
memiliki aktivitas yang sinergis.28
Artemeter merupakan derivat artemisinin yang larut dalam lemak dan
cepat dieliminasi dari plasma dengan waktu paruh dua hingga tiga jam.6,28
Konsentrasi puncak yang cepat menyebabkan penurunan massa parasit
aseksual secara cepat sehingga mengurangi gejala.29 Efek samping dan
toksisitas obat ini sama dengan derivat artemisinin lainnya.6
Lumefantrin merupakan obat anti malaria golongan aryl aminoalcohol
seperti kinin, meflokuin dan halofantrin yang bekerja di vakuola makanan
parasit dengan mengganggu pembentukan hem.6Obat ini dieliminasi dengan
waktu paruh tiga hingga enam hari sehingga memiliki cure rate jangka
panjang setelah pemberian jangka pendek.6,28 Bioavaibilitas oral lumefantrin
bervariasi dan diabsorpsi lebih baik bila diberikan bersama lemak dan
mencapai puncak plasma sekitar 10 jam setelah pemberian.6,29
Efek samping lumefantrin yang dilaporkan umumnya ringan seperti
nyeri kepala, pusing, nyeri perut dan mual.6 Lumefantrin tidak tersedia
Dari beberapa penelitian terhadap keamanan gabungan obat ini
didapati bahwa efek samping yang dapat terjadi adalah peningkatan
temperatur,23nyeri kepala, nyeri perut dan batuk.13,30,31
Saat ini tersedia tablet yang terdiri dari 20 mg artemeter dengan
lumefantrin 120 mg. Dosis artemeter-lumefantrin berdasarkan berat badan
yaitu untuk berat badan 5 – <15 kg sebanyak 1 tablet per kali, 15 – <25 kg
sebanyak 2 tablet per kali, 25 – <35 kg sebanyak 3 tablet perkali dan untuk
berat badan > 35 kg sebanyak 4 tablet per kali beri.31 Pemberian gabungan
obat ini sangat optimal jika diberikan dengan enam dosis regimen, dua kali
sehari selama tiga hari.31 Pemberian dosis kedua berjarak 8 hingga 12 jam
2.7. Kerangka Konseptual Imunitas Genetik Nutrisi Sosioekonomi Pendidikan Agen Spesies Usia nyamuk Kebiasaan makan
Mosquito bite rate Genangan air Musim
Iklim
Kelembaban
Host Vektor Lingkungan
Penularan alamiah Penularan tidak alamiah Secara oral Kongenital Secara mekanik Infeksi Malaria Falciparum
Absorpsi Distribusi Metabolisme Ekskresi
Skizontosidal darah Skizontosidal darah Skizontosidal darah Gametosidal Merusak protein parasit Ikatan endoperoksida
Artesunat Amodiakuin Artemeter Lumefantrin
Hambat proteolisis hemoglobin pada vakuola makanan parasit Skizontosidal darah Gametosidal Merusak protein parasit Ikatan endoperoksida Efikasi : - Kesembuhan
- Penurunan jumlah parasit - Waktu bebas parasit
Resistensi Reinfeksi
Hambat proteolisis hemoglobin pada vakuola makanan
BAB 3. METODE PENELITIAN
3.1. Desain Penelitian
Desain uji klinis acak terbuka dipergunakan dalam penelitian ini untuk
mengetahui manfaat artemeter-lumefantrin sebagai alternatif
artesunat-amodiakuin sebagai terapi standar pada pengobatan
Malaria Falsiparum tanpa komplikasi.
3.2. Tempat dan Waktu Penelitian
Penelitian ini dilakukan di Kabupaten Mandailing Natal, Propinsi
Sumatera Utara pada bulan Oktober sampai Desember 2010.
3.3. Populasi Penelitian
Populasi target adalah anak berusia 6 sampai 18 tahun. Populasi
terjangkau adalah populasi target yang berada di Kabupaten
Mandailing Natal, Propinsi Sumatera Utara selama bulan Oktober
2010. Sampel adalah populasi terjangkau yang memenuhi kriteria
3.4. Estimasi Besar Sampel
Besar sampel dihitung dengan mempergunakan rumus besar sampel
untuk uji klinis negatif, yaitu:32
n 1 = n2 = ( 2PQ (Zα + Zβ) 2)
(P 1– P 2) 2
n 1 = jumlah subjek yang masuk dalam kelompok I
n 2 = jumlah subjek yang masuk dalam kelompok II
α = kesalahan tipe I = 0,05 →Tingkat kepercayaan 95%
Zα = nilai baku normal = 1,96
β = kesalahan tipe II = 0,2 → Power (kekuatan penelitian) 80%
Zβ = 0,84
P1 = Proporsi efek terapi kelompok I = 91% = 0,9126
Q1 = 1- P1= 0,09
P2 = Proporsi efek terapi kelompok II= 99% = 0,99
Q2 = 1- P2= 0,01
P = P1+ P2 = 0,95 2
Q = 1- P = 0,05
Dengan menggunakan rumus di atas didapat jumlah sampel untuk
3.5. Kriteria Inklusi dan Eksklusi
3.5.1. Kriteria inklusi :
1. Dijumpai Plasmodium falciparumpada pemeriksaan darah tepi
2. Densitas parasit < 250.000 parasit aseksual/µL
3. Mengisi surat persetujuan orang tua
3.5.2. Kriteria eksklusi :
1. Penderita malaria dengan komplikasi
2. Gizi buruk
3. Malaria campuran (mixed infection)
4. Terdapat riwayat hipersensitif terhadap obat yang diteliti
5. Muntah sebanyak dua kali, yaitu dalam 30 menit setelah
pemberian obat dan saat pengulangan pemberian obat setelah
muntah yang pertama
6. Mengkonsumsi obat antimalaria selain obat yang diteliti selama
masa penelitian
7. Tidak teratur/menolak minum obat
3.6. Persetujuan/ Informed Consent
yang diberikan dan efek samping pengobatan. Formulir persetujuan setelah
penjelasan (PSP) dan naskah penjelasan kepada orang tua sebagaimana
terlampir dalam laporan penelitian ini.
3.7. Etika Penelitian
Penelitian ini disetujui oleh Komite Etik Kesehatan Fakultas Kedokteran
Universitas Sumatera Utara.
3.8. Cara Kerja dan Alur Penelitian
1. Siswa yang berusia 6 sampai 18 tahun disaring melalui pemeriksaan
darah tepi tipis dan tebal
2. Apusan darah tipis dan tebal disiapkan dengan pewarnaan Giemsa
sesuai prosedur dan dibaca di tempat oleh analis terlatih. Parasit
dihitung dalam 200 sel darah putih. Dianggap negatif jika tidak
dijumpai parasit pada 100 lapangan pandang.
3. Bila pada apusan darah tepi dijumpai malaria lain selain falsiparum
maupun infeksi campuran akan diterapi sesuai dengan jenis malaria
yang diderita
4. Kontrol kualitas apusan darah tepi dilakukan dengan membaca ulang
5. Pemeriksaan antropometri dilakukan pada setiap siswa. Sebelum
dilakukan pemeriksaan, anak melepaskan alas kaki dan
mengeluarkan seluruh isi kantong dan aksesori yang melekat di
tubuhnya. Berat badan ditentukan dengan menggunakan alat
penimbang Camry yang telah ditera sebelumnya dengan kapasitas
sampai 125 kg. Tinggi badan diukur dengan menggunakan alat
Microtoir 2 M terbuat dari metal, dengan ketepatan 0.5 cm.
Pemeriksaan tinggi badan dilakukan dengan posisi tubuh anak berdiri
tegak dengan kedua tumit menyentuh dinding dengan kaki dirapatkan.
Status nutrisi dinilai dengan menggunakan grafik weight-for-height
CDC 2000
6. Orang tua siswa yang memenuhi kriteria inklusi mengisi inform
consent
7. Partisipan yang memenuhi kriteria inklusi secara acak sederhana
dengan menggunakan amplop tertutup dimasukkan ke dalam satu
dari dua kelompok perlakuan yaitu kelompok pertama artesunat
ditambah amodiakuin dan kelompok kedua artemeter-lumefantrin
8. Kelompok pertama (A) mendapat pengobatan per oral artesunat
4mg/kgbb digabung amodiakuin 10mg/kgbb selama 3 hari. Kelompok
<15 kg (1 tablet), 15 – <25 kg (2 tablet), 25 – <35 kg (3 tablet), > 35 kg
(4 tablet)]
9. Sampel dikumpulkan di satu ruangan yang sama dan diberikan obat
oleh tim peneliti
10. Dosis pertama obat anti malaria diberikan sesudah makan makanan
mengandung lemak pada pagi hari. Jika anak muntah dalam 30 menit
setelah pemberian obat, dosis yang sama diberikan kembali. Jika
anak muntah kembali maka anak dieksklusikan dan diberi kinin
selama 7 hari dan doksisiklin diberikan pada anak berusia di atas 8
tahun selama 7 hari
11. Untuk pemberian dosis ke dua artemeter-lumefantrin, tim peneliti
kembali datang untuk mengumpulkan sampel dan memberikan obat 8
sampai 12 jam setelah dosis pertama yang diberikan setelah makan.
Jika sampel tidak datang maka tim peneliti akan mendatangi sampel
12. Antipiretik diberikan pada sampel yang memiliki temperatur aksila >
38.50C untuk memberikan rasa nyaman kepada sampel. Obat yang
diberikan berupa parasetamol dengan dosis 10mg/kgbb/kali.
13. Pemeriksaan fisik dan darah tepi ulangan dilakukan pada hari ke-2, 3,
7,14, 28 dan 42
Alur Penelitian
Populasi terjangkau yang memenuhi kriteria inklusi
Randomisasi Sederhana
Artesunat Amodiakuin Selama 3 hari
1 kali sehari
Artemeter Lumefantrin Selama 3 hari
2 kali sehari
3.9. Identifikasi Variabel
Variabel bebas Skala
Jenis obat Nominal dikotom
Variabel tergantung Skala
Kesembuhan Nominal dikotom
Penurunan jumlah parasit Numerik
Waktu bebas parasit Numerik
Waktu bebas demam Numerik
Kesembuhan
Penurunan jumlah parasit
Waktu bebas parasit
3.10. Definisi Operasional
1. Infeksi Malaria Falsiparum ditetapkan apabila dalam pemeriksaan
apusan darah tepi ditemukan Plasmodium falciparum.14
2. Parasitemia dinilai dengan jumlah parasit per mikroliter darah dengan
menggunakan rumus parasit x 8.000/200.14
3. Malaria falciparum tanpa komplikasi adalah infeksi malaria yang tidak
disertai dengan komplikasi, seperti malaria serebral dengan
kesadaran menurun, anemia berat (hemoglobin ≤ 5 g/dl), dehidrasi,
gangguan asam basa (asidosis metabolik) dan gangguan elektrolit,
hipoglikemia, gagal ginjal, edema paru akut, kegagalan sirkulasi,
kecenderungan terjadinya perdarahan, hiperpireksia, hemoglobinuria,
ikterus dan hiperparasitemia.3,6
4. Efikasi obat antimalaria dinilai dari kesembuhan, penurunan jumlah
parasit, waktu bebas demam dan waktu bebas parasit.6,26,27
5. Kesembuhan dinilai dari Adequate Clinical Parasitological Response
(ACPR) pada hari ke 42 yaitu jika tidak dijumpai Early Therapeutic
Failure (ETF), Late Therapeutic Failure (LTF), dan Parasitological
Failure (PF).6
6. Hari ke 0 adalah hari dimana anak mendapat dosis pertama obat
7. Hari ke 1, 2, 3, 7, 14, 28 dan 42 adalah jumlah hari setelah anak
mendapat dosis pertama obat antimalaria.6
8. Early Therapeutic Failure jika antara hari 1 dan 3 dijumpai malaria
berat atau parasitemia hari ke 2 lebih tinggi dari hari ke 0, ataupun
parasitemia hari ke 3 lebih dari 25% hari ke 0 dan jika pada hari ke 3
dijumpai demam dengan parasitemia.6
9. Late Therapeutic Failure jika ditemukan tanda bahaya atau malaria
berat setelah hari ke 3 disertai dengan parasitemia atau pasien
dengan parasitemia dan demam antara hari ke 3 hingga 28.6
10.Parasitological Failure jika ditemukan parasit pada hari ke 28 pada
apusan darah tepi.6
11. Penurunan jumlah parasit dinilai dari parasitemia sebelum pemberian
obat dengan parasitemia pada hari ke 3.27
12. Waktu bebas demam adalah waktu yang dibutuhkan agar suhu tubuh
kembali normal yang dihitung setelah pemberian obat antimalaria
dosis pertama.26
13. Waktu bebas parasit adalah lamanya parasit tidak dijumpai lagi pada
pemeriksaan darah tepi yang dihitung setelah pemberian obat
antimalaria dosis pertama.26
15. Efek samping adalah tanda, gejala, penyakit yang muncul setelah hari
ke 0 yang diduga akibat obat yang diberikan.13
16. Gejala klinis malaria dapat berupa demam, riwayat demam 48 jam
terakhir, pucat, lemah, nyeri kepala, batuk, muntah dan diare.6
17. Demam apabila dijumpai temperatur aksila > 37,50C.6
18. Pucat dilihat melalui pemeriksaan pada telapak tangan.6
3.11. Analisis dan Penyajian Data
Data yang terkumpul diolah, dianalisis dan disajikan dengan menggunakan
program komputer (SPSS versi 13.0, Microsoft Excell tahun 2003). Interval
kepercayaan yang digunakan adalah 95% dan batas kemaknaan P < 0.05.
Analisis data untuk menilai variabel-variabel kategorikal digunakan uji
kai kuadrat sedangkan untuk mengetahui penurunan jumlah parasit, waktu
bebas demam dan waktu bebas parasit dipakai uji t independen. Penelitian
BAB 4. HASIL
4.1. Populasi terjangkau dan karakteristik subjek
Penelitian dilaksanakan di 10 Sekolah Dasar Negeri Kecamatan Siabu, 2
Sekolah Dasar Negeri Kecamatan Hutabargot, Poliklinik anak RSUD.
Panyabungan, dan Klinik Pusat Penanggulangan Malaria Panyabungan,
Kabupaten Mandailing Natal, Propinsi Sumatera Utara.
Sembilan ratus enam puluh tiga anak diberi informasi tentang penelitian
dan dilakukan penapisan. Empat ratus delapan puluh dua anak menderita
malaria dan direncanakan untuk mendapat terapi. Dua ratus dua orang anak
dikeluarkan dari penelitian oleh karena 2 orang anak menderita malaria
campuran dan 200 anak telah mendapat pengobatan malaria. Sehingga 280
anak diikutsertakan dalam penelitian dan dilakukan randomisasi sederhana, 140
anak diberi terapi dengan artemeter-lumefantrin dan 140 anak diberi terapi
artesunat-amodiakuin (Tabel 4.1).
Pada kelompok artemeter-lumefantrin, 1 orang anak berhenti makan obat
tanpa alasan yang jelas dan 1 orang pindah sehingga tidak dapat diberikan obat.
Alasan pemberhentian makan obat pada anak di kelompok artesunat amodiakuin
karena efek samping pengobatan tersebut, 1 orang anak menderita alergi berupa
ruam kemerahan di seluruh tubuh yang timbul segera setelah pemberian obat
Dari 276 anak yang menyelesaikan pengobatan, hanya 128 orang anak
pada kelompok artemeter-lumefantrin dan 126 orang anak pada kelompok
artesunat-amodiakuin yang menyelesaikan penelitian sampai akhir selama 42
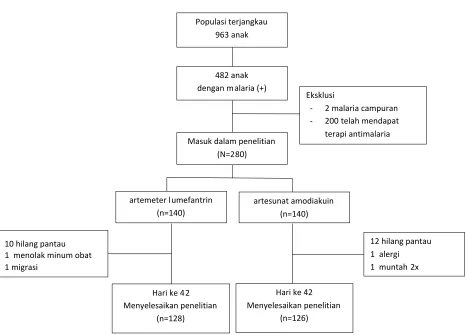
[image:39.612.74.541.225.560.2]hari (Gambar 4.1).
Gambar 4.1. Profil penelitian Tabel 4.1. Karakteristik dasar subjek penelitian
AL ASAQ
Populasi terjangkau 963 anak
482 anak dengan malaria (+)
Masuk dalam penelitian (N=280)
Eksklusi
- 2 malaria campuran - 200 telah mendapat
terapi antimalaria
artemeter lumefantrin (n=140)
artesunat amodiakuin (n=140)
Hari ke 42 Menyelesaikan penelitian
(n=128)
Hari ke 42 Menyelesaikan penelitian
(n=126) 10 hilang pantau
1 menolak minum obat 1 migrasi
Laki-laki 77 (55.0) 63 (45.0) Perempuan 63 (45.0) 77 (55.0) Umur, tahun, mean (SD) 7.89 (1.34) 8 (1.48) Berat badan, kg, mean (SD) 22.3 (4.41) 22.17 (3.91) Tinggi badan, cm, mean (SD) 123.58 (6.84) 124.24 (8.39) Status gizi, n (%)
Gizi baik 60 (42.9) 75 (53.6)
Mild malnutrition 42 (30.0) 36 (25.7)
Moderate malnutrition 7 (5.0) 6 (4.3)
Overweight 31 (22.1) 23 (16.4) Parasitemia, mean (SD) 1071.5 (294.89) 1105.2 (380.86) Keluhan, n (%)
Riwayat demam 48 (34.3) 41 (29.3) Demam 52 (37.1) 37 (26.4) Pucat 44 (31.4) 45 (32.1) Lemah 52 (37.1) 51 (36.4) Sakit kepala 41 (29.3) 24 (17.1) Batuk 20 (14.3) 12 (8.6) Muntah 5 (3.6) 2 (1.4) Mencret 20 (14.3) 22 (15.7) Hepatomegali 15 (10.7) 9 (6.4) Splenomegali 23 (16.4) 17 (12.1)
4.2. Hasil pengobatan
Pada penelitian ini didapatkan ACPR hari ke 42 pada kedua kelompok memiliki
hasil yang tidak berbeda secara signifikan, yaitu kelompok ASAQ 86.4% dan
kelompok AL 90.7% (P=0.260). ETF, LTF dan PF pada kedua kelompok tidak
berbeda bermakna. Perbedaan signifikan tampak pada penilaian waktu bebas
parasit, waktu bebas demam dan penurunan parasit. Dijumpai waktu bebas
parasit yang lebih cepat dan penurunan parasit yang lebih tinggi pada kelompok
Tabel 4.2. Respon pengobatan
Respon pengobatan AL
n = 140
ASAQ
n = 140 P
Waktu bebas parasit hari, mean (SD)
3.2 (1.44) 6.1 (1.87) 0.0001
Waktu bebas demam hari, mean (SD)
1.0 (1.36) 0.7 (1.21) 0.017
ETF, n (%) 2 (1.4) 7 (5.0) 0.090
LTF, n (%) 10 (7.1) 12 (8.6) 0.657
PF, n (%) 1 (0.71) 0 (0) 0.316
ACPR, n (%) 127 (90.7) 121 (86.4) 0.260
Penurunan parasit, %, mean (SD)
95.7 (13.96) 74.8 (21.25) 0.0001
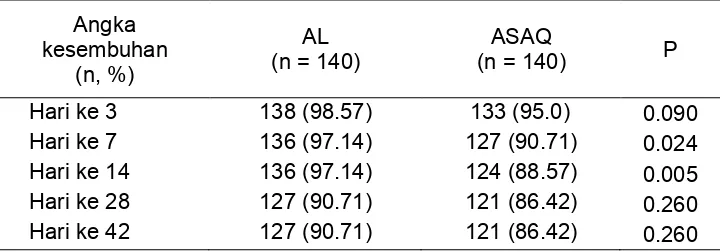
Selama pemantauan, angka kesembuhan pada kedua kelompok tidak didapati
perbedaan yang bermakna pada hari ke 3, 28 dan 42. Namun pada pemantauan hari
ke 7 dan 14, tampak angka kesembuhan yang lebih tinggi pada kelompok AL
dibandingkan kelompok ASAQ (Tabel 4.3).
Tabel 4.3. Perbedaan angka kesembuhan selama pemantauan
Angka kesembuhan
(n, %)
AL (n = 140)
ASAQ
(n = 140) P
Hari ke 3 138 (98.57) 133 (95.0) 0.090
Hari ke 7 136 (97.14) 127 (90.71) 0.024
Hari ke 14 136 (97.14) 124 (88.57) 0.005
Hari ke 28 127 (90.71) 121 (86.42) 0.260
Hari ke 42 127 (90.71) 121 (86.42) 0.260
4.3. Efek Samping Pengobatan
[image:41.612.126.488.458.584.2](3.6%) anak mual, 6 muntah (4.3%), 3 malaise (2.1%) dan 1 pruritus (0.7%). Efek
BAB 5. PEMBAHASAN
Penelitian mengenai obat antimalaria meningkat dalam beberapa tahun terakhir, hal ini
dikarenakan timbulnya resistensi terhadap pengobatan antimalaria dan pengenalan
terhadap regimen pengobatan baru seperti terapi kombinasi artemisinin.33,34 Kabupaten
Mandailing Natal, Propinsi Sumatera Utara telah tercatat memiliki resistensi terhadap
pengobatan klorokuin sebesar 32% pada tahun 2004.35 Tingginya angka resistensi
pada kabupaten ini menjadi salah satu alasan kami melakukan penelitian di sana.
Pilihan pengobatan yang diberikan adalah terapi kombinasi berbasis artemisinin.
Penyakit malaria ditularkan oleh vektor berupa nyamuk Anopheles spp. Di
Indonesia telah dilaporkan terdapat 20 spesies Anopheles yang telah terbukti dapat
menularkan Plasmodium sp. Fluktuasi kepadatan vektor berbeda-beda di setiap
daerah.36 Penelitian kami lakukan di Kecamatan Siabu dan Kecamatan Hutabargot.
Dari sebuah penelitian yang dilakukan di Desa Sihepeng Kecamatan Siabu Kabupaten
Mandailing Natal ditemukan vektor malaria yaitu An. sundaicus, An. kochi dan
An.nigerrimus di persawahan, kolam dan lubang penggalian pasir dengan puncak
kepadatan populasi larva nyamuk pada bulan Desember.37
Gizi kurang dan malaria merupakan dua penyebab utama kematian di
negara-negara berkembang. Namun hubungan antara keduanya masih diperdebatkan. Pada
sebuah penelitian di Etiopia Barat Daya,38 dan Ghana,39 tidak dijumpai adanya
Timur menunjukkan adanya hubungan antara kepadatan parasit dengan status nutrisi
anak sekolah dasar dimana pada penelitian ini didapati dari 8 anak yang memiliki
kepadatan parasit yang tinggi terdapat 7 anak dengan status gizi kurang.41 Pada
penelitian ini, status nutrisi anak terbanyak adalah gizi baik, hal ini mungkin
berhubungan dengan tidak dijumpainya kepadatan parasit yang tinggi pada seluruh
sampel.
Gejala Malaria Falsiparum tanpa komplikasi sangat bervariasi. Demam
merupakan gejala yang sering dikeluhkan.42 Pada tahun penelitian yang dilakukan
terhadap Malaria Falsiparum tanpa komplikasi pada anak didapati keluhan yang sering
berupa demam, pucat dan ikterus.35 Anak yang pucat dan pada pemeriksaan fisis
terdapat splenomegali lebih sering mengalami malaria asimptomatis.39 Hepatomegali
lebih sering terjadi daripada splenomegali pada Malaria Falsiparum akut. Keadaan ini
juga lebih sering pada anak yang lebih muda.43 Splenomegali berhubungan dengan
densitas parasit yang lebih tinggi.44 Penelitian kami mendapatkan gejala yang banyak
dikeluhkan adalah demam, riwayat demam, lemah dan pucat. Beberapa subjek
penelitian juga didapati pembesaran hati dan limpa. Namun pembesaran limpa lebih
banyak kami temukan, hal ini mungkin ada hubungannya dengan keadaan kronis dari
penyakitnya dan usianya yang lebih tua. Splenomegali yang terjadi mungkin
berhubungan dengan densitas parasit yang lebih tinggi daripada densitas parasit pada
anak tanpa splenomegali, namun sayangnya tidak kami nilai pada penelitian ini.
Sub-Sahara Afrika. Efikasi bervariasi antar negara yang diteliti. Hal ini mungkin
berhubungan dengan status penggunaan amodiakuin sebagai monoterapi.45 Resistensi
amodiakuin telah dilaporkan pada beberapa studi yang diperkirakan timbul akibat
struktur dan cara kerjanya yang sangat mirip dengan klorokuin.9,10,46 Resistensi ini
berhubungan dengan polimorfisme gen parasit serta pola geografis dari Plasmodium.47
Pada penelitian yang dilakukan di Kabupaten Mandailing Natal tahun 2006,
didapatkan angka kesembuhan ASAQ mencapai 100% pada hari ke 28.48,49 Penelitian
kami mendapatkan angka kesembuhan ASAQ yaitu 86.4% pada hari ke 28 dan hari ke
42. Penurunan angka kesembuhan ini sangat mungkin berhubungan dengan kondisi
resistensi amodiakuin di daerah tersebut yang mana telah dilaporkan adanya resistensi
terhadap klorokuin yang memiliki struktur yang mirip dengan amodiakuin.9,10,46
Efek samping ASAQ lebih banyak dilaporkan pada kasus dewasa daripada
anak.33 Sebuah penelitian di Kamerun melaporkan efek samping yang sering dijumpai
berupa gejala gastrointestinal dan bronkitis. Sebanyak 13% pasien yang diobati dengan
ASAQ mengalami muntah selama pemberian obat. Pengobatan dihentikan pada 3
orang subjek karena timbulnya efek samping berupa muntah, lemah dan vertigo pada
kelompok yang mendapat ASAQ sekali sehari selama 3 hari. Peneliti
merekomendasikan pembagian ASAQ menjadi dua dosis untuk mengurangi munculnya
efek samping.50
Penelitian kami menggunakan artesunat dengan dosis 4 mg/kgBB/hari dan
muntah berulang dan satu orang anak menderita pruritus sehingga kedua anak tersebut
tidak melanjutkan pengobatan dan diberikan obat lini kedua. Efek samping ASAQ
seperti sakit kepala dan tinitus seperti penelitian yang dilakukan di tahun 2006,51 tidak
kami jumpai.
Gabungan artemeter-lumefantrin merupakan ACT pertama yang tersedia bentuk
fixed-dose.52 Artemeter merupakan derivat artemisinin yang larut dalam lemak.
Lumefantrin merupakan golongan aryl amino alcohol yang baik diabsorpsi bersama
lemak.6 Gabungan kedua obat ini telah dibuktikan memiliki efikasi yang baik diberikan
dalam empat maupun enam regimen.31 Penelitian ini menggunakan AL dalam bentuk
fixed-dose yang diberikan dua kali sehari selama 3 hari berturut-turut setelah memakan
ataupun meminum minuman yang mengandung lemak. Sebuah penelitian di Bangkok,
Thailand yang membandingkan tiga regimen pemberian AL mendapatkan bahwa
pemberian AL dengan enam dosis regimen memiliki efikasi yang tinggi dan keamanan
yang paling baik.53 Pemberian makanan berlemak mempengaruhi efektivitas AL pada
beberapa studi di Ghana.22,54
Efek samping yang dapat muncul pada pengobatan ini adalah gejala
gastrointestinal,52,53 nyeri kepala dan pusing.53 Efek samping yang muncul tidak
berhubungan dengan pemberian obat yang berulang-ulang.52 Pada sebuah penelitian
yang dilakukan pada anak Malaria Falsiparum tanpa komplikasi di Manado, tidak
ditemukan efek samping dalam pemberian enam dosis regimen AL.55 Efek samping AL
yang kami jumpai berupa mual, muntah dan malaise. Penelitian di Uganda,23 dan
Penurunan parasit yang lebih cepat kami dapatkan pada kelompok AL daripada
kelompok ASAQ. Hal ini tidak didukung penelitian sebelumnya yang mendapatkan
bahwa kedua obat ini memiliki waktu penurunan parasit yang cepat dan sudah tidak
dijumpai parasit pada apusan darah tepi hari ketiga.56 Pada kelompok ASAQ, selain
penurunan parasit yang lebih lama kami juga menemukan kegagalan terapi yang lebih
tinggi, namun tidak bermakna secara statistik. Penurunan parasit yang lebih lama telah
dibuktikan berhubungan dengan risiko gagal pengobatan.57
Waktu bebas parasit yang cepat berhubungan dengan waktu bebas demam
yang cepat pula.57 Hal ini bertentangan dengan hasil yang kami jumpai, dimana
kelompok AL memiliki waktu bebas parasit yang lebih cepat namun memiliki waktu
bebas demam yang lebih lama. Sebaliknya, pada kelompok ASAQ memiliki waktu
bebas parasit yang lebih lama namun memiliki waktu bebas demam yang lebih cepat.
Keadaan ini mungkin berhubungan dengan efek samping AL yaitu demam,31,52 namun
kami tidak dapat membuktikan apakah lamanya waktu bebas demam akibat efek
samping dari obat AL. Terdapat dua penelitian yang menyatakan bahwa penggunaan
antipiretik dapat memperlama waktu bebas parasit, walaupun berdasarkan metode
penelitian tersebut sulit ditarik kesimpulan yang dapat dipertanggungjawabkan.58 Pada
penelitian ini terdapat beberapa anak pada masing-masing kelompok yang mendapat
terapi antipiretik karena keluhan demam, namun tidak kami menilai hubungan
penggunaan terapi ini terhadap lamanya waktu bebas parasit.
kejadian efek samping pada kedua kelompok tidak berbeda, namun pada kelompok AL
memiliki penurunan parasit yang lebih besar dan waktu bebas parasit yang lebih cepat
dibandingkan kelompok ASAQ. Pada penelitian ini kami dapatkan efikasi AL lebih baik
dengan ASAQ dalam mengobati anak Malaria Falsiparum tanpa komplikasi. Hal ini
sesuai dengan hasil penelitian di Tanzania,59dan Kamerun.60
Tujuan terapi kombinasi obat antimalaria adalah untuk memperlambat timbulnya
resistensi dengan menggunakan dua jenis obat blood schizontocidal atau lebih yang
memiliki kerja yang berbeda dengan target biokimiawi parasit yang berbeda pula.6
Artemisinin dan derivatnya memiliki efek gametosidal.6,56 Keterbatasan dari penelitian
ini adalah tidak dilakukannya perhitungan terhadap parasit seksual sehingga tidak
BAB 6. KESIMPULAN DAN SARAN
6.1. KESIMPULAN
Gabungan artemeter-lumefantrin memiliki efikasi yang lebih tinggi daripada gabungan
artesunat-amodiakuin untuk pengobatan anak dengan Malaria Falsiparum tanpa
komplikasi. Penelitian ini juga mendapatkan bahwa kedua gabungan obat ini aman
digunakan pada anak.
6.2. SARAN
Diharapkan kepada pemerintah Kabupaten Mandailing Natal khususnya Dinas
Kesehatan untuk mempertimbangkan penggunaan obat alternatif selain kombinasi
artesunat-amodiakuin untuk pengobatan Malaria Falsiparum pada anak.
Sosialisasi mengenai resistensi pengobatan yang dapat timbul bila hanya
mengkonsumsi satu jenis obat saja sebaiknya rutin dilakukan. Skrining penyakit malaria
dan pengobatan ke sekolah-sekolah di akhir tahun sebaiknya dilakukan mengingat
kepadatan vektor yang tinggi di waktu tersebut. Agar proses pendidikan dapat berjalan
dengan baik dan untuk mengoptimalisasi perkembangan anak diharapkan kerjasama
DAFTAR PUSTAKA
1. Daly JP. Malaria. Dalam: Gershon AA, Hotez PJ, Katz SL, penyunting. Krugman’s infectious diseases of children. Edisi ke-11. Philadelphia: Mosby;2004.h.337-51 2. Greenwood BM, Bojang K, Whitty CJ, Targett GA. Malaria. Lancet.2005;
365:1487-98
3. Direktorat Jenderal Pengendalian Penyakit dan Penyehatan Lingkungan. Pedoman tatalaksana kasus malaria di Indonesia. Jakarta: Departemen Kesehatan RI; 2005 4. World Health Organization. Malaria in SEAR countries. Diunduh dari :
http://www.searo.who.int/en/Section10/Section21/Section340_4022.htm. Diakses April 2010
5. Taylor TE, Strickland GT. Malaria. Dalam: Strickland GT, penyunting. Hunter’s tropical medicine and emerging infectious diseases. Edisi ke-8. Philadelphia: Saunders; 2000.h.614-41
6. World Health Organization. Guidelines for the treatment of malaria.Switzerland: World Health Organization; 2006
7. Hastings IM, Korenromp EL, Bloland PB. The anatomy of a malaria disaster: drug policy choice and mortality in african children. Lancet Infect Dis. 2007;7:739-48
8. Pasaribu S, Pasaribu AP, Lubis CP. Combination of artesunate-amodiaquine as a treatment for uncomplicated falciparum malaria in children. Pediatrics. 2008;121:S133
9. Marfurt J, Mueller I, Sie A, Maku P, Goroti M, Reeder JC, dkk. Low efficacy of amodiaquine or chloroquine plus sulfadoxine-pyrimethamine against plasmodium falciparum and P. vivax malaria in Papua New Guinea. Am J Trop Med Hyg. 2007;77(5):947-54
10. Mutabingwa TK, Anthony D, Heller A, Hallet R, Ahmed J, Drakeley C, dkk.
Amodiaquine alone, amodiaquine+sulfadoxine pyrimethamine,
amodiaquine+artesunate, and artemether-lumefantrine for outpatient treatment of malaria in Tanzanian children: a four-arm randomized effectiveness trial. Lancet. 2005;365:1474-80
11. Adjei GO, Goka BQ, Rodrigues OP, Hoegberg LCG, Alifrangis M, Kurtzhals AL. Amodiaquine associated adverse effects after inadvertent overdose and after a standard therapeutic dose. Ghana Med J. 2009;43:135-8
12. Guthman JP, Cohuet S, Rigutto C, Fortes F, Saraiva N, Kiguli J, dkk. Short report: high efficacy of two arteminin-based combinations (artesunate+amodiaquine and artemether-lumefantrine) in Caala, Central Angola. Am J Trop Med Hyg. 2006;75:143-5
malaria in Papua, Indonesia: an open-label randomised comparison. Lancet.2007; 369: 757–65
15. Krogstad DJ. Plasmodium species (malaria). Dalam: Mandell GL, Bennet JE, Raphael D, penyunting. Mandell, Douglas, and Bennett’s principles and practice of infectious diseases. Philadephia: Churcill Livingstone; 2000.h.2817-31
16. Singh B, Sung LK, Metusop A, Radhakrishnan A, Shamsul SS, Singh JC, dkk. A large focus of naturally acquired Plasmodium knowlesi infections in human beings. Lancet. 2004; 363: 1017-24
17. Ng OT, Eong OE, Chuan LC, Jarrod LP, Ching NL, Wong PS, dkk. Naturally acquired human Plasmodium knowlesi infection, Singapore. Emerg Infect Dis; 2008: 1-7
18. Soedarmo SS, Garna H, Hadinegoro SR, Satari HI. Malaria. Dalam: Buku ajar infeksi dan pediatrik tropis. Edisi ke-2. Jakarta: IDAI;2008.h.408-37
19. Lema OE, Carter JY, Nagelkerke N, Wangal MW, Kitenge P, Gikunda SM, dkk. Comparison of five methods of malaria detection in the outpatient setting. Am J Trop Med Hyg; 1999: 177-82
20. Susanto I, Pribadi W. Parasit malaria. Dalam: Susanto I, Ismid IS, Sjarifuddin PK, Sungkar S, penyunting. Buku ajar parasitologi kedokteran. Jakarta: Balai Penerbit FKUI; 2008. h. 189-221
21. World Health Organization. Antimalarial combination drug therapy. Report of a WHO technical consultation. Geneva: WHO; 2001
22. Kobbe R, Klein P, Adjei S, Amemasor S, Thompson WN, Heidemann H, dkk. A randomized trial on effectiveness of artemether-lumefantrine versus artesunate plus amodiaquine for unsupervised treatment of uncomplicated plasmodium falciparum malaria in Ghanaian children. Malar J. 2008: 7: 261
23. Maiteki-Sebuguzi C, Jagannathan P, Yau VM, Clark TD, Njama-Meya D, Nzarubara B, dkk. Safety and tolerability of combination antimalarial therapies for uncomplicated falciparum malaria in Ugandan children. Malar J. 2008;7:106
24. Krishna S, Uhlemann AC, Haynes RK. Artemisinins: mechanisms of action and potential for resistance. Drug Resist Updates.2004;7:233-44
25. Newton P, Suputtamongkol Y, Isavadharm PT, Pukrittayakamee S, Navaratnam V, Bates I, dkk. Antimalarial bioavaibility and disposition of artesunate in acute falciparum malaria. Antimicrob Agents Chemother; 2000: 972-7
26. Adjuik M, Agnamey P, Babiker A, Borrman S, Brasseur P, Cisse M, dkk. Amodiaquine-artesunate versus amodiaquine for uncomplicated Plasmodium falciparum malaria in African children: a randomized, multicentre trial. Lancet. 2002; 359: 1365-72
27. Martensson A, Stromberg J, Sisowath C, Msellem MI, Gil P, Montgomery SM, dkk. Efficacy of artesunate plus amodiaquine versus that of artemether-lumefantrine for the treatment of uncomplicated childhood Plasmodium falciparum malaria in Zanzibar,Tanzania. Clin Inf Dis.2005;41:1079-86
29. Makanga M, Krudsood S. The clinical efficacy of artemether/lumefantrine (coartem). Malaria J. 2009;8 (Supp I):S5-9
30. Djimde A, Lefevre G. Understanding the pharmacokinetics of coartem. Malar J; 2009: S1-4
31. Faye B, Ndiaye JL, Ndiaye D, Dieng Y, Faye O, Gaye O. Efficacy and tolerability of four antimalarial combinations in the treatment of uncomplicated Plasmodium falciparummalaria in Senegal. Malar J. 2007;6:80-8
32. Madiyono B, Moechlisan S, Sastroasmoro S, Budiman I, Purwanto SH. Perkiraan besar sampel. Dalam: Sastroasmoro S, Ismail S, penyunting. Dasar-dasar metodologi penelitian klinis. Edisi ke-3. Jakarta: Sagung Seto;2008.h.302-30
33. Adjei GO, Kudzi W, Dodoo A, Kurtzhals JAL. Artesunate plus amodiaquine combination therapy: reviewing the evidence. Drug Dev Res. 2010;71:33-43
34. World Health Organization. Assessment and monitoring of antimalarial drug efficacy for the treatment of uncomplicated falciparum malaria. Geneva: WHO; 2003
35. Azlin E, Batubara I, Dalimunthe W, Siregar C, Lubis B, Lubis M, dkk. The effectiveness of chloroquine compared to fansidar in treating falciparum malaria. Pediatr Indones.2004; 44: 17-20
36. Munif A, Imron M. Panduan pengamatan nyamuk vektor malaria. Jakarta: Sagung Seto; 2010
37. Marsaulina I. Tempat perkembangbiakan anopheles sundaicus di desa Sihepeng, kecamatan Siabu, Kabupaten Mandailing Natal, Propinsi Sumatera Utara. Info Kesehatan Masyarakat. 2008;12(2):119-23
38. Deribew A, Alemseged F, Tessema F, Sena L, Birhanu Z, Zeynudin A, dkk. Malaria and under-nutrition: a community based study among under-five children at risk of malaria, South-West Ethiopia. PLoS ONE.2010;5(5):e10775
39. Crookston BT, Alder SC, Boakye I, Merill RM, Amuasi JH, Porucznik CA, dkk. Exploring the relationship between chronic undernutrition and asymptomatic malaria in Ghanaian children. Malar J. 2010;9:39
40. Nyakeriga AM, Troye-Blomberg M, Chemtai AK, Marsh K, Williams TN. Malaria and nutritional status in children living on the coast of Kenya. Am J Clin Nutr. 2004;80:1604-10
41. Nurjaya IO. Status gizi dan kepadatan penyakit malaria pada anak usia sekolah dasar di daerah endemis malaria.[tesis].Semarang:Program Pendidikan Dokter Spesialis I Ilmu Kesehatan Anak FKUNDIP, 2004
42. Grobusch MP, Kremsner PG. Uncomplicated malaria. CTMI.2005;295:83-104
43. Sowunmy A. Hepatomegaly in acute falciparum malaria in children. Trans R Soc Trop Med Hyg.1996;90(5):540-2
44. Pasaribu S, Lubis CP. The correlation between parasitemia and spleen size in children with falciparum malaria.e-USU Repository.2004 [diakses bulan Oktober 2011]. Diunduh dari:http://library.usu.ac.id/download/fk/anak-chairuddin20.pdf
sub-46. Nawaz F, Nsobya SL, Kiggundu M, Joloba M, Rosenthal PJ. Selection of parasites with diminished drug sensitivity by amodiaquine-containing antimalarial regimens in Uganda. J Infect Dis. 2009;200(11):1650-7
47. Sa JM, Twu O, Hayton K, Reyes S, Fay MP, Ringwald P, dkk. Geographic patterns of plasmodium falciparum drug resistance distinguished by differential responses to amodiaquine and chloroquine. Proc Natl Acad Sci USA. 2009;106(45):18883-9
48. Pasaribu AP, Yuliati E, Lubis M, Pasaribu S, Lubis CP. Efficacy of artesunate-amodiaquine and quinine-azithromycin combination in treatment of uncomplicated falciparum malaria in children. Majalah Kedokteran Nusantara. 2008;41(4):228-34 49. Fitri P, Armila, Lubis M, Pasaribu S, Lubis CP. Comparison of the efficacy of
artesunate-amodiaquine with quinine-clindamycin for treatment of uncomplicated falciparum malaria in children. Paediatr Indones. 2009;49(2):91-6
50. Ndiaye JL, Randrianarivelojosia M, Sagara I, Brasseur P, Ndiaye I, Faye B, dkk. Randomized, multicentre assessment of the efficacy and safety of ASAQ – a fixed-dose artesunate-amodiaquine combination therapy in the treatment of uncomplicated Plasmodium falciparum malaria. Malar J.2009:8;125
51. Silvana S. Efikasi monoterapi artesunate dengan gabungan artesunate-amodiakuin pada pengobatan malaria falsiparum tanpa komplikasi pada anak.[tesis]. Medan: Program Magister Kedokteran Klinik-Spesialis Ilmu Kesehatan Anak FKUSU, 2008 52. Falade C, Manyando C. Safety profile of coartem: the evidence base. Malar J.
2009;8:1-6
53. Ezzet F, Vugt MV, Nosten F, Looareesuwan S, White NJ. Pharmacokinetics and pharmacodynamics of lumefantrine (benflumetol) in acute falciparum. Antimicrob Agents Microbs. 2000;44(3):697-704
54. Owusu-Agyei S, Asante KP, Owusu R, Adjuik M, Amenga-Etego S, Dosoo DK, dkk.
An open label, randomized trial of artesunate+amodiaquine,
artesunate+chlorproguanil-dapsone and artemether-lumefantrine for the treatment of uncomplicated malaria. PLoS ONE. 2008;3(6): e2530-7
55. Rachmawati, Rampengan NH, Tatura SNN, Rampengan TH. Comparison of the efficacy of artemether-lumefantrine vs artesunate plus sulfadoxine-pyrimethamine in children with uncomplicated falciparum malaria. Paediatr Indones. 2010;50(2):113-7 56. Michael OS, Gbotosho GO, Folarin OA, Okuboyejo T, Sowunmi A, Oduola AM, dkk.
Early variations in plasmodium falciparum dynamics in Nigerian children after treatment with two artemisinin-based combinations: implications on delayed parasite clearance. Malar J.2010; 9: 335-43
57. Sowunmi A, Adewoye EO, Gbotsho GO, Happi CT, Sijuade A, dkk. Factors contributing to delay in parasite clearence in uncomplicated falciparum malaria in children. Malar J. 2010;9:53-64
58. Meremikwu MM, Logan K, Garner P. Antipyretic measures for treating fever in malaria (review). Cochrane Database Syst Rev. 2009;1:1-15
44
LAMPIRAN
1. Personil Penelitian
1. Ketua Penelitian
Nama : dr. Tri Faranita
Jabatan : Peserta PPDS Ilmu Kesehatan Anak
FK-USU/RSHAM
2. Anggota Penelitian
1. Prof. DR. dr. H. Syahril Pasaribu,DTM&H, MSc (CTM), SpA(K)
2. Prof. dr. H. Munar Lubis, SpA(K)
3. dr. Muhammad Ali, SpA(K)
4. dr. Ayodhia Pitaloka, M.Ked(Ped), SpA
5. dr. Erika Panjaitan
6. dr. Mahrani Lubis
7. dr. Washli Zakiah
9. dr. Fadli Syahputra
45
2. Biaya Penelitian
1. Obat - obat
Artemether Lumefantrin Rp. 10.500.000
Artesunat Amodiakuin Rp. 2.800.000
Lain-lain Rp. 500.000
2. Perlengkapan Rp. 3.000.000
3. Akomodasi dan Transportasi Rp. 5.000.000
4. Konsumsi Rp. 2.000.000
5. Penyusunan dan Penggandaan Hasil Rp. 1.000.000 6. Seminar Hasil Penelitian Rp. 1.500.000
Jumlah Rp 26.300.000
3. Jadwal Penelitian
46
4. Penjelasan dan Persetujuan Kepada Orang Tua
LEMBAR PENJELASAN KEPADA ORANG TUA SUBYEK
Yth. Bapak / Ibu ……….
Sebelumnya kami ingin memperkenalkan diri (dengan menunjukkan surat tugas dari Departemen Ilmu Kesehatan Anak FK USU). Nama saya dokter Tri Faranita, dari Departemen Ilmu Kesehatan Anak FK USU / RSUP H. Adam Malik Medan. Saat ini, kami sedang melaksanakan penelitian tentang efek pengobatan malaria pada anak yang menderita malaria.
Malaria adalah penyakit infeksi yang ditularkan melalui nyamuk Anopheles. Malaria seringkali diawali oleh demam, menggigil, berkeringat, pucat dan gejala lainnya. Malaria sering diderita oleh penduduk di daerah endemis malaria seperti daerah Bapak/Ibu. Anak-anak juga dapat terjangkit malaria seperti orang dewasa, namun gejala yang ditimbulkan biasanya lebih berat dan sering menyebabkan ketidakhadiran anak di sekolah, serta mengganggu kegiatan dan perilaku anak di rumah sehari-hari.
Bapak/Ibu, untuk mengetahui anak Bapak/Ibu menderita malaria kami memerlukan pemeriksaan darah dari ujung jari. Jika berdasarkan hasil pemeriksaan kami, anak Bapak / Ibu mengalami malaria, kami berencana untuk mengobati anak Bapak / Ibu dengan memberikan obat yang dapat memusnahkan parasit malaria di dalam tubuhnya, sehingga kita harapkan anak Bapak/Ibu dapat melakukan kegiatan di sekolah dan di rumah dengan baik tanpa ada gangguan akibat malaria. Obat yang akan kami berikan adalah artemeter-lumefantrin atau gabungan artesunat amodiakuin. Setelah itu kami akan kembali memeriksa darah dari anak Bapak / Ibu pada hari ke 2,3,7,14,28 dan 42 untuk melihat efek obat tersebut terhadap malaria.
47
Kerjasama bapak/ibu sangat diharapkan dalam penelitian ini. Bila masih ada hal-hal yang belum jelas menyangkut penelitian ini, setiap saat dapat ditanyakan kepada peneliti : dr. Tri Faranita.
Setelah memahami berbagai hal yang menyangkut penelitian ini, diharapkan bapak/ibu bersedia mengisi lembar persetujuan turut serta terhadap anak bapak/ibu dalam penelitian yang telah disiapkan.
Demikian yang dapat kami sampaikan. Atas perhatian Bapak / Ibu, kami ucapkan terima kasih.
Medan, Oktober 2010