PERLEMAKAN HATI NON ALKOHOLIK
MELATI SILVANI NASUTION
DEPARTEMEN ILMU PENYAKIT DALAM
FAKULTAS KEDOKTERAN UNIVERSITAS SUMATERA UTARA
RSUP H. ADAM MALIK
DAFTAR ISI
I. PENDAHULUAN ... 1
II. Definisi ... 1
III Epidemiologi ... 2
IV Patogenesis ... 2
V Manifestasi Klinik ... 5
VI Diagnosis ... 5
VII Penatalaksanaan ... 13
VIII Kesimpulan ... 17
PERLEMAKAN HATI NON ALKOHOLIK
Melati Silvanni Nst, IlhamdI. PENDAHULUAN
Hubungan antara steatosis, inflamasi dan sirosis dengan obesitas dan diabetes
sudah diketahui sejak tahun 1958. Steatohepatitis pada pasien-pasien non alkoholik
pertama kali disampaikan oleh Peter dkk pada tahun 1975 pada kelompok obesitas
yang menjalani operasi bypass jejunoileal
Perlemakan hati non alkoholik merupakan kondisi yang makin disadari dapat
berkembang menjadi penyakit hati lanjut. Spektrum penyakit perlemakan ini mulai
dari perlemakan hati sederhana (simple steatosis) sampai pada steatohepatitis non
alkoholik (nonalcoholic steatohepatitis = NASH), fibrosis dan sirosis hati.
Steatohepatitis non alkoholik muncul setelah Ludwig dkk (1980) melaporkan
sekelompok pasien yang dapat dikatakan tidak mengkonsumsi alkohol tapi
memperlihatkan gambaran biopsi hati yang sulit dibedakan dengan hepatitis akibat
alkohol.
1
2
II. DEFINISI
Sampai saat ini masih terdapat beberapa ketidaksepahaman dalam terminologi
penyakit perlemakan hati, misalnya mengenai pemilihan istilah perlemakan hati non
alkoholik (nonalcoholic fatty liver = NAFL) atau penyakit perlemakan hati non
alkoholik (nonalcoholic fatty liver disease = NAFLD). Pada umumnya disepakati
bahwa steatohepatitis non alkoholik (nonalcoholic steatohepatitis = NASH)
merupakan perlemakan hati pada tingkat yang lebih berat
Dikatakan sebagai perlemakan hati apabila kandungan lemak di hati (sebagian
besar terdiri atas trigliserida) melebihi 5% dari seluruh berat hati. Karena pengukuran
berat hati sangat sulit dan tidak praktis, diagnosis dibuat berdasarkan analisis
spesimen biopsi jaringan hati, yaitu ditemukannya minimal 5-10% sel lemak dari
keseluruhan hepatosit
2
Kriteria lain yang juga sangat penting adalah pengertian non alkoholik. Batas
untuk menyatakan seseorang minum alkohol yang tidak bermakna sempat menjadi
perdebatan, tetapi lebih banyak ahli yang menyepakati bahwa konsumsi alkohol
sampai 20 gram per hari masih bisa digolongkan sebagai non alkoholik
2
III. EPIDEMIOLOGI
Prevalensi perlemakan hati non alkoholik berkisar antara 15-20% pada
populasi dewasa di Amerika Serikat, Jepang dan Italia. Diperkirakan 20-30%
diantaranya berada dalam fase yang lebih berat (steatohepatitis non alkoholik). Di
Indonesia penelitian mengenai perlemakan hati non alkoholik masih belum banyak.
Lesmana melaporkan 17 pasien steatohepatitis non alkoholik, rata-rata berumur 42
tahun dengan 29% gambaran histologi hati menunjukkan steatohepatitis disertai
fibrosis. Sebuah studi populasi dengan sampel cukup besar oleh Hasan dkk
mendapatkan prevalensi perlemakan hati non alkoholik sebesar 30,6%.
Beberapa karakteristik klinis berhubungan dengan steatohepatitis non
alkoholik, termasuk diabetes mellitus, hiperlipidemia, hipertensi dan obesitas. Semua
penyakit ini berhubungan dengan keadaan resistensi insulin. Perlemakan hati non
alkoholik telah ditunjukkan dari beberapa studi berhubungan dengan resistensi
insulin. Obesitas ditemukan pada 40%-100% pasien perlemakan hati non alkoholik
dengan diabetes dan hiperlipidemia terjadi pada 21-75% dan 21-83%.
2
Perlemakan hati non alkoholik dapat terjadi pada semua usia termasuk
anak-anak, walaupun penyakit ini dikatakan paling banyak pada dekade keempat dan
kelima kehidupan. Jenis kelamin yang dominan berbeda-beda dalam berbagai
penelitian, namun umumnya menunjukkan adanya predileksi perempuan.
1
2
IV. PATOGENESIS
Patogenesis perlemakan hati non alkoholik masih belum jelas. Dua kondisi
yang paling sering berhubungan dengan peningkatan suplai asam lemak ke hati serta
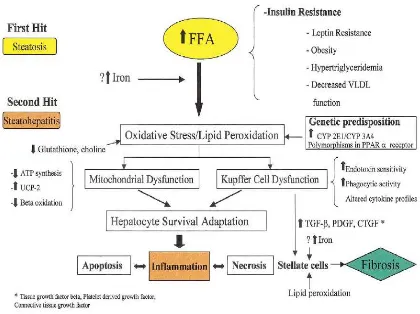
resistensi insulin. Hipotesis yang sampai saat ini banyak diterima adalah the two hit
Gambar 1. Patogenesis Perlemakan Hati Non Alkoholik 1
First Hit
Steatohepatitis terjadi jika homeostasis lemak tidak seimbang. Normalnya,
trigliserida, komponen utama lemak pada hati berasal dari esterifikasi asam lemak
bebas yang berakumulasi di hati. Akumulasi asam lemak bebas ini melalui dua jalur.
Asam lemak bebas dihantarkan ke hati dengan albumin melalui absorpsi GUT atau
lipolisis jaringan adiposa atau disintesa di hati melalui lipogenesis. Asam lemak yang
berakumulasi di hati dapat juga terjadi oksidasi di dalam mitokondria hepatosit,
peroksisom atau mikrosom, atau diesterifikasi menjadi trigliserida. Trigliserida lalu
disekresi menjadi VLDL melalui eksositosis. Homeostasis metabolisme lemak dapat
terganggu dengan peningkatan hantaran asam lemak bebas ke hati, peningkatan
sintesis asam lemak di hati, penurunan β oksidase asam lemak di hati dan/atau
penurunan sintesis atau sekresi VLDL
1,2,3
Perubahan pada sinyal insulin (kemampuan adiposit dalam merespon
perubahan kadar glukosa) dan metabolisme lemak sepertinya menyebabkan terjadinya
steatosis. Seperti yang dijelaskan sebelumnya, resistensi insulin telah ditunjukkan
berhubungan dengan diabetes melitus, peningkatan sirkulasi insulin menyebabkan
peningkatan lipolisis dengan peningkatan hantaran asam lemak bebas ke hati. Di
dalam hepatosit asam lemak disintesis dan oksidasi asam lemak dihambat.
Peningkatan kadar insulin dapat meningkatkan degradasi apolipoprotein B100,
suatu komponen VLDL, sehingga menyebabkan ketidakmampuan trigliserida untuk
dihantarkan ke luar hati.
Secara klinis telah diperlihatkan adanya hubungan antara steatosis dan
peningkatan sirkulasi insulin. Pasien-pasien dengan paparan lokal terhadap insulin
memperlihatkan adanya steatosis hati fokal. Parenkim hati yang mengalami metastase
insulinoma juga dapat berkembang menjadi steatosis hati yang berlanjut.
Leptin, yang dihasilkan oleh adiposit merupakan hormon pengatur yang
memerankan peranan yang penting dalam berkembangnya steatosis hati. Hormon ini
diduga menyebabkan terjadinya resistensi insulin dan mengubah sinyal insulin pada
hepatosit yang menyebabkan peningkatan produksi asam lemak hepatoseluler.
Peningkatan kadar leptin dijumpai pada pasien dengan perlemakan hati non alkoholik
terutama pada pasien dengan BMI yang tinggi.
Second Hit
Faktor-faktor yang menyebabkan inflamasi hepatosit, degenerasi balloning,
nekrosis dan fibrosis masih diteliti. Namun data yang sekarang menduga bahwa
perjalanan penyakit terjadi pada tingkat hepatosit yang menyebabkan beberapa pasien
dengan steatosis berkembang menjadi perlemakan hati non alkoholik. Bagaimana
perjalanan dan peran dari faktor-faktor ini masih dalam penelitian.
1,2,3
Stres oksidatif dipikirkan sebagai salah satu pendorong katalisator dibalik
perkembangan steatosis menjadi perlemakan hati non alkoholik. Stres oksidatif terjadi
oleh berbagai sebab. Asam lemak bebas yang telah berakumulasi didalam hepatosit
mengalami oksidasi melalui mitokondria, mikrosom dan peroksisom, menyebabkan
Reactive Oxygen Species. Peningkatan asam lemak bebas juga merangsang
peningkatan regulasi CYP2E1, sebuah enzim yang bekerja sebagai katalis untuk
peroksidasi lemak. Jalur sitokrom p450 lainnya, seperti CYP3A4 telah juga telah
diimplikasikan sebagai sumber peroksidasi lemak juga. Stres oksidatif yang kronis
menyebabkan deplesi sumber antioksidan alami (glutation) dan menyebabkan
pengeluaran zat oksidatif reaktif di dalam hepatosit. Pengeluaran zat besi juga dapat
Keluarnya zat oksidatif reaktif menyebabkan pengeluaran tumor necrosis
factor (TNF)-α, sitokin proinflamasi, melalui hepatosit, sel kupffer dan jaringan
adiposa. Peningkatan regulasi TNF- α mengaktivasi redox-sensitive kinase spesifik
seperti IKK-β dimana meningkatkan regulasi jalur proinflamasi begitu juga resistensi
insulin
Sanyal dkk telah menunujukkan bahwa adanya stres oksidatif dan
abnormalitas struktur mitokondria pada pasien-pasien dengan perlemakan hati non
alkoholik dibandingkan dengan perlemakan hati sederhana.
Sel kupffer biasanya mengeluarkan sitokin yang memodulasi aktivitas TNF-α
seperti interferon-γ, IL-10 dan IL-12 begitu juga prostaglandin E2, superoksida dan
peroksida hidrogen. Interferon-γ dan IL-6 merupakan sitokin proinflamasi dan IL-10
merupakan sitokin anti inflamasi. Obesitas menyebabkan gangguan pada fungsi sel
kupffer seperti yang ditunjukkan oleh Yang dkk.
V. MANIFESTASI KLINIS
Mayoritas pasien-pasien dengan perlemakan hati non alkoholik asimptomatik.
Beberapa pasien akan mengeluhkan lemah seluruh tubuh, letargi, atau nyeri
epigastrium atau perut kanan atas. Satu studi memperlihatkan bahwa gejala-gejala ini
terjadi pada 30% pasien pada saat diagnosa ditegakkan.
Pada pemeriksaan fisik hepatomegali dijumpai pada sekitar 25% pasien,
walaupun masih diduga akibat habitus tubuh. Tanda klinis penyakit hati yang khas
seperti ginekomasti, spider navy, caput medusa dan penurunan massa otot perifer
tidak dijumpai.
1,2
1,2
IV. DIAGNOSIS
Biopsi hati merupakan baku emas pemeriksaan penunjang untuk menegakkan
diagnosis dan sejauh ini masih menjadi satu-satunya metode untuk membedakan
perlemakan hati non alkoholik dengan perlemakan tanpa atau disertai inflamasi.
Masih menjadi perdebatan apakah biopsi hati perlu dilakukan sebagai pemeriksaan
rutin dalam proses penegakan diagnosis perlemakan hati non alkoholik. Sebagian ahli
menyingkirkan etiologi penyakit hati lain, membedakan steatosis dari steatohepatitis,
memperkirakan prognosis dan menilai progresi fibrosis dari waktu ke waktu. Alasan
dari kelompok yang menentang biopsi hati antara lain prognosis yang umumnya baik,
belum tersedianya terapi yang benar-benar efektif dan resiko serta biaya dari biopsi
itu sendiri.4,5
Tabel 1. Diagnosa Perlemakan Hati Non Alkoholik5
1. Laboratorium
Pemeriksaan laboratorium serum yang digunakan sebagai pemeriksaan non invasif
yang dapat membedakan perlemakan hati non alkoholik dengan perlemakan hati telah
banyak diteliti. Satu atau beberapa pemeriksaan laboratorium yang dapat secara akurat
mengidentifikasi stadium dan tingkatan perlemakan hati non alkoholik dapat
menyaring populasi pasien dengan NAFLD dan menghindari pemeriksaan invasif
Tabel 2. Biomarker non invasif perlemakan hati non alkoholik1
Peningkatan ringan sampai sedang kadar transaminase merupakan kelainan
hasil pemeriksaan laboratorium yang paling sering didapatkan pada pasien-pasien
dengan perlemakan hati non alkoholik. Beberapa pasien datang dengan enzim hati
yang normal sama sekali. Kenaikan enzim hati biasanya tidak melebihi empat kali
dengan rasio AST : ALT kurang dari satu, tetapi pada fibrosis lanjut rasio ini dapat
mendekati atau bahkan melebihi satu. Perlu menjadi perhatian beberapa studi yang
melaporkan bahwa kadar AST dan ALT tidak memiliki korelasi dengan aktivitas
histologis, bahkan kadar enzim dapat tetap normal pada penyakit hati yang sudah
lanjut. Pemeriksaan laboratorium lain seperti alkali posfatase, GGT, feritin darah atau
saturasi transferin juga dapat meningkat sedangkan hipoalbuminemia, waktu
protrombin yang memanjang dan hiperbilirubinemia biasanya ditemukan pada pasien
yang sudah menjadi sirosis.2,5
Stres oksidatif diduga sebagai penyebab utama dalam patogenesis penyakit
hati non alkoholik sehingga pemeriksaan laboratorium yang mengukur stres oksidatif
menggunakan Reactive Oxygen Species (ROS) merupakan pemeriksaan yang sangat
potensial dalam kasus perlemakan hati non alkoholik. Pemeriksaan lain yang dapat
digunakan adalah pemeriksaan yang mengukur kadar adipositokin (dihasilkan oleh
jaringan adiposa) seperti leptin dan adiponektin (ADP). Obesitas dan ambilan
pengantaran asam lemak bebas menuju hati, yang berhubungan dengan steatosis hati.
Pemeriksaan awal menunjukkan hunbungan antara kadar leptin yang tinggi dan
timbulnya perlemakan hati non alkoholik dan tingkatan steatosis walaupun tidak
dijumpai inflamasi atau fibrosis. Namun, beberapa studi telah gagal menunjukkan
adanya hubungan antara kadar leptin dengan ada atau tidaknya steatosis hati,
inflamasi atau fibrosis.
Bertolak belakang dengan leptin, ADP diduga meningkatkan sensitivitas
terhadap insulin dan peningkatan penggunaan glukosa dan oksidasi asam lemak bebas
di hati. Hui dkk menemukan kadar ADP serum yang rendah pada pasien NAFLD
ketika dibandingkan dengan kontrol normal dan individu dengan perlemakan hati.
Targher dkk baru-baru ini menunjukkan kadar ADP berhubungan dengan beratnya
gambaran histologi hati termasuk steatosis, nekroinflamasi dan fibrosis. Walaupun
ketiga komponen gambaran histologi hati tadi berhubungan dengan kadar ADP, hanya
steatosis dan nekroinflamasi yang ditemukan sebagai faktor independen pada analisis
multivariat. Studi yang lebih lanjut diperlukan untuk menggambarkan hubungan
antara ADP dan beratnya penyakit hati pada pasien dengan NAFLD.
5,6
Penanda inflamasi sistemik seperti C-reactive Protein (CRP) juga telah
ditunjukkan berguna. Satu studi di Australia menunjukkan tidak ada perbedaan antara
tingginya kadar CRP pada pasien dengan perlemakan hati dan perlemakan hati non
alkoholik. Hal ini berbeda dengan studi lainnya yang menunjukkan adanya
peningkatan kadar CRP yang signifikan pada pasien perlemakan hati non alkoholik
dan NAFLD.
5
Apoptosis hati merupakan gambaran yang mencolok pada perlemakan hati non
alkoholik dan sepertinya hal ini merupakan pemeriksaan yang cukup potensial dalam
mendeteksi perlemakan hati non alkoholik. Wieckowska dkk menunjukkan hubungan
yang rendah antara kadar cascape-generated cytokeratin-18 plasma, sebuah protein
yang berhubungan dengan akhir apoptosis dan muncul pada pemeriksaan histologi
pada biopsi hati pasien dengan perlemakan hati non alkoholik. Pemeriksaan ini
nampaknya dapat menjadi modalitas yang cukup menjanjikan nantinya dalam
membedakan perlemakan hati dengan perlemakan hati non alkoholik.
5,6
2. Evaluasi Pencitraan
Berbagai modalitas pencitraan telah dicoba untuk mendeteksi perlemakan hati.
Agaknya ultrasonografi merupakan pilihan terapi terbaik saat ini, walaupun
Computerized Tomography (CT) dan Magnetic Resonance Imaging (MRI) juga dapat
digunakan. Pada ultrasonografi, infiltrasi lemak di hati akan menghasilkan
peningkatan difus ekogenisitas (hiperekoik) bila dibandingkan dengan ginjal.
Sensitivitas USG 89% dan spesitivitasnya 93% dalam mendeteksi steatosis.
Infiltrasi lemak di hati menghasilkan gambar parenkim hati dengan densitas
rendah yang bersifat difus pada CT, meskipun adakalanya berbentuk fokal. Gambaran
fokal ini dapat disalahartikan sebagai massa ganas di hati. Pada keadaan seperti ini
MRI bisa dipakai untuk membedakan nodula akibat keganasan dari infiltrasi fokal
lemak di hati.
2,6
2,6
3. Histologi
Secara histologi perlemakan hati non alkoholik tidak dapat dibedakan dengan
kerusakan hati akibat alkohol. Gambaran biopsi hati antara lain berupa steatosis,
infiltrasi sel radang, hepatocyte balloning dan nekrosis, nukleus glikogen, Mallory’s
hyaline dan fibrosis. Sayangnya, gambaran histologi minimal pada perlemakan hati
non alkoholik belum dapat ditemukan. Pada beberapa studi dalam diagnosa histologi
perlemakan hati non alkoholik bergantung ditemukannya steatosis makrovesikuler
dan inflamasi lobuler sendiri. Pemeriksaan histologi perlemakan hati non alkoholik
telah dianjurkan sebagai tahapan yang penting dalam mendiagnosa perlemakan hati
non alkoholik dan mengurangi kebingungan mengenai epidemiologi dan perjalanan
Gambar 2. Gambaran histologi Perlemakan Hati non Alkoholik1
Perubahan gambaran lemak pada perlemakan hati non alkoholik dapat
mempengaruhi lobus hati baik secara difus maupun primer pada zona pusat. Derajat
steatosis berhubungan dengan BMI dan biasanya lebih berat pada perlemakan hati non
alkoholik daripada hepatitis alkoholik. Inflamasi lobuler pada berbagai stadium
dijumpai pada semua kasus dan dapat terdiri dari limfosit, sel mononuklear lainnya
dan netrofil. Nukleus glikogen timbul pada 35-100% kasus perlemakan hati non
alkoholik. Hepatocyte balloning dan/atau nekrosis hepatosit pada berbagai stadium
biasanya dijumpai dan telah disetujui oleh berbagai ahli sebagai penentu diagnosa
perlemakan hati non alkoholik. Mallory’s body biasanya lebih menonjol pada
perlemakan hati non alkoholik yang lebih berat.
Fibrosis periseluler, perisinusoidal dan periportal ditunjukkan pada 37-84% pasien
dengan perlemakan hati non alkoholik. Fibrosis sering terjadi pada zona 3. Fibrosis
lebih sering terjadi pada anak-anak dengan perlemakan hati non alkoholik daripada
dewasa. Pada pemeriksaan biopsi dijumpai fibrosis pada 7-16% pasien dengan
perlemakan hati non alkoholik. Gambaran histologi fibrosis atau sirosis berhubungan
dengan temuan laboratorium dan gambaran klinis yang lebih buruk, namun para
peneliti telah menunujukkan bahwa usia yang lebih tua, obesitas dan diabetes melitus
merupakan prediktor independen derajat fibrosis.
5,6
Sampai saat ini masih terdapat perbedaan pendapat mengenai interpretasi
histopatologis perlemakan hati non alkoholik. Kontroversi terutama dalam hal
penentuan kriteria unutk membedakan perlemakan hati sederhana dengan perlemakan
hati non alkoholik. Klasifikasi dari Brunt merupakan kriteria histopatologis yang
banyak dipakai untuk menentukan derajat perlemakan hati non alkoholik.2,6,7
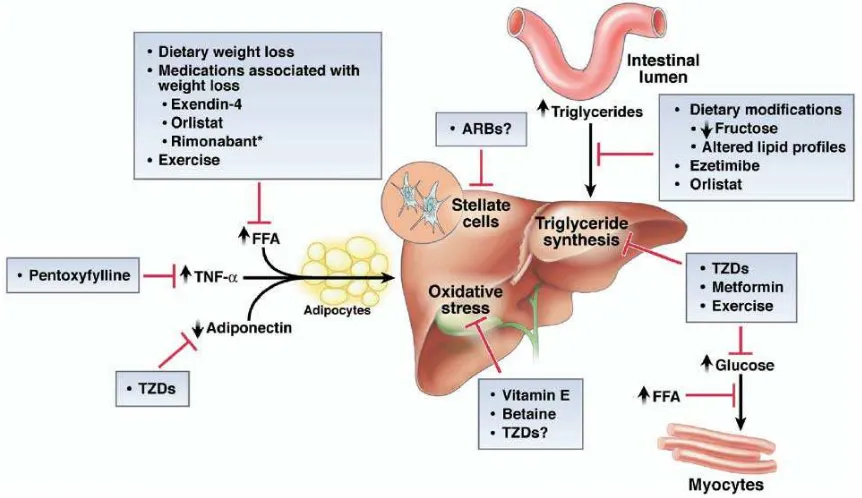
IV. PENATALAKSANAAN
Sampai saat ini modalitas pengobatan yang terbukti baik masih terbatas.
Belum ada terapi yang secara universal dapat dikatakan efektif, strategi pengobatan
cenderung dilakukan dengan pendekatan empiris karena patogenesis penyakit juga
belum begitu jelas diketahui. Penelitian terapi medikamentosa perlemakan hati non
alkoholik yang dipublikasikan sebagian besar merupakan uji klinis tanpa kontrol.
Penelitian yang menggunakan kontrol pada umumnya dilakukan terhadap pasien
dalam jumlah kecil atau bervariasi dalam menentukan kriteria steatohepatitis dan
parameter keberhasilan. Oleh karena pengobatan lebih ditujukan pada tindakan untuk
mengontrol faktor resiko seperti memperbaiki resistensi insulin dan mengurangi
asupan asam lemak ke hati, selanjutnya baru pemakaian obat yang dianggap memiliki
potensi hepatoprotektor.2
1. Pengontrolan Faktor Resiko
a. Pengurangan kalori
Pasien dengan perlemakan hati non alkoholik biasanya overweight atau obese,
resistensi insulin dan memiliki ambilan energi yang lebih tinggi dibandingkan
individu tanpa perlemakan hati.
Derajat pengurangan kalori masih dipertanyakan. Studi kecil oleh Anderson dkk
menunjukkan bahwa pengurangan berat badan yang ekstrim dengan kelaparan
menyebabkan keparahan pada histologi hati termasuk fibrosis. Huang dkk
menganjurkan pasien-pasien untuk melakukan diet 1400 kkal/hari selama 12 bulan
dan pada 15 pemeriksaan biopsi pasien perlemakan hati non alkoholik menunjukkan
pengurangan berat badan 2,9 kg (3% berat badan). 9 diantara 15 pasien (60%)
memiliki kemajuan pada pemeriksaan histopatologi dengan pengurangan berat badan
mencapai 7%.
4
b. Latihan Jasmani
4
Latihan jasmani dan pengaturan diet menjadi inti terapi dalam usaha mengurangi
berat badan. Aktivitas fisik hendaknya berupa latihan bersifat aerobik paling sedikit
30 menit sehari. Sangat penting untuk mencapai target denyut nadi, tetapi tidak perlu
2. Terapi Farmakologis
a. Antidiabetik dan Insulin Sensitizer
Thiazolidindione
Thiazolidindione memperbaiki resistensi insulin di otot rangka, jaringan adiposa
dan hati melalui kerjanya sebagai agonis Peroksisome Proliferator Activated Receptor γ (PPAR- γ) yang meningkatkan kadar adiponektin plasma dan oksidasi asam lemak dan menurunkan sintesis asam lemak. Agen ini telah banyak diteliti banyak digunakan
sebagai insulin sensitizer pada kasus perlemakan hati non alkoholik. Pioglitazone dan
rosiglitazone merupakan jenis obat thiazolidindione yang telah banyak digunakan.
Efek samping Thiazolidindione haruslah diperhatikan. Peningkatan berat badan
2-3 kg telah ditunjukkan menjadi penyebab peningkatan deposisi lemak perifer.
Beberapa studi juga menunjukkan bahwa Thiazolidindione meningkatkan kehilangan
tulang dan dapat menyebabkan terjadinya osteoporosis dan meningkatkan resiko
fraktur terutama pada wanita post menopause.
Resiko untuk terjadinya gagal jantung juga dilaporkan oleh karena adanya efek
retensi cairan dan disfungsi diastolik sehingga tidak dianjurkan pada penderita gagal
jantung dengan NYHA 3-4.4
Metformin
Metformin meningkatkan kerja insulin pada sel hati dan menurunkan produksi
glukosa hati. Lin dkk menunjukkan perbaikan penyakit perlemakan hati pada model
hewan dengan perlemakan hati non alkoholik. Hal ini dianggap terjadi melalui
penghambatan TNF-α sehingga terjadi perbaikan insulin.4,9
Penelitian lain dilakukan oleh Marchesini dkk. 14 pasien perlemakan hati non
alkoholik mendapat terapi metformin 3 x 500 mg /hari selama 4 bulan dan sebagai
kelompok kontrol adalah 6 pasien perlemakan hati non alkoholik yang hanya
mendapat terapi diet. Didapatkan perbaikan kadar rata-rata transaminase, peningkatan
sensitivitas insulin dan penurunan volume hati pada pasien yang mendapatkan terapi
metformin.
4,9
b. Terapi Antioksidan
Pengurangan antioksidan di dalam hepatosit yang menyebabkan gangguan
inaktivasi ROS merupakan dasar pemberian suplemen antioksidan pada terapi pasien
dengan perlemakan hati non alkoholik. Antioksidan larut lemak tokoferol (vitamin E)
telah ditunjukkan menghambat peroksidase lemak dan menekan sitokin inflamasi
seperti TNF-α, dan penggunaannya dalam terapi perlemakan hati non alkoholik telah
banyak diteliti. Satu studi membandingkan 6 bulan pemakaian 1000 IU vitamin E dan
1000 mg vitamin C per hari vs plasebo memperlihatkan perbaikan yang signifikan
fibrosis hati pada kelompok dengan vitamin tapi tidak diantara kelompok dan tidak
ada perubahan pada kadar aminotransferase dan inflamasi hati.
Betain, antioksidan lain pada terapi perlemakan hati non alkoholik, meningkatkan
kadar S-adenosilmetionin dan diduga dapat menurunkan deposisi lemak di hati.
Perbaikan pada kadar aminotransferase, steatosis hati, aktivitas inflamasi dan fibrosis
ditunjukkan pada trial pada 10 pasien perlemakan hati non alkoholik yang diterapi
dengan betain anhidrous 20 mg sehari dalam 12 bulan.
4
4
c. Hepatoprotektor
Ursodeoxycholic acid (UDCA) adalah asam empedu dengan banyak efek seperti
efek imunomodulator, pengaturan lipid dan efek sitoproteksi. Pertama kali digunakan
pada perempuan berusia 66 tahun dengan perlemakan hati non alkoholik yang
menunujukkan normalisasi enzim transaminase setelah terapi UDCA selama 1 tahun.
pasien perlemakan hati non alkoholik. Pada studi terhadap 40 pasien yang mendapat
UDCA 13-15 mg/kb/hari selama 1 tahun terbukti adanya perbaikan ALT, alkali
fosfatase, GGT dan steatosis, tapi tidak ada perbaikan bermakna dalam derajat
inflamasi dan fobrosis. Pada studi lain tes fungsi hati mengalami perbaikan pada 13
pasien setelah mendapat UDCA 10 mg/kgBB/hari selama 6 bulan. Studi paling baru
tentang UDCA dilakukan terhadap 24 pasien dengan dosis 250 mg 3 kali sehari
selama 6-12 bulan. Dilaporkan adanya perbaikan kadar aminotransferase dan petanda
fibrogenesis.2
c. Obat Anti Hiperlipidemia
Studi menggunakan gemfibrozil menunjukkan perbaikan ALT dan kadar lipid
setelah pemberian obat selama 1 tahun, tapi evaluasi histologi tidak dilakukan. Sebuah
studi pendahuluan dengan sampel kecil menunujukkan perbaikan parameter
biokimiawi dan histologi pada kelompok pasien yang mendapat atorvastatin.
Sebaliknya studi lain menunujukkan tidakn adanya perbedaan bermakna antara
kontrol dan pasien menggunakan berbagai jenis statin.2
V. KESIMPULAN
Perlemakan hati non alkoholik merupakan penyakit kronis yang meningkat
pada pasien dengan fungsi hati terganggu. Kebanyakan pasien adalah wanita dan
obesitas dengan DM tipe 2 dan/atau hiperlipidemia. Namun perlemakan hati non
alkoholik dapat juga terjadi pada laki-laki dan perempuan tanpa keadaan yang
disebutkan tadi. Perlemakan hati non alkoholik sangat sulit dibedakan secara histologi
dengan hepatitis alkoholik dan biasanya dengan gambaran steatosis makrovaskuler,
nekroinflamasi, hepatocyte balloning dan fibrosis.
Patogenesis perlemakan hati non alkoholik masih belum jelas namun stres
oksidatif dikatakan paling berperan. Diagnosa perlemakan hati non alkoholik
haruslah dipikirkan pada pasien-pasien dengan fungsi hati abnormal, tidak ada riwayat
konsumsi alkohol, tidak dijumpai tanda-tanda penyakit hati kronis an dijumpai
steatosis hati pada pencitraan. Namun, perlemakan hati non alkoholik merupakan
diagnosa histologi, sehingga biopsi hati sangat penting dilakukan. Tidak ada terapi
definitif perlemakan hati non alkoholik namun penurunan berat badan merupakan
DAFTAR PUSTAKA
1. Harrison SA, MC, MD, Kadakia S, MD. Nonalcoholic Steatohepatitis: What
We Know in the New Millenium. The American Journal of Gastroenterology,
2002; 97; 2714-20
2. Hasan I. Perlemakan Hati Non Alkoholik. Dalam : Buku Ajar Ilmu Penyakit
Dalam, Pusat Penerbitan, Departemen Ilmu Penyakit Dalam Fakultas
Kedokteran Universitas Indonesia, Jakarta, ed 4, jilid I, 2006: 464-67
3. Day, CP, Daly AK. NASH is genetically determined disease. In : Fatty Liver
Disease : NASH and Related Disorder, Blackwell Publishing, 1st ed, 2005,
66-75
4. Torres DM, Harrison SA. Diagnosis and Therapy of Nonalcoholic
Steatohepatitis. Gastroenterology, 2008; 134; 1682-98
5. Harrison SA, Tetri BN. Clinical Manifestation and Diagnosis of NASH. In:
Fatty Liver Disease: NASH and Related Disorder, Blackwell Publishing, 1st
ed, 2005, 159-67
6. Hall, P dela M, Kirch R. Pathology of Hepatic Steatosis, NASH and Related
Condition. In : Fatty Liver Disease: NASH and Related Disorder, Blackwell
Publishing, 1st ed, 2005, 13-22
7. Portincasa P, Grattagliano I. Nonalcoholic steatohepatitis: recent advances
from experimental models to clinical management. Clinical Biochemistry,
2005; 38; 203-17
8. Reid, AE. Nonalcoholic Steatohepatitis. Gastroenterology, 2001 ; 121 ;
710-723
9. Jansen PLM. Nonalcoholic Steatohepatitis. The Journal of Medicine, 2004;