commit to user
i
KADAR KURKUMINOID, TOTAL FENOL DAN AKTIVITAS
ANTIOKSIDAN SIMPLISIA TEMULAWAK
(
Curcuma xanthorrhiza
Roxb.) PADA BERBAGAI TEKNIK
PENGERINGAN
Skripsi
Untuk memenuhi sebagian persyaratan
guna memperoleh derajat Sarjana Teknologi Pertanian di Fakultas Pertanian
Universitas Sebelas Maret
Program Studi Teknologi Hasil Pertanian
Oleh :
Grafianita
H 0607013
FAKULTAS PERTANIAN
UNIVERSITAS SEBELAS MARET
SURAKARTA
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
i
KADAR KURKUMINOID, TOTAL FENOL DAN AKTIVITAS
ANTIOKSIDAN SIMPLISIA TEMULAWAK
(
Curcuma xanthorrhiza
Roxb.) PADA BERBAGAI TEKNIK
PENGERINGAN
Yang dipersiapkan dan disusun oleh
GRAFIANITA
H 0607013
Telah dipertahankan di depan Dewan Penguji
Pada tanggal:
dan dinyatakan telah memenuhi syarat
Susunan Dewan Penguji
Ketua
Ir. Kawiji, MP NIP. 196112141986011001
Anggota I
Edhi Nurhartadi, S.TP, MP NIP. 197606152009121002
Anggota II
Setyaningrum Ariviani, S.TP, M.Sc NIP. 197604292002122002
Surakarta, Juli 2011
Mengetahui
Universitas Sebelas Maret
Fakultas Pertanian
Dekan
commit to user
i
KATA PENGANTAR
Puji syukur penulis panjatkan kepada Allah SWT yang telah memberikan
rahmat dan hidayah-Nya, sehingga penulis dapat menyelasaikan skripsi dengan
judul “Kadar Kurkuminoid, Total Fenol dan Aktivitas Antioksidan Simplisia
Temulawak (Curcuma xanthorrhiza Roxb.) Pada Berbagai Teknik
Pengeringan”. Penulisan skripsi ini merupakan salah satu syarat yang harus
dipenuhi oleh mahasiswa untuk mencapai gelar Sarjana Stratum Satu (S-1) pada
program studi Teknologi Hasil Pertanian, Fakultas Pertanian, Universitas Sebelas
Maret Surakarta.
Penyusunan skripsi ini tidak terlepas dari bantuan berbagai pihak, untuk
itu tidak lupa penulis mengucapkan terima kasih kepada :
1. Bapak Prof. Dr. Ir. Bambang Pujiasmanto, MS selaku Dekan Fakultas
Pertanian Universitas Sebelas Maret Surakarta.
2. Bapak Ir. Kawiji, MP selaku Ketua Jurusan Teknologi Hasil Pertanian dan
selaku Pembimbing Utama Skripsi yang telah memberi bimbingan dan
masukan dalam penyusunan skripsi ini sehingga dapat terselesaikan dengan
baik.
3. Bapak Edhi Nurhartadi, S.TP, MP selaku Pembimbing Pendamping Skripsi yang
memberi masukan sehingga skripsi ini dapat terselesaikan dengan baik.
4. Ibu Setyaningrum Ariviani, S.TP, M.Sc selaku Dosen Penguji Skripsi yang
telah memberikan banyak masukan.
5. Bapak R. Baskara Katri Anandito, S.TP, MP selaku Pembimbing Akademik
yang telah membimbing penulis selama empat tahun masa kuliah.
6. Ibu Sri Liswardani S.TP, Pak Slameto, Pak Giyo, Pak Joko, terima kasih
banyak atas segala bantuannya selama penelitian.
7. Bapak dan Ibu Dosen serta seluruh staff Fakultas Pertanian Universitas
Sebelas Maret Surakarta atas segala bantuan selama masa perkulihan penulis.
8. Skripsi ini, saya persembahkan kepada orang tua saya atas segala dukungan,
kasih sayang, semangat, pengorbanan, dan doanya. Semoga kita selalu dalam
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
i
9. Dian dan Nina yang telah mendukung penulis untuk menyelesaikan skripsi ini
serta senantiasa melatih penulis untuk selalu bersabar dalam menghadapi
setiap tantangan.
10.Teman-teman seperjuangan selama empat tahun Ana, Arin, Ambar, Eni, Nora,
Lorenz, Galuh, Yuli, dan Tina terima kasih atas bantuannya dan
persahabatannya selama ini. Skripsi ini tidak akan terselesaikan tanpa kalian.
11.Theresia yang senantiasa memberikan bantuan dari awal penelitian hingga
terselesaikannya skripsi ini, thanks for my partner.
12.Tarso yang senantiasa memberikan semangat dan motivasi walaupun terpisah
jauh, terima kasih atas cinta dan kasih sayangnya.
13.Angkatan THP 07 yang telah mengisi hari-hari penulis selama empat tahun.
14.Semua pihak yang telah membantu kelancaran penyusunan skripsi ini dan
memberi dukungan, doa serta semangat bagi penulis untuk terus berjuang.
Penulis menyadari bahwa skripsi ini masih jauh dari sempurna. Semoga
skripsi ini bermanfaat bagi penulis khususnya dan bagi pembaca pada umumnya.
Surakarta, Juni 2011
commit to user
i
DAFTAR ISI
HALAMAN JUDUL ... i
HALAMAN PENGESAHAN ... ii
KATA PENGANTAR ... iii
DAFTAR ISI ... v
DAFTAR TABEL ... vii
DAFTAR GAMBAR ... viii
DAFTAR LAMPIRAN ... ix
RINGKASAN ... x
SUMMARY... xi
I. PENDAHULUAN A. Latar Belakang ... 1
B. Perumusan Masalah ... 4
C. Tujuan Penelitian ... 4
D. Manfaat Penelitian ... 4
II. TINJAUAN PUSTAKA A. Temulawak... ... 5
B. Simplisia Temulawak... 8
C. Kurkuminoid... 9
D. Senyawa fenolik... 13
E. Antioksidan... 15
F. Pengeringan ... ... 18
G. Hipotesis... 20
III.METODE PENELITIAN A. Tempat dan Waktu Penelitian ... 21
B. Bahan dan Alat ... 21
1. Bahan ... 21
2. Alat ... 21
C. Tahap Penelitian ... 22
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
i
2. Pengeringan... 22
3. Analisis Senyawa Aktif Oleorasin Temulawak... 23
D. Rancangan Penelitian... 25
IV.HASIL DAN PEMBAHASAN A. Kadar Air... 26
B. Kadar Kurkuminoid Simplisia Temulawak Pada Berbagai Teknik Pengeringan... 28
C. Kadar Total Fenol Simplisia Temulawak Pada Berbagai Teknik Pengeringan... 32
D. Aktivitas Antioksidan Simplisia Temulawak Pada Berbagai Teknik Pengeringan... 36
V. KESIMPULAN DAN SARAN A. Kesimpulan ... 43
B. Saran ... 43
DAFTAR PUSTAKA ... 44
commit to user
i
DAFTAR TABEL
Halaman
Tabel 2.1 Karakteristik Mutu Simplisia Temulawak... 9
Tabel 3.1 Metode Analisis Senyawa Aktif Simplisia Temulawak……… 23
Tabel 3.2 Rancangan Percobaan Acak Lengkap dengan Satu Faktor………… 25
Tabel 4.1 Hasil Analisis Kadar Air Simplisia Temulawak... 27
Tabel 4.2 Hasil Analisis Kadar Kurkuminoid Simplisia Temulawak... 29
Tabel 4.3 Hasil Analisis Total Fenol Simplisia Temulawak... 33
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
i
DAFTAR GAMBAR
Halaman
Gambar 2.1 Tanaman Temulawak... 5
Gambar 2.2 Rimpang Temulawak Berumur 10-12 Bulan... 7
Gambar 2.3 Struktur Kimia Kurkuminoid... 12
Gambar 2.4 Struktur Kimia Fenol... 13
Gambar 3.1 Diagram Alir Penelitian Simplisia Temulawak... 24
Gambar 4.1 Kadar Kurkuminoid Simplisia Temulawak pada Berbagai Teknik Pengeringan... 31
Gambar 4.2 Total Fenol Simplisia Temulawak pada Berbagai Teknik Pengeringan... 35
commit to user
i
DAFTAR LAMPIRAN
Nomor Judul Halaman
1. Metode Analisis... 49
a. Analisis Kadar Air... 49
b. Analisis Kurkuminoid... 49
c. Analisis Total Fenol... 49
d. Analisis Aktivitas Antioksidan... 50
2. Hasil Analisis Kadar Air... 51
3. Hasil Analisis Kimia Pengaruh Berbagai Teknik Pengeringan ... 51
a. Hasil Analisis Kadar Kurkuminoid... 51
b. Hasil Analisis Total Fenol... 53
c. Hasil Analisis Aktivitas Antioksidan... 55
4. Hasil Analisis Menggunakan SPSS (One Way Anova) ... 56
a. Semua data (3 kali perulangan, 3 kali analisis)... 56
b. Rata-Rata Analisis Tiap Perlakuan... 61
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
i
KADAR KURKUMINOID, TOTAL FENOL, DAN AKTIVITAS ANTIOKSIDAN SIMPLISIA TEMULAWAK (Curcuma xanthorrhiza Roxb.)
PADA BERBAGAI TEKNIK PENGERINGAN
Grafianita 1)
Ir. Kawiji, MP 2) Edhi Nurhartadi, S.TP, MP 3)
RINGKASAN
Temulawak (Curcuma xanthorrhiza Roxb.) merupakan komponen penyusun hampir setiap jenis obat tradisional yang dibuat di Indonesia. Temulawak biasanya digunakan dalam bentuk simplisia tunggal atau merupakan salah satu komponen dari suatu ramuan. Temulawak memiliki banyak manfaat kesehatan karena mengandung senyawa aktif, salah satunya berupa kurkuminoid yang merupakan senyawa fenolik dan memiliki aktivitas antioksidan. Saat ini di Indonesia dalam pemanfaatan temulawak di tingkat petani sebagian besar hanya diolah menjadi simplisia. Simplisia temulawak merupakan hasil rajangan temulawak yang telah dikeringkan sampai kadar air tertentu. Pengeringan di tingkat petani hanya terbatas dengan penjemuran langsung sinar matahari yang tentunya tidak dapat mempertahankan senyawa aktif dalam temulawak yang dapat rusak oleh cahaya maupun panas.
Penelitian ini bertujuan untuk mengetahui pengaruh berbagai teknik pengeringan terhadap kadar kurkuminoid, total fenol dan aktivitas antioksidan simplisia temulawak. Selain itu, akan dipilih pengeringan yang paling efektif dan dalam mempertahankan kadar kurkuminoid, total fenol dan aktivitas antioksidan simplisia temulawak. Penelitian ini menggunakan Rancangan Acak Lengkap (RAL) dengan satu faktor yaitu berbagai variasi teknik pengeringan. Berbagai teknik pengeringan yang digunakan adalah SM (pengeringan sinar matahari tanpa kain penutup (k)), SD (solar dryer dengan kain penutup warna putih), CD A
(cabinet dryer suhu 35oC), CD B (cabinet dryer suhu 40oC), dan CD C (cabinet
dryer suhu 45oC).
Hasil penelitian menunjukan bahwa penggunaan cabinet dryer dengan suhu 45oC berpengaruh mempertahankan kadar kurkuminoid, total fenol dan aktivitas antioksidan simplisia temulawak dibandingkan dengan teknik pengeringan lainnya. Pengeringan dengan menggunakan cabinet dryer suhu 45oC menghasilkan kadar kurkuminoid, total fenol dan aktivitas antioksidan masing-masing sebesar 0,495%, 0,933%, dan 57,701%.
commit to user
i
ANTIOXIDANT ACTIVITY, TOTAL PHENOL AND CONCENTRATION CURCUMINOIDS CURCUMA SIMPLICIA
(Curcuma xanthorrhiza Roxb.) IN VARIATION DRYING TECHNIQUE
Grafianita 1)
Ir. Kawiji, MP 2) Edhi Nurhartadi, S.TP, MP 3)
SUMMARY
Curcuma (Curcuma xanthorrhiza Roxb.) is a component that compiler almost every kind of traditional medicine made in Indonesia. Curcuma usually used in kind of single simplicia or become one of component from a ingredients. Curcuma have many function for health because of they contains active compound, the ones of all is curcuminoid that included phenolic compound and have antioxidant activity. Today, in Indonesia using Curcuma in farmer’s community usually just processed as simplisia. Simplisia of Curcuma is the result of cut curcuma that has been drying until certain compound of water. The desiccation in farmer’s community just limiting in using sun drying that of course can not defend active compound in Curcuma that can be broken by light and also heat.
This research is aim to find out the influence variation of drying tehnique concerning curcuminoid compound, total phenol, and antioxidan activity simplicia curcuma. Beside that, will be choose the drying technique that most effective in defend curcuminoid compound, total phenol, and antioxidant activity simplisia curcuma. This research used Completely Randomized Design (CRD) with one factor, that are variety of drying technique. Variety drying technique that we use is SM (sun drying without cover (k)), SD (solar dryer with the white cloth cover), CD 35oC (cabinet dryer temperature 35oC), CD 40oC (cabinet dryer temperature 40oC), dan CD 45oC (cabinet dryer temperature 45oC).
The result of research shows that using cabinet dryer with temperature 45oC influential in defend curcuminoid compound, total phenol, and antioxidant activity simplicia curcuma than using another drying technique. The drying that using cabinet dryer temperature 45oC producing curcuminoid compound, total Fenol, and antioxidan activity each 0,495%, 0,933%, dan 57,701%.
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
1
I. PENDAHULUAN
A. Latar Belakang
Temulawak (Curcuma xanthorrhiza Roxb.) merupakan salah satu
tanaman obat suku Zingiberaceae yang banyak digunakan sebagai bahan baku
dalam industri jamu dan obat di Indonesia. Temulawak merupakan komponen
penyusun hampir setiap jenis obat tradisional di Indonesia. Dalam obat
tradisional Indonesia temulawak digunakan sebagai simplisia tunggal atau
merupakan salah satu komponen dari suatu ramuan. Selain sebagai bahan
baku industri jamu dan obat, olahan temulawak juga digunakan dalam industri
pangan dan kosmetik. Ekspor rimpang temulawak di Indonesia tahun 2006
mencapai US$ 1,255 juta dengan jumlah sebanyak 2.647 ton rimpang
temulawak (BPS, 2006). Temulawak diketahui memiliki banyak manfaat
antara lain sebagai antihepatitis, antiinflamasi, antikarsinogenik, antimikroba,
antiviral, detoksifikasi, dan antioksidan (WHO 1999 dalam Irawati, 2008).
Terkait dengan temulawak sebagai bahan baku obat dan farmasi
menurut Parahita (2007) temulawak diketahui mengandung senyawa kimia
yang mempunyai keaktifan fisiologis, yaitu kurkuminoid dan minyak atsiri.
Menurut Yunus dan Rahayu (2009) temulawak terdiri dari fraksi pati,
kurkuminoid, dan minyak atsiri. Pati merupakan komponen terbesar dalam
rimpang temulawak, yaitu sekitar 30-40% dihitung dari bobot kering,
berbentuk serbuk berwarna putih kekuningan karena mengandung
kurkuminoid. Kurkuminoid terdiri atas senyawa berwarna kuning kurkumin
dan turunannya sebanyak 1,60-2,20% (Kunia, 2006). Minyak atsiri dalam
temulawak sebanyak 6-10% terdiri dari isofuranogermakren, trisiklin,
allo-aromadendren, germakren, dan xanthorrizol (Dalimartha, 2000).
Saat ini penanganan temulawak oleh petani selain dijual dalam bentuk
rimpang hanya sebatas dibuat menjadi simplisia sebagai upaya meningkatkan
nilai ekonominya. Simplisia merupakan hasil pengeringan dari tanaman obat
yang belum diolah lebih lanjut atau baru dirajang saja yang kemudian
commit to user
serbuk, minyak atsiri, ekstrak kental/ oleoresin, ekstrak kering maupun kapsul
(Sembiring, 2008).
Pengeringan yang dilakukan oleh petani (produsen) simplisia
temulawak pada umumnya hanya dengan dijemur dibawah sinar matahari
langsung. Cara ini dianggap oleh masyarakat merupakan cara yang mudah dan
murah karena tidak membutuhkan biaya yang mahal dan dapat dilakukan
dimana saja. Permasalahan yang timbul adalah rendahnya kualitas dan
rendahnya kontinuitas suplai simplisia temulawak. Hal ini dikarenakan
pengeringan langsung dengan sinar matahari di alam terbuka menyebabkan
terjadinya resiko kontaminasi oleh jamur, terganggunya proses pengeringan
pada musim hujan, dan rusaknya kandungan senyawa aktif oleh sinar UV
yang ada cukup tinggi (Widyasari, 2000).
Mengingat manfaat yang besar dari peran temulawak di berbagai
bidang industri baik makanan maupun farmasi maka diperlukan dukungan
teknologi untuk pengembangannya. Teknik pasca panen merupakan periode
kritis yang sangat menentukan kualitas dan kuantitas simplisia temulawak.
Salah satu tahap penting pasca panen temulawak yang dapat mempengaruhi
kandungan senyawa berkhasiat dalam temulawak adalah proses pengeringan.
Menurut Kiswanto (2005) rimpang temulawak segar mengandung air sekitar
75%-80%. Kadar air yang tinggi menyebabkan temulawak mudah mengalami
kerusakan karena gangguan mikroba. Pengeringan pada rimpang temulawak
ini dilakukan dengan tujuan membuang sejumlah air untuk menjamin
penyimpanan dan mencegah terjadinya reaksi enzimatis. Pengeringan dapat
dilakukan dengan dua cara yaitu dengan menggunakan panas buatan ataupun
dengan menjemur langsung di bawah sinar matahari. Dalam pengeringan
harus diperhatikan suhu dan jenis bahan yang akan dikeringan. Menurut
Parahita (2007) bahan simplisia yang mengandung senyawa aktif dan tidak
tahan panas harus dikeringkan pada suhu serendah mungkin, misalnya
30-45oC.
Teknik pengeringan yang bersifat tradisional merupakan salah satu
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
3
aktivitas antioksidan) serta tumbuhnya jamur sehingga menurunkan harga dan
pendapatan petani. Tanpa adanya usaha perbaikan teknik pengeringan
temulawak yang telah ada saat ini akan menyebabkan tidak terjaminnya
kualitas simplisia temulawak yang dihasilkan. Melihat manfaat yang banyak
dari penggunaan temulawak sebagai bahan baku industri dalam bentuk
simplisia maka penelitian ini ditujukan untuk mengetahui kadar kurkuminoid,
total fenol dan aktivitas antioksidan simplisia temulawak (Curcuma
xanthorrhiza Roxb.) pada berbagai teknik pengeringan. Teknik pengeringan
yang digunakan dalam penelitian ini yaitu pengeringan sinar matahari tanpa
kain penutup (kontrol), solar dryer dengan kain penutup warna putih, cabinet
dryer suhu 35oC, cabinet dryer suhu 40oC, dan cabinet dryer suhu 45oC.
Dengan teknik pengeringan yang tepat diharapkan mampu mempertahankan
commit to user
B. Perumusan Masalah
Dari latar belakang di atas, dapat diambil rumusan masalah sebagai
berikut :
1. Bagaimana kadar kurkuminoid, total fenol dan aktivitas antioksidan
simplisia temulawak pada berbagai teknik pengeringan?
2. Teknik pengeringan manakah yang paling efektif dalam mempertahankan
kadar kurkuminoid, total fenol dan aktivitas antioksidan simplisia
temulawak?
C. Tujuan Penelitian
Tujuan dari penelitian ini adalah:
1. Mengetahui kadar kurkuminoid, total fenol dan aktivitas antioksidan
simplisia temulawak pada berbagai teknik pengeringan
2. Mengetahui teknik pengeringan yang paling efektif dalam
mempertahankan kadar kurkuminoid, total fenol dan aktivitas antioksidan
simplisia temulawak
D. Manfaat Penelitian
Manfaat dari penelitian ini adalah dapat memberikan informasi tentang
teknik pengeringan yang paling efektif dan efisien dalam mempertahankan
kadar kurkuminoid, total fenol dan aktivitas antioksidan simplisia temulawak
sehingga dapat menjadi alternatif pengeringan bagi produsen untuk
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
5
II. TINJAUAN PUSTAKA
A. Temulawak
Temulawak merupakan sumber bahan pangan, pewarna, bahan baku
industri (seperti kosmetika dan farmasi), maupun dapat dibuat makanan atau
minuman segar. Temulawak telah dibudidayakan dan banyak ditanam di
pekarangan atau tegalan, sering ditemukan tumbuh liar di hutan jati atau
padang alang-alang. Tanaman ini lebih produktif pada tempat terbuka yang
terkena sinar matahari dan dapat tumbuh mulai dari dataran rendah sampai
dataran tinggi. Akan tetapi, untuk mencapai hasil yang maksimal, sebaiknya
ditanam pada ketinggian sekitar 200-600 mdpl. Rimpang temulawak
termasuk yang paling besar di antara semua rimpang marga Curcuma.
Rimpangnya dipanen jika bagian-bagian tanaman yang ada di atas tanah
sudah mulai kering dan mati (Dalimartha, 2000).
Gambar 2. 1 Tanaman Temulawak
Tanaman temulawak adalah tanaman obat berupa tumbuhan rumpun
berbatang semu (Gambar 2.1). Seluruh batang tanaman temulawak terdiri
dari pelepah-pelepah daun yang menyatu dan mempunyai umbi batang.
Tinggi tanaman antara 50-200 cm. Daun berbentuk jorong, memanjang,
commit to user
20-80 cm, lebar daun 15-30 cm, serta tulang daun menyirip dan licin.
Permukaan bawah daun berwarna hijau pucat dan mengilat. Bunga pendek
dan lebar, berwarna kuning muda atau kuning bertabur warna merah
dipuncaknya, panjang helaian bunga 2,5-3,5 cm, panjang tongkol bunga
10-20 cm (Siswanto, 10-2004).
Kawasan Indo-Malaysia merupakan tempat temulawak berasal dan
kemudian menyebar ke seluruh dunia. Saat ini tanaman ini selain di Asia
Tenggara dapat ditemui pula di Cina, IndoCina, Barbados, India, Jepang,
Korea, di Amerika Serikat dan beberapa negara Eropa. Klasifikasi temulawak
adalah sebagai berikut:
Kerajaan : Plantae
Divisi : Spermatophyta Sub divisi : Angiospermae Kelas : Monocotyledonae Ordo : Zingiberales Keluarga : Zingiberaceae
Genus : Curcuma
Spesies : Curcuma xanthorrhiza Roxb.
(Rukmana, 1995).
Perbedaan umur panen tanaman temulawak dapat mempengaruhi
produktivitas dan mutu rimpang temulawak. Petani umumnya memanen
tanaman temulawak pada umur 9 bulan, bahkan sampai umur 24 bulan. Hasil
penelitian menunjukkan bahwa umur panen 7 bulan menghasilkan
produktivitas rimpang tertinggi (Balai Penelitian Tanaman Industri, 1982
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
7
Gambar 2.2 Rimpang Temulawak Berumur 10-12 Bulan
Menurut Sembiring (2007) rimpang temulawak dipanen setelah
tanaman berumur 10-12 bulan (Gambar 2.2). Temulawak yang dipanen pada
umur tersebut menghasilkan kadar minyak atsiri dan kurkumin yang tinggi.
Rimpang temulawak berbentuk bulat atau bulat telur, dari luar berwarna
kuning tua atau coklat kemerahan, sedang sisi dalam jingga kecoklatan. Dari
induk rimpang akan tumbuh rimpang-rimpang baru ke arah samping.
Rimpang baru ini lebih kecil, berwarna lebih muda, serta bentuknya beraneka
ragam. Aroma rimpang harum, tajam, serta rasanya pahit agak pedas.
Ujung-ujung akar biasanya membengkak, membentuk umbi kecil berbentuk bulat
sampai bulat telur (Siswanto, 2004).
Akar rimpang temulawak terbentuk dengan sempurna dan bercabang
kuat, berwarna hijau gelap. Rimpang induk dapat memiliki 3-4 buah rimpang.
Warna kulit rimpang cokelat kemerahan atau kuning tua, sedangkan warna
daging rimpang oranye tua atau kuning. Tiap rumpun umumnya memiliki 6
buah rimpang tua dan 5 buah rimpang muda (Parahita, 2007).
Rimpang temulawak mengandung zat kuning kurkumin, minyak atsiri,
pati, protein, lemak, selulosa, dan mineral. Di antara komponen yang
dikandung oleh temulawak, yang paling banyak kegunaannya adalah pati,
kurkuminoid, dan minyak atsiri (Husein, 2008 dalam Pandiangan, 2007).
Menurut Yunus dan Rahayu (2009) temulawak terdiri dari fraksi pati,
commit to user
rimpang temulawak, yaitu sekitar 30-40% dihitung dari bobot kering,
berbentuk serbuk berwarna putih kekuningan karena mengandung
kurkuminoid. Fraksi kurkuminoid dalam temulawak terdiri dari dua
komponen, yaitu kurkumin dan desmetoksikurkumin. Kadar kurkuminoid
dalam temulawak berkisar antara 1-2%. Sedangkan fraksi minyak atsiri
temulawak sebesar 6-10% (Parahita, 2007).
Banyaknya manfaat temulawak baik untuk obat tradisional maupun
fitofarmaka karena rimpangnya mengandung protein, pati, zat warna kuning
kurkuminoid dan minyak atsiri. Kandungan kimia minyak atsiri antara lain :
feladren, kamfer, tumerol, tolilmetilkarbinol, arkurkumen, zingiberen,
kuzerenon, germakron, β-tumeron serta xanthorrizol yang memiliki kandungan tertinggi sampai 40% (Rahardjo dan Rostiana, 2004 dalam
Kristina, 2006).
B. Simplisia Temulawak
Simplisia merupakan hasil pengeringan dari tanaman obat yang belum
diolah lebih lanjut atau baru dirajang saja yang kemudian dijemur. Dari
simplisia dapat diolah menjadi berbagai macam produk, seperti serbuk,
minyak atsiri, ekstrak kental/ oleoresin, ekstrak kering maupun kapsul
(Sembiring, 2008).
Irisan temulawak biasanya melintang setebal 2-3 mm. Hasil irisan
langsung dijemur di bawah terik matahari. Irisan rimpang dihamparkan di
bawah terik matahari dan dibalik satu kali. Perlakuan ini akan meningkatkan
kualitas simplisia. Apabila pengirisan dilakukan pada sore hari dan baru
dijemur keesokan harinya, maka kualitas simplisianya kurang baik
(Anonimc, 2010).
Ukuran perajangan tergantung dari bahan yang digunakan dan
ber-pengaruh terhadap kualitas simplisia yang dihasilkan. Perajangan terlalu tipis
dapat mengurangi zat aktif yang terkandung dalam bahan. Sedangkan jika
terlalu tebal, maka pengurangan kadar air dalam bahan agak sulit dan
memerlukan waktu yang lama dalam penjemuran dan kemungkinan besar
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
9
Kualitas simplisia sangat dipengaruhi oleh kandungan bahan aktif,
warna, kontaminasi mikroba dan metabolit sekunder seperti minyak atsiri,
flavonoid, fenolat, dan klorofil. Pada penentuan kualitas simplisia terbagi atas
analisa secara fisik dan kimia. Secara fisik biasanya termasuk
penampakannya secara visual terhadap warna, kotoran dan lainnya,
sedangkan secara kimia adalah analisa kandungan bahan aktifnya. Bahan
tanaman harus langsung dikeringkan setelah dikecilkan ukurannya. Apabila
tertunda, akan terjadi proses fermentasi, pemucatan, dan dekomposisi kimia
bahan aktifnya (Hernani dan Rahmawati, 2009).
Menurut Sembiring dkk (2006), Karakteristik mutu simplisia
temulawak dapat dilihat pada Tabel 2.1.
Tabel 2.1 Karakteristik Mutu Simplisia Temulawak
Karakteristik Hasil Analisis (%) *Standar Mutu (%)
Kadar Air 10,85 <12
Sumber : Materi Medika Indonesia (1979) dalam Sembiring dkk (2006), C. Kurkuminoid
Kurkuminoid adalah kelompok senyawa fenolik yang terkandung dalam
rimpang tanaman famili Zingiberceae antara lain : Curcuma longa syn.
Curcuma domestica (kunyit) dan Curcuma xanthorhiza (temulawak).
Kurkuminoid bermanfaat untuk mencegah timbulnya infeksi berbagai
penyakit (Kristina, 2006).
Kurkuminoid berkhasiat menetralkan racun, menurunkan kadar
kolesterol, dan trigliserida darah, antibakteri, analgetik, dan antiinflamasi.
Sekarang telah banyak diteliti bahwa kurkuminoid dapat digunakan sebagai
antioksidan dan inhibitor virus HIV (Anonim, 2007 dalam Irawati, 2008).
Kurkuminoid merupakan komponen yang memberi warna kuning pada
rimpang temulawak. Kurkuminoid berwarna kuning atau kuning jingga,
commit to user
dan alkali hidroksida. Kurkuminoid mempunyai aroma yang khas dan tidak
bersifat toksik. Bila kurkuminoid terkena cahaya akan terjadi dekomposisi
struktur berupa siklisasi kurkuminoid. Siklisasi kurkuminoid menyebabkan
senyawa kurkuminoid terdegradasi menjadi asam ferulat sehingga kadarnya
dalam ekstrak menjadi rendah (Sidik dkk., 1995).
Fraksi kurkuminoid terdiri dari curcumin (diferuloyl methane atau
kurkumin I) dan turunannya yaitu desmethoxy-curcumin
(feruloyl-p-hydroxy-cinnamoyl methane atau kurkumin II) dan
bis-desmethoxy-curcumin (bis-(p-hydroxycinnamoyl)-methane atau kurkumin III) (Wardini
dan Prakoso, 1999 dalam Devy, 2009).
Sering kali kadar total kurkuminoid dihitung sebagai % kurkumin.
Beberapa penelitian baik fitokimia maupun farmakologi lebih ditekankan
pada kurkumin karena kandungannya yang jauh lebih besar (50-60%)
dibanding komponen penyusun kurkuminoid yang lain yaitu
monodesmetoksikurkumin dan bisdemetoksikurkumin (Sumiyati dan
Adnyana, 2002 dalam Parinussa, 2006).
Menurut Jayaprakasha dkk. (2005), kurkumin merupakan molekul
dengan kadar polifenol yang rendah namun memiliki aktivitas biologi yang
tinggi antara lain memiliki potensi sebagai antioksidan. Gugus hidroksil dan
metoksil pada cincin fenil dan substituen 1,3 diketon memiliki peran yang
sangat signifikan dalam kemampuan kurkumin sebagai antioksidan. Aktivitas
antioksidan meningkat dengan meningkatnya gugus hidroksil pada cincin
fenil pada posisi orto dengan gugus metoksi. Sedangkan menurut Jovanovic
dkk. (2001) aktivitas antioksidan kurkumin disebabkan oleh kemampuan
donor atom hidrogen oleh β-diketon untuk menetralkan radikal bebas.
Kurkumin mempunyai aktivitas antioksidan karena mempunyai gugus
yang berperan penting dalam menangkal radikal bebas. Struktur kurkumin
terdiri dari gugus hidroksi fenolik dan gugus β-diketon. Gugus hidroksi
fenolik kemungkinan berfungsi sebagai penangkap radikal bebas pada fase
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
11
turunannya, demetoksi kurkumin dan bis-demetoksi kurkumin, bertanggung
jawab terhadap efek antioksidan dari turmerik (Tonnesen dan Greenhill,
1992; Majeed et al., 1995 dalam Nugroho, 2006). Kurkumin mempunyai dua
buah cincin aromatik yang mengandung gugus hidroksi fenolik, keduanya
dihubungkan rantai pendek yang terkonjugasi dengan gugus β-diketon. Kurkumin juga memiliki gugus metoksi pada cincin aromatiknya yang
bersifat sebagai pendorong elektron sehingga akan menambah kerapatan
elektron pada ikatan π yang akan mempermudah senyawa dalam menangkap
radikal hidroksi (Nugroho, 2006). Delokalisasi radikal pada posisi fenolik ke
dalam sistem rantai alkil terkonjugasi pada kurkumin dan derivatnya
memegang peranan penting dalam aktivitasnya sebagai antioksidan (Masuda
et al., 1999 dalam Nugroho, 2006).
Sifat kimia kurkuminoid yang menarik adalah sifat perubahan warna
akibat perubahan pH lingkungan. Dalam susana asam, kurkuminoid berwarna
kuning atau kuning jingga, sedangkan dalam suasana basa berwarna merah.
Dalam suasana basa selain terjadi proses disosiasi, kurkumin dapat
mengalami degradasi membentuk asam ferulat dan feruloilmetan. Degradasi
ini terjadi bila kurkumin berada dalam lingkungan pH 8,5-10,0 dalam waktu
yang relatif lama, walaupun hal ini tidak berarti bahwa dalam waktu yang
relatif singkat tidak terjadi degradasi kurkumin, karena proses degradasi
sangat dipengaruhi juga oleh suhu lingkungan. Salah satu hasil degradasi,
yaitu feruloilmetan mempunyai warna kuning coklat yang akan
mempengaruhi warna merah yang seharusnya terjadi (Tonnesen dan Karsen,
1985 dalam Kiswanto, 2005).
Kurkumin mempunyai rumus molekul C21H20O6 dengan bobot molekul
368 g/mol, sedangkan desmetoksikurkumin mempunyai rumus molekul
C20H18O5 dan bobot molekul 338 g/mol (Supriadi, 2008). Struktur kimia
commit to user
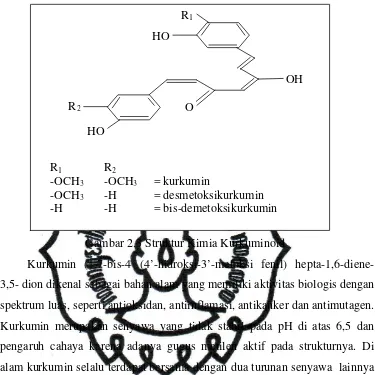
R1 R2
-OCH3 -OCH3 = kurkumin
-OCH3 -H = desmetoksikurkumin -H -H = bis-demetoksikurkumin
Gambar 2.3 Struktur Kimia Kurkuminoid
Kurkumin (1,7-bis-4 (4’-hidroksi-3’-metoksi fenil)
hepta-1,6-diene-3,5- dion dikenal sebagai bahan alam yang memiliki aktivitas biologis dengan
spektrum luas, seperti antioksidan, antiinflamasi, antikanker dan antimutagen.
Kurkumin merupakan senyawa yang tidak stabil pada pH di atas 6,5 dan
pengaruh cahaya karena adanya gugus metilen aktif pada strukturnya. Di
alam kurkumin selalu terdapat bersama dengan dua turunan senyawa lainnya
yaitu dimetoksi kurkumin dan bis-demetoksikurkumin, yang dikenal dengan
nama kurkuminoid (Tonnesen dan Karlsen., 1985 dalam Astuti, 2009).
Dalam Astuti (2009) juga disebutkan, Masuda et al., (1999) telah menemukan
mekanisme penangkapan radikal oleh kurkumin. Berdasarkan mekanisme
Masuda, gugus hidroksi fenolik berperan dalam penangkapan radikal pertama
kali pada kurkumin.
Kurkumin akan mengalami dekomposisi jika terkena cahaya. Produk
degradasinya yang utama adalah asam ferulat, aldehid ferulat,
dehidroksinaftalen, vinilquaikol, vanilin dan asam vanilat. Kurkumin
memperlihatkan kepekaan terhadap radikal bebas, kurkumin dapat bereaksi
selama atom H dilepas atau radikal hidroksil ditambahkan pada molekul
kurkumin. Pengurangan sebuah atom H menghasilkan pembentukan radikal OH
O
HO
HO R1
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
13
kurkumin yang terdekomposisi atau menjadi stabil dengan sendirinya (Van
der Good, 1995 dalam Kurnia, 2010).
D. Senyawa Fenolik
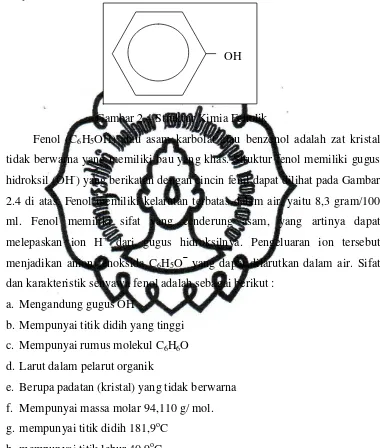
Gambar 2.4 Struktur Kimia Fenolik
Fenol (C6H5OH) atau asam karbolat atau benzenol adalah zat kristal
tidak berwarna yang memiliki bau yang khas. Struktur fenol memiliki gugus
hidroksil (OH-) yang berikatan dengan cincin fenil dapat dilihat pada Gambar
2.4 di atas. Fenol memiliki kelarutan terbatas dalam air, yaitu 8,3 gram/100
ml. Fenol memiliki sifat yang cenderung asam, yang artinya dapat
melepaskan ion H+ dari gugus hidroksilnya. Pengeluaran ion tersebut
menjadikan anion fenoksida C6H5O− yang dapat dilarutkan dalam air. Sifat
dan karakteristik senyawa fenol adalah sebagai berikut :
a. Mengandung gugus OH
b. Mempunyai titik didih yang tinggi
c. Mempunyai rumus molekul C6H6O
d. Larut dalam pelarut organik
e. Berupa padatan (kristal) yang tidak berwarna
f. Mempunyai massa molar 94,110 g/ mol.
g. mempunyai titik didih 181,9oC
h. mempunyai titik lebur 40,9oC
(Anonima,2004).
Fenol mempunyai sifat asam, mudah dioksidasi, mudah menguap,
sensitif terhadap cahaya dan oksigen, serta bersifat antiseptik. Kadar fenol
tersebut akan menurun antara lain dengan perlakuan pencucian, perebusan,
dan proses pengolahan lebih lanjut untuk dijadikan produk yang siap
dikonsumsi (Sundari, 2009).
commit to user
Senyawa fenolik pada bahan makanan dapat dikelompokkan menjadi
fenol sederhana dan asam fenolat (p-kresol, 3-etil fenol, 3,4-dietil fenol,
hidroksiquinon, vanilin dan asam galat), turunan asam hidroksi sinamat
(p-kumarat, kafeat, asam fenolat dan asam klorogenat) dan flavonoid (katekin,
proantosianin, antisianidin, flavon, flavonol dan glikosidanya). Fenol juga
dapat menghambat okidasi lipid dengan menyumbangkan atom hidrogen
kepada radikal bebas. Senyawa fenol (AH) jika berdiri sendiri tidak aktif
sebagai antioksidan, substitusi grup alkil pada posisi 2, 4 dan 6 dapat
meningkatkan densitas elektron gugus hidroksil, sehingga meningkatkan
keaktifannya terhadap radikal lipid (Widiyanti, 2009).
Menurut Andayani (2008) banyak tanaman obat yang mengandung
antioksidan dalam jumlah besar. Efek antioksidan terutama disebabkan
karena adanya senyawa fenolik seperti flavonoid, asam fenolat. Senyawa
fenolik memiliki efek antioksidan karena mempunyai gugus hidroksi yang
tersubstitusi pada posisi ortho dan para terhadap gugus –OH dan –OR.
Senyawa alami antioksidan tumbuhan umumnya adalah senyawa
fenolik atau polifenolik yang dapat berupa golongan flavonoid turunan
asam sinamat, kumarin, tokoferol. Senyawa ini diklasifikasikan dalam 2
bagian yaitu fenol sederhana dan polifenol. Senyawa-senyawa polifenol
seperti flavonoid dan galat mampu menghambat antioksidan melalui
mekanisme penangkapan radikal (radical scavenging) dengan cara
menyumbangkan satu elektron kepada elektron yang tidak berpasangan
dalam radikal bebas sehingga banyaknya radikal bebas menjadi berkurang
(Yuswantina, 2009).
Antioksidan fenolik yang berasal dari tanaman cenderung larut air dan
banyak terdapat sebagai glikosida dan berada pada vakuola sel. Mekanisme
antioksidan dari senyawa fenolik : (1) antioksidan fenolik alami (natural
phenolic antioxidant) menghalangi proses oksidasi dengan mendonorkan
atom hidrogen ke radikal (RO*), reaksinya : RO* + NPH NP*+ ROH,
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
15
terminator dari propagasi dengan cara bereaksi dengan radikal lainnya,
reaksinya RO* + NP* RONP (Abdullah, 2009).
Antioksidan yang termasuk golongan fenol mempunyai intensitas
warna yang rendah atau kadang-kadang tidak berwarna dan banyak
digunakan karena tidak beracun. Antioksidan golongan fenol meliputi
sebagian besar antioksidan yang dihasilkan oleh alam dan sejumlah kecil
antioksidan sintetis, serta banyak digunakan dalam lemak atau bahan pangan
berlemak. Beberapa contoh antioksidan yang termasuk golongan ini antara
lain hidrokuinon gossipol, pyrogallol, catechol resorsinol dan eugenol.
Aktivitas antioksidan tipe fenol mempunyai hubungan dengan proses
kesetimbangan oksidasi-reduksi (redoks) antara quinol dengan quinon
(Ketaren, 1986).
E. Antioksidan
Radikal bebas adalah atom atau molekul yang tidak stabil dan sangat
reaktif karena mengandung satu atau lebih elektron tidak berpasangan pada
orbital terluarnya. Untuk mencapai kestabilan atom atau molekul, radikal
bebas akan bereaksi dengan molekul di sekitarnya untuk memperoleh
pasangan elektron. Reaksi ini akan berlangsung terus-menerus dalam tubuh
dan bila tidak dihentikan akan menimbulkan berbagai penyakit seperti
kanker, jantung, katarak, penuaan dini, serta penyakit degeneratif lainnya.
Oleh karena itu, tubuh memerlukan suatu substansi penting yaitu antioksidan
yang mampu menangkap radikal bebas tersebut sehingga tidak dapat
menginduksi suatu penyakit (Kikuzaki, et al.,2002; Sibuea, 2003; dan
Halliwell, 2000 dalam Andayani, 2008).
Antioksidan adalah zat yang berfungsi melindungi tubuh dari serangan
radikal bebas. Yang termasuk ke dalam golongan zat ini antara lain vitamin,
polifenol, karoten dan mineral. Secara alami, zat ini sangat besar peranannya
pada manusia untuk mencegah terjadinya penyakit. Antioksidan melakukan
semua itu dengan cara menekan kerusakan sel yang terjadi akibat proses
oksidasi radikal bebas. Radikal bebas sebenarnya berasal dari molekul
commit to user
lingkungan. Aktivitas lingkungan yang apat memunculkan radikal bebas
antara lain radiasi, polusi, merokok dan lain sebagainya (Anonimb, 2008).
Menurut Kochar dan Tossel dalam Hudson (1990) dalam Yuswantina
(2009) berkaitan dengan fungsinya senyawa-senyawa antioksidan dapat
diklasifikasikan dalam 5 tipe antioksidan yaitu:
1. Primary Antioxidant yaitu senyawa, terutama
senyawa-senyawa fenol yang mampu memutus rantai reaksi pembentukan radikal
bebas asam lemak. Dalam hal ini memberikan atom hidrogen yang
berasal dari gugus hidroksi senyawa fenol sehingga terbentuk senyawa
yang stabil. Senyawa antioksidan yang termasuk kelompok ini misalnya:
BHA, BHT, TBHQ, PG dan tokoferol.
2. Oxygen Scavengers yaitu senyawa-senyawa yang berperan sebagai
pengikat oksigen sehingga tidak mendukung reaksi oksidasi. Dalam hal
ini, senyawa tersebut akan mengadakan reaksi dengan oksigen yang
berada dalam sistem sehingga jumlah oksigen akan berkurang.
Contoh dari senyawa-senyawa kelompok ini adalah vitamin C (asam
askorbat) askorbil palmitat, asam eritorbat dan sulfit.
3. Secondary Antioxydant yaitu senyawa-senyawa yang mempunyai
kemampuan untuk mendekomposisi hidroperoksida menjadi produk
akhir yang stabil. Pada umumnya tipe antioksidan ini digunakan untuk
menstabilkan polyoefin resin contohnya adalah asam tiodipropionat dan
dilauril tipropionat.
4. Antioxidant Enzyme yaitu enzim yang berperan mencegah terbentuknya
radikal bebas. Contohnya: glukosaoksidase, superoksidadismutase (SOD)
glutation perioksidase dan katalase.
5. Chelator Sequestrants yaitu senyawa-senyawa yang mampu
mengikat logam seperti besi (Fe) dan tembaga (Cu) yang mampu
mengkatalisa reaksi oksidasi lemak. Senyawa antioksidan yang
termasuk didalamnya adalah asam sitrat, asam amino, etylenediaminetetra
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
17
Berdasarkan sumbernya antioksidan digolongkan menjadi 2 macam,
yaitu antioksidan alami dan antioksidan buatan (sintetik). Antioksidan alami
mampu melindungi tubuh terhadap kerusakan yang disebabkan spesies
oksigen reaktif, mampu menghambat terjadinya penyakit degeneratif serta
mampu menghambat peroksidasi lipid pada makanan. Peroksidasi lipid
merupakan salah satu faktor yang cukup berperan dalam kerusakan selama
dalam penyimpanan dan pengolahan makanan. Antioksidan tidak hanya
digunakan dalam industri farmasi, tetapi juga digunakan secara luas dalam
industri makanan, industri petroleum, industri karet, dan sebagainya (Ilham,
2007).
Fungsi utama antioksidan digunakan sebagai upaya untuk memperkecil
terjadinya proses oksidasi dari lemak dan minyak, memperkecil terjadinya
proses kerusakan dalam makanan, memperpanjang masa pemakaian dalam
industri makanan, meningkatkan stabilitas lemak yang terkandung dalam
makanan serta mencegah hilangnya kualitas sensori dan nutrisi. Peroksidasi
lipid merupakan salah satu faktor yang cukup berperan dalam kerusakan
selama dalam penyimpanan dan pengolahan makanan (Hernani dan Raharjo,
2005).
Skema mekanisme reaksi pembentukan radikal bebas adalah sebagai
berikut :
1. Pada tahap inisiasi, radikal lipid terbentuk dari molekul lipid dan
terjadi pengurangan atom hidrogen oleh radikal reaktif misalnya radikal
hidrogen.
RH→ R* + H *
2. Selanjutnya tahap propagasi, radikal lipid diubah menjadi radikal lipid
yang berbeda dan mengakibatkan pengurangan atom hidrogen dari
molekul lipid atau penambahan atom oksigen pada radikal alkil.
R* + O2→ ROO*
ROO* + RH → ROOH + R*
3. Pada tahap terminasi, radikal bebas bergabung untuk membentuk
commit to user
ROO* + ROO *→ ROOR + O2
ROO * +R *→ ROOR
R *+ R *→ RR
(Rohman dan Riyanto, 2004 dalam Astuti, 2009).
F. Pengeringan
Pengeringan merupakan usaha untuk menurunkan kadar air bahan
sampai ke tingkat yang diinginkan dan menghilangkan aktivitas enzim yang
bisa menguraikan lebih lanjut kandungan zat aktif. Beberapa faktor yang
mempengaruhi proses pengeringan, antara lain waktu pengeringan, suhu
pengeringan, kelembapan udara di sekitarnya, kelembapan bahan atau
kandungan air dari bahan, ketebalan bahan yang dikeringkan, sirkulasi udara
dan luas permukaan bahan. Suhu pengeringan sangat berpengaruh terhadap
kualitas, terutama pada perubahan kadar fitokimia atau senyawa aktif. Bila
menggunakan suhu tinggi konsekuensinya dapat menghilangkan kandungan
atsiri, akan tetapi pada suhu rendah akan meningkatkan jumlah mikroba.
Untuk bahan yang mengandung minyak atsiri, suhu pengeringan yang terbaik
adalah 35-45°C (Hernani dan Rahmawati, 2009).
Dengan menerima panas matahari langsung, irisan rimpang temulawak
akan bisa benar-benar kering (kadar air di bawah 15%) dalam jangka waktu 4
hari penuh. Tanda irisan rimpang temulawak telah benar-benar kering adalah,
bisa dipatahkan dengan mudah dan tidak bisa digigit. Warna irisan rimpang
temulawak kering kualitas baik adalah merah bata merata. Apabila
dipatahkan bekas patahan berwarna oranye cerah dan aromanya segar. Kalau
dikunyah rasanya tajam dan pahit (Anonimc, 2010).
Pada umumnya suhu pengeringan adalah antara 40-60oC dan hasil yang
baik dari proses pengeringan adalah simplisia yang mengandung kadar air
10%. Pada umumnya bahan (simplisia) yang sudah kering memiliki kadar air
± 8-10%. Dengan jumlah kadar air tersebut kerusakan bahan dapat ditekan
baik dalam pengolahan maupun waktu penyimpanan (Sembiring, 2007).
Semakin tinggi suhu pengeringan yang digunakan menyebabkan
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
19
enzim akan semakin rendah, kerusakan fenol semakin kecil. Akan tetapi
stabilitas fenol juga akan terganggu oleh semakin meningkatnya suhu
pengeringan sehingga jumlah total fenol terdeteksi akan mencapai puncak
maksimum kemudian konstan dan cenderung menurun (Susanti, 2008).
Pengeringan temu-temuan dapat dilakukan di atas para-para dengan
menggunakan sinar matahari dan ditutupi dengan kain hitam juga dapat
dilakukan dengan kombinasi antara sinar matahari dengan alat. Hasil dari
pengeringan untuk temulawak diperoleh kadar kurkumin 1,36%, kadar
xantorizol 1,92%, kadar minyak atsiri 6,48% (Sembiring, 2008).
Solar drying merupakan metode pengeringan yang saat ini sering
digunakan untuk mengeringkan bahan-bahan makanan hasil panen. Metode
ini bersifat ekonomis pada skala pengeringan besar karena biaya operasinya
lebih murah dibandingkan dengan pengeringan dengan mesin. Prinsip dari
solar drying ini adalah pengeringan dengan menggunakan bantuan sinar
matahari. Perbedaan dari pengeringan dengan sinar matahari biasa adalah
solar drying dibantu dengan alat sederhana sedemikian rupa sehingga
pengeringan yang dihasilkan lebih efektif. Metode solar drying sering
digunakan untuk mengeringkan padi. Namun karena pada prinsipnya
pengeringan adalah untuk mengurangi jumlah air (kelembaban) bahan, maka
metode ini juga dapat diaplikasikan untuk bahan makanan lain. Cara kerja
solar dryer adalah sebagai berikut: bahan yang ingin dikeringkan dimasukkan
ke dalam bilik yang berada pada ketinggian tertentu dari permukaan tanah.
Udara sekitar masuk melalui saluran yang dibuat lebih rendah daripada bilik
pemanasan dan secara otomatis terpanaskan oleh sinar matahari secara
konveksi pada saat udara tersebut mengalir menuju bilik pemanasan. Udara
yang telah terpanaskan oleh sinar matahari kemudian masuk kedalam bilik
pemanas dan memanaskan bahan makanan. Pengeringan bahan makanan jadi
lebih efektif karena pemanasan yang terjadi berasal dari dua arah, yaitu dari
sinar matahari secara langsung (radiasi) dan aliran udara panas dari bawah
commit to user
Pengering berbentuk kabinet memiliki rak-rak untuk menempatkan
bahan yang akan dikeringkan. Satu alat pengering kabinet rata-rata memiliki
3 atau 4 rak sebagai wadah atau tempat hasil tanaman yang akan dikeringkan,
rak-rak ditempatkan secara tersusun dalam alat dan dengan penyebaran udara
panas kedalamnya selama waktu yang telah ditentukan, pengeringan akan
berlangsung dengan baik mendekati pengeringan sempurna dengan sinar
matahari (Riata, 2010). Menurut Yissaluthana (2010)setelah ruangan ditutup,
maka udara panas dialirkan ke dalam ruang pemanas hingga semua bahan
menjadi kering. Udara panas yang masuk dari sebelah bawah ruang
menyebabkan material yang ada kolom yang paling bawah menjadi yang
paling pertama kering. Setelah tenggat waktu tertentu, tray akan dikeluarkan
dan material yang telah kering diambil. Material lain yang ingin dikeringkan
dimasukkan dan prosedur terjadi berulang-ulang sehingga dapat disebut juga
batch dryer.
G. Hipotesis
Hipotesis dari penelitian ini adalah penggunaan teknik pengeringan
yang berbeda (pengeringan sinar matahari tanpa kain penutup (kontrol), solar
dryer dengan kain penutup warna putih, cabinet dryer suhu 35oC, cabinet
dryer suhu 40oC, dan cabinet dryer suhu 45oC) diduga mempengaruhi kadar
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
21
III. METODE PENELITIAN
A. Tempat dan Waktu Penelitian
Penelitian ini dilaksanakan di Laboratorium Rekayasa Proses
Pengolahan Pangan dan Hasil Pertanian, Jurusan Teknologi Hasil Pertanian,
Fakultas Pertanian, Universitas Sebelas Maret Surakarta. Penelitian
dilaksanakan dalam jangka waktu 4 bulan mulai bulan Januari-April 2011.
B. Bahan dan Alat
1. Bahan
Dalam penelitian ini bahan utama yang digunakan adalah rimpang
temulawak yang dirajang dengan ukuran 3 mm. Dalam analisis akan
digunakan bahan-bahan sebagai berikut :
a. Analisis Kadar Air : toluene (xylene)
b. Analisis Kadar Kurkuminoid : kurkuminoid standar, etanol 96%
c. Analisis Antioksidan : DPPH (Diphenyl picrylhydrazyl), metanol
d. Analisis Total Fenol : aquadest, folin Ciocalteu, Na2CO3 2%, dan
fenol murni
2. Alat
Alat-alat yang digunakan dalam proses pembuatan simplisia
temulawak adalah mesin perajang (slicer); 3 buah tampah; solar dryer;
kain putih; cabinet dryer; mesin penepungan dengan ayakan kecil 80
mesh; dan termometer. Sedangkan alat-alat yang digunakan untuk analisis
antara lain :
a. Analisis Kadar Air : gelas ukur, labu destilasi, pipet, alat destilasi.
b. Analisis Kadar Kurkuminoid : spektrofotometer UV-Vis, beker glass,
pipet, gelas ukur, vortex, tabung reaksi.
c. Analisis Antioksidan : spektrofotometer UV-Vis, vial, pipet volume dan vortex.
d. Analisis Total Fenol : erlenmeyer 100 ml, gelas ukur, vortex, tabung
commit to user
C. Tahap Penelitian
Tahapan-tahapan dalam penelitian ini adalah sebagai berikut :
1. Penyiapan Bahan dan Perajangan
Rimpang temulawak yang digunakan berasal dari Batu, Wonogiri
dengan umur rata-rata 10-12 bulan. Rimpang tersebut dicuci sampai
bersih dan dilakukan proses perajangan dengan menggunakan mesin
perajang. Proses perajangan dilakukan untuk mempercepat proses
pengeringan dengan memperluas permukaan bahan. Ketebalan rimpang
temulawak mengacu pada Anonimc (2010) rajangan temulawak biasanya
melintang setebal 2-3 mm.
2. Pengeringan
Proses pengeringan bertujuan untuk mengurangi kadar air yang
terkandung dalam rimpang temulawak. Penghentian proses pengeringan
mengacu pada Cahyono (2007) pada umumnya indikator yang digunakan
oleh para petani dalam memperoleh gambaran mengenai kadar air
simplisia jika simplisia tersebut bisa dipatahkan. Umumnya kadar air
simplisia yang bisa dipatahkan kira-kira antara 10-12%. Proses
pengeringan ini dilakukan dengan beberapa variasi teknik pengeringan
yaitu dijemur alami tanpa kain penutup (kontrol), solar dryer dengan kain
penutup warna putih, cabinet dryer suhu 35oC, cabinet dryer suhu 40oC,
dan cabinet dryer suhu 45oC. Teknik pengeringan ini selain mengacu dari
penelitian terdahulu yaitu penelitian Nugraha (2010), pemilihan suhu
pada cabinet dryer didasarkan pada Hernani dan Rahmawati (2009)
bahwa untuk bahan yang mengandung minyak atsiri, suhu pengeringan
yang terbaik adalah 35-45°C. Dikatakan juga menurut Parahita (2007)
bahan simplisia yang mengandung senyawa aktif dan tidak tahan panas
harus dikeringkan pada suhu serendah mungkin, misalnya 30-45oC.
Pengujian kadar air dilakukan dengan pengambilan sampel secara
acak dengan menggunakan metode thermovolumetri (Sudarmadji dkk,
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
23
3. Analisis senyawa aktif simplisia temulawak
Metode analisis senyawa aktif pada simplisia temulawak dapat
dilihat pada Tabel 3.1.
Tabel 3.1 Metode Analisis Senyawa Aktif Simplisia Temulawak
No Macam uji Metode
1 Kurkuminoid Spektrofotometri (Zahro, 2009 dalam Nugraha, 2010)
2 Total fenol Folin Ciocalteu (Senter et al., 1989 dalam Sundari, 2009)
commit to user
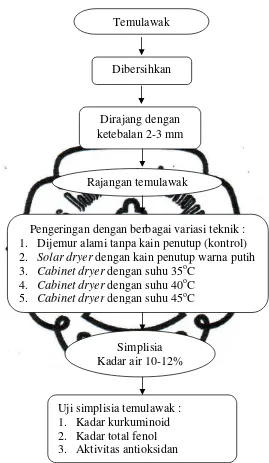
Gambar 3.1 Diagram Alir Penelitian Simplisia Temulawak Rajangan temulawak
Simplisia Kadar air 10-12%
Pengeringan dengan berbagai variasi teknik : 1. Dijemur alami tanpa kain penutup (kontrol)
2. Solar dryer dengan kain penutup warna putih
3. Cabinet dryer dengan suhu 35oC
4. Cabinet dryer dengan suhu 40oC
5. Cabinet dryer dengan suhu 45oC
Uji simplisia temulawak : 1. Kadar kurkuminoid 2. Kadar total fenol 3. Aktivitas antioksidan 4.
Dirajang dengan ketebalan 2-3 mm
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
25
D. Rancangan Penelitian
Dalam penelitian ini digunakan Rancangan Acak Lengkap dengan
menggunakan satu faktor, yaitu variasi teknik pengeringan (dijemur alami
tanpa kain penutup (k), solar dryer dengan kain penutup warna putih, cabinet
dryer suhu 35oC, cabinet dryer suhu 40oC, dan cabinet dryer suhu 45oC ).
Percobaan dilakukan dengan tiga kali pengulangan untuk setiap perlakuan dan
tiga kali pengulangan analisis. Tabel rancangan percobaan Acak Lengkap
dengan satu faktor yaitu variasi teknik pengeringan dapat dilihat pada Tabel
3.2.
Tabel 3.2 Rancangan Percobaan Acak Lengkap dengan Satu Faktor
Percobaan SM SD CD 35oC CD 40oC CD 45oC
1 SM 1 SD 1 CD 35oC 1 CD 40oC 1 CD 45oC 1 2 SM 2 SD 2 CD 35oC 2 CD 40oC 2 CD 45oC 2 3 SM 3 SD 3 CD 35oC 3 CD 40oC 3 CD 45oC 3 Keterangan :
SM = pengeringan sinar matahari tanpa kain penutup (kontrol)
SD = solar dryer dengan kain penutup putih
CD 35oC = cabinet dryer T 35oC CD 40oC = cabinet dryer T 40oC CD 45oC = cabinet dryer T 45oC 1, 2, 3 = ulangan percobaan
Data yang diperoleh dari percobaan selanjutnya dianalisis dengan
menggunakan uji analisis varian (ANOVA). Analisis ini bertujuan untuk
mengetahui ada tidaknya perbedaan pada masing-masing teknik pengeringan
commit to user
26
IV. HASIL DAN PEMBAHASAN
Simplisia temulawak merupakan hasil rajangan temulawak yang telah
dikeringkan. Simplisia temulawak dapat diolah menjadi berbagai macam produk,
seperti serbuk, minyak atsiri, ekstrak kental/ oleoresin, ekstrak kering maupun
kapsul temulawak. Permasalahan yang muncul adalah rendahnya kualitas dan
kontinuitas suplai simplisia temulawak. Hal ini dikarenakan proses pengeringan
yang dilakukan oleh para petani (produsen) masih mengandalkan pada
pengeringan langsung dengan sinar matahari di alam terbuka. Sehingga resiko
terkontaminasi oleh jamur, terganggunya proses pengeringan pada musim hujan,
dan rusaknya kandungan senyawa aktif oleh sinar UV yang cukup tinggi. Melihat
manfaat yang banyak dari penggunaan temulawak sebagai bahan baku industri
dalam bentuk simplisia maka penelitian ini ditujukan untuk mengetahui
kandungan senyawa aktif simplisia temulawak berbagai teknik pengeringan.
Pada pembuatan simplisia temulawak, langkah pertama yaitu rimpang
temulawak setelah dicuci kemudian dirajang dengan ketebalan yang sama yaitu
2-3 mm. Hasil rajangan temulawak dikeringkan dengan berbagai variasi teknik
pengeringan yaitu pengeringan sinar matahari tanpa kain penutup sebagai kontrol,
solar dryer dengan kain penutup warna putih yang merupakan hasil terbaik dari
penelitian sebelumnya (Nugraha, 2010), cabinet dryer suhu 35oC, cabinet dryer
suhu 40oC, dan cabinet dryer suhu 45oC. Pengeringan dihentikan ketika kadar air
telah mencapai 10-12% dengan indikator temulawak mudah dipatahkan
dilanjutkan dengan uji kadar air untuk memastikannya. Setelah itu dilakukan
pengujian kadar kurkuminoid, total fenol dan aktivitas antioksidan simplisia
temulawak dari berbagai teknik pengeringan.
A. Kadar Air
Air merupakan komponen penting dalam bahan makanan karena air
dapat mempengaruhi penampakan, tekstur, serta cita rasa makanan. Semua
bahan mengandung air dalam jumlah yang berbeda-beda, baik itu bahan
makanan hewani maupun nabati. Kandungan air dalam bahan makanan
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
27
pada akhirnya juga akan mempengaruhi mutu bahan pangan tesebut. Kadar air
bahan merupakan jumlah air yang terikat secara fisik dalam bahan sehingga
bahan dapat dinyatakan sebagai suatu material basah atau kering (Siswanto,
2004). Umumnya untuk mengurangi kadar air dalam bahan dilakukan
pengeringan, baik secara alami atau menggunakan alat pengering buatan.
Menurut Riata (2010) pengeringan akan mencegah agar simplisia
tidak berjamur dan kandungan kimia yang berkhasiat tidak berubah karena
proses fermentasi. Adanya air yang masih tersisa dalam simplisia pada kadar
tertentu dapat menjadi media pertumbuhan kapang dan jasad renik lainnya.
Enzim tertentu dalam sel, masih dapat bekerja menguraikan senyawa aktif
sesaat setelah sel mati dan selama bahan simplisia tersebut masih mengandung
kadar air tertentu. Dengan mengurangi kadar air dan menghentikan reaksi
enzimatik melalui pengeringan, dapat mencegah penurunan kualitas atau
kerusakan senyawa aktif simplisia.
Salah satu parameter utama untuk menentukan kualitas simplisia
temulawak adalah dengan menentukan kadar airnya. Dalam penelitian ini uji
kadar air menggunakan metode thermovolumetri (Sudarmadji dkk, 1997)
dengan pengambilan secara acak pada masing-masing sampel. Hasil analisis
kadar air simplisia bubuk temulawak dapat dilihat pada Tabel 4.1
Tabel 4.1 Hasil Analisis Kadar Air Simplisia Temulawak Simplisia
Hasil penelitian menunjukkan kadar air rata-rata simplisia
temulawak dengan 3 kali ulangan yaitu dengan pengering sinar matahari
sebesar 10,83%; dengan solar dryer tanpa kain penutup sebesar 10,33%;
dengan cabinet dryer suhu 35oC sebesar 11,33%; dengan cabinet dryer suhu
40oC sebesar 10,83%; dan dengan cabinet dryer suhu 45oC sebesar 10,00%.
commit to user
dalam penelitian Sembiring, dkk (2006) adalah maksimal 12%. Dari hasil
yang didapat menunjukkan bahwa kadar air simplisia temulawak pada
keseluruhan sampel yang diwakili dari pengambilan sebagian pada
masing-masing sampel kadar airnya kurang dari 12%. Dengan kadar air yang telah
memenuhi standar, dilakukan pengujian terhadap senyawa bioaktif simplisia
temulawak untuk mengetahui efektivitas pengeringan terhadap senyawa
bioaktifnya. Senyawa bioaktif dalam simplisia temulawak akan lebih dapat
dipertahankan dengan teknik pengeringan yang tepat pada standar kadar air
yang sama. Penghentian proses pengeringan berdasarkan pada Cahyono
(2007) bahwa pada umumnya indikator yang digunakan oleh para petani
dalam memperoleh gambaran mengenai kadar air simplisia jika simplisia
tersebut bisa dipatahkan. Umumnya kadar air simplisia yang bisa dipatahkan
antara 10-12%.
B. Kadar Kurkuminoid Simplisia Temulawak Pada Berbagai Teknik
Pengeringan
Salah satu parameter kualitas simplisia temulawak adalah senyawa
aktif dalam temulawak berupa pigmen warna kuning yang disebut
kurkuminoid. Kurkuminoid berbentuk serbuk dengan rasa pahit, larut dalam
aseton, alkohol, asam asetat, dan alkali hidroksida. Bila kurkuminoid terkena
cahaya akan terjadi dekomposisi struktur berupa siklisasi kurkuminoid.
Siklisasi kurkuminoid menyebabkan senyawa kurkuminoid terdegradasi
menjadi asam ferulat sehingga kadarnya dalam ekstrak menjadi rendah (Sidik
dkk., 1995). Oleh karena itu, dibutuhkan teknik pengeringan yang tepat untuk
mempertahankan kurkuminoid dalam temulawak agar tetap memiliki
keaktifan fisiologis. Pada penelitian ini digunakan berbagai teknik
pengeringan dalam menghasilkan simplisia temulawak yaitu pengeringan sinar
matahari tanpa kain penutup (kontrol), solar dryer dengan kain penutup putih,
dan cabinet dryer (35oC, 40oC, dan 45oC). Hasil analisis kadar kurkuminoid
simplisia temulawak dinyatakan dalam persen berat kering/ %db (dry basis).
Kadar kurkuminoid simplisia temulawak dari berbagai teknik pengeringan
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
29
Tabel 4.2. Hasil Analisis Kadar Kurkuminoid Simplisia Temulawak Teknik Pengeringan Kadar Kurkuminoid tinglat signifikansi α 0,05
Dari hasil analisis statistik didapatkan hasil uji kadar kurkuminoid
simplisia temulawak berbeda nyata pada tiap teknik pengeringan yang
ditunjukkan dengan huruf yang berbeda. Simplisia temulawak dengan
pengeringan sinar matahari tanpa kain penutup kadar kurkuminoid yang
didapat sebesar 0,248%, simplisia temulawak yang dikeringkan dengan solar
dryer dan ditutup kain putih kadar kurkuminoidnya sebesar 0,402%.
Sedangkan simplisia temulawak yang dikeringkan dengan cabinet dryer suhu
35oC kadar kurkuminoidnya sebesar 0,323%, cabinet dryer suhu 40oC kadar
kurkuminoidnya sebesar 0,446% dan cabinet dryer suhu 45oC kadar
kurkuminoidnya sebesar 0,495%.
Dari hasil tersebut diperoleh kadar kurkuminoid terendah dihasilkan
oleh simplisia temulawak dengan pengeringan sinar matahari langsung tanpa
kain penutup. Telah disebutkan oleh Sidik dkk. (1995) bahwa bila
kurkuminoid terkena cahaya akan terjadi dekomposisi struktur berupa siklisasi
kurkuminoid, sehingga kadarnya dalam ekstrak menjadi rendah. Siklisasi
kurkuminoid menyebabkan senyawa kurkuminoid terdegradasi. Produk
degradasi kurkumin yang utama adalah asam ferulat, aldehid ferulat,
dehidroksinaftalen, vinilquaikol, vanilin dan asam vanilat (Van der Good,
1995 dalam Kurnia, 2010). Selain itu, pengeringan sinar matahari langsung
sangat dipengaruhi oleh keadaan cuaca sehingga memerlukan waktu yang
relatif lebih lama dibanding dengan pengering buatan. Menurut Hernani dan
Rahmawati (2009) suhu sinar matahari yang sangat bervariasi (35-47oC) juga
commit to user
Pada pengeringan dengan solar dryer ditutup kain putih menghasilkan
kadar kurkuminoid simplisia temulawak yang lebih tinggi dibanding dengan
pengeringan sinar matahari. Fungsi kain penutup putih pada pengeringan
simplisia dengan solar dryer ini adalah untuk melindungi bahan yang
dikeringkan dari panas sinar matahari yang dapat menyebabkan rusaknya
kandungan dalam bahan yang dikeringkan karena kain putih bersifat
memantulkan semua spektrum cahaya termasuk sinar UV yang dapat
mendegradasi kurkuminoid (Yadie, 2009 dalam Nugraha, 2010).
Menurut Yissaluthana (2010) pengeringan bahan makanan dengan solar
dryer lebih efektif karena pemanasan yang terjadi berasal dari dua arah, yaitu
dari sinar matahari secara langsung (radiasi) dan aliran udara panas dari bawah
(konveksi). Pemanasan yang berasal dari dua arah inilah yang mempercepat
proses pengeringan, sehingga didapat kadar kurkuminoid simplisia temulawak
yang dikeringkan dengan solar dryer ditutup kain putih lebih besar atau
dengan kata lain lebih dapat mempertahankan kadar kurkuminoid dibanding
simplisia temulawak yang dikeringkan dengan cabinet dryer suhu 35oC karena
waktu pengeringannya juga lebih singkat. Berdasarkan Susilowati (2010)
penurunan kadar kurkuminoid ekstrak rimpang temulawak semakin besar
seiring lamanya waktu pemanasan walaupun suhu yang digunakan lebih
rendah. Kemungkinan yang sama juga terjadi dalam proses pengeringan
simplisia temulawak. Selama pemanasan, kurkuminoid mengalami degradasi
dan membentuk asam ferulat dan ferulloimetan yang berwarna kuning
kecoklatan (Mohammad dkk., 2007 dalam Susilowati, 2010). Pembentukan
asam ferulat akibat degradasi kurkuminoid menjadikan kadarnya dalam
ekstrak menjadi rendah (Sidik dkk., 1995).
Dari hasil penelitian diperoleh kadar kurkuminoid simplisia temulawak
yang dikeringkan dengan cabinet dryer suhu 45oC lebih besar dibandingkan
kedua suhu di bawahnya dengan alat pengering yang sama. Didapat pula kadar
kurkuminoid tertinggi dari semua teknik pengeringan dihasilkan oleh simplisia
dengan pengeringan cabinet dryer suhu 45oC. Suhu pengeringan sangat
perpustakaan.uns.ac.id digilib.uns.ac.id
commit to user
31
senyawa aktif (Hernani dan Rahmawati, 2009). Dengan menggunakan
pengeringan buatan dapat diperoleh simplisia dengan mutu yang lebih baik
karena pengeringan akan lebih merata dan waktu pengeringan akan lebih
cepat, tanpa dipengaruhi oleh keadaan cuaca (Kiswanto, 2005). Pengeringan
dengan cabinet dryer suhunya lebih stabil dibanding dengan kedua teknik
pengeringan lainnya yang masih bergantung pada panas matahari dan cuaca.
Selain itu, pengeringan dengan cabinet dryer menghindarkan bahan dari
paparan sinar UV matahari yang merupakan salah satu faktor penyebab
kerusakan senyawa aktif terutama kurkuminoid.
Perbandingan kadar kurkuminoid simplisia temulawak pada berbagai
teknik pengeringan dapat dilihat pada Gambar 4.1.
Keterangan :
SM = pengeringan sinar matahari tanpa kain penutup (kontrol)
SD = solar dryer dengan kain penutup putih
CD 35C = cabinet dryer T 35oC CD 40C = cabinet dryer T 40oC CD 45C = cabinet dryer T 45oC
Gambar 4.1 Kadar Kurkuminoid Simplisia Temulawak pada Berbagai Teknik Pengeringan
Dari gambar di atas diperoleh kadar kurkuminoid antara
0,248-0,495%. Hasil yang diperoleh jauh lebih kecil dibanding dengan Parahita
(2007) dimana kadar kurkuminoid dalam temulawak berkisar antara 1-2%.