AKTIVITAS SENYAWA ANTIMIKROBA
Bacillus
sp.
TERHADAP BIOFILM BAKTERI PATOGEN OPORTUNIS
ASAL TAMBAK UDANG INTENSIF
SKRIPSI
Diajukan untuk melengkapi tugas dan memenuhi syarat gelar
Sarjana Sains
YANTI LAMTARULI SIMANULLANG
080805024
DEPARTEMEN BIOLOGI
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMATERA UTARA
i
i DEPARTEMEN BIOLOGI FMIPA USU
PERSETUJUAN
Judul : Aktivitas Senyawa Antimikroba Bacillus sp. Terhadap Biofilm Bakteri Patogen Oportunis Asal Tambak Udang Intensif
Kategori : Skripsi
Nama : Yanti Lamtaruli Simanullang
NIM : 080805024
Program Sudi : Sarjana (S1) Biologi Departemen : Biologi
Fakultas : Matematika Dan Ilmu Pengetahuan Alam (FMIPA) Universitas Sumatera Utara
Disetujui di Medan, Agustus 2014
Komisi Pembimbing :
Pembimbing 2, Pembimbing 1,
Prof. Dr. Erman Munir, M.Sc Dr. It Jamilah, M.Sc
NIP. 19651101 199103 1 002 NIP. 19631012 199103 2 003
Disetujui oleh
Departemen Biologi FMIPA USU Ketua,
Dr. Nursahara Pasaribu, M.Sc NIP. 19630123 199003 2 001
PERNYATAAN
AKTIVITAS SENYAWA ANTIMIKROBA
Bacillus
sp.
TERHADAP BIOFILM BAKTERI PATOGEN OPORTUNIS
ASAL TAMBAK UDANG INTENSIF
SKRIPSI
Saya mengakui bahwa skripsi ini adalah hasil kerja saya sendiri. Kecuali beberapa kutipan dan ringkasan yang masing-masing disebutkan sumbernya.
Medan, Agustus 2014
iii
iii DEPARTEMEN BIOLOGI FMIPA USU
PENGHARGAAN
Puji dan syukur penulis haturkan kepada Tuhan yang Maha Esa atas berkat dan kasihNya sehingga penulis dapat menyelesaikan hasil penelitian yang berjudul
Aktivitas Antimikroba Bacillus sp. Terhadap Biofilm Bakteri Patogen Oportunis Asal Tambak Udang Intensif sebagai syarat untuk melengkapi dan memenuhi syarat mendapatkan gelar Sarjana Sains di Departemen Biologi Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Sumatera Utara.
Terimakasih penulis sampaikan kepada Ibu Dr. It Jamilah. M. Sc selaku dosen Pembimbing I, terima kasih tak terhingga Bu atas kesabarannya selama ini dan juga Bapak Prof. Dr. Erman Munir, M.Sc selaku dosen Pembimbing II yang telah banyak memberikan bimbingan, masukan, dan ilmu dalam penyelesaian skripsi ini,. Ucapan terima kasih juga penulis ucapkan kepada Ibu Dra. Nunuk Priyani, M.Sc selaku penguji dan Kepala Laboratorium mikrobiologi dan Bapak Mizwar Budi Mulya, M.Si selaku Dosen Penguji yang telah banyak memberikan masukan serta saran untuk kesempurnaan penyelesaian skripsi ini. Penulis juga mengucapkan terimakasih kepada Dikti, Departemen Pendidikan Nasional, yang telah mendanai penelitian ini a.n Dr. It Jamilah dibawah Penelitian Hibah Bersaing tahun 2012.
Ucapan syukur yang tak terhingga penulis haturkan kepada Tuhan Yesus atas anugrah dan sukacita yang luar biasa di dalam hidup penulis, Engkau sungguh baik Bapa. Terima kasih kepada Orang tua terkasih Bapak Manullang dan Ibu Pasaribu atas dukungan dalam doa, dana, dan dorongan semangat serta kesabarannya selama ini (aku mencintai kalian). Terima kasih juga untuk adik-adik tercinta Yerni Apriani, Yustri Magdalena, dan Yobert Samuel atas dukungan dan kasih sayangnya. Terima kasih juga untuk Tante-Tante tersayang, Tante Hendri dan Tante Angel atas dukungan semangat dan dana, semoga Tuhan membalas kebaikan kalian semua.
Terima kasih penulis ucapkan kepada kakak sekaligus sahabat Jessica Sarah, SE atas dukungan dalam banyak hal, teman-teman yang luar biasa yaitu Nina, Dessy, Rani, Destri, Indri, serta Sari atas dukungan selama penelitian dan penyelesaian skripsi ini, tanpa bantuan kalian tentunya penyelesaian skripsi ini tidak akan berwarna. Untuk teman-teman Biologi 2008 yang tidak dapat saya sebutkan satu persatu, terima kasih juga atas kerjasamanya selama perkuliahan hingga akhirnya kita masing-masing menyelesaikan masa studi. Terima kasih juga kepada junior Biologi 2009, Adrian Tan, Agustina S,Si, Febrin, S.Si dan Norton Pane untuk tenaga dan bantuannnya selama penelitian di Laboratorium Mikrobiologi, sukses selalu untuk kalian. Terima kasih penulis ucapkan kepada teman-teman IMPERATIF 2008, Ira, Zai, Era, Stef dan Leli, murid-murid penulis, Lia, Vero, dan Rika, Bang Daniel Limbong S.Sn, Josua Silaban serta kakak, abang, dan adik-adik IMPERATIF atas dukungan semangat, semoga kita kelak bisa menjadi pemimpin bagi bangsa Indonesia dan menjadi berkat dimanapun kita berada. Amin
AKTIVITAS SENYAWA ANTIMIKROBA
Bacillus
sp.
TERHADAP BIOFILM BAKTERI PATOGEN OPORTUNIS
ASAL TAMBAK UDANG INTENSIF
ABSTRAK
Bakteri Salmonella sp., Staphylococcus aureus, dan Escherechia coli merupakan patogen oportunistik pada tambak udang dan mampu membentuk biofilm pada permukaan padat. Tujuan penelitian ini ialah untuk mengetahui kemampuan senyawa antimikroba yang dihasilkan Bacillus sp. dalam menghambat pertumbuhan biofilm bakteri patogen oportunistik. Bakteri patogen oportunis diisolasi dari air, sedimen, dan dari permukaan padat menggunakan cotton bud dari tambak udang intensif di beberapa lokasi di provinsi Sumatera Utara. Bakteri patogen oportunis diuji antagonis dengan isolat Bacillus sp. B1, B4, B9, B11, dan B12, untuk melihat kemampuan penghambatan Bacillus sp. Isolat Bacillus sp. B9 mampu menghambat 3 jenis bakteri patogen sedangkan isolat Bacillus sp. B12 mampu melakukan penghambatan terhadap 2 jenis bakteri patogen kecuali Escherechia coli. Pembentukan biofilm bakteri patogen oportunis menggunakan stainless steel sebagai bahan pelekatan, diinkubasi selama 1, 3, dan 6 hari, kemudian direndam dalam 10 ml senyawa antimikroba ekstrak kasar Bacillus sp. dan dihitung jumlah bakteri yang dapat hidup. Sel biofilm untuk Salmonella sp. Dan Staphylococcus aureus bertambah seiring waktu inkubasi, kecuali untuk Escherechia coli yang menurun pada inkubasi hari ke-6. Senyawa antimikroba ekstrak kasar isolat Bacillus sp. B9 dan B12 mampu mengendalikan biofilm bakteri patogen oportunis inkubasi hari ke-6 dengan jumlah penurunan hingga 102-103 CFU/ml dalam waktu 24 jam.
v
v DEPARTEMEN BIOLOGI FMIPA USU
ANTIMICROBIAL COMPOUND ACTIVITY OF
Bacillus
sp.
AGAINTS BIOFILM OF OPPORTUNISTIC PATHOGEN
BACTERIAL ORIGIN INTENSIVE SHRIMP POND
ABSTRACT
Salmonella sp., Staphylococcus aureus, and Escherechia coli are opportunistic pathogenic bacteria found in shrimp ponds and able to form biofilm on solid surfaces. The purpose of this study was to determine the ability of antimicrobial compounds produced by Bacillus sp. in inhibiting the growth of opportunistic pathogenic bacterial biofilms. Opportunistic pathogens bacteria were isolated from water, sediment and from solid surface using cotton swab of intensive shrimp ponds in several location in North Sumatera Province. Opportunistic pathogenic bacteria were antagonist tested against isolates of Bacillus sp. B1, B4, B9, B11, and B12, to see the ability of inhibition of Bacillus sp. Isolate of Bacillus sp. B9 were able to inhibit 3 types of pathogen bacteria, while B12 only able to inhibit two types of pathogenic bacteria, except Escherechia coli. Opportunistic pathogenic bacterial biofilm was form using stainless steel as an attachment surfaces, incubated for 1, 3, and 6 days, then immersed in 10 ml of antimicrobial crude extract and the number of bacteria viability were counted. Biofilm cells increased with time of incubation, except for Escherechia coli that decreased on the 6th day of incubation. The crude extract of antimicrobial compounds of Bacillus sp. B9 and B12 isolates were able to reduce the opportunistic pathogen bacteria biofilm up to 102-103 CFU/ml within 24 hours.
Key words: Bacillus sp., Biofilm, Opportunistic pathogen bacteria, Supernatant.
DAFTAR ISI
Halaman
PERSETUJUAN i
PERNYATAAN ii
PENGHARGAAN iii
ABSTRAK iv
ABSTRACT v
DAFTAR ISI vi
DAFTAR TABEL viii
DAFTAR GAMBAR ix
DAFTAR LAMPIRAN x
BAB 1. PENDAHULUAN
1.1. Latar Belakang 1
1.2. Perumusan Masalah 4
1.3. Tujuan Penelitian 4
1.4. Hipotesis 4
1.5. Manfaat Penelitian 5
BAB 2. TINJAUAN PUSTAKA
2.1. Tambak 6
2.1.1. Sistem Ekstensif 7
2.1.2. Sistem Semi-Ekstensif 7
2.1.3. SistemIntensif 7
2.1.4. Sistem Super Intensif 8
2.2. Perkembangan Ekspor Udang Indonesia 8 2.3. Penyebab Penurunan Ekspor Udang Indonesia 10
2.3.1. Penurunan Kualitas Air 10
2.3.1.1. Padat Penebaran 10
2.3.1.2. Pakan yang Berlebihan 11
2.3.1.3. Akumulasi Bahan Organik 12
2.3.2. Penyakit 12
2.3.2.1. Virus 13
2.3.2.2. Bakteri 13
2.3.3. Penggunaan Antibiotik 14
2.3.4. Patogen Oportunis 15
2.4. Penggunaan Probiotik 16
2.5. Bacillus sp. Sebagai Agen Biokontrol (mikroba probiotik) 17
2.6. Biofilm 18
2.6.1. Beberapa Bakteri yang Mampu Membentuk Biofilm 20
2.6.1.1. Bacillus 20
2.6.1.2. Pseudomonas 21
vii
vii DEPARTEMEN BIOLOGI FMIPA USU
2.6.1.4. Aeromonas 21
2.7. Beberapa Pengaruh Bakteri PatogenTerhadap Kesehatan 22 Manusia
2.7.1. Escherechia coli 22
2.7.2. Salmonella typhi, salmonella paratyphi A, 22 Salmonella paratyphi B, Salmonella paratyphi C
BAB 3. METODE PENELITIAN
3.1. Waktu dan Tempat 24
3.2. Alat dan Bahan 24
3.3. Prosedur Penelitian 24
3.3.1. Pengambilan Sampel Bakteri Patogen Oportunistik 24
3.3.2. Penghitungan Sel Bakteri 25
3.3.3. Pembentukan dan Penghitungan Sel Bakteri 25 3.3.4. Kurva Pertumbuhan Bacillus sp. 26 3.3.5. Uji Tantang Sel Bacillus sp. Terhadap Bakteri Uji 26 3.3.6. Uji Penghambatan Senyawa Antimikroba Ekstrak 26
Kasar Bacillus sp. Terhadap Bakteri Uji
3.3.7. Pengontrolan Sel Biofilm Patogen Oportunistik ` 27 dengan Senyawa Antimikroba Bacillus sp.
BAB 4. HASIL DAN PEMBAHASAN
4.1. Isolasi dan Karakterisasi Bakteri 28
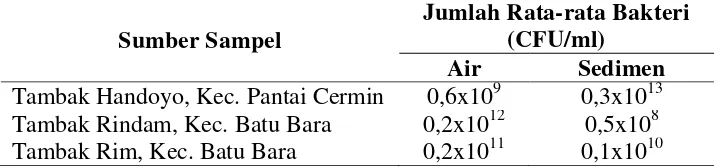
4.1.1. Populasi Bakteri Pada Beberapa Tambak Udang 28 Intensif
4.1.2. Isolasi Bakteri Patogen Oportunistik 29 4.2. Uji Potensi Bacillus sp. Terhadap Bakteri Patogen 31 Oportunistik
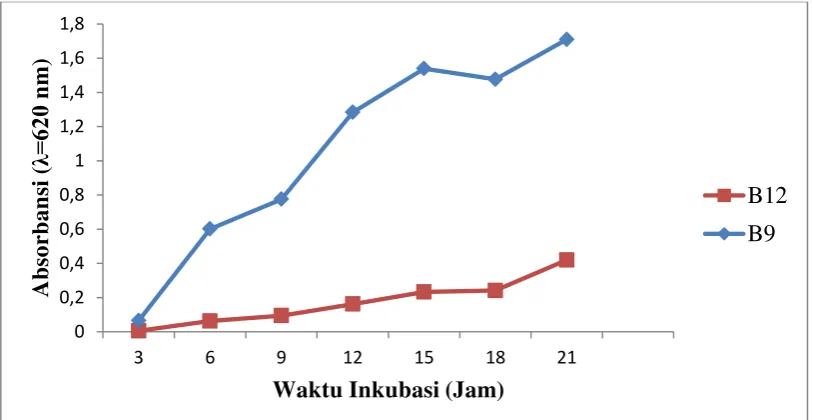
4.3. Kurva Pertumbuhan Bacillus sp. 34
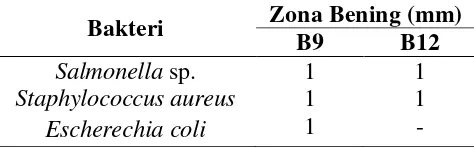
4.4. Jumlah Sel Biofilm Bakteri Patogen Oportunistik 36 4.5. Uji Penghambatan Senyawa Antimikroba Ekstrak Kasar 37
Terhadap Bakteri Patogen Oportunistik dengan Metode Cawan Sebar
4.6. Pengontrolan Sel Biofilm Bakteri Patogen Oportunistik 39 dengan Senyawa Antimikroba
BAB 5. KESIMPULAN DAN SARAN
5.1. Kesimpulan 41
5.2. Saran 42
DAFTAR PUSTAKA 43
LAMPIRAN 50
DAFTAR TABEL
Nomor Judul Halaman Tabel
2.1. Perkembangan Volume Ekspor Udang Tahun 2000-2006 10
4.1. Populasi Bakteri Pada Setiap Tambak 28
4.2.Jumlah Bakteri Patogen Oportunistik Pada Setiap Tambak 30 Udang
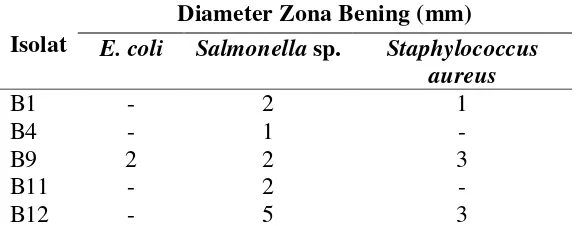
4.3.Aktifitas Penghambatan Isolat Bacillus sp. B1, B4, B9, 32 B11, dan B12 Terhadap Bakteri Uji dengan Metode Cawan
Sebar
4.4.Jumlah Bakteri Pada Stainless Steel Dalam Media 36 Sea Water Complete (SWC) Cair
4.5.Uji Penghambatan Senyawa Antimikroba Terhadap Bakteri 38 Patogen Oportunistik dengan Metode Cawan Sebar
ix
ix DEPARTEMEN BIOLOGI FMIPA USU
DAFTAR GAMBAR
Nomor Judul Halaman
Gambar
4.1. Deteksi Senyawa Antimikroba Bacillus sp. B9 dan B12 33 Terhadap Bakteri Patogen Oportunistik
4.2. Pertumbuhan Bacillus sp. B9 dan B12 Pada Media 34 SWC Cair
DAFTAR LAMPIRAN
Nomor Judul Halaman
Lamp
1. Diagram Alir Penelitian 50
2. Komposisi Media Cair Sea Water Complete (SWC) dan 51 Larutan NaCl 0,9%
3. Alur Kerja Pengambilan dan Penghitungan Sampel Bakteri 52 Patogen Oportunistik
4. Pembentukan dan Penghitungan Sel Biofilm 54
5. Kurva Pertumbuhan Bacillus sp. 55
6. Uji Tantang Sel Bacillus sp. Terhadap Bakteri Uji 56 7. Uji Penghambatan Senyawa Antimikroba Ekstrak Kasar 57
Bacillus sp. Terhadap Bakteri Uji
8. Pengontrolan Sel Biofilm Patogen Oportunistik dengan 58 Senyawa Antimikroba Bacillus sp.
9. Foto Tambak Udang Intensif 59
10. Foto Alat 60
iv
iv DEPARTEMEN BIOLOGI FMIPA USU
AKTIVITAS SENYAWA ANTIMIKROBA
Bacillus
sp.
TERHADAP BIOFILM BAKTERI PATOGEN OPORTUNIS
ASAL TAMBAK UDANG INTENSIF
ABSTRAK
Bakteri Salmonella sp., Staphylococcus aureus, dan Escherechia coli merupakan patogen oportunistik pada tambak udang dan mampu membentuk biofilm pada permukaan padat. Tujuan penelitian ini ialah untuk mengetahui kemampuan senyawa antimikroba yang dihasilkan Bacillus sp. dalam menghambat pertumbuhan biofilm bakteri patogen oportunistik. Bakteri patogen oportunis diisolasi dari air, sedimen, dan dari permukaan padat menggunakan cotton bud dari tambak udang intensif di beberapa lokasi di provinsi Sumatera Utara. Bakteri patogen oportunis diuji antagonis dengan isolat Bacillus sp. B1, B4, B9, B11, dan B12, untuk melihat kemampuan penghambatan Bacillus sp. Isolat Bacillus sp. B9 mampu menghambat 3 jenis bakteri patogen sedangkan isolat Bacillus sp. B12 mampu melakukan penghambatan terhadap 2 jenis bakteri patogen kecuali Escherechia coli. Pembentukan biofilm bakteri patogen oportunis menggunakan stainless steel sebagai bahan pelekatan, diinkubasi selama 1, 3, dan 6 hari, kemudian direndam dalam 10 ml senyawa antimikroba ekstrak kasar Bacillus sp. dan dihitung jumlah bakteri yang dapat hidup. Sel biofilm untuk Salmonella sp. Dan Staphylococcus aureus bertambah seiring waktu inkubasi, kecuali untuk Escherechia coli yang menurun pada inkubasi hari ke-6. Senyawa antimikroba ekstrak kasar isolat Bacillus sp. B9 dan B12 mampu mengendalikan biofilm bakteri patogen oportunis inkubasi hari ke-6 dengan jumlah penurunan hingga 102-103 CFU/ml dalam waktu 24 jam.
Kata kunci: Bacillus sp., Bakteri patogen oportunistik, Biofilm, Supernatan.
ANTIMICROBIAL COMPOUND ACTIVITY OF
Bacillus
sp.
AGAINTS BIOFILM OF OPPORTUNISTIC PATHOGEN
BACTERIAL ORIGIN INTENSIVE SHRIMP POND
ABSTRACT
Salmonella sp., Staphylococcus aureus, and Escherechia coli are opportunistic pathogenic bacteria found in shrimp ponds and able to form biofilm on solid surfaces. The purpose of this study was to determine the ability of antimicrobial compounds produced by Bacillus sp. in inhibiting the growth of opportunistic pathogenic bacterial biofilms. Opportunistic pathogens bacteria were isolated from water, sediment and from solid surface using cotton swab of intensive shrimp ponds in several location in North Sumatera Province. Opportunistic pathogenic bacteria were antagonist tested against isolates of Bacillus sp. B1, B4, B9, B11, and B12, to see the ability of inhibition of Bacillus sp. Isolate of Bacillus sp. B9 were able to inhibit 3 types of pathogen bacteria, while B12 only able to inhibit two types of pathogenic bacteria, except Escherechia coli. Opportunistic pathogenic bacterial biofilm was form using stainless steel as an attachment surfaces, incubated for 1, 3, and 6 days, then immersed in 10 ml of antimicrobial crude extract and the number of bacteria viability were counted. Biofilm cells increased with time of incubation, except for Escherechia coli that decreased on the 6th day of incubation. The crude extract of antimicrobial compounds of Bacillus sp. B9 and B12 isolates were able to reduce the opportunistic pathogen bacteria biofilm up to 102-103 CFU/ml within 24 hours.
DEPARTEMEN BIOLOGI FMIPA USU
BAB 1
PENDAHULUAN
1.1 Latar Belakang
Udang windu (Panaeus monodon) merupakan komoditi ekspor yang penting bagi perekonomian Indonesia. Budi daya udang windu (P. monodon) di Indonesia telah dilakukan sejak tahun 70-an dan sampai sekarang masih merupakan salah satu kegiatan perikanan yang cukup potensial. Usaha budidaya udang windu (P. monodon) berkembang cukup pesat pada tahun 90-an, dimana pada saat tersebut kegiatan budi daya bukan hanya melalui intensifikasi lahan, tetapi juga melalui pembukaan areal hutan bakau menjadi lahan pertambakan (Muliani et al. 2003).
Data yang dihimpun sejak tahun 1984 sampai 1999 menunjukkan produksi udang meningkat lebih dari 6 kali lipat (FAO, 2001). Tahun 1994, produksi udang windu budidaya mencapai 250.000 ton/tahun. Produksi tersebut menempatkan Indonesia sebagai produsen udang windu terbesar di dunia. Namun dengan cepat prosuksi udang windu Indonesia mengalami penurunan dan menuju kehancuran dan sejak tahun 2002, udang vanname mulai menggantikan posisi udang windu (Kordi, 2010). Beberapa kajian diketahui penyebab penurunan produksi budi daya udang adalah merosotnya kualitas lingkungan perairan budidaya yang memicu mewabahnya serangan penyakit (Rukyani, 2000; Harris, 2000).
Salah satu penyebab penurunan kualitas perairan tambak selama operasional adalah tingginya konsentrasi limbah organik dan nutrien sebagai konsekuensi dari sisa pakan dan feses yang terlarut ke dalam air (Boyd et al. 1998; Boyd, 1999; Horowitz, 2000; Montoya & Velasco, 2000). Pencemaran bahan organik di tambak merangsang timbulnya penyakit udang yang disebabkan bakteri patogen dan virus. Dalam ekosistem tambak, tidak semua pakan yang diberikan dimakan oleh udang, sebagian sisa pakan akan tersuspensi di dalam air dan sebagian besar lainnya akan mengendap di dasar tambak. Penguraian bahan organik sisa pakan tersebut akan memerlukan oksigen. Dengan demikian penambahan bahan organik secara langsung akan meningkatkan pengunaan oksigen di lingkungan tambak. Kondisi ini akan terus berjalan sampai titik kritis yang akan menghasilkan ammonia (NH3) dan hidrogen sulfide (H2S) (Isdarmawan, 2005).
Kandungan ammonia di dalam media pemeliharaan berasal dari penguraian bahan organik berkadar nitrogen, baik yang berasal dari feses maupun urin udang. Ammonia NH3 bersifat racun, umumnya dominan pada pH tinggi dan ammonium (NH4+) yang tidak beracun pada pH rendah. Ion ammonium dianggap tidak beracun karena tidak mampu menembus membran sel udang, sebaliknya konsentrasi ammonia yang tinggi dalam air dapat menurunkan permeabilitas membran sel sehingga dapat meracuni udang. Permeabilitas membran sel, menghambat kelancaran ganti kulit serta mengurangi efisiensi pemanfaatan pakan (Patang, 2012).
Bakteri patogen oportunis pada tambak udang ialah bakteri yang ada bukan secara alamiah di perairan tambak, tetapi masuk ke tambak akibat tercemarnya lingkungan dengan limbah manusia. Beberapa diantaranya ialah kelompok koliform, E. coli, Salmonella sp. Staphylococcus aureus (Harish et al. 2003; Hatha et al. 2003). Bakteri patogen oportunistik tidak menyebabkan penyakit pada udang, namun dapat menurunkan kualitas udang ketika diekspor, karena keberadaan bakteri ini tidak diperbolehkan terdapat pada udang ekspor. Berbagai upaya telah dilakukan untuk menanggulangi bakteri patogen pada udang windu (P. Monodon) antara lain dengan menggunakan obat-obatan kimia dan antibiotik. Penanggulangan patogen dengan menggunakan obat-obatan kimia dan antibiotik dapat membawa dampak serius karena masalah residu bahan antibiotik pada udang dan timbulnya resistensi bakteri terhadap antibiotik (Muliani et al. 2003).
Pemakaian antibiotik untuk mengatasi mikroba patogen di tambak udang dapat menimbulkan resistensi pada mikroba sehingga efeknya sangat beresiko terhadap kesehatan udang maupun konsumen. Residu antibiotik yang tinggi pada produk menyebabkan penolakan produk oleh konsumen pengimpor karena tidak lulus persyaratan keamanan yang telah ditetapkan masing-masing negara yaitu Jepang dan Uni Eropa (Putro, 2008). Bacillus sp. merupakan bakteri yang dapat menghasilkan antimikroba (Bintarti, 2008). Beberapa penelitian melaporkan adanya bakteri oportunistik pada perairan tambak udang seperti E. coli, Salmonella, Staphylococcus dan bakteri ini dapat membentuk biofilm. Keberadaan biofilm berdampak pada aspek kesehatan, karena bakteri E. coli, Salmonella, Staphylococcus dapat menyebabkan penyakit pada manusia.
Biofilm merupakan lapisan gel yang terbentuk dari satu atau multispesies mikroorganisme dan matrik yang tersusun tidak beraturan, serta bahan-bahan organik
3
3 DEPARTEMEN BIOLOGI FMIPA USU
bakteri menempel pada permukaan daripada mengapung. Bakteri yang membentuk biofilm memproduksi suatu senyawa yaitu eksopolisakarida (Lappin-Scott et al. 1992). Sel yang membentuk biofilm 10-1000 kali lebih resisten terhadap antimikroba (O‟Toole
et al. 2001). Oleh sebab itu jika biofilm ditemukan pada aliran pemerosesan makanan, pengontrolannya memerlukan usaha yang lebih keras dan teknik-teknik sanitasi yang khusus seperti konsentrasi yang lebih tinggi dari bahan antimikroba, pemakain chlorin, pemanasan yang lebih lama pada suhu tinggi, dan lain-lain. Beberapa kerugian yang disebabkan biofilm diantaranya adalah korosi logam, pertumbuhan pada alat-alat rumah sakit, kontaminasi pada alat pendistribusian air minum, dan menyebabkan lapisan berlendir pada permukaan pemrosesan makanan (Lappin-Scott, 1992).
Pemanfaatan musuh alami pada budi daya perairan merupakan alternatif yang bisa digunakan untuk mengatasi masalah penggunaan antibiotik (Geovany et al. 2007). Menurut Lestari (2007) Bacillus sp. mampu menekan pertumbuhan bakteri patogen pada udang. Bacillus sp. merupakan bakteri Gram-positif yang mampu menghasilkan berbagai jenis zat antimikroba, diantaranya ialah bakteriosin. Zat antimikroba tersebut memiliki efek bakteriosida atau bakteriostatik (Verschuere et al. 2000). Karakterisasi zat antimikroba isolat Bacillus sp. memperlihatkan aktivitas penghambatan terhadap
Escherichia coli, dan Staphylococcus aureus (Bintarti, 2008).
Bacillus sp. hasil penelitian terdahulu (Jamilah et al, 2009; Jamilah & Barus, 2010) telah diuji aktivitas enzim protease dan amilasenya yang berpotensi untuk mereduksi cemaran sisa pakan sehingga meningkatkan kualitas perairan. Namun kemampuan Bacillus sp. ini belum diketahui aktivitas senyawa antimikrobanya dalam mengendalikan biofilm, sehingga penelitian ini penting dilakukan untuk mengetahui kemampuan Bacillus sp. dalam mengontrol sel biofilm patogen oportunistik dalam persiapan isolat ini sebagai kandidat probiotik.
1.2 Perumusan Masalah
Bakteri patogen oportunis di tambak udang seperti E. coli, Salmonella, Staphylococcus aureus dapat membentuk biofilm (Arlyza, 2008), sehingga pengendaliannya perlu terus dilakukan. Oleh sebab itu perlu dilakukan suatu usaha untuk mengetahui pengendalian sel biofilm dengan menggunakan senyawa antimikroba bakteri yaitu dengan melihat aktivitas penghambatan senyawa antimikroba yang dihasilkan isolat
Bacillus sp..
1.3 Tujuan Penelitian
Tujuan dari penelitian ini ialah:
1. untuk mendapatkan isolat bakteri patogen oportunistik asal tambak udang intensif, 2. mengetahui kemampuan bakteri patogen oportunistik yang diisolasi dalam membentuk
biofilm,
3. mengetahui kemampuan senyawa antimikroba Bacillus sp. dalam menghambat pertumbuhan bakteri patogen oportunistik dari tambak udang baik dalam bentuk sel bebas maupun biofilm.
1.4 Hipotesis
Hipotesis dari penelitian ini ialah senyawa antimikroba yang dihasilkan bakteri
Bacillus sp. dapat menghambat pertumbuhan sel biofilm bakteri patogen oportunistik
pada tambak udang.
1.5 Manfaat
Manfaat dari penelitian ini ialah:
1. bagi penulis, bisa menerapkan ilmu pengetahuan yang diperoleh di bangku kuliah untuk menyelesaikan masalah-masalah yang ada yang terjadi di lingkungan sehingga ilmu yang dikuasai tidak hanya bersifat teoritis;
2. bagi kalangan akademik, diharapkan penyusunan skripsi ini nantinya dapat dijadikan sebagai bahan studi serta sebagai bahan pertimbangan untuk penelitian dan pengembangan lebih lanjut;
DEPARTEMEN BIOLOGI FMIPA USU
BAB 2
TINJAUAN PUSTAKA
2.1. Tambak Udang
Sistem budi daya udang di Indonesia berkembang dengan cepat, dari sistem
tradisioanal (ekstensif) menjadi semi-intensif, intensif, dan tambak super intensif.
Sayangnya perkembangan teknologi budi daya udang yang cepat ini tidak
diimbangi dengan kesiapan sumber daya manusia dan cara budi daya udang yang
benar. Teknologi budi daya udang intensif benar-benar hanya berkutat pada
peningkatan padat penebaran yang tinggi, penggunaan pakan berkualitas dan
cukup, serta pengunaan kincir dan pompa air. Budi daya udang intensif hanya
sebatas upaya meningkatkan produksi maupun pembukaan lahan baru untuk
pertambakan. Karena itu, budi daya udang intensif tidak hanya merusak ekosistem
mangrove yang dikonversi menjadi tambak, tetapi meningkatkan pencemaran di
pantai dan munculnya serangan penyakit udang yang merata di seluruh kawasan,
hingga seluruh dunia (Kordi, 2010).
Budi daya udang intensif juga menghasilkan udang yang membawa residu
bahan kimia berbahaya yang tidak baik untuk kesehatan manusia. Penggunaan
bahan kimia berbahaya seperti pestisida anorganik untuk pemberantasan hama
dan penanggulangan penyakit memunculkan masalah baru dalam budi daya
udang. Permasalahan yang menghancurkan industri perudangan Indonesia pada
tahun 1995-1997 itu kemudian memunculkan inovasi-inovasi baru dalam budi
daya udang maupun akuakultur secara umum. Sistem budi daya udang organik,
bandeng organik, polikultur rumput laut, bandeng, dan sebagainya adalah bagian
dari inovasi untuk bertahan dalam usaha budi daya udang. Menurut Kordi (2010)
sistem tambak dapat dibagi menjadi
2.1.1. Sistem ekstensif
Budi daya udang sistem ekstensif atau tradisional masih mendominasi
tambak-tambak rakyat di Indonesia. Sistem ini memang sangat sederhana,
sehingga pengelolaannya tidak rumit namun hasilnya memang sangat rendah,
antara 50-500 kg/ha/musim tebar. Pengelolaannya bergantung pada kemurahan
alam. Tambak berisi beragam spesies udang dan ikan laut. Berkembang lebih
lanjut, tambak tradisional mulai diberi pupuk dan udang di tambak diberi pakan
tambahan secara tidak teratur. Pengelolaan tambak tradisional terus mengalami
perkembangan yang dikenal sebagai tambak tradisional plus, dimana persiapan
tambak sudah dilakukan dengan pengeringan, pengapuran, dan pemupukan.
Penebaran dengan menggunakan benih berukuran seragam dengan kepadatan 8-10
ekor/m2. Pemberian pakan dilakukan tidak teratur. Namun, hasil panen dapat
ditingkatkan hingga mencapai 500-600 kg/ha/musim setelah pemeliharaan 7-8
bulan. Jika predator di tambak dapat dikurangi, maka hasil panen dapat mencapai
700 kg.
2.1.2. Sistem Semi-Intensif
Budi daya udang sistem semi-intensif atau madya merupakan sistem yang
sudah maju. Persiapan tambak mengikuti pola umum yaitu: pengeringan,
pembajakan, pemupukan, dan pengapuran. Padat penaburan antara 15-20 ekor/m2
untuk udang windu dan 25-40 ekor/m2 untuk udang vanname. Untuk pengelolaan
air, tambak dilengkapi dengan pompa air dan kincir. Pemberian pakan dilakukan
secara berkelanjutan sebanyak 2-3 kali sehari. Pakan yang diberikan berupa pelet
yang mengandung protein 30-40%. Udang juga diberi pakan tambahan berupa
udang rebon dan ikan rucah yang dicacah secukupnya. Dengan pengelolaan yang
lebih baik, hasil panen tambak intensif mencapai 2-3 ton/ha/musim.
2.1.3. Sistem Intensif
Budi daya udang secara intensif menerapkan padat penebaran tinggi dan
pengelolaan optimal. Padat penebaran udang windu antara 30-50 ekor/m2 dan
udang vanname antara 40-100 ekor/m2. Pemberian pakan dilakukan 4-6 kali
sehari. Hasil panen yang diharapkan adalah 4-8 ton/ha/musim untuk udang windu
dan 10 ton untuk udang vanname. Perkembangan budi daya udang intensif di
Indonesia dimulai pada akhir tahun 1980-an. Pada awal tahun 1990-an, tambak
intensif di Indonesia sudah menerapkan padat penebaran antara 30-0 ekor/m2.
7
7 DEPARTEMEN BIOLOGI FMIPA USU
pencemaran perairan pantai, penyakit udang, dan rendahnya kelangsungan hidup
(survival rate).
Semakin tinggi padat penebaran makin lambat pertumbuhan udang. Pada
padat penebaran sampai 40.000 ekor/ha belum memerlukan kincir air, padat
penebaran sampai dengan 75.000 ekor/ha cukup 1 kincir air, sedangkan untuk
padat penebaran di atas 30.000 ekor/ha perlu 8-10 unit kincir air/ha. Padat
penebaran rendah umumnya udang tetap sehat dan jarang terserang penyakit.
Sebaliknya pada padat penebaran di atas 300.000/ha, kasus gangguan fisik dan
penyakit sangat tinggi.
2.1.4. Sistem Super Intensif
Sistem super intensif merupakan sistem budi daya yang menerapkan padat
penebaran sangat tinggi. Pada sistem ini udang windu dapat ditebar 50-80
ekor/m2, sedangkan udang vanname antara 100-150 ekor/m2. Hasil panen yang
diharapkan adalah 6-10 ton untuk udang windu dan 12-16 ton untuk udang
vanname. Namun dengan pengelolaan yang optimal, pada udang vanname padat
penebarannya dapat ditingkatkan hingga mencapai 500 ekor/m2. Budi daya udang
super intensif membutuhkan pengelolaan yang super dan penggunaan teknologi
yang memadai. Kontrol kualitas air dilakukan super ketat dengan menggunakan
peralatan-peralatan laboratorium yang maju. Perkerjaan tersebut harus dilakukan
oleh tenaga-tenaga terlatih dan berpengalaman.
2.2. Perkembangan Ekspor Udang Indonesia
Meningkatnya daya beli masyarakat di negara-negara maju mengubah pola
konsumsi bahan pangan ke arah bahan pangan yang lebih bermutu dan bergengsi.
Jika pada awalnya udang tergolong bahan pangan „mewah‟ pada akhirnya dapat
terjangkau oleh masyarakat negara maju. Sehingga kecenderungan peningkatan
permintaan udang di pasaran internasional sudah tampak nyata. Bagi kebanyakan
negara berkembang yang memiliki sumber daya udang, menguatnya harga udang
di pasaran internasional secara langsung mempengaruhi pula jumlah pendapatan
ekspornya. Akrabnya konsumen di negara maju terhadap udang tidak terlepas
pula dari mutu udang itu sendiri (Murty, 1991).
Indonesia pernah mengalami masa kejayaan dalam budi daya udang pada
tahun 1994-an. Tahun 1994, produksi udang windu budi daya mencapai 250.000
ton/tahun. Produksi tersebut menempatkan Indonesia sebagai produsen udang
windu terbesar di dunia. Namun dengan cepat produksi udang windu Indonesia
mengalami penurunan dan menuju pada titik kehancuran (Kordi, 2010).
Jepang dan Amerika Serikat adalah negara pangsa pasar udang terbesar di
dunia. Pemerintah Amerika Serikat memiliki satu badan yaitu FDA (Food and
Drug Administration), dalam upaya melindungi kepentingan konsumen di
negaranya. Peraturan dan pemeriksaan khususnya terhadap produk pangan
terbilang ketat dan tidak pandang bulu. Indonesia pun tak luput dari penahanan
FDA. Pada tanggal 18 Maret 1983, 09 Juni 1983, dan 06 Agustus 1984 Jepang
melakukan penahanan terhadap udang beku karena ditemukannya Vibrio cholera
(Murty, 1991).
Udang yang telah terkontaminasi bakteri patogen jelas tidak memenuhi
persyaratan untuk dikonsumsi. Menurut Murti (1991), apabila kita mengkaji titik
pangkal terjadinya penahanan produk udang yang diproduksi di negara-negara
berkembang, kemungkinan disebabkan oleh:
- penggunaan prasarana dan sarana pengolahan udang yang kurang memenuhi
persyaratan higenis pengolahan;
- penggunaan bahan baku atau bahan oleh udang yang kurang terjamin
kesegarannya;
- faktor lingkungan kerja yang kumuh;
- kurangnya disiplin kerja, seperti sering diabaikannya penggunaan sarung
tangan dan penutup mulut serta hidung.
Untuk mencapai mutu produk hasil perikanan yang dapat diterima secara
internasional, FAO/WHO telah menetapkan syarat-syarat penanganan dan
pengolahan hasil perikanan yang dituangkan dalam Codex Alimentarius. Tujuan
yang sama agar produk perikanan Indonesia dapat diterima di pasaran
internasional, Direktorat Jenderal Perikanan-Departemen Partanian R.I.,
mengeluarkan pula panduan yang disebut Syarat-syarat Teknik dan Higiene
9
9 DEPARTEMEN BIOLOGI FMIPA USU
Tabel 2.1. Perkembangan volume ekspor udang Indonesia tahun 2000-2006 (dalam ton)
Negara
Tujuan 2000 2001 2002 2003 2004 2005 2006
Jepang 54.064 59.559 59.618 60.235 48.623 46.051 50.581
USA 16.216 16.153 16.837 21.901 49.966 50.698 61.235
Uni Eropa 17.833 20.056 16.140 23.689 26.317 27.179 35.232
Sumber: Murty, 1991
Dalam beberapa tahun terakhir ini, nilai ekspor udang di pasar dunia
cenderung mengalami penurunan, karena muncul berbagai hambatan perdagangan
seperti isu dumping, isu lingkungan, serta persyaratan mutu yang dikemas dalam
berbagai macam aturan seperti zero tolerance terhadap residu antibiotik,
Bioterrorism Act, dan Traceability (Putro, 2008).
2.3 Penyebab Penurunan Ekspor Udang Indonesia 2.3.1 Penurunan Kualitas Air
Kualitas air tambak mengalami penurunan disebabkan oleh banyak faktor, baik
faktor internal (di dalam tambak) seperti pengelolaan air, pakan, kepadatan dan
lain-lain, maupun faktor eksternal (di luar) seperti cuaca dan sumber air. Kordi
(2010) mengemukakan beberapa faktor penyebab menurunnya kualitas air.
2.3.1.1. Padat Penebaran
Daya dukung atau mutu lingkungan berpengaruh nyata pada kehidupan
udang yang dimanifestasikan pada kesehatan, pertumbuhan dan kelangsungan
hidup. Kondisi berjejal di dalam tambak yang ditimbulkan oleh padat penebaran
tinggi, berpengaruh nyata pada pertumbuhan, kelangsungan hidup dan kesehatan
udang. Padat penebaran juga berpengaruh nyata dengan penurunan kualitas air.
Semakin tinggi padat penebaran semakain cepat penurunan kualitas air, sehingga
pada tambak yang menerapkan padat penebaran tinggi membutuhkan pengelolaan
kualitas air yang ekstra. Pada tambak tradisioonal yang menerapkan padat
penebaran rendah, kurang dari 5.000 ekor/ha tidak memerlukan pengelolaan air
yang ketat, seperti tidak perlu pegantian air yang sering dan tidak perlu kincir. Di
Indonesia, tambak intensif menerapkan padat penebaran antara 40.000-400.000
benih/ha (udang vanname dapat ditebar 1.000.000-5.000.000 benih/ha), tetapi
tingginya padat penebaran tersebut berbanding lurus dengan mortalitas
(kematian), artinya semakin tinggi padat penebaran, semakin tinggi mortalitasnya.
Mortalitas yang tinggi ini terkait dengan daya dukung tambak, termasuk kualitas
air. Tingginya mortalitas (rendahnya kelangsungan hidup/survival rate) udang
windu dan semakin kecilnya ukuran hasil panen sejalan dengan peningkatan padat
penebaran. Dari segi ekonomi, padat penebaran sekitar 250.000 ekor/ha dianggap
baik, namun tidak boleh melupakan kondisi tambak.
2.3.1.2. Pakan yang Berlebihan
Pengelolaan pakan sangat penting dalam budi daya udang, bukan saja
karena merupakan biaya pengeluaran terbesar (55-70% total biaya produksi),
melainkan juga sangat berpengaruh terhadap kualitas air tambak dan lingkungan
sekitarnya (Cholik et al. 1988 dalam Sudradjat et al. 1998). Menurut Poernomo
(1997) bahwa budi daya udang dengan kepadatan 16 ekor/m2 dan pemberian
pakan 2,5-5% dari bobot biomassa/hari dapat meningkatkan kandungan bahan
organik total dari 10,0 ppm menjadi 29,5 ppm dan ammonia dari 0,7 ppm menjadi
4,5 ppm setelah 14 minggu pemeliharaan. Masukan bahan organik terbesar di
tambak berupa senyawa nitrogen, berasal dari pakan 93%, selebihnya dari pupuk
2% dan bahan lain yang terbawa air dan masuk ke petakan tambak sekitar 5%.
Dengan begitu, pada tambak intensif, kualitas air cepat mengalami penurunan
karena jumlah pakan yang diberikan kepada udang sangat banyak. Kualitas air
cepat mengalami penurunan bila sisa pakan yang tertimbun sangat besar. Bila
penimbunan pakan di dasar tambak tidak segera diantisipasi, maka sebagai bahan
organik akan terjadi proses dekomposisi. Proses dekomposisi membutuhkan
sejumlah besar oksigen. Kebutuhan oksigen ini semakin besar dengan makin
meningkatnya kandungan limbah dari bahan organik (di dalamnya termasuk sisa
pakan) tersebut. Bila suplai oksigen tidak cukup, kondisi anaerobik pada dasar
tambak tak dapat dihindarkan. Tentu ini sangat membahayakan udang budi daya
yang memang sebagian besar aktivitasnya di dasar tambak. Lebih buruk, kondisi
11
11 DEPARTEMEN BIOLOGI FMIPA USU
2.3.1.3. Akumulasi Bahan Organik
Menumpuknya bahan organik pada tambak semi-intensif dan super intensif
memang tidak bisa dihindari. Sisa pakan, kotoran udang, organisme dan plankton
yang mati serta material organik berupa padatan tersuspensi maupun terlarut yang
terangkut lewat pemasukan air (inflow water) merupakan sumber bahan organik di
tambak udang. Input bahan organik ini semakin bertambah sejalan dengan
aktivitas budi daya udang, sebab tuntutan kebutuhan pakan udang mengikuti
pertumbuhan biomassanya. Tentu akumulasi bahan organik ini lebih besar dengan
semakin tingginya padat tebar per luasan tambak. Konsekuensinya, padat tebar
yang tinggi akan menuntut kemampuan manajemen teknis yang tinggi pula di
samping menimbulkan resiko yang lebih besar, terutama karena limbah yang
dihasilkan dari kegiatan budi daya udang tersebut.
Selama ada bahan organik, selama itu pula proses dekomposisi berlangsung.
Bahan-bahan organik kompleks, seperti karbohidrat, protein, dan lemak, oleh
bakteri-bakteri heterotrofik dipecah menjadi senyawa-senyawa yang lebih
sederhana. Tahap berikutnya, senyawa sederhana berupa bahan anorganik oleh
baktri autotrofik dirombak menjadi senyawa-senyawa yang tidak berbahaya lagi
bagi udang. Contohnya, melalui proses nitrifikasi, ammonia (NH3) dioksidasi
menjadi nitrit (NO2) oleh bakteri aerob autotrofik Nitrosomonas, selanjutnya nitrit
dioksidasi menjadi nitrat (NO3) oleh Nitrobacter. Tahap lebih lanjut, nitrat akan
direduksi menjadi unsur N oleh bakteri denitrifikasi lewat proses denitrifikasi.
2.3.2. Penyakit
Penyakit adalah segala sesuatu yang dapat menimbulkan gangguan suatu fungsi
atau struktur dari alat-alat tubuh atau sebagian alat tubuh, baik secara langsung
maupun tidak langsung. Pada prinsipnya penyakit yang menyerang udang budi
daya tidak datang begitu saja, melainkan melalui proses hubungan antara tiga
faktor yaitu kondisi lingkungan (kualitas air), kondisi inang (udang) dan adanya
patogen. Dengan demikian, timbulnya serangan penyakit itu merupakan hasil
interaksi yang tidak seimbang antara lingkungan, inang (udang) dan organisme
penyakit. Interaksi yang tidak serasi ini menyebabkan stress pada udang, sehingga
mekanisme pertahanan diri yang dimilikinya menjadi lemah dan akhirnya mudah
diserang penyakit (Kordi, 2010).
Dalam pembudidayaannya penyakit udang dapat menyerang udang dalam
jumlah besar dan dapat menyebabkan kematian udang, sehingga kerugian yang
ditimbulkannya pun sangat besar. Kerugian yang ditimbulkannya bergantung pada
beberapa faktor, yaitu: (1) umur udang yang sakit (udang yang terserang
penyakit); (2) persentase populasi yang terserang penyakit; (3) parahnya penyakit;
dan (4) adanya infeksi sekunder. Menurut Kordi (2010) beberapa virus dan bakteri
yang menyerang udang adalah
2.3.2.1.Virus
Virus umum yang menyerang udang dan sangat mematikan adalah WSSV
(White Spot Syndrom Virus), IHHNV (Infectious Hypodermal and Hematopoietic
Necrosis Virus), TSV (Taura Syndrom Virus), dan IMV (Infectious Myonecrosis
Virus). Dua virus pertama menyerang udang windu dan udang putih diberbagai
negara Asia, termasuk di Indonesia pada sekitar tahun 1993. Sementara TSV dan
IMV merupakan virus yang masuk ke Indonesia melalui udang vanname. TSV
pertama kali ditemukan tahun 1992 di muara sungai Taura, Guayaquil, Equador.
Virus ini sangat mematikan dan menyerang benih udang di hatchri maupun
tambak pembesaran, dan umunnya terjadi pada akhir ganti kulit tubuh yang
banyak bekas luka yang menghitam. Di Indonesia, TSV pertama kali ditemukan
tahun 2003 di Situbondo, Jawa Timur, sedangkan virus myo masuk ke Indonesia
pda akhir tahun 2006 yang diduga terbawa oleh indukan vanname dari Amerika
Serikat.
2.3.2.2. Bakteri
Bakteri yang ditemukan menyerang udang budi daya antara lain: Vibrio harveyii,
V. parahaemolyticus, V. alginolyticus, V cambelii, V. anguillarum, V.costicola, V.
mimicus, Aeromonas sp., Pseudomonas sp., Mycobacterium sp., Flavobacterium
sp., Filamentous bacteri, Aerococcus viridatus, Acid-fast bacteria, Benekea sp.,
Pasteurella sp., Morella sp., Acromobacter sp., Yersinia sp., dan Leucotrix sp..
13
13 DEPARTEMEN BIOLOGI FMIPA USU
paling berbahaya. Hasil pengamatan menunjukkan bahwa penyakit
kunang-kunang bersifat patogen pada larva bila populasinya mencapai 104 sel/ml. Udang
yang diserang mulai dari fase zoea, mysis, pra larva dan post larva. Stadium
yang paling sensitif terhadap infeksi kunang-kunang adalah stadium zoea.
Sedangkan pada stadium nauplius, larva belum mempunyai saluran pencernaan
dan belum melakukan aktivitas makan, sehingga penyakit kunang-kunang hanya
menempel pada permukaan tubuh.
Udang yang terinfeksi penyakit ini dapat dikenali dari larva kelihatan
menyala apabila diamati pada saat keadaan sekelilingnya gelap terutama malam
hari, keadaan larva lemah, tidak aktif berenang dan nafsu makan berkurang,
terlihat bercak-bercak di bagian badannya. Bagian tubuh udang yang terinfeksi
adalah hepatopankreas. Pada penyerangan tingkat awal, hepatopankreas
mengalami perubahan warna menjadi kecoklatan. Sedangkan pada penyerangan
yang lebih parah, warna berubah menjadi cokelat kehitaman. Serangan
kunang-kunang kini sangat ganas dan terjadi secara cepat, dalam waktu 3 hari dapat
memusnahkan larva. Penyakit kunang-kunang ini resisten terhadap beberapa jenis
antibiotik, seperti Chloramphenciol, Kanamycin, Streptomycin dan Erythromycin.
Sehingga sangat beralasan bila penggunaan antibiotik untuk menekan kasus
kunang-kunang belum ditemukan dosis yang efektif dan ampuh.
2.3.3.Penggunaan Antibiotik
Berbagai usaha penanggulangan penyakit udang telah banyak dilakukan,
diantaranya dengan pemberian antibiotik. Penggunaan antibiotik dalam
penanganan penyakit udang dapat menyebabkan resistensi pada bakteri,
menimbulkan residu antibiotik dan pencemaran lingkungan. Oleh karena itu, perlu
adanya alternatif biokontrol dalam penanggulangan penyakit udang yang bebas
bakteri patogen dan residu antibiotik yang sesuai syarat mutu produk pangan
(Kordi, 2010).
Antibiotik adalah bahan organik yang berasal dari mikroba yang dapat
merupakan racun ataupun dapat menghambat pertumbuhan organisme lain.
Nilainya yang tinggi dalam pengobatan penyakit menular terutama bergantung
pada daya racun yang selektif, yang ditujukan kepada penyebab penyakit, tetapi
tidak kepada inang yang kena infeksi. Penemuan antibiotik adalah empiris, dan
cara tindakannya yang khusus terhadap organisme yang rentan itu baru ditantukan
jauh kemudian. Telah dibuktikan sekarang bahwa banyak golongan antibiotik
memperlihatkan daya racunnya yang selektif itu karena kenyataan bahwa
sasarannya itu ialah sktruktur (atau fungsi) yang khusus baik bagi sel prokariotik
maupun bentuk eukariotik (Stanier et al. 1982).
Sejumlah besar antibiotik menggangu langkah-langkah sintetis protein,
dan banyak yang khususnya menghambat fungsi baik ribosom 70S (khas bagi
prokariota) maupun ribosom 80S (khas bagi eukariota). Akan tetapi, karena
ribosom kloroplast dan mitokondria dalm fungsinya sama dengan ribosom
prokariotik, maka sintesis protein pada organel eukariotik juga dapat dipengaruhi.
Akan tetapi, konsentrasi antibiotik yang diperlukan untuk mempengaruhi kegiatan
mitokondria atau kloroplast itu jauh lebih tinggi daripada yang perlu untuk
menghambat pertumbuhan bakteri, mungkin sekali karena bagian luar membran
organel ini meletakkan penghalang yang sebagian dapat ditembus (Stanier et al.
1982).
2.3.4. Patogen Oportunis
Bakteri patogen oportunis pada tambak udang ialah bakteri yang ada bukan secara
alamiah di perairan tambak, tapi masuk ke tambak akibat tercemarnya lingkungan
dengan limbah manusia. Beberapa diantaranya ialah Coliform, E. coli, Salmonella
sp. Staphylococcus aureus dan Vibrio (Harish et al. 2003; Hatha et al. 2003).
Biasanya bakteri yang menyebabkan kematian pada budidaya udang windu adalah
bakteri genus Vibrio sp. Dan setelah diidentifikasi didapatkan 5 spesies bakteri
Vibrio yakni bakteri V. harveyii, V. mimicus, V. alginolyticus, V.
parahaemolyticus, V. splindidus dari benih yang diperoleh dari panti benih di
Kabupaten Barru pada organ hepatopankreas dan haemolymphnya (Nurjanna,
2003).
Menurut FAO (2010), jalur yang memnungkinkan kontaminasi Salmonella
pada system aquakultur yaitu
15
15 DEPARTEMEN BIOLOGI FMIPA USU
Selama musim penghujan, meningkatkan aliran bahan organik ke dalam kolam
memungkinkan terjadinya kontaminasi ke sistem akukultur
b. Hewan (hewan domestik, katak, hewan pengerat, burung, serangga, reptil, dsb)
Pembuangan beragam hewan berpotensi sebagai sumber Salmonella.
Pembuangan hewan masuk melalui pembuangan burung yang sedang terbang
dan katak yang hidup di sekitar kolam
c. Pemupukan kolam
Pada beberapa sistem akuakultur pupuk hewan digunakan untuk menstimulasi
produksi alga. Penggunaan pupuk non-composted dapat menuju produksi
sistem yang terkontaminasi Salmonella.
d. Point sourcecontamination
Sebagai contoh pelepasan toilet ke dalam kolam atau berintegrasi dengan
sistem peternakan dimana kandang hewan dekat dengan kolam akuakultur.
e. Kontaminasi sumber air
f. Kontaminasi makanan (kondisi yang tidak higenis)
Beberapa bakteri patogen portunis dapat membentuk biofilm bukan saja
pada udang, tempat pemrosesan, maupun pada permukaan substrat di perairan
tambak. Biofilm merupakan sekelompok sel yang dihasilkan oleh bakteri tertentu
yang bersifat tidak dapat berubah dan menutupi permukaan dengan bahan utama
berupa polisakarida (Donlan, 2002). Mikroorganisme merupakan agen utama
yang mengambil tempat di permukaan untuk menghasilkan biofilm (Bishop,
2007). Material non-selular seperti kristal mineral, bahan korosi, tanah liat bahkan
komponen darah dalam lingkungan merupakan tempat berkembangnya biofilm
selain itu juga akan ditemukan matrik biofilm. Biofilm memiliki bentuk yang
beragam dan terdapat pada permukaan merupakan jaringan hidup dan dapat
merusak peralatan kesehatan, industri, pipa saluran air, dan saluran mata air
(Donlan, 2002; Callow & Callow, 2008). Menurut Lens et al. tahun 2003,
terungkap bahwa biofilm memiliki ketahanan terhadap antibakteri, biosida dan
temperatur yang tinggi.
2.4. Penggunaan Probiotik
Probiotik adalah mikroorganisme hidup yang sengaja dimasukkan ke dalam
tmabak udang untuk memberikan efek menguntungkan bagi udang. Tujuannya
adalah memperbaiki dan mempertahankan lingkungan, menekan bakteri
merugikan, menghasilkan enzim yang dapat membantu system pencernaan,
menghasilkan nutrisi yan bermanfaat, serta meningkatkan imunitas (kekebalan)
udang. Istilah lain untuk probiotik antara lain probion, bioremedasi, sistem bakteri
teruus, atau agen mikrobia. Beberapa jenis probiotik yang telah dikenal luas
antara lain Spirulina, Bacillus, Lactobacillus, Alteromonas, Cellulomonas,
Aerobacter, Bifdobacterium, Nitrosomonas, Nitrobacter, Rhodopseudomonas,
Rhodobacter, Rhodococcus, Chromaticeae, Saccharomyces cereviciae,
Tetraselmis, dan Chlorella. Untuk menekan bakteri merugikan dan mencegah
timbulnya senyawa beracun, diperlukan pemberian (inokulasi) bakteri yang
menguntungkan, yaitu probiotik dan pemasangan aerator. Pemberian probiotik
dilakukan dengan dua cara, melalui lingkungan dan pakan. Keduanya mempunyai
tujuan yang berbeda, tetapi intinya memacu pertumbuhan udang (Suprapto, 2007).
Pemberian probiotik melalui lingkungan (air dan dasar tambak) bertujuan:
(a) memperbaiki serta mempertahankan kualitas air tambak, mengoksidasi
senyawa organic sisa pakan, kotoran udang, plankton, dan oranisme yang mati;
(b) menurunkan senyawa metabolit beracun, misalnya ammonia, nitrit, dan H2S;
(c) mempercepat pembentukan dan kestabilan plankton; (d) menekan
pertumbuhan bakteri merugikan; (e) penyedia pakan alami dalam bentuk flok
bakteri; dan (f) menumbuhkan baktri pengurai (Rajab, 2006; Suprapto, 2007).
2.5.Bacillus sp. Sebagai Agen Biokontrol (bakteri probiotik)
Salah satu mikrob probiotik yang banyak diteliti ialah jenis Bacillus. Bacillus
merupakan bakteri Gram-positif berbentuk batang, memiliki endospore, bersifat
motil dan tergolong dalam bakteri aerob atau fakultatif anaerob. Genus Bacillus
merupakan bakteri yang sangat baik digunakan sebagai kandidat agen biokontrol
karena dapat menghasilkan beberapa metabolit aktif seperti antibiotik, proteinase
17
17 DEPARTEMEN BIOLOGI FMIPA USU
Pada tahun 1939, Rene Dubos telah mengisolasi dari tanah New Jersey
suatu kultur Bacillus brevis yang membentuk suatu substansi yang mampu
mematikan banyak bakteri Gram-positif. Ekstrak bebas sel yang diperoleh dari B.
brevis ditemukan mengandung dua bahan aktif, yang sekarang dikenal dengan
nama gramisidin dan tirosidin (Pelczar & Chan, 2005).
Spesies dalam genus Bacillus menghasilkan suatu kelompok antibiotik
yang memiliki banyak sifat biologis dan kimiawi yang sama. Polimiksin
dihasilkan oleh Bacillus polymyxa, sedangkan basitrasin oleh B. subtilis.
Antibiotik-antibiotik ini secara kimiawi digolongkan ke dalam polipeptida.
Polimiksin aktif terhadap banyak bakteri Gram-negatif termasuk Pseudomonas
aeruginosa, yang seringkali menyebabkan infeksi pada saluran kemih atau pada
orang-orang yang menderita luka bakar yang parah. Basitrasin aktif terhadap
bakteri Gram-positif tetapi tidak terhadap Gram-negatif; antibiotik ini sangat
beracun sehingga penggunaannya dibatasi sebagai obat luar saja. Polimiksin juga
beracun bila digunakan secara internal, tetapi telah diformulasi beberapa siapan
yang sesuai untuk penggunaan parenteral, yaitu melalui suntikan subkutan (di
bawah kulit), intravenous (di dalam pembuluh darah) atau intramuscular (di
dalam otot) (Pelczar & Chan, 2005).
Basitrasin menghambat sintesis struktur dinding sel bakteri dan dapat
mempengaruhi integritas membran sitoplasma, sedangkan polimiksin merusak
struktur dinding sel. Antibiotik itu bergabung dengan membrane sel,
menyebabkan disorientasi komponen-komponen lipoprotein serta mencegah
berfungsinya membran sebagai perintang osmotik. Basitrasin indikasi utama
hanya untuk infeksi kulit, terlalu toksik untuk pemakaian parenteral efek samping
(Hare, 1993).
2.6.Biofilm
Molekul organik dan ion inorganik terakumulasi dengan cepat pada permukaan
padat yang teraliri air yang membentuk lapisan yang disebut dengan “conditioning film”. Awal penempelan bakteri pada permukaan secara berkelanjutan melibatkan
bagian dari sel bakteri, flagel atau eksopolisakarida, sementara sel bakteri
berkeliling. Selama sinyal penempelan ulang-balik, bakteri menggunakan
motilitasnya untuk menahan kontak dengan permukaan sambil mencari apakah
lokasi permukaan tersebut tepat. Pencarian ini disebut dengan chemosensoring
jika bakteri lebih memilih substrat spesifik yang tersedia pada permukaan atau
yang diproduksi bakteri lain. Metode translokasi permukaan yang dilakukan
motilitas flagel bakteri disebut dengan mekanisme memposisikan (positioning
mechanism). Motilitas dari flagel memungkinkan Escherechia coli melakukan dua
hal yaitu pendekatan dan berpindah lokasi pada permukaan (Mattila, 2002).
Di alam, biofilm terdiri dari lapisan gel yang terbentuk dari multispesies
mikroorganisme dan matrik yang tersusun secara tidak beraturan serta
bahan-bahan organik yang terperangkap didalamnya yang melekat kuat (irreversibel)
pada suatu permukaan padat. Pelekatan ke suatu material terjadi dengan
menggunakan matrik ekstrasellular (O‟Toole et al. 2001), yang terutama terdiri dari polisakarida. Sel kemudian membelah diri dalam matrik ini untuk
menghasilkan sel anak. Sel anak dapat terlepas dari biofilm, kemudian akan
mengkoloni permukaan dan dapat membentuk biofilm baru jika kondisi makanan
mencukupi (Lappin-Scott, 1992). Dalam kondisi yang diperlakukan di
laboratorium biofilm dapat terbentuk dari satu jenis mikroorganisme (O‟Toole et al. 2001).
Awal penempelan 1 sel bakteri berdasarkan interaksi antara sel dan
substrat. Pertumbuhan selanjutnya dan kematangan biofilm bergantung pada
interaksi antarsel yang disebut dengan co-agregasi. Co-agregasi dapat
didefinisikan sebagai pengenalan dan pelekatan antara bakteri berbeda secara
genetik. Pembentukan kumpulan sel biofilm, co-agregasi, diatur dengan sistem
sinyal diantara sel yang saling berkomunikasi di lokasi yang sama, entah bakteri
tersebut saling berhubungan ataupun tidak. Quorum sensing merupakan sinyal
antarsel, merupakan phenomena yang sangat penting dalam komunitas bakteri.
Hasil penelitian menunjukkan bahwa hal inilah yang mengatur pembentukan
biofilm (Davies et al. 1998; Whitehead et al. 2001).
Sistem Quorum sensing memainkan peranan penting dalam komunitas
biofilm dewasa. Sistem sinyal mengatur transformasi morfologi bakteri ketika
bakteri tersebut menjadi bagian permanen dari biofilm: sintesis pembentukan
19
19 DEPARTEMEN BIOLOGI FMIPA USU
menjadi penyokong dalam memperkuat struktur biofilm. Sel berlokasi pada senter
kerumunan biofilm dan tidak bercabang atau dapat bercabang namun secara
perlahan. Difusi produk bacterial dari sel ke sel lain bertanggangunjawab untuk
komunikasi interselular. Alasan mengapa komunikasi metabolik, seperti quorum
sensing tidak efisien pada plantonik bakteria, adalah karena difusi molekul akan
terbilas air dan hanya sedikit jumlahnya yang mampu ditangkap oleh bakteri
disekitarnya (Matilla, 2002).
Penempelan permanen dari bakteri ada dua tahapan: (1) reversible
attachment, daya tarik transitory phycochemical; dan (2) irreversible attachment,
dimana secara biologis menengahi reaksi stabilisasi. Reversible attachment
berfungsi sebagai atraksi awal dari bakteri terhadap permukaan dan dikontrol
dengan beberapa gaya yang saling bersaing, termasuk didalamnya hidropobik,
elektrostatik, dan gaya Van der Waals. Gaya Van der Waals beratraksi pada
permukaan padat, sedangkan gaya hidropobik dan elektrostatik dapat menjadi
aktif maupun tidak, bergantung pada sifat permukaan bakteri dan permukaan
padat. Sifat permukaan padat dapat dimodifikasi dengan kehadiran conditioning
film dari bahan-bahan organik. Sumber bahan-bahan organik hidropobik
didekomposisi dari material organik, pengeluaran organisme hidup, atau produk
litik dari organisme mati. Bahan organik yang menempel pada permukaan padat
menupakan sumber nutrient bagi bakteri, khususnya pada lingkungan oligotropik
dimana keberadaan nutrisi terbatas. Awal reversible attachment organisme pada
permukaan dapat menjadi permanen. Irreversible attachment diawali dengan
pengeluaran polimer ekstraselular dengan pelekatan bakteri yang reversible.
Polimer ekstraselular menghasilkan matriks yang menyelubungi sel dan
membentuk jembatan ikatan kuat terhadap permukaan padat. Perubahan dari awal
pembentukan hingga kematangan biofilm berhak bukan saja pada
perkembangbiakan penempelan sel namun juga berlanjut memposisikan sel-sel
dari disekitarnya (Maier et al, 2009).
Efek yang ditimbulkan oleh biofilm menyangkut area yang luas yaitu (1)
kehilangan energi dalam unit pemindah panas, (2) korosi logam, (3) pertumbuhan
pada alat-alat rumah sakit, (4) kontaminasi pada alat pendistribusian air minum
dan (5) kontaminasi permukaan alat pemerosesan makanan (Lappin-Scott, 1992).
Meskipun banyak masalah yang ditimbulkan karena keberadaan biofilm, ada
beberapa keuntungan dari pertumbuhan biofilm, seperti aktivasi sludge, trickling
filters atau anaerobic digesters pada industri pengolahan limbah (Matilla, 2002).
2.6.1. Beberapa Bakteri yang Mampu Membentuk Biofilm 2.6.1.1. Bacillus
Bacillus merupakan bakteri mesofilik, erobik, memiliki bentuk spora
ellipsoidal hingga silindris. Peptidoglikan bakteri ini mengandung berbagai variasi
peptide yang terdiri atas asam amino L-Ala-D-Glu-m-Dap-n-Ala, sedang
jembatan terminal tersusun atas D karbon dari m-Dap hingga –COOH dari D-Ala
(Lamanna et al. 1973). Ukuran sel Bacillus vegetatif kurang dari 0,9 µm. hidup
pada pH 6.0 dalam acetyl-methylcarbinol, gelatin terhidrolisis. Bakteri tersebut
menghidrolisis pati dan mereduksi nitrat menjadi nitrit. Dari pengamatan di
bawah mikroskop didapatkan bakteri berbentuk gulungan kusut rantai panjang.
Bakteri tersebut ditemukan bersamaan dengan air yang turun saat hujan ( Burrows
et al. 1968).
2.6.1.2.Pseudomonas
Pseudomonas merupakan bakteri berbentuk batang dan memiliki flagella
polar. Bakteri ini termasuk anggota Gram-negatif aerobik. Memiliki sifat resisten
terhadap antibiotik dan desinfektan. Pseudomonas aeruginosa menghasilkan
ekskret ekstraselular berwarna hijau-biru yang dapat berdifusi ke media. Bakteri
ini banyak ditemukan di tanah dan alam secara umum tidak sehat. Antibiotik dari
kelompok carboxypenicilin, seperti carbenicilin dan ticarcilin memiliki
kemampuan melawan infeksi bakteri ini. Adapun Aminoglycodides berjenis
Gentamicin dapat mencegah sintesis protein bakteri ini dan bersifal bakterisidal
(Tortora et al. 1994).
2.6.1.3. Vibrio
Vibrio merupakan Gram-negatif berbentuk batang-koma (curve-rod)
dengan satu flagella polar. Bakteri ini dapat bertahan di lingkungan laut dan darat
setra berkoloni dalam saluran pencernaan, khususnya usus halus (Purmoko, 2007).
21
21 DEPARTEMEN BIOLOGI FMIPA USU
berasosiasi dengan bakteri Gram-positif. Vibrio harveyii merupakan patogen yang
signifikan pada krustacea, kuda laut dan finfish (Work et al. 2003). Bakteri ini
memiliki autoinducer Nacylated homoserine lactone (OHL) yang merupakan
derivat dari N-(3-hydroxybutanol)-L-homoserine lactone (Hydroxy-BHL).
2.6.1.4. Aeromonas
Aeromonas merupakan bakteri Gram-negatif, anaerobik fakultatif, batang
motil, lurus, kemo-organotrofik diantara metabolism oksidatif dan fermentasi,
sitokrom-oksidase, katalase-positif, mereduksi nitrit menjadi nitrat tanpa
membentuk gas dan resisten terhadap vibriostatik. Tumbuh secara optimal selama
24 jam pada suhu 280C dalam medium TSA, tetapi keseluruhan strain Aeromonas
dapat hidup pada suhu 420C setelah 24-48 jam (Statner et al. 1988; Taylor at al.
1999; Huys et al. 2002). Bakteri ini menghasilkan pigmen terlarut dalam medium
TSA., dan memiliki protein (19-kDa) yang dapat berfungsi sebagai
arginin-hydrolase, lysine decarboxylase, indole. Tidak memproduksi urease, trypthopan
deaminase, ornithine decarboxylase atau H2S. Selain itu, Aeromonas dapat hidup
dalam substrat yang mengandung karbon dan sumber seperti: acetate,
N-acetyl-d-glucosamine, cis-aconitate. Keseluruhan strain resistan terhadap ampicillin,
penicillin, clindamycin, erythromycin, spectynomicin, sulfachloropyridazine,
sulfadimethoxine, tiamulin tilmicosin tylosin tetapi sensitif terhadap kanamycin,
apramycin, ceftiofur, enrofloxacin, gentamycin dan neomycin. Selain itu juga
mempunyai resistensi terhadap nelidixic acid, streptomycin dan tetracycline.
Memproduksi cytotoxin (Hird et al. 1983; Zemelman et al. 1983; Loewy et al.
1993; Huys et al. 2002; Maueal et al. 2002 dan Aydin et al. 2004).
2.7. Beberapa Pengaruh Bakteri Patogen Terhadap Kesehatan Manusia 2.7.1. Escherichia coli
Merupakan basil berbentuk batang pendek (0,004-0,005 µm) tanpa kapsul
atau spora tetapi memiliki flagella sehingga dapat bergerak. Semuanya
Gram-negatif. Organisme ini selalu terdapat di dalam saluran cerna manusia sebagai
flora normal tetapi dapat menyebabkan peritonitis jika isi usus memasuki rongga
peritoneum. Kuman ini juga dapat menyebabkan infeksi kandung kencing dan
pyelonephritis. Galur-galur tertentu dapat menyebabkan gastroenteritis pada anak.
Akhir-akhir ini juga ditemukan bahwa kuman ini bisa mengakibatkan syok
bakterimia karena invasinya yang mendadak ke dalam peredaran darah (Hare,
1993).
2.7.2. Salmonella typhi, salmonella paratyphi A, Salmonella paratyphi B, Salmonella paratyphi C
Dalam gambarannya organisme tersebut tersebut sangat mirip dengan basil
koliform, tetapi beberapa diantaranya tidak memiliki flagella. Tidak satupun
diantaranya yang dapat meragi laktosa. Kuman ini mencapai penderita melalui
makanan, air atau susu dan menyerang jaringan limfoid pada bercak peyer usus
kecil. Setelah kira-kira 12 hari masa inkubasi kuman mencapai peredaran darah.
Pasien segera merasakan sakit disertai demam yang semakin tinggi dan bercak
kemerahan pada kulit yang khas pada tifoid dan paratifoid. Penyebaran abses
dapat terjadi pada hamper setiap bagian tubuh. Yang lebih penting adalah
melemahnya dinding usus pada bercak Peyer sehingga dapat terjadi perforasi ke
dalam rongga peritoneum atau pendarahan akibat pecahnya pembuluh darah
dinding usus. Penyakit ini dapat sembuh dalam waktu 3 minggu atau lebih.
DEPARTEMEN BIOLOGI FMIPA USU
BAB 3
METODE PENELITIAN
3.1. Waktu dan Tempat
Penelitian ini dilaksanakan dari bulan Februari 2012-April 2013, bertempat di Laboratorium Mikrobiologi dan Laboratorium Central Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas Sumatera Utara, Medan.
3.2. Alat dan Bahan
Alat yang digunakan dalam penelitian ini adalah: neraca, water bath shaker, oven, autoklaf, inkubator bakteri, pipet serologi, mikroskop, lemari pendingin, vortex, hot plate, glass bead, stainless steel, sentrifugasi, spektrofotometer, mikro pipet dan tube. Bahan yang digunakan adalah isolat Bacillus sp. (Jamilah et al, 2009; Jamilah & Barus, 2010), bakteri patogen oportunistik, media Eosin Metylen Blue (EMB), Salmonella-Shigella Agar (SSA), Manitol Salt Agar (MSA), Sea Water Complete (SWC) cair dan padat, bufer fosfat 0.2 M, Plate Count Agar (PCA), dan media uji biokimia seperti Sulfide Indole Motility (SIM), Simmon’s Citrat Agar (SCA), Triple Sugar Iron Agar (TSIA),
Starch Agar (SA), dan larutan H2O2 3%.
3.3. Prosedur Penelitian
3.3.1. Pengambilan Sampel Bakteri Patogen Oportunistik
Isolat diisolasi dari tambak udang pada 3 tambak, yaitu Kecamatan Pantai Cermin 1 tambak dan Kecamatan Batubara 2 tambak. Pada lokasi tambak diambil secara random pada salah satu tambak. Sumber isolat diambil dari air, sedimen dan apusan
cotton bud pada permukaan substrat untuk deteksi sel biofilm. Sampel air diambil sebanyak 100 ml dimasukkan ke botol sampel kaca steril. Sedimen bagian paling atas diambil sebanyak 100 g, dimasukkan ke dalam botol sampel. Sampel biofilm bakteri diambil dengan mengoles bahan padat dengan cotton bud steril, permukaan sustrat dibilas sebelumnya dengan aquadest steril untuk menghindari bakteri planktonik. Cotton bud dan sampel bakteri dimasukkan ke tabung reaksi steril dan dimasukkan ke dalam kotak es, di bawa ke laboratorium. Alur kerja isolasi bakteri dapat dilihat pada Lampiran 3 pada halaman 51.
3.3.2. Penghitungan Sel Bakteri
Di laboratorium semua sampel kteri di simpan dalam lemari es (± 4 °C). Dari setiap sampel dibuat pengenceran berseri dalam larutan garam fisiologis 0,9 %, kemudian 0.1 ml larutan disebar pada media PlateCount Agar (PCA) untuk menghitung sel bakteri, kemudian media differensial dan selektif untuk mendapatkan bakteri patogen oportunistik. Isolasi E. coli dengan menyebar 0,1 ml kultur pada media Eosin Metilen Blue (EMB), Salmonella pada Salmonella-Shiegela agar, Staphyloccoccus aureus pada media Manitol Salt Agar. Konsentrasi sel pada masing-masing media selektif dihitung dalam CFU/ml. Isolat dimurnikan melalui penggoresan pada media SWC, kemudian koloni tunggal digores pada media SWC miring dan disimpan dalam lemari es sampai digunakan. Alur kerja penghitungan sel bakteri dapat dilihat pada Lampiran 3 pada halaman 51.
3.3.3. Pembentukan dan Penghitungan Sel Biofilm
Lempeng stainless stell (SS) dipotong seluas 1 cm2, dicuci dengan deterjen (tergazyme) pada bak sonikator kemudian dibilas dengan akuades, disterilkan dengan autoklaf selama 15 menit, tekanan 1 atm, suhu 121°C