Monkeys (Macaca fascicularis) in Acclimation Condition. Cultivated by AGIK SUPRAYOGI and ARYANI SISMIN SATYANINGTIJAS.
This study was aimed to evaluate a blood chemistry profiles especially glucose, cholesterol, triglycerides, SGPT, SGOT, serum urea, and creatinin of long-tailed monkey (Macaca fascicularis) in acclimation condition. Four years old of ten Macaca fascicularis was used in this study. Macaca fascicularis were placed in two rooms which were contained five monkeys with individual cage. This research divided into three stages: adaptation stage for seven days (without temperature and humidity setting), acclimation stage for 14 days (with temperature setting at 25°C temperature and 78% rel. humidity), and post-acclimation stage for 14 days (without temperature and humidity setting). Blood collection was done at the 7th day (adaptation stage); 8th, 11th, 14th, and 21st day (acclimation stage); and 35th day (post-acclimation stage). The results showed that adaptation and post-acclimation stage, the animal model showed signs of stress. Stress in the adaptation stage was indicated by the decreasing in blood glucose, while the stress in the post-acclimation stage was indicated by decreased levels of triglycerides. It could be supposed that temperatur conditions of acclimation stage (25.79 ± 1.16)°C dan (80.19 ± 9.05)% relative humidity is more comfortable for Macaca fascicularis.
MUHAMMAD FARIED HILMY
FAKULTAS KEDOKTERAN HEWAN
INSTITUT PERTANIAN BOGOR
Dengan ini saya menyatakan bahwa skripsi yang berjudul “Profil Kimia Darah Monyet Ekor Panjang (Macaca fascicularis) pada Kondisi Aklimasi” adalah benar merupakan hasil karya sendiri dan belum diajukan dalam bentuk apapun kepada perguruan tinggi manapun. Semua sumber dan informasi yang berasal atau dikutip dari karya yang diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam daftar pustaka di bagian akhir skripsi ini.
Bogor, Maret 2012
Muhammad Faried Hilmy
MUHAMMAD FARIED HILMY. Profil Kimia Darah Monyet Ekor Panjang (Macaca fascicularis) pada Kondisi Aklimasi. Dibimbing oleh AGIK SUPRAYOGI dan ARYANI SISMIN SATYANINGTIJAS.
Penelitian ini bertujuan untuk mengetahui dan mendapatkan profil kimia darah terutama glukosa, kolesterol, trigliserida, SGPT, SGOT, ureum dan kreatinin dalam serum darah monyet ekor panjang (Macaca fascicularis) pada kondisi aklimasi. Pada penelitian ini digunakan sepuluh ekor Macaca fascicularis berjenis kelamin jantan yang berumur kurang lebih empat tahun. Macaca fascicularis kemudian ditempatkan pada dua buah ruangan masing-masing berisi lima ekor dengan masing-masing kandang individu. Penelitian ini dibagi menjadi tiga tahap, yaitu tahap adaptasi selama tujuh hari (tanpa pengaturan suhu dan kelembaban), tahap aklimasi selama 14 hari (dengan pengaturan suhu dan kelembaban) dan tahap postaklimasi selama 14 hari (tanpa pengaturan suhu dan kelembaban). Pengambilan darah dilakukan pada hari ke-7 (tahap adaptasi), hari ke-8, 11, 14, dan 21 (tahap aklimasi), dan hari ke-35 (tahap postaklimasi). Hasil penelitian menunjukkan bahwa pada kondisi adaptasi dan postaklimasi hewan model menunjukkan tanda-tanda stress. Stress pada kondisi adaptasi diindikasikan dengan penurunan glukosa darah, sedangkan stress pada kondisi postaklimasi diindikasikan dengan penurunan kadar trigliserida. Dapat diperkirakan kondisi aklimasi yaitu pada suhu (25,79 ± 1,16)ºC dan kelembaban (80,19 ± 9,05)% rel. humidity merupakan kondisi yang nyaman bagi Macaca fascicularis.
Monkeys (Macaca fascicularis) in Acclimation Condition. Cultivated by AGIK SUPRAYOGI and ARYANI SISMIN SATYANINGTIJAS.
This study was aimed to evaluate a blood chemistry profiles especially glucose, cholesterol, triglycerides, SGPT, SGOT, serum urea, and creatinin of long-tailed monkey (Macaca fascicularis) in acclimation condition. Four years old of ten Macaca fascicularis was used in this study. Macaca fascicularis were placed in two rooms which were contained five monkeys with individual cage. This research divided into three stages: adaptation stage for seven days (without temperature and humidity setting), acclimation stage for 14 days (with temperature setting at 25°C temperature and 78% rel. humidity), and post-acclimation stage for 14 days (without temperature and humidity setting). Blood collection was done at the 7th day (adaptation stage); 8th, 11th, 14th, and 21st day (acclimation stage); and 35th day (post-acclimation stage). The results showed that adaptation and post-acclimation stage, the animal model showed signs of stress. Stress in the adaptation stage was indicated by the decreasing in blood glucose, while the stress in the post-acclimation stage was indicated by decreased levels of triglycerides. It could be supposed that temperatur conditions of acclimation stage (25.79 ± 1.16)°C dan (80.19 ± 9.05)% relative humidity is more comfortable for Macaca fascicularis.
©Hak Cipta milik IPB, tahun 2012
Hak Cipta dilindungi Undang-Undang
Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau menyebutkan sumbernya. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik, atau tinjauan suatu masalah, dan pengutipan tersebut tidak merugikan kepentingan yang wajar IPB.
MUHAMMAD FARIED HILMY
Skripsi
Sebagai salah satu syarat untuk memperoleh gelar Sarjana Kedokteran Hewan pada
Fakultas Kedokteran Hewan
FAKULTAS KEDOKTERAN HEWAN
INSTITUT PERTANIAN BOGOR
NIM : B04060808
Disetujui
Prof. Dr. drh. Agik Suprayogi, M.Sc. AIF Dr. drh. Aryani Sismin S., M.Sc. AIF Pembimbing 1 Pembimbing 2
Diketahui
Drh. Agus Setiyono, MS, Ph.D, APVet Wakil Dekan Fakultas Kedokteran Hewan
Puji syukur penulis panjatkan kehadirat Allah SWT atas Rahmat dan HidayahNya sehingga karya ilmiah ini berhasil diselesaikan. Penelitian ini dimulai bulan Mei sampai Juni 2009 dengan mengambil judul Profil Kimia Darah Monyet Ekor Panjang (Macaca fascicularis) pada Kondisi Aklimasi. Penyelesaian
skripsi ini tidak lepas dari bantuan dari berbagai pihak. Penulis juga mengucapkan terima kasih khususnya kepada PT. LG ELECTRONIC Indonesia yang telah mendukung penelitian ini melalui bentuk kerjasamanya dengan FKH IPB tahun 2009 yang diketuai oleh Prof. Dr. Drh. Agik Suprayogi. M.Sc. AIF. dengan judul Uji Keamanan Pendingin Udara LG Berkhasiat Antinyamuk pada Hewan Model Primata dan Rodentia. Penulis juga mengucapkan terima kasih kepada kedua orangtua, Ahmad Sholeh dan Anifah, serta adik-adikku (M. Afthon Al Fikri, M. Zidni Rizqon A., dan M. Robith Hasymi A.) yang telah memberikan dorongan moral dan doanya. Ucapan terimakasih juga penulis ucapkan kepada:
1. Prof. Dr. Drh. Agik Suprayogi. M.Sc. AIF. dan Dr. Drh. Aryani Sismin S., M.Sc. AIF. selaku pembimbing yang telah memberikan pengarahan dan bimbingan.
2. Prof. Drh. Tutik Wresdiati, MS, Ph.D selaku dosen pembimbing akademik. 3. Pak Joni dan Mas Ari yang telah membantu di kandang.
4. Staf laboratorium Analisis Darah Bagian Fisiologi, Departemen AFF FKH-IPB 5. Sofia Ramadhani atas bantuan, perhatian, semangat, dan dukungannya
6. Teman satu penelitian (Ridzki M. F. Binol, Harlendo Swedianto dan Sutan P. Nasution), Teman-teman Aesculapius 43, IKALUM, serta masih banyak lagi teman-teman yang telah membantu penyelesaian skripsi ini.
Semoga karya ilmiah ini dapat bermanfaat dikemudian hari untuk masyarakat luas.
Bogor, Maret 2012
DAFTAR TABEL ... X
II.1 Ciri-ciri Morfologi Macaca fascicularis ... 4
II.1.1 Klasifikasi dan Morfologi ... 4
II.1.2 Pemanfaatan Macaca fascicularis ... 5
II.1.3 Habitat ... 6
II.2 Parameter Fisiologis Macaca fascicularis ... 8
II.2.1 Glukosa ... 8
II.3.2 Termoregulasi dan Adaptasi Tubuh ... 21
II.3.3 Stres ... 21
III BAHAN DAN METODE ... 23
III.1 Waktu dan Tempat Penelitian ... 23
III.2 Alat dan Bahan Penelitian ... 23
III.3 Persiapan Bahan Penelitian ... 23
III.4 Protokol Penelitian ... 25
IV HASIL DAN PEMBAHASAN ... 27
V SIMPULAN DAN SARAN ... 33
Halaman
1 Prosedur Perlakuan terhadap Hewan Coba ... 26
2 Kadar Glukosa, Kolesterol dan Trigliserida ... 27
Halaman
1 Macaca fascicularis ... 5
2 Peran GPT dan GOT dalam Deaminasi Protein ... 16
3 Kandang Macaca fascicularis yang akan dipergunakan ... 24
4 Makanan yang diberikan berupa pisang ... 24
1.1 Latar Belakang
Monyet ekor panjang (Macaca fascicularis) termasuk ke dalam famili Cercopithecidae merupakan satwa dilindungi menurut CITES Appendik II. Jenis primata ini mempunyai daerah penyebaran yang sangat luas (kosmopolitan). Hal ini disebabkan karena tingginya adaptasi terhadap perubahan lingkungan. Monyet ekor panjang (Macaca fascicularis) merupakan salah satu spesies primata yang sering digunakan sebagai hewan model dalam penelitian bidang kedokteran hewan, kedokteran umum, biologi dan biomedis. Hal ini karena monyet ekor panjang memiliki kedekatan kekerabatan dengan manusia. Selain itu monyet ekor panjang memiliki kemiripan genetik dan fisiologis, kerentanan terhadap penyakit menular dan kemiripan karakteristik reproduksi yang mirip dengan manusia. Hewan percobaan atau hewan laboratorium adalah hewan yang sengaja dipelihara dan diternakkan untuk dipakai sebagai hewan model, dan juga untuk mempelajari dan mengembangkan berbagai macam bidang ilmu dalam skala penelitian atau pengamatan laboratorik. Animal model atau hewan model adalah objek hewan sebagai imitasi (peniruan) manusia (atau spesies lain), yang digunakan untuk menyelidiki fenomena biologis atau patobiologis (Hau and Hoosier Jr., 2003).
Nilai fisiologis monyet ekor panjang sebagai hewan percobaan sangat diperlukan, mengingat data tersebut akan sangat bermanfaat untuk tujuan penelitian maupun diagnosa. Saat ini referensi yang digunakan untuk merujuk nilai fisiologis monyet ekor panjang adalah nilai fisiologis yang berasal dari literatur asing (luar Indonesia). Nilai-nilai tersebut kemungkinan sangat berbeda bila pengukurannya dilakukan pada monyet ekor panjang yang ada di kondisi iklim Indonesia. Penelitian ini diharapkan mampu melengkapi nilai fisiologis monyet ekor panjang yang telah ada untuk membantu para peneliti maupun tenaga medis dalam mendapatkan data yang akurat mengenai nilai fisiologis monyet ekor panjang di Indonesia.
fisiologis primata sebagai hewan model harus dapat diketahui sebagai referensi yang ada di wilayah Indonesia.
Selain adanya pengaruh iklim tropis Indonesia, nilai fisiologis hewan model tersebut juga dipengaruhi oleh kondisi mikroklimat di ruang kandang tempat hewan model tersebut. Kondisi temperatur dan kelembaban ruangan sangat mempengaruhi kondisi fisiologis hewan. Oleh karena itu, dalam pelaksanaan penelitian yang menggunakan hewan model harus diperhatikan mikroklimat ruangan yang mengarah pada nilai zona nyaman bagi hewan tersebut. Pengaturan ruangan pada zona nyaman biasanya diperlukan proses aklimasi hewan tersebut. Aklimasi adalah suatu perubahan kondisi fisiologis organisme untuk mengurangi tekanan yang disebabkan pemberian cekaman secara eksperimental (Kendeigh 1980).
Sampai saat ini belum banyak informasi mengenai nilai fisiologis hewan model sebagai referensi di wilayah tropis, khususnya parameter kimia darah. Di samping itu, belum diketahui bagaimana nilai fisiologis tersebut dalam kondisi adaptasi dan aklimasi. Oleh karena itu perlu dilakukan penelitian untuk mengetahui pengaruh aklimasi di ruang kandang terhadap profil kimia darah monyet ekor panjang sebagai hewan model.
1.2 Tujuan Penelitian
Penelitian ini bertujuan untuk:
1. Mengkaji profil kimia darah terutama kadar glukosa, kolesterol, trigliserida, SGPT, SGOT, ureum dan kreatinin dalam serum darah pada monyet ekor panjang (Macaca fascicularis) pada kondisi aklimasi di ruang kandang. 2. Mendapatkan profil nilai fisiologis kimia darah pada saat Macaca
fascicularis berada pada kondisi adaptasi, aklimasi dan postaklimasi.
2.1Manfaat Penelitian
penelitian maupun praktisi di bidang kedokteran hewan, kedokteran umum, biologi dan biomedis.
2.2Hipotesis Penelitian
Penelitian ini menduga bahwa kondisi aklimasi di ruang laboratorium tidak akan mempengaruhi kadar glukosa, lipid, SGPT, SGOT, ureum dan kreatinin oleh monyet ekor panjang sebagai bahan atau objek penelitian. Hipotesis tersebut dinilai sebagai berikut:
H0 : kondisi aklimasi di ruang laboratorium secara signifikan dapat mempengaruhi kadar glukosa, kolesterol, trigliserida, SGPT, SGOT, ureum dan kreatinin monyet ekor panjang.
II.1 Ciri-ciri Morfologi Macaca fascicularis
II.1.1 Klasifikasi dan Morfologi
Menurut Lang (2006) taksonomi monyet ekor panjang (Macaca
fascicularis) sebagai berikut :
Kelas : Mamalia
Ordo : Primata
Sub Ordo : Anthropoidea
Infra Ordo : Catarrhini
Super Famili : Cercopithecoidea
Famili : Cercopithecidae
Genus : Macaca
Spesies : Macaca fascicularis
Sub Spesies : M. f. atriceps, M. f. aurea, M. f. condorensis, M.
f.fascicularis, M. f. fusca, M. f. karimondjawae, M. f. lasiae, M. f. philipines, M. f. tua, M. f. umbosa.
Monyet ekor panjang sering disebut juga long-tailed macaque, crab eating monkey, dan cinomolgus monkey. Nama lokal monyet ekor panjang di berbagai daerah di Indonesia adalah Cigaq (Minangkabau), Karau (Sumatera), Warik
(Kalimantan), Warek (Dusun), Bedes (Tengger), Ketek (Jawa), Kunyuk (Sunda),
Motak (Madura) dan Belo (Timor) (Supriatna dan Wahyono 2000). Monyet ekor
panjang (Macaca fascicularis) adalah satwa primata yang menggunakan kaki depan dan belakang dalam berbagai variasi untuk berjalan dan berlari
(quandrapedalisme), memiliki ekor yang lebih panjang dari panjang kepala dan badan. Disamping itu memiliki bantalan duduk (ischial sallosity) yang melekat pada tulang duduk (ischial) dan memiliki kantong makanan di pipi (cheek pouches) (Napier and Napier 1985).
Lekagul and McNeely (1988) juga menjelaskan Macaca fascicularis
dinamakan monyet ekor panjang karena memilki ekor yang panjang, dan berkisar
antara 80% hingga 110% dari total panjang kepala dan tubuh. Ukuran panjang
telinga 30-45 mm, bobot 2400-6500 gram (Suyanto, 2002). Monyet ekor panjang
dapat dilihat pada Gambar 1.
Gambar 1. Monyet Ekor Panjang (Macaca fascicularis) Sumber: NBII (2009)
Supriatna dan Wahyono (2000) menyatakan bahwa monyet ekor panjang
(Macaca fascicularis) memiliki panjang tubuh berkisar antara 385 mm hingga 668 mm. Bobot tubuh jantan dewasa berkisar antara 3,5 kg hingga 8,0 kg, sedangkan
bobot tubuh rata-rata betina 3 kg. Smith dan Mangkoewidjojo (1988) menyatakan
bahwa monyet jantan dewasa mempunyai bobot badan berkisar antara 5,5 kg
hingga 10,9 kg dan betina antara 4,3 kg hingga 10,6 kg
Monyet ekor panjang (Macaca fascicularis) mempunyai dua warna utama yaitu coklat keabu-abuan dan kemerah-merahan dengan berbagai variasi warna
menurut musim, umur dan lokasi (Lekagul and McNeely 1988). Napier and
Napier (1985) secara umum menyatakan warna bulu monyet ekor panjang
(Macaca fascicularis) agak kecoklatan sampai abu-abu, pada bagian punggung lebih gelap dibanding dengan bagian perut dan dada, rambut kepalanya pendek
tertarik kebelakang dahi, rambut-rambut sekeliling wajahnya berbentuk jambang
yang lebat, ekornya tertutup bulu halus.
II.1.2 Pemanfaatan Macaca fascicularis
Satwa primata adalah salah satu sumber daya alam yang memiliki peranan
penting dalam kehidupan manusia. Hal ini disebabkan karena secara anatomis dan
dengan hewan model lainnya (Sajuthi et al. 1993). Menurut Sulaksono (2002), bahwa variasi nilai rujukan parameter faal Macaca fascicularis menurut sentra hewan dan jenis kelamin, masih dalam batas yang dapat ditolerir untuk hewan
percobaan yang dipelihara dengan kondisi pemeliharaan konvensional, sehingga
dengan demikian para peneliti Indonesia yang menggunakan kera sebagai model
penelitiannya dapat menggunakan nilai rujukan tersebut sebagai salah satu
referensinya.
II.1.3 Habitat
Pemeliharaan monyet sebagai hewan penelitian harus memenuhi
persyaratan yang telah diatur oleh sebuah komisi kesejahteraan hewan. Menurut
Moss (1992) kesejahteraan dalam arti luas yaitu menyangkut masalah fisik atau
mental dari hewan dan dapat bertingkah laku sesuai dengan kebiasaannya di alam
bebas. Komisi kesejahteraan memperhitungkan keselamatan hewan, orang
disekitarnya dan kemungkinan terjadi kecelakaan kerja. Komisi tersebut
memutuskan yang terbaik bagi hewan yaitu mendapat cukup kebebasan dalam
bergerak tanpa kesulitan berputar, merawat diri, berdiri, berbaring dan
merengangkan badan. Komisi ini juga mempertimbangkan keadaan pakan yang
diberikan. Hewan harus terbebas dari rasa lapar dan haus.
Habitat monyet ekor panjang (Macaca fascicularis) tersebar mulai dari hutan hujan tropika, hutan musim sampai hutan rawa-mangrove, dan di hutan
iklim sedang (Cina dan Jepang) (Napier and Napier 1985). Supriatna dan
Wahyono (2000) menyatakan bahwa monyet ekor panjang (Macaca fascicularis)
hidup pada habitat hutan primer dan sekunder mulai dari dataran rendah sampai
dataran tinggi sekitar 1.000 m di atas permukaan laut. Pada umumnya, habitat asli
Macaca fascicularis selalu berada disepanjang lembah yang berbatasan dengan air, baik di daratan terbuka maupun pinggiran sungai ataupun hutan, sehingga
monyet ekor panjang ini dapat menyesuaikan diri pada semua peringkat ekologi
(Ecologically diverse). Aktivitas fisik monyet ekor panjang ini secara teratur dimulai dari matahari terbit hingga tenggelam lagi, hidupnya berkelompok dengan
jumlah kelompok sekitar 20 – 50 ekor dan selalu berpindah-pindah mengikuti
yang cukup baik bagi kehidupan Macaca fascicularis berkisar diantara 25-27°C. Namun, perubahan suhu yang tidak menentu disaat sekarang ini menyebabkan
kondisi lingkungan bagi Macaca fascicularis tidaklah nyaman serta pakan yang diperoleh dialam juga semakin menipis akibat dari kerusakan alam yang
dilakukan oleh manusia yang tidak bertanggungjawab. Menurut Napier and
Napier (1985), habitat dan penyebarannya ditentukan oleh beberapa hal yang
dibutuhkan untuk bertahan hidup yaitu sumber makanan, sungai atau mata air, dan
pohon untuk tidur dan beristirahat. Keterbatasan sumber makanan dan minuman
menyebabkan kemungkinan adanya daerah tertentu yang merupakan daerah
jelajah dari dua kelompok atau lebih. Perkelahian kelompok sering terjadi untuk
memperebutkan wilayah jelajah tersebut.
Kandang monyet harus dipertimbangkan untuk keperluan tingkah laku,
emosi, dan sosial. Monyet ekor panjang (Macaca fascicularis) tidak boleh dikandangkan sendirian dan terpencil, karena akan menimbulkan suatu bentuk
cekaman yang mengganggu proses tingkah laku dan fisiologi normal (Smith dan
Mangkoewidjojo 1988). Satwa primata harus dikandangkan di ruang atau daerah
sejauh mungkin dari kandang hewan lain. Syarat ini untuk mengurangi resiko
penularan penyakit dan keamanan dalam memelihara (Smith dan Mangkoewidjojo
1988). Kandang monyet harus dibuat dengan konstruksi yang kuat untuk
mencegah terjadinya kerusakan yang disebabkan dari monyet itu sendiri. Jenis
kandang kelompok yang terbuat dari ram kawat perlu dilengkapi tempat
peristirahatan yang agak tinggi dan bentuknya harus memadai. Kandang individu
harus dilengkapi dinding belakang geser (kandang jepit), sehingga monyet dapat
didorong ke bagian depan kandang. Fungsi kandang tersebut untuk mempermudah
dalam melakukan pemeriksaan, pemberian obat atau penyuntikan dan penanganan
lain yang harus dilakukan terhadap monyet tersebut. Setiap jenis kandang baik
kandang kelompok maupun kandang individu harus dilengkapi dengan tempat
II.2 Parameter Fisiologis Macaca fascicularis
II.2.1 Glukosa
Glukosa merupakan hasil akhir dari pencernaan karbohidrat dalam saluran
pencernaan. Fungsi utama karbohidrat adalah sebagai bahan bakar utama untuk
oksidasi dan menyediakan energi untuk proses metabolisme. Bila karbohidrat
yang masuk ke dalam tubuh lebih banyak daripada yang digunakan untuk
menyediakan energi, maka kelebihannya dengan segera akan disimpan dalam
bentuk glikogen yang disimpan dalam hati dan otot. Apabila masih terdapat
kelebihan karbohidrat, maka karbohidrat akan diubah menjadi trigliserida dan
kemudian disimpan di dalam jaringan adiposa (Guyton and Hall 1993).
Jumlah glukosa yang diambil dan dilepaskan oleh hati dan dipergunakan
oleh jaringan-jaringan perifer tergantung dari keseimbangan fisiologis dari
beberapa hormon. Hormon-hormon ini dapat diklasifikasikan sebagai 1) hormon
yang merendahkan kadar glukosa darah yaitu, insulin 2) hormon yang
meningkatkan kadar glukosa darah yaitu, glukagon, epinefrin, glukokortikoid dan
hormon pertumbuhan. Insulin disekresikan oleh sel beta pulau Langherhans
pankreas. Sedangkan hormon yang meningkatkan kadar glukosa darah, antara lain
1) Glukagon yang disekresikan sel alpha pulau Langherhans pankreas, 2)
Epinefrin yang disekresikan oleh medula adrenal dan jaringan kromafin, 3)
Glukokortikoid yang disekresikan oleh korteks adrenal, dan 4) hormon
pertumbuhan yang disekresikan oleh kelenjar hipofisis anterior. Hormon yang
meningkatkan glukosa membentuk suatu mekanisme counter–regulator yang
mencegah timbulnya hipoglikemia akibat pengaruh insulin (Wilson and Price
1995).
Organ hati, jaringan ekstrahepatik dan hormon berperan untuk
mempertahankan kadar glukosa dalam darah agar tetap stabil (Girindra 1988).
Pengaturan konsentrasi gula darah sangat erat hubungannya dengan hormon
insulin dan hormon glukagon yang dihasilkan oleh pankreas. Kecepatan
pengangkutan glukosa juga dengan pengangkutan beberapa monosakarida lain
ditingkatkan oleh insulin, kecepatan pengangkutan glukosa ke dalam sebagian
besar sel meningkat sampai 10 kali lipat atau lebih dibandingkan kecepatan
konsentrasi glukosa darah terhadap sekresi glukagon bertentangan dengan efek
glukosa terhadap insulin. Glukagon adalah hormon yang disekresikan oleh sel
alpha pankreas, apabila konsentrasi gula darah turun sangat rendah, glukagon
merangsang pembentukan siklik AMP terutama di dalam sel-sel hati. Pengaruh
utama glukagon adalah mengubah glikogen hati menjadi glukosa dan
melepaskannya ke dalam darah (Guyton and Hall 1996).
Masuknya glukosa ke dalam darah setelah makan akan meningkatkan kadar
glukosa darah menyebabkan insulin diekskresikan dengan cepat yang
menyebabkan absorb glukosa untuk kemudian disimpan di hati dalam bentuk
glikogen. Mekanisme insulin menurut Guyton and Hall 1993 yang menyebabkan
absorb dan penyimpanan glukosa di dalam hati meliputi:
1. Menghambat fosforilase, enzim yang menyebabkan glikogen hati dipecah menjadi glukosa.
2. Meningkatkan ambilan glukosa dari darah oleh sel-sel hati.
3. Meningkatkan aktivitas enzim yang meningkatkan sintesis glikogen.
Peningkatan kadar glukosa setelah makan menyebabkan peningkatan
pengambilan glukosa oleh hati, otot dan jaringan lemak. Glukosa yang disimpan
di dalam hati nantinya akan dikonversi menjadi asam lemak dan asam lemak ini
diangkut ke dalam jaringan adiposa. Selain dikonversi menjadi asam lemak,
kelebihan glukosa akan ditransportasikan ke dalam sel otot dalam bentuk glikogen
otot. Glikogen otot berbeda dengan glikogen hati karena tidak dapat dikonversi
kembali menjadi glukosa dan dilepaskan ke dalam cairan tubuh (Guyton and Hall
2008). Ketika masuknya proses penyerapan glukosa dari saluran pencernaan
terhenti, maka kadar glukosa darah mulai menurun dan memberi isyarat untuk
mengambil proses kebalikan dari mekanisme sekresi hormon pankreas (Linder
1992). Mekanisme pengaturan glukosa darah menurut Ganong 1999, meliputi :
a. Fungsi hati sebagai buffer glukosa, yaitu apabila glukosa darah meningkat
setelah makan menjadi konsentrasi yang sangat tinggi maka kecepatan
sekresi insulin juga meningkat. Sebanyak duapertiga glukosa diabsorbsi
oleh usus dan segera disimpan dalam hati dalam bentuk glikogen, maka hati
b. Fungsi insulin dan glukagon sebagai umpan balik terpisah dan sangat
penting untuk mempertahankan konsentrasi glukosa darah yang normal.
c. Pada keadaan hipoglikemia efek glukosa darah yang rendah pada
hipotalamus akan merangsang susunan saraf simpatis. Sebaliknya epinefrin
yang disekresikan oleh kelenjar adrenal menyebabkan pelepasan glukosa
lebih lanjut ke hati, hal ini untuk mengatasi hipoglikemia berat.
d. Hormon pertumbuhan dan kortisol disekresikan dalam respon terhadap
hipoglikemia yang berkepanjangan, yang akan menurunkan kecepatan
pengunaan glukosa oleh bagian terbesar sel-sel tubuh.
Kadar glukosa darah adalah suatu indikator klinis dari kurang atau tidaknya
asupan makanan sebagai sumber energi. Faktor yang menentukan kadar glukosa
adalah kesimbangan antara jumlah glukosa yang masuk dan yang dikeluarkan
melalui aliran darah. Hal ini dipengaruhi oleh masuknya makanan, kecepatan
masuk ke dalam sel otot, jaringan lemak dan organ lain serta aktivitas sintesi
glikogen dari glukosa oleh hati (Ganong 1999). Kadar gula darah merupakan
refleksi dari keadaan nutrisi, emosi dan fungsi endokrin (Girindra 1988).
Pada keadaan kadar glukosa dalam darah menurun maka secara bertahap
hati akan mengubah persediaan glikogen menjadi glukosa yang menggantikan
glukosa yang berkurang dalam sirkulasi. Setelah glikogen berkurang, tubuh mulai
mengubah asam-asam amino dari jaringan otot menjadi glukosa dan energi.
Sebelum persediaan asam amino berkurang, tubuh mulai mengurangi lemak yang
tersimpan di dalam jaringan hati menjadi asam lemak. Meski termasuk sumber
energi, asam lemak tidak dapat diubah menjadi glukosa. Hampir semua sel pada
tubuh mampu memetabolisir asam lemak, kecuali sel-sel otak dan sistem saraf
pusat yang hanya mengandalkan glukosa darah. Agar tidak terjadi kekurangan
energi lebih lanjut pada sistem saraf pusat, hati akan mengubah asam lemak
menjadi keton sebagai pengganti glukosa. Biasanya keton mulai diproduksi pada
hari ketiga puasa atau pada saat persediaan sudah sangat berkurang. Begitu kadar
keton dalam darah meningkat (disebut juga ketosis), otak dan organ-organ lain
Kadar glukosa plasma pada suatu saat ditentukan oleh keseimbangan antara
jumlah glukosa yang masuk ke dalam aliran darah dan yang keluar dari aliran
darah. Penentu utama masuknya glukosa ke dalam aliran darah adalah:
a. Diet nutrisi yang masuk.
b. Kecepatan pemasukan ke dalam sel otot, jarigan adiposa dan organ lain.
c. Aktivitas glukostatik hati.
Konsentrasi glukosa darah harus dijaga agar tidak terlalu tinggi karena:
a. Glukosa sangat berpengaruh terhadap tekanan osmotik cairan ekstraseluler
dan apabila meningkat akan menimbulkan dehidrasi selular.
b. Konsentrasi glukosa yang tinggi menyebabkan keluarnya glukosa dari urin.
c. Keadaan di atas menimbulkan dieresis osmotik oleh ginjal, yang dapat
mengurangi jumlah cairan tubuh dan elektrolit yang dapat menimbulkan
berbagai macam penyakit (Guyton and Hall 1996).
Glukagon dengan konsentrasi abnormal yang sangat besar akan
menimbulkan efek, yaitu:
a. Meningkatnya kekuatan jantung.
b. Meningkatnya sekresi empedu.
c. Menghambat sekresi asam lambung (Ganong 1999).
II.2.2 Kolesterol
Lemak atau lipid merupakan senyawa kimia dalam makanan yang terdiri
dari lemak netral (trigliserida), fosfolipid, kolesterol, dan beberapa senyawa lain.
Di dalam tubuh, lemak berfungsi sebagai sumber energi yang efisien ketika
disimpan dalam jaringan adiposa. Sejumlah kecil lemak dapat dicerna di dalam
lambung di bawah pengaruh lipase lambung. Namun, sebagian besar lemak
dicerna di dalam usus halus yang dipengaruhi lipase pankreas. Tahap awal
pencernaan lemak adalah emulsifikasi lemak oleh asam empedu. Kemudian lemak
yang teremulsi tersebut akan dipecah menjadi asam lemak (trigliserida dan
fosfolipid), gliserol, dan gliserida (Guyton and Hall 1993). Lemak di hati
disintesis dari karbohidrat dan protein yang berlebih. Setelah lemak disintesis
dalam hati, lemak ditransport dalam lipoprotein ke seluruh jaringan lemak untuk
Kolesterol diklasifikasikan ke dalam golongan lemak berkomponen alkohol
steroid. Kolesterol sangat larut dalam lemak dan mampu membentuk ester dengan
asam lemak. Hampir 70% kolesterol dalam lipoprotein plasma adalah bentuk ester
kolesterol. Kolesterol diperoleh melalui dua jalur, yaitu eksogen dan endogen
(Guyton and Hall 1997). Kolesterol eksogen yaitu kolesterol yang diperoleh dari
hasil absorbs saluran pencernaan setiap hari. Sedangkan kolesterol endogen
adalah kolesterol yang diperoleh dari hasil pembentukan dalam sel tubuh. Pada
dasarnya kolesterol endogen yang beredar dalam lipoprotein plasma dibentuk
oleh hati, tetapi semua sel lain dalam tubuh juga sedikit membentuk kolesterol.
Sesuai dengan kenyataan bahwa banyak struktur membran sel terbentuk dari
kolesterol. Sebagian kolesterol dalam darah berasal dari hasil sintesis dalam tubuh
kurang lebih 1 gram/hari, sedangkan 0,3 gram/hari diperoleh dari makanan
(Harper et al. 1988; Clarenburgh 2001; Bachorik et al. 2001).
Kolesterol yang bersifat endogen dipengaruhi oleh proses sintesis asam
lemak jenuh, lipoprotein, dan energi yang digunakan. Sedangkan kolesterol
eksogen dipengaruhi oleh konsumsi kolesterol dalam makanan (Sitopoe 1992;
Clarenburgh 2001; Bachorik et al. 2001). Kadar kolesterol juga dipengaruhi oleh faktor individu terhadap kemampuan mensintesis kolesterol serta kemampuan
mensekresi sterol dan garam empedu dari tubuh (Harper et al. 1988; Clarenburgh 2001; Bachorik et al 2001). Dalam tubuh kolesterol diabsorbsi oleh usus dan diangkut oleh kilomikron yang kemudian dibawa ke hati untuk dimetabolisme.
Dalam hati terjadi peristiwa umpan balik negatif untuk mengatur kolesterol tubuh,
bila pemasukan kolesterol dalam diet meningkat maka sintesis menurun, begitu
pula sebaliknya (Guyton and Hall 1997).
Sekitar satu gram kolesterol dieliminasi dari tubuh setiap hari. Kurang lebih
separuhnya akan diekskresikan ke dalam feces setelah dikonversi menjadi asam
empedu, sisanya akan diekskresikan sebagai kolesterol. Sejumlah besar kolesterol
yang disekresikan ke dalam empedu akan direabsorbsi, dan diyakini bahwa
sebagian kolesterol merupakan precursor senyawa sterol feces dari mukosa
intestinal. Koprostanol merupakan sterol utama di dalam feces, senyawa ini
dibentuk dari kolesterol oleh bakteri yang ada di usus besar. Sejumlah besar
kemudian diambil oleh hati untuk diekskresikan kembali ke empedu, keadaan ini
dikenal sebagai sirkulasi enterohepatik. Asam empedu atau derivatnya yang tidak
direabsorbsi akan diekskresikan ke dalam feces (Harper et al. 2003).
Asam empedu primer (asam kolat dan asam kenodeoksikolat) disintesis dari
kolesterol. Reaksi 7α-hidroksilasi pada kolesterol merupakan tahap awal pada
biosintesis asam empedu, dan reaksi ini membatasi laju pada sintesis asam
empedu tersebut. Reaksi tersebut dikatalis oleh enzim mikrosomal yaitu enzim
7α-hidroksilase. Reaksi 7α-hidroksilasi ini memerlukan oksigen, NADPH serta
sitrokom P450. Defisiensi vitamin C akan mengganggu pembentukan asam
empedu pada tahap 7α-hidroksilasi dan menyebabkan akumulasi kolesterol serta
aterosklerosis. Asam empedu primer kemudian akan memasuki getah empedu
sebagai konjugat glisin dan taurin. Karena getah empedu mengandung kalium dan
natrium dalam jumlah cukup besar, maka asam empedu dan konjugatnya akan
membentuk garam empedu. Sebagian asam empedu primer di dalam usus
mengalami beberapa perubahan oleh aktivitas bakteri usus. Perubahan ini meliputi
reaksi dekonjugasi dan 7α-hidroksilasi yang menghasilkan asam empedu
sekunder, yaitu asam deoksikolat dari asam kolat, dan asam litokolat dari asam
kenodeoksikolat (Harper et al 2003).
Kolesterol diedarkan dalam plasma dalam bentuk lipoprotein, dapat pula
dinamakan kompleks antara lipid dengan apoliprotein. Sejumlah kolesterol dalam
makanan dapat diserap dalam berbagai bentuk tergantung dari macam-macam
spesies dan makanan (Clarenburgh 2001). Kolesterol merupakan prekursor
hormon steroid antara lain progesteron, glukokortikoid, mineralokortikoid,
androgen dan estrogen, selain itu kolesterol juga sebagai prekursor asam empedu
dan vitamin D (Harper et al. 1988; Clarenburgh 2001; Bachorik et al. 2001). Kolesterol merupakan pengatur permeabilitas membran untuk mempertahankan
integritas sel tubuh sehingga dapat mencegah penguapan air secara berlebihan
pada permukaan kulit. Selain itu kolesterol adalah pembentuk sel otak dan vitamin
II.2.3Trigliserida
Trigliserida atau lemak netral adalah asam organik hidrokarbon sederhana
berantai panjang. Trigliserida terbentuk dari suatu ester gliserol, dibentuk oleh
reaksi dua molekul asil-lemak-KoA dengan gliserol 3-fosfat membentuk asam
fosfatidat, yang mengalami defosforilasi menjadi diasilgliserol. Sebagian besar
lemak dan minyak di alam terdiri atas 98-99% trigliserida. Molekul ini kemudian
diasilasi oleh molekul ketiga asil-lemak-KoA menjadi triasilgliserol. Apabila
terdapat satu asam lemak dalam ikatan dengan gliserol maka dinamakan
monogliserol. Fungsi utama trigliserida adalah sebagai penyedia energi. Lemak
disimpan di dalam tubuh dalam bentuk trigliserida. Apabila sel membutuhkan
energi, enzim lipase dalam lemak akan memecah trigliserida menjadi gliserol dan
asam lemak serta melepasnya ke pembuluh darah. Oleh sel-sel yang
membutuhkan kemudian dibakar dan menghasilkan energi, karbondioksida dan air
yang menggantikan kehilangan air ketika bernafas (Guyton and Hall 1997;
Clarenburgh 2001; Bachorik et al. 2001).
Oksidasi lemak dapat menghasilkan cukup energi untuk mempertahankan
suhu tubuh, untuk sintesis aktif asam amino dan protein, selain untuk aktivitas lain
yang membutuhkan energi, seperti transport membran. Selain itu, degradasi
trigliserida menjadi glukosa darah, setelah fosforilasi enzimatik menjadi gliserol
fosfat dan oksidasinya menjadi dihidroksi aseton fosfat (Clarenburgh 2001).
Pada hewan normal, biosintesis dan oksidasi trigliserida terjadi bersamaan
dalam keadaan imbang sehingga jumlah lemak dalam tubuh relatif konstan selama
jangka waktu panjang, walaupun mungkin terjadi sedikit perubahan dalam jangka
waktu pendek, bersamaan dengan waktu berfluktuasinya kalori yang terpakai.
Kecepatan biosintesis trigliserida diubah secara drastis oleh aktivitas beberapa
hormon. Insulin contohnya, melangsungkan perubahan karbohidrat menjadi
trigilserida. Trigliserida juga dapat digunakan sebagai cadangan makanan pada
hewan yang tinggal di daerah bersuhu rendah saat hibernasi (Clarenburgh 2001).
Hampir seluruh lemak dari diet, dengan pengecualian asam lemak rantai
pendek, diabsorbsi dari usus ke dalam limfe. Selama pencernaan sebagian besar
trigliserida dipecah menjadi monogliserida dan asam lemak. Kemudian sewaktu
baru yang berkumpul dan masuk ke dalam limfe dalam bentuk droplet kecil yang
tersebar yang disebut kilomikron (Guyton and Hall 1997).
II.2.4 SGPT (Serum Glutamat Piruvat Transminase) dan SGOT (Serum Glutamat Oksaloasetat Transminase)
Aspartate aminotransferase (AST atau SGOT) dan alanine aminotransferase
(ALT atau SGPT) adalah enzim-enzim hati yang paling sensitif dan digunakan
secara luas mendeteksi kerusakan hati. AST (SGOT) normalnya ditemukan dalam
suatu keanekaragaman dari jaringan termasuk hati, jantung, otot, ginjal, dan otak.
SGOT dilepaskan kedalam serum ketika satu saja dari jaringan-jaringan ini
rusak. ALT (SGPT) normalnya ditemukan sebagian besar di hati. SGPT dilepas
ke dalam aliran darah sebagai akibat dari kerusakan hati. Oleh karenanya SGPT
digunakan sebagai suatu indikator yang cukup spesifik dari keadaan (status) hati
(Guyton dan Hall 1997).
SGPT dan SGOT merupakan dua enzim transminase yang dihasilkan
terutama oleh sel-sel hati. Bila sel-sel hati rusak, biasanya kadar kedua enzim
meningkat. Batasan normal SGOT adalah 5 sampai 40 unit per liter serum (bagian
cair dari darah). Sedangkan batasan normal SGPT adalah 7 sampai 56 unit per
liter serum. Enzim SGPT berperan dalam deaminasi asam amino, pengeluaran
gugus amino dari asam amino (Guyton dan Hall 1997; Hayes 2007). SGPT akan
memindahkan gugus amino pada alanin ke gugus keton dari α-ketoglutarat
membentuk glutamat dan piruvat. Selanjutnya piruvat akan diubah menjadi laktat.
Reaksi tersebut dikatalisasi oleh enzim laktat dehidrogenase (LDH) yang
membutuhkan NADH dalam reaksi yang dikatalisasinya. SGOT juga berperan
dalam deaminasi asam amino, SGOT mengkatalisasi pemindahan gugus amino
pada aspartat ke gugus keton dari α-ketoglutarat membentuk glutamat dan
oksaloasetat dan selanjutnya oksaloasetat diubah menjadi malat. Reaksi tersebut
dikatalisasi oleh enzim malat dehidrogenase (MDH) yang membutuhkan NADH
dalam reaksi ini (Poedjiadi 1994). Secara normal organ mengalami regenerasi sel,
termasuk hati. Pada keadaan ini sel yang telah rusak digantikan oleh sel yang
baru, jadi pada keadaan normal, keberadaan SGPT dalam darah itu normal, hal
Gambar 2. Peran GPT dan GOT dalam Deaminasi Protein Sumber: Poedjiadi (1994)
Adanya kerusakan sel-sel parenkim hati atau permeabilitas membran akan
mengakibatkan enzim GOT dan GPT, arginase, laktat dehidrogenase, dan γ
-glutamil transminase bebas keluar sel, sehingga enzim masuk ke pembuluh darah
melebihi keadaan normal dan kadarnya dalam darah meningkat (Girindra 1986).
Namun demikian, indikator yang lebih baik untuk mendeteksi kerusakan jaringan
hati adalah SGPT dan SGOT, karena kedua enzim tresebut akan meningkat
terlebih dahulu dan peningkatannya lebih drastis dibanding enzim-enzim lainnya
(Amin 1995; Callbreath 1992). Oleh karena itu melalui hasil tes laboratorium,
keduanya dianggap memberi gambaran adanya gangguan pada hati (Girindra
1986).
Oleh karena itu menurut pemaparan di atas faktor yang erat kaitannya
dengan perubahan kadar SGPT dan SGOT yaitu laju metabolisme protein, dan
laju regenerasi sel, yang mungkin diantaranya dapat dipengaruhi oleh tingkat
aktivitas fisik (Girindra 1986, Suarsana et al. 2006).
II.2.5 Ureum
Ureum merupakan hasil akhir dari metabolisme protein dalam tubuh.
Senyawa-senyawa ini harus dikeluarkan dari dalam tubuh secara terus-menerus
untuk memastikan terus berlangsungnya metabolisme protein dalam sel (Price
2005). Ureum dihidrolisis di dalam air dengan bantuan urease sehingga dihasilkan
amonia dan CO2 (Guyton and Hall 1997). Kadar ureum dalam darah bergantung
ginjal dan diekskresikan melalui urin. Ketika air direabsorbsi dari tubulus,
konsentrasi ureum dalam tubulus akan meningkat sehingga muncul gradien
konsentrasi yang menyebabkan reabsorbsi urea. Ureum tidak bisa memasuki
tubulus sebanyak air, sehingga ureum direabsorbsi secara pasif dari tubulus.
Ureum yang masih tertinggal akan masuk ke dalam urin untuk akhirnya
diekskresikan (Raphael 1987). Ureum dengan kadar tinggi dalam tubuh akan
bersifat toksik karena sifatnya yang mendenaturasikan protein (Doxey 1983).
Ginjal adalah organ ekskresi utama dalam tubuh yang terletak pada dinding
posterior abdomen di luar rongga peritonium. Ginjal memiliki tiga bagian utama
yaitu, korteks (bagian luar), medulla, dan pelvis renalis (Guyton 1995). Menurut
Price 2005, ginjal merupakan organ penyaring plasma dan unsur-unsur plasma
darah, secara selektif ginjal menyerap kembali air dan unsur-unsur berguna dari
filtrat kemudian mengekskresi kelebihan dan produk buangan plasma. Menurut
Raphael 1987, pembentukan urin dimulai dengan proses filtrasi glomerulus
plasma. Aliran plasma ginjal kira-kira 660 ml/menit yang setara dengan sekitar
25% curah jantung. Seperlima dari plasma dialirkan melalui glomerulus ke
kapsula Bowman yang dikenal sebagai laju filtrasi glomerulus. Sel-sel darah dan
molekul-molekul protein yang besar atau bermuatan negatif secara efektif tertahan
oleh seleksi glomerulus, sedangkan molekul berukuran kecil atau bermuatan
positif langsung tersaring. Saat filtrat mengalir melalui tubulus ada beberapa zat
yang diambil atau ditambahkan ke dalam filtrat sehingga hanya sekitar 1,5 L/hari
yang diekskresikan sebagai urin.
Ginjal memiliki fungsi yang multipel antara lain sebagai pengatur
keseimbangan air dan elektrolit, pengatur konsentrasi osmolitas cairan tubuh,
pangatur keseimbangan asam basa, ekskresi produk sisa metabolik dan bahan
kimia asing, dan sekresi hormon (Ganong 2003). Guyton 1995 menyebutkan
bahwa efek dari gagal ginjal akut atau kronis secara umum dapat berupa edema
umum, asidosis, tingginya konsentrasi nitrogen non-protein terutama urea, dan
tingginya konsentrasi produk retensi urin lainnya, termasuk kreatinin, asam urat,
fenol, basa guanidine, sulfat, fosfat dan kalium. Maka dari itu sangat penting
pemeriksaan laboratorium ginjal antara lain pemeriksaan kadar kreatinin dan
ureum dalam serum darah (Raphael 1987).
Ureum selain direabsorbsi secara pasif dari tubulus ternyata juga diabsorbsi
ke medulla ginjal dan berperan terhadap 40% osmolaritas interstisium medulla
ginjal saat ginjal membentuk urin pekat secara maksimal (Guyton 1995).
Mekanisme reabsorbsi ureum ke medulla ginjal, yaitu air mengalir ke cabang
asenden ansa Henle dan masuk ke tubulus distal dan tubulus koligentes kortikalis
hanya sedikit ureum yang direabsorbsi karena segmen ini impermiabel terhadap
ureum. Dengan tingginya konsentrasi ADH, air direabsorbsi secara cepat dari
tubulus koligentes kortikalis dan konsentrasi ureum juga meningkat dengan cepat.
Selanjutnya, cairan tubulus mengalir ke bagian medulla duktus koligentes
sehingga konsentrasi ureum semakin tinggi dan berdifusi ke interstitium ginjal
dan pada akhirnya konsentrasi ureum dalam urin tetap tinggi meskipun sebagian
telah direabsorbsi. Hal ini meyebabkan kadar ureum normal sangat tinggi dalam
urin sedangkan dalam darah kebalikannya (Price 2005). Ureum merupakan
produk ekskresi primer dari katabolisme protein yang dibentuk di hati dengan
bahan dari amonia dan CO2 melalui proses biokimia yang dikenal dengan siklus
Ornithin (Raphael 1987). Gangguan ginjal kronik akan menyebabkan penurunan
laju filtrasi glomerulus (fungsi penyaringan ginjal) sehingga kemampuan ginjal
menyaring ureum maupun kreatinin juga menurun, akibatnya zat-zat tersebut
meningakt jumlahnya dalam darah (Doxey 1983).
II.2.6 Kreatinin
Kreatinin adalah produk endogenous akhir dari metabolisme kreatin fosfat
yang terjadi di dalam otot dan dilepaskan dari otot dengan kecepatan yang hampir
konstan serta diekskresikan dalam urin dengan kecepatan yang sama (Guyton and
Hall 1997). Ekskresi kreatinin pada setiap individu terkait erat dengan ukuran
jaringan otot. Zat ini dijumpai dalam jumlah yang besar di otot dan hadir di darah
dan urin dalam jumlah yang sangat kecil dalam kondisi normal.
Melalui reaksi dehidrasi dalam otot kreatin akan diubah menjadi kreatinin
yang mudah diperfusi ke seluruh cairan tubuh dan diekskresikan melalui urin
keberadaannya dalam tubuh dengan jumlah yang tinggi ataupun rendah dapat
memberi dampak buruk bagi tubuh. Peningkatan kadar kreatinin dapat
mengakibatkan gagal ginjal akut dan kronis, nekrosis tubular akut,
glomerulonefritis, dehidrasi, penurunan aliran darah ke ginjal (syok
berkepanjangan, gagal jantung kongestif), leukemia. Kreatinin dalam jumlah
rendah dapat mengakibatkan distrofi otot dan myasthenia gravis. (Riswanto
2010). Sisa metabolisme harus diekskresikan melalui ginjal, oleh karena itu jika
terjadi peningkatan atau penurunan kadar kreatinin dalam tubuh maka interpretasi
klinik akan cenderung pada gangguan fungsi ginjal.
Kreatinin diekskresi dalam urin melalui proses filtrasi dalam glomerulus
tetapi tidak direabsorbsi di tubulus bahkan sejumlah kecil disekresi oleh tubulus
terutama bila kadar kreatinin dalam serum tinggi (Todd and Sanford 2008).
Kreatinin dengan bebas melintasi membran glomerulus dan hanya sebagian kecil
disekresi ke dalam tubulus nefron. Kreatinin merupakan indeks GFR yang lebih
cermat dibandingkan ureum karena kecepatan produksinya sedkit sekali
mengalami perubahan daalm massa otot. Oleh karena itu, pada kondisi normal
kreatinin dijumpai dalam urin dengan konsentrasi sedikit. Konsentrasi dan
ekskresi total harian kreatinin tetap konstan meskipun ada perubahan pola
makanan (Frandson 1992).
Selain faktor diet, faktor katabolik, jenis kelamin dan aktivitas juga
diketahui tidak berpengaruh signifikan terhadap jumlah kreatinin dalam plasma.
Akan tetapi kadang dijumpai bahwa kadar kreatinin dalam plasma hewan yang
masih muda lebih tinggi jumlahnya daripada hewan dewasa (Doxey 1983).
Peningkatan kadar kreatinin dalam darah dapat dipengaruhi berbagai hal. Salah
satu diantaranya yaitu gangguan fungsi ginjal sehingga fungsi nefron menurun
dan ekskresi kreatinin juga menurun dan pada akhirnya kadar kreatinin dalam
plasma akan meningkat (Frandson 1992).
II.3 Fisiologi Adaptasi
II.3.1 Suhu dan Kelembaban
Suhu merupakan suatu keadaan yang menunjukkan kondisi panas atau
semakin tinggi suhu benda tersebut. Suhu tubuh makhluk hidup merupakan suhu
dalam atau suhu inti di bagian dalam makhluk hidup tersebut. Suhu tubuh normal
Macaca fascicularis berada pada kisaran 37ºC sampai dengan 40ºC (Chantalakhana and Skunmun 2002).
Suhu tubuh merupakan suhu yang berada di bagian dalam tubuh, atau
disebut juga suhu inti. Kondisi suhu tubuh relatif stabil, kecuali jika terjadi
gangguan seperti demam. Suhu tubuh bukan suhu permukaan yang mengacu pada
suhu kulit atau jaringan di bawah kulit, karena suhu permukaan ini mudah
mengalami kenaikan dan penurunan sesuai dengan suhu lingkungan. Namun, kulit
merupakan system pengatur radiator panas yang efektif dan aliran darah ke kulit
permukaan mekanisme penyebaran panas yang paling efektif dari inti tubuh ke
kulit. Tetapi, tidak ada tingkat suhu tubuh yang dapat dianggap normal karena
pengukuran pada banyak orang menunjukkan suatu rentang suhu normal. Suhu
tubuh dapat bervariasi tergantung kerja fisik dan kondisi lingkungan yang ekstrim
(Guyton and Hall 2008).
Kelembaban adalah kandungan partikel air di udara. Besaran yang sering
dipakai untuk menyatakan kelembaban udara adalah kelembaban nisbi yang
diukur dengan higrometer. Kelembaban nisbi adalah perbandingan massa uap air
terhadap massa udara kering yang dinyatakan dalam persen. Kelembaban nisbi
dapat berubah sesuai tempat dan waktu. Saat siang hari kelembaban nisbi
berangsur-angsur turun kemudian meningkat pada sore hingga menjelang pagi
hari. Kelembaban berkaitan dengan suhu, semakin rendah suhu umumnya
meningkatkan nilai kelembaban. Kelembaban dapat mempengaruhi kecepatan
hilangnya panas dari tubuh hewan melalui kulit dan saluran pernafasan
(Chantalakhana and Skunmun 2002). Hewan yang diperlakukan pada suhu tinggi
dalam waktu yang cukup lama dapat mengalami perubahan pada ketebalan lemak
tubuh dan rontoknya bulu (Suprayogi et al. 2006). Suhu dan kelembaban udara yang tinggi menimbulkan perubahan fisiologis dan biokimiawi pada makhluk
hidup. Perubahan fisiologis dan biokimiawi ini mengakibatkan proses
homeostasis tubuh agar kondisi menjadi normal kembali. Apabila proses
mengubah tingkah laku, metabolisme, aliran darah, respirasi, nafsu makan dan
sistem fisiologis lainnya pada makhluk hidup (Suprayogi et al. 2009).
II.3.2 Termoregulasi dan Adaptasi Tubuh
Proses fisiologis yang dilakukan tubuh untuk menjaga keseimbangan suhu
internal tubuh pada kondisi normal disebut termoregulasi. Termoregulasi pada
manusia diatur pada hipotalamus anterior. Pengaruh suhu terhadap hewan
digolongkan menjadi poikiloterm dan homoioterm. Hewan homoioterm memiliki
suhu tubuh lebih stabil, karena adanya reseptor dalam otak yang dapat mengatur
suhu tubuh (Swenson 1997). Hewan berdarah panas (homoioterm) merupakan
hewan yang dapat menjaga suhu tubuhnya pada suhu yang konstan yang
umumnya lebih tinggi dibandingkan suhu lingkungan. Contoh hewan berdarah
panas adalah bangsa burung dan mamalia (termasuk Macaca fascicularis). Hewan berdarah dingin adalah hewan yang suhu tubuhnya kurang lebih sama dengan
suhu lingkungan (Guyton and Hall 1993).
Zona nyaman adalah kondisi nyaman seekor hewan dalam kondisi fisiologis
sehingga hewan dapat menjalankan aktivitas hidupnya secara normal (White
2009). Kondisi fisiologis dipengaruhi oleh lingkungan (suhu dan kelembaban
lingkungan) dan perilaku hewan tersebut. Keberadaan zona nyaman atau kondisi
fisiologis dapat mempengaruhi tingkat metabolik dan produksi hewan.
Mekanisme kehilangan panas melalui kulit terjadi melalui konveksi, konduksi,
radiasi dan evaporasi. Jika suhu kulit lebih tinggi daripada suhu lingkungan, maka
tubuh kehilangan panas melalui mekanisme konveksi, konduksi, radiasi dan
evaporasi. Namun, jika suhu lingkungan lebih tinggi daripada suhu kulit, maka
tubuh mendapatkan panas melalui makanan dan fermentasi rumen atau sekum
yang diatur oleh hormon (tiroksin, hormon pertumbuhan dan glukokortikod) dan
aktivitas tubuh (Yousef 1984; Suprayogi et al. 2006).
II.3.3 Stres
Stres merupakan gejala yang tidak baik berdasarkan keadaan klinis dan
fisiologis. Respon tubuh terhadap stres terjadi karena aktivasi sistem saraf dan
akan terjadi stimulasi terhadap hipotalamus yang kemudian akan menskresikan
corticotrophin releasing hormone (CRH) yang memberikan sinyal kepada kelenjar hipofisis anterior yang menyebabkan pelepasan sejumlah besar
adrenocorticotropin hormone (ACTH) dan kemudian meneruskan stimulasi pada kelenjar adrenal terutama korteks adrenal pada fase fasciculata untuk
memproduksi glukokortikoid yang mempresentasikan kortisol untuk disekresi
lebih banyak. Efek fisiologis glukokortikoid terhadap metabolisme adalah
stimulasi glukoneogenesis oleh hati, mobilisasi asam amino dari jaringan
ekstra-hepatik sehingga lebih banyak asam amino yang tersedia dalam plasma untuk
masuk ke dalam proses glukoneogenesis dalam hati, pengurangan penggunaan
glukosa oleh sel dan menekan transpor glukosa ke dalam sel, dan mobilisasi asam
lemak dari jaringan adiposa (Guyton and Hall 1993). Hal ini dilakukan oleh tubuh
untuk memperoleh tambahan energi. Kondisi stres juga dapat mempengaruhi
perilaku, penurunan kecernaan pakan, peningkatan konsumsi air yang pada
III.1 Waktu dan Tempat Penelitian
Penelitian ini dilakukan pada bulan Mei sampai Juni 2009 di Kandang Fakultas Kedokteran Hewan, Institut Pertanian Bogor. Hewan percobaan atau model yang dipergunakan pada penelitian ini adalah monyet ekor panjang (Macaca fascicularis) yang berasal dari PT. Wanara Satwaloka, Bogor-Indonesia sejumlah 10 ekor. Pemerikasaan sampel darah dilakukan di Laboratorium Analisis Darah Bagian Fisiologi Departemen Anatomi, Fisiologi dan Farmakologi FKH-IPB.
III.2 Alat dan Bahan Penelitian
Alat-alat yang digunakan antara lain ruangan, air conditioner (AC), kandang monyet dilengkapi tempat air minum dan pakan, higrotermometer, ember, gelas ukur, spuid, needle, timbangan dan MiraMax Kit Test. Bahan-bahan yang digunakan dalam penelitian ini adalah obat bius (ketamine HCl 10%), pakan monyet impor (monkey chow), pisang dan air.
III.3 Persiapan Penelitian
Sepuluh monyet ekor panjang berjenis kelamin jantan dengan kisaran bobot badan 4-5 Kg dan berumur sekitar 4-5 tahun dimasukkan pada dua ruangan, masing-masing ruangan berisi lima ekor monyet. Hal ini dilakukan agar kondisi ruangan tidak terlalu padat dan agar sesuai dengan kapasitas alat pendingin ruangan sebesar satu pk, sehingga terjadi distribusi suhu ruangan yang merata dan optimal. Setiap ruangan berukuran lebar 2,5 meter, panjang 4 meter dan tinggi 2,75 meter yang di dalamnya terdapat kandang individu yang terbuat dari besi dengan ukuran lebar 60 cm, panjang 80 cm dan tinggi 80 cm. Masing-masing ruangan mendapat perlakuan sama, yaitu dipasang alat pendingin ruangan yang diatur pada suhu 25ºC.
8-10% dan energi 3.858 kal/g. Kandungan nutrisi pada pisang adalah protein 2,3%, serat 23%, lemak 0,13%, kadar air 66% dan energi 136 kal/100 g. setiap monyet diberi pakan sebanyak 200 gram monkey chow dan 100 gram pisang pada pagi dan sore setiap hari selama penelitian. Pemberian air minum dilakukan ad libitum.
Gambar 3. Kandang Macaca fascicularis yang akan dipergunakan (Suprayogi et al. 2009)
Gambar 4. Makanan yang diberikan berupa pisang (Suprayogi et al. 2009)
III.4 Protokol Penelitian
Pengkondisian adaptasi merupakan proses penyesuaian diri terhadap lingkungan diberikan waktu selama 7 hari. Hal ini dilakukan agar hewan coba dapat berperilaku seperti biasanya walaupun ruang gerak dibatasi dan untuk mengurangi tingkat stres. Pada proses ini pakan dan air minum diberikan tanpa dilakukan perhitungan atau pengukuran terlebih dahulu. Hari ke-7 tahap adaptasi hewan diambil darahnya untuk diambil serumnya dan dilakukan analisis terhadap parameter profil kimia darah.
Pengkondisian kedua yaitu aklimasi temperatur dan kelembaban dengan mesin AC pada kondisi hidup dengan pengaturan suhu 25ºC selama 14 hari (hari ke-8 sampai hari ke-21). Pada tahap ini pakan dan air minum yang diberikan pagi dan sore hari dengan ditimbang terlebih dahulu agar setiap hewan coba mendapatkan jumlah pakan dan minum yang sama. Jumlah pakan yang diberikan sebanyak 100 gram monkey chow, 50 gram pisang dan 500 ml air minum. Pengambilan darah tahap aklimasi dilakukan pada hari 8, 11, 18 dan ke-21.
Pengkondisian ketiga (postaklimasi) merupakan tahap setelah aklimasi tanpa mempergunakan pendingin ruangan selama 14 hari. Pencatatan suhu dan kelembapan dilakukan tiga kali dalam sehari, yaitu pada pukul 06.00-07.00, 12.00-13.00, dan 17.00-18.00 WIB. Pemberian pakan dan air minum pada tahap ini masih seperti pada tahap kedua yakni, diberikan pagi dan sore hari dengan ditimbang terlebih dahulu agar setiap hewan coba mendapatkan jumlah pakan dan minum yang sama. Pengambilan darah tahap postaklimasi dilakukan pada hari ke-35.
kimia darah dilakukan dengan menganalisis parameter serum darah untuk mengetahui kadar SGPT dan SGOT untuk mengetahui fungsi hati, kadar ureum dan kreatinin untuk mengetahui fungsi ginjal, kadar glukosa, kolesterol, dan trigliserida untuk mengetahui fungsi metabolisme lainnya. Analisis dilakukan menggunakan Kit-test (ST Reagensia®) dan pembacaan dilakukan dengan mesin analisis MiraMax.
Tabel 1 Prosedur Perlakuan terhadap Hewan Coba
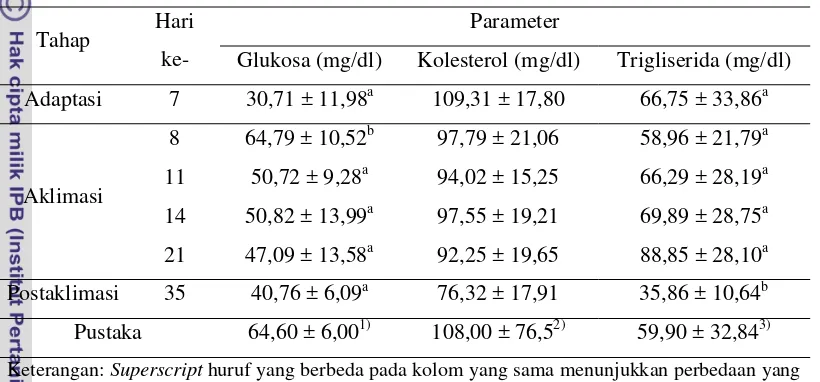
Kadar glukosa, kolesterol, dan trigliserida pada monyet ekor panjang (Macaca fascicularis) pada setiap tahapan adaptasi, aklimasi, dan postaklimasi dapat dilihat pada Tabel 2.
Tabel 2 Kadar Glukosa, Kolesterol dan Trigliserida
Tahap Hari
ke-
Parameter
Glukosa (mg/dl) Kolesterol (mg/dl) Trigliserida (mg/dl)
Adaptasi 7 30,71 ± 11,98a 109,31 ± 17,80 66,75 ± 33,86a
Keterangan: Superscript huruf yang berbedapada kolom yang sama menunjukkan perbedaan yang nyata (P<0,05)
Pustaka: 1): Malinow et al. 1987; 2): Andrade et al. 2004; 3):Ungerer et al.1992
glukosa merupakan sumber energi satu-satunya yang dapat dimanfaatkan oleh otak (Guyton and Hall 2008). Kadar glukosa yang normal terjadi pada kondisi aklimasi, dapat dimungkinkan pada kondisi aklimasi ini hewan model mampu melakukan proses homeostasis dan merasa nyaman dengan kondisi kandang saat aklimasi sehingga tidak mengalami stress.
Saat stres glukokortikoid (kortisol) disekresi lebih banyak menyebabkan adanya stimulasi glukoneogenesis di hati, mobilisasi asam amino dari jaringan ekstra-hepatik sehingga lebih banyak asam amino yang tersedia dalam plasma untuk masuk ke dalam proses glukoneogenesis dalam hati, pengurangan penggunaan glukosa oleh sel dan menekan transpor glukosa ke dalam sel (Guyton and Hall 1993).
Temperatur lingkungan juga merupakan salah satu penyebab stres. Sehingga temperatur juga berpengaruh terhadap kadar glukosa dalam tubuh. Pada saat suhu rendah (dingin) tubuh akan meningkatkan pengeluaran hormon tiroid. Hormon tiroid merangsang hampir semua aspek metabolisme karbohidrat, termasuk pengambilan glukosa yang cepat oleh sel, meningkatkan glikolisis, meningkatkan glukoneogenesis, meningkatkan kecepatan absorbsi dari traktus gastrointestinalis, dan juga meningkatkan sekresi insulin. Hormon tiroid secara tidah langsung akan menurunkan jumlah glukosa dalam tubuh (Guyton and Hall 1993).
Fluktuasi kadar glukosa darah pada hewan model dapat diakibatkan jumlah pakan yang dikonsumsi. Saat stres makhluk hidup cenderung mengalami penurunan konsumsi pakan. Sesaat setelah makan menyebabkan jumlah insulin yang diekskresikan meningkat. Jika insulin yang diekskresikan meningkat, maka kadar glukosa darah menurun karena insulin akan meningkatkan uptake glukosa ke dalam sel bila ada kehadiran reseptor terhadap insulin pada sel (Guyton and Hall 1993).
Keadaan ini dapat terjadi karena peningkatan penimbunan lemak dalam hati, yang kemudian memperbesar jumlah asetil-KoA dalam sel hati, sehingga terjdi peningkatan kolesterol (Guyton and Hall 1997).
Kadar trigliserida mengalami penurunan pada tahap postaklimasi meskipun masih normal dibandingkan nilai pustaka. Hal ini dapat terjadi karena monyet menunjukkan tanda-tanda stres. Saat stres (kortisol meningkat), akan mengakibatkan stimulasi glukoneogenesis oleh hati. Apabila konsentrasi glukosa dalam darah sudah sangat berkurang maka penggunaan glukosa untuk energi akan dialihkan ke penggunaan trigliserida sebagai gantinya. (Guyton and Hall 1997). Peningkatan signifikan trigliserida sangat mungkin terjadi karena trigliserida dapat terbentuk dari berbagai diet yang dikonsumsi, seperti karbohidrat, protein, dan lemak (Clarenburg 2001). Trigliserida banyak dihasilkan ketika mengkonsumsi karbohidrat, dan karbohidrat juga dapat menginduksi terbentuknya trigliserida meski dalam jumlah sedikit (Volek et al. 2008).
Temperatur lingkungan berpengaruh terhadap kadar kolesterol dan trigliserida dalam tubuh. Pada saat suhu rendah (dingin) tubuh akan meningkatkan pengeluaran hormon tiroid dengan tujuan meningkatkan metabolisme lemak karena lemak merupakan sumber utama suplai energi setelah glukosa. Pada intinya hormon tiroid akan mempengaruhi semua aspek yang berkaitan dengan metabolisme lemak (Guyton and Hall 1993).
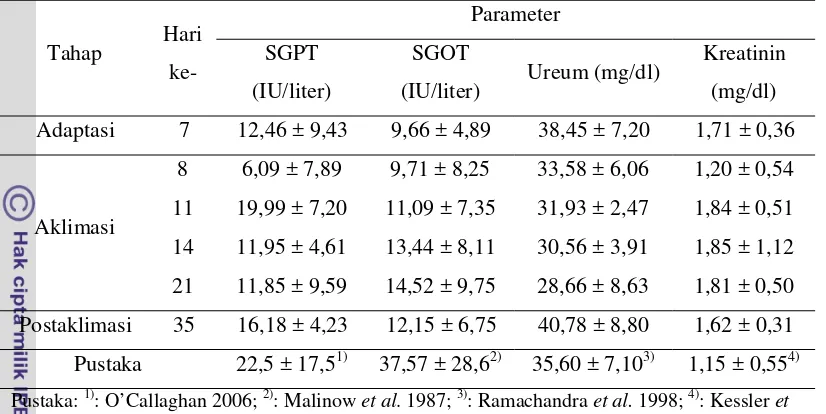
Tabel 3 Kadar SGPT, SGOT , Ureum dan Kreatinin
Berdasarkan data Tabel 3, dapat dikatakan bahwa kadar SGPT dan SGOT monyet ekor panjang selama penelitian masih berada dalam kisaran normal meskipun cukup rendah dibandingkan nilai normal menurut pustaka. Nilai kadar SGOT dan SGPT yang normal ini menunjukkan bahwa fungsi hati dalam melaksanakan tugasnya sebagai pusat metabolisme di tubuh tidak mengalami gangguan. Nilai SGPT dan SGOT yang rendah ini juga kemungkinan juga dapat diakibatkan kerusakan hati yang sudah terlalu parah sehingga tidak mampu lagi melakukan regenerasi sel hati. Saat sel hati mengalami regenerasi, SGPT dan SGOT akan keluar dan masuk ke dalam peredaran darah, oleh karena itu SGPT dan SGOT tetap ada dalam darah secara normal. Pada keadaan keadaan nonpatologis, keberadaan SGPT dan SGOT dalam darah itu normal, hal tersebut terjadi karena regenerasi sel hati yang secara normal terjadi (Girindra 1986). Fluktuasi kadar parameter yang terjadi walaupun masih pada kisaran normal merupakan suatu upaya fisiologis tubuh monyet untuk melakukan proses homeostasis.
sedangkan kandungan protein dalam pakan adalah 18-21%. Fluktuasi kadar parameter yang terjadi walaupun masih pada kisaran normal merupakan suatu upaya fisiologis tubuh monyet untuk melakukan proses homeostasis.
Diskusi Umum
Berdasarkan literatur yang ada, parameter-parameter yang diamati selama penelitian ini masih dalam kisaran normal. Kecuali untuk parameter glukosa pada kondisi adaptasi yaitu 30,71 ± 11,98 mg/dl dan postaklimasi 40,76 ± 6,09 mg/dl yang berada di bawah nilai normal menurut Malinow et al. (1987) yaitu 64,60 ± 6,00mg/dl. Parameter glukosa pada kondisi adaptasi mengalami penurunan nyata bila dibandingkan nilai normal dan nilai pada kondisi aklimasi H8. Pada kondisi adaptasi ini, hewan model menunjukkan tanda-tanda stress (Binol 2010) akibat kondisi temperatur dan kelembaban yang kurang nyaman. Saat stress ini ada kemungkinan hewan model mengalami peningkatan metabolisme yang mengakibatkan glukosa darah dimobilisasi dengan cepat ke jaringan atau sel (Guyton and Hall 1993).
kebutuhan energi pada kondisi stress ini maka proses glukoneogenesis terjadi melalui perombakan trigliserida menjadi energi.
Parameter kolesterol selama penelitian berada pada nilai normal menurut Andrade et al. (2004) yaitu 108,00 ± 76,5 mg/dl. Parameter SGPT dan SGOTselama penelitian berada dalam kisaran normal antara 22,5 ± 17,5 IU/liter menurut O’Callaghan (2006) dan 37,57 ± 28,6 IU/liter menurut Malinow et al. (1987). Parameter ureum dan kreatinin selama penelitian juga berada dalam kisaran nilai normal menurut Ramachandra et al. (1998) yaitu 35,60 ± 7,10 mg/dl dan Kessler et al. (1983) yaitu 1,15 ± 0,55 mg/dl. Artinya ginjal masih melakukan fungsinya dengan baik. Hal ini menunjukkan bahwa ketiga kondisi baik adaptasi, aklimasi, dan postaklimasi tidak mengganggu fungsi organ hati dan ginjal.
V.1 Simpulan
Penelitian ini menyimpulkan bahwa pada kondisi adaptasi dan postaklimasi hewan model menunjukkan tanda-tanda stress. Stress pada kondisi adaptasi diindikasikan dengan penurunan glukosa darah, sedangkan stress pada kondisi postaklimasi diindikasikan dengan penurunan kadar trigliserida. Kondisi aklimasi pada suhu (25,79 ± 1,16)°C dan (80,19 ± 9,05)% rel. dapat diperkirakan sebagai kondisi nyaman bagi hewan model di daerah tropis, yang ditandai dengan nilai profil kimia darah (glukosa, kolesterol, trigliserida, SGPT, SGOT, ureum, dan kreatinin) yang relatif normal.
V.2 Saran
Amin I. 1995. Pengaruh Pemberian Seduhan Rimpang Kunyit (Curcuma Domestica) Terhadap Aktivitas SGPT dan SGOT Ayam. Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor. Bogor. Andrade MCR, Ribeiro CT, Silva FV da, Molinaro EM, Gonçalves MAB,
Marques MAP, Cabello PH, Leite JPG. 2004. Biologic data of Macaca mulatta, Macaca fascicularis, and Saimiri sciureus used for research at the Fiocruz Primate Center. Mem Inst Oswaldo Cruz, Rio de Janeiro 2004;99(6):581–589.
Bachorik PS, Denke MA, Stein EA, Rifkind BM. 2001. Lipids and Dislipoproteinemia. Di dalam: John BH, editor. Clinical Diagnosisand Management by Laboratory Methods: Lipid and Dislipoproteinemia. Ed ke-20. Philadelphia: saunders Company.
Binol, RMF. 2010. Dinamika Profil Hematologi dan Rasio Netrofil:Limfosit Monyet Ekor Panjang (Macaca fascicularis) pada Pengaturan Mikroklimat Ruangan. [Skripsi]. Bogor: Fakultas Kedokteran Hewan, Institut Pertaninan Bogor.
Callbreath DF. 1992. Clinical Chemistry. WB Saunders Company, USA.
Chantalakhana C, and Skunmun P.2002. Sustainable Smallholder Animal Systems in the Tropics. Kasetsart University press, Bangkok.
Clarenburgh R. 2001. Lipid Metabolisms, Physiologycal Chemistry of Domestic Animals. Amerika: Mosby Year Book.
Doxey DL. 1983. Clinical Pathology and Diagnostic Procedurs. London: Bailliere Tindal.
Frandson RD. 1992. Anatomi Fisiologi Ternak Edisi ke-4. Gajah Mada University Press Yogyakarta. Terjemahan dari: Srigando B, Koen P.
Ganong WF. 1999. Fisiologi Kedokteran Edisi ke-14. Jonathan Oswari. Penerbit Buku Kedokteran EGC. Jakarta. Penerjemah: Petrus Andrianto.
Ganong WF. 2003. Fisiologi Kedokteran Edisi ke-21. English: McGraw-Hill. Girindra A. 1986. Patologi Klinik Veteriner. Fakultas Kedokteran Hewan IPB,
Bogor.
Girindra A. 1988. Biokimia Patologi Hewan. Jurusan Biokimia, Fakultas Kedokteran Hewan. Institut Pertanian Bogor. Bogor.
Gunawan A. 2004. Puasa yang Benar: Penyembuhan dan Peremajaan Alami (bagian pertma). Http://www.Indonesiainteractive.htm [25 Februari 2010]. Guyton and Hall. 1993. Textbook of Medical Physiology. Penerbit Buku
Kedokteran EGC. Jakarta.
Guyton and Hall. 1996. Buku Ajar Fisiologi Kedokteran Edisi ke-9. Penerbit Buku Kedokteran EGC. Jakarta. Terjemahan dari: Irawati, Ken Arita Tenggadi dan Alex Santoso.
Guyton and Hall. 1997. Textbook of Medical Physiology. Penerbit Buku Kedokteran EGC. Jakarta.
Guyton and Hall. 2008. Textbook of Medical Physiology. 11th Edition. Philadelphia: W.B. saunders Company.
Harper HA, Murray RK, Granner DK, Mayes PA, Rodwell VW. 1988. Biochemistry. California: Aplleton and Lange, Nowarlk, Connecticut.
Harper HA, Murray RK, Granner DK, Mayes PA, Rodwell VW. 2003. Biochemistry. California: Aplleton and Lange, Nowarlk, Connecticut.
Hau J, and Hoosier Jr, GL. (2003). Handbook of Laboratory Animal Science Second Edition. Boca Raton: CRC Press.
Hayes M.A. 2007. Pathophysiology of the Liver. Saunders Company, USA.
Hutapea AM. 1993. Menuju Gaya Hidup Sehat, Kiat Praktis untuk Setiap Orang Sibuk yang ingin Sehat dan Fit. Jakarta: PT. Gramedia Pustaka Utama. Kendeigh SC. 1980. Ecology with Special Reference to Animal and Mans.
Prentice Hall, New Jersey.
Kessler MJ, and Rawlins, R. G. 1983. The hemogram, serum biochemistry and electrolyte profile of the free-ranging Cayo Santiago Macaques rhesus (Macaca mulatta). Amer. J. Primatol., 4: 107-116.
Kim CY, Han JS, Suzuki T, Han SS. 2005. Indirect Indicator of Transport Stress in Hematological Values in Newly Acquired Cynomolgus Monkeys. J Med Primatol. 34: 188-192.
Lamb E, Newman DJ, Price CP. Kidney Function Test. Dalam: Burtis CA, Ashwood ER, Burns DE. 2006. Tietz Textbook of Clinical Chemistry and Molecular Diagnostic 4th ed. Philadelphia: Elsevier Saunders, 4: 797-826. Lang CKA. 2006. Primate factsheets: long-tailed macaque (Macaca fascicularis)
taxonomy, morphology & ecology. http://pin.primate.wisc.edu/factsheets/ long-tailed_macaque. [2 Agustus 2009].
Lekagul B and McNeely. 1988. Mamals of Thailand 2nd edition. Kurusapha Ladprao Press, Bangkok.
Linder MC. 1992. Biokimia Nutrisi dan Metabolisme dengan Pemakaian secara Klinis. UI Press. Jakarta. Terjemahan dari: Aminuddin Parakkasi.
Malinow MR, McLoughlin P, Staffort C. 1987. Prevension of hypercholesterolemia in monkeys (Macaca fascicularis) by digitonin. Am. J. Clin. Nutr. 35:814-818.
Moss R. 1992. Livestock Health and Welfare. Longman Scientific & Technical, United Kingdom.
National Research Council. 2003. Nutrient Requirement Consumtion Of Nonhuman Primate. Ed 2nd Rev. Washington DC. The National Academic Press.
O’Callaghan C. 2006. The Renal System at a Glance second editition. Blackwell Publishing Ltd. England.
Price SA. 2005. Patofisiologi Konsep Klinis Proses-proses Penyakit. Tennessee. The University of Tennessee Health Science Center.
Poedjiadi A. 1994. Dasar-dasar Biokimia. UIP Jakarta.
Ramachandra SG, Ramesh V, Krishnamuthy HN, Avindranath N, Shetty KT. 1998. Normal Hematological and Plasma Boichemical Parameters of the Captive Bonnet monkey. Primates 39(2): 127-134.
Raphael S. 1987. Lynch’s Medical Laboratory Technology Edisi ke-4. London: WB Saunders Company.
Riswanto. 2010. Kreatinin Darah (Serum). http://labkesehatan.blogspot.com/ 2010/03/kreatinin-darah-serum.html. [5 Oktober 2011]
Sajuthi D. 1984. Satwa Primata Sebagai Hewan Laboratorium. Institut Pertanian Bogor, Bogor.
Sajuthi D, Lelana FPA, Iskandriati D dan Joeniman B. 1993. Karakteristik satwa primata sebagai hewan model untuk penelitian biomedis. Makalah Seminar. Bogor.
Sitopoe M. 1992. Kolesterolfobia, Keterkaitannya dengan Penyakit Jantung. Jakarta: Gramedia.
Smith JB, dan Mangkoewidjojo S. 1988. Pemeliharaan, Pembiakan dan Penggunaan Hewan Percobaan di Daerah Tropis. Penerbit Universitas Indonesia, Jakarta.
Suarsana Nyoman, Suprayogi A, Ni Nyoman Werdi S, Tutik W. 2006. J. Vet. Penggunaan Ekstrak Tempe Terhadap Fungsi Hati Tikus dalam Kondisi Stres.
Sulaksono ME. 2002. Penentuan nilai rujukan parameter faal hewan percobaan sebagai model penyakit manusia dan hewan. http://digilib.litbang.depkes.go.id. [10 September 2009].
Suprayogi A, Astuti DA, Satrija F, Suprianto. 2006. Physiological Status of Sheep Reared Indoor System Under the Tropical Rain Forest Climatic Zone. Proceeding of the 4th ISTAP “Animal Production and Sustainable Agriculture in the Tropic”66-69.
Suprayogi A, Satyaningtijas AS, Kiranadi B, Kusumorini N, Murtini S, Darusman HS. 2009. Uji Keamanan Pendingin Udara LG Berkhasiat Antinyamuk pada Hewan Model Primata dan Rodentia. Bogor: Fakultas Kedokteran Hewan Institut Pertanian Bogor.