PEMACUAN KEMATANGAN GONAD
IKAN LELE DUMBO (Clarias sp.) BETINA
DENGAN KOMBINASI HORMON PMSG DAN Spirulina
NOVI MAYASARI
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
SUMBER INFORMASI
Dengan ini saya menyatakan bahwa tesis Pemacuan Kematangan Gonad Ikan Lele Dumbo (Clarias sp.) Betina dengan Kombinasi Hormon PMSG dan Spirulina
adalah karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apapun kepada perguruan tinggi manapun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka pada bagian akhir tesis ini.
Bogor, Januari 2012
Novi Mayasari
ABSTRACT
NOVI MAYASARI. Induction of gonadal maturation in female catfish (Clarias sp.) with PMSG hormone and Spirulina. Under direction of AGUS OMAN SUDRAJAT and TJANDRA CHRISMADHA
The demand of catfish in the market has been growing annually. It is a significant errand for farmers to provide an amount of seed continually in an adequate number in order to support catfish production. Rematuration is one of the ways to enhance spawning frequency. The aim of the research was to develop a process for accelerate gonad maturity of female catfish using combination of Pregnant Mare Serum Gonadotropin (PMSG) mix hormone and the addition of Spirulina in feeds. PMSG dosage used were 0 IU, 5 IU, 10 IU and 20 IU , whereas Spirulina were 0%, 1.5% and 3%. The results showed that gonad maturity process of female catfish could be accelerated only in 4 weeks by administering the combination of PMSG mix hormone and Spirulina supplementation in the feeds. The treatment of PMSG mix 5 IU/kg weight seemed to be significantly effective to accelerate gonad maturity in female catfish.
Keywords : catfish, gonad maturation, PMSG mix, Spirulina
(Clarias sp.) Betina dengan Kombinasi Hormon PMSG dan Spirulina. Dibimbing oleh AGUS OMAN SUDRAJAT dan TJANDRA CHRISMADHA.
Ikan lele merupakan salah satu dari sepuluh komoditas perikanan unggulan yang ditetapkan oleh Kementrian Perikanan dan Kelautan (KKP).
Permintaan akan ikan lele di pasar semakin meningkat dari tahun ke tahun. Oleh karena itu produksi ikan ini pun semakin meningkat setiap tahun. Salah satu upaya untuk meningkatkan produksi adalah dengan peningkatan frekuensi pemijahan. Oleh karena itu proses percepatan kematangan gonad/rematurasi perlu dilakukan. Jika ditinjau dari segi endokrin maupun dari segi penambahan nutrisi aditif pada pakan maka hal ini sangat mungkin dilakukan. Dari segi endokrin, aplikasi hormon eksogen untuk merangsang reproduksi ikan sering dilakukan karena biasanya sinyal lingkungan kurang mampu mengaktivasi ikan untuk segera bereproduksi. Melalui penggunaan pakan dengan kualitas yang baik dapat menunjang reproduksi ikan sehingga produktivitas yang dihasilkan pun semakin tinggi.
Pregnant mare serum gonadotropin (PMSG) merupakan chorionic gonadotropin dari jenis kuda yang disekresikan oleh endometrium di rahim kuda hamil. Hormon PMSG biasa digunakan untuk menginduksi superovulasi pada mamalia. Hormon ini adalah hormon yang kandungannya berupa folikel stimulating hormone (FSH) dan luteinizing hormone (LH). PMSG merangsang terjadinya lonjakan kadar GnRH yang selanjutnya akan mempengaruhi pituitary
untuk memproduksi gonadotropin. Setelah itu gonadotropin akan merangsang
ovary untuk proses pematangan telur pada ikan. Hormon PMSG ini mampu merangsang pertumbuhan sel interstisial ovarium, pertumbuhan dan pemasakan folikel. Dengan kemampuan tersebut, PMSG diharapkan mampu meningkatkan diameter telur ikan dan selanjutnya menyebabkan kematangan telur terjadi.
Spirulina merupakan salah satu jenis mikroalga yang memiliki nilai nutrisi yang cukup tinggi. Kadar protein Spirulina dilaporkan berkisar antara 60-70%. Spirulina merupakan sumber gamma linolenic acid (GLA), asam lemak esensial tak jenuh ganda. Asam lemak esensial ini adalah prekursor untuk prostaglandin. Prostaglandin berperan sebagai hormon yang membantu pada ovulasi yaitu saat pecahnya sel folikel. Penggunaan 3% Spirulina dalam pakan ikan patin (Pangasius bocourti) mampu meningkatkan kemampuan reproduksi ikan tersebut. Penelitian lain juga menyebutkan bahwa ikan nila yang hanya diberi makan Spirulina saja bisa tetap normal bereproduksi sepanjang tiga generasi. Penggunaan Spirulina dalam pakan kerang/bay scallops juga berhasil untuk pematangan gonad yang normal serta menghasilkan fekunditas dan derajat penetasan yang tinggi.
Penelitian dilaksanakan di Laboratorium Pengembangbiakan dan Genetika Ikan, Fakultas Perikanan dan Ilmu Kelautan, Institut Pertanian Bogor. Penelitian ini dilaksanakan pada bulan Mei 2011 sampai dengan November 2011. Pakan merupakan pakan laboratorium (kadar protein 30%) yang biasa digunakan untuk pembesaran ikan lele. Penambahan Spirulina dilakukan sewaktu pembuatan pakan sesuai dengan dosis yang diinginkan. Selama pemeliharaan ikan diberi makan dengan feeding rate sebesar 3% dari bobot tubuhnya. Frekuensi pemberian pakan yaitu 2 kali pada pukul 08.00 dan 16.00 WIB.
Induk ikan lele dumbo (Clarias sp.) yang digunakan berasal dari petani ikan di daerah Cianjur dan Sawangan (Depok). Bobot induk yang digunakan berkisar antara 216-858 g/ ikan. Adaptasi pakan dilakukan terlebih dahulu selama 1 minggu sebelum penelitian dimulai. Penyeragaman tingkat kematangan gonad dilakukan sebelum penelitian sehingga ikan dalam keadaan kosong (tidak ada telur). Hormon PMSG mix yang digunakan merupakan produk dari Intervet dengan nama dagang PG600. Penelitian ini menggunakan wadah berupa 12 buah bak semen berukuran 2.5 x 1.2 x 0.5 m. Selain itu juga digunakan wadah plastik sebanyak 80 buah dengan ukuran 25 x 25 x 10 cm yang akan digunakan pada proses inkubasi, penetasan telur dan pemeliharaan larva.
Perlakuan yang diujicobakan dalam penelitian ini sebanyak 12 perlakuan yang merupakan kombinasi dari dosis hormon PMSG mix dan dosis Spirulina. Dosis PMSG yang akan diujicobakan sebanyak 4 dosis masing-masing sebesar 0 IU, 5 IU, 10 IU dan 20 IU, sedangkan dosis Spirulina sebanyak 3 dosis yaitu 0%, 1.5% dan 3%. Penyuntikan hormon dilakukan sebanyak 4 kali dengan interval selama 1 minggu. Setiap perlakuan menggunakan satu wadah dan tiap wadah diisi 9 ekor ikan. Sebanyak 5 ikan diamati performa reproduksinya pada akhir penelitian sedangkan 4 lainnya masing-masing diambil seekor tiap minggu untuk pengamatan histologi gonad.
Penambahan Spirulina dalam pakan menyebabkan peningkatan terhadap kadar lemak maupun kadar protein pakan. Akan tetapi kadar serat kasar mengalami penurunan dengan adanya penambahan Spirulina. Kadar asam lemak jenuh dan asam lemak monoenoat di pakan menurun dengan adanya penambahan 1.5% Spirulina, namun dengan penambahan yang semakin tinggi (3%) menyebabkan kadar asam lemak tersebut naik kembali. Hal yang sama juga terjadi pada kadar asam lemak n-3, eicosapentaenoic Acid (EPA) dan
docosahexaenoic Acid (DHA). Sebaliknya terlihat ada peningkatan kadar asam lemak n-6 dan juga GLA dalam pakan seiring dengan bertambahnya dosis Spirulina yang digunakan. Rasio asam lemak n-6 dibanding dengan n-3
rata-rata sebesar 137291 (yang berkisar antara 98467 – 195618) butir telur/kg induk.
Penambahan Spirulina dalam pakan dengan dosis berbeda memberikan pengaruh yang berbeda nyata terhadap diameter telur, dimana dosis 3% memberikan hasil yang terbaik (p<0.10). Perlakuan penyuntikan hormon PMSG mix memberikan pengaruh yang berbeda nyata terhadap diameter telur ikan (p<0.10). Secara umum terlihat bahwa diameter telur ikan lele dumbo bertambah seiring dengan lamanya waktu penelitian. Perkembangan kematangan gonad juga dapat terlihat dari nilai GSI dan HSI pada penelitian ini.
Perlakuan penyuntikan hormon PMSG mix dibandingkan dengan perlakuan kontrol (tanpa hormon) juga memberikan pengaruh yang berbeda nyata terhadap FR dan HR (p<0.10). Pemberian perlakuan kombinasi hormon PMSG mix dan Spirulina (pada perlakuan C sampai perlakuan L) jika dibandingkan dengan perlakuan A (0%; 0 IU) dan perlakuan B (1.5%; 0 IU) memberikan pengaruh yang berbeda nyata terhadap nilai FR dan HR (p<0.10). Nilai FR dan HR yang diperoleh pada penelitian ini (perlakuan C sampai perlakuan L) juga cukup besar yaitu lebih dari 80%.
Hasil uji Dunn terhadap data SR4 menunjukkan bahwa perlakuan hormon
PMSG mix dan penambahan Spirulina dalam pakan memberikan pengaruh yang berbeda nyata terhadap SR4 jika dibandingkan dengan perlakuan A dan B
(p<0.10). Penambahan Spirulina 1.5% dan hormon PMSG mix 20 IU (pada perlakuan K) memberikan pengaruh yang lebih baik dimana hasil rata-rata SR4
lebih besar dibandingkan perlakuan lainnya. Persentase abnormalitas larva pada penelitian ini berkisar antara 0-0.91%. Penambahan Spirulina 1.5% dalam pakan ikan (perlakuan E dan H) mampu mengurangi persentase abnormalitas jika dibandingkan dengan perlakuan yang tidak ditambah Spirulina.
Hasil penelitian menunjukkan proses rematurasi pada ikan lele dumbo betina dapat dipercepat menjadi hanya 4 minggu (28 hari) pasca pemijahan dengan penyuntikan hormon PMSG mix dan pemberian pakan bersuplemen
© Hak Cipta milik IPB, Tahun 2012
Hak Cipta dilindungi Undang-Undang
Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau menyebutkan sumbernya. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik dan tinjauan suatu masalah; dan pengutipan tersebut tidak merugikan kepentingan yang wajar IPB
PEMACUAN KEMATANGAN GONAD
IKAN LELE DUMBO (Clarias sp.) BETINA
DENGAN KOMBINASI HORMON PMSG DAN Spirulina
NOVI MAYASARI
Tesis
Sebagai salah satusyarat untuk memperoleh gelar Magister Sains pada
Program Studi Ilmu Akuakultur
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
Judul : Pemacuan Kematangan Gonad Ikan Lele Dumbo (Clarias sp.) Betina dengan Kombinasi Hormon PMSG dan Spirulina
Nama : Novi Mayasari NRP : C151090181
Disetujui Komisi Pembimbing
Dr.Ir. Agus Oman Sudrajat, M.Sc.
Ketua Anggota
Drs. Tjandra Chrismadha, M.Sc
Diketahui
Ketua Program Studi Dekan Sekolah Pascasarjana
Ilmu Akuakultur
Prof.Dr. Enang Harris Dr. Ir. Dahrul Syah, M.Sc.Agr.
PRAKATA
Puji dan syukur penulis panjatkan kepada Allah SWT atas segala karunia-Nya sehingga karya ilmiah ini berhasil diselesaikan. Tema yang dipilih dalam penelitian yang dilaksanakan sejak bulan Mei sampai dengan November 2011 ini ialah rematurasi pada ikan lele dumbo, dengan judul Pemacuan Kematangan Gonad Ikan Lele Dumbo (Clarias sp.) Betina dengan Kombinasi Hormon PMSG dan Spirulina
Dengan keikhlasan hati penulis mengucapkan terima kasih kepada :
1. Dr.Ir. Agus Oman Sudrajat, M.Sc., Drs. Tjandra Chrismadha, M.Sc. selaku pembimbing yang telah memberikan arahan, masukan dan pembimbingan terhadap kesempurnaan tesis ini.
2. Prof.Dr. Enang Harris selaku Ketua Program Studi Ilmu Akuakultur (AKU) SPs IPB.
3. Ir. Harton Arfah, M.Si atas saran dan masukan yang diberikan dalam ujian akhir untuk kesempurnaan tesis ini.
4. Pimpinan LIPI melalui Bapak Sekertaris Utama-LIPI yang telah memberikan kesempatan kepada penulis melanjutkan studi di Sekolah Pascasarjana IPB melalui karyasiswa LIPI.
5. Dr. Tri Widiyanto, M.Si. selaku Kepala Pusat Penelitian Limnologi-LIPI dan Ir. Lukman, M.Si. selaku Kepala Bidang Produktivitas Perairan Darat, Puslit Limnologi-LIPI yang telah memberikan ijin dan dukungan kepada penulis untuk melanjutkan studi.
6. Ayahanda Marsidi (Alm), Ibunda Sumiyati, Ayahanda Sukiran, Ibunda Ngatini, Eyang Kakung Sahli serta Eyang Putri Sarni yang selalu memberikan doa dan dukungan selama penulis menyelesaikan pendidikan 7. Suami tercinta Agus Waristriatmaja dan ananda Nararya Hylmi Kenzie yang
selalu memberikan semangat dan doa selama penulis menyelesaikan pendidikan
8. Teman-teman Akuakultur 2009 yang selalu menemani penulis mulai dari awal pendidikan hingga selesai
9. Seluruh anggota Laboratorium Pengembangbiakan dan Genetika Ikan BDP-IPB, terutama Erna Thalib, Wahyuni Fanggitasik, Safrizal dan Aras Syazili serta Fajarruddin Manurung yang telah menemani dan memberikan bantuan selama penelitian.
10.Seluruh teknisi di Kolam Percobaan, FPIK IPB yang telah memberikan bantuan selama penelitian.
11.Semua pihak yang membantu baik secara langsung maupun tidak langsung yang tidak bisa disebutkan satu persatu.
Semoga karya ilmiah ini bermanfaat.
Bogor, Januari 2012
Penulis dilahirkan di Metro, Lampung pada tanggal 7 Oktober 1983. Penulis merupakan anak dari Bapak Marsidi (alm) dan Ibu Sumiati. Penulis adalah bungsu dari dua bersaudara.
DAFTAR ISI
Halaman
DAFTAR ISI ... xiii
DAFTAR TABEL ... xiv
DAFTAR GAMBAR ... xv
DAFTAR LAMPIRAN ... xvi
PENDAHULUAN ... 1
Latar Belakang ... 1
Tujuan dan Manfaat ... 3
Hipotesis ... 3
TINJAUAN PUSTAKA ... 5
Perkembangan Gonad Ikan ... 5
Peranan Hormon PMSG ... 8
Peranan Spirulina ... 10
BAHAN DAN METODE ... 13
Waktu dan Tempat Penelitian ... 13
Bahan dan Alat ... 13
Metode Penelitian ... 14
Pelaksanaan Penelitian ... 17
Analisis Statistik ... 18
HASIL DAN PEMBAHASAN ... 21
Hasil ... 21
Pembahasan ... 42
SIMPULAN DAN SARAN ... 49
Simpulan ... 49
Saran …. ... 49
DAFTAR PUSTAKA ... 51
Halaman
1. Kandungan asam lemak esensial dalam Spirulina ... 11
2. Perlakuan penelitian pemacuan kematangan gonad ikan lele
dumbo betina dengan hormon PMSG dan Spirulina ... 15
3. Analisa proksimat (% bobot kering) dan total asam lemak
(% area) terhadap Spirulina dan pakan perlakuan ... 21
4. Diameter telur ikan lele dumbo selama penelitian ... 22
5. Perkembangan kematangan gonad ikan lele dumbo dengan
pemberian kombinasi hormon PMSG dan Spirulina ... 23
6. Perkembangan kematangan gonad dan kinerja reproduksi ikan
lele dumbo betina yang diberi perlakuan kombinasi hormon
PMSG dan Spirulina (variabel pada uji Kruskal wallis
dikelompokkan berdasarkan hormon PMSG) ... 37
7. Perkembangan kematangan gonad dan kinerja reproduksi ikan
lele dumbo betina yang diberi perlakuan kombinasi hormon
PMSG dan Spirulina (variabel pada uji Kruskal wallis
dikelompokkan berdasarkan Spirulina) ... 38
8. Perkembangan kematangan gonad dan kinerja reproduksi ikan
lele dumbo betina yang diberi perlakuan kombinasi hormon
PMSG dan Spirulina (variabel pada uji Kruskal wallis
dikelompokkan berdasarkan kombinasi hormon PMSG dan
Spirulina) ... 39
DAFTAR GAMBAR
Halaman
1. Struktur histologis gonad ikan lele dumbo pada kombinasi
hormon PMSG mix 0 IU dan Spirulina 0% ... 24
2. Struktur histologis gonad ikan lele dumbo pada kombinasi
hormon PMSG mix 0 IU dan Spirulina 1.5% ... 25
3. Struktur histologis gonad ikan lele dumbo pada kombinasi
hormon PMSG mix 0 IU dan Spirulina 3% ... 26
4. Struktur histologis gonad ikan lele dumbo pada kombinasi
hormon PMSG mix 5 IU dan Spirulina 0% ... 27
5. Struktur histologis gonad ikan lele dumbo pada kombinasi
hormon PMSG mix 5 IU dan Spirulina 1.5% ... 28
6. Struktur histologis gonad ikan lele dumbo pada kombinasi
hormon PMSG mix 5 IU dan Spirulina 3% ... 29
7. Struktur histologis gonad ikan lele dumbo pada kombinasi
hormon PMSG mix 10 IU dan Spirulina 0% ... 30
8. Struktur histologis gonad ikan lele dumbo pada kombinasi
hormon PMSG mix 10 IU dan Spirulina 1.5% ... 31
9. Struktur histologis gonad ikan lele dumbo pada kombinasi
hormon PMSG mix 10 IU dan Spirulina 3% ... 32
10.Struktur histologis gonad ikan lele dumbo pada kombinasi
hormon PMSG mix 20 IU dan Spirulina 0% ... 33
11.Struktur histologis gonad ikan lele dumbo pada kombinasi
hormon PMSG mix 20 IU dan Spirulina 1.5% ... 34
12.Struktur histologis gonad ikan lele dumbo pada kombinasi
hormon PMSG mix 20 IU dan Spirulina 3% ... 35
13.Kelangsungan hidup larva setelah 4 hari / SR4 (%) ... 40
Halaman
1. Produksi perikanan budidaya lele (ton) ... 57
2. Produksi benih ikan lele ... 57
3. Komposisi pakan laboratorium untuk ikan lele dumbo ... 58
4. Prosedur analisis proksimat ... 59
5. Prosedur penyiapan preparat histologi gonad ... 63
6. Histogram diameter telur ikan lele dumbo betina yang diberi perlakuan hormon PMSG dan Spirulina ... 66
7. Hasil analisa asam lemak pada pakan perlakuan yang ditambahkan Spirulina ... 68
8. Kinerja reproduksi induk ikan lele dumbo yang diberi perlakuan hormon PMSG dan Spirulina ... 69
9. Hasil analisa data dengan program SPSS ver.16 ... 72
10.Contoh perhitungan uji Dunn ... 82
11.Perhitungan analisa ekonomi ... 85
PENDAHULUAN
Latar BelakangIkan lele merupakan salah satu dari sepuluh komoditas perikanan
unggulan yang ditetapkan oleh Kementrian Perikanan dan Kelautan (KKP).
Permintaan akan ikan lele di pasar semakin meningkat dari tahun ke tahun. Oleh
karena itu produksi ikan ini pun semakin meningkat setiap tahun. KKP (2010)
melaporkan bahwa selama periode tahun 2005-2009 terjadi peningkatan produksi
sebesar 108.62% (Lampiran 1) atau rata-rata peningkatan produksi setiap
tahunnya yaitu 23.33% . Pada kegiatan pembenihan, faktor induk menjadi penentu
keberhasilan kegiatan. Ketersediaan benih yang berkualitas dalam jumlah cukup
dan kontinu menjadi suatu keharusan bagi pembudidaya untuk menunjang
peningkatan produksi. Selama periode tahun 2008-2009 terjadi peningkatan
produksi benih lele yaitu sebesar 2.21% (Lampiran 2).
Pemijahan induk lele pada skala produksi massal seringkali dilakukan
melalui induce spawning maupun induce breeding. Diketahui bahwa ikan lele
dumbo (Clarias sp.) mampu memijah sepanjang tahun. Dalam satu tahun secara
alami (dengan pemberian pakan biasa) ikan lele mampu memijah sampai dengan
3 kali. Untuk dapat meningkatkan produksi maka diperlukan peningkatan
frekuensi pemijahan. Oleh karena itu proses percepatan kematangan
gonad/rematurasi perlu dilakukan. Jika ditinjau dari segi endokrin maupun dari
segi penambahan nutrisi aditif pada pakan maka hal ini sangat mungkin
dilakukan. Dari segi endokrin, aplikasi hormon eksogen untuk merangsang
reproduksi ikan seringkali dilakukan karena biasanya sinyal lingkungan kurang
mampu mengaktivasi ikan untuk segera bereproduksi. Melalui penggunaan pakan
dengan kualitas yang baik dapat menunjang reproduksi ikan sehingga
produktivitas yang dihasilkan pun semakin tinggi.
PMSG (pregnant mare serum gonadotropin) atau chorionic gonadotropin
dari jenis kuda disekresikan oleh endometrium di rahim kuda hamil.
Hormon ini dapat ditemukan dalam darah kuda hamil antara hari ke-40 dan 120
kehamilan, mencapai puncaknya sekitar hari ke-60. Sebelum pengukuran PMSG
dibutuhkan tes khusus untuk kehamilan karena hormon hanya ditemukan dalam
lagi. Hormon PMSG biasa digunakan untuk menginduksi superovulasi pada
mamalia. Hormon ini adalah hormon yang kandungannya berupa FSH (folikel
stimulating hormone) dan LH (luteinizing hormone). PMSG merangsang
terjadinya lonjakan kadar GnRH yang selanjutnya akan mempengaruhi pituitary
untuk memproduksi gonadotropin (Bolamba et al. 1992). Setelah itu gonadotropin
akan merangsang ovary untuk proses pematangan telur pada ikan. Menurut
Partodiharjo (1987) dalam Basuki (1990), PMSG sangat banyak mengandung
unsur daya kerja FSH dan sedikit LH, sedangkan HCG (Human Chorionic
Gonadotropin) memiliki potensi LH yang amat kuat.
Perbaikan yang dilakukan pada nutrisi dan pemberian pakan ke induk
ikan telah menunjukkan peningkatan yang besar tidak hanya pada sperma dan
telur, akan tetapi juga pada produksi benih. Perkembangan gonad dan fekunditas
(jumlah telur yang dihasilkan induk) juga dipengaruhi beberapa nutrien tertentu,
terutama pada ikan yang memijah secara terus-menerus dengan periode
vitelogenesis yang pendek (Izquierdo et al. 2001).
Dalam proses pematangan gonad, induk ikan perlu mendapatkan nutrisi
yang mampu menunjang perkembangan gonadnya. Spirulina merupakan salah
satu jenis mikroalga yang memiliki nilai nutrisi yang cukup tinggi. Kadar protein
Spirulina dilaporkan berkisar antara 55-70%. Penelitian mengenai penggunaan
Spirulina dalam pakan ikan patin (Pangasius bocourti) dilaporkan mampu
meningkatkan performa reproduksi ikan tersebut (Meng-Umphan 2009).
Penelitian lain juga menyebutkan bahwa ikan nila yang hanya diberi makan
Spirulina saja bisa tetap normal bereproduksi sepanjang tiga generasi (Lu &
Takeuchi 2004). Zhou et al. (1991) melaporkan bahwa penggunaan Spirulina
dalam pakan kerang/bay scallops berhasil untuk pematangan gonad yang normal
serta menghasilkan fekunditas dan derajat penetasan yang tinggi.
Dengan melakukan pendekatan dari segi hormonal (PMSG mix) maupun
dari segi nutrisi aditif dalam pakan (Spirulina) maka diharapkan adanya
percepatan kematangan gonad dari ikan lele dumbo. Selain itu diharapkan pula
telur yang dihasilkan berkualitas baik sehingga derajat pembuahan dan derajat
penetasannya tinggi. Proses pemacuan kematangan gonad pada ikan lele betina di
penambahan Spirulina dalam pakan diharapkan mampu meningkatkan produksi
sehingga ketersediaan benih cukup dan kontinu.
Tujuan dan Manfaat
Penelitian ini bertujuan untuk mengembangkan proses percepatan
kematangan gonad pada ikan lele dumbo (Clarias sp.) betina di luar musim
pemijahan dengan menggunakan kombinasi dosis PMSG mix serta penambahan
Spirulina dalam pakan. Hasil dari penelitian ini diharapkan mampu memberikan
kontribusi terhadap peningkatan produksi ikan lele dumbo.
Hipotesis
Penggunaan kombinasi penyuntikan hormon PMSG mix dan penambahan
Spirulina dalam pakan mampu memacu kematangan gonad dari ikan lele dumbo
(Clarias sp.) betina sehingga reproduksinya lebih cepat daripada pemeliharaan
5
TINJAUAN PUSTAKA
Perkembangan Gonad Ikan
Effendie (1997) menyebutkan bahwa pengetahuan mengenai tingkat
kematangan gonad (TKG) sangat penting dan akan menunjang keberhasilan
pembenihan ikan. Hal ini karena pengetahuan tersebut akan mempermudah dalam
pemilihan calon-calon induk ikan yang akan dipijahkan. Seiring dengan
berkembangnya TKG, diameter telur yang ada dalam gonad juga semakin
membesar sebagai hasil dari akumulasi kuning telur, hidrasi, dan pembentukan
butir-butir minyak yang berjalan secara berurutan.
Perkembangan gonad pada ikan dapat dibagi menjadi dua tahap, yaitu
tahap pertumbuhan gonad hingga mencapai tingkat dewasa kelamin dan tahap
pematangan produksi seksual. Tahap pertumbuhan berlangsung sejak ikan
menetas hingga dewasa kelamin, sedangkan tahap pematangan berlangsung
setelah ikan dewasa. Tahap pematangan akan terus berlangsung dan
berkesinambungan selama fungsi reproduksi berjalan normal (Lagler et al. 1977).
Selama proses reproduksi, sebagian energi akan dipakai untuk
perkembangan gonad. Bobot gonad ikan akan mencapai maksimum sesaat ikan
akan memijah dan kemudian akan menurun dengan cepat selama proses
pemijahan berlangsung hingga selesai. Effendie (1997) menyatakan umumnya
pertambahan bobot gonad ikan betina pada saat stadium matang gonad dapat
mencapai 10-25% dari bobot tubuh dan pada ikan jantan 5-10%. Selain itu,
disebutkan pula bahwa dengan semakin meningkatnya tingkat kematangan gonad,
diameter telur yang ada dalam gonad juga akan bertambah semakin besar.
Tingkat kematangan gonad ikan menurut Nikolsky (Bagenal dan Braum 1968)
yang diacu dalam Effendie (1979):
1. Tidak masak
Individu muda belum berhasrat dalam reproduksi; gonad sangat kecil
2. Tahap istirahat
Produk seksual belum mulai berkembang; gonad kecil ukurannya; telur
3. Pemasakan
Telur-telur dapat dibedakan oleh mata biasa; pertambahan berat gonad
dengan cepat sedang berjalan
4. Masak
Produk seksual masak; gonad mencapai berat yang maksimum tetapi
produk seksual tersebut belum keluar bila perutnya ditekan
5. Reproduksi
Produk seksual keluar bila perut ditekan perlahan; berat gonad turun
dengan cepat dari awal pemijahan sampai selesai
6. Kondisi salin
Produk seksual telah dikeluarkan; lubang pelepasan kemerah-merahan;
gonad seperti kantung kempis; ovari biasanya berisi beberapa telur sisa
7. Tahap istirahat
Produk seksual sudah dilepaskan; lubang pelepasan tidak
kemerah-merahan lagi; gonad bentuknya kecil; telur belum dapat dibedakan oleh
mata biasa.
Tingkat kematangan gonad (TKG) ikan belanak (Mugil dussumieri) modifikasi
dari Cassie (Effendie dan Subardja 1977 dalam Effendie 1979) :
1. TKG I
Ovari seperti benang, panjang sampai ke depan rongga tubuh. Warna
jernih. Permukaan licin.
2. TKG II
Ukuran ovari lebih besar. Pewarnaan lebih gelap kekuning-kuningan.
Telur belum terlihat jelas dengan mata.
3. TKG III
Ovari berwarna kuning. Secara morfologi telur mulai kelihatan butirnya
dengan mata
4. TKG IV
Ovari makin besar, telur berwarna kuning, mudah dipisahkan. Butir
5. TKG V
Ovari berkerut, dinding tebal, butir telur sisa terdapat di dekat pelepasan.
Banyak telur seperti pada TKG II.
Perkembangan ovarium dapat terlihat dari adanya peningkatan nilai indeks
gonad somatik yang disebabkan oleh perkembangan stadia oosit. Pada saat
perkembangan oosit terjadi pula perubahan morfologis yang mencirikan
masing-masing stadianya. Chinabut et al. (1991) membagi oosit dalam 6 kelas/stadium
untuk Clarias sp, dimana setiap stadium dicirikan sebagai berikut:
Stadium 1 : oogonia dikelilingi satu lapis set epitel dengan pewarnaan
hematoksilin-eosin plasma berwarna merah jambu, dengan inti yang besar
di tengah.
Stadium 2 : oosit berkembang ukurannya, sitoplasma bertambah besar, inti
biru terang dengan pewarnaan, dan terletak masih di tengah sel. Oosit
dilapisi oleh satu lapis epitel.
Stadium 3 : pada stadium ini berkembang sel folikel dan oosit membesar
dan provitilin nukleoli mengelilingi inti.
Stadium 4 : euvitilin inti telah berkembang dan berada disekitar selaput
inti. Stadium ini merupakan awal vitelogenesis yang ditandai dengan
adanya butiran kuning telur pada sitoplasma. Pada stadium ini, oosit
dikelilingi oleh dua lapis sel dan lapisan zona radiata tampak jelas pada
epitel folikular.
Stadium 5 : stadia peningkatan ukuran oosit karena diisi oleh kuning telur.
Butiran kuning telur bertambah besar dan memenuhi sitoplasma dan zona
radiata terlihat jelas.
Stadium 6 : inti mengecil dan selaput inti tidak terlihat, inti terletak di tepi.
Zona radiata, sel folikel dan sel teka terlihat jelas.
Ukuran telur juga memiliki peran penting dalam kelangsungan hidup ikan.
Benih ikan brown trout yang berasal dari telur yang berukuran besar mempunyai
daya hidup yang lebih tinggi daripada benih ikan yang berasal dari telur yang
berukuran kecil. Hal ini terjadi karena kandungan kuning telur yang berukuran
makanan yang cukup untuk membuat daya tahan tubuh yang lebih tinggi
dibanding dengan telur-telur yang berukuran kecil (Bagenal 1969).
Woynarovich dan Horvath (1980) menyatakan bahwa induk yang pantas
dipijahkan adalah induk yang telah melewati fase pembentukan kuning telur (fase
vitellogenesis) dan masuk ke fase dorman. Fase pembentukan kuning telur
dimulai sejak terjadinya penumpukan bahan-bahan kuning telur da!am sel telur
dan berakhir setelah sel telur mencapai ukuran tertentu atau nukleolus tertarik ke
tengah nukleus. Setelah fase pembentukan kuning telur berakhir, sel telur tidak
mengalami perubahan bentuk selama beberapa saat, tahap ini disebut fase istirahat
(dorman). Menurut Lam (1985), apabila rangsangan diberikan pada saat ini, maka
akan menyebabkan terjadinya migrasi inti ke perifer, kemudian inti pecah atau
melebur pada saat pematangan oosit, ovulasi (pecahnya folikel), dan oviposisi.
Apabila kondisi lingkungan tidak cocok dan rangsangan tidak tersedia maka telur
dorman tersebut akan mengalami degenerasi (rusak) lalu diserap kembali oleh
lapisan folikel (atresia). Faktor-faktor eksternal lain yang menyebabkan terjadinya
atresia adalah ketersediaan pakan, sedangkan faktor internal adalah umur telur.
Ukuran sel telur juga berhubungan dengan fekunditas. Makin banyak telur
yang dipijahkan maka ukuran telurnya makin kecil, misalnya ikan cod
(diameternya 1-1,7mm) produksinya 10 juta telur dan Salmon Atlantik yang
memiliki diameter telur 5-6 mm, produksi telurnya 2.000-3.000 butir (Blaxter
1969).
Peranan Hormon PMSG
Superovulasi merupakan suatu cara untuk meningkatkan jumlah anak per
kelahiran dan sekresi hormon mammogenik seperti estradiol dan progesteron
selama kebuntingan (Manalu et al. 1999). Superovulasi pada kambing etawa
dengan dosis PMSG sebesar 15 IU/kg bobot badan dapat meningkatkan
produktivitas kambing berdasarkan produksi susu dan bobot badan anak serta
keuntungan, yang sejalan dengan peningkatan jumlah korpus luteum, konsentrasi
hormone progesteron, estrogen selama bunting, volume ambing dan bobot badan
anak (Adriani et al. 2003).
Hormon yang bekerja pada proses pematangan gonad ikan adalah
gonadotropin yang sering digunakan dalam penelitian-penelitian. Hormon PMSG
ini memiliki aktivitas biologi serupa FSH dan LH dimana pengaruh FSH-nya
lebih besar. PMSG merangsang terjadinya lonjakan kadar GnRH yang selanjutnya
akan mempengaruhi pituitary untuk memproduksi gonadotropin (Bolamba et al.
1992). Setelah itu gonadotropin akan merangsang ovari untuk proses pematangan
telur pada ikan.
PMSG lebih sering digunakan pada superovulasi sapi perah daripada FSH
dan LH karena memiliki waktu paruh yang lebih panjang mencapai 123 jam
(Menzer and Schams 1979 dalam Supriatna et al. 1998), namun terhadap hipofisis
menyebabkan penekanan produksi LH (Yadav 1983 dalam Supriatna et al. 1998).
Penelitian bioassay menunjukkan bahwa hormon PMSG ada dalam peredaran
darah dari kelinci dan kuda (Catchpole et al. 1935; Cole et al. 1967 dalam
McIntosh et al. 1975), tikus (Parlow and Ward 1961 dalam McIntosh et al. 1975)
selama paling sedikit 20 jam setelah penyuntikan intravenous. Sebaliknya, FSH
dan LH secara cepat akan hilang dari peredaran darah manusia (Kohler et al.
1968; Coble et al. 1969 dalam McIntosh et al. 1975) dan kambing (Akbar et al.
1974 dalam McIntosh et al. 1975).
Hormon PMSG ini mampu merangsang pertumbuhan sel interstisial
ovarium, pertumbuhan dan pemasakan folikel. Dengan kemampuan tersebut,
PMSG diharapkan mampu meningkatkan diameter telur ikan dan selanjutnya
menyebabkan kematangan telur terjadi. Jika ikan sudah matang gonad (diameter
telur bertambah dan telur sudah matang) maka telur akan siap untuk diovulasikan.
Proses tersebut membutuhkan rangsangan hormon sehingga ovulasi pun dapat
terjadi. Untuk itu digunakan hormon HCG (Human Chorionic Gonadotropin)
yang kandungannya adalah LH. Hormon HCG ini memiliki peranan penting untuk
merangsang ovulasi, pecahnya folikel dan pengeluaran oosit yang telah matang
(Rudiana 2000).
Pemberian salmon Gonadotropin Realizing Hormone analog + anti
dopamine (sGnRH-a + ad) dan PMSG secara terpisah dapat menstimulasi
kematangan telur tahap akhir dan ovulasi dari induk ikan gabus. Induksi dengan
PMSG menghasilkan diameter telur yang lebih besar dibandingkan dengan
terovulasi dengan induksi sGnRH-a + ad lebih banyak dibandingkan jumlah telur
terovulasi dengan induksi PMSG. Perlakuan dengan sGnRH-a + ad dan PMSG
menghasilkan daya fertilitas dan daya tetas telur yang tinggi. Kelangsungan hidup
dari larva yang didapat dengan induksi hormonal dengan PMSG selama
pemeliharaan 14 hari yaitu 100% (Fitriliyani 2005).
Peranan Spirulina
Di antara mikroalga digunakan sebagai bahan makanan, makanan
suplemen dan pakan ternak di banyak bagian dunia, Spirulina sp. adalah yang
paling populer karena memiliki nilai gizi yang tinggi dan efektivitas biaya pada
skala budidayanya. Spirulina adalah sumber asam linolenat gamma (GLA, ~ 1%),
asam lemak esensial tak jenuh ganda. Asam lemak esensial ini adalah prekursor
untuk prostaglandin tubuh (PGE1), hormon utama yang mengontrol banyak fungsi
tubuh. PGE1 terlibat dalam banyak tugas termasuk pengaturan tekanan darah,
sintesis kolesterol, inflamasi dan proliferasi sel. PGE1 biasanya terbentuk dari
asam linolenat yang ada di makanan dan GLA diubah menjadi PGE1.
Lemak jenuh yang berlebih dalam pakan dapat menyebabkan defisiensi
GLA dan menekan pembentukan prostaglandin. Beberapa penelitian
menunjukkan bahwa pada banyak problem kesehatan dan penyakit ditemukan
adanya kekurangan GLA. Oleh karena itu asupan GLA dari makanan sangatlah
penting. Sumber GLA dari makanan yaitu air susu ibu, ekstrak minyak dari
evening primrose, blackcurrant dan borage seed. Spirulina merupakan salah satu
sumber GLA, dimana 10 gram Spirulina mengandung 135 mg GLA (Tabel 1).
Kandungan GLA dalam Spirulina lebih tinggi dibandingkan dengan sumber
makanan lainnya (Henrikson 2009).
James et al. (2006) menyebutkan penggunaan Spirulina dalam akuakultur
adalah dalam bentuk pakan cair yang dipakai untuk ikan-ikan muda, sedangkan
bentuk pakan padat digunakan untuk ikan dewasa. Spirulina mengandung protein
sebesar 60—70% dan merupakan sumber vitamin B-12 dan β-karoten yang tinggi
(20 kali lipat dari wortel), sumber mineral, asam-asam amino esensial (62%) dan
asam lemak. Spirulina memperbaiki flora usus pada ikan dengan cara memecah
komponen pakan yang tidak tercerna sehingga lebih banyak nutrien dari pakan
kaya akan mukoprotein sehingga akan meningkatkan lapisan mucus alami dari
kulit ikan yang pada akhirnya menghasilkan penampilan sisik yang mengkilap dan
meningkatkan resistensi terhadap infeksi melalui kulit.
Tabel 1. Kandungan asam lemak esensial dalam Spirulina
James et al. (2009) dalam penelitiannya mendapati bahwa penggunaan
kombinasi dosis Spirulina sebesar 30 g/kg diet dan penambahan vitamin E 300
mg menghasilkan pertumbuhan, berat gonad dan fekunditas ikan maskoki
Carassius auratus yang lebih baik dibandingkan perlakuan lainnya (p<0.01).
Selain itu pada semua perlakuan kombinasi Spirulina 30 g/kg diet dengan dosis
vitamin E didapati bahwa penampilan warna dari ikan maskoki tersebut pun lebih
cerah.
Pada banyak spesies ikan, penggunaan Spirulina dalam pakan mampu
meningkatkan laju pertumbuhan. Spirulina dilaporkan juga meningkatkan
kecernaan dari pakan. Penelitian yang dilakukan oleh Kato (1989) dalam Vonshak
(2002), mendapatkan hasil bahwa ikan yang diberi pakan dengan Spirulina
memiliki lemak perut yang lebih sedikit dan juga FCR yang bagus. Penelitian
lainnya menunjukkan bahwa dengan pemberian pakan bersuplemen Spirulina
menghasilkan produksi ikan dengan kualitas yang lebih baik, rasa enak, daging
yang lunak, dan juga warna tubuh yang lebih cemerlang (Hirano 1985, Suyama
Vonshak (2002) juga menyebutkan pemberian Spirulina dalam pakan juga
menurunkan tingkat mortalitas dari fingerling maupun pada stadia post larva.
Penambahan 0,5 sampai 1% Spirulina dalam pakan memberikan pengaruh yang
berbeda nyata terhadap pertumbuhan (peningkatan sekitar 17-25%) dan
menurunkan mortalitas (30-50%), tergantung pada spesies ikan dan dosis
Spirulina yang digunakan. Ungsethaphand et al. (2010) menyatakan bahwa tidak
terdapat perbedaan yang nyata (p> 0,05) pada hasil proksimat daging dari ikan
yang diberi tambahan Spirulina dalam pakannya jika dibandingkan dengan
kontrol. Lebih lanjut, disebutkan bahwa penggantian tepung ikan oleh Spirulina
sampai dengan konsentrasi 20% tidak mempengaruhi pertumbuhan ikan nila
13
BAHAN DAN METODE
Waktu dan Tempat PenelitianPenelitian dilaksanakan di Laboratorium Pengembangbiakan dan Genetika
Ikan, Fakultas Perikanan dan Ilmu Kelautan, Institut Pertanian Bogor. Penelitian
ini dilaksanakan pada bulan Mei 2011 sampai dengan November 2011. Analisa
histologi gonad dilakukan di Laboratorium Kesehatan Ikan,FPIK, IPB. Sedangkan
analisa proksimat pakan dilakukan di Laboratorium Pusat Antar Universitas, IPB
dan analisa asam lemak pakan dilakukan di Laboratorium Kimia Terpadu IPB
Baranangsiang.
Bahan dan Alat Pakan uji
Semua pakan yang digunakan dalam penelitian ini memiliki kadar protein
yang sama (sebelum ditambahkan Spirulina) yaitu 30%. Pakan merupakan pakan
laboratorium (Lampiran 3) yang biasa digunakan untuk pembesaran ikan lele.
Penambahan Spirulina dilakukan sewaktu pembuatan pakan sesuai dengan dosis
yang diinginkan. Pakan kemudian dioven pada suhu 60oC selama 12 jam. Pakan
kemudian dianalisa proksimat untuk melihat kandungan nutrisinya (Takeuchi
1988). Selain itu pakan juga dianalisa kandungan asam lemaknya. Selama
pemeliharaan ikan diberi makan dengan feeding rate sebesar 3% dari bobot
tubuhnya. Frekuensi pemberian pakan yaitu 2 kali pada pukul 08.00 dan 16.00
WIB.
Hewan Uji
Induk ikan lele dumbo (Clarias sp.) yang digunakan berasal dari petani
ikan di daerah Cianjur dan Sawangan (Depok). Penelitian ini menggunakan induk
yang sudah pernah memijah untuk dirematurasi. Induk yang digunakan beratnya
berkisar antara 216-858 gram/ekor. Umur induk yang digunakan ± 8 bulan dan
sudah matang gonad. Sebelum penelitian dimulai dilakukan adaptasi pakan
terlebih dahulu selama 1 minggu. Sebelum perlakuan penelitian dimulai,
dilakukan penyeragaman tingkat kematangan gonad sehingga ikan dalam keadaan
kosong (tidak ada telur). Pengeluaran telur dilakukan dengan stripping setelah
sebelumnya induk ikan diinduksi ovaprim (1 bagian ovaprim diencerkan dengan 2
bagian larutan fisiologis) dengan dosis 0.6 ml/kg ikan. Sekitar 10 jam setelah
penyuntikan ovaprim, telur dikeluarkan dari induk dengan cara stripping. Setelah
telur dikeluarkan, induk diamati nafsu makannya selama 2-3 hari. Bila nafsu
makan induk sudah normal maka penelitian segera dilaksanakan. Selama
penelitian, dari tiap-tiap perlakuan diambil 1 ekor ikan untuk pembuatan preparat
histologi gonad.
Hormon yang digunakan
Hormon PMSG (pregnant mare serum gonadotropin) mix yang digunakan
merupakan produk dari Intervet dengan nama dagang PG600. Masing-masing
vialnya (5 ml) berisi 400 IU PMSG dan 200 IU HCG. Sebelum digunakan hormon
tersebut diencerkan terlebih dahulu menggunakan larutan fisiologis (NaCl 0.9%)
hingga mencapai dosis yang diinginkan. Selain itu juga digunakan hormon
luteinizing hormone releasing hormone (LHRH)+ anti dopamine (nama dagang
Ovaprim; produk dari Syndel, Canada) untuk merangsang pemijahan ikan di akhir
penelitian.
Wadah
Penelitian ini menggunakan wadah berupa 12 buah kolam semen
berukuran 2.5 x 1.2 x 0.5 m. Pada permukaan atas wadah diberi jaring penutup
untuk mencegah agar ikan uji tidak melompat ke luar wadah. Selain itu juga
digunakan wadah plastik sebanyak 80 buah dengan ukuran 25 X 25 X 10 cm yang
akan digunakan pada proses inkubasi, penetasan telur, dan pemeliharaan larva.
Metode Penelitian Perlakuan
Perlakuan yang diujicobakan dalam penelitian ini sebanyak 12 perlakuan
yang merupakan kombinasi dari dosis hormon PMSG mix dan dosis Spirulina.
Dosis PMSG mix yang akan diujicobakan sebanyak 4 dosis masing-masing
sebesar 0 IU, 5 IU, 10 IU dan 20 IU sedangkan dosis Spirulina sebanyak 3 dosis
dengan interval selama 1 minggu. Secara lengkap, perlakuan dalam penelitian ini
Tabel 2. Perlakuan penelitian pemacuan kematangan gonad ikan lele dumbo
betina dengan hormon PMSG dan Spirulina
Spirulina
Dosis PMSG mix (400 IU PMSG& 200 IU HCG)
0 IU 5 IU 10 IU 20 IU
0 % A/kontrol
(0 IU;0%) D (5 IU; 0%) G (10 IU; 0%) J (20 IU; 0%)
1.5 % B (0 IU; 1.5%) E (5 IU; 1.5%; H (10 IU; 1.5%) K (20 IU; 1.5%)
3 % C(0 IU; 3%) F (5 IU; 3%) I (10 IU; 3%) L (20 IU; 3%)
Setiap perlakuan menggunakan satu wadah dan tiap wadah diisi 9 ekor
ikan. Sebanyak 4 ekor ikan diambil seekor setiap minggu untuk pengamatan
histologi gonad serta analisis Gonadosomatik Indeks (GSI) dan Hepatosomatik
Indeks (HSI). Sedangkan 5 ekor ikan lainnya diamati performa reproduksinya
pada akhir penelitian.
Parameter yang dievaluasi
Dalam penelitian ini, parameter yang diamati yaitu sebagai berikut :
1) Analisa proksimat Spirulina dan pakan perlakuan (Takeuchi 1988;
Lampiran 4).
2) Analisa asam lemak pada Spirulina dan pakan perlakuan (metode gas
chromatografi).
3) Pengamatan kematangan gonad, yang dilakukan dengan membuat
preparat histologis ovarium (Lampiran 5). Pengamatan ini akan
dilakukan pada hari ke-0, 7, 14 dan 21.
4) Diameter telur. Pengamatan dilakukan dengan menggunakan
mikroskop yang dilengkapi mikrometer okuler dengan pembesaran
40x pada preparat histologis gonad dan telur pemijahan (Lampiran 6).
Induk yang matang gonad ditentukan dengan persentase diameter telur
≥ 0.9 mm sebanyak 60-70%. Selain itu dilihat juga keadaan perut dari
induk, dipilih induk yang perutnya lebih besar dan lembek.
5) Gonad Somatik Indeks (GSI)
��� = ������������
6) Hepato Somatik Indeks (HSI)
��� = �����ℎ���
���������ℎ���� � 100
7) Fekunditas relatif, merupakan perbandingan antara jumlah telur yang
dihasilkan dengan bobot tubuh induk (kg). Perhitungannya dengan
cara mengambil 0.1 gr telur hasil ovulasi kemudian dihitung jumlah
telurnya. Pengambilan telur dilakukan sebanyak tiga kali dan jumlah
telur tersebut dirata-ratakan. Nilai rata-rata ini kemudian dikalikan
dengan bobot telur yang diovulasikan.
8) Derajat pembuahan telur (FR), perhitungan FR dilakukan 12 jam
setelah pembuahan, sebanyak tiga kali terhadap sampel telur yang
diambil dan hasilnya kemudian dirata-ratakan.
�� (%) = �����ℎ���������������ℎ�
�����ℎ�������������������� � 100
9) Derajat penetasan (HR), perhitungan HR dilakukan sebanyak tiga kali
terhadap sampel telur yang diambil dan hasilnya kemudian
dirata-ratakan.
�� (%) = �����ℎ����������������
�����ℎ���������������ℎ� ���������� � 100
10)Survival rate larva (SR4), perhitungan SR ini dilakukan sebanyak tiga
kali dan hasilnya kemudian dirata-ratakan.
�� (%) = �����ℎ��������������ℎ���������� 4 ℎ���
�����ℎ��������� � 100
11)Persentase abnormalitas pada larva
������������ (%) = �����ℎ�����������������
Pelaksanaan Penelitian
Sebelum induk ikan dimasukkan ke dalam wadah pemeliharaan berupa
bak, dilakukan pemeriksaan bak dari kebocoran. Bila ada kebocoran pada bak
maka bak terlebih dahulu ditambal. Bak kemudian diisi air dengan kedalaman
40-50 cm. Selama penelitian ini tidak dilakukan pergantian air karena khawatir ikan
menjadi stress. Jika ketinggian air berkurang maka dilakukan penambahan air ke
dalam bak. Sebelum dilakukan percobaan, ikan uji diadaptasikan selama 1
minggu. Selama periode adaptasi, ikan diberi pakan dari perlakuan kontrol
sebanyak 3% bobot tubuh perhari. Ikan uji yang digunakan dalam penelitian ini
ditandai secara individu dengan menggunting sedikit siripnya. Setiap perlakuan
menggunakan satu wadah dan tiap wadah diisi 9 ekor induk betina. Selama
penelitian, ikan tersebut diberi pakan perlakuan 2 kali sehari dengan FR sebesar
3% dari bobot tubuh. Pengukuran parameter kualitas air untuk suhu dilakukan
setiap hari yaitu di pagi dan sore hari. Kandungan oksigen (DO) dan pH diukur
sekali seminggu, sedangkan kandungan alkalinitas dan amonia diukur tiga kali,
yaitu pada awal, tengah, dan akhir penelitian.
Pengamatan perkembangan gonad dilakukan setiap minggu berbarengan
dengan waktu penyuntikan hormon. Evaluasi gonad ikan uji yang terpilih secara
acak dilakukan secara mikroskopis dengan membuat preparat histologis
(Lampiran 5). Evaluasi gonad ini dilakukan sebanyak 4 kali selama penelitian
yaitu pada hari ke-0 (awal penelitian), hari ke-7, hari ke-14 dan hari ke-21.
Saat pemeriksaan kematangan telur, induk yang telah matang gonad segera
dipindahkan ke wadah lain untuk persiapan pelaksanaan pemijahan buatan.
Pemijahan buatan dilakukan dengan menyuntikkan ovaprim dosis 0.6 ml/kg ikan
secara intramuscular. Sekitar 10 jam setelah penyuntikan, dilakukan pengecekan
kesiapan induk untuk memijah. Kemudian telur dikeluarkan dengan cara
stripping/pengurutan. Telur-telur hasil pengurutan tersebut kemudian ditampung
di mangkuk kecil dan ditimbang. Sebanyak ± 0.1 gram sampel telur diambil untuk
penghitungan fekunditas relatif. Perhitungan fekunditas ini dilakukan sebanyak
tiga kali dan nilai yang didapat kemudian dirata-ratakan.
Sampel telur yang diambil kemudian dicampurkan dengan sperma yang
dimasukkan air untuk mengaktifkan sperma supaya terjadi pembuahan. Sebelum
dipindahkan ke wadah penetasan, telur dibilas sebanyak 3 kali dengan air untuk
mencegah terjadinya penjamuran.
Untuk mendapatkan sperma, induk jantan lele dibedah hidup-hidup, lalu
gonadnya diambil. Sperma yang didapat kemudian diencerkan dengan
menggunakan larutan fisiologis dengan perbandingan 1:20. Induk jantan yang
digunakan untuk membuahi telur berasal dari induk jantan yang dipelihara
terpisah dengan induk betina di bak lain.
Untuk penetasan telur digunakan wadah plastik yang berukuran 25 x 25 x
10 cm yang disi air dengan ketinggian 9 cm. Telur yang sudah dibuahi dengan
sperma kemudian disebarkan secara merata pada wadah penetasan. Penghitungan
jumlah telur dan FR dilakukan 12 jam setelah pembuahan. Telur yang tidak
terbuahi ditandai dengan warnanya yang memutih, sedangkan telur yang terbuahi
terlihat adanya pembelahan sel pada telur tersebut. Telur yang menetas dan yang
tidak menetas dihitung untuk mendapatkan nilai HR. Telur-telur yang tidak
menetas segera dipindahkan dengan menggunakan pipet.
Pemeliharaan larva tetap dilakukan di wadah penetasan hingga 4 hari
setelah larva menetas. Jika selama pemeliharaan larva, air terlihat keruh maka air
segera diganti untuk menunjang kualitas air yang baik selama pemeliharaan larva.
Jumlah larva yang masih hidup sampai dengan 4 hari pemeliharan kemudian
dihitung untuk mendapatkan nilai SR4. Pengamatan terhadap abnormalitas larva
juga dilakukan bersamaan dengan penghitungan SR4.
Analisis statistik
Rancangan perlakuan dari penelitian ini adalah Rancangan Acak Lengkap
Faktorial (RAL Faktorial). Sementara analisis data dilakukan dengan analisis non
parametrik yaitu uji Kruskal-Wallis (p<0.10) menggunakan SPSS versi 16. Hal ini
dilakukan karena asumsi kenormalan data dan kehomogenan ragam data tidak
terpenuhi untuk melakukan analisa ragam (analisa parametrik). Upaya untuk
membuat data menjadi normal dan ragamnya homogen melalui transformasi data
pun tidak berhasil. Sehingga diputuskan untuk menggunakan analisis non
signifikan antara perlakuan dianalisis lebih lanjut dengan menggunakan uji Dunn
(Dunn 1964 in Hollander & Wolfe 1973). Jika tidak terdapat perbedaan nyata
[image:35.595.111.517.49.801.2](p>0.10) maka semua data akan dianalisa secara deskriptif dalam bentuk tabel dan
gambar. Khusus untuk data persentase abnormalitas larva dianalisa secara
21
HASIL DAN PEMBAHASAN
HasilKomposisi bahan yang dipakai untuk pakan perlakuan adalah sama untuk
setiap pakan. Perbedaan hanya terdapat pada jumlah Spirulina yang ditambahkan
dalam pakan. Tabel 3 menunjukkan bahwa Spirulina yang digunakan memiliki
kadar protein yang cukup besar. Penambahan Spirulina dalam pakan
menyebabkan peningkatan terhadap kadar lemak maupun kadar protein pakan.
Akan tetapi kadar serat kasar mengalami penurunan dengan adanya penambahan
Spirulina. Penambahan sebesar 1.5% Spirulina dalam pakan menyebabkan kadar
protein meningkat 1.97% dan kadar lemak meningkat 0.49% dibandingkan
dengan pakan kontrol (A). Kadar protein pada pakan yang ditambah Spirulina 3%
meningkat 2.1% dan kadar lemaknya meningkat 0.72% dibandingkan dengan
pakan kontrol.
Tabel 3. Analisa proksimat (% bobot kering) dan total asam lemak (% area)
terhadap Spirulina dan pakan perlakuan
Spirulina (tepung)
Pakan
A1 (0% SP) A2 (1.5% SP) A3 (3% SP)
Komposisi proksimat :
Protein 61.47 ± 1.12 29.52 ± 0.11 31.49 ± 0.17 31.62 ± 0.35
Lemak 3.90 ± 0.30 9.27 ± 0.07 9.76 ± 0.06 9.99 ± 0.09
Serat Kasar 0 5.80 ± 0.36 4.91 ± 0.28 4.47 ± 0.24
Abu 7.35 ± 0.23 17.55 ± 0.07 18.11 ± 0.33 17.45 ± 0.21
Asam lemak :
∑ A l. jenuh 16.28 21.37 20.62 21.67
∑ monoenoat 3.24 2.88 2.59 2.92
∑ A l. n-6 12.05 0.42 0.49 0.61
∑ A l. n-3 0.78 5.45 4.96 5.86
Rasio A l. n-6/n-3 15.449 0.077 0.099 0.104
EPA 0.28 1.58 1.41 1.85
DHA 0.31 2.54 2.38 2.8
GLA 11.75 0.05 0.13 0.23
Kadar asam lemak jenuh dan asam lemak monoenoat di pakan menurun
dengan adanya penambahan 1.5% Spirulina, namun dengan penambahan yang
[image:37.595.97.510.415.698.2]yang sama juga terjadi pada kadar asam lemak n-3, eicosapentaenoic Acid (EPA)
dan docosahexaenoic Acid (DHA). Sebaliknya terlihat ada peningkatan kadar
asam lemak n-6 dan juga GLA dalam pakan seiring dengan bertambahnya dosis
Spirulina yang digunakan (Tabel 3, Lampiran 7). Dari tabel tersebut terlihat pula
bahwa rasio asam lemak n-6 dibanding dengan n-3 mengalami kenaikan sejalan
dengan peningkatan dosis Spirulina dalam pakan.
Secara umum terlihat bahwa diameter telur ikan lele dumbo bertambah
seiring dengan lamanya waktu penelitian (Tabel 4, Lampiran 6). Pengamatan
perlakuan A dan B pada hari ke-28 tidak didapati ikan yang matang gonad. Oleh
karena itu diameter telur kedua perlakuan tersebut tidak diamati. Perkembangan
[image:38.595.95.473.200.796.2]kematangan gonad juga dapat dilihat dari nilai GSI dan HSI (Tabel 5).
Tabel 4. Diameter telur ikan lele dumbo selama penelitian
Perlakuan
Pengamatan pada
hari ke-0 hari ke-7
hari
ke-14
hari
ke-21 hari ke-28
A (0 IU;0%)
0.65±0.11
0.69±0.11 0.74±0.08 0.70±0.12 -
B (0 IU;1.5%) 0.48±0.17 0.36±0.10 0.75±0.13 -
C (0 IU;3%) 0.69±0.12 0.75±0.09 0.74±0.13 1.09 ± 0.05
D (5 IU;0%) 0.65±0.10 0.74±0.11 0.72±0.13 1.04 ± 0.10
E (5 IU;1.5%) 0.64±0.12 0.74±0.07 0.69±0.16 1.03 ± 0.11
F (5 IU;3%) 0.71±0.09 0.71±0.14 0.72±0.14 1.03 ± 0.09
G (10 IU;0%) 0.69±0.14 0.72±0.09 0.69±0.11 1.09 ± 0.04
H (10 IU;1.5%) 0.66±0.11 0.73±0.11 0.70±0.12 1.07 ± 0.08
I (10 IU;3%) 0.68±0.14 0.76±0.08 0.70±0.12 1.10 ± 0.07
J (20 IU;0%) 0.61±0.10 0.70±0.09 0.70±0.10 1.05 ± 0.04
K (20 IU;1.5%) 0.66±0.11 0.69±0.10 0.70±0.11 1.00 ± 0.05
Tabel 5. Perkembangan kematangan gonad ikan lele dumbo betina dengan
pemberian kombinasi hormon PMSG dan Spirulina
Diameter telur yang bertambah besar merupakan hasil dari pengendapan
kuning telur, hidrasi dan pembentukan bulir-bulir minyak di dalam telur tersebut
(Gambar 1). Nilai HSI akan menurun seiring dengan bertambahnya tingkat
kematangan gonad. Hal ini terlihat pada nilai HSI di awal penelitian dibandingkan
dengan HSI pada hari ke-21 (Tabel 5). Hati merupakan organ tempat
diproduksinya vitellogenin . Vitellogenin ini selanjutnya akan dibawa ke gonad
untuk pembentukan kuning telur.
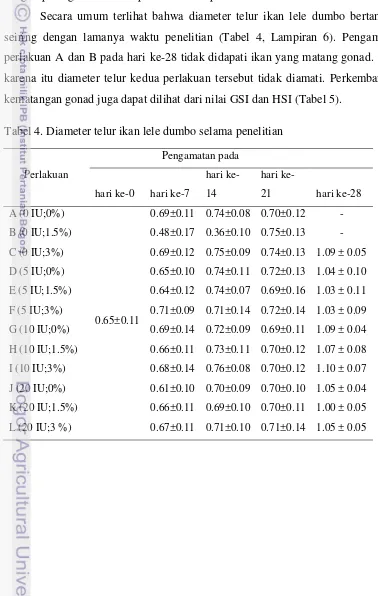
Pada gambar 1a terlihat persentase dari oosit muda dan germ cell yang
cukup tinggi. Oosit mulai terlihat tumbuh, berkembang dan bertambah
diameternya seiring dengan bertambahnya waktu pengamatan (Gambar 1b, 1c dan
1d). Sampai dengan hari ke-21, butiran telur semakin terlihat jelas dan nukleolus
masih terlihat di tengah (TKG III). Akan tetapi pada akhir penelitian, tidak
diperoleh ikan yang matang gonad pada perlakuan A.
Perlakuan hari ke-0 hari ke-7 hari ke-14 hari ke-21 hari ke-28 G S I H S I G S I H S I G S I H S I G S I H S I G S I
A (0 IU;0%)
3.26
(2.19-4.33)
1.07
(0.94-1.19)
1.94 1.37 6.96 2.08 11.27 1.08 -
B (0 IU;1.5%) 1.54 0.84 0.99 0.97 8.15 1.30 -
C (0 IU;3%) 7.19 1.17 5.94 0.79 9.24 0.89 11.39 (9.31-13.47)
D (5 IU;0%) 8.49 1.02 9.48 1.09 7.04 0.79 14.37 (11.06-19.78)
E (5 IU;1.5%) 6.04 1.56 3.92 0.85 5.20 1.15 10.13 (8.83-11.43)
F (5 IU;3%) 6.58 0.82 4.40 0.80 2.59 1.24 9.66 (4.91-14.40)
G (10 IU;0%) 5.11 1.56 5.03 1.73 7.79 1.19 8.83 (3.75-13.90)
H (10 IU;1.5%) 5.18 1.03 3.21 0.70 3.01 0.86 8.95 (8.39-9.36)
I (10 IU;3%) 5.14 1.29 6.69 0.92 3.07 0.85 8.11 (6.40-9.82)
J (20 IU;0%) 4.00 1.46 8.73 1.16 13.72 0.70 8.45 (6.89-10.02)
K (20 IU;1.5%) 5.10 1.26 11.76 0.88 11.71 0.98 9.08 (7.44-10.71)
[image:39.595.89.509.56.812.2]Gambar 1. Struktur histologis gonad ikan lele dumbo pada kombinasi hormon PMSG mix 0 IU dan Spirulina 0% (Pengamatan histologis pada bagian tengah ovarium dengan Bouin’s HE, perbesaran 40x)
Keterangan: n = nukleolus f = folikel
a
b
c
d
n
n
n
n f
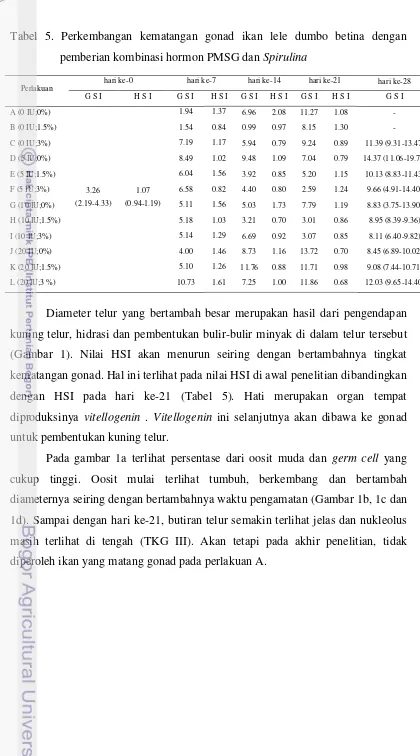
Gambar 2. Struktur histologis gonad ikan lele dumbo pada kombinasi hormon PMSG mix 0 IU dan Spirulina 1.5% (Pengamatan histologis pada bagian tengah ovarium dengan Bouin’s HE, perbesaran 40x)
Keterangan: n = nukleolus f = folikel
Pada gambar 2a terlihat persentase dari oosit muda dan germ cell yang
cukup tinggi. Begitu pula pada Gambar 2b dan 2c terlihat persentase oosit dan
germ cell yang lebih besar. Walaupun demikian oosit mulai terlihat tumbuh,
berkembang dan bertambah diameternya seiring dengan bertambahnya waktu
pengamatan (Gambar 1d). Sampai dengan hari ke-21, gonad ikan terlihat pada
kondisi menuju ke TKG III. Tahapan ini ditunjukkan dengan makin membesarnya
diameter telur sebagai akibat proses vitellogenesis dan proses pertumbuhan gonad.
Seperti pada perlakuan A, di akhir penelitian tidak diperoleh ikan yang matang
gonad pada perlakuan B.
a
b
c
d
n
n
n n
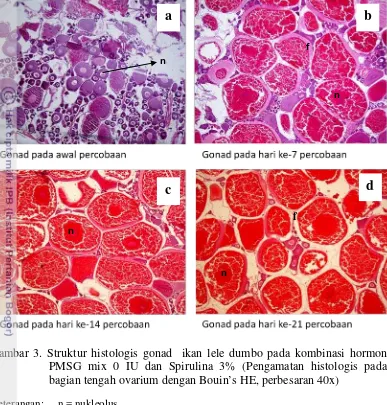
Gambar 3. Struktur histologis gonad ikan lele dumbo pada kombinasi hormon PMSG mix 0 IU dan Spirulina 3% (Pengamatan histologis pada bagian tengah ovarium dengan Bouin’s HE, perbesaran 40x)
Keterangan: n = nukleolus f = folikel
Seiring dengan bertambahnya waktu pengamatan, terlihat oosit tumbuh,
berkembang dan bertambah diameternya (Gambar 3). Sampai dengan hari ke-21
terlihat oosit sudah memasuki tahap TKG III. Tahap ini ditunjukkan dengan
makin membesarnya diameter telur sebagai akibat proses vitellogenesis dan
proses pertumbuhan gonad. Posisi inti sel telur masih di tengah. Pada akhir
penelitian (setelah hari ke-28) diperoleh persentase kematangan gonad sebesar
40% pada perlakuan C (Tabel 6).
a
b
c
d
n
n
n
f
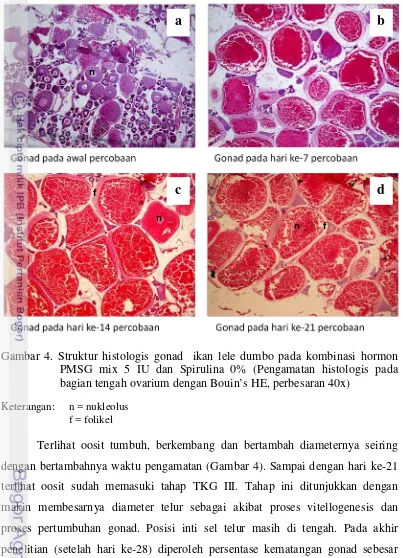
Gambar 4. Struktur histologis gonad ikan lele dumbo pada kombinasi hormon PMSG mix 5 IU dan Spirulina 0% (Pengamatan histologis pada bagian tengah ovarium dengan Bouin’s HE, perbesaran 40x)
Keterangan: n = nukleolus f = folikel
Terlihat oosit tumbuh, berkembang dan bertambah diameternya seiring
dengan bertambahnya waktu pengamatan (Gambar 4). Sampai dengan hari ke-21
terlihat oosit sudah memasuki tahap TKG III. Tahap ini ditunjukkan dengan
makin membesarnya diameter telur sebagai akibat proses vitellogenesis dan
proses pertumbuhan gonad. Posisi inti sel telur masih di tengah. Pada akhir
penelitian (setelah hari ke-28) diperoleh persentase kematangan gonad sebesar
80% pada perlakuan D (Tabel 6).
a
b
c
d
n
n f
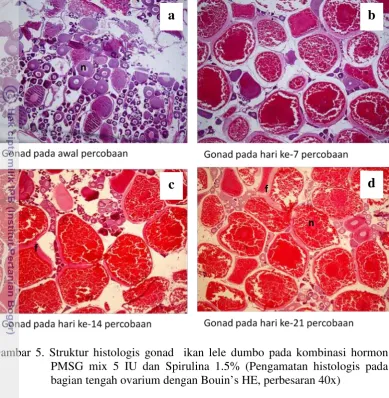
[image:43.595.98.501.112.670.2]Gambar 5. Struktur histologis gonad ikan lele dumbo pada kombinasi hormon PMSG mix 5 IU dan Spirulina 1.5% (Pengamatan histologis pada bagian tengah ovarium dengan Bouin’s HE, perbesaran 40x)
Keterangan: n = nukleolus f = folikel
Seiring dengan bertambahnya waktu pengamatan, terlihat oosit tumbuh,
berkembang dan bertambah diameternya (Gambar 5). Sampai dengan hari ke-21
terlihat oosit sudah memasuki tahap TKG III. Tahap ini ditunjukkan dengan
makin membesarnya diameter telur sebagai akibat proses vitellogenesis dan
proses pertumbuhan gonad. Posisi inti sel telur masih di tengah. Pada akhir
penelitian (setelah hari ke-28) diperoleh persentase kematangan gonad sebesar
40% pada perlakuan E (Tabel 6).
a
b
c
d
n
n f
[image:44.595.107.497.118.517.2]Gambar 6. Struktur histologis gonad ikan lele dumbo pada kombinasi hormon PMSG mix 5 IU dan Spirulina 3% (Pengamatan histologis pada bagian tengah ovarium dengan Bouin’s HE, perbesaran 40x)
Keterangan: n = nukleolus f = folikel
Terlihat oosit tumbuh, berkembang dan bertambah diameternya seiring
dengan bertambahnya waktu pengamatan (Gambar 6). Sampai dengan hari ke-21
terlihat oosit sudah memasuki tahap TKG III. Tahap ini ditunjukkan dengan
makin membesarnya diameter telur sebagai akibat proses vitellogenesis dan
proses pertumbuhan gonad. Pada Gambar 6d tampak bahwa masih terdapat oosit
muda dan germ cell dalam jumlah yang relatif banyak. Posisi inti sel telur masih
di tengah. Pada akhir penelitian (setelah hari ke-28) diperoleh persentase
kematangan gonad sebesar 40% pada perlakuan F (Tabel 6).
a
b
c
d
f
f n
[image:45.595.94.501.76.817.2]Gambar 7. Struktur histologis gonad ikan lele dumbo pada kombinasi hormon PMSG mix 10 IU dan Spirulina 0% (Pengamatan histologis pada bagian tengah ovarium dengan Bouin’s HE, perbesaran 40x)
Keterangan: n = nukleolus f = folikel
Gambar 7 menunjukkan bahwa seiring dengan bertambahnya waktu
pengamatan, terlihat oosit tumbuh, berkembang dan bertambah diameternya.
Sampai dengan hari ke-21 terlihat oosit sudah memasuki tahap TKG III. Tahap ini
ditunjukkan dengan makin membesarnya diameter telur sebagai akibat proses
vitellogenesis dan proses pertumbuhan gonad. Posisi inti sel telur masih di tengah.
Pada akhir penelitian (setelah hari ke-28) diperoleh persentase kematangan gonad
sebesar 40% pada perlakuan G (Tabel 6).
a
b
c
d
n
n f
n
[image:46.595.108.497.116.508.2]Gambar 8. Struktur histologis gonad ikan lele dumbo pada kombinasi hormon PMSG mix 10 IU dan Spirulina 1.5% (Pengamatan histologis pada bagian tengah ovarium dengan Bouin’s HE, perbesaran 40x)
Keterangan: n = nukleolus f = folikel
Gambar 8 menunjukkan bahwa seiring dengan bertambahnya waktu
pengamatan, terlihat oosit tumbuh, berkembang dan bertambah diameternya.
Sampai dengan hari ke-21 terlihat oosit sudah memasuki tahap TKG III. Tahap ini
ditunjukkan dengan makin membesarnya diameter telur sebagai akibat proses
vitellogenesis dan proses pertumbuhan gonad. Posisi inti sel telur masih di tengah.
Pada akhir penelitian (setelah hari ke-28) diperoleh persentase kematangan gonad
sebesar 60% pada perlakuan H (Tabel 6).
a
b
c
d
n
n f
f f
[image:47.595.95.501.109.651.2]Gambar 9. Struktur histologis gonad ikan lele dumbo pada kombinasi hormon PMSG mix 10 IU dan Spirulina 3% (Pengamatan histologis pada bagian tengah ovarium dengan Bouin’s HE, perbesaran 40x)
Keterangan: n = nukleolus f = folikel
Seiring dengan bertambahnya waktu pengamatan, terlihat oosit tumbuh,
berkembang dan bertambah diameternya (Gambar 9). Sampai dengan hari ke-21
terlihat oosit sudah memasuki tahap TKG III. Tahap ini ditunjukkan dengan
makin membesarnya diameter telur sebagai akibat proses vitellogenesis dan
proses pertumbuhan gonad. Posisi inti sel telur masih di tengah. Pada akhir
penelitian (setelah hari ke-28) diperoleh persentase kematangan gonad sebesar
40% pada perlakuan I (Tabel 6).
a
b
c
d
n f
[image:48.595.106.498.110.525.2]Gambar 10. Struktur histologis gonad ikan lele dumbo pada kombinasi hormon PMSG mix 20 IU dan Spirulina 0% (Pengamatan histologis pada bagian tengah ovarium dengan Bouin’s HE, perbesaran 40x)
Keterangan: n = nukleolus f = folikel
Terlihat oosit tumbuh, berkembang dan bertambah diameternya seiring
dengan bertambahnya waktu pengamatan (Gambar 10). Sampai dengan hari ke-21
terlihat oosit sudah memasuki tahap TKG III. Tahap ini ditunjukkan dengan
makin membesarnya diameter telur sebagai akibat proses vitellogenesis dan
proses pertumbuhan gonad. Posisi inti sel telur masih di tengah. Pada akhir
penelitian (setelah hari ke-28) diperoleh persentase kematangan gonad sebesar
40% pada perlakuan J (Tabel 6).
a
b
c
d
n f
[image:49.595.90.498.52.814.2]Gambar 11. Struktur histologis gonad ikan lele dumbo pada kombinasi hormon PMSG mix 20 IU dan Spirulina 1.5% (Pengamatan histologis pada bagian tengah ovarium dengan Bouin’s HE, perbesaran 40x)
Keterangan: n = nukleolus f = folikel
Gambar 11 menunjukkan bahwa seiring dengan bertambahnya waktu
pengamatan, terlihat oosit tumbuh, berkembang dan bertambah diameternya.
Sampai dengan hari ke-21 terlihat oosit sudah memasuki tahap TKG III. Tahap ini
ditunjukkan dengan makin membesarnya diameter telur sebagai akibat proses
vitellogenesis dan proses pertumbuhan gonad. Posisi inti sel telur masih di tengah.
Pada akhir penelitian (setelah hari ke-28) diperoleh persentase kematangan gonad
sebesar 40% pada perlakuan K (Tabel 6).
a
b
c
d
[image:50.595.107.496.116.509.2]Gambar 12. Struktur histologis gonad ikan lele dumbo pada kombinasi hormon PMSG mix 20 IU dan Spirulina 3% (Pengamatan histologis pada bagian tengah ovarium dengan Bouin’s HE, perbesaran 40x)
Keterangan: n = nukleolus f = folikel
Gambar 12 menunjukkan bahwa seiring dengan bertambahnya waktu
pengamatan, terlihat oosit tumbuh, berkembang dan bertambah diameternya.
Sampai dengan hari ke-21 terlihat oosit sudah memasuki tahap TKG III. Tahap ini
ditunjukkan dengan makin membesarnya diameter telur sebagai akibat proses
vitellogenesis dan proses pertumbuhan gonad. Posisi inti sel telur masih di tengah,
hanya ada beberapa yang bergeser ke pinggir. Pada akhir penelitian (setelah hari
ke-28) diperoleh persentase kematangan gonad sebesar 40% pada perlakuan L
(Tabel 6).
a
b
c
d
n f
[image:51.595.97.501.118.659.2]Setelah 28 hari perlakuan, induk ikan yang matang gonad kemudian
dipijahkan secara buatan. Dari Tabel 6 terlihat bahwa semua ikan pada setiap
perlakuan mengalami pertumbuhan dan perkembangan gonad, walaupun dimulai
pada waktu yang berbeda. Dari tabel tersebut terlihat bahwa pada akhir penelitian,
baik pada perlakuan A maupun B tidak terdapat induk ikan yang matang gonad.
Pada perlakuan A (kontrol), induk ikan mulai terlihat bunting setelah hari ke-22
(setelah 3 minggu perlakuan). Sedangkan pada perlakuan lainnya (perlakuan B
sampai L) didapati induk mulai terlihat bunting setelah hari ke-15 (2 minggu
perlakuan). Persentase tertinggi dari ikan yang matang gonad diperoleh pada
perlakuan D (0%; 5 IU) yaitu sebesar 80%.
Fekunditas relatif yang diperoleh pada penelitian ini cukup besar berkisar
antara 66968 sampai dengan 137291 butir telur/kg induk. Perlakuan penyuntikan
hormon PMSG mix secara tunggal memberikan pengaruh yang nyata terhadap
diameter telur, fekunditas relatif, FR, HR dan SR4 (p<0.10). Perlakuan hormon
PMSG mix 10 IU/kg induk menghasilkan diameter telur yang lebih besar
dibandingkan perlakuan lainnya walaupun tidak berbeda nyata jika dibandingkan
dengan perlakuan 5 IU dan 20 IU/kg induk. Perlakuan penyuntikan hormon
PMSG jika dibandingkan dengan perlakuan kontrol (tanpa hormon) memberikan
Tabel 6. Perkembangan kematangan gonad dan kinerja reproduksi ikan lele
dumbo betina yang diberi perlakuan kombinasi hormon PMSG dan
Spirulina (variabel pada uji Kruskal wallis dikelompokkan berdasarkan
hormon PMSG)
Perlakuan ∑ ikan awal Pertama kali terlihat bunting Akhir penelitian Fekunditas (butir/kg induk) Diameter
telur (mm) FR (%) HR (%) %
ikan bun-ting
% ikan matang gonad Waktu (hari ke-) % ikan bun-ting A
(0 IU; 0%) 5 22 40 100 0 -a -a -a -a
B
(0 IU; 1.5%) 5 15 40 100 0 -a -a -a -a
C
(0 IU; 3%) 5 15 40 100 40 95496 ± 34783a 1.09 ± 0.05a 98.03 ± 2.40a 87.74 ± 6.97a D
(5 IU; 0%) 5 15 60 100 80 137291 ± 45921b 1.04 ± 0.10ab 99.05 ± 0.82b 91.75 ± 11.5b
E
(5 IU; 1.5%) 5 15 60 100 40 95022 ± 23049b 1.03 ± 0.11ab 99.95 ± 0.10b 82.28 ± 15.46b F
(5 IU; 3%) 5 15 60 100 40 75696 ± 50825b 1.03 ± 0.09ab 97.27 ± 2.05b 97.69 ± 2.82b
G
(10 IU; 0%) 5 15 60 100 40 72316 ± 51845ab 1.09 ± 0.04b 97.32 ± 4.06b 94.87 ± 6.48b H
(10 IU; 1.5%) 5 15 60 100 60 87251 ± 27777ab 1.07 ± 0.08b 99.29 ± 0.75b 95.31 ± 3.63b
I
(10 IU; 3%) 5 15 40 100 40 66968 ± 16410ab 1.10 ± 0.07b 97.54 ± 4.78b 98.94 ± 1.26b J
(20 IU; 0%) 5 15 40 100 40 77031 ± 25195b 1.05 ± 0.04ab 99.38 ± 0.55b 94.52 ± 5.84ab
K
(20 IU; 1.5%) 5 15 40 100 40 93341 ± 22654b 1.00 ± 0.05ab 99.22 ± 0.99b 89.61 ± 3.64ab L
(20 IU; 3 %) 5 15 60 100 40 85405 ± 30190b 1.05 ± 0