BAB 3
BAHAN DAN METODE
3.1 Alat dan Bahan 3.1.1 Alat
- Buret 25 mL pyrex
- Pipet ukur 10 mL pyrex
- Gelas ukur 100 mL pyrex
- Labu Erlenmeyer 250 mL pyex
- Labu ukur 100 & 1000 mL pyrex
- Botol aquades - Hot plate
3.1.2 Bahan - Aquades - KMnO4 0,01 N
- H2SO4 8 N
- H2C2O4 0,01 N
- Air minum - Air bersih
3.2 Penyediaan Sampel
3.3 Prosedur
1. Asam sulfat, H2SO4
a. Pindahkan 222 mL H
8N yang bebas zat organic
2SO4
suling dalam gelas piala sambil didinginkan dan encerkan sampai 1000mL dalam labu ukur 1000mL
pekat sedikit demi sedikit ke dalam 500mL, air
b. Pindahkan kembali ke dalam gelas piala dan tetesi dengan larutan KMnO sampai berwarna merah muda
4
c. Panaskan pada temperature 80o
hilang selama pemanasan, tambahkan kembali larutan KMnO
C selama 10 menit, bila warna merah
4
2. Kalium Permanganat, KMnO
0,01N sampai warna merah stabil
4
Larutkan 3,16 gr KMnO
0,1 N
4
3. Asam oksalat, (COOH)
dengan air suling dalam labu ukur 1000 mL. simpan dalam botol gelap selama 24 jam sebelum digunakan
2.2H2
Larutkan 3,16 gr (COOH)
O 0,01 N
2.2H2
• Standarisasi Larutan KMnO
O dengan air suling sampai volume 1000mL
4
a) Pipet 100 mL air suling, masukkan ke dalam Labu erlenmeyer 300 mL, panaskan hingga 70
c) Tambahkan 10 mL larutan KMnO
8N yang bebas zat organik
4
d) Tambahkan 10 mL larutan baku asam oksalat 0,01N menggunakan pipet volume
0,01N
e) Titrasi dengan larutan KMnO4 0,01N sampai warna merah muda, dan catat
f) Hitung normalitas KMnO4 yang dengan rumus
Dimana :
V1 = volume larutan baku asam oksalat =10 mL
N1 = normalitas larutan baku asam oksalat = 0.01 N
V2 = volume larutan baku kalium permanganat = volume titrasi
N2
• Prosedur Analisa
= normalitas larutan baku kalim permanganate yang sebenarnya (yang mau dicari)
1. Dipipet 100 mL sampel, masukkan kedalam Labu erlenmeyer 300 mL dan tambahkan 3 butir batu didih
2. Ditambahkan KMnO4
3. Ditambahkan 5 mL asam sulfat 8N bebas zat organik
0,01N beberapa tetes kedalam sampel sehingga terjadi warna merah muda
4. Dipanaskan di atas pemanas listrik pada suhu 1050C, bila terdapat bau H2
5. Ditambahkan 10 mL larutan aku KMnO
S pendidihan diteruskan beberapa menit
4
6. Dipanaskan hngga mendidih selama 10 menit 0,01N
7. Ditambahkan 10 mL larutan baku asam oksalat 0.01N 8. Dititrasi dengan KMnO4
9. Dicatat volume pemakaian KMnO 0,01N
4 0,01N lebih dari 7 mL, ulangi
Rumus: KMnO4 = x f
Keterangan :
a : Volume KMnO4 0,01 N yang dibutuhkan pada titrasi
b : Normalitas KMnO4 0,01 N yang sebenarnya
c : Normalitas asam oksalat d : Volume sampel
BAB 4
HASIL DAN PEMBAHASAN
4.1 Data Percobaan
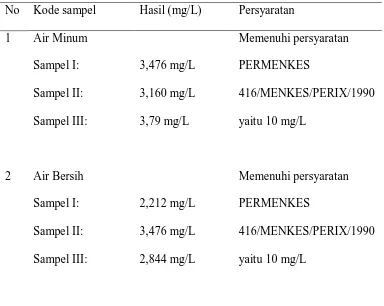
Dari hasil analisis yang dilakukan diperoleh kadar angka permanganat dari air minum, dan air bersih di Balai Laboratorium Dinas Kesehatan Medan adalah:
Tabel 4.1 Tabel Hasil Penelitian Kadar Angka Permanganat No Kode sampel Hasil (mg/L) Persyaratan 1 Air Minum
4.2 Perhitungan
Penentuan kadar Angka Permanganat:
Keterangan :
a : Volume KMnO4 0,01 N yang dibutuhkan pada titrasi
b : Normalitas KMnO4
• Untuk sampel air minum
0,01 N yang sebenarnya c : Normalitas asam oksalat
d : Volume sampel
f : Faktor pengenceran sampel
Sampel I: KMnO4 mg/L =
=
=
= 3,476
Sampel II: KMnO4 mg/L =
=
=
= 3,160
Sampel III: KMnO4 mg/L =
=
=
• Untuk sampel air bersih
Sampel I: KMnO4 mg/L =
=
=
= 2,212
Sampel II: KMnO4 mg/L =
=
=
= 3,476
Sampel III: KMnO4 mg/L =
=
=
= 2,844
1. Reaksi oksidasi KMnO4
2KMnO
dalam suasana asam:
4 + 3H2SO4 2MnSO4 + K2SO4 + 5On
2. Reaksi oksidasi KMnO4
2KMnO
dalam suasana basa:
4 + H2O 2MnO2 + KOH + 3On + 3H2
C
O 3. Reaksi oksidasi zat organik
2H2O + On 2CO2 + H2
Dimana kadar zat organik pada air minum lebih tinggi daripada air bersih. Hal ini dikarenakan air minum yang di konsumsi bukan berasal dari air sumur melaikan berasal dari depot air minum. Air minum isi ulang adalah air yang mengalami beberapa proses yaitu chlorinasi, aerasi, filtrasi dan penyinaran dengan sinar ultra violet. Air minum isi ulang biasanya tidak habis dalam sekali pakai melainkan dalam beberapa hari. Semakin lama penyimpanan memungkinkan adanya pertumbuhan mikroorganisme yang akan berkembang menjadi bakteri patogen dan menyebabkan kadar zat organik menjadi meningkat
O
4.4 Pembahasan
Dari pengukuran zat organik pada air minum dan air bersih dengan menggunakan metode titrasi permanganometri dimana titik akhir ditandai dengan berubahnya warna larutan dari bening menjadi merah lembayung didapatkan hasil dari air minum ketiga sampel adalah 3,476 mg/L, 3,160 mg/L dan 3,79 mg/L. Pada air bersih ketiga sampel adalah 2,212, mg/L, 3,476 mg/L dan 2,844 mg/L.
aktif granular untuk mengendalikan senyawa organik sintetik dan juga senyawa organik alami yang terdapat dalam sumber air minum.
BAB 5
KESIMPULAN DAN SARAN
5.1. Kesimpulan
Air merupakan salah satu kebutuhan pokok manusia yang dibutuhkan secara berkelanjutan. Penggunaan air sangat penting untuk konsumsi rumah tangga, kebutuhan industri dan tempat umum. Dalam hal ini, air minum dan air bersih yang akan dianalisis di BTKL & PP Medan yaitu air minum dan air bersih yang berasal dari sumur warga di kelurahan pasar 4 Mabar hilir kecamatan Medan Deli. Dari analisis yang dilakukan kadar angka permanganat pada sampel air minum dan sampel pada air bersih, yaitu pada melewati baku mutu menurut peraturan Menteri Kesehatan RI NO 416 / MENKES/ PER/ IX/ 1990 Tentang Standar kualitas Air Bersih.
5.2. SARAN
− Air minum dan air bersih yang akan digunakan sebaiknya diteliti kadar angka
permanganatnya, karena jika kadar angka permanganat tinggi hal ini menunjukkan adanya pencemaran organik pada air tersbut.
− sebaiknya warga di psr 4 Mabar hilir Kecamatan Medan Deli mengkonsumsi air