BAB 3
METODE PENELITIAN
3.1 Alat-alat
1. Kromatografi gas spektroskopi massa (GC-MS)
2. Penangas air 3. Oven
4. Inkubator
5. Spektrofotometri uv 6. zVortex
7. Lemari Pendingin
8. Neraca Analitis Mettler AE 200
9. Blender 10. Botol vial 11. Autoklaf 12. Kertas Cakram 13. Kuvet
14. Gelas Beaker 500mL/1000mL Pyrex
15. Gelas Erlenmeyer 250 mL Pyrex
16. Jangka sorong 17. Corong Kaca 18. Pipet mikro 19. Spatula
20. Batang Pengaduk 21. Jarum ose
22. Tabung Reaksi Pyrex
24. Cawan petri
3.2 Bahan-bahan 1. Biji Nangka
2. n-heksan Teknis
3. Spritus 4. Aquadest
5. Nutrient Agar (NA) p.a Oxoid
6. Nutrient Broth (NB) p.a Oxoid 7. Mueller Hinton Agar (MHA)
8. Bakteri Esherichia coli
9. Bakteri Staphylococcus aureus 10. Bakteri Streptococcus mutans 11. Kapas
12. Kertas lebel 13. Benang Bola 14. Sarung tangan 15. Masker
16. Aluminium Foil 17. Alkohol 70% 18. Clin wrap
3.3Prosedur Penelitian 3.3.1 Penyediaan Sampel
3.3.2 Ektraksi Asam Lemak Biji Nangka
Sampel yang sudah kering di timbang sebnyak 1000 gram kemudian di masukkan kedalam wadah yang telah disediakan kemudian dimasukan pelarut N-heksan kedalam wadah yang berisi sample lalu di rendam selama 48 jam sampai warna dari pelarut dan sampel tersebut seperti warna yang mengeluarkan minyak . kemudian di saring sedikit demi sedikit dengan menggunakan pipet untuk mengambil pelarutnya dan di saring dengan menggunakan corong kaca yang dilapisi dengan kapas lalu setelah itu pelarut yang sudah disaring di panaskan dengan penangas air sampai pelarut N-heksanya hilang dengan mendapatkan asam lemak yang murni dari pelarut yang telah bercampur antara n-heksan dengan biji nangka setelah itu di masukkan kedalam botol vial lalu di timbang berat murni dri sampel
3.3.3 Pembuatan Metil Ester Asam Lemak dari Biji Nangka
3.3.4 Pengujian Sifat Antibakteri Asam Lemak dari Biji Nangka(artpcarpus heterophyllus lam)
3.3.4.1 Pembuatan Media Nutrient Agar
Sebanyak 7 g nutrient agar dimasukkan dalam gelasErlenmeyerlaludilarutkan dalam 250 ml aquades dan dipanaskan hingga semua larut dan mendidih. Lalu disterilkan di autoklaf pada suhu 121ºC selama 15 menit.
3.3.4.2 Pembuatan Media Agar Miring dan Stok Kultur Bakteri
Kedalam tabung reaksi yang steril dimasukkan 3 ml media nutrient agar steril, didiamkan pada temperatur kamar sampai memadat pada posisi miring membentuk sudut 30-45º. Biakan bakteri Streptococcus aureusdari strain utama diambil dengan jarum ose steril lalu diinokulasikan pada permukan media nutrient agar miring dengan cara menggores, kemudian diinkubasi pada suhu 35 ± 20C selama 18-24 jam. Hal yang sama juga dilakukan pada biakan bakteri E.coli dan S.Mutans
3.3.4.3 Pembuatan Media Mueller Hinton Agar (MHA)
Sebanyak8g serbuk mueller hinton agar dimasukkan dalam gelas erlenmeyerlaludilarutkan dalam 250 ml aquades dan dipanaskan hingga semua larut dan mendidih. lalu disterilkan di autoklaf pada suhu 121ºC selama 15 menit
3.3.4.4 Penyiapan Suspensi Bakteri
Sebanyak 10 ml aquadest dalam tabung reaksi , distrerilisasi dalam autoklaf selama 15 menit pada suhu 121ºC. Dimasukkan biakan stok kultur bakteri S.aureus menggunakan jarum ose steril, kemudian dihomogenkan suspensi menggunakan vortex, disamakan kekekeruhan dengan larutan Mc.Farland (108 CFU/ml). Hal yang sama dilakukan untuk koloni bakteri E.colidan S. mutan
3.3.4.5 Uji Aktivitas Antibakteri Biji Nangka (Artocarpus heterophyllus lam)
45 – 50oC dihomogenkan sampai media dan bakteri tercampur rata, kemudian dibiarkan sampai media memadat. Dimasukkan kertas cakram yang telah direndam dengan asam lemak biji nangka dengan berbagai konsentrasi kedalam cawan petri yang telah berisi bakteri , kemudian diinkubasi dalam inkubator pada suhu 35 ± 2oC selama 18-24 jam. Selanjutnya diukur diameter daerah hambat di sekitar larutan penguji. Dilakukan dengan cara yang sama terhadap bakteri E.coli dan S.mutans
3.4 Bagan Penelitian
3.4.1 Ekstraksi Asam Lemak Biji Nangka
Dipisahkan dari kulit buah Dikeringkan
Dihaluskan Serbuk Biji nangka
Dimaserasi dengan N-heksana Disaring
Filtrat
Diuapkan sampai pelarut n-heksan habis Biji Nangka
Ampas
3.4.2 Bagan pembuatan Metil Ester 20 g sampel lemak/minyak
Dimasukkan ke dalam labu leher tiga Ditambahkan 40 ml metanol
Ditambahkan 80 ml benzena
Dirangkai alat refluks yang dilengkapi tabung CaCl2
Diteteskan H2SO4(p) sebanyak 2 ml secara perlahan-lahan melalui corong penetes Direfluks selama 3 jam pada suhu 70-80oC Campuran
Didinginkan pada suhu kamar
Diuapkan kelebihan metanol dan benzena dengan rotary evaporator
Destilat Residu
Diekstraksi dengan 100 ml n-heksana
Dicuci dengan 10 ml aquadest sebanyak 3 kali
Lapisan atas Lapisan bawah
Dikeringkan air dengan Na2SO4 anhidrous Disaring
Filtrat Residu
Diuapkan pelarutnya dengan alat rotari evaporator Hasil
3.4.3 Pembuatan MediaMueller Hinton Agar
19 gram media MHA (Mueller Hinton Agar)
Dilarutkan dengan 500ml aquadest di dalam
labu erlenmeyer
Dipanaskan dan diaduk hingga larut dan
mendidih
Disterilkan didalam autoklaf pada suhu 121
0selama 15 menit
3.4.4 Pembuatan Stok Kultur Bakteri
7 gram Media NA (Nutrient Agar
Dilarutkan dengan 250 ml Aquadest kedalam gelas erlenmeyer
Dipanaskan sambil diaduk hingga larut dan mendidih
Disterilkan dalam autoklaf pada suhu 1210C selama 15 menit
Media NA ( Nutrient Agar) Steril
Dituangkan kedalam tabung reaksi sebnyak 3 ml
Dibiarkan pada temperatur kamar sampai memadat pada posisi miring membentuk sudut 30-450
Diambil biakan bakteri Staphylococcus aureus dari strain utama dengan jarum ose lalu digoreskan pada media NA
yang telah memadat
Didinkubasi pada suhu 350C selama 18-24 jam
Stok Kultur Bakteri
3.4.5 Penyiapan untuk Suspensi Bakteri
10 ml Aquadest
Dimasukkan kedalam tabung reaksi ditutup rapat menggunakan kapas
disterilkan dalam autoklaf pada suhu 121oC selama 15 menit
Aquadest steril
Diambil koloni bakteri dari stok kultur Bakteri Staphylococcus aureus dengan menggunakanjarum ose
Disuspensikan kedalam Aquadest steril lalu dihomogenkan
Diukur kekeruhan larutan pada panjang gelombang 580-600nm sampai diperoleh transimitan 25 (disamakan kekeruhan dengan standard Mecfarland)
Inokulum bakteri Staphylococcus aureus
3.4.6. Pengujian Aktivitas Bakteri Ektrak N-heksan dari Biji Nangka
0,1 ml Inokulum Bakteri
Dimasukkan kedalam cawan petri
steril
Ditambahkan dengan 15 ml media Mueller
Hinton Agar (MHA) dengan suhu 45-50
0C
Dihomogenkan sampai media dan bakteri
tercampur rata
Dibiarkan sampai media memadat
Dimasukkan kertas cakram yang sudah direndam
dengan asam lemak dari biji nangka kedalam cawan petri yang
telah berisi bakteri
Diinkubasi selama 18-24 jam pada suhu 35
0C
Diukur diameter zona bening disekitar cakram
dengan jangka sorong
BAB 4
HASIL DAN PEMBAHASAN
4.1 Hasil Penelitian
4.1.1 Metode Penentuan Kadar Asam Lemak Dari Biji Nangka
Kadar asam lemak dari Biji Nangka (Artocarpus heterophyllus lamk) diperoleh hasil minyak berdasarkan metode perendaman dengan menggunakan pelarut N-heksan selama 2 hari diperoleh sebanyak 4,5 gram dalam 1000 g biji nangka
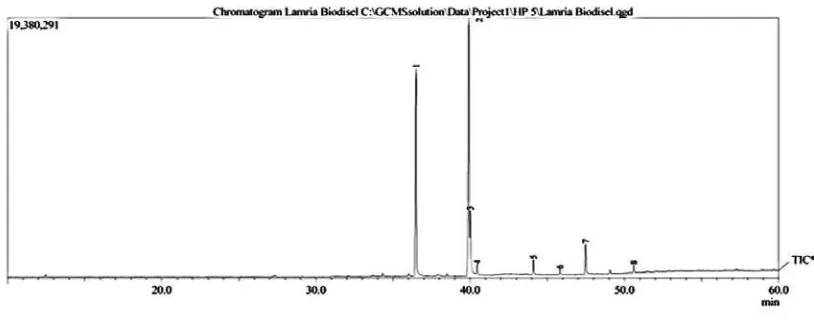
4.1.2. Hasil Analisa dengan GC-MS )
Asam lemak biji nangka hasil perendaman dengan n-Heksan dan sudah di metil ester kemudian dianalisa dengan Gas Cromatography –Mass Spectroscopy (GC-MS)
4.1.3 Data Komatogram GC-MS
Hasil analisa melalui pemeriksaan GC-MS terhadap metil ester asam lemak dari biji nangka diperoleh kromatogram denga memberikan puncak sebanyak 8 jenis
Dari kromatogram asam lemak terdeteksi 8 jenis senyawa seperti pada gambar table 4.2
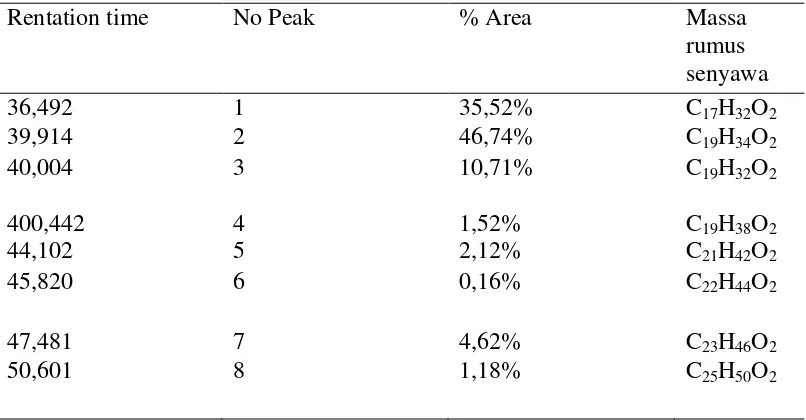
Tabel 4.2 Hasil Analisis GC-MS metil ester Asam lemak biji nangka
Rentation time No Peak % Area Massa
rumus senyawa
36,492 1 35,52% C17H32O2
39,914 2 46,74% C19H34O2
40,004 3 10,71% C19H32O2
400,442 4 1,52% C19H38O2
44,102 5 2,12% C21H42O2
45,820 6 0,16% C22H44O2
47,481 7 4,62% C23H46O2
50,601 8 1,18% C25H50O2
Spesifikasi GC-MS metil ester asam lemak dari biji nangka Asam lemak dari biji nangka hasil maserasi yang sudah di metil ester kemudian di analisis Gas Cromatography-Mass Spektroscopy (GC-MS)
Analisa dengan GC-MS dilakukan dengan kondisi sebagai berikut : Column Oven Temp : 50,0 C
Injection Temp : 300,00 C
Injection Mode : Split
Flow Control Mode : Pressure
Pressure : 13,0 kPa
Total Flow : 40,8 mL/min
Linear Velocity :26,7 cm/sec
Purge Flow : 3,0 mL/min
Split Ratio :68,8
High Pressure Injection : OFF
Carrier Saver : OFF
Oven Temp Program
Rate Temperatur (C) Hold Time ( Min)
5,00 50,0 4,00
290,0 18,00
4.2 Hasil Uji Aktivitas Antibakteri Asam Lemak dari Ekstraksi Biji Nangka
Sifat antibakteri asam lemak dari ekstraksi biji nangka menunjukkan zona hambat pada pertumbuhan beberapa bakteri yaitu Escherichia coli,Staphylococcusaureus dan Streptococcus mutans seperti yang ditunjukkan pada gambar 4.4 dan gambar 4.2 dan 4.3 dibawahini :
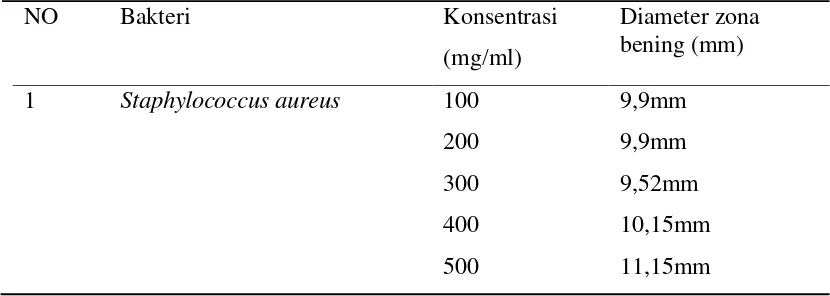
Tabel 4.3.Hasil Zona Bening dari Uji Aktivitas Antibakteri Asam Lemak dari Biji Nangka
NO Bakteri Konsentrasi
(mg/ml)
Diameter zona bening (mm)
1 Staphylococcus aureus 100 9,9mm
200 9,9mm
300 9,52mm
400 10,15mm
2 Escherichia coli 100 9,57mm
200 11,27mm
300 12,4mm
400 23,9mm
500 26,77mm
3 Streptococcus mutans 100 12,77mm
200 13,4mm
300 13,77mm
400 14,15mm
500 16,65mm
Keterangan:
Blanko= kertas cakram direndam dengan pelarut
Dari Tabel 4.4 dapat di ketahui bahwa zona bening yang di ukur dari beberapa bakteri dan beberapa konsentrasi dimana zona bening yang paling aktif menghambat pertumbuhan bakteri yaitu pada bakteri Eschrichi coli dengan konsentrasi 500mg/ml terdapat 26,77 mm
Berikut hasil uji aktivitas antibakteri dari asam lemak biji nangka dengan metode difusi cakram dari beberapa konsentrasi.
4.2. Gambar Zona Hambat Bakteri Staphylococcus aureus
B.Gambar Zona Hambat C. Gambar Zona Hambat dengan dengan Konsentrasi 400mg/ml Konsentrasi 300mg/ml
D.Gambar Zona Hambat E. Gambar Zona Hambat dengan dengan Konsentrasi 200mg/ml Konsentrasi 100mg/ml
4.3 Gambar Zona Hambat Untuk Bakteri Esherichia coli
C.Gambar Zona Hambat D. Gambar Zona Hambat dengan dengan Konsentrasi 300mg/ml Konsentrasi 200mg/ml
E.Gambar Zona Hambat dengan Konsentrasi 100mg/ml
4.4 Gambar Zona Hambat Untuk Bakteri Streptococcus mutan
C.Gambar Zona Hambat D. Gambar Zona Hambat dengan dengan Konsentrasi 300mg/ml Konsentrasi 200mg/ml
E.Gambar Zona Hambat dengan Konsentrasi 100mg/ml
4.3 Pembahasan
4.3.1 Pembuatan Metil Ester Asam Lemak dari Biji Nangka
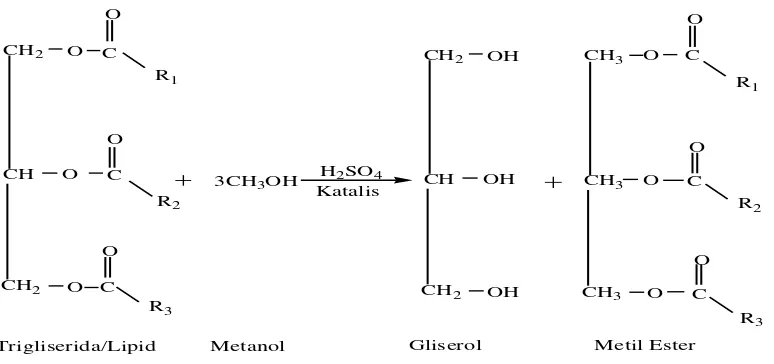
CH2 O C
Trigliserida/Lipid Metanol Gliserol Metil Ester
Gambar 4.3 Reaksi Metanolisis trigliserida membentuk metil ester asam lemak
4.3.2 Analisis GC-MS Metil Ester Asam Lemak Biji Nangka
Untuk menentukan komposisi asam lemak yang terdapat pada biji nangka maka hasil spektrum massa dari masing-masing puncak unknown dibandingkan dengan spektrum massa senyawa yang ada pada daftar libarary GC-MS terdapat 8 jenis senyawa yang dapat teridentifikasi, dilakukan fragmentasi terhadap 6 jenis senyawa yang massa rumus senyawanya dapat disesuaikan dengan standard dari libarary
A. Puncak (peak) 2 dengan Rt 39,914 (46,74%)
A. Sample
B. Standar library
Gambar 4.5 : Spektrum Metil Linoleate Keterangan : A. Sampel B. Standar library
O
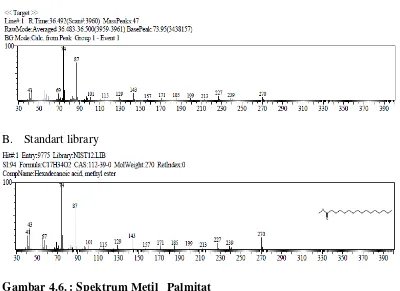
diperoleh dengan data spektrum pada libarary. Yang ;ebih mendekati adalah metil ester hexadecanoic atau metil ester palmitat (Gambar 4.6)
A.Sample
B. Standart library
Gambar 4.6. : Spektrum Metil Palmitat
Keterangan :A. Sampel B. Standart libarary
C.Puncak (peak) 3 dengan Rt 40,004 (10,71%)
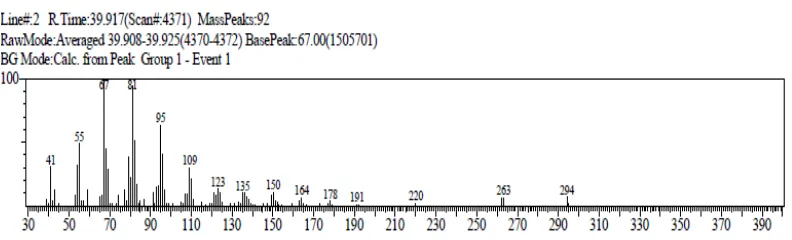
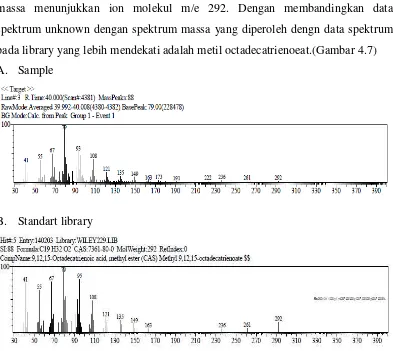
Spektrum ini merupakan senyawa dengan rumus molekul C19H32O2. Data spektum massa menunjukkan ion molekul m/e 292. Dengan membandingkan data spektrum unknown dengan spektrum massa yang diperoleh dengn data spektrum pada library yang lebih mendekati adalah metil octadecatrienoeat.(Gambar 4.7) A. Sample
B. Standart library
Gambar 4.7 : Spektrum Metil Octadecatrienoeat Keterangan : A. Sampel B. Standart library
O
A. Sample
B. Standart library
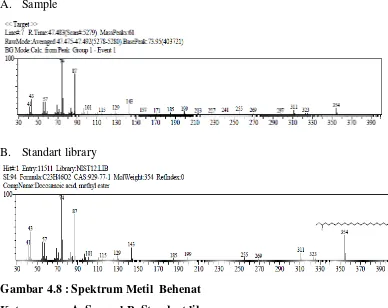
Gambar 4.8 : Spektrum Metil Behenat Keterangan : A. Sampel B. Standart library
E. Puncak (peak) 5 dengan Rt 44,102 (2,12%)
Spektrum ini merupakan senyawa dengan rumus molekul C21H42O2.Data spektum massa menunjukkan ion molekul m/e 326 Dengan membandingkan data spektrum unknown dengan spektrum massa yang diperoleh dengn data spektrum pada library yang lebih mendekati adalah metil ester eicosanoic atau metil ester arahidat (Gambar 4.9)
A. Sample
B. Standart Library
Gambar 4.9 : Spektrum Metil Arachidat Keterangan : A. Sampel B. Standart Library
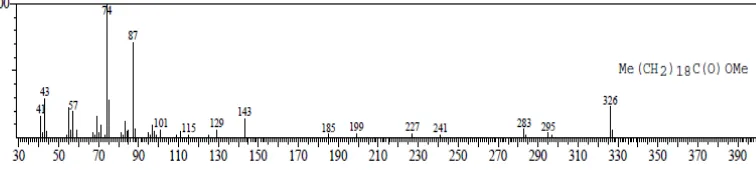
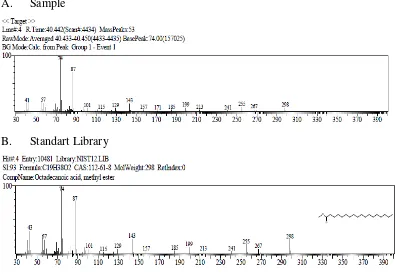
F. Puncak (peak) 4 dengan Rt 40.442 (1,52%)
Spektrum ini merupakan senyawa dengan rumus molekul C19H38O2.Data spektum massa menunjukkan ion molekul m/e 298 Dengan membandingkan data spektrum unknown dengan spektrum massa yang diperoleh dengn data spektrum pada library yang lebih mendekati adalah metil ester Octadecanoic atau metil ester stearat (Gambar 4.10)
A. Sample
B. Standart Library
Gambar 4.10 : Spektrum Metil Stearat Keterangan : A. Sampel B. Standart Library
O
4.3.3 Uji Aktivitas Antibakteri Asam Lemak dari Biji Nangka
penelitian ini adalah metode difusi agar.Pada metode ini aktivitas bakteri terhadap sampel uji ditunjukkan dengan terbentuknya zona hambat disekitar kertas cakram yang menandakan daerah pertumbuhan bakteri.
Pada penelitian ini menggunakan bakteri patogen yang berasal dari gram positif dan gram negatif.Bakteri patogen yang digunakan adalah Staphylococcus aureusEscherichia coli dan Streptococcus Mutans.Berdasarkan Clinical and Laboratory Standars Institute (2012) bahwa suatu senyawa memiliki aktivitas antibakteri dengan zona hambat ≤ 14 mm lemah .(resistant), 15 hingga 19 msm sedang (intermediate) dan ≥ 20 mm kuat. Hasil uji aktivitas antibakteri asam lemak dari biji nangka efektif menghambat perrtumbuhan bakteri S.aureus dan E.coli.
Pada gambar 4.2, 4.3, 4.4 memperlihatkan bahwa asam lemak dari biji nangka memiliki aktivitas antibakteri dengan kategori sedang pada masing-masing konsentrasi dengan zona hambat masing-masing-masing-masing sebesar 16,65 mm dan 14,15 mm terhadap bakteriS.aureus dan pada konsentrasi 500 mg/ml dengan zona hambatmasing-masing sebesar 11,15 mm dan terhadap bakteri E.colipada konsentrasi 500mg/ml sebesar 26,77mm. Adanya perbedaan diameter zona hambat pada kedua bakteri menunjukkan bahwa terdapat perbedaan sentivitas ekstrak pada mikroba uji tersebut.Senyawa yang bersifat sebagai antimikroba dapat menyebabkan kerusakan pada dinding sel serta kerusakan pada membran sel berupa denaturasi protein dan lemak yang menyusun membran sel.
zona hambat pada bakteri E.coli lebih besar karena bakteri tersebut memiliki kandungan lipid yang tinggi.
Munurut Sumitra,telah menguji asam lemak dari daun sirih dan telah diuji aktivitas antibaktri dari asam lemak daun sirih menunjukkan antibakteri yang sangat aktif dengan MIC 6,25��/�� ini dikarenakan komposisi asam lemak dari uji GC-MS. Sedangkan MIC dari asam lemak pada bakteri S.mutans terlihat pada lampiran bahwa asam lemak jenuh menunjukan sangat relatif dibandingkan dengan asam lemak tak jenuh sebesar MIC 3,13��/��tetapi juga pada fraksi asam yang sangat kuat menghambat pertumbuhan aktifitas antibakteri yaitu sebesar 50��/�� pada campuran asam lemak . dan pada pemurnian n-heksana dengan campuran asam lemak menunjukan petumbuhan aktifitas antibakteri yang lebih panjang dengan MIC 12,5��/�� .
BAB 5
KESIMPULAN DAN SARAN
5.1 KESIMPULAN
1. Hasil analisa asam biji nangka yang telah di metil esterkan dengan metode GC-MS dan di peroleh delapan komponen asam lemak dan dimana terdapat dua asam lemak tak jenuh dan enam asam lemak jenuh yaitu :(Metil linoleat 46,74%,Metil palmitat 35,52%, Metil octadecatrienoeat 10,71%, Metil behenat 4,62%, Metil Stearat 1,52%, Metil lignocerat 1,18%,Metil Arahidat 2,12%, Metil heneicosanoeat0,16%.
2. Hasil uji aktifitas antibakteri menunjukan bahwa komponen asam lemak dari biji nangka memiliki aktifitas anti bakteri katagori sedang pada konsentrasi 500mg/ml dengan zona hambat 11,15mm dan 10,15mm untuk bakteri S.aureus dan untuk konsentrasi 500mg/ml dengan zona hambat 23,9mm dan 26,77mm untuk bakteri E.coli dan untuk konsentrasi 500mm dengan zona hambat 14,15mm dan 16,65mm dan dapat disimpulkan bahwa uji aktifitas antibakteri pada ketiga bakteri yang dapat menghambat pertumbuhan bakteri ditunjukan pada bakteri E.coli
5.2 SARAN