LAPORAN PRAKTIKUM KIMIA ORGANIK (KI2051)
PERCOBAAN 4
KROMATOGRAFI KOLOM & KROMATOGRAFI LAPIS
TIPIS: ISOLASI KURKUMIN DARI KUNYIT (
Curcuma longa
L.
) DAN PEMISAHAN ZAT PEWARNA MAKANAN
Nama : Ganjar Abdillah Ammar
NIM : 11213021
Kelompok : 3
Tanggal Percobaan : 8 Oktober 2014 Tanggal Laporan : 15 Oktober 2014 Asisten : Fakhri / 10511070
LABORATORIUM KIMIA ORGANIK
PROGRAM STUDI KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN
ALAM
PERCOBAAN 4
Kromatografi Kolom & Kromatografi Lapis Tipis: Isolasi
Kurkumin dari Kunyit (
Curcuma Longa L.
) dan Pemisahan Zat
Pewarna Makanan
I. Tujuan Percobaan
1. Menentukan nilai Rf hasil perolehan kemurnian fraksi kurkumin dengan uji Kromatografi Lapis Tipis (KLT).
2. Menentukan nilai Rf hasil pemisahan zat warna pada tiap-tiap fraksi eluat kromatografi kolom.
II. Teori Dasar
Kurkumin atau 1,7-bis-(4 hidroksi-3-metoksi fenol) hepta-1,6-diena-3,5 dien merupakan senyawa hasil isolasi dari tanaman Curcuma sp. (Meiyanto, 1999). Kurkumin yang dikenal sebagai bahan alam berupa zat warna kuning ini memiliki berat molekul 386.126 gram per mol. Senyawa kurkumin biasanya terdapat sekitar 1.5-2% dari berat rimpang kunyit kering (Aggarawal et al., 2003).
III. Data Pengamatan
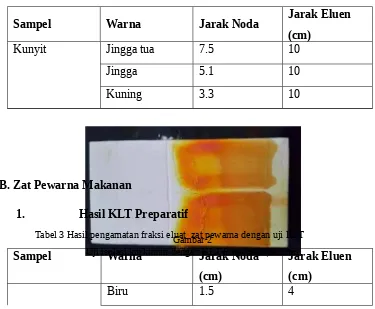
Sampel Warna Jarak Noda Jarak Eluen (cm)
Uji isolasi kurkumin dengan KLT Preparatif (7x5cm) Tabel 1 Hasil pengamatan isolasi kurkumin dengan uji KLT
Tabel 2 Hasil pengamatan isolasi kurkumin dengan uji KLT Preparatif
Pewarna Coklat Merah 1.3 4
Ungu 0.9 4
2. Hasil KLT Referensi
Sampel Warna Jarak Noda(cm) Jarak Eluen (cm)
Jingga tua 1.7 4
Pewarna Ungu Jingga 1.5 4
kuning 1.1 4
Gambar 4
Uji warna coklat hasil isolasi pewarna makanan dengan KLT Gambar 3
Uji isolasi pewarna makanan dengan KLT; Biru, jingga dan ungu (dari bawah ke atas)
Gambar 5
Uji pewarna makanan dengan KLT
Gambar 6
Uji pewarna makanan dengan KLT
IV. Perhitungan dan Pengolahan Data
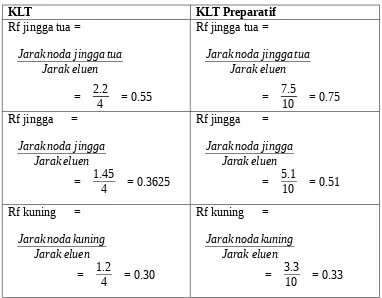
Tabel 5 Perhitungan Rf KLT dan KLT Preparatif isolat kurkumin
= 1.3
Penyampuran 20 gram rimpang kunyit kering -yang digunakan saat percobaan adalah bubuk rimpang- dengan 50 ml diklorometana akan menjadi suatu larutan. Larutan tersebut kemudian direfluks selama 1 jam (sambil menunggu melakukan percobaan pemisahan zat pewarna makanan). Digunakan CHCl2 / diklorometana karena pelarut organik yang baik dan
mudah menguap. Proses refluks dimaksudkan agar memekatkan larutan rimpang kunyit-diklorometana, dengan menguapkan senyawa diklorometana. Selanjutnya refluktan (campuran pekat) di saring dengan penyaring vakum lalu ambil filtrat berupa larutan kuning. Kemudian larutan dipekatkan melalui distilasi penangas air 50 oC, diperoleh distilat berupa
diklorometana dan residu berupa kurkumin. Residu kemerah-merahan yang didapat kemudian dicampurkan dengan 20 ml n-heksana dan diaduk merata. Penambahan n-heksanan pada campuran bertujuan untuk menggumpalkan campuran menjadi padat, memisahkan diri dari pelarut dan kemudian disaring lagi dengan penyaring vakum. Penyaringan dimaksudkan agar diperoleh kurkumin murni berupa padatan yang tertinggal (residu) pada saringan vakum. Selanjutnya padatan dianalisis dengan kromatografi lapis tipis menggunakan eluen CH2Cl2 : MeOH = 97:3, akan memunculkan 3
komponen utama. 3 komponen utama yang didapat, timbul warna (Rf) adalah kuning (1.2), jingga (1.45) dan jingga tua (2.2).
KLT preparatif 1 kelompok untuk 2 percobaan. Perlu menyiapkan sampel yang akan dielusi, yaitu 0.1 gram ekstrak kasar (residu vakum) dilarutkan sesedikit mungkin pelarut CH2Cl2 : MeOH = 99:1. Setelah itu diteteskan
perlahan, secara menyebar dengan menggunakan pipet tetes. Perlakuan dilakukan beberapa kali untuk memastikan semua sampe terserap pada pelat silikat KLT preparatif. Perlu dicatat, setiap pengulangan tetesan, tunggu sampai kering penetasan sebelumnya dan tetesan selanjutnya berada di lokasi tetesan sebelumnya
Setelah noda kering, dilakukan elusi dengan eluen CH2Cl2 : MeOH =
97:3 untuk melihat pergerakan sampel. Digunaka eluen tersebut karena sebagai fasa gerak pada pengujian yang merupakan senyawa polar disamping fasa diam berupa silika gel, senyawa polar. Langkah selanjutnya sampel beserta KLT preparatif dilihat dibawah sinar lampu UV, untuk memunculkan dengan jelas pita komponen warna utama. Akhirnya diperoleh 3 warna utama hasil uji sampel, yaitu kuning 0.33 cm, jingga 0.51 cm dan jingga tua 7.5 cm. Diketahui bahawa zat yang memiliki kepolaran tinggi akan tertahan lebih lama pada fasa diam, saat ini ditunjukkan oleh senyawa demetoksi kurkumin yang berwarna kuning. Kepolaran lebih rendah diikuti oleh bisdemetoksi kurkumin (warna jingga) dan jarak terjauh diperoleh oleh kurkumin ditunjukkan warna jingga tua.
Sebenarnya sebelum mengecek jarak noda 3 warna utama, dilakukan dahulu pemisahan komponen yang dipilih dengan mengerok lapisan silika dan ditampung pada kertas. Silika Silika dipindahkan ke dalam gelas kimia dan dilarutkan saring dan cuci dengan diklorometana. Filtrat kemudian diuapkan dengan evaporator (atau distilasi penangas air 60 oC. Yang terakhir
dilakukan uji kemurnian fraksi dengan KLT (eluen CH2Cl2 : MeOH = 97:3).
Sembari percobaan seputar isolasi kurkumin dilakukan, diuji cobakan juga pemisahan zat pewarna makanan. Penyiapan sampel adalah dengan zat pewarna makanan sebesar 0.5 gram dilarutkan dalam sedikit air atau etanol:air = 1:2. Larutan disimpan setelah penyiapan kromatografi kolom selesai.
Kromatografi kolom dapat dibuat dengan dua car, yaitu dengan syringe plastik ditambah 1.5 – 2 gram silika gel atau dengan kolom pipet tetes bersama silika gel yang memenuhi 3/4 kolom. Yang dipilih dalam percobaan menggunakan syringe plastik bersama 1.5-2 gram silika gel.. yang sebelum ditambah silika gel diberi kapas atau tisu yang di gumpalkan didasar syringe (output point). Setelah itu digunakan pelarut larutan NaCl 1% untuk membasahi dan mengembangkan silika gel dalam kolom.
Setelah didapat hasil pemisahan warna, warna-warna sebelum dan sesudah kromatografi kolom di uji pada KLT dengan menotolkan sampel zat pewarna dengan larutan warna baku yang telah tersedia pada pelat KLT 7x5cm. Perlu digunakan pelarut butanol:etanol:ammonia 2% = 3:1:2 sebagai eluen. Didapat 3 warna penyusun warna utama, yaitu biru dengan jarak 1.5 cm, merah dengan jarak 1.3 cm dan ungu dengan jarak 0.9 cm. Dari sini dapat diketahui bahwa biru menempati posisi teratas dalam pemisahan warna, yang menunjukkan sifat warna biru, dengan Rf= 0.375, yang lebih nonpolar dari yang lainnya (karena tidak tertahan lama pada fasa diam). Sedangkan ungu memiliki sifat zat yang paling polar dengan Rf= 0.225 dan merah berada diantara kedua sifat biru dan ungu dengan Rf = 0.325.
Telah diketahui Rfref dari pada KLT zat pewarna makanan, yaitu warna
biru= 0.425, merah= 0.375 dan ungu= 0.275. Terdapat perbedaan yang signifikan antara Rf hasil percobaan dengan Rf referensi. Rfref selalu
VI. Kesimpulan
Berdasarkan hasil percobaan diperoleh nilai Rf hasil perolehan kemurnian fraksi kurkumin pada KLT yaitu 0.55 dan pada KLT Preparatif sebesar 0.75 yang ditunjukkan oleh warna jingga tua. Nilai Rf hasil pemisahan zat pewarna pada masing-masing fraksi adalah warna biru sebesar 0.375, warna merah sebesar 0.325 dan warna ungu sebesar 0.225.
VII. Daftar Pustaka
Khopkar, S.M. 2003. Konsep Dasar Kimia Analitik. Jakarta: UI-Press Mayo, D.W., Pike, R.M., Forbes, D.C. 2011. Microscale Organix
Laboratory: with Multistep and Multiscale Syntesis, 5th
edition,. John Willey & Sons. New York. P. 61-67; 129-140.
Meiyanto, E. 1999. Kurkumin Sebagai Obat Anti Kanker: Menelusuri
Mekanisme Aksinya, “Majalah Farmasi Indonesia”. 10(4).
Pasto, D., Johnson, C., Miller, M. 1992. Experiments and Techniques in
Organic Chemistry. Prentice Hall Inc., New Jersey. P. 47-55;
396-398.
Williamson. 1999. Macroscale and Microscale Organic Experiments, 3rd
edition. Boston. P 82-121.