LAPORAN PRAKTIKUM KIMIA ORGANIK DISTILASI MINYAK ATSIRI
Tujuan Percobaan : 1. Mempelajari teknik pemisahan senyawa berdasarkan perbedaan titik didih.
2. Mempelajari metode ekstraksi minyak atsiri menggunakan prinsip hidrostilasi.
Pendahuluan
Pemisahan suatu senyawa berdasarkan perbedaan titik didih dapat digunakan sebagai salah satu dasar proses distilasi. Distilasi digunakan untuk memisahkan senyawa volatil dari senyawa nonvolatil. Senyawa volatil berbau yang tak larut dalam air salah satunya yaitu minyak atsiri. Alasan tersebut adalah hal yang mendasari praktikum ini. Praktikum distilasi minyak atsiri menggunakan prinsip hidrodistilasi (Tim Penyusun, 2016).
Penguapan dan distilasi umumnya merupakan proses pemisahan satu tahap. Proses hidrodistilasi memerlukan air agar proses tersebut dapat berjalan dengan baik. Uap panas dihasilkan dari air yang dimasukkan kedalam labu kemudian dipanaskan pada temperatur tinggi. Air yang dihasilkan saat dicampur dengan senyawa hidrokarbon lainnya akan menimbulkan bau dari senyawa hidrokarbon yang bercampur tersebut (Harper, 1986).
tersebut dipisahkan dengan separator pemisah minyak untuk diambil minyaknya (Guenther, 1987).
Komponen kimia minyak atsiri pada umunya terdapat dalam suatu tanaman dan dipengaruhi oleh lingkungan tempat tumbuh, maupun metode isolasi yang digunakan. Isolasi minyak atsiri dari bahan alam seperti sereh dan cengkeh dilakukan melalui penyulingan bersama air (hidrodistilasi). Air panas akan memecah ester menjadi alkohol dan asam karboksilat. Minyak atsiri bersifat mudah menguap karena titik didihnya rendah. Minyak atsiri masuk dalam golongan senyawa organik terpenoid dan fenil propan yang bersifat larut dalam lemak (lipofil). Penyusunan minyak atsiri dari kelompok terpenoid dapat berupa terpena yang tidak membentuk cincin, bercincin satu maupun bercincin dua. Minyak atsiri yang berasal dari bunga cengkeh banyak mengandung senyawa eugenol (Guenther, 1987).
Minyak atsiri dari beberapa tanaman yang bersifat sebagai antibakteri. Senyawa turunan hidrokarbon teroksigenasi (fenol) memiliki daya antbakteri yang kuat. Fenol merupakan senyawa dengan gugus –OH yang terikat langsung pada cincin aromatik. Beberapa contoh fenol adalah metil salisilat, didapat dari pohon menjalar diamerika serikat, tirosin yang merupakan asam amino yang terdapat pada protein dan eugenol yang terdapat dalam minyak dari daun cengkeh. Senyawa fenol seringkali disebut dengan sebagai senyawa hidroksi. Senyawa fenol banyak terdapat dialam dan merupakan intermediet bagi industri untuk berbagai macam produk seperti adesif dan antiseptik (Riswiyanto, 2009).
Material Safety Data Sheet (MSDS) a. Magnesium Sulfat
Magnesium sulfat memiliki rumus kimia MgSO4. Magnesium sulfat memiliki sifat kimia dan sifat fisik berupa padatan dan mudah larut dalam air dingin. Berat molekul magnesium sulfat yaitu 120,38 g/mol. Bahan ini berbahaya jika terjadi kontakkulit, mata, tertelan maupun terhirup. Penanganan pertama saat magnesium sulfat terkena mata yaitu lepakan kontak mata dan basuh mata menggunakan air dingin selama 15 menit (Anonim, 2016).
b. Aquades
Aquades merupakan senyawa kimia yang mempunyai rumus molekul H2O.
berbau. Aquades memiliki berat molekul 18,02 g/mol. Titik didih aquades adalah 100℃ ( 212℉ ) dan pH 7 (netral). Bahan kimia ini memiliki berat jenis 1, dan tekanan uap 2,3 kPa pada suhu 20℃ . Bahan ini tidak bersifat korosif atau merusak baik untuk kulit, mata, pernafasan maupun pencernaan (Anonim, 2016). Prinsip Kerja
Adapun prinsip kerja dalam percobaan distilasi minyak atsiri adalah mengisolasi minyak atsiri dari bagian tanaman dengan metode distilasi. Distilasi memiliki prinsip kerja utama dimana terjadi pemanasan dan salah satu komponen campurannya akan menguap setelah mencapai titik didihnya, yang paling dahulu menguap merupakan yang bersifat volatil atau mudah menguap. Uap tersebut akan masuk ke dalam pipa pada kondensor sehingga dihasilkan tetesan-tetesan yang turun ke erlenmeyer yang disebut juga destilat. Pemisahan zat dengan perbedaan titik didih ini dapat dilakukan dengan menggunakan prinsip dari hidrodestilasi. Kemudian terbentuklah minyak atsiri dalam wujud cair.
Alat
Pisau, satu set alat distilasi dan gelas ukur 5 mL. Bahan
Bunga cengkeh, sereh, magnesium sulfat anhidrat, batu didih. Prosedur Kerja
Sampel bunga cengkeh dan sereh dipotong kecil-kecil dan disiapkan satu set alat distilasi. Sampel sebanyak 50 gram dimasukkan kedalam labu alas bulat ukiuran 250 mL dan ditambahkan akuades hingga setengah volume total labu kemudian ditambahkan batu didih. Labu alas bulat dipanaskan pada mantel pemanas secara perlahan-lahan dan dihentikan setelah diperoleh distilat sebanyak 100 mL atau setelah dipanaskan selama 1-1,5 jam. Volume distilat yang didapatkan dicatat dan didiamkan beberapa saat sampai diperoleh 2 fasa, yaitu
aqueous phase dan organic phase. Minyak atsiri dipisahkan dari air yang ada
didalam campuran distilat lalu ditambahkan sedikit magnesium sulfat pada distilat minyak atsiri. Minyak atsiri diperoleh secara dekantasi dan dicatat volume yang didapatkan. Rendemen minyak atsiri yang didapatkan dihitung serta diamati bau dan wrna dari minyak atsiri tersebut.
No .
Perlakuan Waktu
1. Preparasi alat dan bahan 10 menit 2. Pemanasan labu pada mantel 1-1,5 jam Data dan Perhitungan
No. Perlakuan Volume Keterangan
Destilat Minyak atsiri
1. Pemanasan cengkeh -Berbau cengkeh
yang sangat
menyengat
-Terbentuk dua fase -Tidak berwarna -Terdapat gelembung seperti minyak
2. Penambahan MgSO4 -Larutan berwarna putih
-Berbau tetap seperti sebelum penambahan -Terdapat minyak pada permukaan namun sangat sedikit Hasil
No Perlakuan Gambar Pengamatan Keterangan
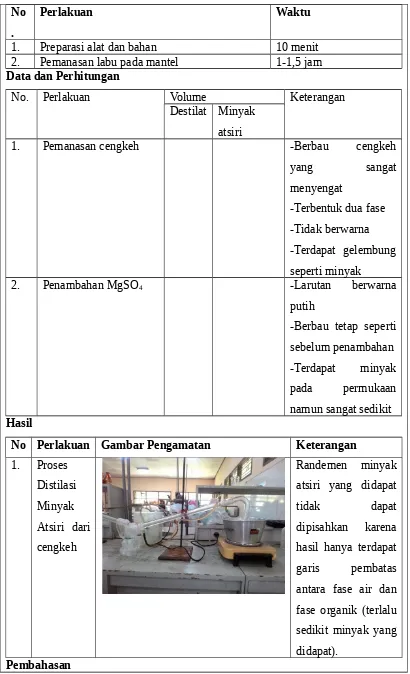
1. Proses Distilasi Minyak Atsiri dari cengkeh
Randemen minyak atsiri yang didapat tidak dapat dipisahkan karena hasil hanya terdapat garis pembatas antara fase air dan fase organik (terlalu sedikit minyak yang didapat).
Distilasi merupakan salah satu teknik pemisahan berdasarkan perbedaan titik didih sehingga zat (senyawa) yang memiliki titik didih terendah akan menguap terlebih dahulu, kemudian pada saat didinginkan akan mengembun dan menetes sebagai zat murni (destilat). Prinsip distilasi yaitu memisahkan senyawa volatil dari senyawa nonvolatil. Metode distilasi ini digunakan untuk mendistilasikan minyak atsiri yang terkandung dalam sereh dan cengkeh. Distilasi minyak atsiri menggunakan prinsip hidrodistilasi, yaitu penyulingan suatu campuran yang berwujud cairan yang tidak saling bercampur, sehingga membentuk dua fase atau dua lapisan. Proses hidrodistilasi dilakukan dengan bantuan air yang seluruh bahannya terendam dalam labu. Faktor penting dalam hidrodistilasi adalah air dalam labu harus selalu dalam jumlah yang cukup selama proses distilasi untuk mencegah overheat dan rusaknya sampel.
Prosedur pertama dari proses distilasi yaitu pemanasan yang menggunakan labu alas bulat pada penangas air, namun pemanasan menggunakan penangas air sangat tidak efektif karena membutuhkan waktu yang sangat lama. Penangas air yang digunakan saat proses distilasi tidak menghasilkan distilat sama sekali, maka dari itu proses distilasi diubah menggunakan mantel pemanas. Pemanasan sampel dilakukan dengan penambahan pelarut air. Penambahan air berguna sebagai pelarut karena air memiliki sifat kepolaran yang berbeda dengan minyak atsiri sehingga minyak atsiri akan mudah dipisahkan dari distilat karena air dan minyak atsiri tidak saling melarutkan.
Distilat yang dihasilkan dari pemanasan sampel (cengkeh) yaitu kandungan minyak yang dihasilkan cukup banyak dibandingkan dengan sampel sereh, hal ini dikarenakan luas permukaan dari cengkeh lebih besar daripada luar permukaan dari sereh. Menurut literatur, kandungan minyak atsiri dalam cengkeh yaitu sekitar %, namun pada praktikum ini tidak didapatkan minyak atsiri sama sekali. Kegagalan mendapatkan minyak atsiri dalam sampel dikarenakan beberapa faktor, diantaranya yaitu distilasi dalam skala laboratorium merupakan distilasi sederhana dengan skala kecil. Hasil distilasi sederhana dengan skala kecil ini juga menghasilkan distilat yang sedikit pula. Metode distilasi sebenarnya efektif digunakan untuk memisahkan suatu senyawa dengan prinsip perbedaan titik didih dengan syarat pemisahan tersebut harus menggunakan skala dengan kapasitas yang besar sehingga menghasilkan distilat atau minyak yang banyak pula. Faktor selanjutnya yaitu komposisi perbandingan air dan bahan yang tidak seimbang. Massa sampel yang digunakan saat praktikum ini yaitu hanya 25 gram sedangkan air yang digunakan tidak dihitung volumenya.
Mekanisme ekstraksi minyak atsiri pada daun cengkeh yaitu dengan cara penyulingan atau metode distilasi yang dilakukan pada praktikum ini. Bahan yang akan di suling dimasukkan kedalam labu alas bulat yang telah diisi air sebagai pelarut. Uap yang dihasilkan dari perebusan air dan sampel dialirkan melalui pipa kondensor dan ditampung dalam erlenmeyer. Distilat yang diperoleh terdiri dari lapisan minyak dan air yang dapat dipisahkan. Minyak daun cengkeh diberi tetesan MgSO4, hal ini bertujuan untuk mengikat air agar minyak atsiri dalam cengkeh dapat diketahui jumlah kandungannya. Persamaan reaksi yang terjadi saat penambahan MgSO4 yaitu sebagai berikut :
MgSO4 (aq) + H2O (l) MgOH (aq) + HSO4- (aq)
Bau yang dihasilkan setelah penambahan MgSO4 tidak berubah, sama seperti sebelum penambahan MgSO4.
Kesimpulan
Distilasi merupakan metode pemisahan senyawa berdasarkan perbedaan titik didih. Salah satu metode distilasi adalah hidrodistilasi yang menggunakan air sebagai pelarutnya. Sampel cengkeh yang digunkan adalah 25 gram dengan waktu distilasi selama 1 jam. Distilat yang dihasilkan tidak dapat dipisahkan antara air dan minyak atsirinya dikarenakan beberapa faktor, yaitu pemisahan dalam skala kecil akan menghasilkan distilat atau minyak atsiri yang sedikit pula sehingga susah untuk dipisahkan. Faktor yang kedua yaitu perbandingan jumlah sampel yang digunakan tidak seimbang dengan air atau pelarut yang ditambahkan.
Referensi
Guenther, E. 1987. Minyak Atsiri Jilid I. Penerjemah S. Ketaren. Jakarta : UI Press.
Harper. 1986. Dayri Technology and Engineering. Jakarta: PT Aksara Cipta. Riswiyanto, 2009. Kimia Organik. Jakarta: Erlangga.
Tim Penyusun. 2015. Petunjuk Praktikum Kimia Organik. Jember: FMIPA Universitas Jember
Saran
Diharapkan untuk praktikum selanjutnya, massa sampel yang digunakan untuk distilasi disesuaikan dengan volume dari labu alas bundar agar distilat yang dihasilkan sesuai dengan yang diharapkan sehingga minyak atsiri yang dihasilkan dapat dipisahkan dari air.