BAB II
TINJAUAN PUSTAKA
2.1 Ruang Lingkup Lingkungan
Lingkungan merupakan media atau suatu areal, tempat atau wilayah yang
di dalamnya terdapat bermacam-macam bentuk aktivitas yang berasal dari
ornamen-ornamen penyusunnya. Ornamen-ornamen yang ada dalam dan
membentuk lingkungan, merupakan suatu bentuk sistem yang saling mengikat,
saling menyokong kehidupan mereka. Keadaan yang saling mengikat sering
menyebabkan ketidakseimbangan dalam lingkungan yang sering disebut keadaan
tercemar. Lingkungan dikatakan tercemar sebagai akibat masuk dan atau
dimasukkannya suatu zat atau benda asing ke dalam tatananan lingkungan itu.
Perubahan sebagai akibat dari kemasukkan benda asing itu, memberikan pengaruh
(dampak) buruk terhadap organisme yang sudah ada dan hidup dengan baik dalam
tatanan lingkungan tersebut (Palar,2008).
Perubahannya yang terjadi pada lingkungan juga merupakan akibat dari
adanya interaksi antara manusia dengan lingkungan. Interaksi yang terjadi antara
manusia dengan lingkungan tidak selalu mendapatkan keuntungan, tetapi bisa
juga mendapatkan kerugian (Soemirat,2009). Perubahan dalam lingkungan
sebagai akibat dari adanya interaksi antara manusia dengan lingkungan
menyebabkan banyak hal terjadi. Salah satunya ialah adanya limbah yang
memberi dampak pada manusia. Menurut Palar (2008) Limbah dapat digolongkan
atas beberapa jenis yaitu :
a. Limbah berdasarkan jenis yaitu limbah padat dan limbah cair.
b. Limbah berdasarkan pada sifatnya yaitu limbah organik dan limbah
an-organik.
c. Limbah berdasarkan pada sumbernya yaitu limbah rumah tangga
(domestik) dan limbah industri.
2.2 Ikan Asin
Ikan asin merupakan bahan makanan yang banyak dikonsumsi masyarakat
(Esti,2000). Pada dasarnya proses pembuatan ikan asin yang paling pokok adalah
penggaraman dan pengeringan. Menurut Siregar (2005) secara umum proses
penggaraman dapat dilakukan dengan tiga cara, yaitu:
a. Penggaraman kering (Dry salting)
Penggaraman kering dilakukan dengan menaburkan garam kristal pada lapisan
ikan yang disusun rapi. Selama penggaraman berlangsung terjadi penetrasi ke
dalam tubuh ikan karena adanya perbedaan konsentrasi. Cairan tersebut akan
cepat melarutkan kristal-kristal garam (Afrianto dan Liviawaty, 1994). Dalam
proses penggaraman ini cairan tubuh ikan akan diserap oleh kristal-kristal garam.
Akibatnya, kristal garam akan mencair dan terbentuk larutan garam pekat.dalam
kondisi demikian larutan garam pekat tersebut akan meresap ke dalam daging ikan
sehingga akan mengubah rasa dan tekstur(kekenyalan) daging ikan tersebut.
b. Penggaraman basah (Wet salting)
Penggaraman basah dilakukan dengan merendam ikan dalam larutan garam
pekat. Pada dasarnya cara ini mirip dengan penggaraman kering. Bedanya larutan
garam perendaman ikan dibuat lebih dulu sehingga konsentrasi kepekatan larutan
ini dapat dibuat sesuai dengan selera dan keperluan. Untuk perendaman ikan
berukuran besar dan waktu perendamannya cukup singkat diperlukan larutan
garam jenuh dengan konsentrasi yang cukup tinggi . Dalam hal ini bisa pula
menggunakan larutan garam yang konsentrasinya lebih rendah, tetapi selama
proses perendaman harus ditambahkan kristal garam secukupnya untuk
meningkatkan konsentrasinya.
c. Pelumuran garam (Kench salting)
Pada proses ini, pengawetan ikan dengan kristal garam pada dasarnya mirip
dengan penggaraman kering, tetapi larutan garam yang terbentuk dibiarkan
mengalir ke luar wadah. Wadah yang digunakan tidak kedap air tetapi berupa
keranjang. Ikan yang dilumuri garam ditumpuk dalam keranjang dan dipadatkan
serta ditutup rapat. Menurut Agus (1995) untuk ukuran kristal garam yang
digunakan sebaiknya juga disesuaikan dengan besar kecilnya ukuran ikan. Untuk
ikan-ikan kecil sebaiknya menggunakan butiran garam yang lebih halus agar
meresapnya lebih mudah sedangkan untuk ikan-ikan sedang dan besar, sebaiknya
menggunakan butiran garam ukuran sedang.
2.3 Dampak Mengkonsumsi Ikan Asin
Menurut Hendrawan Ariwibowo (2013) paparan non-viral yang paling
konsumsi ikan asin. Konsumsi ikan asin meningkatkan risiko 1,7 sampai 7,5 kali
lebih tinggi dibandingkan yang tidak mengkonsumsi. Potensi karsinogenik ikan
asin didukung dengan penelitian pada tikus disebabkan proses pengawetan dengan
garam tidak efesien sehingga terjadi akumulasi nitosamin yang dikenal karsinogen
pada hewan. Enam puluh dua persen pasien karsinoma nasofaring mengkonsumsi
secara rutin makanan fermentasi yang diawetkan.
2.4 Klasifikasi Laut Berdasarkan Kedalaman
Menurut Nyabekken (1988) berdasarkan kedalamannya, laut dibagi
menjadi 4 zona, yaitu zona lithoral, zona neritis, zona bathial, dan zona abisal.
a. Zona Lithoral
Zona Lithoral adalah wilayah pantai atau pesisir atau shore. Pada saat air
laut pasang wilayah ini tergenang air dan pada saat air laut surut wilayah ini
berubah menjadi daratan. Zona Lithoral juga merupakan daerah pantai yang
terletak di antara pasang tertinggi dan surut terendah. Oleh karena itu wilayah ini
sering juag disebut wilayah pasang surut.
b. Zona Neritis
Zona Neritis (wilayah laut dangkal) yaitu batas wilayah pasang surut
hingga kedalaman 50 m. Pada zona ini masih dapat ditembus oleh sinar matahari,
sehingga pada wilayah ini paling banyak terdapat berbagai jenis kehidupan baik
c. Zona Bathial
Zona Bathial (wilayah laut dalam) adalah wilayah laut yang memilki
kedalaman antara 50 m hingga 1800 m. Wilayah ini tidak dapat tertembus sinar
matahari. Oleh karena itu kehidupan organismmenya tidak sebanyak yang
terdapat di wilayah Neritis. Menurut Darmono (2001) kandungan logam berat di
laut dalam lebih rendah daripadan di laut dangkal. Hal ini disebabkan karena
lautan dapat melarutkan dan menyebarkan bahan-bahan tersebut sehingga
konsentrasinya menjadi menurun, terutama di daerah laut dalam. Kehidupan laut
dalam juga terbukti lebih sedikit terpengaruh daripada laut dangkal. Daerah
pantai, terutama daerah muara sungai sering mengalami pencemaran berat, yang
disebabkan karena proses pencemaran yang berjalan terus-menerus secara
perlahan sehingga terjadi akumulasi.
d. Zona Abisal
Zona Abisal (wilayah laut sangat dalam) yaitu wilayah laut yang memilki
kedalaman di atas 1800 m. Di wilayah ini suhunya sangat dingin dan tidak ada
tumbuh-tumbuhan. Jenis hewan yang dapat hidup di wilayah ini sangat terbatas.
2.5 Pencemaran Logam Berat di Perairan
Pesatnya pembangunan dan penggunaan berbagai bahan baku logam bisa
berdampak negatif, yaitu munculnya kasus pencemaran yang melebihi batas
sehingga mengakibatkan kerugian dan meresahkan masyarakat yang tinggal di
sekitar daerah perindustrian maupun masyarakat penggunaan produk industri
menimbulkan efek gangguan terhadap kesehatan manusia. Efek logam berat
secara langsung akan menghalangi kerja enzim yang menyebabkan metabolisme
tubuh terganggu, alergi, bersifat mutagen atau karsinogen bagi manusia maupun
hewan (Wahyu dkk,2008).
Logam berat menjadi berbahaya disebabkan sistem bioakumulasi.
Bioakumulasi berarti peningkatan konsentrasi unsur kimia tersebut dalam tubuh
makhluk hidup. Akumulasi atau peningkatan konsentrasi logam berat di alam
mengakibatkan konsentrasi logam berat di tubuh manusia sangat tinggi. Jumlah
yang terakumulasi setara dengan jumlah logam berat yang tersimpan dalam tubuh
ditambah yang diambil dari makanan, minuman, atau udara yang terhirup. Jumlah
logam berat yang terakumulasi lebih cepat dibandingkan dengan jumlah yang
terekskresi dan terdegradasi (Martaningtyas,2005).
Menurut Wahyu (2008) polutan logam yang mencemari lingkungan baik
di lingkungan udara, air, dan tanah berasal dari proses alami dan kegiatan industri.
Proses alami antara lain siklus alamiah sehingga bebatuan gunung berapi bisa
memberikan kontribusi ke lingkungan udara, air, dan tanah. Kegiatan manusia
yang bisa menambah polutan bagi lingkungan berupa kegiatan industri,
pertambangan, pembakaran bahan bakar, serta kegiatan domestik lain yang
mampu meningkatkan kandungan logam di lingkungan udara, air, dan tanah.
Pencemaran logam di darat, yakni di tanah, selanjutnya akan mencemari bahan
pangan, baik yang berasal dari tanaman atau hewan dan akhirnya dikonsumsi oleh
manusia. Pencemaran logam, baik dari industri, kegiatan domestik, maupun
mencemari manusia melalaui ikan, air minum, atau sumber irigasi lahan pertanian
sehingga tanaman sebagai sumber pangan manusia tercemar logam. Pencemaran
logam melalui udara terjadi beberapa jalur. Salah satunya adalah melaui kontak
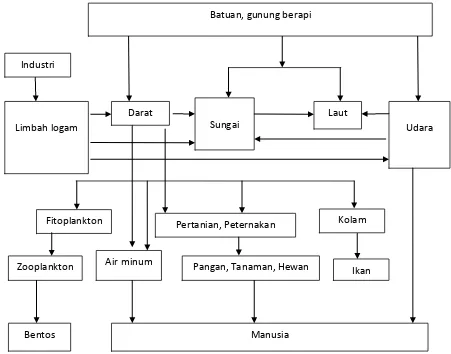
langsung dengan manusia atau proses inhalasi. Hal ini bisa dilihat lebih jelas pada
gambar berikut
Gambar 2.1 Perjalanan Logam Sampai ke Tubuh Manusia (Klaassen et al, 1986; Marnonof, 2003)
Salah satu dampak tercemarnya lingkungan, adanya keberadaan logam di badan
perairan. Keberadaan logam di perairan dapat berasal dari sumber-sumber alamiah
dan dari aktivitas yang dilakukan oleh manusia. Di samping itu, partikel-partikel
Batuan, gunung berapi
Industri
Limbah logam
Darat
Sungai
Laut
Udara
Fitoplankton
Zooplankton
Pertanian, Peternakan Kolam
Air minum
Pangan, Tanaman, Hewan Ikan
logam yang ada di udara, dikarenakan oleh hujan, juga dapat menjadi sumber
logam di badan perairan. Logam-logam berat yang terlarut pada badan perairan
pada konsentrasi tertentu akan berubah fungsi menjadi sumber racun bagi
kehidupan perairan. Ada banyak faktor yang mempengaruhi daya racun logam
berat yang terlarut dalam air yaitu :
a) Bentuk logam dalam air
Bentuk logam dalam air akan mempengaruhi tingkat keracunan logam
berat tersebut pada kehidupan perairan. Adapun bentuk logamnya terbagi menjadi
dua senyawa yaitu senyawa organik dan senyawa anorganik. Senyawa organik
dan senyawa anorganik ini terbagi lagi menjadi dua yaitu yang larut dalam air dan
yang tidak dapat larut dalam air. Senyawa-senyawa organik yang larut dalam air
mempunyai tingkat racun yang lebih tinggi, karena dengan mudah diserap oleh
biota yang ada dalam air. Bryan (1976) menyatakan bahwa logam berat yang
mencemari perairan mengalami perpindahan minimal melalui tiga proses yaitu
pengendapan, adsorbsi, dan adsorbsi oleh ikan, kerang, udang, dan tumbuhan air.
Jika konsentrasi logam berat lebih tinggi daripada daya larut minimal komponen
yang terbentuk dari logam dan anion, maka akan terjadi endapan.
b). Keberadaan logam-logam lain
Adanya logam-logam lain dalam perairan dalam air dapat menyebabkan
logam-logam tertentu menjadi sinergentis atau sebaliknya, menjadi antagonis bila
telah membentuk suatu ikatan. Di samping itu, interaksi antara logam-logam
tersebut bisa juga gagal atau tidak terjadi sama sekali. Tetapi untuk logam-logam
membentuk senyawa dapat berubah fungsi menjadi racun yang sangat berbahaya
dan atau mempunyai daya racun yang berlipat ganda. Sebaliknya, untuk
logam-logam berat yang bersifat antagonis, apabila terjadi persenyawaan dengan
pasangannya maka daya racun yang ada pada logam berat tersebut akan
berkurang(semakin kecil).
c). Fisiologis dari biota (organismenya)
Proses fisiologi yang terjadi pada setiap biota turut mempengaruhi tingkat
logam berat yang menumpuk (akumulasi) dalam tubuh dari biota perairan. Besar
kecilnya jumlah logam berat yang terkandung dalam tubuh akan daya racun yang
ditimbulkan oleh logam berat. Di samping itu proses fisiologi ini turut
mempengaruhi peningkatan kandungan logam berat dalam badan perairan. Ada
biota-biota tertentu yang mempunyai kemampuan untuk
menetralisasi(mentoleransi) logam-logam berat tertentu sampai pada konsentrasi
tertentu pula (mempunyai toleransi tinggi). Sementara itu, biota-biota lainnya
tidak memiliki kemampuan untuk menetralisasi daya racun dari logam-logam
berat yang masuk(toleransi rendah). Menurut Moriaty (1987) , logam berat yang
masuk ke perairan dapat merubah struktur komunitas perairan, jaringan makanan,
genetik, bentuk fisik , dan resistensi biota air. Logam berat dapat merusak
stabilitas, keanekaragaman, dan kedewasaan ekosistem perairan.
d). Kondisi biota
kondisi dari biota-biota berkaitan dengan fase-fase kehidupan yang dilalui
oleh biota dalam hidupnya( Palar,2008). Menurut Manahan (2002) akumulasi
logam berat dalam air, kadar logam berat dalam sedimen, Ph air dan Ph sedimen
dasar perairan, tingkat pencemaran air dalam bentuk COD (Chemical Oxygen
Demand), kandungan sulfur dalam air dan sedimen, jenis ikan, umur dan ukuran
tubuh. Bila konsentrasi logam berat tinggi dalam air, ada kecenderungan
konsentrasi logam berat tinggi dalam air, ada kecenderungan konsentrasi logam
tersebut tinggi dalam sedimen, dan akumulasi logam berat dalam tubuh ikan
semakin tinggi.
Pergerakan logam berat serta ketersediaanya di lingkungan perairan
tentunya akan memberikan dampak yang buruk pada biota perairan salah satunya
adalah ikan yang mana akan berdampak juga pada manusia. Hal ini terlihat dari
adanya hasil penelitian. Sedangkan menurut hasil penelitian Rosmidah pada tahun
2004 diketahui bahwa kadar merkuri pada ikan tongkol sebesar 0,0001265 ppm,
ikan gembung 0,0000779 ppm, ikan dencis sebesar 0,0001151 ppm, ikan pari
sebesar 0,0001122 ppm, ikan kerapu sebesar 0,0001179 ppm, ikan gabus pasir
sebesar 0,0001322 ppm, ikan mujair sebesar 0,0001408 ppm dan pada kerang
sebesar 0,0000493 ppm. Sedangkan menurut hasil penelitian Uly (2011) kadar
kadmium pada ikan sembilang dan ikan asin kepala batu ditemukan
masing-masing adalah 0,033-0,04 ppm dan 0,004-0,06 ppm.
Akumulasi kadmium pada rantai makanan tertinggi yaitu manusia menurut
hasil penelitian Ida (2004) di rambut konsumen dari keluarga nelayan Bagan Deli
Belawan antara 4,342-5,107 ppm. Sedangkan pada keluraga bukan nelayan dari
kelurahan sicanang ditemukan logam kadmium pada rambut antara 2,67-3,10
2.6 Jenis-jenis Ikan Asin
1. Ikan Lemuru (Sardinella aurita)
Ikan lemuru merupakan ikan yang berukuran kecil, ramping, dan mempunyai
panjang tubuh sekitar 15 cm. Ikan lemuru dilekatkan pada beberapa spesies dari
marga Amblygaster yang mana kerabat terdekatnya Sardinella. Ikan lemuru yang
lebih dikenal dengan ikan dencis yang sering digunakan pada ikan kaleng sering
ditemukan dekat permukaan laut tidak jauh dari pantai. Lemuru diketahui
memangsa plankton yang ada di lingkungannya. Ikan lemuru biasa dijual dalam
keadaan segar, akan tetapi kebanyakan ikan ini diolah menjadi ikan asin, ikan
pindang atau sarden.
Sebagai salah satu hasil perairan laut, ikan lemuru merupakan jenis ikan yang
tergolong mudah rusak (perishable food). Tubuh ikan lemuru ini mempunyai
kadar air yang tinggi (60-84%). Di perairan Indonesia ikan lemuru (Sardinella sp)
banyak dijumpai di Indonesia (Afrianto dan Liviawaty,1989) .Menurut Nontji
(1993) dalam Rosmidah ikan ini biasanya hidup bergerombol. Badannya langsing
dengan warna biru kehijau-hijaun pada bagian punggung dan keperak-perakan
pada bagian bawahnya. Makanan utamanya adalah plankton. Untuk itu, ia
dilengkapi dengan tapis insang (gill rakers) untuk menapis atau menyaring
2. Ikan Gelama (Pseudoceina amoyensis)
Ikan Gelama atau ikan kepala batu merupakan salah satu ikan yang tidak
hanya ditemukan dalam bentuk segar tetapi jugan dalam bentuk diasinkan.
Menurut Sunyoto (2000) ikan gelama atau ikan kepala batu merupakan ikan yang
habitatnya di daerah laut dangkal terutama di daerah muara sungai dan selalu
dimanfaatkan sebagai salah satu ikan yang diproduksi secara tradisional dalam
bentuk ikan asin. Ikan ini memiliki nilai ekonomis yang baik dan dalam proses
pengangkapannya juga tidak sukar.
3. Ikan Kresek (Tryssa mystax)
Ikan kresek termasuk ikan pelagis yang suka bergerombol. Ikan kresek hidup
di perairan pantai dan muara sungai. Ikan ini memilki bentuk badan sangat pipih,
bagian atas badan berwarna sawo matang atau kuning agak pucat dan siripnya
berwarna putih perak. Adapun panjang ikan ini pada umumnya 17,5 cm sampai 20
cm. Ikan kresek merupakan ikan yang digemari masyarakat dalam bentuk ikan
asin. Ikan kresek juga merupakan bahan dalam pembuatan terasi (Direktorat
jendral perikanan, 1979). Menurut Weber dan Beaufort (1965) ikan ini sering
memasuki perairan manggrove dan perairan payau.
4. Ikan Kembung (Rastrelliger kanagurta)
Ikan kembung mempunyai dua jenis yaitu kembung jantan dan kembung
betina. Kembung jantan mempunyai tubuh yang lebih lansing, dan biasanya
terdapat di perairan yang agak jauh dari pantai. Sedangkan kembung betina
pantai. Ikan kembung termasuk jenis ikan yang hidupnya secara bergerombol di
tengah-tengah laut, yaitu antara dasar dan permukaan yang kondisi airnya hangat
(Agus,1995).
Ikan kembung termasuk ikan benthopelagik, yang kadang-kadang hidup
bentik (hidup di dasar daerah tepian landasan benua bawah air, antara jurang
continental shelf dan tepi pantai), kadang-kadang hidup dekat permukaan laut
bergantung kepada musim, seringkali ikan ini berkumpul bergerombolan dan
banyak sekali ke permukaan pada musim tertentu (Ridwansyah,2002).
5. Ikan Cincaru (Eleutheronema tetradactylum)
Ikan Cincaru mempunyai nilai ekonomis yang penting. Ikan ini selain dalam
bentuk segar jugan dikelola dalam bentuk ikan asin (Ratna,2001). Di Indonesia
terdapat banyak jenis ikan Cincaru. Habitat dari ikan Cincaru ini yaitu di air
payau, air laut, dan air tawar. Ikan ini juga terdapat di tambak-tambak dan
sungai-sungai. Jika sungai tersebut terhubung ke danau, maka ikan cincaru ini akan
menetap di danau tersebut. Ikan ini banyak dikonsumsi di beberapa negara salah
satunya adalah Indonesia (Anugerah,1993).
2.7 Merkuri
2.7.1 Karakteristik merkuri
Logam merkuri atau air raksa, mempunyai nama kimia hydragyrum yang
berarti perak cair. Logam merkuri dilambangkan dengan Hg. Pada tabel periodika
unsur-unsur kimia menempati urutan (NA) 80 dan mempunyai bobot atom
Logam ini dihasilkan dari sebijih sinabar, HgS, yang mengandung unsur merkuri
antara 0,1%-4% (Palar,2008).
Merkuri(Hg) pada udara yang jenuh mengandung 15 mg/m³ pada suhu
20ᵒC dan 68 mg/m³ pada suhu 40ᵒC. Merkuri dan senyawa garamnya mempunyai
batas yang diperbolehkan. Dosis fatal garam merkuri, misalnya sublimat 1 gram.
Sedangkan batas paparan senyawa alkil merkuri adalah 0,01 mg/m³. Batas kadar
alkil merkuri dalam makanan tidak lebih dari 0,5 mg/kg dan konsumsinya tidak
lebih dari 0,5 kg (Robbert et all,1987).
Kelimpahan Hg di bumi menempati urutan ke-67 di antara elemen lainnya
pada kerak bumi. Merkuri (Hg) akan memadat pada tekanan 7.640 Atm. Merkuri
dapat larut dalam asam sulfat atau asam nitrit, tetapi tahan terhadap basa. Hg juga
mudah membentuk alloy amalgama dengan logam lainnya, seperti emas (Au),
perak (Ag), platinum (Pt), dan tin (Sn). Salah satu gabungan senyawa merkuri
yang bersifat toksik adalah HgCl2 (Wahyu dkk,2008).
Menurut Palar (2008), secara umum logam merkuri memiliki sifat-sifat
yaitu ;
a. Berwujud cair pada suhu kamar (25ᵒC) dengan titik beku paling rendah
sekitar -39ᵒC.
b. Masih berwujud cair pada suhu 396ᵒC. Padatemperatur 396ᵒC ini telah
terjadi pemuaian secara menyeluruh.
c. Merupakan logam yang paling mudah menguap jika dibandingkkan
d. Tahanan listrik yang dimiliki sangat rendah, sehingga menempatkan
merkuri sebagai logam yang sangat baik untuk menghantarkan daya listrik.
e. Dapat melarutkan bermacam-macam logam untuk membentuk alloy yang
disebut juga amalgam.
f. Merupakan unsur yang sangat beracun bagi semua mahkluk hidup, baik itu
dalam bentuk unsur tunggal (logam) ataupun dalam bentuk persenyawaan.
Organisme perairan dapat mengakumulasi merkuri (Hg) dari air, sedimen, dan
makanan yang dikonsumsi. Pengambilan melalui makan merupakan sumber
penting keberadaan logam berat yang terdapat dalam tubuh organisme. Pentreath
(1976) membandingkan akumulasi dan distribusi merkuri (Hg) dalam jaringan
ikan plaice yang dikontaminasikan pada merkuri anorganik dan MeHg dalam
makanan dan dalam air, serta menemukan bahwa hanya hewan uji yang
dikontaminasi melalui makananlah yang mengakumulasi merkuri secara efektif
dan merkuri tersebut terdistribusi di dalam jaringan. Melalui proses akumulasi
secara biologi (bioakumulasi), proses perpindahan secara biologi (biotransfer),
dan pembesaran secara biologi (biomagnifikasi) yang terjadi secara alamiah
organisme laut mengakumulasi merkuri dalam konsentrasi tinggi dan selanjutnya
terjadi keracunan pada manusia yang mengkonsumsinya (Yasuda,2000).
Menurut Palar (2008), logam merkuri yang masuk ke badan air atau sungai
dan mengendap pada sedimen akan diubah oleh aktivitas bakteri pada sedimen
dasar perairan menjadi senyawa Hg2+ dan Hg0. Karena dipengaruhi oleh faktor
fisika maka senyawa-senyawa tersebut mudah menguap ke udara. Kemudian
datangnya hujan. Selanjutnya ion merkuri yang mengendap dalam lumpur
kembali akan mengalami perubahan metil merkuri yang mana mudah larut dalam
air dan dimakan oleh biota perairan seiring dengan rantai makanan.
2.7.2 Sumber Logam Merkuri
Sumber Hg secara alami dari kerak bumi termasuk tanah, sungai, dan laut,
diperkirakan sebesar 25.000-150.000 ton/tahun. Sementara itu, Hg di atmosfer
sebagian besar berasal dari sektor transportasi. Pada tahun 1976, sumber Hg yang
berasal dari aktivitas manusia tercatat sebesar 8.000-10.000 ton/tahun. Bahan
bakar mengandung Hg sebanyak 1 ppm dan diperkirakan kurang lebih 5.000
ton/tahun emisi gas Hg berasal dari pembakaran batu bara, gas alam, dan
pemurnian bahan bakar minyak (BBM) (Klaassen et al,1986).
Dalam bidang industri sumber Hg berasal dari indusri yang memproses
klorin, reduksi coustic soda,industri pertambangan, dan proses pengolahan bijih
Hg, industri metalurgi dan electroplating, industri kimia, pabrik tinta, pabrik
kertas, penyamakan kulit, pabrik tekstil, serta perusahaan farmasi
(Wijayanto,2005).
2.7.3 Kegunaan Logam Merkuri
Dalam keseharian, pemakaian bahan merkuri telah berkembang sangat
luas. Merkuri digunakan dalam bermacam-macam perindustrian, untuk peralatan
elektris, digunakan untuk alat-alat ukur,dalam dunia pertanian, dan
a. Dalam industri khor-alkali, merkuri digunakan untuk menangkap logam
natrium (Na). Logam natrium tersebut dapat ditangkap oleh merkuri
melalui prses elektrolisa dari larutan garam natrium khlorida (NaCl).
b. Pada peralatan listrik, merkuri digunakan pada pembuatan lampu listrik.
c. Pada laboratorium, logam merkuri digunakan sebagai alat ukur.
Contohnya sepeti termometer.
d. Dalam bidang pertanian, senyawa merkuri banyak digunakan sebagai
fungisida yang berfungsi untuk membunuh jamur. Senyawa yang
digunakan yang sering digunakan dalam bidang pertanian adalah senyawa
metil merkuri disiano diamida (CH2-Hg-NH-CNHNHCN)2 metil merkuri
nitrit (CH2-Hg-CN), metil merkuri asetat (CH2-Hg-COOH)2 dan senyawa
etil merkuri khlorida (C2H5-Hg-Cl).
e. Pada industri pulp dan kertas, merkuri digunakan adalah senyawa FMA
(Fenil Merkuri Asetat) yang bertujuan untuk mencegah pembentukan
kapur pada pulp dan kertas basah selama proses penyimpanan
(Palar,2008).
2.7.4 Bentuk Merkuri di Lingkungan
A. Merkuri Anorganik
Toksisitas senyawa merkuri anorganik tergantung pada berbagai faktor,
antara lain bentuk senyawa Hg, jalur paparan Hg, lamanya paparan, serta
kandungan unsur lain yang terdapat di dalam makanan. Merkuri anorganik
dari protein, purin, pteridin, dan porfirin, sehingga Hg bisa terlibat dalam proses
seluler. Toksisitas ini terjadi pada umumnya karena interaksi Hg dengan
kelompok thiol dari protein (Wahyu dkk,2008).
Salah satu contoh bentuk dari merkuri anorganik yaitu garam merkuri
anorganik. Garam merkuri anorganik dapat mengakibatkan presipitasi protein,
merusak mukosa alat pencernaan, termasuk mukosa usus besar, dan merusak
membran ginjal ataupun membran filter glomelurus, menjadi lebih permeabel
terhadap protein plasma yang sebagian besar akan masuk ke dalam urin.
Senyawa merkuri anorganik, seperti Hg(NO3), HgCl2, dan HgO pada
toksisitas akut akan terjadi gelaja muntah, kehilangan kesadaran, mulut terasa
tebal, sakit abdominal, diare disertai darah dalam feses, oliguria, albuminuria,
anuria, ureamia, ulserasi, dan stomatitis. Sedangkan toksisitas kronis dari merkuri
anorganik akan terjadi gejala gangguan sistem syaraf, antara lain berupa tremor,
terasa pahit di mulut, gigi tidak kuat dan rontok, anemia, albuminuria, dan gejala
lain berupa kerusakan ginjal serta kerusakan mukosa usus.
B. Merkuri Organik
Senyawa merkuri organik seperti metil merkuri dan alkil merkuri lebih
toksik dibandingkan merkuri anorganik. Hal ini disebabkan karena alkil merkuri
yang merupakan salah satu senyawa dari merkuri organik bisa membentuk
senyawa liphophilus yang mampu melintasi membran sel dan lebih mudah
diabsorpsi serta berpenetrasi menuju sistem saraf. Demikian juga alkil merkuri
tubuh. Sedangkan metil merkuri juga memiliki toksisitas yang tinggi sehingga
mengakibatkan disfungsi blood-brai barrier , merusak permeabilitas membran,
menghambat beberapa enzim, menghambat sintesis protein, dan menghambat
penggunaan substrat protein. Namun demikian, alkil merkuri ataupun metil
merkuri tidak mengakibatkan kerusakan membran mukosa sehingga toksisitas
merkuri organik lebih lambat dari toksisitas merkuri anorganik(Wahyu dkk,2008).
Senyawa merkuri organik lainnya adalah akil-merkuri. Senyawa ini di
lingkungan banyak ditemukan dalam bentuk FMA (fenil merkuri asetat). Sama
halnya dengan senyawa merkuri organik lainnya, fenil merkuri asetat setelah
sampai dalam darah akan mengalami oksidasi dan berubah menjadi senyawa
merkuri anorganik. Beberapa pengujian yang dilakukan bahwa senyawa fenil
merkuri asetat tersebut akan berikatan dengan sel-sel darah merah (eritrosit).
Meski untuk penyerapan senyawa ini sangat ditentukan oleh kelarutan dan ukuran
partikelnya, fenil merkuri asetat cenderung untuk lebih mudah diserap
dibandingkan senyawa merkuri anorganik (Palar,2008).
2.7.5 Toksikokinetika Merkuri
Perjalanan suatu bahan toksik dalam tubuh sampai timbulnya efek
terhadap tubuh mengalami beberapa tahapan atau proses yaitu : absorbsi,
distribusi, metabolisme dan ekskresi (Soemirat,2009). Adapun tahap atau proses
perjalanan merkuri di dalam tubuh sampai dibuang sebagai hasil samping dari
1. Absorbsi
Absorbsi metal merkuri di dalam tubuh manusia dapat terjadi melalui
makanan, minuman, dan pernafasan serta kontak kulit. Paparan merkuri melalui
jalur kulit biasanya berupa senyawa HgCl2, yang mana jumlah Hg yang diabsorbsi
tergantung kepada jalur masuknya, lama paparan, dan bentuk senyawa merkuri.
Menurut beberapa penelitian metal merkuri akan diserap melalui saluran cerna,
uap senyawa metal merkuri seperti uap metil merkuri klorida yang dapat diserap
melalui pernafasan. Penyerapa metil merkuri dapat juga melalui kulit. Merkuri
setelah di absorbsi di jaringan mengalami oksidasi membentuk merkuri divalent
(HG2+) yang dibantu oleh enzim katalase. Inhalasi merkuri bentuk uap akan di
absorbsi melalui sel darah merah, lalu ditransformasikan menjadi merkuri divalen.
Sebagian akan menuju otak, yang kemudian diakumulasi di dalam jaringan.
2. Distribusi
Pada saat terpapar oleh logam merkuri dan di absorbsi dalam jaringan,
logam merkuri akan ditransper ke dalam darah, seperti uap logam merkuri (Hg)
akan terserap oleh alveoli dan diteruskan ke dalam darah. Dalam darah akan
mengalami proses oksidasi dengan bantuan enzim hidrogeperoksida katalase
sehingga berubah menjadi divalen, selanjutnya dibawa ke seluruh tubuh bersama
peredaran darah dan terakumulasi di hati dan ginjal. Sebagian merkuri dikeluarkan
bersama urine.
Selain menumpuk, ternyata merkuri dapat menembus membran plasenta
plasenta karena dibawa oleh peredaran darah ke janin. Sehingga dapat merusak
otak janin dan bayi lahir kemungkinan akan cacat.
3. Metabolisme
Pada proses metabolisme dalam tubuh setelah di absorbsi di dalam jaringan,
merkuri organik dan anorganik akan sangat mudah berikatan dengan protein dan
berbagai jenis enzim katalase. Sebagian dari senyawa merkuri organik seperti alkil
merkuri akan diubah menjadi senyawa anorganik. Setelah leawt waktu paruh
senyawa merkuri akan dikeluarkan dari dalam tubuh sebagai hasil samping
metabolisme. Hanya sebagian kecil yang dikeluarkan jika dibandingkan dengan
jumlah uap atau senyawa merkuri yang masuk ke dalam tubuh. Sebagian besar
senyawa atau uap merkuri akan ditranspormasikan melalui sel darah merah
selanjutnya akan terakumulasi dalam berbagai organ bagian dalam tubuh seperti
hati, ginjal, dan otak.
4. Ekskresi
Ekskresi merkuri dari tubuh melalui urin dan feses dipengaruhi oleh bentuk
senyawa merkuri, besar dosis merkuri, serta waktu paparan. Merkuri yang masuk
ke dalam hati akan terbagi dua. Sebagian akan terakumulasi di dalam hati, dan
sebagian lainnya akan dikirim ke empedu. Di dalam kantung empedu merkuri
organik dirombak menjadi merkuri anorganik kemudian akan dikirim lewat darah
ke ginjal, dimana sebagian akan terakumulasi dalam ginjal dan sebagian lagi akan
dibuang bersama dengan urine. Sedangkan ekskresi merkuri organik sebagian
besar terjadi dengan ekskresi feses. Waktu paruh pada merkuri untuk bisa dibuang
2.7.6 Efek Pencemaran Merkuri
Toksisitas logam berat dapat dikelompokan menjadi 3 sifat ¸ yaitu bersifat
toksik tinggi yang terdiri dari unsur-unsur Hg, Cd, Pb, Cu, dan Zn; bersifat toksik
sedang, yang terdiri dari unsur-unsur Cr,Ni, dan Co; dan bersifat toksik rendah,
yang terdiri atas unsur Mn dan Fe. Logam berat tersebut bersifat toksik karena
tidak bisa dihansurkan (non-degradable) oleh organisme hidup yang ada di
lingkungan sehingga logam-logam tersebut terakumulasi ke lingkungan (Wahyu
dkk,2008).
Ion merkuri dapat menyebabkan toksik terhadap manusia karena dapat
berikatan dengan protein, menghambat kerja enzim dan bersifat korosif. Ion
merkuri juga dalam darah dapat berikatan dengan gugus sulfuhidril fosforil,
amida dan amina, dimana dalam gugus tersebut reaksi fungsi enzim akan
terganggu. Pengaruh toksisitas merkuri pada manusia, seperti bentuk merkuri
(HgCl2) lebih toksik daripada merkuri HgCl karena bentuk divalent lebih mudah
larut dibandingkan dengan bentuk monovalen, dan juga lebih cepat dan mudah di
absorbsi sehingga daya toksisitasnya lebih tinggi (Darmono,2001).
Masuknya merkuri ke dalam tubuh dan kemudian tubuh
mengakumulasinya menyebabkan efek terhadap tubuh. Adapun efek yang bisa
ditimbulkan adalah :
1. Keracunan Akut
Keracunan akut yang disebabkan oleh logam merkuri umumnya terjadi
merkuri sebagai bahan baku, katalis dan pembentuk almagam atau pestisida
(Palar,2008).
Menurut Robert (1987) masuknya logam merkuri kedalam tubuh yang
menyebabkan keracunan akut dapat melalui:
1. Melalui mulut
Keracunan merkuri melalui mulut menimbulkan rasa logam, haus, sakit
perut yang berat, muntah, dan diare berdarah. Diare berdarah dapat terjadi selama
beberapa minggu. Antara 1 sampai ¸ minggu setelah keracunan, pengeluaran urin
dapat berhenti, dan kematian terjadi disebabkan oleh uremia. Pada keracunan
merkuri klorida dapat terjadi penyempitan esofagus, usus, dan lambung.
2. Melalui inhalasi
Keracunan uap merkuri kadar tinggi melalui inhalasi dapat segera
menimbulkan dispnea, batuk, demam, mual, muntah, diare, stomatis, salivasi, dan
rasa logam. Gejala ini dapat berkembang menjadi pneumonitis, bronkitis kronik
nekrotik, edema paru, dan pneumotoraks. Pada saat anak-anak gejala ini dapat
berakibat fatal. Selain itu dapat terjadi asidosis dan kerusakan ginjal dengan gagal
ginjal. Sedangkan pada keracunan senyawa merkuri organik yang mudah
menguap dengan kadar tinggi dapat menimbulkan rasa logam, kepala pening,
diare, bicara tidak jelas, dan kadang-kadang konvulsi yang berakibat fatal.
2. Keracunan kronik
Keracunan kronis merupakan keracunan yang terjadi secra perlahan dan
penderita tidak mengetahui bahwa di dalam tubuhnya telah menumpuk sejumlah
racun, sehingga pada batas daya tahan yang dimiliki tubuh, racun yang telah
mengendap dalam selang waktu yang panjang akan terus bekerja dan pengobatan
akan menjadi sangat sulit untuk dilakukan (Palar,2008).
Menurut Robbert (1987) masuknya logam merkuri ke dalam tubuh dapat
melalui:
a. Melalui mulut dan suntikan
Keracunan karena suntikan senyawa merkuri organik, atau keracunan
melalui senyawa merkuri organik atau garam merkuri organik yang tidak larut
atau sedikit terdisosiasi dalam waktu lama dapat menyebabkan urtikaria yang
dapat berkembang menjadi dermatitis, stomatitis, salivasi, diare, anemia,
leukopenia, kerusakan hati, dan kerusakan ginjal yang dapat berkembang menjadi
gagal ginjal akut dengan anuria. Suntikan senyawa organik sebagai obat diuretika,
menyebabkan fungsi jantung tidak teratur atau depresi, dan reaksi anafilatik.
b. Melalui inhalasi dan kontak kulit
Inhalasi debu dan uap merkuri serta senyawa merkuri organik, atau
absorpsi merkuri dan senyawa merkuri melalui kulit dalam waktu lama, dapat
menyebabkan “merkurialisme” dengan gejala yang timbul bervariasi, termasuk
tremor, salivasi, stomatitis, gigi rontok, garis biru hitam pada gusi, rasa sakit dan
kebas pada anggota badan, nefritis, diare, gelisah, sakit kepala, berat badan
menurun, anoreksia, depresi mental, insomnia, iritabilitas, instabilitas, halusinasi,
Merkuri (Hg) selain diakumulasi pada berbagai organ juga mampu
menembus membran plasenta sehingga bisa mencapai janin. Hasil penelitian
menunjukan bahwa otak janinlebih rentan terhadap metil merkuri dibandingkan
otak orang dewasa. Hal ini bisa terlihat pada tabel berikut
Tabel 2.1 Konsentrasi Hg Pada Berbagai Organ Induk dan Janin
Organ Hg pada induk (µg/g) Hg pada janin (µg/g)
Ginjal 518 5,8
Paru-paru 77,5 0,6
Hati 8 10,1
Cerebrum 10,9 0,05
Cerebellum 5,8 0,24
Jantung 3,¸ 0,15
Limpa 5,¸ 1,8
Darah 15 µg/100 ml 2,35µg/100ml
Sumber : Smith dalam Palar, 1994
2.7.7 Kadar Batas Aman
Kadar batas aman yang diperbolehkan di perairan menurut Kepmen LH
No.54 tahun 2004 untuk merkuri di perairan adalah 0,001. Sedangkan menurut M
Peraturan Pemerintah No 82 tahun 2001 kadar batas aman merkuri yang
diperbolehkan di perairan adalah 0,03 mg/L. Konsentrasi merkuri (Hg) pada
makanan yang diolah di Indonesia diatur dalam Surat Keputusan Badan
Pengawasan Obat dan Makanan (BPOM) NOMOR HK.00.06.1.52.4011 tahun
2009 kadar batas aman yang diperbolehkan adalah 0.5 ppm. Sedangkan standar
yang dikeluarkan oleh Food and Drug Agency (FDA USA) juga 0,5 ppm
2.8 Kadmium (Cd)
2.8.1 karakteristik Kadmium
Kadmium memiliki nomor atom 40 dan berat atom 112,4 gr/mol.
Kadmium mempunyai titik didih 767 dan juga titik leleh 321ᵒC (Wahyu dkk,
2008).Logam Cd atau cadmium(Kadmium) mempunyai penyebaran yang sangat
luas di alam. Hanya ada satu jenis mineral kadmium di alam, taitu greennockite
(CdS) yang selalu ditemukan bersamaan dengan mineral spalerite (ZnS). Mineral
greennockite ini sangat jarang ditemukan di alam, sehingga dalam eksploitasi
kadmium, biasanya merupakan produksi sampingan dari peristiwa peleburan dan
refining bijih-bijih seng (Zn). Biasanya pada konsentrasi bijih Zn, didapatkan
0,2-0,3% logam kadmium. Di samping itu kadmium (Cd) juga di produksi dari
peleburan bijih-bijih Pb (timah hitam) dan Cu (tembaga). Namun demikian, Zn
merupakan sumber utama dari logam kadmium, sehingga produksi dari logam
tersebut sangat dipengaruhi oleh Zn (Palar,2008).
Kadmium (Cd) merupakan logam yang paling banyak ditemukan pada
lingkungan khususnya lingkungan perairan, serta memiliki efek toksik yang tinggi
bahkan pada konsentrasi yang rendah (Almeida et al,2009). Menurut Patrick
(2003) kadmium diketahui memiliki waktu paruh yang panjang dalam tubuh
organisme dan pada umumnya akan terakumulasi di dalam hepar dan ginjal.
Seperti halnya unsur-unsur kimia lainya terutama golongan logam, logam
kadmium mempunyai sifat tersendiri. Menurut Palar (2008) adapun
a. Kadmium merupakan logam yang lunak, ductile, berwarna putih
seperti putih perak akan kehilangan kilapnya bila berada dalam
udara yang basah atau lembab serta akan mengalami kerusakan bila
terkontaminasi oleh uap amonia (NH3) dan sulfur hidroksida (SO2)
b. Kadmium merupakan logam yang mudah bereaksi dan tahan
terhadap tekanan.
c. Kadmium bisa bersifat tidak stabil jika membentu ion Cd2+
d. Kadmium akan menghasilkan kadmium oksida bila dipanaskan
e. Kadmium dapat dimanfaatkan untuk pencampuran logam lain
seperti: nikel (Ni), emas (Au), cuprum (Cu), dan besi (Fe).
2.8.2 Sumber logam Kadmium
Sumber kadmium yang ada di lingkungan berasal dari dari alam dan
aktivitas manusia. Kadmium yang berasal dari alam terdapat pada kerak bumi
bersamaan dengan seng (Zn). Sedangkan yang berasal dari aktivitas manusia
bersumber dari bidang industri yang melibatkan Cd dalam proses operasional
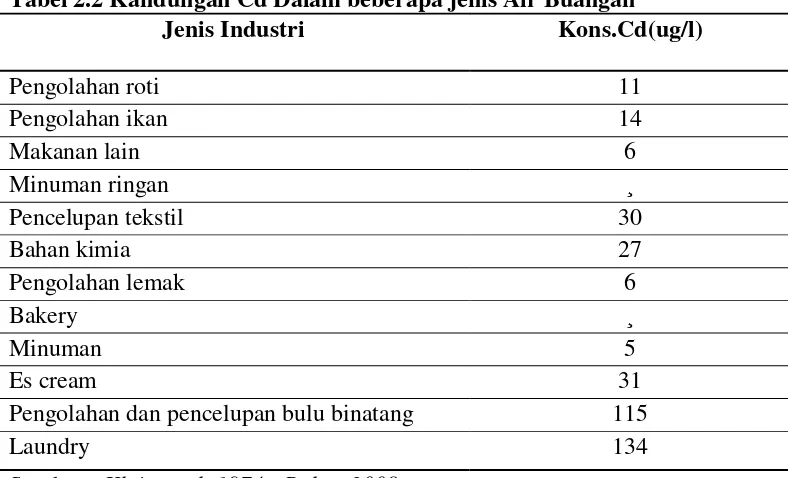
industrinya menjadi sumber pencemaran kadmium. Penelitian yang pernah
dilakukan Klein (1974) dapat diketahui kandungan rata-rata Cd dalam air bungan
Tabel 2.2 Kandungan Cd Dalam beberapa jenis Air Buangan
Jenis Industri Kons.Cd(ug/l)
Pengolahan roti 11
Pengolahan ikan 14
Makanan lain 6
Minuman ringan ¸
Pencelupan tekstil 30
Bahan kimia 27
Pengolahan lemak 6
Bakery ¸
Minuman 5
Es cream 31
Pengolahan dan pencelupan bulu binatang 115
Laundry 134
Sumber : Klein et al, 1974 ; Palar, 2008
2.8.3 Kegunaan Kadmium (Cd)
Logam kadmium sangat banyak digunakan dalam kehidupan sehari-hari
manusia. Logam ini telah digunakan semenjak tahun 1950 dan total produksi
dunia adalah sekitar 15.000-18.000 per tahun. Prinsip dasar atau prinsip utama
dalam penggunaan kadmium adalah sebagai bahan “stabilisasi” sebagai bahan
pewarna dalam industri plastik dan pada elektroplating. Namun sebagian dari
substansi logam Kadmium ini juga digunakan untuk solder dan alloy-alloynya
digunakan pula pada baterai. Umumnya logam Kadmium (Cd) senyawa oksidasi
dari Kadmium (CdO), hidrat (CdH2), dan khloridanya paling banyak digunakan
Adapun penggunaan dan pemanfaatan Kadmium meliputi :
1. Senyawa CdS dan CdSes yang banyak digunakan sebagai zat
warna.
2. Senyawa Cd sulfat (CdSO4) yang digunakan dalam industri baterai
yang berfungsi sebagai pembuatan sel wseton karena memiliki
potensial voltase stabil, yaitu 1,0186 volt.
3. Senyawa Cd-bromida (CdBr) dan Cd-ionida (CdI2) yang digunakan
untuk fotografi.
4. Senyawa dietil-Cd [(C2H2)2Cd] yang digunakan untuk pembuatan
tetraetil-Pb.
5. Senyawa Cd-Stearat untuk perindustrian manufaktur
polyvinikhlorida (PVC) sebagai bahan untuk stabilizer (Wahyu
dkk, 2008).
2.8.4 Toksikokinetika Kadmium (Cd)
Masuknya logam kadmium kedalam tubuh hewan atau manusia dapat
melalui beberapa cara meliputi ;
1. Dari udara yang tercemar, misalnya asap rokok dan asap
pembakaran batu bara.
2. Melalui wadah/tempat berlapis Cd yang digunakan untuk tempat
makanan atau minuman
3. Melalui kontaminasi perairan dan hasil pertanian yang tercemar
kadmium
5. Melalui konsumsi daging yang diberi obat anthelminthes yang
mengandung kadmium
Dari beberapa cara tersebut, kadmium yang masuk ke tubuh akan mengalami
proses absorpsi, distribusi, metabolisme, dan ekskresi di dalam tubuh. Adapun
tahap-tahap tersebut meliputi ;
a. Absorpsi
Kadmium yang masuk akan diabsorpsi baik di dalam tubuh. Menurut
Supriharyono (2009) logam berat kadmium mudah diabsopsi dalam bentuk garam
Cd terlarut . Namun kadmium tidak diabsorpsi dengan baik ketika kadar kadmium
5-8%. Akan tetapi, itu tetap lebih tinggi dibandingkan absorpsi mineral dan sulit
dieleminasi dalam tubuh sehingga akan di deposit di dalam tubuh. Tubuh yang
terpapar dengan kadmium akan diabsorpsi yang mana proporsi kadmium dalam
tubuh organisme dipengaruhi oleh umur. Hal ini bisa terlihat dari mencit muda
bisa menyimpan 10% dari kadmium yang diberikan secara oral ¸ minggu setelah
pemberian, sedangkan mencit dewasa hanya mengabsorpsi 1%. Mencit dan tikus
yang baru lahir mengabsorpsi kadmium lebih besar daripada mencit dewasa
(Wahyu dkk, 2008).
Dalam pencernaan absorpsi kadmium dipengaruhi oleh beberapa faktor antara
lain ; spesies, jenis, dan susunan kimia kadmium serta dosis dan frekuensi paparan
kadmium (Cd), absorpsi kadmium dalam saluran pencernaan meliputi 2 tahap
1. Penyerapan kadmium dari lumen usus melewati membran brush border
ke dalam sel mukosa
2. Transpor kadmium ke dalam aliran darah dan deposisi dalam jaringan
terutama di deposit di hati dan ginjal. Seperti halnya Zn, kadmium(Cd)
memiliki afinitas yang tinggi pada testis sehingga konsentrasi pada
jaringan testis juga lebih tinggi dibandingkan pada jaringan lainnya.
b. Distribusi
Kadmium yang diabsorpsi oleh tubuh kemudian akan ditransportasikan dalam
darah yang berikatan dengan sel darah merah dan protein berat molekul tinggi
dalam plasma, khususnya oleh albumin. Sedangkan pada kadar yang kecil
kadmium akan ditransformasikan oleh metalotionin. Kadar kadmium dalam darah
pada orang dewasa yang terpapar kadmium secara berlebihan biasanya 1ug/l,
sedangkan pada bayi baru lahir mengandung kadmium cukup rendah, yaitu kurang
dari 1mg dari beban total tubuh.
c. Metabolisme
Kadmium yang ditranformasikan dalam darah berikatan dengan protein yang
memiliki berat molekul rendah, yaitu metalotionin yang memiliki berat molekul
6.000. metalotionin merupakan protein yang sangat peka dan akurat sebagai
indikator pencemaran. Menurut Hall (2002), pada dasarnya metalotionin dapat
terbentuk dari tionein yang berikatan dengan segala macam logam baik logam
esensial maupun non esensial/logam berat. Hal itu didasarkan pada suatu
organisme karena adanya protein tersebut. Setelah toksikan kadmium memasuki
darah, toksikan didistribusikan dengan cepat ke seluruh tubuh. Pengikatan
toksikan dalam jaringan tersebut menyebabkan lebih tingginya kadar toksikan
dalam jaringan tersebut. Kadmium memiliki afinitas yang kuat terhadap hepar dan
ginjal. Sekitar 50-70% kadmium yang berada di dalam tubuh terdapat pada organ
tersebut. Apabila protein metalotionin hepar dan ginjal tidak mampu lagi
melakukan detoksifikasi, maka akan terjadi kerusakan hepar dan ginjal
(Wahyu,dkk, 2008).
d. Ekskresi
Kadmium(Cd) yang masuk ke dalam tubuh yang masuk melalui pencernaan
akan dibuang melalui feses sekitar 2-4 minggu setelah terpapar Cd dan sebagian
kecil dikeluarkan melalui urin (Haas, 2005). Pada umumnya, kadmium yang ada
di dalam tubuh manusia akan diekskresikan melalui urin, sedangkan pada hewan,
sebagian besar diekskresikan melalui feses.
Cardenas (1991) meneliti pada wanita yang berhubungan dengan kegiatan
peleburan kadmium yang bekerja selam 8 tahun membuktikan bahwa kandungan
kadmium pada urin wanita yang tidak terpapar memiliki kadar 0,31µg/g kreatinin
dan wanita yang terpapar kadmium memiliki kadar 35,7µg/g kreatinin . Sementara
itu, kadar kadmium dalam darah wanita yang tidak terpapar kadmium adalah
2.8.5 Efek pencemaran Kadmium (Cd)
Toksisitas logam dapat bersifat akut dan kronis selain tergantung pada
lamanya pajanan, juga dikarenakan oleh tinggi rendahnya dosis pajanan (Kosnett,
2007). Orang yang rentan terpapar kadmiun adalah pekerja di lingkungan industri,
perokok aktif, perokok pasif , pekerja di penanmbangan seng (Zn), dan orang
yang mengkonsumsi makanan yang tercemar kadmium. Akan tetapi rentannya
tubuh terhadap toksisitas kadmium dipengaruhi oleh beberapa faktor, salah
satunya adalah kemampuan tubuh untuk menyediakan tempat ikatan pada protein
metalotionin. Ketika tubuh tidak mampu menyediakannya maka akan terjadi efek
terhadap tubuh. Menurut Wahyu (2008) efek yang ditimbulkan dapat bersifat akut
dan juga kronis.
A. Keracunan Akut
Menurut Rand (2000) keracunan akut terjadi bila tanggapan terhadap
suatu ransang berisfat berat dan cepat, biasanya dalam waktu 4 hari untuk ikan
dan organisme akuatik lainnya. Keracunan akut disebabkan oleh kadmium, sering
terjadi pada pekerja di industri-industri yang berkaitan dengan logam ini.
Peristiwa keracunan akut ini dapat terjadi karena para pekerja tersebut terkena
paparan uap logam kadmium (Cd) atau CdO. Gejala-gejala keracunan akut yang
disebabkan oleh logam kadmium adalah timbulnya rasa sakit dan panas pada
bagian dada. Akan tetapi gejala keracunan akut tersebut tidak langsung muncul
begitu si penderita terpapar oleh uap logam kadmium Cd atau CdO. Gejala
keracunan akut ini muncul setelah 4-10 jam sejak si penderita terpapar oleh uap
penyakit paru-paru yang akut. Penyakit paru-paru akut ini terjadi bila penderita
terpapar oleh uap kadmium dalam waktu 24 jam, lebih jauh keracunan akut yang
disebabkan oleh uap kadmium (Cd) atau CdO dapat menimbulkan kematian bila
konsentrasi yang mengakibatkan keracunan tersebut berkisar dari 2500 sampai
2900mg/m³.
B. Keracunan kronis
Keracunan yang bersifat kronis yang disebabkan oleh daya racun yang
dibawa oleh logam kadmium, terjadi dalam selang waktu yang sangat panjang.
Keracunan akut terjadi bila adanya tanggapan organisme terhadap rangsang
bersifat ringan, berlangsung dalam waktu yang panjang, sampai 1/10 atau lebih
masa hidupnya (Klaassen, 2001). Peristiwa ini terjadi karena logam kadmium
yang masuk ke dalam tubuh dalam jumlah kecil, sehingga dapat ditolerir oleh
tubuh. Akan tetapi karena proses masuknya logam kadmium ke dalam tubuh
terjadi terus-menerus secara berkelanjutan, maka tubuh pada batas akhir tidak lagi
mampu memberikan toleransi terhadap daya racun yang dibawa oleh logam
kadmium. Keracunan yang bersifat kronis ini membawa akibat yang lebih buruk
dan lebih berbahaya dari pada penderita keracunan akut.
Keracunan kronis yang disebabkan oleh logam kadmium, umumnya
berupa kerusakan-kerusakan pada banyak sistem fisiologis pada tubuh. Sistem
tubuh yang dirusak oleh keracunan kronis logam kadmium adalah pada sistem
urinaria (ginjal), sistem respirasi (pernafasan/paru-paru), sistem sirkulasi (darah)
sistem penciuman dan bahkan dapat mengakibatkan kerapuhan pada tulang (Palar,
2008).
2.8.6 Kadar Batas Aman
Menurut Kepmen LH No.54 tahun 2004 kadar batas aman merkuri di perairan
yang diperbolehkan adalah 0,001. Sedangkan konsentrasi kadmium (Cd) pada
makanan yang diolah di Indonesia yang diatur dalam Surat Keputusan Badan
Pengawasan Obat dan Makanan (BPOM) NOMOR HK.00.06.1.52.4011 tahun
2009 kadar batas aman yang diperbolehkan adalah 0.1 ppm dan menurut
FAO/WHO kadar batas aman yang diperbolehkan pada dalam tubuh hewan laut
yang dapat dikonsumsi manusia yakni 0,1 ppm.