BAB I
PENDAHULUAN
A. Latar Belakang
Tanaman Kelapa (Cocos nucifera L) sering dikatakan sebagai pohon kehidupan. Karena mulai dari akar, batang, daun, bunga, dan buah dapat dimanfaatkan untuk memenuhi sebagian besar kebutuhan manusia (Heryani, 2000). Buah kelapa merupakan salah satu bahan baku pembuatan minyak nabati yang utama, daging buah kelapa kaya akan kandungan lemak, karbohidrat, protein dan vitamin. Jumlah protein tersebar dalam daging buah (endosperm) kelapa yang setengah tua, sedangkan kandungan kalori dan lemak mencapai maksimal pada buah kelapa tua (Setiawan, 2004).
Adapun ayat yang berhubungan dalam penelitian ini yaitu terdapat dalam Al-quran surah Ar-Ra’d (13) :4 :
ٌلي ِخَن َو ٌع أرَز َو ٍباَنأعَأ أنِم ٌتاَّنَج َو ٌتاَرِواَجَتُم ٌعَطِق ِض أرَ ألْا يِف َو
ِ ضَفُن َو ٍد ِحا َو ٍءاَمِب ٰىَقأسُي ٍنا َوأن ِص ُرأيَغ َو ٌنا َوأن ِص
ٰىَلَع اَهَضأعَب ُل
َنوُلِقأعَي ٍم أوَقِل ٍتاَي َلَ َكِلَٰذ يِف َّنِإ ۚ ِلُكُ ألْا يِف ٍضأعَب
Terjemahan ayat :
“Dan di bumi ini terdapat bagian-bagian yang berdampingan, dan kebun-kebun anggur, tanaman-tanaman dan pohon kurma yang bercabang dan
sebahagian tanam-tanaman itu atas sebahagian yang lain tentang
rasanya. Sesungguhnya pada yang demikian itu terdapat tanda-tanda
(kebesaran Allah) bagi kaum yang berpikir”.
Hasil penelitian menunjukkan bahwa minyak kelapa mempunyai khasiat yang besar bagi kesehatan. Asam laurat merupakan asam dominan yang terkandung pada minyak kelapa dan memiliki khasiat sebagai antimikroba (Ketaren, 2008). Selain itu, manfaat lain dari minyak kelapa adalah membantu mengontrol diabetes, mencegah kolesterol, kanker, osteoporosis dan jantung koroner (Estien, 2005).
Tuminah (2009) menyatakan bahwa asam lemak jenuh yang terdapat pada minyak kelapa lebih tinggi daripada minyak sawit, minyak kacang tanah, minyak kedelai, minyak jagung dan minyak bunga matahari. Berdasarkan penelitian Enig dan kelompoknya asam lemak jenuh rantai sedang yang terdapat dalam minyak kelapa mudah dimetabolisme dan tidak meningkatkan kolesterol darah (Enig, 1999).
Suryani (2005) menyatakan bahwa secara umum mutu minyak kelapa tradisional hasil olahan masyarakat desa Sidodadi Kabupaten Polmas memenuhi standar mutu nasional untuk minyak kelapa.
tidak berkualitas karena memiliki gugus peroksida dan senyawa radikal bebas (Arghainc, 2008).
Berdasarkan uraian diatas, maka akan dilakukan analisis mutu minyak kelapa murni buatan industri rumah tangga asal desa Pasarwajo, Buton, Sulawesi Tenggara melalui pengujian secara organoleptik, fisika dan kimia (berdasarkan SNI 7381:2008) dan analisis gugus menggunakan FTIR.
B. Rumusan Masalah
Apakah minyak kelapa murni buatan industri rumah tangga asal desa Pasarwajo, Buton, Sulawesi Tenggara sesuai dengan standar mutu minyak kelapa murni berdasarkan SNI 7381:2008 ?
C. Maksud dan Tujuan Penelitian
1. Maksud penelitian
Maksud dilakukannya penelitian ini adalah untuk menganalisis mutu minyak kelapa murni secara fisika, kimia dan dengan menggunakan Spektrofotometer Infra Merah (FTIR).
2. Tujuan Penelitian a. Tujuan Umum
b. Tujuan Khusus
Tujuan khusus penelitian ini adalah untuk menentukan mutu minyak kelapa murni buatan industri rumah tangga asal desa Pasarwajo, Buton, Sulawesi Tenggara berdasarkan standar mutu minyak kelapa murni (SNI 7381:2008).
D. Manfaat Penelitian 1. Manfaat Teoritis
Menambah data ilmiah tentang mutu minyak kelapa murni buatan industri rumah tangga berdasarkan Standar Nasional Indonesia (SNI 7381:2008).
2. Manfaat Praktis
BAB II
TINJAUAN PUSTAKA
A. Kelapa (Cocos nucifera L)
Kelapa merupakan tumbuhan asli daerah tropis. Di Indonesia, pohon kelapa dapat ditemukan hampir di seluruh provinsi, dari daerah pantai yang datar sampai ke daerah pegunungan yang agak tinggi. Kelapa sangat bermanfaat bagi kehidupan manusia sehari-hari. Tidak hanya buahnya, tetapi seluruh bagian tanaman mulai dari akar, batang, sampai ke pucuk tanaman dapat dimanfaatkan, sehingga pohon kelapa sering disebut pohon kehidupan (Warisno, 2003).
Sistematika tumbuhan kelapa (Suhardiman, 1999., Cronquist, 1981., Backer, 1986) :
Kingdom : Plantae
Divisi : Magnoliophyta Sub Divisi : Spermatophyta Kelas : Monocotyledoneae Ordo : Palmales
Family : Palmae Genus : Cocos
Spesies : Cocos nucifera L
Tanaman kelapa dikelompokkan kedalam famili yang sama dengan sagu (Metroxylon sp), salak (Salaca edulis), dan aren (Arenga pinata).
perbedaan umur pohon mulai berbuah, bentuk dan ukuran buah, warna buah, serta sifat-sifat khusus yang lain (Warisno, 2003)
Seperti tumbuhan monokotil lainnya, kelapa mempunyai sistem perakaran serabut. Akar serabut yang tumbuh mendatar dapat mencapai panjang 10 m-15 m, sedangkan akar yang tumbuh ke bawah dapat menembus tanah sampai 2 m-3 m. Diameter akar kelapa rata-rata 1 cm. Pada umumnya, batang kelapa tumbuh lurus ke atas dan tidak bercabang, kecuali jika ditanam di tepi sungai atau tebing. Tinggi batang kelapa dapat mencapai 30 m, dengan diameter antara 20 cm-30 cm (Warisno, 2003).
Daun kelapa bersirip genap dan bertulang sejajar. Daun memiliki pelepah daun yang terdapat pada anak-anak daun pada sis kiri dan kanannya. Pada pohon yang sudah dewasa, panjang anak daun 100- 300 lembar. Anak daun berukuran panjang antara 1 m – 1,5 m dengan tulang daun ditengahnya yang biasa di sebut lidi (Warisno, 2003).
B. Minyak Kelapa
Kelapa segar mengandung 30-50% minyak, bila dikeringkan menjadi kopra kadar lemaknya mencapai 63-65%. Kadar minyak sangat dipengaruhi oleh tingkat ketuaan buah, semakin tua buah semakin tinggi kadar minyaknya. Buah kelapa yang sudah tua atau matang umumnya dipanen pada umur 11-12 bulan (Rindengan et al., 1995).
Minyak kelapa sebagaimana minyak nabati lainnya merupakan senyawa trigliserida yang tersusun atas asam lemak dan 90% diantaranya yaitu asam lemak jenuh. Setiap minyak nabati memiliki sifat dan ciri yang ditentukan oleh struktur asam lemak pada rangkaian trigliseridanya. Minyak kelapa kaya akan asam lemak berantai sedang (C8 – C14),
khususnya asam laurat dan asam meristat (Ketaren, 2008). Ada beberapa cara pembuatan minyak kelapa murni yaitu : a. Cara Tradisional
Pembuatan minyak kelapa murni sudah lama dilakukan oleh masyarakat pedesaan. Umumnya minyak kelapa murni yang dihasilkan digunakan untuk minyak goreng. Proses pembuatan minyak kelapa murni dengan cara tradisional sangat mudah dilakukan. Pada proses pembuatan minyak kelapa, santan dipanaskan pada suhu 100-1100C.
b. Cara Pemanasan Bertahap
Cara ini dilakukan untuk penyempurnaan pembuatan minyak kelapa murni cara tradisional. Perbedaan antara pembuatan minyak kelapa tradisional dan cara pemanasan bertahap adalah suhunya. Suhu yang digunakan dalam pembuatan minyak kelapa cara pemanasan bertahap adalah 60-750C. Untuk menjaga suhu santan
agar tetap konstan selama pemanasan, perlu dilakukan control selama pemanasan. Apabila suhu telah mencapai 750C nyala kompor harus
dimatikan, demikian bila suhunya mendekatai 600C nyala kompor
dihidupkan kembali (Prayugo dan Setiaji, 2006). c. Cara Fermentasi
Pada pembuatan minyak kelapa murni dengan cara fermentasi ketika santan terbentuk, emulsi santan ditambahkan ragi. Ragi yang digunakan umumnya adalah ragi tape, ragi roti dan ragi tempe. Proses fermentasi dilakukan selama delapan jam. Minyak kelapa yang dihasilkan cukup banyak namun memiliki bentuk yang kurang baik, sehingga sering dilakukan pemanasan untuk memisahkan minyak dengan sempurna (Dede et al, 2005).
d. Cara pancingan
sendirinya. Kelebihan minyak kelapa murni yang dibuat dengan cara ini adalah kandungan asam lemak rantai sedang dan antioksidannya tidak mengalami denaturasi (Prayugo dan Setiaji, 2006).
e. Cara enzimatis
Proses pembuatan dengan cara ini yaitu dengan adanya penambahan enzim pada santan. Biasanya enzim yang digunakan pada pembuatan minyak kelapa murni adalah papain dari getah papaya, enzim bromelin dari nenas dan enzim protease dari kepiting sungai. Kelebihan cara enzimatis adalah prosesnya lebih cepat dibandingkan cara fermentasi. Kekurangan cara ini adalah dapat mengeluarkan enzim-enzim yang terkandung dalam minyak kelapa (Baswardojo, 2005).
f. Cara Sentrifugasi
Sentrifugasi merupakan salah satu cara pembuatan minyak kelapa secara mekanik dengan upaya untuk memutuskan ikatan lemak-protein pada santan. Minyak kelapa yang dihasilkan dengan cara ini memiliki beberapa kelebihan yaitu berwarna jernih dan bau khas minyak kelapa, daya simpan cukup lama, proses pembuatannya sangat cepat, kandungan asam lemak rantai sedang dan antioksidannya tidak mengalami denaturasi (Prayugo dan Setiaji, 2006).
bebas lainnya, hal ini dapat menimbulkan kanker. Selain itu menggunakan minyak goreng yang berulang-ulang dapat meningkatkan lipoprotein LDL, dan menurunkan lipoprotein HDL, sehingga meningkatkan jantung koroner (Hartin dan Surtami, 2005).
Tabel 1. Standar Mutu Minyak Kelapa Murni Berdasarkan SNI 7381:2008
No Jenis Uji Persyaratan
1.
Air dan senyawa yang menguap Bilangan Iod
Asam lemak bebas (dihitung sebagai asam laurat)
C. Minyak dan Lemak
Lemak dan minyak merupakan salah satu kelompok yang termasuk golongan lipid. Suatu sifat yang khas dan mencirikan golongan lipid (termasuk minyak dan lemak) adalah kelarutannya dalam pelarut organik (pelarut non polar) dan sebaliknya ketidaklarutannya dalam pelarut air dan pelarut polar lainnya (Rohman dan Sumantri, 2013).
Kelompok-kelompok lipid dapat dibedakan berdasarkan polaritasnya atau berdasar struktur kimia tertentu. Kelompok-kelompok lipid tersebut adalah (Rohman dan Sumantri, 2013):
1. Kelompok trigliserida (minyak, lemak)
2. Kelompok turunan asam lemak (lilin, aldehid asam lemak) 3. Fosfolipid dan serebrosid (termasuk glikolipid)
4. Sterol-sterol dan steroid 5. Karotenoid
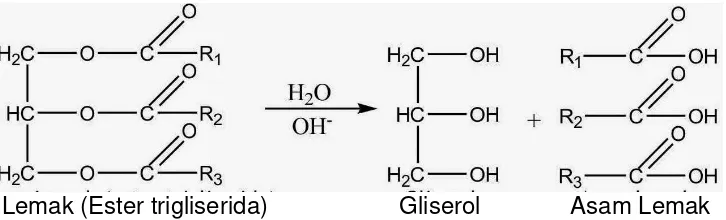
Lemak (Ester trigliserida) Gliserol Asam Lemak Gambar 1. Reaksi hidrolisis lemak menghasilkan gliserol dan asam lemak bebas. R1, R2, R3 dapat berbeda atau sama.
Secara umum, lemak diartikan sebagai trigliserida yang dalam kondisi suhu ruang berada dalam keadaan padat, sedangkan minyak adalah trigliserida yang dalam suhu ruang berbentuk cair. Metode-metode analisis senyawa-senyawa lemak, resin, dan sebagainya biasanya terdiri atas penentuan sejumlah bilangan-bilangan fisika dan kimia yang umumnya dikenal sebagai suatu konstanta meskipun dalam batas-batas tertentu (Rohman dan Sumantri, 2013). Lemak yang secara alami banyak mengandung berbagai asam lemak yang meliputi asam lemak dengan jumlah atom karbon 2-40 tetapi yang paling dominan adalah C18 dan C20
(Winarno, 1992).
Asam lemak adalah asam monokarboksilat rantai lurus tanpa cabang yang mengandung atom karbon genap mulai dari C-4, tetapi yang paling banyak adalah C-16 dan C-18. Asam lemak dapat dikelompokkan berdasarkan panjang rantai, ada tidaknya ikatan rangkap dan isomer
fatty acids, MCFA) mengandung atom karbon C-10 dan C-12, dan asam lemak rantai panjang (long chain fatty acids, LCFA) mengandung jumlah atom karbon C-14 atau lebih (White, 2009).
Berdasarkan jumlah ikatan rangkap asam lemak terdiri dari asam lemak jenuh dapat dibagi tiga golongan, asam lemak jenuh (saturated fatty acid; SFA) karena tidak mempunyai ikatan rangkap, asam lemak tak jenuh tunggal (mono unsaturated fatty acids; MUFA) hanya memiliki satu ikatan rangkap dan asam lemak tak jenuh jamak (polyunsaturated fatty acids, PUFA) memiliki lebih dari satu ikatan rangkap (White, 2009).
D. Analisis Minyak dan Lemak 1. Organoleptik
2. Cara Fisika a. Kadar Air
Kadar air adalah jumlah (dalam %) bahan yang menguap pada pemanasan dengan suhu dan waktu tertentu. Jika dalam minyak terdapat air, maka akan mengakibatkan reaksi hidrolisis yang dapat menyebabkan kerusakan rasa dan bau tengik pada minyak (Haryani, 2006).
Kadar air makanan terdapat dalam berbagai bentuk diantaranya air terikat secara lemah, air teradsorbsi pada permukaan makromolekul seperti protein, pektin, pati dan selulosa (Sudarmadji, 1989).
b. Bobot Jenis
Bobot jenis merupakan perbandingan berat suatu volume minyak atau lemak pada suhu 250C dengan berat air pada volume
dan suhu yang sama (Rohman dan Sumantri, 2013). Cara ini dapat digunakan untuk semua minyak dan lemak yang dicairkan. Alat yang digunakan untuk penentuan ini adalah piknometer (Badan Standar Nasional, 2008).
3. Cara Kimia
a) Bilangan Asam
dalam 1 gram minyak, lemak, resin, balsam, atau senyawa-senyawa organik serupa dengan komposisi yang kompleks (Rohman dan Sumantri, 2013).
Bilangan asam juga dapat diungkapkan sebagai banyaknya mililiter natrium hidroksida (NaOH) 0,1 N yang dibutuhkan untuk menetralkan asam bebas dalam 10 gram minyak atau lemak. Bilangan ini ditentukan dengan cara titrasi terhadap sejumlah sampel dalam alkohol atau dalam larutan alkohol-eter menggunakan larutan baku alkali dengan indikator fenolftalein (pp) (Rohman dan Sumantri, 2013).
Angka asam yang besar menunjukkan asam lemak bebas yang berasal dari hidrolisa minyak ataupun karena proses pengolahan yang kurang baik. Makin tinggi angka asam maka semakin rendah kualitas dari minyak (Haryani, 2006).
b) Bilangan Penyabunan
Bilangan penyabunan atau nilai penyabunan atau bilangan koettsdorfer didefinisikan sebagai banyaknya milligram KOH yang dibutuhkan untuk menyabunkan lemak secara sempurna dari 1 gram lemak atau minyak (Rohman dan Sumantri, 2013).
c) Bilangan Iodium
kuantitatif yang menyatakan banyaknya asam-asam lemak tidak jenuh, baik dalam bentuk bebas atau dalam bentuk ester, yang terdapat dalam minyak atau lemak karena asam lemak ini mempunyai sifat yang mampu menyerap iodium (Rohman dan Sumantri, 2013).
d) Uji Angka Peroksida (ketengikan)
Angka peroksida merupakan angka terpenting untuk menentukan derajat kerusakan pada minyak atau lemak. Asam lemak tidak jenuh dapat mengikat oksigen pada ikatan rangkapnya sehingga membentuk peroksida. Adanya peroksida dapat ditentukan secara iodometri. Angka peroksida atau bilangan peroksida dinyatakan sebagai banyaknya mili-ekuivalen peroksida dalam setiap 1000 g (1 kilogram) minyak, lemak, dan senyawa-senyawa lain (Rohman dan Sumantri, 2013).
4. Pengujian Menggunakan Spektrum Infra Merah (FTIR)
Spektrofotometer Infra Merah adalah salah satu alat yang banyak dipakai untuk mengidentifikasi senyawa baik alami maupun buatan. Bila sinar inframerah dilewatkan melalui cuplikan organik, maka sejumlah frekuensi akan diserap sedang frekuensi yang lain diteruskan atau ditransmisikan tanpa diserap (Watson, 2010).
diberikan terhadap molekul cukup mengalami vibrasi. Macam-macam vibrasi ada 2 yaitu ada vibrasi regangan atau stretching dan vibrasi
bending (Watson, 2010).
Dua jenis instrument yang biasa digunakan untuk memperoleh spektrum Infra Merah adalah instrument dispersive, yang menggunakan suatu monokromaton untuk memilih masing-masing bilangan gelombang secara berurutan untuk memantau intensitasnya setelah radiasi melewati sampel, dan instrument transformasi fourier, yang menggunakan suatu interferometer. Interferometer menggunakan cermin bergerak untuk memindahkan bagian radiasi yang dihasilkan oleh suatu sumber (Watson, 2010).
Instrument spektrofotometer Infra Merah (Watson, 2010): a. Sumber radiasi
Pada sistem optik FTIR digunakan radiasi LASER (Light Amplification by Stimulated Emmision of Radiation) yang berfungsi sebagai radiasi yang diinterferensikan dengan radiasi inframerah agar sinyal radiasi inframerah yang diterima oleh detektor secara utuh dan lebih baik.
b. Sampel kompartemen
c. Interferometer
Komponen utama spektrofotometer FTIR adalah interferometer yang mempunyai fungsi menguraikan radiasi InfraMerah menjadi komponen-komponen frekuensi.
d. Detektor
Detektor mengubah sinyal radiasi InfraMerah menjadi sinyal listrik.
Gambar 2. Interferometer yang digunakan dalam instrument FTIR (Stuart, 2004)
Keuntungan mnggunakan spektrofotometer InfraMerah adalah hasil pindai spektrum dapat diperoleh dalam 1 detik. Selain itu, instrument tersebut dihubungkan dengan komputer. Spektrum FTIR mempunyai sifat fisik yang spesifik yaitu kemungkinan dua senyawa punya spektrum yang sama adalah sangat kecil. Sinar mengalami perubahan dahulu kemudian masuk ke sampel (Watson, 2010).
sampel (padat, cair, dan gas). Hasil berupa spektra dapat digunakan untuk analisis kualitatif dan kuantitatif (Hof, 2003).
Komponen dasar spektrometer IR sama dengan UV-tampak, tetapi sumber, detektor, dan komponen optiknya sedikit berbeda. Mula-mula sinar infra merah dilewati melalui sampel dan larutan pembanding, kemudian dilewatkan pada monokromaton untuk menghilangkan sinar yang tidak diinginkan (stray radiation). Berkas ini kemudian didispersikan melalui prisma atau grating. Dengan melewatkannya melalui slit, sinar tersebut dapat difokuskan pada detektor (Khopkar, 1990).
Alat IR umumnya dapat merekam sendiri absorbansinya secara tepat. Temperature dan kelembaban ruang harus dikontrol. Kelembaban maksimum yang diperoleh adalah 50%. Jika kelembaban melebihi batas tersebut, permukaan prisma dan sel alkali halida akan menjadi suram. Perubahan suhu akan berpengaruh pada ketepatan dan kalibrasi panjang gelombang. Karena alasan-alasan tersebut, maka alat berkas ganda lebih popular dibanding berkas tunggal (Khopkar, 1990).
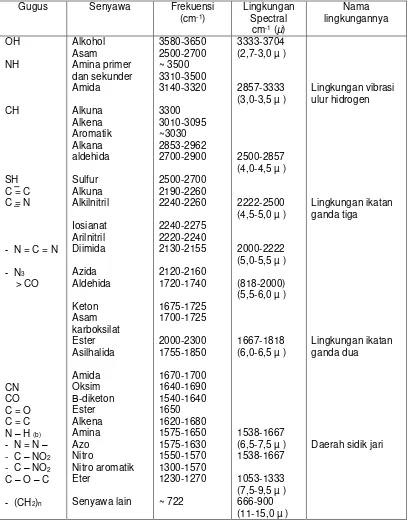
Tabel 2. Pita Absorpsi Infra Merah pada beberapa panjang gelombang (Khopkar, 1990):
BAB III
METODE PENELITIAN A. Waktu Dan Tempat Penelitian
Penelitian ini dilakukan pada bulan September 2015 sampai April 2016 di Laboratorium Kimia Farmasi, Fakultas farmasi, Universitas Muslim Indonesia, Laboratorium Teknik Kimia, Politeknik Ujung Pandang dan Laboratorium Biokimia, FMIPA, Universitas Hasanuddin.
B. Populasi dan Sampel
Populasi dalam penelitian ini adalah minyak kelapa murni industri rumah tangga, sampel yang digunakan dalam penelitian ini adalah minyak kelapa murni asal desa Pasarwajo, Kabupaten Buton, Sulawesi Tenggara.
C. Metode Kerja
Penelitian ini dilakukan secara eksperimental laboratorium dengan menggunakan metode analisis minyak dan lemak secara fisika, kimia dan Spektrofotometri Infra Merah (FTIR).
D. Alat dan Bahan 1. Alat-alat yang Digunakan
2. Bahan-bahan yang Digunakan
Bahan-bahan yang digunakan dalam peneletian ini antara lain, aquades, alkohol 95% netral 50 mL, indikator fenolftalein (pp), kloroform 10 mL, larutan asam asetat-kloroform (3:2) 30 mL, larutan baku HCl 0,4768 N, larutan baku KOH 0,0993 N, larutan baku natrium tiosulfat (Na2S2O3) 0,0982 N, larutan jenuh KI 0,5 mL, larutan KI 15%
10 mL, larutan KOH-etanolik 50 mL, larutan pati 1% 2 mL, pereaksi iodium-bromida 25 mL, sampel minyak kelapa murni.
E. Prosedur Penelitian 1. Penyiapan Alat dan Bahan
Alat dan bahan disiapkan sesuai dengan kebutuhan penelitian yang akan dilaksanakan.
2. Pengambilan dan Pengolahan Sampel
Sampel berupa minyak kelapa murni buatan industri rumah tangga diambil dari desa Pasarwajo, Buton, Sulawesi Tenggara.
3. Prosedur Pengujian a. Organoleptik
b. Cara Fisika a) Kadar Air
Wadah tahan panas dioven pada suhu 105 – 110oC
selama 30 menit kemudian ditempatkan pada desikator. Setetah dingin wadah ditimbang sehingga diperoleh berat wadah kosong. Ke dalam wadah ditambahkan dengan lebih kurang 5,0 gram minyak kelapa kemudian dioven pada suhu 105 – 110oC
selama 30 menit. Wadah yang berisi sampel didinginkan dalam desikator kemudian ditimbang sampai berat konstan (Suastuti, 2009).
Kadar Air (%) = 𝑏𝑒𝑟𝑎𝑡 𝑎𝑤𝑎𝑙 – 𝑏𝑒𝑟𝑎𝑡 𝑎𝑘ℎ𝑖𝑟
𝑏𝑒𝑟𝑎𝑡 𝑎𝑤𝑎𝑙 𝑥 100 %
b) Bobot Jenis
Sampel minyak atau lemak dimasukkan kedalam piknometer lalu ditutup dan direndam dalam air pada suhu 250C
± selama 30 menit. Bagian luar piknometer dikeringkan lalu ditimbang. Dengan cara yang sama, piknometer diisi air dengan jumlah volume yang sama lalu ditimbang (Rohman dan Sumantri, 2013).
Bobot jenis minyak = (𝑎−𝑏)
(𝑐−𝑏)
c. Cara Kimia (Rohman dan Sumantri, 2013): a) Bilangan Asam
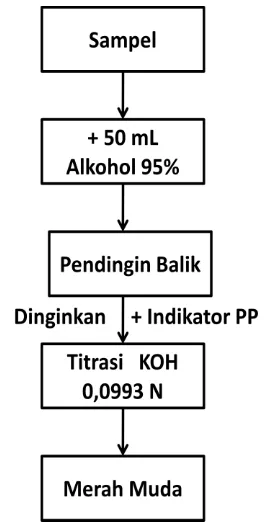
Sebanyak lebih kurang 5 g minyak ditimbang secara seksama, lalu dimasukkan kedalam Erlenmeyer, dan ditambah 50 mL alkohol 95% netral. Setelah ditutup dengan pendingin balik, larutan dipanaskan sampai mendidih dan digojok kuat-kuat untuk melarutkan asam lemak bebasnya. Setelah dingin, larutan dititrasi dengan larutan baku KOH 0,0993 N menggunakan indikator fenolftalein (pp). Titik akhir titrasi tercapai apabila terbentuk warna merah muda yang tidak hilang selama 0,5 menit.
Bilangan asam = 𝑚𝐿 𝐾𝑂𝐻 𝑥 𝑁 𝐾𝑂𝐻 𝑥 56,1
𝑏𝑒𝑟𝑎𝑡 𝑠𝑎𝑚𝑝𝑒𝑙 (𝑔)
Keterangan : N = Normalitas b) Bilangan Penyabunan
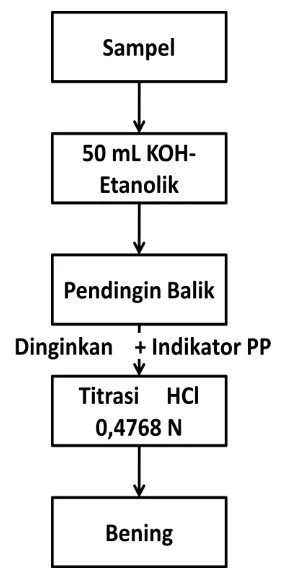
yakni dengan prosedur yang sama kecuali tanpa bahan lemak atau minyak.
Bilangan penyabunan :
=56,1 𝑥 𝑁 𝑥 (𝑉 𝐻𝐶𝑙 𝑏𝑙𝑎𝑛𝑘𝑜 – 𝑉 𝐻𝐶𝑙 𝑠𝑎𝑚𝑝𝑒𝑙) 𝑏𝑒𝑟𝑎𝑡 𝑠𝑎𝑚𝑝𝑒𝑙 (𝑔)
Keterangan : V = Volume titrasi N = Normalitas c) Bilangan Iodium
Sebanyak kurang lebih 0,2 g bahan minyak ditimbang secara seksama, lalu dimasukkan dalam labu iodium (Iodine Flask). Larutan selanjutnya ditambah 10 mL kloroform dan 25 mL pereaksi iodium-bromida dan dibiarkan di tempat gelap selama 30 menit dengan kadangkala digojog. Larutan kemudian ditambah 10 mL larutan KI 15% dan 50 mL akuades yang telah dididihkan, lalu dititrasi segera dengan larutan baku natrium tiosulfat (Na2S2O3) 0,0982 N sampai larutan berwarna kuning
Bilangan iodium = (V tio blanko – V tio sampel) x N tio x 12,691
berat sampel (g)
Keterangan :
V tio = Volume titrasi iodium N tio = Normalitas titrasi iodium d) Uji angka peroksida (ketengikan)
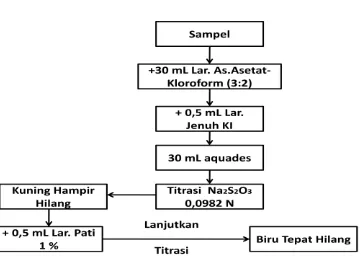
Sebanyak kurang lebih 5 gram sampel ditimbang secara seksama, lalu dimasukkan dalam Erlenmeyer bertutup 250 mL dan ditambah 30 mL larutan asam asetat-kloroform (3:2). Larutan digoyangkan sampai bahan terlarut semua lalu ditambah 0,5 mL larutan jenuh KI. Larutan selanjutnya didiamkan selama 1 menit dengan kadangkala digoyang kemudian ditambah 30 mL akuades. Iodium yang dibebaskan dititrasi dengan larutan baku natrium tiosulfat (Na2S2O3) 0,0982
N sampai warna kuning hampir hilang lalu ditambah 2 mL larutan pati 1 %. Titrasi dilanjutkan sampai warna biru tetap hilang.
d. Pengujian Menggunakan Spektrofotometri (FTIR)
4. Pengujian Menggunakan Spektrofotometri FTIR
Gugus fungsi Kode Sampel
A B C
C-H Aldehid 2852,81 2851,85 2853,78 Alkana 2921,29 2919,36 2924,18
C=O Ester 1742,74 1742,74 1744,67
Keterangan :
B. PEMBAHASAN
Minyak kelapa murni buatan industri rumah tangga atau dengan cara tradisional, umumnya dihasilkan dari wilayah-wilayah Sumatera, Sulawesi, Kalimantan, Maluku, dan daerah Indonesia timur lainnya. Dalam penelitian ini diperoleh sampel minyak A, B, dan C asal desa Pasarwajo, Buton, Sulawesi Tenggara dan diperoleh data analisis baik secara organoleptik, fisika, kimia dan analisis gugus menggunakan FTIR.
Uji kualitas minyak kelapa murni secara organoleptik pada sampel A, B, dan C memiliki aroma khas kelapa segar dan tidak tengik. Rasa normal khas minyak kelapa dan memiliki warna kekuningan.
Dalam penelitian ini, dilakukan analisis secara fisika meliputi analisis kadar air dan bobot jenis. Jika dalam minyak terdapat air, maka akan mengakibatkan reaksi hidrolisis yang dapat menyebabkan kerusakan rasa dan bau tengik pada minyak. Hasil yang diperoleh dalam analisis kadar air sampel minyak kelapa murni adalah sampel A = 0,024%, B = 0,005% dan C = 0,006%. Ini menunjukkan bahwa ketiga sampel tersebut sesuai dengan standar SNI:2008 yaitu nilai kadar air maksimal 0,2%.
Analisis secara kimia meliputi analisis bilangan asam, bilangan penyabunan, bilangan iodium dan uji angka peroksia. Penentuan bilangan asam dilakukan untuk menentukan banyaknya asam lemak bebas yang terdapat dalam sampel. Bilangan ini ditentukan dengan cara titrasi sejumlah minyak dan alkohol menggunakan larutan baku alkali dengan indikator fenolftalein (pp). Hasil yang diperoleh adalah sampel A = 1,5473, B = 0,6486, dan C = 0,4708. Hal ini tidak sesuai dengan standar SNI:2008 yakni nilai bilangan asam adalah maksimal 0,2. Angka asam yang besar menunjukkan asam lemak bebas yang berasal dari hidrolisa minyak atau karena pengolahan yang kurang baik.
dengan bobot molekul kecil memiliki rantai karbon pendek, sebaliknya minyak dengan bobot molekul besar memiliki rantai karbon panjang.
Analisis bilangan iodium bertujuan untuk menentukan banyaknya ikatan rangkap dalam asam lemak. Penentuan bilangan iodida diperoleh melalui titrasi iodometri yang dilakukan setelah reaksi adisi berlangsung sempurna. Kelebihan bromin direaksikan dengan KI (Kalium Iodida) agar terbentuk I2 . Selanjutnya I2 direaksikan dengan Na2S2O3. Hasil yang
diperoleh adalah sampel A = 1,3605, B = 1,1578, dan C = 0,911. Data yang diperoleh tidak sesuai dengan standar SNI:2008 yakni nilai bilangan iodin yaitu 4,1-11,0 (g iod/g). Hal ini disebabkan karena sampel tersebut memiliki ikatan rangkap yang sedikit.
Untuk penentuan bilangan peroksida dapat ditentukan secara iodometri yaitu dengan mengoksidasi minyak dengan KI dan Iod yang dilepaskan. Kemudian dititrasi dengan larutan standar Natrium Tiosulfat. Dalam analisis, digunakan campuran asam asetat dan kloroform untuk melarutkan minyak karena alkali iodida akan bereaksi dengan sempurna dalam larutan bersuasana asam. Digunakan larutan jenuh KI untuk membebaskan iodin yang ditandai dengan terbentuknya warna kuning pada sampel. Penambahan indikator amilum/pati adalah sebagai indikator I2 sebelum titrasi dengan Na2S2O3. Hasil yang diperoleh adalah sampel A =
oksigen pada ikatan rangkapnya sehingga membentuk peroksida dan tingginya angka peroksida menunjukkan semakin rendahnya mutu suatu minyak atau lemak. Sedangkan pada sampel B dan C sesuai dengan standar SNI:2008 yaitu maksimal 2,0 (mg ek/kg).
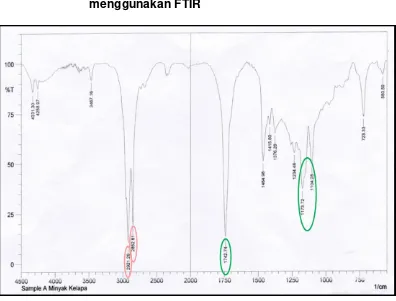
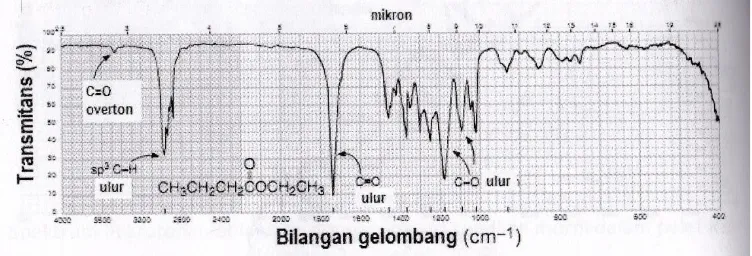
Dalam pengujian menggunakan spektrofotometri FTIR pada sampel A, B dan C diperoleh puncak yang menandakan adanya gugus C-H yang dapat berupa alkana dan aldehid (Lampiran 7 dan 8). Hal ini sesuai dengan komposisi asam lemak yang terdapat dalam minyak kelapa diantaranya yaitu asam laurat (C12) dan asam miristat (C14) (Alamsyah,
2005). Selain itu, terdapat puncak yang menandakan adanya gugus C=O yaitu ester (Lampiran 7 dan 8). Hal ini sesuai dengan literatur yaitu adanya vibrasi ulur C=O terjadi di 1739 cm-1 dalam ester alifatik. Ester-ester ini
mempunyai dua pita yang kuat disekitar 1200-1100 cm-1 (Lampiran 9).
(Rohman dan Gandjar, 2012).
menjadi senyawa “monolaurin” yang berfungsi sebagai antimikroba
BAB V
KESIMPULAN DAN SARAN
A. Kesimpulan
Dari hasil penelitian yang telah dilakukan terhadap analisis mutu minyak kelapa murni buatan industri rumah tangga secara menyeluruh bahwa ketiga sampel tersebut tidak memenuhi standar mutu SNI 3781:2008 sebagai minyak kelapa.
B. Saran
DAFTAR PUSTAKA
Alamsyah, A.N., 2005, Mengenal Lebih Dekat: Virgin coconut oil, Agromedia Pustaka Cet-1, Jakarta.
Arghainc., 2008, Minyak Sawit, Chemical Engineering, WordPress.
Badan Standardisasi Nasional., 2008, SNI 7381:2008, Minyak Kelapa Virgin (VCO), Jakarta, Badan Standardisasi Nasional.
Baswardojo, D., 2005, Seluk Beluk Pembuatan Minyak Kelapa & VICO,
INDO COCO, Jakarta.
Backer, C.A., Van den Brink, B., 1986, Flora of Java (Spermatophytes Only), Vol. III, Wolter-Noordhoff, NVP, Groningen.
Cronquist, A., 1981, An Integrated System of Classification of Flowering Plants, Columbia University Press, New York.
Dede., Zainal, G., Yuni, H., 2005, Bebas Segala Penyakit Dengan VCO,
Puspa Swara, Jakarta.
Dirjen POM., 1995, Farmakope Indonesia edisi IV, Depkes RI, Jakarta. Enig, M.G., 1999, Coconut: In Support Of Good Health In The 21st
Century, USA (http://coconutoil.com/coconut_oil_21st _century) Estien, Y., 2005, Kimia Fisika Untuk Paramedis, Andi Press, Yogyakarta. Hartin, R dan Surtami., 2005, Taklukan Penyakit Dengan VCO (Virgin
Coconut Oil), Seri Agrisehat, Cetakan Ketiga, Penebar Swadaya, Jakarta.
Haryani, K., Widayat., Suherman., 2006, Optimasi Proses Adsobsi Minyak Goreng Bekas Dengan Adsorben Zeolit Alam, Studi Pengurangan Bilangan Asam, Teknik Gelagar, Jakarta.
Heryani, N,J., Towaha., Wahyudi., dan Wagyono., 2000, Pembuatan Minyak Secara Fermentasi, Makalah Penelitian Tenaga Instruktur Penerapan Teknologi Perkebunan Propinsi Riau.
Ketaren, S., 2008, Pengantar Teknologi Minyak Dan Lemak Pangan,
Cetakan Pertama, Universitas Indonesia Press, Jakarta.
Khopkar, S, M., 1990, Konsep Dasar Kimia Analitik, Penerbit Universitas 1995, Karakterisasi daging buah Kelapa Hibrida untuk bahan baku industri makanan, Laporan Hasil Penelitian, Kerjasama Proyek Pembinaan Kelembagaan Penelitian Pertanian nasional, Badan Litbang.
Rohman, A., 2014, Spektroskopi Inframerah dan Kemometrika untuk Analisis Farmasi, Pustaka Pelajar, Yogyakarta.
Rohman, A., Gandjar, G.I., 2012, Analisis Obat Secara Spektrofotometri Dan Kromatografi, Pustaka Pelajar, Yogyakarta.
Rohman, A., Sumantri., 2013, Analisis Makanan, Gajah Mada University Press, Yogyakarta.
Rohman, A., Yaakob B.Che Man., 2012, Pengembangan Metode Deteksi Minyak Kedelai Dalam Campuran Minyak Kelapa Murni dengan Spektroskopi Infra Merah dan Kemometrika, AGRITECH, Vol. 32, No.2. Universitas Gajah Mada, Yogyakarta.
Setiaji, B., Prayugo, S., 2006, Membuat VCO Berkualitas Tinggi, Penebar Swadaya, Jakarta.
Setiawan, O., Ruskandi., 2004, Pembuatan Minyak Kelapa Secara Tradisional dengan Pelakuan Suhu Air yang Berbeda, Prosiding Temu Teknis Nasional Tenaga Fungsional Pertanian, Parungkuda Sukabumi.
Soekarto., 1990, Penilaian Organoleptik Untuk Industri Pangan dan Hasil Pertanian, Bhatara Aksara, Jakarta.
Stuart, B., 2004, Infra red Spectroscopy: Fundamentals and applications
John, Wiley and Sons, Chichester, UK
Suastuti, D.A., 2009, Kadar Air dan Bilangan Asam dari Minyak Kelapa yang dibuat dengan cara Tradisional dan Fermentasi, Jurusan KimiaFMIPA, Universitas Udayana, Bukit Jimbaran.
Sudarmaji., Budiono., Ningrum, S., 1989, Analisis Badan Makanan dan
Pertanian, Liberty, Yogyakarta.
Suhardiman, D., 1999, Bertanam Kelapa Hibrida, Penebar Swadaya,
Jakarta.
Suryani, A.D., 2005, Analisis Mutu Minyak Kelapa Tradisional asal desa Sidodadi Kabupaten Polmas, UMI, Makassar.
Tuminah, S., 2009, Efek Asam Lemak Jenuh Dan Asam Lemak Tak Jenuh
“Trans” Terhadap Kesehatan”, Media Peneliti dan Pengembang Kesehatan Volume XIX, Suplemen II, Biomedis Dan Farmasi.
Wahab, A.W., Dewang, S., Armynah, B., Ponganan, K., 2011, Analisis Spektrum Infra Merah dari Minyak Goreng Kelapa untuk Identifikasi perubahan Panjang Gelombang akibat Variasi Temperatur, Jurusan Kimia FMIPA UH, Universitas Hasanuddin.
Warisno., 2003, Budidaya Kelapa Genjah, Kanisius, Yogyakarta. Watson., David., 2010, Analisis Farmasi, EGC, Jakarta.
White, B., 2009, Dietary Fatty Acid American Family Physician.
Lampiran 1. Pembuatan Pereaksi
a. Larutan Baku KOH 0,1 N (Dirjen POM, 1995)
Ukur saksama lebih kurang 25 mL asam klorida 0,1 N, encerkan dengan 50 mL air, tambahkan 2 tetes fenolftalein 0,1 %, dan titrasi dengan larutan kalium hidroksida etanol hingga terjadi warna merah muda pucat yang mantap.
b. Larutan Baku HCl 0,5 N (Dirjen POM, 1995)
Timbang seksama lebih kurang 1,5 g baku primer natrium karbonat anhidrat yang sebelumnya telah dipanaskan pada suhu 2700 selama 1
jam. Larutkan dalam 100 mL air dan tambahkan 2 tetes merah metil.
Tambahkan asam perlahan-lahan dari buret sambil diaduk hingga larutan berwarna merah muda pucat. Panaskan larutan hingga mendidih, dinginkan dan lanjutkan titrasi. Panaskan lagi hingga mendidih, dan titrasi lagi bila perlu hingga warna merah muda pucat tidak hilang dengan pendidihan lebih lanjut.
c. Larutan Baku Na2S203 0,1 N (Dirjen POM, 1995)
Timbang saksama lebih kurang 210 mg kalium bikromat p yang sebelumnya telah dihaluskan dan dikeringkan pada suhu 1200 selama 4
dengan air dan titrasi iodum yang dibebaskan dengan larutan natrium tiosulfat hingga warna hijau kekuningan. Tambahkan 3 mL kanji dan lanjutkan titrasi sampai warna biru tepat hilang.
d. Larutan Jenuh Kalium Iodida (KI)
Aquades sebanyak 5 mL dimasukkan kedalam tabung reaksi lalu ditambahkan serbuk kalium iodida. Setalah itu, larutan tersebut diaduk sampai serbuk kalium iodida tidak larut lagi sehingga berbentuk larutan kalium iodida jenuh.
e. Larutan Amilum (Pati)
Lampiran 2. Skema Kerja Analisis Minyak Kelapa Murni
Gambar 5. Skema kerja penentuan bilangan iodine
Lampiran 3. Sampel minyak kelapa murni
Lampiran 4. Perhitungan (Sampel A) 4.1 Kadar Air
Diketahui : Berat wadah kosong = 52,4933 g Berat sampel = 5,0345 g
Berat wadah + sampel setelah pemanasan = 57,5136 g % Kadar Air =(52,4933 + 5,0345) − 57,5136(52,4933 + 5,0345) x100%
=57,5279 − 57,513657,5279 x100%
= 0,0248%
4.2 Bobot Jenis
Diketahui : Berat piknometer kosong = 32,2049 g Berat piknometer + sampel = 77,6553 g Berat piknometer + air = 81,6504 g Bobot Jenis = (77,6553−32,2049)
(81,6504−32,2049)=
45,4504
49,4455= 0,9192 𝑔
4.3 Bilangan asam
Diketahui : Berat sampel = 5,4002 g Volume titrasi KOH = 1,5 mL Normalitas KOH = 0,0993 N Bilangan Asam =1,5 x 0,0993 x 56,1
4.4 Bilangan Penyabunan
Diketahui : Berat sampel = 1,6817 g Volume titrasi HCl = 10,25 mL Volume titrasi blanko = 24,55 mL Normalitas HCl = 0,4768 N Bilangan Penyabunan = 56,1 x 0,4768 (24,55−10,25)
1,6817 = 227,449 (mg KOH/gr)
4.5 Bilangan Iodin
Diketahui : Berat sampel = 0,229 g Volume titrasi Na2S2O3 = 6,75 mL
Volume titrasi blanko = 7 mL Normalitas Na2S2O3 = 0,0982 N
Bilangan Iodin = (7−6,75)
0,229 x 0,0982 x 12,691 = 1,3605 (g iod/100g)
4.6 Bilanga Peroksida
Diketahui : Berat sampel = 5,3135 g Volume titrasi Na2S2O3 = 0,3 mL
Normalitas Na2S2O3 = 0,0982 N
Bilangan Peroksida = 0,3 x 0,0982 x 1000
Lampiran 5. Perhitungan (Sampel B) 5.1 Kadar Air
Diketahui : Berat wadah kosong = 55,8560 g Berat sampel = 5,0071 g
Berat wadah + sampel setelah pemanasan = 60,8600 g % Kadar Air =(55,8560 + 5,0071) − 60,8600(55,85603 + 5,0071) x100%
= 60,8631 − 60,860060,8631 x100%
= 0,005224832941%
5.2 Bobot Jenis
Diketahui : Berat piknometer kosong = 31,7454 g Berat piknometer + sampel = 77,3632 g Berat piknometer + air = 81,3831 g Bobot Jenis = (77,36325−31,74544)
(81,38315−31,74544 =
45,61781
49,63771= 0,9190 𝑔
5.3 Bilangan asam
Diketahui : Berat sampel = 5,1527 g Volume titrasi KOH = 0,6 mL Normalitas KOH = 0,0993 N Bilangan Asam =0,6 x 0,0993 x 56,1
5.4 Bilangan Penyabunan
Diketahui : Berat sampel = 1,7318 g Volume titrasi HCl = 10,4 mL Volume titrasi blanko = 24,55 mL
N HCl = 0,4768 N
Bilangan Penyabunan = 56,1 x 0,4768 x (24,55−10,4)
1,7318 = 218,552 (mg KOH/gr)
5.5 Bilangan Iodin
Diketahui : Berat sampel = 0,2691 g Volume titrasi Na2S2O3 = 6,75 mL
Volume titrasi blanko = 7 mL Normalitas Na2S2O3 = 0,0982 N
Bilangan Iodin = (7−6,75)
0,2691 x 0,0982 x 12,691 = 1,1578 (g iod/100g)
5.6 Bilanga Peroksida
Diketahui : Berat sampel = 5,4943 g Volume titrasi Na2S2O3 = 0,1 mL
Normalitas Na2S2O3 = 0,0982N
Bilangan Peroksida = 0,1 x 0,0982x 1000
Lampiran 6. Perhitungan (Sampel C) 6.1 Kadar Air
Diketahui : Berat wadah kosong = 55,5737 g Berat sampel = 5,0068 g
Berat wadah + sampel setelah pemanasan = 60,5767 g
% Kadar Air =(55,5737 + 5,0068) − 60,5767(55,5737 + 5,0068) x100%
= 60,5806 − 60,576760,5806 x100%
= 0,00633866078%
6.2 Bobot Jenis
Diketahui : Berat piknometer kosong = 31,8716 g Berat piknometer + sampel = 77,4111 g Berat piknometer + air = 81,4237 g Bobot Jenis = (77,4111−31,8716)
(81,4237−31,8716)=
45,5395
49,5520= 0,9190 𝑔
6.3 Bilangan asam
Diketahui : Berat sampel = 5,3246 g Volume titrasi KOH = 0,45 mL Normalitas KOH = 0,0993 N Bilangan Asam = 0,45 x 0,0993 x 56,1
6.4 Bilangan Penyabunan
Diketahui : Berat sampel = 1,5639 g Volume titrasi HCl = 10,75 mL Volume titrasi blanko = 24,55 mL
N HCl = 0,4768 N
Bilangan Penyabunan = 56,1 x 0,4768 x (24,55−10,75)
1,5639 = 236,030 (mg KOH/gr)
6.5 Bilangan Iodin
Diketahui : Berat sampel = 0,2052 g Volume titrasi Na2S2O3 = 6,85 mL
Volume titrasi blanko = 7 mL Normalitas Na2S2O3 = 0,0982 N
Bilangan Iodin = (7−6,85)
0,2052 x 0,0982 x 12,691 = 0,911 (g iod/100g)
6.6 Bilanga Peroksida
Diketahui : Berat sampel = 5,0717 g Volume titrasi Na2S2O3 = 0,1 mL
Normalitas Na2S2O3 = 0,0982 N
Bilangan Peroksida = 0,1 x 0,0982 x 1000
Lampiran 7. Hasil analisis spektrum minyak kelapa murni menggunakan FTIR
Keterangan :
Gugus C-H : Aldehid (2852,81) Alkana (2921,29)
Gugus C=O : Ester (1742,74) dan (1173,72 dan 1104,28)
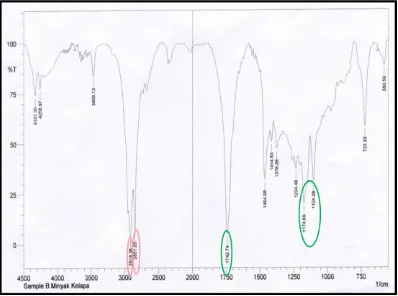
Keterangan :
Gugus C-H : Aldehid (2851,85) Alkana (2919,36)
Gugus C=O : Ester (1742,74) dan (1174,69 dan 1104,28)
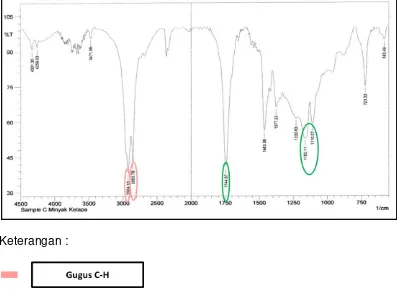
Keterangan :
Gugus C-H : Aldehid (2853,78) Alkana (2924,18)
Gugus C=O : Ester (1744,67) dan (1163,11 dan 1110,07)
Lampiran 8. Hasil Interpretasi Spektrum Infra Merah Minyak Kelapa Murni (Rohman, 2014):
Gugus Jenis Vibrasi Frekuensi (Cm-1)
C-H Alkana (ulur) 3000-2850
Aldehid 2900-2800
Lampiran 9. Hasil Interpretasi spektrum InfraMerah yang menunjukkan adanya ester (Pavia et al, 2009)