BAB 2 TINJAUAN PUSTAKA 2.1 Tumbuhan Bawang Merah 2.1.1 Morfologi Bawang Merah (Allium cepa L.) - Isolasi Senyawa Flavonoida Dari Kulit Bawang Merah (Allium cepa L.)
Teks penuh
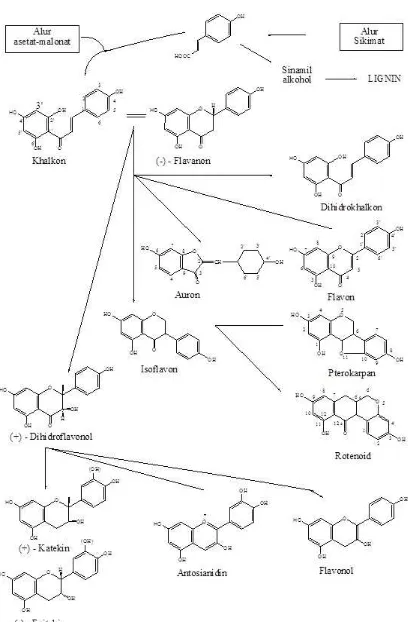
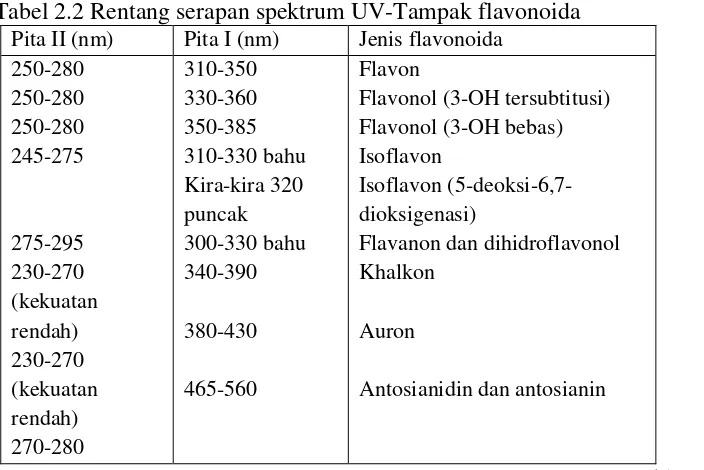
Gambar

Dokumen terkait
pada tahap pra produksi ini kegiatan yang dilakukan penulis adalah melakukan segala persiapan untuk tahap produksi, seperti pengumpulan ide dan brainstorming,
Dalam hal dengan sofware aplikasi komputer yang digunakan maka telah dilakukan penginstalan sistem operasi untuk komputer yaitu windows XP Profesional serta
Strategi Mahasiswa berwirausaha dalam mencapai tujuannya menjadi mahasiswa yang wajib mengikuti kegiatan akademis (kuliah) dan menjalankan usaha untuk menambah
Faktor-faktor yang menimbuklkan stigma dan diskriminasi pada masyarakat adalah penyakit HIV/AIDS merupakan penyakit yang mematikan dan dapat mengancam nyawa,informasi yang kurang
Prompt diagnosis and treatment of colibacillosis are crucial to ensure optimal productivity in poultry farms.The aim of the study was to provide the latest
Kepastian, ketertiban, dan perlindungan hukum menuntut antara lain bahwa lalu lintas hukum dalam kehidupan masyarakat memerlukan adanya alat bukti yang
pada awalnya kalimat diisi oleh Keterangan waktu, kemudian diikuti oleh Subjek, unsur pengisi subjeknya adalah Nomina (N), unsur pengisi Predikat adalah berupa Verba (V),
Berdasarkan hasil penelitian dan pembahsan yang diuraikan di atas, dapat ditarik kesimpulan bahwa pembelajaran berbasis masalah pada kegiatan praktikum fotosintesis dan