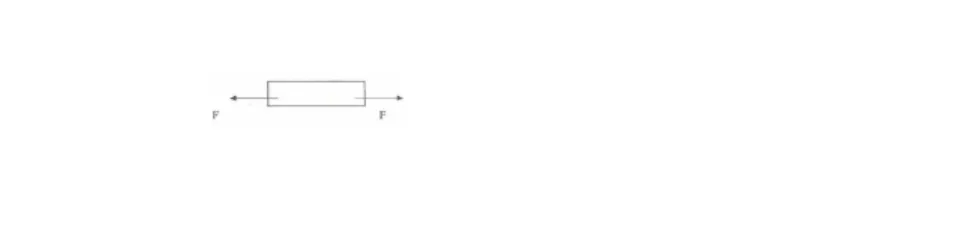SKRIPSI SKRIPSI
Diajukan untuk melengkapi tugas dan memenuhi syarat mencapai gelar Sarjana Sains Diajukan untuk melengkapi tugas dan memenuhi syarat mencapai gelar Sarjana Sains
OLEH: OLEH: PUTRI RIZKY PUTRI RIZKY NIM : 140822018 NIM : 140822018 DEPARTEMEN KIMIA DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA UNIVERSITAS SUMATERA UTARA
MEDAN MEDAN 2017 2017 ii ii
PERSETUJUAN PERSETUJUAN
Judul
Judul : : PEMBUATANPEMBUATAN EDIBLE EDIBLE FILM FILM PATI SUKUN PATI SUKUN (( ARTOCARPUS ARTOCARPUS ALTILIS)ALTILIS) DARI DARI PROSESPROSES ASETILASI MENGGUNAKAN ASETAT ASETILASI MENGGUNAKAN ASETAT ANHIDRAT
ANHIDRAT Kategori
Kategori : : SkripsiSkripsi Nama
Nama : Putri Rizky: Putri Rizky Nomor Induk Mahasiswa
Nomor Induk Mahasiswa : 140822018: 140822018 Program
Program : : Sarjana(S1) Sarjana(S1) KimiaKimia Departemen
Departemen : : KimiaKimia Fakultas
Fakultas : : Matematika Matematika dan dan Ilmu Ilmu pengetahuan pengetahuan Alam Alam UniversitasUniversitas Sumatera Utara
Sumatera Utara
Disetujui di Disetujui di Medan,
Medan, Maret Maret 20172017 Komisi Pembimbing :
Komisi Pembimbing : Pembimbing
Pembimbing II II Pembimbing Pembimbing II
Dr.
Dr. Mimpin Mimpin Ginting, Ginting, MS MS Dr. Dr. Cut Cut Fatimah Fatimah Zuhra, Zuhra, M.SiM.Si NIP. 195510131986011001
NIP. 195510131986011001 NIP. 197404051999032001NIP. 197404051999032001
Diketahui/Disetujui oleh Diketahui/Disetujui oleh
Departemen Kimia FMIPA USU Departemen Kimia FMIPA USU Ketua, Ketua, Dr. Rumondang Bulan, MS Dr. Rumondang Bulan, MS NIP. 195408301985032001 NIP. 195408301985032001 iii iii
PERSETUJUAN PERSETUJUAN
Judul
Judul : : PEMBUATANPEMBUATAN EDIBLE EDIBLE FILM FILM PATI SUKUN PATI SUKUN (( ARTOCARPUS ARTOCARPUS ALTILIS)ALTILIS) DARI DARI PROSESPROSES ASETILASI MENGGUNAKAN ASETAT ASETILASI MENGGUNAKAN ASETAT ANHIDRAT
ANHIDRAT Kategori
Kategori : : SkripsiSkripsi Nama
Nama : Putri Rizky: Putri Rizky Nomor Induk Mahasiswa
Nomor Induk Mahasiswa : 140822018: 140822018 Program
Program : : Sarjana(S1) Sarjana(S1) KimiaKimia Departemen
Departemen : : KimiaKimia Fakultas
Fakultas : : Matematika Matematika dan dan Ilmu Ilmu pengetahuan pengetahuan Alam Alam UniversitasUniversitas Sumatera Utara
Sumatera Utara
Disetujui di Disetujui di Medan,
Medan, Maret Maret 20172017 Komisi Pembimbing :
Komisi Pembimbing : Pembimbing
Pembimbing II II Pembimbing Pembimbing II
Dr.
Dr. Mimpin Mimpin Ginting, Ginting, MS MS Dr. Dr. Cut Cut Fatimah Fatimah Zuhra, Zuhra, M.SiM.Si NIP. 195510131986011001
NIP. 195510131986011001 NIP. 197404051999032001NIP. 197404051999032001
Diketahui/Disetujui oleh Diketahui/Disetujui oleh
Departemen Kimia FMIPA USU Departemen Kimia FMIPA USU Ketua, Ketua, Dr. Rumondang Bulan, MS Dr. Rumondang Bulan, MS NIP. 195408301985032001 NIP. 195408301985032001 iii iii
PERNYATAAN PERNYATAAN
PEMBUATAN
PEMBUATAN
E D I B L E F I L M
E D I B L E F I L M
PATI SUKUN ( PATI SUKUN (A
Arto
rtoca
carpu
rpus
s a
alt
ltiilis
lis))
TERMODIFIKASI DARI PROSES ASETILASITERMODIFIKASI DARI PROSES ASETILASI MENGGUNAKAN ASETAT ANHIDRAT MENGGUNAKAN ASETAT ANHIDRAT
SKRIPSI SKRIPSI
Saya mengakui bahwa skripsi ini adalah hasil kerja saya sendiri, kecuali beberapa Saya mengakui bahwa skripsi ini adalah hasil kerja saya sendiri, kecuali beberapa kutipan dan ri
kutipan dan ringkasan yang ngkasan yang masing-masing disebutkan masing-masing disebutkan sumbernya.sumbernya.
Medan,
Medan, Maret Maret 20172017
PUTRI RIZKY PUTRI RIZKY 140822018 140822018
PENGHARGAAN
Puji dan syukur penulis panjatkan kepada Tuhan Yang Maha Pemurah dan Maha Penyayang, dengan limpah karunia-Nya penulis dapat menyelesaikan penyusunan skripsi ini dengan judul Pembuatan Edible Film Pati Sukun ( Artocarpus altilis) Termodifikasi Dari Proses Asetilasi Menggunakan Asetat Anhidrat. Untuk itu pada kesempatan ini penulis mengucapkan terimakasih kepada :
1. Bapak Dr.Kerista Sebayang, M.S selaku Dekan FMIPA USU
2. Ibu Dr. Rumondang Bulan MS dan Bapak Drs. Albert Pasaribu M.Sc selaku ketua dan sekretaris departemen Kimia FMIPA USU.
3. Ibu Dr. Cut Fatimah Zuhra, M.Si selaku pembimbing I dan Bapak Dr. Mimpin Ginting, MS selaku pembimbing II yang telah banyak meluangkan waktu dan sabar membimbing serta memotivasi penulis dalam penelitian dan menyelesaikan skripsi ini hingga selesai.
4. Bapak Prof. Dr. Jamaran Kaban, M.Sc selaku Ketua Bidang Kimia Organik FMIPA USU
5. Kepala Laboratorium Kimia Organik FMIPA USU Medan Bapak Dr. Mimpin Ginting, MS beserta Dosen dan Staff Laboratorium Kimia Organik FMIPA USU.
6. Seluruh Dosen Departemen Kimia FMIPA USU yang telah memberikan waktunya untuk memberi bimbingan selama penulis mengikuti kuliah di Departemen Kimia USU, terkhusus kepada Ibu Dr. Cut Fatimah Zuhra, M.Si selaku dosen wali yang telah memberikan pengarahan kepada penulis.
7. Sahabat penulis Fitra, Reisya, Azlia, kak Rizma, Ayu, Eva yang banyak membantu penulis selama kuliah dan seluruh asisten Kimia Organik USU dan teman-teman ekstensi stambuk 2014.
Secara khusus, penulis mengucapkan terima kasih yang sebesar-besarnya kepada kedua orang tua penulis, Ayah TercintaIr. H. Mansyur, MSi dan Ibunda Tersayang Hj. Hadijah Gultom S.Pd. Kons serta kakak dan adik tercinta Rika Silvany, Resti A. Ningrum dan Mhd. Mirza Fadillah yang senantiasa memberikan doa dan dukungan moril dan materil hingga akhirnya penulis menyelesaikan studi. Penulis menyadari bahwa skripsi ini masih jauh dari kesempurnaan karena keterbatasan penulis. Untuk itu dengan segala kerendahan hati, penulis mengharapkan saran yang bersifat membangun demi kesempurnaan skripsi ini.
Akhir kata penulis berharap semoga skripsi ini dapat bermanfaat bagi penelitian dan kemajuan ilmu pengetahuan.Tuhan memberkati kita semua.
Penulis
PEMBUATAN
E D I B L E F I L M
PATI SUKUN (Artocarpus altilis
) TERMODIFIKASI DARI PROSES ASETILASIMENGGUNAKAN ASETAT ANHIDRAT
ABSTRAK
Edible film pati asetat diperoleh dari pati sukun termodifikasi melalui reaksi asetilasi dengan asetat anhidrat. Pembuatan pati asetat termodifikasi melalui reaksi esterifikasi antara pati sukun ( Artocarpus altilis) dengan asetat anhidrat pada variasi pH yaitu 6, 7, 8 dan 9. Hasil modifikasi kemudian diuji gugus fungsi dengan FT-IR dan dihitung derajat substitusinya. Terbentuknya pati asetat didukung oleh spektrum FT-IR dengan munculnya puncak gugus fungsi C=O ester pada pH 6, 7, 8 dan 9 masing-masing pada bilangan gelombang 1635,64 cm-1, 1651,07 cm-1, 1635,64 cm-1 dan 1635,64 cm-1. Hasil pengukuran derajat substitusi dilakukan pada pati asetat pH 6, 7, 8 dan 9 berturut-turut nilai derajat substitusinya yaitu 0,5255; 0,7165; 1,0501; 0,3220. Derajat substitusi yang paling tinggi diperoleh pada pati asetat hasil modifikasi pH 8. Edible film dibuat dari pati sukun dan pati asetat pH 8 menggunakan gliserol sebagai plasticizer. Edible film pati sukun dan pati asetat pH 8 yang diperoleh diuji karakteristiknya dengan hasil sebagai berikut: nilai kuat tarik = 2,1 MPa dan 11,2 MPa. Nilai persen keregangan = 6,17 % dan 8,50 %. Nilai WVTR = 0,1243 Kgm-2 jam-1 dan 0,1130 Kgm-2 jam-1. Nilai derajat mengembang (% Swelling ) = 85,84 % dan 66,10 %. Hasil analisa SEM edible film pati sukun lebih halus permukaan nya sedangkan pati asetat permukaannya kasar atau tidak homogen.
Kata Kunci : Pati sukun, asetat anhidrat, pati asetat, edible film
E D I B L E F I L M
MAKING STARCH BREADFRUIT (Artocarpus altilis
) MODIFIED FROM USING ACETICANHYDRIDE ACETYLATION
ABSTRACT
Edible starch acetate films obtained from breadfruit starch modified with acetic anhydride. Manufacture of modified starch acetate by the esterification reaction between starch breadfruit ( Artocarpus altilis) with acetic anhydride in the variation of pH is 6, 7, 8 and 9. The results were then tested modifications of functional groups by FT-IR and calculated the degree of substitution. The formation of starch acetate is supported by FT-IR spectra with peak emergence of functional groups C=O ester at pH 6, 7, 8 and 9 respectively at wave
number 1635.64 cm-1, 1651.07 cm-1, 1635.64 cm-1 and 1635.64 cm-1.The results of measurements performed on the degree of substitution of starch acetate pH 6, 7, 8 and 9 respectively the degree of substitution is 0.5255; 0.7165; 1.0501; 0.3220. The highest degree of substitution obtained on modified starch acetate pH 8. Edible films made from breadfruit starch and starch acetate pH 8 using glycerol as a plasticizer. Edible films breadfruit starch and starch acetate pH 8 obtained characteristics as follows: the value of tensile strength = 2.1 MPa and 11.2 MPa. Value percent tenseness = 6.17% and 8.50%. WVTR value = 0.1243 kgm-2h-1 and 0.1130 kgm-2h-1. Value degrees expands (% Swelling) = 85.84% and 66.10%. The results of SEM analysis of the edible film more refined starch breadfruit its surface while starch acetate or homogeneous rough surface.
Keywords : Breadfruit starch, Acetic anhydride, starch acetate, edible film
DAFTAR ISI Halaman Persetujuan ii Pernyataan iii Penghargaan iv Abstrak V Abstract Vi
Daftar isi Vii
Daftar tabel Ix Daftar gambar X Daftar lampiran Xi BAB 1 PENDAHULUAN 1.1. Latar Belakang 1 1.2. Permasalahan 4 1.3. Pembatasan Masalah 4 1.4. Tujuan Penelitian 4 1.5. Manfaat Penelitian 5 1.6. Lokasi Penelitian 5 1.7. Metodologi Percobaan 5
BAB 2 TINJAUAN PUSTAKA 2.1
.
Sukun(Artocarpus altilis) 6
2.2. Pati 7 2.3. Modifikasi Pati 9 2.3.1. Modifikasi Fisika 10 2.3.2. Modifikasi Kimia 10 2.3.3. Modifikasi Enzimatis 10 2.3.4. Modifikasi Genetika 10 2.4. Pati Asetat 11 2.5. Asetat Anhidrat 12 2.6. Edible Film 13 2.6.1 Pembuatan Edible Film 15
2.6.2 Sifat Fisiko Kimia Biologi Edible Film
16
2.6.3 Plasticizer Gliserol 17
2.6.4 Edible Film Dari Pati Alami dan Pati Termodifikasi
19
2.7. Karakterisasi 19
2.7.1 Fourier Transform Infrared (FT-IR)
19
2.7.2 Swelling power 20
2.7.3 Scanning Electron Microscopy (SEM)
21
2.7.4 Kuat Tarik 21
BAB 3 METODE PENELITIAN
3.1. Alat-alat 24
3.2. Bahan-bahan 25
3.3. Prosedur Penelitian 25
3.3.1. Pembuatan Larutan NaOH 0,3 M 25
3.3.2. Preparasi Sampel 25
3.3.3. Pembuatan Pati Asetat 26
3.3.4. Analisa Derajat Asetilasi Pati Asetat
26
3.3.5. Penentuan Derajat Mengembang (Swelling Power )
27
3.3.6. Pembuatan Edible Film Pati Asetat
27
3.3.7. Analisa Edibel Film 28
3.4. Bagan Penelitian 30
3.4.1. Preparasi Sampel 30
3.4.2. Pembuatan Pati Asetat 31
3.4.3. Pembuatan Edible Film 32
BAB 4 HASIL DAN PEMBAHASAN
4.1. Hasil 33
4.1.1. Pati Sukun 33
4.1.2. Pembuatan Pati Asetat 34
4.1.3. Persen Asetat dan Derajat Substitusi
36
4.1.4. Penentuan Derajat Mengembang (Swelling Power ) Pati Sukun dan Pati Asetat pH 8
37
4.1.5. Uji Mekanik Edible Film Pati Sukun
37
4.1.6. Analisis WVTR Edible Film Pati Sukun dan Pati Asetat pH 8
38
4.1.7. Pengukuran Derajat mengembang Edible Film Pati Sukun dan Pati
Asetat pH 8
38
4.1.8. Analisa SEM Edible Film Pati Sukun dan Pati Asetat pH 8
39
4.2. Pembahasan 40
4.2.1. Pati Hasil Isolasi Buah Sukun 40
4.2.2. Pembuatan Pati Asetat 40
4.2.3. Penentuan Persen Asetat dan Derajat Substitusi
44 4.2.4. Analisis Kekuatan Swelling Pati
Asetat
44 4.2.5. Analisis Sifat Mekanik Edible
Film Pati Sukun dan Pati Asetat pH 8
45
4.2.6. Analisa WVTR Edible Film Pati Sukun dan Pati Asetat pH 8
46 4.2.7. Analisa Pengukuran Swelling
Edible Film Pati Sukun dan Pati Asetat pH 8
47
4.2.8. Analisa SEM Edible Film Pati Sukun dan Pati Asetat pH 8
47
BAB 5 KESIMPULAN DAN SARAN
5.1 Kesimpulan 48
5.2 Saran 48
DAFTAR PUSTAKA 49
LAMPIRAN 53
DAFTAR TABEL
Nomor Tabel
Judul Tabel Halaman
2.1 Kandungan Gizi Buah Sukun 7
2.2 Sifat Fisika Asetat Anhidrat 13
2.3 Perbandingan Sifat Mekanik Pati Cron, Kitosan Dan Film Komposit Dengan Film Sintetik Komersial
15 4.1 Hasil Penentuan Persen Asetat dan Derajat Substitusi
Pati Asetat
36 4.2 Hasil Penentuan swelling power Pati Sukun dan Pati
Asetat pH 8
37 4.3 Nilai Kuat Tarik, Kemuluran, Ketebalan Edible Film
Pati Sukun dan Pati Asetat pH 8
37 4.4 Hasil WVTR Edible Film Pati Sukun dan Pati Asetat
pH 8
38 4.5 Hasil Swelling Edible Film Pati Sukun dan Pati Asetat
pH 8
38
DAFTAR GAMBAR
Nomor Gambar
Judul Halaman
2.1 Buah Sukun 6
2.2 Struktur dari Amilosa dan Amilopektin 8
2.3 Skema Reaksi dari Asetat dengan Pati 12
2.4 Struktur Asetat Anhidrat 12
2.5 Gliserol 18
2.6 Gambaran Singkat Uji Tarik 22
2.7 Pembebanan Tarik 22
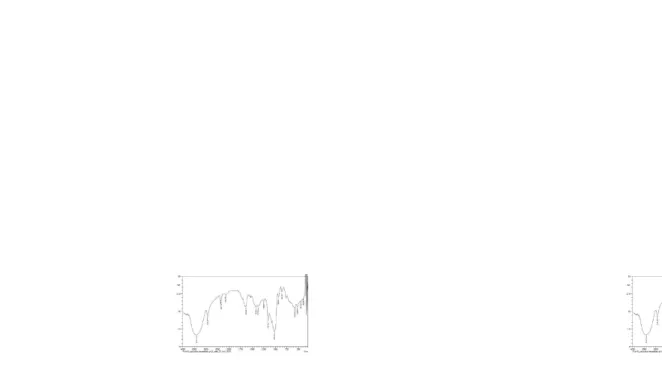
4.1 Spektrum FT-IR Pati Sukun 33
4.2 Spektrum FT-IR Pati Asetat Hasil Asetilasi pH = 6 34 4.3 Spektrum FT-IR Pati Asetat Hasil Asetilasi pH = 7 35 4.4 Spektrum FT-IR Pati Asetat Hasil Asetilasi pH = 8 35 4.5 Spektrum FT-IR Pati Asetat Hasil Asetilasi pH = 9 36
4.6 Hasil SEM Edible FilmPati Sukun 39
4.7 Hasil SEM Edible FilmPati Asetat pH 8 39
4.8 Reaksi Amilosa Asetat 42
4.9 Reaksi Amilopektin Asetat 43
DAFTAR LAMPIRAN
Nomor Lampiran
Judul Halaman
1. Perhitungan Persen Asetil dan Derajat Substitusi (DS)
53
2. Perhitungan KekuatanSwelling 54
3. Gambar Pati Sukun dan Pati Asetat 56
4. Perhitungan Kekuatan Tarik dan Elogasi Pada Edible Film Pati Sukun dan Pati Asetat pH 8
56 5. Gambar Edible FilmPati Sukun dan Pati Asetat pH 8 57 6. Hasil SEM (Scanning Electron Microscopy) Edible
Film Pati Sukun dan Pati Asetat Ph 8
58 7. Perhitungan Nlai WVTR Edible Film Pati Sukun dan
Pati Asetat pH 8
60
PENDAHULUAN
Bahan makanan pada umumnya sangat sensitif dan mudah mengalami penurunan kualitas karena faktor lingkungan, kimia, biokimia, dan mikrobiologi. Penurunan kualitas tersebut dapat dipercepat dengan adanya oksigen, air, cahaya, dan temperatur. Salah satu cara untuk mencegah atau memperlambat fenomena tersebut adalah dengan pengemasan yang tepat.
Pengemas merupakan bahan yang sangat diperlukan untuk mempertahankan kualitas suatu bahan pangan agar tetap baik, karena apabila suatu bahan pangan dibiarkan terbuka dan terinfeksi dengan lingkungan seperti adanya kontak dengan oksigen maka bahan pangan tersebut akan cepat rusak, sehingga dapat menurunkan kualitas dan umur simpan dari bahan pangan ters ebut. Umumnya jenis pengemas yang sering digunakan adalah plastik. Plastik merupakan bahan pengemas yang dapat mencemari lingkungan karena mempunyai karakter yang nonbiodegradable, selain itu plastik dapat mencemari bahan pangan yang dikemas karena adanya zat-zat tertentu yang berpotensi karsinogen yang dapat berpindah ke dalam bahan pangan yang dikemas (Khusnul, 2006). Untuk mendapatkan bahan pengemas yang memiliki karakter biodegradable kuat dan elastis sangat perlu dikembangkan untuk diteliti. Oleh karena itu pada saat ini dibutuhkan penelitian mengenai bahan pengemas yang dapat diuraikan (biodegradable) (Wahyu, 2009).
Edible film merupakan bahan kemasan yang ramah lingkungan karena sifatnya yang biodegradable dan dapat dimakan sehingga tidak mencemari lingkungan. Walaupun tidak dimaksudkan untuk menggantikan secara total kemasan dari bahan sintetik, akan tetapi keunggulan dari edible film yaitu dapat dimakan, biokompatibilitas, tidak beracun, tidak menyebabkan polusi, memiliki
sifat sebagai penghambat transfer massa (uap air, oksigen dan zat terlarut) dan harganya murah.
Komponen utama penyusun edible film ada tiga kelompok yaitu hidrokoloid, lemak dan komposit. Salah satu bahan utama yang digunakan dalam pembuatan edible film ini yaitu pati yang termasuk kelompok hidrokoloid, yang merupakan bahan yang mudah didapat, harganya murah, serta jenisnya beragam di Indonesia (Setiani, 2013).
Pati adalah salah satu sumber bahan makanan yang paling penting. Pati terdapat dalam biji-bijian, umbi-umbian, dan buah dari tanaman hijau yang berbentuk butiran kecil (granula). Penggunaan pati sebagai bahan baku industri
sangat luas diantaranya pada industri makanan, tekstil, kosmetik, dan kertas (Sembiring, 2011).
Salah satu sumber pati yang mudah tumbuh di daerah tropis adalah sukun ( Artocarpus altilis). Tanaman sukun tumbuh dari dataran rendah hingga dataran tinggi 700 m di atas permukaan laut, dengan suhu antara 21 – 33 °C, dan curah hujan 1500 – 2500 mm/tahun. Pati yang diperoleh dari sukun menghasilkan 18,5 g/100 g dengan kemurnian 98,86 % dan kandungan amilosa 27,68 % dan amilopektin 72,32 % (Rincom dan Fanny, 2004).
Modifikasi sifat pati dan teknik pengolahan pati sudah berkembang saat ini, pati alami dapat dimodifikasi sehingga mempunyai sifat-sifat yang lebih baik. Modifikasi disini dimaksudkan sebagai perubahan struktur molekul yang dapat dilakukan secara kimia, fisik maupun enzimatis. Dewasa ini metode yang banyak digunakan untuk memodifikasi pati adalah modifikasi menggunakan asam (asetilasi), enzim, oksidasi dan ikatan silang. Setiap metode modifikasi tersebut menghasilkan pati termodifikasi dengan sifat yang berbeda-beda (Koswara, 2006).
Modifikasi secara asetilasi berkerja dengan adanya distribusi gugus asetil yang menggantikan gugus – OH (hidrolsil). Modifikasi dengan asetilasi
menghasilkan produk dengan swelling power , solubility dan viskositas yang lebih tinggi. Selain itu proses modifikasi dengan asetilasi membutuhkan biaya yang lebih rendah, sehingga lebih menguntungkan apabila digunakan pada industri pangan (Artiani, 2009).
Yuliasih, dkk (2014) telah menggunakan pati sagu termodifikasi sebagai bahan starch-based plastics untuk mendapatkan edible film yang mempunyai sifat hidrofobik dan kompatibel dengan pelastik sintetik. Dengan melakukan variasi suhu 30, 35, 40 dan 45 oC dan waktu 15, 30, 45, 60, 90, 105, dan 120 menit. Kondisi proses asetilasi yang digunakan untuk membuat edible film adalah pada suhu 40oC dan lama waktu 75 menit.
Arianti, dkk (2009) telah melakukan modifikasi cassava starch dengan proses asetilasi asam asetat untuk menghasilkan produk pangan yang memiliki peningkatan swelling power dan peningkatan persen solubility dengan melakukan variasi waktu dari 30, 60, 90, 120 menit dan pH 6, 7, 8, 9. Kondisi reaksi asetilasi yang menghasilkan starch asetat paling baik adalah pada waktu 90 menit pH 8 dan suhu 45 oC. Dengan hasil swelling power 16,90 dan persen solubility 34,50 %
Pudjiastuti, dkk (2014) telah melakukan pembuatan plastik layak santap (edible plastic) dari tapioka termodifikasi yang menghasilkan edible film ketebalan 41,72 MPa, nilai kuat tarik antara 27,01 Kgf/cm2 - 217,7 Kgf/cm2, kemuluran antara 2,55% - 62,89 % dan laju transmisi uap air antara 590,37 g/m2/24 jam sampai dengan 824,25 g/m2/24 jam.
Berdasarkan latar belakang di atas, peneliti tertarik untuk membuat edible film dari pati sukun ( Artocarpus altilis) termodifikasi dari proses asetilasi
1.2 Permasalahan
1. Bagaimana pH reaksi asetilasi pati sukun ( Artocarpus altilis) dari asetat anhidrat untuk menghasilkan pati asetat dengan derajat substitusi yang paling tinggi?
2. Bagaimana karakteristik dari edilble film pati sukun dan pati asetat meliputi ketebalan, kuat tarik/kemuluran, uji SEM, uji WVTR dan uji swelling ?
1.3 Pembatasan Masalah
Adapun pembatasan masalah dalam penelitian ini adalah sebagai sebagai berikut :
1. Perolahan sampel dibatasi hanya pati dari buah sukun dari Kecamatan Medan Denai.
2. Parameter yang dianalisa pada pati asetat yang dihasilkan dari proses asetilasi adalah analisa FT-IR dan derajat substitusi.
3. Parameter yang dianalisa pada edible film adalah sifat mekanik (ketebalan, kemuluran. keregangan) dan sifat fisik SEM (Scanning Electron Microscope), Uji WVTR (Water Vapour Transmission Rate) dan swelling .
1.4 Tujuan Penelitian
1. Untuk menentukan pH reaksi asetilasi pati sukun ( Artocarpus altilis) dari asetat anhidrat untuk menghasilkan pati asetat dengan derajat substitusi yang paling tinggi
2. Untuk menentukan karakterisasi dari edible film pati suku dan pati asetat yang meliputi ketebalan, kuat tarik/kemuluran, uji SEM, uji WVTR dan uji swelling
1.5 Manfaat Penelitian
Hasil penelitian ini diharapkan dapat dijadikan sumber informasi untuk mengetahui modifikasi pati buah sukun ( Artocorpus altilis) dengan proses asetilasi dengan menggunakan asetat anhidrat sehingga menghasilkan pati asetat dan menghasilkan edible film sebagai bahan pengemas makanan yang bersifat mudah terdegradasi secara alami serta ramah lingkungan.
1.6 Lokasi Penelitian
Proses asetilasi, pembuatan edible film, Uji sifat mengembang dan Uji WVTR (Water Vapour Transmission Rate) dilakukan Penelitian dilakukan di Laboratorium Kimia Fisika PTKI-Medan. Uji kuat tarik, % Kemuluran dan pengukuran ketebalan dilakukan di laboratorium penelitian Teknik Kimia
Fakultas Teknik USU. Uji FT-IR ( Fourier Transform Infra Red ) dilakukan di Laboratorium Kimia Organik FMIPA UGM. Uji SEM (Scanning Electron Microscopy) di Pusat Laboratorium Geologi ITB.
1.7 Metodologi Penelitian
Penelitian ini dilakukan melalui eksperimen laboratorium meliputi isolasi pati dari buah sukun, pembuatan pati asetat dari pati sukun dengan menambahkan asetat anhidrat dengan variasi pH 6, 7, 8 dan 9 pada suhu 45 oC selama 60 menit kemudian di uji derajat substitusi dan FT-IR. Pembuatan edible film dari pati sukun dan pati asetat pH 8 dengan penambahan plasticizer gliserol dan diaduk hingga homogen, dituangkan ke plat akrilik dengan ukuran 10 x 10 cm kemudian di keringkan di oven pada suhu 450C selama 2 hari, kemudian dianalisis : Kuat tarik, Persen kemuluran, Ketebalan, untuk mengetahui sifat mekaniknya. Scanning Electron Miroscope (SEM) untuk mengetahui morfologi permukaan Edible film, Water Vapour Transmition Rate (WVTR), dan Uji sifat derajat
TINJAUAN PUSTAKA
2.1. Sukun (
Ar tocarpus altilis)
Tanaman sukun ( Artocarpus altilis Park.) dapat digolongkan menjadi sukun yang berbiji disebut breadnut dan yang tanpa biji disebut breadfruit . Sukun tergolong tanaman tropik sejati, tumbuh paling baik di dataran rendah yang panas. Tanaman ini tumbuh baik di daerah basah, tetapi juga dapat tumbuh di daerah yang sangat kering asalkan ada air tanah dan aerasi tanah yang cukup. Sukun bahkan dapat tumbuh baik di pulau karang dan di pantai. Di musim kering, di saat tanaman lain tidak dapat atau merosot produksinya, justru sukun dapat tumbuh dan berbuah dengan lebat (Koswara, 2006). Gambar buah sukun dapat dilihat pada gambar 2.1.
Menurut Hasibuan (2013), taksonomi tanaman sukun sebagai berikut : Kingdom : Plantae Divisi : Spermatophyta Subdivisi : Magnoliophyta Kelas : Magnoliopsida Ordo : Urticales Famili : Moraceae Genus : Artocarpus
Species : Artocarpus altilisPark.
Buah sukun berbentuk bulat atau agak lonjong dengan diameter kurang lebih 25 cm. Warna kulit buah hijau muda sampai kekuning-kuningan. Ketebalan kulit antara 1-2 mm. Buah muda berkulit kasar dan buah tua berkulit halus. Daging buah berwarna putih agak krem, teksturnya kompak dan berserat halus. Rasanya agak manis dan memiliki aroma yang spesifik. Tangkai buah sekitar 5 cm. Berat buah sukun dapat mencapat 1 kg per buah (Widowati, 2003).
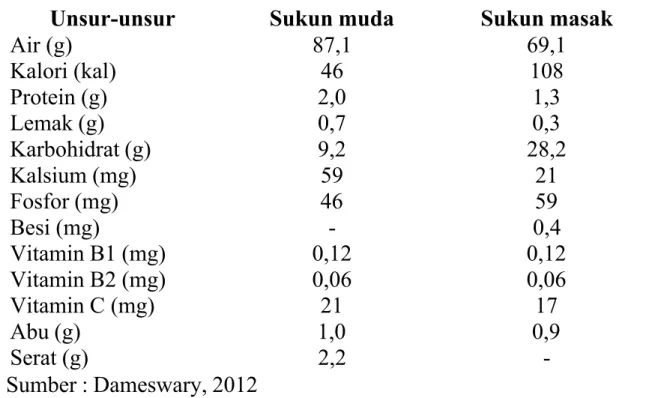
Kandungan zat gizi pada buah sukun tergantung dari umur buah sukun atau tingkat kematangan buah sukun. Kandungan gizi buah sukun muda berbeda dengan kandungan gizi buah sukun yang sudah masak. Menurut Dameswary, (2012) Komposisi kimia buah sukun yang muda dan tua atau masak dapat dilihat pada Tabel 2.1
Tabel 2.1 Komposisi kimia dan zat gizi buah sukun per 100 gram buah
Unsur-unsur Sukun muda Sukun masak
Air (g) 87,1 69,1 Kalori (kal) 46 108 Protein (g) 2,0 1,3 Lemak (g) 0,7 0,3 Karbohidrat (g) 9,2 28,2 Kalsium (mg) 59 21 Fosfor (mg) 46 59 Besi (mg) - 0,4 Vitamin B1 (mg) 0,12 0,12 Vitamin B2 (mg) 0,06 0,06 Vitamin C (mg) 21 17 Abu (g) 1,0 0,9 Serat (g) 2,2 -Sumber : Dameswary, 2012 2.2. Pati
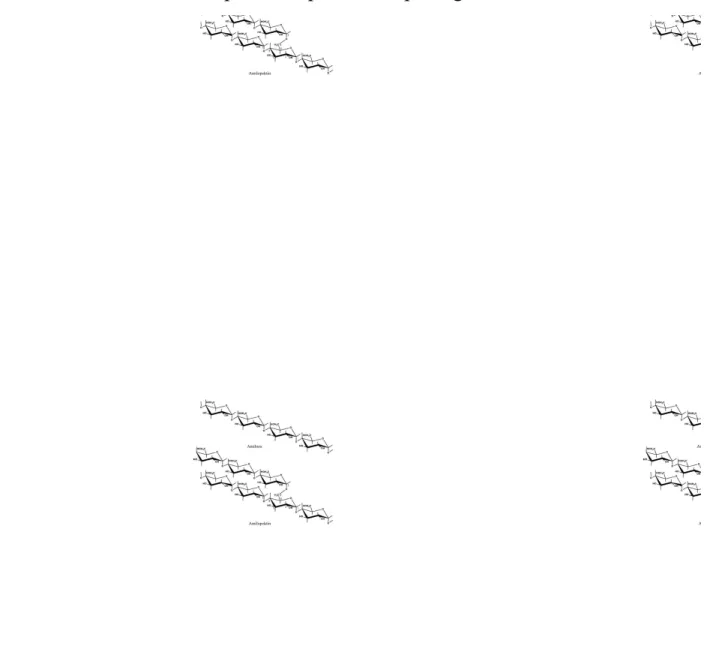
Pati adalah nama umum yang ditunjukan untuk granular atau tepung, tidak berbau, tidak berasa, merupakan karbohidrat kompleks (C6H10O5)n, terdapat pada biji- bijian tanaman dan umbi-umbian. Pati merupakan polimer dari glukosa. Glukosa terbentuk pada tanaman sebagai hasil fotosentesis. Pati tersusun atas dua komponen yaitu amilosa, merupakan polisakarida rantai lurus, dan amilopektin merupakan polisakarida rantai bercabang. Bagian yang larut dalam air disebut
amilosa, bila ditambah iodium akan memberikan warna biru. Bagian yang lain yaitu yang tak larut dalam air, disebut amilopektin yang mempunyai berat molekul antara 70.000-106, dengan iodium memberikan warna ungu hingga merah. Kandungan amilosa sekitar 20-30 % dan amilopektin 70-80 % (Polnaya, 2006). Pati memiliki beberapa ciri-cirinya diantaranya:
1. Rasa tidak manis
2. Terdapat dalam biji, buah dan umbi-umbian dari tanaman 3. Berfungsi sebagai sumber energi di dalam tubuh
4. Memiliki bentuk dan ukuran granula yang berbeda-beda 5. Sukar atau tidak larut dalam air dingin
6. Dalam air panas dapat membentuk pasta dan gel (Sembiring, 2011).
Struktur amilosa dan amilopektin dapat dilihat pada gambar 2.2
Bila pati mentah dimasukkan kedalam air dingin, granula patinya akan menyerap air dan membengkak. Namun demikian jumlah air yang terserap dan pembengkakannya terbatas. Air yang terserap tersebut hanya dapat mencapai kadar 30 % . Peningkatan volume granula pati yang terjadi didalam air pada suhu antara 55 0C sampai 65 0C merupakan pembengkakan pati yang sesungguhnya, dan setelah pembengkakan ini granula pati dapat kembali pada kondisi semula. Perubahan tersebut disebut gelatinisasi. Suhu pada saat granula pati pecah disebut suhu gelatinasi yang dapat dilakukan dengan penambahan air panas.
Pati yang telah mengalami gelatinasi dapat dikeringkan, tetapi molekul molekul tersebut tidak dpat kembali lagi ke sifat-sifatnya sebelum gelatinasi. Bahan yang telah kering tersebut masih mampu menyerap air dalam jumlah yang besar. Suhu gelatinasi tergantung juga pada konsentrasi pati. Makin kental larutan, suhu tersebut makin lambat tercapai, sampai suhu tertentu kekentalan tidak bertambah, bahkan kadang-kadang turun. Suhu gelatinasi berbeda-beda bagi tiap jenis pati dan merupakan suatu kisaran. Dengan viskosimeter suhu gelatinasi dapat ditentukan, misalnya pada jagung 62-70 0C, beras 68-78 0C, gandum 54,5-640C (Winarno, 2002).
2.3. Modifikasi Pati
Pati termodifikasi adalah pati yang gugus hidroksilnya telah diubah lewat suatu reaksi kimia (esterifikasi, eterifikasi atau oksidasi) atau dengan menggangu struktur asalnya. Pati termodifikasi dapat diperoleh dengan metode fisika, kimia maupun enzimatis.
Pati yang telah termodifikasi akan mengalami perubahan sifat yang dapat disesuaikan untuk keperluan-keperluan tertentu. Sifat-sifat yang diinginkan adalah pati yang memiliki viskositas yang stabil pada suhu tinggi dan rendah, daya tahan
terhadap “ sharing ” mekanis yang baik serta daya pengental yang tahan terhadap
kondisi asam dan suhu sterilisasi. Sifat pati termodifikasi yang dihasilkan dipengaruhi oleh pH, suhu inkubasi dan konsentrasi pati yang digunakan selama proses modifikasi (Koswara, 2009).
Ada beberapa teknik untuk modifikasi pati,yaitu : a. Metode Fisika
Modifikasi fisik dari pati pada dasarnya mengubah sturuktu granula dan mengubah pati biasa menjadi pati yang larut dalam air dingin atau kristal mikro pati. Beberapa metode yang telah dikembangkan saat ini yaitu Heat-moisture
treatment (HMT), penguatan (terhadap air), retrogradasi, pembekuan, ultra high pressure treatment, glow discharge plasma treatment, Osmotic-Pressure
Treatment, hambatan termal dan gelatinisasi (Neelam,et al. 2012).
b. Metode Kimia
Metode kimia melibatkan gugus fungsi awal pada molekul pati, menghasilkan perubahan secara nyata sifat fisiko-kimianya. Contoh dari teknik ini yaitu,
eterifikasi, esterifikasi, ikat silang, penambahan asam, oksidasi dan dwi modifikasi (Neelam, et al . 2012).
c. Metode Enzimatis
Metode ini meliputi tentang suspensi pati menjadi sejumlah dari enzim-enzim utam termasuk hidrolisis enzim yang cenderung untuk menghasilkan turunan fungsional yang besar. Beberapa enzim yang telah diteliti yaitu, amilomaltase, siklomaltodekstrinase, siklomaltodekstrin dan glukanosiltransferase (Neelam, et al. 2012).
d. Metode Modifikasi Genetika
Teknik – teknik pada metode ini meliputi teknologi transgenik bahwa target enzim yang terlibat dalam biosintesis pati demikian hakikat dari keuntungan dari bahaya kimia lingkungan paska panen dan modifikasi enzimatis. Beberapa metode yang telah diteliti yaitu pati bebas amilosa, pati tinggi amilosa dan altered amilopektin structure(Neelam,et al. 2012).
2.4. Pati Asetat
Metode modifikasi pati secara asetilasi dengan substitusi (degree of substitution =DS) yang rendah telah digunakan secara luas oleh industri makanan selama
bertahun-tahun. Hal ini disebabkan oleh keunggulan sifat fisik-kimia yang dimiliki oleh pati terasetilasi seperti suhu gelatinisasi, swelling power , solubility, dan tingkat kejernihan pasta yang tinggi, serta memiliki stabilitas penyimpanan dan pemasakan yang lebih baik jika dibandingkan dengan pati asalnya. Selain itu, kualitas produk yang dihasilkan dari pati terasetilasi lebih stabil dan tahan terhadap retrogradasi. Sifat fisik-kima pada pati yang terasetilasi ini dipengaruhi oleh jumlah distribusi gugus asetil yang menggantikan gugus hidroksil (OH-) pada pati. Metode asetilasi merupakan metode yang sangat penting untuk
memodifikasi karakteristik pati karena metode ini dapat memberikan efek pengentalan pada berbagai makanan, reagen yang biasa digunakan pada metode
asetilasi adalah vinil asetat, asam asetat dan asam anhidrat (Teja, 2008).
Esterifikasi adalah suatu reaksi ionik yang merupakan gabungan dari reaksi adisi dan reaksi penataan ulang dieliminasi (Davidek, 1990). Esterifikasi juga dapat didefenisikan sebagai reaksi antara asam karboksilat dan alkohol
(Gandhi, 1997). Esterifikasi dapat dilakukan dengan menggunakan katalis enzim (lipase) dan asam anorganik (asam sulfat dan asam klorida), dengan berbagai variasi alkohol biasanya metanol, etanol, 1-propanol, 1-butanol, amyl alkohol, dan lain-lain (Ozgulsun, 2008). Asam anorganik yang digunakan sebagai katalis akan menyebabkan asam karboksilat mengalami konjugasi sehingga asam konjugat dari asam karboksilat tersebutlah yang akan berperan sebagai substrat.
Cara lain dalam pembentukan ester adalah dengan melewatkan HCl ke dalam campuran reaksi tersebut dan direfluks. Cara ini dikenal dengan nama metode Fischer-Spieser . Esterifikasi tanpa katalis dapat juga dilakukan dengan satu molekul asam karboksilat dan satu pereaksi secara berlebih. Pertambahan hasil juga dipengaruhi oleh dehidrasi yang artinya menarik air terbentuk sebagai hasil samping reaksi.
Reaksi antara pati dengan asetat anhidrida akan berlangsung mengikuti mekanisme pada gambar 2.3. Selain reaksi utama tersebut, reaksi esterifikasi pati sagu dengan asetat anhidrat juga akan melibatkan reaksi samping, dimana asetat
anhidrida dapat terhidrolisis menjadi asam asetat. Reaksi lengkap dapat dilihat pada gambar berikut ini
Gambar 2.3 Mekanisme Reaksi Asetilasi Pati Dengan Asetat Anhidrida Dan Natrium Asetat (Naoac) Sebagai Katalis (Muljana, 2012)
2.5. Asetat Anhidrat
Asetat anhidrat (CH3CO)2O merupakan larutan aktif, tidak berwarna, serta memiliki bau yang tajam. Kapasitas produksi Amerika untuk produk asetat anhidrat ini cukup besar, yaitu lebih dari 900.000 ton per tahun. Asetat anhidrat merupakan suatu senyawa yang memiliki kegunaan yang sangat bervariasi. Asetat anhidrat digunakan dalam pembuatan cellulose asetate, serat asetat, obat-obatan, aspirin, dan berperan sebagai pelarut dalam penyiapan senyawa organik (Stembayo, 2008). Asetat anhidrat memiliki struktur seperti pada gambar 2.4.
Gambar 2.4 Struktur Asetat Anhidrat
Asetat anhidrat memiliki berbagai macam kegunaan antara lain sebagai fungisida dan bakterisida, pelarut senyawa organik, berperan dalam proses asetilasi, pembuatan aspirin, dan dapat digunakan untuk membuat acetylmorphine.
Asam asetat anhidrat paling banyak digunakan dalam industri selulosa asetat untuk menghasilkan serat asetat, plastik serat kain dan lapisan. Adapun sifat kimia asam asetat anhidrat yaitu :
a. Mudah menguap dan mudah terbakar
b. Larut dalam air membentuk asam asetat, dengan alcohol membentuk etil asetat, larut dalam kloroform dan eter
c. Asam anhidrat merupakan cairan yang sangat reaktif
d. Menyebabkan iritasi dan matinya jaringan, hindari kontak dengan kulit dan mata
e. Asetat anhidrat digunakan sebagai pelarut.
Adapun sifat fisika asam asetat anhidrat dapat dilihat di tabel 2.2
Tabel 2.2 Sifat Fisika Asetat Anhidrat
Rumus Molekul (CH3CO)2O
Bobot molekul 102,09 gr/mol
Titik beku -73 oC
Titik didih (760 mmHg) 139,06 oC
Densitas pada 20 oC 1,08 gr/ml
Viskositas pada 25 oC 0,843 mPa.s
(http://fadillahahmaddedi.blogspot.co.id/2015/04/aspirin.html)
2.6.
E dible F ilm
Edible film merupakan istilah ilmiah bagi kemasan yang bisa dimakan. Saat ini gencar dikembangkan bersamaan dengan kemasan yang gampang terurai atau yang diberi nama biodegradable film. Edible film sudah pasti tergolong biodegradable film, tetapi biodegradable belum tentu edible film. Edible film adalah suatu lapisan tipis yang terbuat dari bahan yang dapat dimakan, dibentuk melapisi makanan dengan cara pembungkusan dan pencelupan. Batasan makna kemasan bisa dimakan bergantung pada proses peracikan, proses pengemasan dan segala modifikasi perlakuan yang terkait. Jika bahan baku dan bahan racikannya adalah bahan yang bisa dimakan dan hanya perubahan struktur bahan baku yang
terjadi selama proses pemasakan, perubahan pH atau modifikasi enzimatis, maka kemasan tersebut digolongkan kemasan bisa dimakan (Bardant dan Dewi, 2007).
Baldwin (1994) dan Wong et al . (1994) mengatakan bahwa secara teoritis bahanedible film harus memiliki sifat-sifat seperti:
1. Menahan kehilangan air bahan pangan.
2. Memiliki permeabilitas selektif terhadap gas tertentu.
3. Mengendalikan perpindahan padatan terlarut untuk mempertahankan kualitas
bahan pangan.
4. Menjadi pembawa bahan aditif seperti pewarna, pengawet, dan penambah aroma yang dapat memperbaiki mutu bahan pangan.
Film sebagai pengemasan (edible packaging ) pada dasarnya dibagi atas tiga bentuk pengemasan yaitu:
1. Edible film merupakan bahan pengemas yang telah dibentuk terlebih dahulu berupa lapisan tipis ( film) sebelum digunakan untuk mengemas produk pangan.
2. Edible coating berupa pengemas yang dibentuk langsung pada produk dan bahan pangan.
3. Enkapsulasi yaitu suatu aplikasi yang ditujukan untuk membawa
komponen-komponen bahan tambahan makanan tertentu untuk meningkatkan penanganan terhadap suatu produk pangan sesuai dengan yang diinginkan.
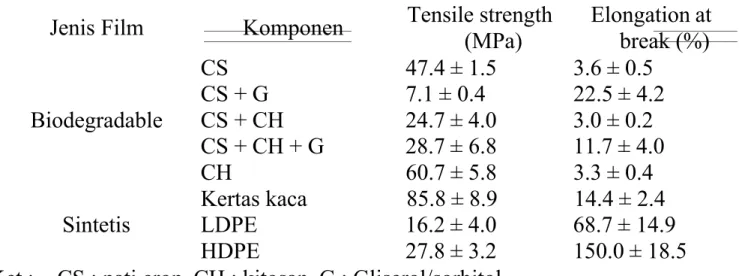
Menurut Embuscado (2009), sifat mekanik film tergantung pada interaksi aditif-matrix, dan juga sangat dipengaruhi oleh fisik, kimia dan suhu kondisi, yang mempengaruhi stabilitas film dan fleksibilitas. kinerja mekanik dari film biasanya ditandai dengan persen perpanjangan putus, kekuatan tarik dan modulus elastisitas. Tabel 2.3. membandingkan sifat mekanik ditentukan untuk kedua film biodegradable dan sintetis di bawah kondisi pengujian yang sama yaitu
Tabel 2.3. Perbandingan Sifat Mekanik Pati Cron, Kitosan Dan Film Komposit Dengan Film Sintetik Komersial
Jenis Film Komponen Tensile strength (MPa) Elongation at break (%) Biodegradable CS 47.4 ± 1.5 3.6 ± 0.5 CS + G 7.1 ± 0.4 22.5 ± 4.2 CS + CH 24.7 ± 4.0 3.0 ± 0.2 CS + CH + G 28.7 ± 6.8 11.7 ± 4.0 CH 60.7 ± 5.8 3.3 ± 0.4 Sintetis Kertas kaca 85.8 ± 8.9 14.4 ± 2.4 LDPE 16.2 ± 4.0 68.7 ± 14.9 HDPE 27.8 ± 3.2 150.0 ± 18.5
Ket : CS : pati cron, CH : kitosan, G : Gliserol/sorbitol
2.6.1 Pembentukan
E dible F ilm
Faktor-faktor yang berpengaruh terhadap pembentukan edible film antara lain: a. Suhu
Perlakuan panas diperlukan untuk membentuk pati tergelatinasi sehingga terbentuk pasta pati yang merupakan bentuk awal edible film. Suhu pemanasan pati akan menentukan sifat mekanik edible film yang terbentuk. Suhu pemanasan akan menentukan tingkat gelatinisasi yang terjadi yang pada akhirnya menentukan sifat fisik dari pasta yang terbentuk.
b. Konsentrasi pati
Konsentrasi pati memberikan kontribusi terhadap kadar amilosa dalam laruta n pati sehingga berpengaruh terhadap sifat pasta yang dihasilkan.
c.
Plasticizer
dan bahan aditif lainKonsentrasi plasticizer dan bahan aditif lain yang ditambahkan ke dalam formula film akan berpengaruh terhadap sifat film yang terbentuk bahan-bahan tersebut
2.6.2 Sifat Fisiko-Kimia-Biologi
E dible F ilm
a. Ketebalan
Film
Menurut McHugh dan Krochta (1994) ketebalan juga sangat mempengaruhi sifat fisik dan mekanik edible film, seperti tensile strength, elongation, dan water vapor transmission rate (WVTR). Faktor yang dapat mempengaruhi ketebalan edible film adalah konsentrasi padatan terlarut pada larutan pembentuk film dan ukuran pelat pencetak. Semakin tinggi konsentrasi padatan terlarut, maka ketebalan film akan meningkat. Sebagai kemasan, semakin tebal edible film maka kemampuan penahanannya semakin besar, sehingga umur simpan produk akan semakin panjang.
b.
Tensile strength
(MPa) / Kekuatan Renggang Putus (%)Tensile Strength adalah ukuran untuk kekuatan film secara spesifik, merupakan tarikan maksimum yang dapat dicapai sampai film tetap bertahan sebelum putus/sobek (Krochta and Mulder-johnston, 1997). Pengukuran ini untuk mengetahui besarnya gaya yang diperlukan untuk mencapai tarikan maksimum pada setiap luas area film. Sifat tensile strength tergantung pada konsentrasi dan jenis bahan penyusunedible filmterutama sifat kohesi struktural.
c.
E longasi
/ KemuluranXu et al . (2005) menyatakan bahwa film dengan bahan dasar pati bersifat rapuh karena adanya amilosa, sehingga makin tinggi konsentrasi pati akan menurunkan fleksibilitas film yang dihasilkan. Menurut Chick dan Hernandez (2002) bahwa meningkatnya kadar air akan menurunkan tensile strength film yang tidak menggunakan wax, tetapi dengan adanya wax akan meningkatkan tensile strength dan menurunkan elongation. Sedangkan menurut Cheng et al . (2006) bahwa peningkatan konsentrasi gliserol dan sorbitol tidak memberi pengaruh secara signifikan terhadap tensile strength film, tetapi meningkatkan flexibilitas dan ekstensibilitas film.
d. Laju Transmisi Uap Air (WVTR)
Laju transmisi uap air (WVTR) adalah jumlah uap air yang melalui suatu permukaan persatuan luas atau slope jumlah uap air dibagi luas area. Edible film
dengan bahan dasar polisakarida umumnya sifat barrier terhadap uap airnya rendah. Film hidrofilik seringkali memperlihatkan hubungan-hubungan positif antara ketebalan dan permeabilitas uap air. Studi-studi sebelumnya sudah menandai hubungan-hubungan yang serupa antara ketebalan film dan sifat permeabilitas di dalam sistem film yang hidrofilik (Liu dan Han, 2005). Nilai laju transmisi uap air suatu bahan dipengaruhi oleh struktur bahan pembentuk dan konsentrasi plasticizer . Penambahan plasticizer seperti gliserol akan meningkatkan permeabilitas film terhadap uap air karena gliserol bersifat hidrofilik (Gontard et al. 1993).
e. Daya larut (%)
Daya larut merupakan salah satu sifat fisik edible film yang menunjukkan persentase berat kering terlarut setelah dicelupkan dalam air selama 24 jam
(Gontard et al. 1993). Daya larut film sangat ditentukan oleh sumber bahan dasar pembuatan film. Edible film berbahan dasar pati tingkat kelarutannya dipengaruhi oleh ikatan gugus hidroksi pati. Makin lemah ikatan gugus hidroksil pati, makin tinggi kelarutan film. Edible film dengan daya larut yang tinggi menunjukkan film tersebut mudah dikonsumsi.
2.6.3 Plasticizer Gliserol
Plasticizer adalah salah satu komponen bahan dasar pembuatan edible film yang berfungsi untuk mengatasi sifat rapuh lapisan film. Menurut Gulbert dan Biquet (1996) ada beberapa jenis plastisizer yang sering digunakan dalam pembuatan edible film yaitu:
a) Mono, di-, dan oligosakarida;
b) Poliol (seperti gliserol dan turunannya, polyetilen glikol, sorbitol), dan
c) Lipid dan turunannya (asam lemak, monogliserida dan esternya, asetogliserida, pospholipida dan emulsifierlain).
Edible film membutuhkan plasticizer dengan berat molekul rendah untuk meningkatkan fleksibilitas dan ketahanannya, dengan cara menginterupsi interaksi rantai polimer dan menurunkan suhu Transition Glass (Brody, 2005). Menurut Winarno (1992), Gliserol adalah senyawa alkohol polihidrat (polyol) dengan 3 buah gugus hidroksil dalam satu molekul atau disebut alkohol trivalent.
Strukturnya dapat dilihat pada gambar 2.5.
Gambar 2.5 Gliserol
Rumus kimia gliserol adalah C3H8O3, Berat molekul gliserol 92,10 massa jenisnya 1,23 g/cm3 dan titik didihnya 204 0C. Gliserol mempunyai sifat mudah larut air, meningkatkan viskositas larutan, mengikat air dan menurunkan Aw (Lindsay, 1985). Gliserol merupakan salah satu plasticizer yang banyak digunakan karena cukup efektif mengurangi ikatan hidrogen internal sehingga akan meningkatkan jarak intermolekuler. Secara teoritis plasticizer dapat menurunkan gaya internal diantara rantai polimer, sehingga akan menurunkan tingkat kegetasan dan meningkatkan permeabilitas terhadap uap air (Gontard et al . 1993). Rodriguez et al . (2006) menambahkan bahwa gliserol merupakan plasticizer yang bersifat hidrofilik, sehingga cocok untuk bahan pembentuk film yang bersifat hidrofilik seperti pati. Ia dapat meningkatkan sorpsi molekul polar seperti air. Peran gliserol sebagai plasticizer dan konsentrasinya meningkatkan fleksibilitas film (Gontard et al . 1993; Mali et al. 2005; Bertuzi et al . 2007). Molekul plasticizer akan mengganggu kekompakan pati, menurunkan interaksi intermolekuler dan meningkatkan mobilitas polimer. Selanjutnya mengakibatkan peningkatan elongation dan penurunan tensile strength seiring dengan peningkatan konsentrasi gliserol. Penurunan interaksi intermolekuler dan peningkatan mobilitas molekul akan memfasilitasi migrasi molekul uap air
(Rodriguez et al . 2006).
OH HO
OH Gliserol
2.6.4. Edible Film dari Pati Alami dan Pati Termodifikasi
Pati alami seperti tapioka, pati jagung, sagu dan pati-pati lainnya mempunyai beberapa kendala jika dipakai sebagai bahan baku dalam industry pangan maupu non pangan. Jika dimasak pati membutuhkan waktu yang lama, juga pasta yang terbentuk berbentuk keras dan tidak bening. Kendala-kendala tersebut menyebabkan pati alami terbatas penggunaannya dalam industry. Pati alami dapat dibuat menjadi pati termodifikasi (Artiani, 2009). Menurut Yuliasih (2014), Pati sagu dapat diaplikasikan sebagai bahan baku industri, baik pangan maupun non pangan. Salah satu aplikasinya adalah sebagai bahan starch-based plastics.
Potensi penggunaan pati sebagai bahan bioplastik berkisar 85-90% dari pasar bioplastik yang ada. Karakteristik termoplastik pati dapat ditingkatkan dengan melakukan modifikasi pati. Modifikasi pati secara esterifikasi dilakukan untuk meningkatkan karakteristik termoplastik pati, seperti sifat hidrofobik dan kristalinitas. Asetilasi merupakan salah satu modifikasi pati secara esterifikasi. Asetilasi terhadap pati dan amilopektin akan membentuk film yang lemah dan patah, sedangkan hasil pengujian terhadap film amilosa asetat menunjukkan sifat
lebih fleksibel dan kuat. Untuk membentuk film dan gel yang kuat, digunakan pati dengan kandungan amilosa yang tinggi.
2.7. Karakterisasi
2.7.1
F ourier Transform I nfrared
(FT-IR)Spektrofotometri infra-merah adalah sangat penting dalam kimia modern, terutama dalam bidang kimia organik. Ia merupakan alat rutin dalam penemuan gugus fungsional, pengenalan senyawa, dan analisa campuran. Kebanyakan gugus, seperti CH, O-H, C=N, dan C=N, menyebabkan pita absorpsi infra-merah, yang berbeda hanya sedikit dari satu molekul ke yang lain tergantung pada substituen yang lain (Day dan Underwood,1990).
Serapan radiasi inframerah oleh suatu molekul terjadi karena interaksi vibrasi ikatan kimia yang menyebabkan perubahan polarisabilitas dengan medan listrik gelombang elektromagnetik (Wirjosentono, 1987). Terdapat dua macam getaran molekul, yaitu getaran ulur dan getaran tekuk. Getaran ulur adalah suatu
gerakan berirama di sepanjang sumbu ikatan sehingga jarak antar atom bertambah atau berkurang. Getaran tekuk dapat terjadi karena perubahan sudut-sudut ikatan antara ikatan-ikatan pada sebuah atom, atau karena gerakan sebuah gugusan. Contohnya liukan (twisting ), goyangan (rocking ), dan getaran punter yang menyangkut perubahan sudut-sudut ikatan dengan acuan seperangkat koordinat yang disusun arbiter dalam molekul. Hanya getaran yang menghasilkan perubahan momen dwikutub secara berirama saja yang teramati di dalam infra merah (Hartomo, 1986)
Pancaran infra-merah pada umumnya mengacu pada bagian spektrum elektromagnet yang terletak di antara daerah tampak dan daerah gelombang mikro. Bagi kimiawan organik, sebagian besar kegunaannya terbatas di antara 4000 cm-1 dan 666 cm-1 (2,5 – 15,0 µm). Akhir-akhir ini muncul perhatian pada daerah infra-merah dekat, 14.290 – 4000 cm-1 (0,7 – 2,5 µm) dan daerah infra-merah jauh, 700 - 200 cm-1 (14,3 - 50 µm) (Silverstein, dkk., 1986). Spektrofotometri infra-merah juga digunakan untuk penentuan struktur, khususnya senyawa organik dan juga untuk analisis kuantitatif, seperti analisa kuantitatif pencemaran udara, misalnya karbon monoksida dalam udara dengan teknik non-dispersive (Khopkar, 2003).
2.7.2
Swelling power
Daya kembang pati atau swelling power didefinisikan sebagai pertambahan volume dan berat maksimum yang dialami pati dalam air (Balagopalan, et al., 1988). Swelling power terjadi karena adanya ikatan non-kovalen antara molekul-molekul pati. Bila pati dimasukkan ke dalam air dingin, granula pati akan menyerap air dan membengkak. Namun demikian, jumlah air yang terserap dan pembengkakannya terbatas hanya mencapai 30% (Winarno, 2002).
Swelling power dipengaruhi oleh kemampuan molekul pati untuk mengikat air melalui pembentukan ikatan hidrogen. Setelah gelatinisasi iktatan hidrogen antara molekul pati terputus dan digantikan oleh ikatan hidrogen dengan air. Sehingga pati dalam tergelatinisasi dan granula-granula pati yang
mengembang secara maksimal. Proses mengembangnya granula pati ini disebabkan banyaknya air yang terserap kedalam tiap granula pati dan granula pati yang mengembang tersebut mengakibatkan swelling power menjadi meningkat (Herawati, 2010).
Faktor-faktor seperti rasio amilosa-amilopektin, distribusi berat molekul dan panjang rantai, serta derajat percabangan dan konformasinya menentukan
swelling power dan kelarutan (Moorthy, 2004). Swelling merupakan sifat yang dipengaruhi oleh amilopektin. Proporsi yang tinggi pada rantai cabang amilopektin memiliki kontribusi dalam peningkatan nilai swelling. Selain itu, terdapat korelasi yang negatif antara swelling power dengan kadar amilosa,
swelling power menurun seiring dengan peningkatan kadar amilosa ( Li dan Yeh, 2001).
2.7.3
Scanning E lectron Microscopy
(SEM)SEM adalah alat yang dapat membentuk bayangan permukaan spesimen secara makroskopik. Berkas elektron dengan diameter 5-10 nm diarahkan pada spesimen interaksi berkas elektron dengan spesimen menghasilkan beberapa fenomena yaitu hamburan balik berkas elektron, sinar x, elektron sekunder, absorbsi elektron.
Teknik SEM pada hakikatnya merupakan pemeriksaan dan analisa permukaan. Data atau tampilan yang diperoleh adalah data dari permukaan atau
dari lapisan yang tebalnya sekitar 20 µm dari permukaan yang diperoleh merupakan gambar tofografi dengan segala tonjolan, lekukan, dan lubang permukaan (Wirjosentono, 1996).
2.7.4 Kuat Tarik
Uji tarik mungkin adalah cara pengujian bahan yang paling mendasar. Pengujian ini sangat sederhana, tidak mahal dan sudah mengalami standarisasi di seluruh dunia, misalnya di Amerika dengan ASTM E8 dan Jepang dengan JIS 2241. Dengan menarik suatu bahan kita akan segera mengetahui bagaimana bahan tersebut bereaksi terhadap tenaga tarikan dan mengetahui sejauh mana material itu bertambah panjang. Alat eksperimen untuk uji tarik ini harus memiliki
cengkeraman (grip) yang kuat dan kekakuan yang tinggi (highly stiff). Banyak hal yang dapat kita pelajari dari hasil uji tarik. Bila kita terus menarik suatu bahan sampai putus, kita akan mendapatkan profil tarikan yang lengkap yang berupa kurva seperti digambarkan pada gambar. 2.6
Gambar 2.6 Gambaran Singkat Uji Tarik
Kurva ini menunjukkan hubungan antara gaya tarikan dengan perubahan panjang. Profil ini sangat diperlukan dalam desain yang memakai bahan tersebut..
Proses pengujian tarik mempunyai tujuan utama untuk mengetahui kekuatan tarik bahan uji. Bahan uji adalah bahan yang akan digunakan sebagaikonstruksi, agar
siap menerima pembebanan dalam bentuk tarikan seperti gambar 2.7. Pembebanan tarik adalah pembebanan yang diberikan pada benda dengan memberikan gaya yang berlawanan pada benda dengan arah menjauh dari titik tengah atau dengan memberikan gaya tarik pada salah satu ujung benda dan ujung benda yang lain diikat.
Gambar 2.7 Pembebanan Tarik
Penarikan gaya terhadap bahan akan mengakibatkan terjadinya perubahan bentuk (deformasi) bahan tersebut. Hasil yang diperoleh dari proses pengujian
tarik adalah grafik tegangan regangan, parameter kekuatan dan keliatan material pengujian dalam prosen perpanjangan, kontraksi atau reduksi penampang patah, dan bentuk permukaan patahannya. Tegangan dapat diperoleh dengan membagi beban dengan luas. Penampang mula-mula benda uji ( Dieter, 1993) :
σ =
Dimana : σ = Tegangan nominal (kg/mm2) P = Gaya tarik aksial (kg) A0 = Luas penampang normal (mm2 ) (Dieter, 2000)
METODE PENELITIAN
3.1 Alat
Alat-alat yang digunakan dalam penelitian ini adalah :
- Blender philiphs
- pH Meter pocket-sized
- Gelas Erlenmeyer pyrex
- Oven memmert
- Hotplate Stirer Ika
- Neraca Analitis shimazu
- Gelas Beaker pyrex
- Gelas Ukur pyrex
- Thermometer france
- Corong pyrex
- Labu Takar pyrex
- Desikator
- Statif dan Klem - Magnetik Stirrer
- Spketroskopi FT-IR shimadzu
- Pipet volume Pyrex
- Plat akrilik 10x10 cm
- Scanning Electron Microscope (SEM) JSM-35 C Shumandju - Spektrofotometer FT-IR Shimadzu
- Alat Uji Tarik ASTM Al – 7000 gotech - Sel cup
3.2
3.2 BahanBahan
Adapun bahan-bahan yang digun
Adapun bahan-bahan yang digunakan dalam penelitian ini adalah :akan dalam penelitian ini adalah : -- Pati sukunPati sukun
-- NaOH 0,3 M NaOH 0,3 M p.a p.a E’ Merck E’ Merck -- Asetat AnhidratAsetat Anhidrat p.a. E’ Merck p.a. E’ Merck -- AkuadesAkuades
-- GliserolGliserol p.a. E’ Merck p.a. E’ Merck -- Indikator UniversalIndikator Universal
-- Silica GelSilica Gel
3.3
3.3 Prosedur PenelitianProsedur Penelitian 3.3.1
3.3.1 Pembuatan Larutan NaOH 0,3 MPembuatan Larutan NaOH 0,3 M Ditimbang sebanyak
Ditimbang sebanyak 1,2 g NaO1,2 g NaOH, lalu dimasukkan H, lalu dimasukkan kedalam kedalam labu takar volumelabu takar volume 100 ml yang telah di isi 20
100 ml yang telah di isi 20 – – 50 ml akuades. Kemudian diaduk hingga larut 50 ml akuades. Kemudian diaduk hingga larut selanjutnya diencerkan hingga garis batas,
selanjutnya diencerkan hingga garis batas, kemudian dihomogenkan.kemudian dihomogenkan.
3.3.2
3.3.2 PreparasPreparasi i SampelSampel
Buah sukun yang kulitnya sudah menguning dikupas dan dihilangkan tangkai Buah sukun yang kulitnya sudah menguning dikupas dan dihilangkan tangkai buahnya,
buahnya, kemudian kemudian dicuci dicuci hingga hingga bersih bersih sampai sampai tidak tidak bergetah. bergetah. Buah Buah sukunsukun dipotong-potong hingga kecil, kemudian dicampur dengan akuades kemudian dipotong-potong hingga kecil, kemudian dicampur dengan akuades kemudian diblender hingga halus dan selanjutnya diperas dan disaring menggunakan kain diblender hingga halus dan selanjutnya diperas dan disaring menggunakan kain kasa untuk mendapatkan ekstrak pati bersama air. Ekstrak pati dibiarkan selama kasa untuk mendapatkan ekstrak pati bersama air. Ekstrak pati dibiarkan selama 24 jam sampai pati mengendap dan dipisahkan dari airnya melalui proses 24 jam sampai pati mengendap dan dipisahkan dari airnya melalui proses dekanter. Pati yang diperoleh dikeringkan dalam oven pada temperatur 45 dekanter. Pati yang diperoleh dikeringkan dalam oven pada temperatur 45 ooCC selama 24 jam. Pati kasar yang diperoleh digiling dan diayak kemudian ditimbang selama 24 jam. Pati kasar yang diperoleh digiling dan diayak kemudian ditimbang dan disimpan dalam desikator. Pati sukun yang diperoleh setelah dilakukan dan disimpan dalam desikator. Pati sukun yang diperoleh setelah dilakukan pengujian
pengujian dengan dengan larutan larutan iodine iodine memberikan memberikan warna warna biru biru dilanjutkan dilanjutkan analisisanalisis dengan menggunakan Spektrokopi FT-IR dan penentuan derajat mengembang dengan menggunakan Spektrokopi FT-IR dan penentuan derajat mengembang ((Swelling Power Swelling Power ).).
3.3.3
3.3.3 Pembuatan Pati AsetatPembuatan Pati Asetat
Kedalam gelas Beaker dimasukan sebanyak 75 g pati sukun, dalam 80 ml Kedalam gelas Beaker dimasukan sebanyak 75 g pati sukun, dalam 80 ml aquades. pH larutan diatur sesuai variabel yang ditentukan (pH 6, 7, 8, dan 9) aquades. pH larutan diatur sesuai variabel yang ditentukan (pH 6, 7, 8, dan 9) menggunakan NaOH 0,3 M disertai pengadukan selama 20 menit. Setelah itu menggunakan NaOH 0,3 M disertai pengadukan selama 20 menit. Setelah itu diaduk dan ditambahkan 4,7 ml asetat anhidrat dalam larutan tersebut dan diaduk dan ditambahkan 4,7 ml asetat anhidrat dalam larutan tersebut dan dipanaskan hingga suhu 45
dipanaskan hingga suhu 45 ooC selama 60 menit. Kemudian larutan difiltrasiC selama 60 menit. Kemudian larutan difiltrasi dengan kertas saring dan endapan yang tertinggal dicuci dengan aquades. Endapan dengan kertas saring dan endapan yang tertinggal dicuci dengan aquades. Endapan dikeringkan dalam oven pada suhu 50
dikeringkan dalam oven pada suhu 50 ooC dan pati asetat yang dihasilkanC dan pati asetat yang dihasilkan dihaluskan dan dikeringkan kembali pada suhu 50
dihaluskan dan dikeringkan kembali pada suhu 50 ooC selama 1 jam, selanjutnyaC selama 1 jam, selanjutnya dimasukkan kedalam desikator kemudian ditimbang. Pati asetat yang diperoleh dimasukkan kedalam desikator kemudian ditimbang. Pati asetat yang diperoleh dianalisis dengan menggunakan Spektokopi FT-IR dan derajat substitusi dianalisis dengan menggunakan Spektokopi FT-IR dan derajat substitusi mengikuti metode titrasi. Pati asetat dengan derajat substitusi (derajat asetilasi) mengikuti metode titrasi. Pati asetat dengan derajat substitusi (derajat asetilasi) yang terbaik digunakan dalam pembuatan
yang terbaik digunakan dalam pembuatan edible filmedible film..
3.3.4
3.3.4 Analisis Derajat Asetilasi Pati AsetatAnalisis Derajat Asetilasi Pati Asetat
Ditimbang sebanyak 1 g pati asetat lalu dilarutkan ke dalam 50 ml etanol pada Ditimbang sebanyak 1 g pati asetat lalu dilarutkan ke dalam 50 ml etanol pada suhu 50
suhu 50 ooC selama 30 menit. kemudian didinginkan pada suhu ruangan,C selama 30 menit. kemudian didinginkan pada suhu ruangan, ditambahkan 40 ml KOH 0,5 M dan didiamkan selama 15 menit pada suhu ditambahkan 40 ml KOH 0,5 M dan didiamkan selama 15 menit pada suhu ruangan. Kemudian dititrasi dengan HCl 0,5 M dengan menggunakan indikator ruangan. Kemudian dititrasi dengan HCl 0,5 M dengan menggunakan indikator fenolftalein hingga terjadi perubahan warna dari
fenolftalein hingga terjadi perubahan warna dari merah rose menjadi bening.merah rose menjadi bening. Dihitung derajat asetilasinya dengan menggunakan rumus :
Dihitung derajat asetilasinya dengan menggunakan rumus : % % == (( )) 0,043 0,043 100% 100% Dimana : Dimana : V
Voo = = volume volume HCl HCl untuk untuk titrasi titrasi blanko blanko (ml)(ml) V
Vnn = = volume volume HCl HCl untuk untuk sampel sampel (ml)(ml) N
N = normalitas HCl= normalitas HCl M
M = = massa massa sampel sampel kering kering (g)(g) 43
== 162162 ×× % % 43
430000 ((42 42 ×× % % AseAsetiltil))
Dimana : Dimana : 162
162 = = berat berat molekul molekul anhidrit anhidrit glukosa glukosa (C(C66HH1010OO55)) 4300
4300 = = berat berat molekul molekul asetil asetil (CH(CH33CO) x 100CO) x 100 42
42 = = selisih selisih antara antara berat berat molekul molekul gugus gugus asetat asetat dengan dengan gugus gugus OHOH
--3.3.5
3.3.5 Penetuan Derajat Mengembang (Penetuan Derajat Mengembang (
Sw
Swe
elling Po
lling Pow
we
er
r
))Sampel pati ditimbang sebanyak 2-3 gram kemudian letakkan pada cawan kering Sampel pati ditimbang sebanyak 2-3 gram kemudian letakkan pada cawan kering yang telah diketahui beratnya, kemudian disimpan dalam desikator yang di yang telah diketahui beratnya, kemudian disimpan dalam desikator yang di dalamnya sudah diberi larutan KCl jenuh dan diamati pertambahan berat sampel dalamnya sudah diberi larutan KCl jenuh dan diamati pertambahan berat sampel dengan ditimbang
dengan ditimbang selama kurun waktu 6, selama kurun waktu 6, 12, 24 12, 24 48, 72 jam dan dihi48, 72 jam dan dihitung dengantung dengan rumus berikut : rumus berikut : (%) W absorpsi = (%) W absorpsi = bb h bb h ((jj))−bb cwn dn p ()−bb cwn dn p () bb p bb p x 100 % x 100 % Dilakukan prosedur yang sama untuk pati asetat.
Dilakukan prosedur yang sama untuk pati asetat.
3.3.6
3.3.6 PembuatanPembuatan
EE d
dibl
ible
e FF ilm
ilm
Pati Asetat Pati Asetat PembuatanPembuatan edible filmedible film digunakan pati asetat yang derajat substitusi terbaik yaitu digunakan pati asetat yang derajat substitusi terbaik yaitu perlakuan pada kondisi aseyilasi
perlakuan pada kondisi aseyilasi pH = 8. Sebanyak pH = 8. Sebanyak 5 g pati 5 g pati asetat di asetat di masukkan kemasukkan ke dalam gelas Beaker yang telah diisi dengan 100 mL akuades, ditambah 1 ml dalam gelas Beaker yang telah diisi dengan 100 mL akuades, ditambah 1 ml gliserol. Diaduk hingga homogen. Dipanaskan diatas hotplate pada suhu ±50 gliserol. Diaduk hingga homogen. Dipanaskan diatas hotplate pada suhu ±50 ooCC hingga bercampur menjadi cairan kental. Campuran dituang ke plat akrilik dan hingga bercampur menjadi cairan kental. Campuran dituang ke plat akrilik dan diratakan. Dikeringkan didalam oven pada suhu ±40
diratakan. Dikeringkan didalam oven pada suhu ±40 ooC selama 48 jam. KemudianC selama 48 jam. Kemudian dilepas film dari plat akrilik, lalu dilakukan analisa kuat tarik, keregangan, dilepas film dari plat akrilik, lalu dilakukan analisa kuat tarik, keregangan, ketebalan, WVTR, SEM,
ketebalan, WVTR, SEM, % Swelling % Swelling ..
Dilakukan prosedur yang sama untuk pembuatan
3.3.7 Analisa
E dible F ilm
3.2.7.1 Uji Tarik / Uji Keregangan
Kekuatan tarik suatu bahan didefinisikan sebagai besarnya beban maksimum (Fmaks) yang digunakan untuk memutuskan spesimennya bahan diba gi dengan luas
penampang awal (A0).
= Fmaks A0 Keterangan :
σ = kekuatan tarik bahan (kgf/mm2) F = tegangan maksimum (kgf) A0 = luas penampang (mm2)
Disamping bersama kekuatan tarik (σ) sifat mekanik bahan juga diamati dari sifat kemulurannya () yang dilakukan dengan memilih hasil spesimen dengan ketebalan 0,1 mm dan dipotong membentuk spesimen untuk penguji kemuluran. Kedua spesimen dijepit pada alat kemuluran kemudian dicatat perubahan panjang (mm) berdasarkan besar kecepatan 50 mm/menit.
Perhitungan dilakukan sebagai berikut : = It I0 I0 × 100% = I0 × 100% Keterangan: = Kemuluran (%)
I0 = Panjang spesimen mula-mula (mm)
It = Panjang spesimen setelah diberi beban (mm)
3.2.7.2 Pengukuran ketebalan
Film yang dihasilkan diukur ketebalannya dengan menggunakan mikrometer dengan ketelitian alat 0,0001 mm.
3.3.7.3 Uji WVTR (Laju Tansmisi Uap Air)
Pengukuran berdasarkan gaya gravimetri. Permeasi sel digunakan dari bahan plastik yang mengandung 25 g silica gel. Pada permukaan sel dilubangi dengan diameter 1,3 cm. Film ditempelkan pada lubang permeasi sel. Sel ditempatkan pada desikator yang mengandung air suling. Sel ditimbang setiap 1 jam sekali selama 8 jam. Kemudian dihitung slope dari pertambahan berat silika terhadap waktu dengan persamaan garis regresi.
Perhitungan Laju transmisi
WVTR = (∆W / (∆t.A) g. s-1.m-2
Dimana : ∆W/∆t = Jumlah air transfer air per unit waktu (kg.s-1)
A = Luas Daerah yang terbuka terhadap transfer air pada film (m2)
3.2.7.4 Analisa SEM (
Scanning E lectron Mi croscopy
)Sampel diletakkan pada sel holder dengan perkat ganda. Sampel dimasukkan kedalam Scanning Electron Miscroscope (SEM), lalu gambar permukaan diamati dan dilakukan perbesaran sesuai yang diinginkan. Selanjutnya dilakukan pemotretan.
3.2.7.5 Uji Sifat mengembang ( % Swelling)
Edible film dipotong dengan ukuran 2 cm x 2 cm. Kemudian ditimbang masing-masing berat edible film. Kemudian dimasukkan kedalam Beaker glass yang masing-masingnya berisi 40 ml aquadest. Dibiarkan selama 2 hari dan dilihat perubahan dari edible film. Kemudian diangkat dan ditimbang dalam keadaan basah. Pengukuran derajat swelling dapat dihitung melalui rumus :
= Wg Wo
Wo 100 % dimana :
Wg = Berat sampel yang mengembang Wo = Berat sampel awal
3.3 Bagan Penelitian 3.4.1 Preparasi Sampel
Buah Sukun
Dikupas dan dihilangkan tangkai buah nya
Dicuci dengan air hingga kotoran dan getahnya hilang Dipotong-potong lalu dicuci kembali
kemudian diblender
Diperas menggunakan kain kasa
Residu Filtrat
Dibiarkan selama 24 jam
Digiling dan diayak Pati Sukun
FTIR
Dikeringkan dalam oven pada temperatur 45 oC
Endapan Filtrat
3.4.2 Pembuatan Pati Asetat
75 g Pati Sukun
Dimasukan kedalam gelas Beaker 1 L
Ditambahkan NaOH 0,3 M sampai pH 6 Diaduk menggunakan magnet stirer selama 20 menit
Filtrat Endapan
Dicuci dengan aquades
Dikeringkan dalam oven pada suhu 50 oC
Pati Asetat
Ditambahkan aquades 80 mL
Campuran Pati
Ditambahkan asetat anhidrat 4,7 mL Diaduk selama 60 menit pada suhu 45oC Disaring
FTIR DS Swelling
3.4.3 Pembuatan Edible Film
Pati Sukun
ditimbang sebanyak 5 g
ditambahkan 100 ml aquades diaduk hingga homogen
dimasukan ke dalam Beaker glass
Larutan Putih Susu
Larutan Putih Kental
dituangkan ke plat akrilik dan diratakan dikeringkan di dalam oven dengan suhu 40oC selama 2 hari
dipanaskan diatas hotplate dengan suhu 50oC
ditambahkan 1 ml gliserol diaduk hingga homogen
Edible Film
Kuat Tarik Kemuluran Ketebalan WVTR SEM Swelling
BAB 4
HASIL DAN PEMBAHASAN
4.1 Hasil
4.1.1 Pati Sukun
Pati yang digunakan dalam penelitian ini adalah hasil isolasi pati yang diperoleh dari buah sukun ( Artocarpus altilis) dimana dari sebanyak 10 kg buah sukun yang digunakan diperoleh sebanyak 680 g (6,8%) pati sukun. Uji kualitatif dari larutan pati menggunakan pereaksi larutan iodine memberikan larutan warna biru. Dari
spektrum hasil analisis spektroskopi FT-IR, pati hasil isolasi memberikan spektrum dengan puncak-puncak vibrasi pada daerah bilangan gelombang 3387cm-1 ; 2931 cm-1 ; 1157,29 cm-1 (Gambar 4.1).
4.1.2 Pembuatan Pati Asetat
Pati asetat merupakan hasil reaksi esterifikasi antara pati dan asam asetat anhidrat dengan bantuan larutan NaOH untuk mengaktifkan gugus hidroksil dimana dalam hal ini mengubah ikatan kovalen gugus hidroksil dari pati (Starch-O-H) menjadi bentuk ikatan ionik pada natrium pati (Starch-O Na- +) melalui pengontrolan variasi pH campuran (6, 7, 8 dan 9) yang mana sebelumnya pH dari pati = 5. Hasil analisis spektrokopi FT-IR masing-masing hasil asetilasi memberikan spektrum pada puncak-puncak vibrasi pada daerah bilangan gelombang 3387 cm-1 gugus –
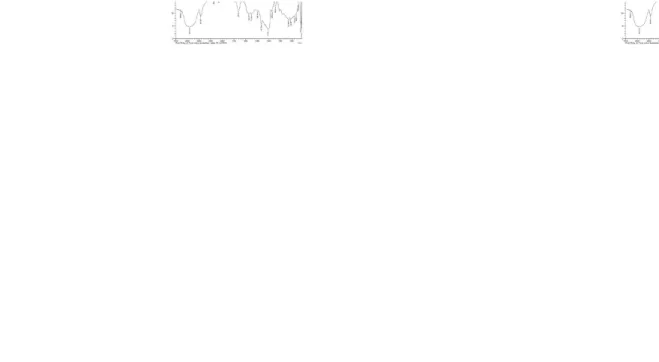
OH, 2931 cm-1 menunjukkan gugus C-H stretching , 1157,29 cm-1 menunjukkan gugus C-O-C dari eter dan gugus C=O ester muncul untuk pH 6 (Gambar 4.2) muncul puncak pada bilangan gelombang 1635,64 cm-1; pH 7 (Gambar 4.3) muncul puncak pada bilangan gelombang 1651,07 cm-1; pH 8 (Gambar 4.4) muncul puncak pada bilangan gelombang 1635,64 cm-1 dan pH 9 (Gambar 4.5) muncul puncak pada bilangan gelombang 1635,64 cm-1.
Gambar 4.3 Spektrum FT-IR Pati Asetat Hasil Asetilasi pH=7
Gambar 4.5 Spektrum FT-IR Pati Asetat Hasil Asetilasi pH=9
4.1.3 Persen Asetil dan Derajat Substitusi
Hasil penelitian persen asetil dan derajat substitusi yang ditentukan secara titrasi asidi alkalimetri tidak langsung, berturut-turut untuk masing-masing kondisi pH reaksi yang bervariasi dilihat pada Tabel 4.1, serta perhitungan persen asetil dan derajat substitusi dapat dilihat pada lampiran 1.
Tabel 4.1 Hasil Penentuan Persen Asetil dan Derajat Substitusi Pati Asetat
pH Persen Asetil DS
6 12,2765 0,5255
7 16,039 0,7165
8 21,9085 1,0501
4.1.4 Penentuan Derajat Mengembang (
Swelling Power
) Pati Sukun dan Pati Asetat pH=8Derajat mengembang (Swelling Power ) untuk pati sukun hasil isolasi dan pati
asetat yang diperoleh pada kondisi reaksi pH=8 dapat dilihat pada Tabel 4.2, serta perhitungan derajat mengembang dapat dilihat pada lampiran 2.
Tabel 4.2 Hasil Penentuan Swelling Power Pati sukun dan Pati asetat pH 8
Waktu (jam) W absorpsi(%)
Pati Sukun Pati Asetat pH 8
6 0,6122 0,5678
12 1,7173 1,1955
24 3,7682 2,8942
48 5,1869 3,8706
72 7,9944 4,7972
4.1.5 Uji Mekanik
E dible F ilm
Pati Sukun dan Pati Asetat pH 8Hasil Uji Kekuatan Tarik, Kemuluran dan Ketebalan Edible film dari variasi pati
sukun dan pati asetat pH 8 dengan plasticizer gliserol ditunjukkan pada Tabel 4.3,
serta perhitungan uji kekuatan tarik dan kemuluran dapat dilihat pada lampiran 4.
Tabel 4.3 Nilai Kuat Tarik; Kemuluran; dan Ketebalan Edible film Pati Sukun dan
Pati Asetat pH 8
No Parameter Pati Sukun Pati Asetat pH 8
1 Kuat Tarik (MPa) 2,1 11,2
2 Keregangan % 6,17 8,50