LAPORAN PRAKTIKUM KIMIA DASAR I LARUTAN ELEKTROLIT DAN NON ELEKTROLIT
Disusun Oleh:
Disusun Oleh
1. Saira Macap : NIM.148420616017 2. Novranseo Massa : NIM.148420616016 3. Soraya Radjab : NIM.148420616019 4. Sari Lestari Simanjuntak : NIM.148420616018 5. Annisa L. Wugaje : NIM.148420616003
Dosen Pengampu Abdul Rachman Tiro, M.Pd
NIDN. 1401118701
PROGRAM STUDI PENDIDIKAN IPA
SEKOLAH TINGGI KEGURUAN DAN ILMU PENDIDIKAN (STKIP) MUHAMMADIYAH SORONG
PRAKTIKUM KIMDAS I
Judul percobaan : Larutan Elektrolit Dan Nonelektrolit
Tujuan Percobaan : Menguji daya hantar listrik berbagai larutan yang digunakan dalam kehidupan sehari – hari.
Tempat : Laboratorium MIPA STKIP Muhammadiyah Sorong
I. DASAR TEORI
Larutan didefinisikan sebagai campuran homogen antara dua atau lebih zat. Suatu larutan tersusun dari komponen pelarut yang jumlahnya banyak, serta komponen zat terlarut yang jumlahnya sedikit.
Berdasarkan sifat listriknya, larutan dapat dibedakan sebagai berikut :
1. Larutan Elektrolit
Larutan ini dapat menghantarkan arus listrik. Contohnya adalah larutan garam dapur, larutan asam sulfat, air sungai dan air laut. Daya hantar listrik larutan ini tergantung pada jenis dan konsentrasinya sehingga dapat dibedakan menjadi elektrolit lemah dan elektrolit kuat. Elektrolit lemah memiliki daya hantar yang lemah. Elektrolit kuat memiliki daya hantar yang kuat. Contoh elektrolit lemah adalah asam cuka dan larutan amonia, sedangkan contoh dari elektrolit kuat:
• larutan garam ion dalam air, seperti NaCl, KBr dan NaBr
• lelehan senyawa ion yang tidak larut dalam air, seperti PbI2
• larutan asam-asam mineral dalam air, seperti HCl
• larutan basa dalam air, seperti NaOH dan KOH
2. Larutan Nonelektrolit
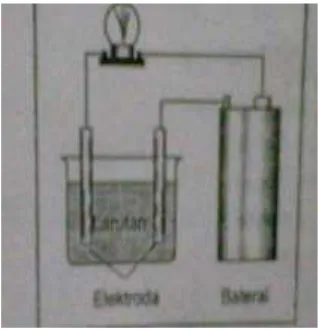
Hantaran listrik melalui larutan dapat ditunjukkan oleh alat penguji seperti gambar :
Jika larutan elektrolit bersifat elektrolit, lampu pada alat penguji akan menyala atau terjadi perubahan seperti timbulnya gelembung – gelembung gas. Bila berupa larutan nonelektrolit, perubahan – perubahan di atas tidak terjadi. Larutan elektrolit kuat dapat membuat lampu menyala, tetapi larutan elektrolit lemah hanya menimbulkan gelembung – gelembung pada kedua elektrode.
Hantaran listrik melalui larutan diterangkan dengan teori ion yang dikemukakan oleh Svante August Arrhenius (1859 – 1927) dari Swedia pada tahun 1887. menurut Arrchenius, larutan elektrolit mempunyai ion – ion yang bergerak bebas. Keberadaan ion – ion inilah yang akan menghantarkan arus. Ion – ion bergerak bebas karena zat – zat nonelektrolit yang dilarutkan dalam air akan terionisasi (terurai menjadi ion – ion) yaitu ion positif (kation) dan ion negatif
(anion). Sedangkan, pada pelarutan zat – zat nonelektrolit dalam air tidak akan terjadi ion – ion (zat nonelektrolit tidak terionisasi dalam air) sehingga tidak dapat
menghantarkan arus listrik. Contoh :
NaOH dalam air akan terurai menjadi ion – ion dengan persamaan reaksi : NaOH(aq) Na+(aq) + OH-(aq)
Dalam larutan HCl terurai menjadi ion H+ dan ion Cl- dengan reaksi ionisasi sebagai berikut :
HCl(aq) H+(aq) + Cl-(aq)
Ion H+ akan bergerak ke katode, kemudian mengambil elektron dan berubah menjadi gas hidrogen. Reaksinya sebagai berikut :
2H+(aq) + 2e- H2(g)
Dan, ion Cl- ke anode, kemudian melepas elektron dan berubah menjadi gas klorin. Reaksinya sebagai berikut :
2Cl-(aq) Cl2(g) + 2e
-Dengan demikian terjadi aliran listrik secara terus menerus. Peristiwa ini dinamakan elektrolisis dan secara lengkap reaksi elektrolisis larutan HCl dapat
ditulis sebagai berikut
2H+(aq) + 2Cl-(aq) H2(g) + Cl-(g)
Zat yang dapat menghasilkan ion, dalam larutan berupa senyawa ion atau senyawa kovalen polar.
1) Senyawa Ion
dapat kmbali bergerak bebas dan senyawanya dapat menghantarkan listrik. Contoh larutan elektrolit yang berupa senyawa ion adalah larutan NaCl.
2) Senyawa Kovalen Polar
Air merupakan pelarut polar sehingga antara molekul air dan molekul zat terlarut yang polar terjadi tarik – menarik yang cukup kuat sehingga dapat
memutuskan salah satu ikatan dan membentuk ion. Asam yang termasuk elektrolit jenis ini, contohnya asam klorida (HCl). Lelehan senyawa kovalen polar tidak dapat menghantarkan listrik karena lelehan tersebut terdiri atas molekul – molekul netral.
Kekuatan elektrolit ditunjukkan oleh derajat ionisasi (α).
α= mol zat yang terurai mol zat mula - mula
Untuk elektrolit kuat,α= 1 (terionisasi sempurna)
Untuk nonelektrolit,α=0 (tidak terionisasi)
Untuk elektrolit lemah, 0 <α< 1 (terionisasi sebagian)
II. ALAT DAN BAHAN
1. Alat yang digunakan : - Gelas Kimia 100 mL 3 buah - Kabel 2 Meter
- Batang Karbo (Batrei Bekas) 2 Buah - Baterai 1,5 V 3 buah
- Bola Lampu 1,5 V 1 buah
2. Bahan yang digunakan : - Larutan Asam Cuka (CH3COOH) - Larutan Garam (NaCl)
1. Menyusun alat penguji elektrolit sehingga dapat bekerja dengan baik. 2. Menyediakan 3 gelas kimia 100 mL yang bersih dan memberi label nama
3. Memasukkan bahan yang akan diuji ke dalam gelas kimia sesuai dengan label namanya masing – masing.
4. Menguji daya hantar larutan asam cuka dengan mencelupkan ke dua
elektrode. Mengamati dan mencatat perubahan yang terjadi pada lampu dan kedua elektrode.
5. Mengangkat elekrode. Kemudian membersihkan elektrode dengan menyemprotkan air dan mengeringkan dengan kertas tissue/ serbet.
6. Melakukan dengan cara yang sama untuk larutan – larutan lainnya.
IV. HASIL PENGAMATAN
No. Variabel Yang Di Amati Lampu Kondisi Elektrode 1. Jeruk Nipis Menyala Redup Timbul gelembung 2. CH3COOH Tidak menyala Timbul gelembung
3. NaCl Menyala Terang Timbul gelembung
4. Susu Tidak menyala Tidak timbul gelembung
5. Ca(OH)2 Tidak menyala Timbul gelembung 6. Sukrosa Tidak menyala Tidak timbul gelembung
V. PEMBAHASAN
Percobaan mengenai larutan elektrolit dan nonelektrolit ini dimaksudkan untuk menguji daya hantar listrik dalam berbagai larutan. Pada percobaan ini larutan yang diujikan diantaranya jeruk nipis, CH3COOH, NaCl, susu, Ca(OH)2 dan sukrosa.
Pada percobaan pra-praktikum, sample larutan yang telah ditentukan
menggunakan larutan CH3COOH, ternyata tidak menimbulkan lampu menyala namun hanya terdapat gelembung pada elektrodanya. Hal ini dikarenakan larutan CH3COOH tergolong larutan elektrolit lemah, dimana molekul yang bergerak
hanya sedikit sehingga hanya menimbulkan gelembung saja. Dan ini sesuai dengan literatur yang ada. Percobaan yang ketiga menggujikan larutan NaCl,
didapatkan hasil untuk lampu menyala dengan terang dan kondisi elektrodenya menimbulkan gelembung. Hal ini dikarenakan ion Na+ dan ion Cl- pada larutan bergerak dengan bebas sehingga menimbulkan lampu menyala dengan terang. Reaksinya sebagai berikut :
NaCl(aq) Na+(aq) + Cl-(aq)
Percobaan keempat menggunakan larutan susu, ternyata untuk larutan susu lampunya tidak menyala, begitu pula untuk elektrodanya tidak menimbulkan gelembung. Larutan susu tergolong larutan nonelektrolit. Dimana untuk zat nonelektrolit dalam larutan tidak terurai menjadi ion-ion tetapi hanya berupa molekul saja sehingga tidak dapat menghantarkan listrik karena tidak ada ion-ion yang bergerak bebas. Kemudian percobaan berikutnya menggujikan larutan Ca(OH)2 yang didapatkan hasilnya ternyata lampu tidak menyala namun hanya menimbulkan gelembung. Menurut literatur, Ca(OH)2 termasuk larutan kuat namun dalam percobaan hanya terdapat gelembung. Hal ini mungkin dikarenakan larutan sudah terkontaminasi dengan zat lain dan larutannya menjadi kotor sehingga ion-ion berkurang. Percobaan yang terakhir menggujikan larutan glukosa, dimana dalam percobaan lampu tidak menyala dan tidak menimbulkan gelembung. Ini seperti halnya pada pengujian larutan larutan susu, larutan glukosa
tergolong larutan nonelektrolit dimana untuk zat nonelektrolit dalam larutan tidak terurai menjadi ion-ion tetapi hanya berupa molekul saja sehingga tidak dapat
menghantarkan listrik karena tidak ada ion-ion yang bergerak bebas.
didapatkan lampu tidak menyala namun timbul gelembung. Dan hal ini sesuai dengan literatur yang ada. Rekasinya :
CH3COOH(aq) CH3COO-(aq) + H+(aq)
Percobaan ketiga menggunakan larutan NaCl didapatkan hasil pengamatan setelah percobaan ternyata lampu tidak menyala namun timbul gelembung.
Menurut literature seharusnya pada NaCl lampu menyala tetapi pada waktu melakukan percobaan, hasil pengamatan yang didapatkan ternyata lampu tidak menyala. Hal ini mungkin dikarenakan konsentrasi larutan tersebut terlalu kecil atau karena larutan yang digunakan berulang kali sehingga lrutan sudah terkontaminasi dengan zat lain. Selain itu rangkaian alat yang digunakan tidak dapat dirangkai dengan baik sehingga mempengaruhi pengujian daya hantar larutan tersebut.
Percobaan yang keempat menggujikan larutan susu. Untuk larutan susu ternyata didapatkan lampu tidak menyala dan juga tidak timbul gelembung. Hal ini dikarenakan susu merupakan larutan nonelektrolit dimana untuk zat nonelektrolit dalam larutan tidak terurai menjadi ion-ion tetapi hanya berupa molekul saja sehingga tidak dapat menghantarkan listrik karena tidak ada ion-ion yang bergerak bebas.
Percobaan selanjutnya menggujikan larutan Ca(OH)2, setelah percobaan didapatkan hasil ternyata lampu tidak menyala namun hanya timbul gelembung. Menurut literature Ca(OH)2 tergolong larutan elektrolit kuat. Tidak menyalanya lampu pada larutan ini dikarenakan konsentrasi larutan tersebut terlalu kecil atau karena larutan yang digunakan berulang kali sehingga larutan sudah
terkontaminasi dengan zat lain. Selain itu rangkaian alat yang digunakan tidak dapat dirangkai dengan baik sehingga mempengaruhi pengujian daya hantar
larutan tersebut.
Dari percobaan-percobaan yang dilakukan pada saat praktikum dengan pada saat dipraktikumkan (saat diasistenkan) ternyata didapatkan hasil yang berbeda terutama pada larutan jeruk nipis dan NaCl. Perbedaan hasil pengamatan
ini dikarenakan konsentrasi larutan yang digunakan pada waktu pra-praktikum dan waktu praktikum berbeda. Percobaan saat dipraktikumkan, konsentrasi yang
digunakan lebih kecil dibandingkan pada saat diujicobakan. Selain itu, alat yang digunakan pun berbeda. Dimana pada saat dipraktikumkan alat yang digunakan hanya merangkaikan baterai dengan kabel secara manual. Berbeda halnya pada saat diujicobakan menggunakan rangkaian alat yang lebih modern. Selebihnya untuk penggujian larutan yang lain hasilnya sama.
VI. KESIMPULAN DAN SARAN A. Kesimpulan
1. Larutan elektrolit kuat mampu menghantarkan listrik dengan kuat dapat menyebabkan lampu terang dan timbul gelembung gas.
2. Larutan elektrolit lemah hanya mampu menghantarkan arus listrik dengan lemah sehingga tidak mampu membuat lampu menyala, dan hanya mampu menimbulkan gelembung gas.
3. Larutan nonelektrolit tidak mampu menghantarkan lisrik sehingga tidak membuat lampu menyala dan tidak menimbulkan gelembung. 4. Larutan yang digunakan dapat digolongkan berdasarkan daya
hantarnya. Diantaranya : larutan NaCl dan larutan Ca(OH)2 termasuk elektrolit kuat. Larutan jeruk nipis dan CH3COOH termasuk larutan
elektrolit lemah. Larutan sukrosa dan susu termasuk larutan nonelektrolit.
B. Saran
1. Alat yang digunakan hendaknya lebih baik lagi.
2. Dalam melakukan percobaan hendaknya lebih teliti dan seksama. 3. Bahan yang digunakan hendaknya lebih banyak agar kesalahan dalam
VII. KENDALA-KENDALA
1. Alat yang digunakan terlalu sederhana sehingga memungkinkan untuk terjadi kesalahan.
2. Bahan yang digunakan terlalu sedikit sehingga hasil yang ingin dicapai kurang maksimal.
VIII. DAFTAR PUSTAKA
Anshory, Irfan.2003.Kimia SMU untuk kelas I. Jakarta: Erlangga
Susilowati, Endang. 2004. Sains Kimia Prinsip dan Terapannya. Solo : PT. Tiga Serangkai Pustaka Mandiri.
LAMPIRAN
Pertanyaan !!!
1. Di antara bahan yang diperiksa, larutn manakah yang merupakan larutan elektrolit ? Dan larutan manakah yang merupakan larutan nonelektrolit ? 2. Mengapa larutan elektrolit dapat menghantarkan listrik ?
Jawaban :
1. Di antara bahan yang diperiksa larutan yang bersifat elektrolit adalah CH3COOH, NaCl, larutan jeruk dan Ca(OH)2, sedangkan larutan yang merupakan larutan nonelektrolit adalah larutan susu dan larutan gula. 2. Larutan elektrolit dapat menghantarkan arus listrik karena mengandung