BAB II
TINJAUAN PUSTAKA
2.1 Penyakit Peptic Ulcer 2.1.1 Gambaran umum
Penyakit peptic ulcer adalah putusnya kontinuitas mukosa lambung yang meluas sampai di bawah epitel. Gambaran klinis utamanya adalah rasa nyeri yang
terjadi pada bagian lambung dan akan mereda setelah makan atau sesudah
menelan antasida. Nyeri biasanya timbul 2 - 3 jam setelah makan atau pada
malam hari sewaktu lambung kosong. Nyeri ini seringkali digambarkan sebagai
nyeri teriris, terbakar, atau rasa tidak enak. Sekitar seperempat dari penderita
mengalami perdarahan, walaupun hal ini lebih lazim terjadi pada ulkus
duodenum. Gejala dan tanda penyakit ini adalah muntah, muntahan berwarna
merah atau “seperti kopi”, mual, anoreksia, dan penurunan berat badan (Price dan
Wilson, 2005).
Peptic ulcer dapat terjadi disetiap bagian saluran cerna yang terkena getah asam lambung, yaitu esofagus, lambung, duodenum, dan setelah
gastroenterostomi, juga jejunum (Price dan Wilson, 2005).
2.1.2 Etiologi penyakit Peptic Ulcer
Kebanyakan penyakit peptic ulcer disebabkan karena adanya asam lambung dan enzim pepsin ketika Helicobacter pylori, NSAIDs, atau faktor lainnya mengganggu sistem pertahanan mukosa dan penyembuhan mukosa.
Hipersekresi dari asam lambung dan pepsin ini yang menghambat mekanisme
2.1.3 Patofisiologi
Penyebab terjadinya peptic ulcer saat ini masih sering diperdebatkan. Namun dipercaya bahwa penyebab terjadinya peptic ulcer dikarenakan ketidakseimbangan antara faktor agresif (Helicobacter pylori, NSAIDs, asam lambung) dan faktor pertahanan (mucin, bikarbonat, prostaglandin), yang
menyebabkan gangguan pada jaringan mukosa (Sunil, et al., 2012).
Banyak faktor yang berperan dalam hal terjadinya peptic ulcer. Bakteri
Helicobacter pylori dijumpai pada sekitar 90% penderita peptic ulcer (Price dan Wilson, 2005).
2.1.4 Helicobacter pylori
Helicobacter pylori berbentuk spiral, pH sensitif, gram negatif, bakteri mikroaerofilik yang terletak antara lapisan mukus dan permukaan sel ephitel di
lambung, atau pada berbagai lokasi lapisan sel ephitel dapat ditemukan.
Kombinasi antara bentuk tubuh spiral dan flagel dari bakteri yang membantunya
berpindah-pindah disekitar lumen dalam lambung (Berardi dan Welage, 2005).
Helicobacter pylori memproduksi dalam jumlah besar enzim urease, enzim ini menghidrolisis urea yang terdapat dalam cairan lambung dan
mengubahnya menjadi amonia dan karbondioksida. Efek netralisir dari amonia
yang dihasilkan akan membentuk suasana netral dan mengelilingi tubuh bakteri,
yang mana hal ini membantu melindungi bakteri dari pengaruh asam di lambung.
Bakteri ini juga memproduksi senyawa protein penghambat asam yang
membantunya untuk beradaptasi di lingkungan dengan pH yang rendah dalam
2.1.5 Sawar mukosa lambung
Lapisan mukosa lambung yang tebal merupakan garis depan pertahanan
terhadap trauma mekanis dan agen kimia. Prostaglandin terdapat dalam jumlah
berlebihan dalam mukus lambung dan tampaknya berperan penting dalam
pertahanan mukosa lambung. Sawar mukosa penting untuk perlindungan lambung
dan duodenum (Price dan Wilson, 2005).
Ketika lapisan mukosa mengalami kerusakan, maka dengan segera sel-sel
pertahanan mukosa beregenerasi membentuk sistem pertahanan yang baru.
Pemeliharaan lapisan mukosa ini berkaitan dengan produksi prostaglandin, yang
membantu dalam pemulihan kerusakan mukosa dan pertahanan mukosa (Berardi
dan Welage, 2005).
Destruksi sawar mukosa diduga merupakan faktor penting dalam
patogenesis peptic ulcer. Aspirin, alkohol, garam empedu, dan zat-zat lain yang dapat merusak mukosa lambung. Kerusakan yang terjadi dapat dilihat pada
gambar di bawah ini.
2.2 Drug Delivery System 2.2.1 Uraian Drug Delivery System
Pemberian obat secara oral telah lama dikenal sebagai rute pemberian obat
yang paling banyak digunakan jika dibandingkan dengan rute pemberian obat
lainnya dan telah dikembangkan untuk penyampaian obat secara sistemik dengan
berbagai bentuk sediaan dengan formulasi yang berbeda. Saat ini para ilmuwan
farmasi berusaha mengembangkan sistem pemberian obat “Drug Delivery System” yang ideal. Sistem pemberian obat yang ideal ini harus memiliki kemampuan untuk satu dosis pemberian obat dapat digunakan selama pengobatan
dan harus menyampaikan obat langsung di lokasi tertentu yang diinginkan dalam
pengobatan. Para ilmuwan ini telah berhasil mengembangkan sistem penyampaian
obat yang mendekati sistem penyampaian yang ideal tersebut dan mendorong para
ilmuwan untuk mengembangkan sistem penyampaian obat yang terkontrol atau
“Controlled Release System” (Kumar, et al., 2012).
Desain penyampaian obat secara oral ini, obat pelepasannya dipertahankan
berlangsung terus menerus ditujukan untuk mencapai pelepasan obat yang efektif,
konsentrasi obat dalam jaringan target dapat ditentukan dan mengoptimalkan efek
terapetik obat yang dilakukan dengan cara mengendalikan pelepasan obat di
dalam tubuh dengan dosis obat tertentu. Biasanya obat konvensional diberikan
dalam dosis berkala yang diformulasikan sedemikian rupa untuk memastikan
stabilitas, aktivitas dan bioavalabilitas sediaan obat (Kumar, et al., 2012). Dengan
demikian penyampaian obat dengan cara ini dapat mengurangi frekuensi
pemberian dosis obat. Obat diberikan dalam dosis tunggal untuk memperpanjang
obat langsung di lokasi tempat kerjanya atau lokasi target (Neetika dan Manish,
2012).
2.3 Sustained Release Drug Delivery System
Sistem penyampaian obat ini menyediakan pelepasan obat yang
diperlambat selama jangka waktu tertentu dan juga pelepasan obat dikontrol di
dalam tubuh. Dengan cara demikian sistem penyampaian obat ini berhasil
mempertahankan tingkat konsentrasi obat yang konstan dalam jaringan target atau
sel. Sistem penyampaian obat dengan cara ini dikelompokkan ke dalam dua
sistem penyampaian obat yaitu “Controlled Release” dan “Extended Release” (Lee , 1987).
a. Controlled Release
Sistem ini mencakup sistem penyampaian obat yang pelepasannya secara
perlahan selama waktu tertentu, yang mana pelepasan obatnya diperpanjang
(Lee, 1987). Sistem penyampaian obat secara terkontrol ini pelepasan obat dapat
ditentukan, dapat diprediksi, dan kecepatan pelepasannya dapat dikendalikan.
Pelepasan obat secara terkontrol ini memiliki manfaat seperti terapi yang optimal
dengan konsentrasi obat dalam darah dapat ditentukan dalam jangka waktu yang
panjang, peningkatan aktivitas kerja obat dengan waktu paruh yang pendek,
penghilangan efek samping, mengurangi frekuensi pemberian dosis obat dan juga
mengurangi penggunaan obat secara berlebih. Sehingga terapi dan faktor
kepatuhan pasien menjadi lebih baik. Dalam pengembangan sistem penyampaian
obat dengan cara ini membutuhkan pemahaman tentang beberapa aspek penting
seperti karakteristik sifat fisika kimia obat dan juga harus memperhatikan sistem
memformulasikan bentuk sediaan obat yang diinginkan, sehingga dapat diterima
oleh pasien (Narang, 2010).
b. Extended Release
Sistem penyampaian obat ini melepaskan obat lebih lambat dari pelepasan
obat secara normal pada umumnya dan dapat mengurangi frekuensi dosis obat
(Lee , 1987).
2.4 Gastro Retentive Drug Delivery System
Sistem penyampaian obat yang bertahan di lambung atau yang lebih
dikenal “Gastro Retentive Delivery System” ini dapat mempertahankan obat tetap berada di dalam lambung selama beberapa jam dan karenanya dapat
memperpanjang waktu tinggal obat di lambung secara signifikan. Peningkatan
waktu tinggal di lambung dapat meningkatkan bioavailabilitas atau ketersediaan
hayati, mengurangi residu obat, dan meningkatkan kelarutan obat yang kurang
larut dalam lingkungan pH tinggi. Sistem ini juga diaplikasikan dalam pengobatan
lokal untuk bagian perut dan bagian atas usus kecil. Motilitas saluran cerna yang
melambat dengan pemberiaan bersamaan dengan obat ini juga meningkatkan
waktu tinggal obat di dalam lambung (Neetika dan Manish, 2012).
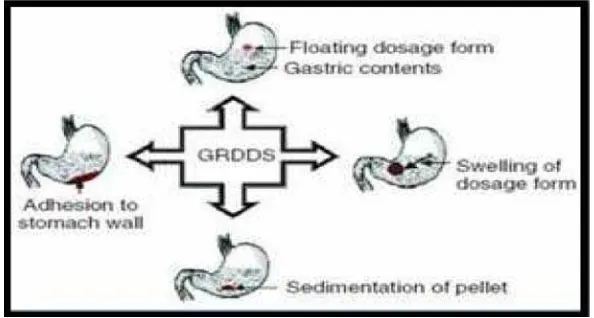
Berbagai pendekatan dari sistem Gastroretentive dapat dilihat pada Gambar 2.2. Retensi lambung dapat dikendalikan dari berbagai bentuk sediaan
dengan mekanisme mukoadhesif, mengapung, sedimentasi, ekspansi, dan sistem
modifikasi bentuk atau dengan pemberian bahan tertentu, yang menunda
pengosongan lambung (Neetika dan Manish, 2012).
2.4.1 Lambung
Lambung memiliki fungsi utama untuk memproses dan mengangkut
makanan. Selain itu lambung sebagai tempat penyimpanan makanan dalam jangka
waktu singkat, yang memungkinkan untuk mengkonsumsi makanan dalam jumlah
yang banyak secara cepat. Proses pencernaan secara enzimatik berlangsung di
dalam lambung (Narang, 2011).
Anatomi lambung dibagi menjadi 3 wilayah yaitu bagian fundus, bagian
badan dan bagian antrum (pilorus). Bagian proksimal terdiri dari bagian fundus
dan bagian badan yang bertindak sebagai tempat untuk bahan tercerna, sedangkan
bagian antrum adalah bagian utama untuk gerakan mencampur makanan dan juga
bertindak sebagai pompa dalam pengosongan lambung untuk mendorong
makanan menuju bagian saluran pencernaan selanjutnya (Narang, 2011).
Lambung berbentuk seperti huruf J yang melebar pada bagian sisinya. Saluran
pencernaan pada dasarnya adalah sebuah tabung dengan panjang sekitar sembilan
meter yang membentang melalui bagian tengah tubuh dari mulut sampai ke anus
dan termasuk di dalamnya tenggorokan (faring), kerongkongan, lambung, usus
kecil (terdiri dari duodenum, jejunum dan ileum) dan usus besar (terdiri dari
sekum, usus buntu, usus besar dan rektum). Dinding saluran pencernaan memiliki
sampai anus, dengan beberapa variasi untuk masing-masing bagian tertentu
(Neetika dan Manish, 2012).
Lambung merupakan organ tubuh dengan kapasitas tertentu untuk tempat
penyimpanan dan pencampuran makanan. Di dalam lambung makanan
mengalami proses pencernaan kompleks. Rata-rata panjang lambung pada
umumnya sekitar 0,2 meter (m) dan luas permukaan penyerapannya sekitar 0,1
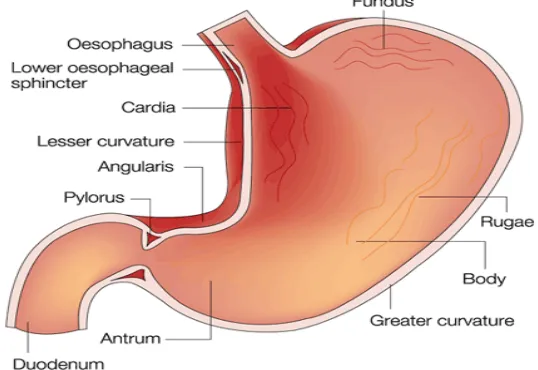
meter persegi (m2). Gambaran anatomi lambung dapat dilihat pada Gambar 2.3.
Gambar 2.3 Anatomi lambung (Arunachalam, et al., 2011)
Waktu pengosongan lambung saat berpuasa ataupun saat makan
dipengaruhi beberapa faktor dalam tubuh. Hal ini berkaitan dengan gerakan atau
motilitas dari otot-otot lambung yang mengakibatkan perbedaan waktu
pengosongan lambung diantara kedua keadaan ini. Masing-masing individu
memiliki waktu pengosongan lambung yang berbeda, hal ini dipengaruhi faktor
biologis di dalam tubuh. Siklus yang baik makanan melalui lambung dan usus
setiap 2 - 3 jam. Siklus ini disebut siklus mioelektrik bagian saluran pencernaan
atau perpindahan suatu bahan tercerna dalam saluran pencernaan yang
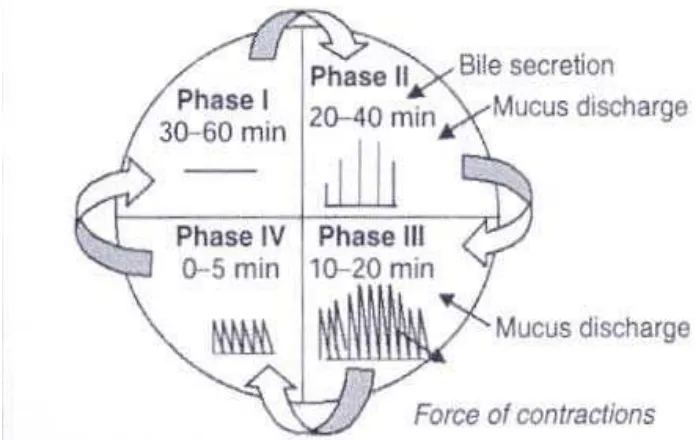
Dalam siklus ini dibagi dalam 4 tahapan:
1. Tahap I (fase basal) yang berlangsung selama 30 sampai 60 menit dengan
terjadinya awal motilitas kontraksi.
2. Tahap II (fase preburst) yang berlangsung selama 20 sampai 40 menit
dengan potensial aksi dan motilitas kontraksi. Dalam fase ini berlangsung
dengan intensitas dan frekuensi motilitas kontraksi yang meningkat secara
bertahap.
3. Tahap III (fase burst) yang berlangsung 10 sampai 20 menit. Fase ini
mencakup kontraksi intens dan rutin yang terjadi dalam waktu singkat. Hal
ini dikarenakan seluruh bahan tercerna dalam lambung diteruskan menuju
usus kecil. Hal ini dikenal dengan “Housekeeper wave”.
4. Tahap IV berlangsung selama 0 sampai 5 menit dan terjadi diantara fase
III dan fase I yang terjadi motilitas kontraksi secara terus-menerus
(Washington, et al., 2001).
Tahapan siklus kontraksi ini dapat dilihat pada Gambar 2.4.
Motilitas lambung dikendalikan oleh susunan sistem saraf dan sistem
hormonal. Kontrol dari sistem saraf ini berasal dari sistem saraf enterik yang juga
sebagai sistem saraf parasimpatis (terutama saraf vagus) dan sistem saraf simpatis.
Pengaruh hormonal telah terbukti mempengaruhi motilitas lambung seperti
adanya gastrin dan kolesistokinin yang bertindak dalam membantu relaksasi
bagian proksimal lambung dan meningkatkan kontraksi pada bagian distal
lambung (Sharma, et al., 2011).
Motilitas atau kontraksi otot polos lambung memiliki dua fungsi dasar
yaitu: (a) Menghancurkan, mencampurkan, mencairkan makanan yang ditelan
untuk membentuk chyme (kimus).
(b) Chyme (kimus) didorong melalui saluran pilorus ke dalam usus kecil,
proses ini disebut pengosongan lambung (Sharma, et al., 2011).
Volume cairan lambung pada saat berpuasa atau dalam keadaan lambung
kosong adalah 25 - 50 ml. Terdapat perbedaan sekresi asam lambung pada
individu normal dengan yang memiliki masalah terhadap sekresi asam lambung
atau achlorhydric individu. Pengaruh pH lambung terhadap penyerapan obat sangatlah berarti terutama untuk sistem penghantaran obat secara oral, pH cairan
lambung dalam keadaan berpuasa berkisar antara 1,2 – 2,0 dan dalam keadaan
makan 2,0 – 6,0 (Sharma, et al., 2011).
2.5 Floating Drug Delivery System
Sistem penghantaran obat ini dengan sistem mengapung atau sistem
hidrodinamis dikendalikan dengan berat jenis yang kecil sehingga dapat
mengapung di atas cairan lambung dan tetap mengapung di lambung tanpa
Sementara dalam sistem mengapung ini, obat dilepaskan perlahan pada tingkatan
yang diinginkan dari sistem ini. Setelah pelepasan obat, sistem residual ini
dikosongkan dari lambung. Hal ini menyebabkan peningkatan waktu retensi
lambung yang lebih baik sehingga terjadi peningkatan konsentrasi obat dalam
plasma (Gopalakrishnan dan Chenthilnathan, 2011).
2.5.1 Pembagian sistem Floating
Sistem penghantaran obat floating diklasifikasikan dalam dua variabel formulasi yaitu sistem Effervescent dan sistem Non-effervescent.
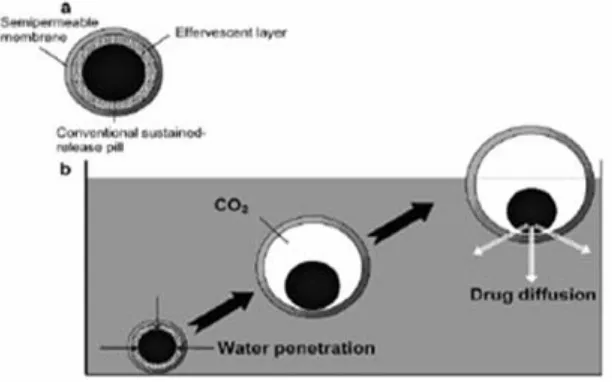
a. Effervescent Floating
Sistem ini dibuat dalam bentuk matriks dengan menggunakan polimer
yang dapat mengembang seperti HPMC, senyawa polisakarida lain, kitosan, dan
berbagai komponen effervescent seperti natrium bikarbonat, kalsium karbonat,
asam sitrat atau asam tartrat. Sediaan ini dirancang sedemikian rupa, sehingga
ketika kontak dengan cairan lambung, maka gas karbondioksida (CO2) akan
terlepas dan terperangkap dalam sistem hidrokoloid yang mengembang. Hal ini
membantu sediaan untuk mengapung (Goyal, et al., 2011).
b. Non-effervescent Floating
Sistem Non-effervescent ini bekerja dengan mekanisme pengembangan
polimer, bioadhesif dari polimer pada lapisan mukosa saluran pencernaan. Pada
umumnya dalam formulasi sistem non-effervescent ini menggunakan bahan yang
mampu membentuk gel atau memiliki kemampuan mengembang yang baik
seperti senyawa hidrokoloid, polisakarida. Juga biasa digunakan bentuk matriks
dari polimer seperti polimetakrilat, poliakrilat, polistiren, dan bioadhesif polimer
yaitu kitosan dan karbopol (Goyal, et al., 2011).
2.5.2 Kandidat obat untuk sediaan Floating
Dalam sistem penghantaran obat ini dimaksudkan untuk obat-obat dengan
tujuan pemakaian tertentu, dengan maksud untuk penghantaran dan aktivitas kerja
obat yang lebih baik. Berbagai macam kandidat obat yang tepat untuk
diformulasikan dalam sistem penghantaran obat floating diantaranya: a. Obat-obat yang aktif bekerja secara lokal di lambung.
Seperti: Misoprostol, antasida.
b. Obat-obat yang memiliki tapak absorpsi yang sempit dalam saluran pencernaan.
Seperti: L-DOPA, p-aminobenzoic acid, furosemid, riboflavin.
c. Obat-obat yang tidak stabil dalam lingkungan basa di bagian usus atau kolon.
Seperti: Captopril, ranitidine HCl, metronidazol.
d. Obat-obat yang mengganggu aktivitas kerja mikroba di kolon.
Seperti: Antibiotik yang digunakan dalam pengobatan Helicobacter Pylori, diantaranya tetracyclin, clarithromycin, amoxicilin.
e. Obat-obat yang menunjukkan kelarutan yang rendah pada pH yang tinggi.
Berikut beberapa contoh sediaan obat yang diformulasikan dalam bentuk
sediaan Floating ditunjukkan dalam tabel di bawah ini.
Tabel 2.1 Berbagai contoh formulasi bentuk sediaan Floating (Gopalakrishnan dan Chenthilnathan, 2011).
No Bentuk Sediaan Nama Obat
1 Tablet Chlorpheniramin maleat, Theophyllin, Furosemid,
Ciprofloxacin, Captopril, Asam Asetilsalisilat, Nimodipin,
Amoxicillin, Verapamil HCl, Isosorbide dinitrate,
Isosorbide mononitrate, Acetaminophen, Dilitiazem,
Florouracil, Prednisolon.
2 Kapsul Nicardipin, Chlordiazepoxide HCl, Furosemid,
Misoprostol, Diazepam, Propanolol, Urodeoxycholic.
3 Mikrosper Aspirin, Griseofulvin, p-nitroanilline, Ketoprofen,
Ibuprofen, Terfenadin.
4 Granul Indometasin, Na-Diklofenak, Prednisolon.
5 Film Cinnarizine
Tabel 2.2 Sediaan Floating yang telah tersedia di pasaran (Gopalakrishnan dan Chenthilnathan, 2011).
No Bentuk Sediaan Nama Obat Brand Name Perusahaan, Negara Produsen)
2 Floating Capsule Diazepam VALRELEASE Hoffman-LaRoche, USA
TOPALKAN Pierre Fabre Drug, FRANCE
Ciprofloxacin CIFRAN OD Ranbaxy, INDIA
7 Bilayer floating Capsule
2.5.3 Keuntungan FloatingDrug Delivery System
Sistem penghantaran obat melalui sistem floating ini merupakan teknologi
penghantaran obat dengan retensi lambung yang lebih lama dan memiliki
beberapa keuntungan dalam pemberian obat dengan sistem ini. Keuntungan ini
meliputi:
a. Peningkatan penyerapan obat, karena peningkatan waktu tinggal di lambung
dan peningkatan waktu kontak obat dengan daerah penyerapan.
b. Penghantaran obat yang dapat dikendalikan pelepasannya.
c. Penghantaran obat secara lokal untuk daerah kerja di lambung.
d..Meminimalkan terjadinya iritasi pada mukosa lambung karena obat-obatan
tertentu, dengan cara melepaskan obat secara lambat pada tingkat terkendali.
e. Digunakan untuk pengobatan gangguan pencernaan.
f. Menggunakan peralatan yang sederhana dan konvensional dalam formulasinya.
g. Kemudahan dalam penggunaannya dan meningkatkan faktor kepatuhan pasien
menjadi lebih baik.
h. Penghantaran obat pada daerah tertentu (Sharma, et al., 2011).
Berbagai keuntungan ini yang menjadikan sistem lebih dikembangkan lagi
untuk menghasilkan sistem penghantaran yang ideal (Sharma, et al., 2011).
2.5.4 Kekurangan Floating Drug Delivery System
Disamping memiliki banyak keuntungan dalam sistem floating ini,
terdapat pula kekurangan dari sistem ini. Kekurangan ini meliputi:
a. Retensi lambung dipengaruhi oleh banyak faktor seperti makanan, pH dan
motilitas lambung. Faktor-faktor ini tidak pernah tetap dan karenanya daya
b. Obat-obatan yang menyebabkan iritasi dan lesi pada mukosa lambung tidak
cocok untuk sistem pemberian obat ini.
c. Variabilitas tinggi dalam waktu pengosongan lambung serta membutuhkan
cairan lambung yang cukup untuk mempertahankan sediaan tetap berada di
lambung.
d. Pengosongan lambung untuk pasien dalam keadaan tidur tidak dapat
diprediksi dan bergantung pula pada diameter dan ukuran sediaan floating
tersebut. Oleh karena itu sebaiknya tidak diberikan sediaan ini saat pasien akan
tidur (Sharma, et al., 2011).
2.6 Metronidazol 2.6.1 Uraian bahan
Rumus Bangun :
Rumus Molekul : C6H9N3O3
Nama Kimia : 2-(2-methyl-5-nitro-1H-imidazol-1-yl)ethanol
Berat Molekul : 171,16
Pemerian : Serbuk hablur;putih atau kuning gading; bau lemah;rasa
pahit dan agak asin.
Kelarutan : Larut dalam 100 bagian air, dalam 200 bagian etanol
(95%) P dan dalam 250 bagian kloroform P; sukar larut
2.6.2 Farmakologi metronidazol
Metronidazol mempunyai aktivitas antibakteri yang mampu melawan
semua cocci anaerobik positif dan anaerobik gram negatif (termasuk Bacteroides
spp.) serta basil anaerobik gram positif penghasil spora (Brunton, et al., 2008).
Metronidazol memperlihatkan daya amubasid langsung. Pada biakan
E. histolytica dengan kadar metronidazol 1 - 2 mcg/ml, semua parasit musnah dalam 24 jam. Sampai saat ini belum ditemukan amuba yang resisten terhadap
metronidazol. Metronidazol juga menunjukkan daya trikomoniasid langsung pada
biakan Trichomonas vaginalis (Syarif dan Elysabeth., 2007).
Mekanisme kerjanya yakni berinteraksi dengan DNA menyebabkan
perubahan struktur helik DNA dan putusnya rantai sehingga sintesa protein
dihambat dan kematian sel. (Sukandar, dkk., 2008).
2.6.3 Farmakokinetik metronidazol
Metronidazol adalah suatu prodrug yang diaktivasi dengan cara reduksi
gugus nitro oleh organisme yang suseptibel. Berbeda dengan patogen aerobik,
patogen anaerobik dan mikroaerofilik seperti T. vaginalis, E. hystolitica, dan G. lamblia serta bakteri anaerobik mempunyai komponen transpor elektron untuk mendonorkan elektron kepada metronidazol. Transpor elektron menghasilkan
anion nitro radikal yang sangat reaktif yang membunuh bakteri yang suseptibel
melalui mekanisme radical-mediated yang merusak DNA (Brunton, et al., 2008). Absorpsi metronidazol berlangsung dengan baik sesudah pemberian oral.
Satu jam setelah pemberian dosis tunggal 500 mg per oral diperoleh kadar plasma
kira-kira 10 mcg/ml. Umumnya untuk kebanyakan protozoa dan bakteri yang
berkisar antara 8 - 10 jam. Pada beberapa kasus terjadi kegagalan karena
rendahnya kadar sistemik. Ini mungkin disebabkan oleh absorpsi yang buruk atau
metabolisme yang terlalu cepat (Syarif dan Elysabeth, 2008).
Metronidazol dieksresi melalui urin dalam bentuk asal dan bentuk
metabolit hasil oksidasi dan glukuronidasi. Urin mungkin berwarna coklat
kemerahan karena mengandung pigmen tak dikenal yang berasal dari obat.
Metronidazol juga dieksresi melalui air liur, air susu, cairan vagina, dan cairan
seminal dalam kadar yang rendah (Syarif dan Elysabeth, 2008).
2.6.4 Efek samping metronidazol
Efek samping hebat yang memerlukan penghentian pengobatan jarang
ditemukan. Efek samping yang paling sering dikeluhkan ialah sakit kepala, mual,
mulut kering dan rasa kecap logam. Muntah, diare dan spasme usus jarang
dialami. Lidah berselaput, glositis dan stomatitis dapat terjadi selama pengobatan
dan ini mungkin berkaitan dengan moniliasis. Efek samping lain dapat berupa
pusing, vertigo, ataksia, parestesia pada ekstremitas, urtikaria, flushing, pruritus,
disuria, sistitis, rasa tekan pada pelvik, juga kering pada mulut, vagina dan vulva.
Metronidazol ialah suatu nitroimidazol, sehingga ada kemungkinan dapat
menimbulkan gangguan darah. Pada pasien dengan riwayat penyakit darah atau
dengan gangguan SSP, pemberian obat ini tidak dianjurkan (Syarif dan Elysabeth,
2008).
Dosis metronidazol perlu dikurangi pada pasien yang memiliki penyakit
obstruksi hati yang berat, sirosis hati dan gangguan fungsi ginjal yang berat. Dosis
metronidazol perlu disesuaikan pada pengguanaan bersama obat fenobarbital,
Sedangkan simetidin dapat menghambat metabolisme metronidazol di hati (Syarif
dan Elysabeth, 2008).
2.7 Kapsul
Kapsul dapat didefinisikan sebagai bentuk sediaan padat, dimana satu
macam obat atau lebih dan/atau bahan inert lainnya yang dimasukkan ke dalam
cangkang atau wadah kecil yang umumnya dibuat dari gelatin bisa lunak dan bisa
juga keras. Kebanyakan kapsul-kapsul yang diedarkan di pasaran adalah kapsul
yang semuanya dapat ditelan oleh pasien, untuk keuntungan dalam pengobatan.
Kapsul gelatin yang keras merupakan jenis yang digunakan oleh ahli farmasi
masyarakat dalam menggabungkan obat-obat secara mendadak dan di lingkungan
para pembuat sediaan farmasi dalam memproduksi kapsul pada umumnya (Ansel,
2008).
Kulit kapsul dibuat dari gelatin pelentur, dan air. Kulit kapsul dapat juga
mengandung bahan-bahan tambahan seperti pengawet, bahan pewarna dan bahan
pengeruh, pemberi rasa, gula, asam, dan bahan obat untuk mendapat efek yang
diinginkan. Plasticizier (pelentur) yang digunakan dengan gelatin pada pembuatan kapsul lunak relatif sedikit. Yang paling banyak adalah Gliserin USP, Sorbitol
USP, Pharmaceutical Grade Sorbitol Special, dan kombinasi-kombinasinya. Perbandingan berat plastisator kering terhadap gelatin kering menentukan
kekerasan kulit/cangkang gelatin, dengan anggapan tidak ada pengaruh dari bahan
yang dikapsulkan (Lachman, dkk., 2008). Gelatin bersifat stabil diudara bila
dalam keadaan kering, akan tetapi mudah mengalami peruraian oleh mikroba bila
menjadi lembap atau disimpan dalam larutan berair. Biasanya cangkang kaspul
lingkungan dengan kelembapan yang tinggi, penambahan uap air akan diabsorbsi
oleh kapsul dan kapsul keras ini akan rusak dari bentuk kekerasannya. Sebaliknya
dalam lingkungan udara yang sangat kering, sebagian dari uap air yang terdapat
dalam kapsul gelatin mungkin akan hilang, dan kapsul ini menjadi rapuh serta
mungkin akan remuk bila dipegang (Ansel, 2008). Laju pengeringan kapsul juga
mempengaruhi kekerasan dan kerapuhan kapsul, kemampuan pelarutan, dan
kecenderungan untuk melekat satu sama lain. Kondisi penyimpanan yang
direkomendasikan untuk bentuk sediaan kapsul berkisar 15 - 30oC dan 30 - 60%
kelembaban relatif (Margareth, et. al., 2009).
Cangkang kapsul keras gelatin harus dibuat dalam dua bagian yaitu badan
kapsul dan bagian tutupnya yang lebih pendek. Kedua bagian saling menutupi bila
dipertemukan, bagian tutup akan menyelubungi bagian tubuh secara tepat dan
ketat (Ansel, 2008).
2.8 Natrium Alginat
Alginat sangatlah berlimpah dialam indonesia karena alginat ini sebagai
kompoenen struktural yang terdapat dalam alga coklat (Phaeophyceae), yang
komponennya mencapai 40% dari bahan keringnya (Draget, et al., 2005)
Natrium Alginat merupakan produk pemurnian karbohidrat yang
diekstraksi dari alga coklat (Phaeophyceae) dengan menggunakan basa lemah.
Natrium alginat larut dengan lambat dalam air, membentuk larutan kental, tidak
larut dalam etanol dan eter. Alginat ini diperoleh dari spesies Macrocystis pyrifera, Laminaria, Aschophyllum dan Sargassum (Belitz, et. al., 2009).
japonica, Edonia maxima, Lessonia nigrescens, Durvillea antarctica, dan Sargassum sp (Draget, et al., 2005).
Tabel dibawah ini menunjukkan perbandingan asam uronat dalam
berbagai spesies alga yang berasal dari alam dan ditentukan dengan spektroskopi
NMR high-field.
Tabel 2.3 Perbandingan asam uronat dalam berbagai spesies alga (Draget, et al., 2005).
Source FG FM FGG FMM FGG,MG
Laminaria japonica 0.35 0.65 0.18 0.48 0.17
Laminaria digitata 0.41 0.59 0.25 0.43 0.16
Laminaria hyperborea, blade 0.55 0.45 0.38 0.28 0.17
Laminaria hyperborea, stipe 0.68 0.32 0.56 0.20 0.12
Laminaria hyperborea, outer cortex 0.75 0.25 0.66 0.16 0.09
Lessonia nigrescens 0.38 0.62 0.19 0.43 0.19
Ecklonia maxima 0.45 0.55 0.22 0.32 032
Macrocystis pyrifera 0.39 0.61 0.16 0.38 0.23
Durvillea antarctica 0.29 0.71 0.15 0.57 0.14
Ascophyllum nodosum, fruiting body 0.10 0.90 0.04 0.84 0.06
Ascophyllum nodosum, old tissue 0.36 0.64 0.16 0.44 0.20
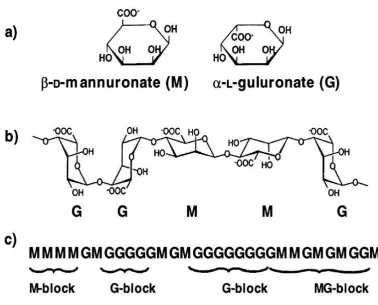
Asam alginat merupakan kopolimer biner yang terdiri dari residu β
-D-mannuronat (M) dan α-L-asam guluronat (G) yang tersusun dalam blok-blok yang
membentuk rantai linier (Grasdalen, et al., 1979). Kedua unit tersebut berikatan
pada atom C1 dan C4 dengan susunan homopolimer dari masing-masing residu
(MM dan GG) dan suatu blok heteropolimer dari dua residu (MG) (Thom, et al.,
1980).
Asam alginat tidak larut dalam air, karena itu yang digunakan dalam
dari natrium alginat adalah mempunyai kemampuan membentuk gel dengan
penambahan larutan garam-garam kalsium seperti kalsium glukonat, kalsium
tartrat dan kalsium sitrat. Pembentukan gel dengan ion kalsium, disebabkan oleh
adanya ikatan silang membentuk khelat antara ion kalsium dan anion karboksilat
pada blok G-G melalui mekanisme antar rantai. Natrium alginat mempunyai
rantai poliguluronat yang menunjukkan sifat pengikatan ion kalsium yang lebih
besar (Morris, et al., 1980).
Gambar 2.6 Struktur Alginat (a) monomer alginat (b) ikatan antar monomer (c) gambaran blok monomer alginat
Asam alginat bersifat asam, dan sering digunakan dalam granulasi asam
atau netral. Jika digunakan dalam garam basa atau garam asam organik, zat ini
cenderung membentuk alginat yang larut atau tidak larut yang mempunyai sifat
konsentrasi 1% sampai 5%, sedangkan natrium alginat digunakan antara 2,5%
sampai 10%. Asam alginat dan garamnya merupakan suatu kombinasi yang baik
dengan pengembangan yang cukup dengan kelekatan minimal dan konsentrasi
serendah mungkin antara 4% sampai 5% sudah memadai dalam memberikan sifat
pengembangan tersebut (Siregar dan Wikarsa, 2010).
Kelarutan alginat dalam air ditentukan dan dibatasi oleh tiga parameter
berikut, antara lain:
(i) pH pelarut merupakan parameter penting karena akan menentukan
adanya muatan elektrostatik pada residu asam uronat.
(ii) Kekuatan ionik total zat terlarut juga berperan penting (terutama efek
salting-out kation-kation non-gelling), dan
(iii) Kandungan dari ion-ion pembentuk gel dalam pelarut membatasi
kelarutan (Draget, et al., 2005).
Kegunaan alginat dan kemampuannya mengikat air bergantung pada
jumlah ion karboksilat, berat molekul dan pH. Kemampuan mengikat air
meningkat bila jumlah ion karboksilat semakin banyak dan jumlah residu kalsium
alginat kurang dari 500, sedangkan pH dibawah 3 terjadi pengendapan. Secara
umum, alginat dapat mengabsorpsi air dan dapat digunakan sebagai pengemulsi
dengan viskositas yang rendah (Zhanjiang, 1990).
Dilaboratorium Farmasi Fisik Fakultas Farmasi USU dalam beberapa
tahun terakhir telah dikembangkan kapsul yang tahan terhadap asam lambung.
Dimana cangkang kapsul tersebut dibuat dengan bahan dasar berupa natrium
alginat dengan kalsium klorida menggunakan cetakan. Telah terbukti bahwa
(pH 1,2). Utuhnya cangkang kapsul alginat di dalam medium lambung buatan pH
1,2 disebabkan komponen penyusun cangkang kapsul alginat yaitu kalsium
guluronat masih utuh (Bangun, dkk., 2005).
2.9 Uji Disolusi
Pelepasan obat dari bentuk sediaan dan absorbsi dalam tubuh dikontrol
oleh sifat fisika kimia dari obat dan bentuk yang diberikan, serta sifat-sifat fisika
kimia dan fisiologis dari sistem biologis. Konsentrasi obat, kelarutan dalam air,
ukuran molekul, bentuk kristal, ikatan protein, dan pKa adalah faktor-faktor fisiko
kimia yang harus dipahami untuk mendesain sediaan pelepasan terkontrol
(controlled release) atau terkendali (sustained release). Lepasnya suatu obat dari bentuk sediaan meliputi faktor disolusi atau difusi (Martin, dkk., 2008).
Disolusi merupakan percobaan secara in vitro yang mengukur kecepatan
dan tingkat kelarutan suatu obat di dalam medium air dimana di dalam obat
mengandung satu atau lebih bahan tambahan lainnya. Masalah bioavailabilitas
dapat ditemukan dalam metode disolusi ini. Akan tetapi, dalam percobaan disolusi
dapat dinyatakan masalah bioavailabilitas yang berbeda untuk setiap formulasi
obat (Shargel dan Yu, 1998).
Sejumlah metode untuk menguji disolusi secara in vitro telah dilakukan.
Bila suatu sediaan obat dimasukkan ke dalam beaker glass yang berisi air atau
dimasukkan ke dalam saluran cerna (saluran gastrointestin), obat tersebut mulai
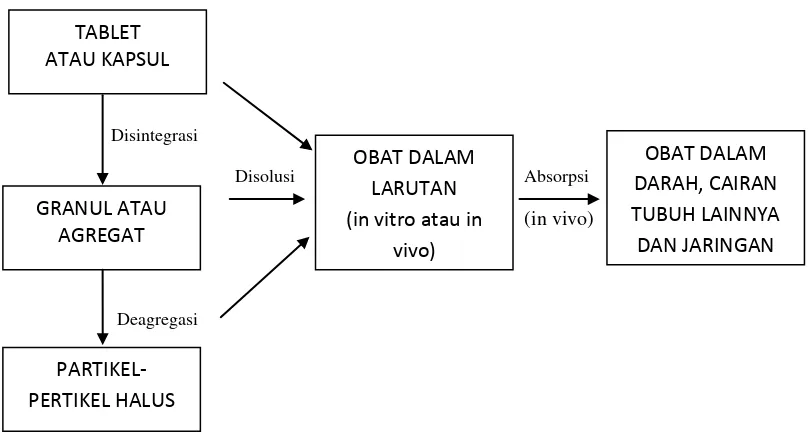
masuk ke dalam larutan dari bentuk padatnya. Disintegrasi, deagregasi dan
disolusi bisa berlangsung secara serentak dengan melepasnya suatu obat dari
bentuk dimana obat tersebut diberikan. Tahapan-tahapan ini dapat dilihat pada
Faktor-faktor yang mempengaruhi disolusi dibagi atas 3 kategori yaitu:
a. Faktor-faktor yang berhubungan dengan sifat fisikokimia obat, meliputi:
i. Efek kelarutan obat. Kelarutan obat dalam air merupakan faktor utama
dalam menentukan laju disolusi. Kelarutan yang besar menghasilkan laju
disolusi yang cepat.
ii. Efek ukuran parrtikel. Ukuran partikel berkurang dapat memperbesar luas
permukaan obat yang berhubungan dengan medium, sehingga laju disolusi
akan meningkat.
b. Faktor-faktor yang berhubungan dengan sediaan obat, meliputi:
i. Efek formulasi. Laju disolusi suatu bahan obat dapat dipengaruhi bila
dicampur dengan bahan tambahan. Bahan pengisi, pengikat dan
penghancur yang bersifat hidrofil dapat memberikan sifat hidrofil pada
bahan obat yang hidrofob, oleh karena itu disolusi bertambah. Sedangkan
bahan tambahan yang hidrofob dapat mengurangi laju disolusi. Hal ini
kaitannya dengan kelarutan bahan tambahan yang digunakan.
ii. Efek faktor pembuatan sediaan. Metode granulasi dapat mempercepat laju
disolusi obat-obat yang kurang larut. Penggunaan bahan pengisi yang
bersifat hidrofil seperti laktosa dapat menambah hidrofilisitas bahan aktif
dan dapat menambah laju disolusi.
c. Faktor-faktor yang berhubungan dengan uji disolusi, meliputi:
i. Tegangan permukaan medium disolusi. Tegangan permukaan mempunyai
pengaruh nyata terhadap laju disolusi bahan obat. Surfaktan dapat
menurunkan sudut kontak, oleh karena itu dapat meningkatkan proses
penetrasi medium disolusi ke matriks. Formulasi tablet dan kapsul
konvensional juga menunjukkan penambahan laju disolusi obat-obat yang
sukar larut dengan penambahan surfaktan ke dalam medium disolusi.
ii. Viskositas medium. Semakin tinggi viskostas medium, semakin kecil laju
disolusi bahan obat.
iii. pH medium disolusi. Larutan asam cenderung memecah tablet sedikit
lebih cepat dibandingkan dengan air, oleh karena itu akan mempercepat
laju disolusi (Gennaro, 2000).
United States Pharmacopeia (USP) XXI memberi beberapa metode resmi untuk melaksanakan uji pelarutan yaitu:
a. Metode Keranjang (Basket)
Metode keranjang terdiri atas keranjang silindrik yang ditahan oleh
tangkai motor. Keranjang menahan cuplikan dan berputar dalam suatu labu bulat
yang berisi media pelarutan. Keseluruhan labu tercelup dalam suatu bak yang
bersuhu konstan 37oC. Kecepatan berputar dan posisi keranjang harus memenuhi
kalibrasi pelarutan untuk meyakinkan bahwa syarat secara mekanik dan syarat
operasi telah dipenuhi.
b. Metode Dayung (Paddle)
Metode dayung terdiri dari suatu dayung yang dilapisi bahan khusus, yang
berfungsi memperkecil turbulensi yang disebabkan oleh pengadukan. Dayung
diikat secara vertikal ke suatu motor yang berputar dengan suatu kecepatan yang
terkendali. Tablet atau kapsul diletakkan dalam labu pelarutan yang beralas bulat
yang juga berfungsi untuk memperkecil turbulensi dari media pelarutan. Alat
ditempatkan dalam suatu bak air yang bersuhu konstan, seperti pada metode
basket dipertahankan pada suhu 37oC. Posisi dan kesejajaran dayung ditetapkan
dalam USP. Metode dayung sangat peka terhadap kemiringan dayung. Pada
beberapa produk obat, kesejajaran dayung yang tidak tepat secara drastis dapat
mempengaruhi hasil pelarutan. Standar kalibrasi pelarutan yang sama digunakan
untuk memeriksa peralatan sebelum uji dilaksanakan.
c. Metode Disintegrasi yang Dimodifikasi
Metode ini dasarnya memakai disintegrasi USP “Basket and Rack” dirakit untuk uji pelarutan. Bila alat ini dipakai untuk uji pelarutan maka cakram
dihilangkan. Saringan keranjang juga diubah sehingga selama pelarutan partikel
tidak akan jatuh melalui saringan. Metode ini jarang digunakan dan dimasukkan
dalam USP untuk suatu formulasi obat lama. Jumlah pengadukan dan getaran
membuat metode ini kurang sesuai untuk uji pelarutan yang tepat (Shargel dan