3 BAB II
TINJAUAN PUSTAKA
2.1 Biskuit
Menurut SNI 2973-2011 biskuit adalah produk makanan kering yang dibuat dengan cara memanggang adonan yang terbuat dari tepungterigu dengan atau substitusinya, minyak atau lemak dengan atau tanpa penambahan bahan pangan lain dan bahan tambahan pangan yang diizinkan.
Biskuit dapat dikelompokkan menjadi krekers, kukis, wafer dan pai. Krekers merupakan jenis biskuit yang dalam pembuatannya memerlukan proses fermentasi sehingga menghasilkan bentuk pipih bila dipatahkan dan penampangnya tampak berlapis-lapis.Kukis merupakan jenis biskuit yang dibuat dari adonan lunak, berkadar lemak tinggi, renyah dan apabila dipatahkan penampangannya bertekstur kurang padat. Wafer merupakan biskuit yang dibuat dari adonan cair, berpori-pori kasar, renyah dan jika dipatahkan penampang tampak berongga-rongga.Pai merupakan jenis biskuit yang berserpih (flaky) yang dibuat dari adonan dilapisi dengan lemak padat atau emulsi lemak sehingga mengembang selama pemanggangan dan bila dipatahkan penampangnya tampak berlapis-lapis (SNI, 2011).
4 2.1.1 Komposisi Kimia Biskuit
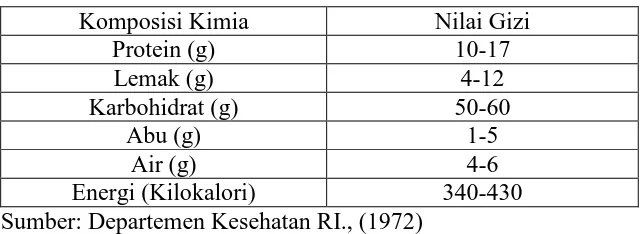
Komposisi kimia biskuit per 100 gram bahan dapat dilihat pada Tabel 2.1 Tabel 2.1 Komposisi kimia pada biskuit per 100 gram bahan
Komposisi Kimia Nilai Gizi
Protein (g) 10-17
Lemak (g) 4-12
Karbohidrat (g) 50-60
Abu (g) 1-5
Air (g) 4-6
Energi (Kilokalori) 340-430 Sumber: Departemen Kesehatan RI., (1972)
2.1.2 Bahan-bahan Pembuatan Biskuit
Menurut Fajar (2013) beberapa bahan yang digunakan dalam pembuatan biskuit yaitu tepung terigu, telur, gula, baking powder, garam, minyak/lemak, susu bubuk dan air.
1. Tepung terigu
Tepung terigu merupakan bahan utama dalam pembuatan biskuit. Prinsip penentuan penggunaan tepung terigu dalam pembuatan biskuit yaitu berdasarkan kualitas dan kuantitas protein dimana gluten akan terbentuk ketika tepung dicampur dengan air. Fungsi penggunaan tepung terigu untuk memberikan kualitas seperti rasa yang enak dan warna serta tekstur yang bagus.
2. Telur
5 3. Gula
Fungsi gula dalam pembuatan biskuit adalah sebagai pemberi rasa manis, pembentuk tekstur dan pemberi warna pada permukaan biskuit. Gula dalam adonan biskuit akan terlarut dan menyebar tergantung dari kandungan airnya. 4. Baking powder
Baking powder atau soda kue merupakan senyawa natrium bikarbonat
yang memiliki sifat sebagai bahan pengembang. Bahan pengembang adalah senyawa kimia yang apabila terurai akan menghasilkan gas dalam adonan. Kelebihan baking powder dalam pembuatan biskuit dapat mengakibatkan biskuit terasa asam, tekstur yang renyah dan warna yang kurang menarik.
5. Garam
Garam ditambahkan dalam makanan untuk memberi rasa, memperkuat tekstur dan mengikat air. Selain itu garam dapat membuat adonan tidak lengket dan tidak mengembang secara berlebihan.
6. Minyak/Lemak
Minyak/lemak berfungsi untuk melembutkan, membantu pengembangan, membantu penyebaran, memberikan rasagurih dan menambah aroma. Jenis lemak yang biasa digunakan berasal dari lemak susu (butter) atau dari lemak nabati (margarine).
7. Susu Bubuk
6 8. Air
Air berfungsi untuk melarutkan bahan-bahan lain agar bisa bercampur. Air yang ditambahkan kedalam adonan biskuit akan hilang selama proses pemanasan (pemanggangan).
2.1.3 Cara Pembuatan Biskuit
Menurut Muaris (2007) cara pembuatan biskuit meliputi beberapa proses yaitu :
1. Campurkan mentega, kuning telur, garam, gula lalu mixer sampai rata (adonan 1).
2. Campurkan tepung terigu, baking powder, susu bubuk lalu diayak (adonan 2). Adonan 1 dan adonan 2 dicampurkan lalu tambahkan air dan diadoni selama 15 menit.
3. Adonan dipipihkan kemudian dicetak sesuai selera dan letakkan adonan yang telah dibentuk dalam loyang yang sudah diolesi mentega. Panggang adonan hingga matang.
7 2.1.4 Persyaratan Mutu Biskuit
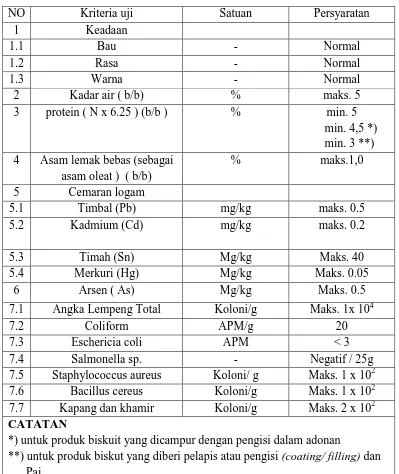
Persyaratan mutu biskuit dapat dilihat pada Tabel 2.2 Tabel 2.2 Persyaratan mutu biskuit
NO Kriteria uji Satuan Persyaratan
1 Keadaan
1.1 Bau - Normal
1.2 Rasa - Normal
1.3 Warna - Normal
2 Kadar air ( b/b) % maks. 5
3 protein ( N x 6.25 ) (b/b ) % min. 5 min. 4,5 *)
min. 3 **) 4 Asam lemak bebas (sebagai
asam oleat ) ( b/b)
% maks.1,0
5 Cemaran logam
5.1 Timbal (Pb) mg/kg maks. 0.5
5.2 Kadmium (Cd) mg/kg maks. 0.2
5.3 Timah (Sn) Mg/kg Maks. 40
5.4 Merkuri (Hg) Mg/kg Maks. 0.05
6 Arsen ( As) Mg/kg Maks. 0.5
7.1 Angka Lempeng Total Koloni/g Maks. 1x 104
7.2 Coliform APM/g 20
7.3 Eschericia coli APM < 3
7.4 Salmonella sp. - Negatif / 25g
7.5 Staphylococcus aureus Koloni/ g Maks. 1 x 102 7.6 Bacillus cereus Koloni/g Maks. 1 x 102 7.7 Kapang dan khamir Koloni/g Maks. 2 x 102 CATATAN
*) untuk produk biskuit yang dicampur dengan pengisi dalam adonan
**) untuk produk biskut yang diberi pelapis atau pengisi (coating/ filling) dan Pai
8 2.2 Protein
Istilah protein berasal dari kata Yunani proteos, yang berarti ‘‘yang utama’’ atau ‘‘yang didahulukan’’. Kata ini diperkenalkan oleh seorang ahli kimia Belanda, Gerardus Mulder (1802-1880) ia berpendapat bahwa protein adalah zat yang paling penting pada setiap organisme. Protein adalah molekul makro yang mempunyai berat lima ribu hingga beberapa juta. Unsur nitrogen adalah unsur utama proteinkarena terdapat di dalam di dalam semua protein, akan tetapi tidak terdapat di dalam karbohidrat dan lemak.Molekul protein merupakan rantai panjang yang tersusun oleh rantai-rantai asam amino. Asam amino terdiri atas atom karbon yang terikat pada satu gugus karboksil (–COOH), satu gugus amino (–NH2) yang salah satunya terletak pada atom C tepat disebelah gugus karboksil (atom C alfa). Asam-asam amino dengan gugus amino dari asam amino yang disampingnya (Almatsier, 2001).
2.2.1 Struktur Protein
Menurut Girindra (1986) struktur protein dapatdibagimenjadibeberapabentukyaitustruktur primer, sekunder, tersierdankuarterner.
1. Struktur Primer
Susunan linier asam amino dalam protein merupakanstruktur primer.Susunantersebutmerupakansuaturangkaiandariasam amino yang
menentukansifatdasardariberbagai protein
9 2. StrukturSekunder
Struktursekunder protein adalahstrukturduadimensidari
protein.Padastrukturiniterjadilipatanberaturanseperti α-heliksdan β-sheet,
akibatadanyaikatanhidrogen di antaragugus-gugus polar dariasam amino dalamrantai protein.
3. StrukturTersier
Dalamhalinirantaipolipeptidacenderunguntukmembelitataumelipatmemben tukstruktur yang kompleks.Kestabilanstrukturinibergantungpadagugus R padasetiapasam amino yang membentuknyadandistabilkanolehikatanhidrogen, ikatandisulfit daninteraksihidrofobik.
4. StrukturKuarterner Molekulprotein
initerbentukdaribeberapatersierdanbiasaterdiridariprotomer yang samaatauprotomer yang berlainan. Protein yang dibentukolehprotomer yang
samadisebuthomogenus. Jikaterdiridariprotomerberlainandisebutheterogenus. 2.2.2 Karakteristik Protein
10
Protein sangat cenderung mengalami beberapa bentuk perubahan yang dinyatakan sebagai denaturasi.Denaturasi protein adalah perubahan struktur sekunder, tersier dan kuartener tanpa diikuti oleh struktur primer. Denaturasi terjadi pada suhu 50-60℃ dan 10-15℃. Pada suhu yang tinggi maka protein mengalami perubahan fisik. Salah satu sifat yang tampak adalah kelarutannya yang menurun(Martoharsono, 1988).
2.2.3 Fungsi Protein
Menurut Budiyanto (2004)protein mempunyai fungsi bagi tubuh yaitu : 1. Pertumbuhan dan pemeliharaan tubuh. Pertumbuhan berarti penambahan sel
atau jaringan dan pemeliharaan yaitu mengatur sel-sel yang rusak serta pembentukan senyawa-senyawa penting tubuh, seperti hormon dan enzim. 2. Pembentukan antibodi tubuh, yaitu zat yang digunakan untuk memerangi
organisme atau bahan asing yang masuk ke dalam tubuh seperti virus dan bakteri.
3. Berperan dalam pengangkutan zat gizi, yakni pengangkutan dari saluran cerna ke dalam darah dan dari darah ke ke jaringan-jaringan serta ke sel-sel. 4. Sumber energi, protein merupakan sumber energi tubuh. Jika tubuh
kekurangan energi, fungsi protein sebagai pembangun untuk menyediakan energi.
2.3Metode Penetapan Kadar Protein
11
Menurut SNI 2973-2011 prinsippenetapankadar protein adalahsenyawa nitrogen diubahmenjadi ammonium sulfatolehasamsulfatpekat, kemudiandiuraikandengannatriumhidroksida. Ammoniayang di bebaskandiikatdenganasamboratdankemudiandititardenganlarutanbakuasam.
Kadar protein diperolehdarihasil kali total nitrogen dengan 6,25.
AnalisisdenganmetodeKjeldahlpadadasarnyadapatdibagimenjaditigatahapy aitu proses destruksi, proses destilasidantahaptitrasi. Pada proses
destruksisampeldipanaskandalamasamsulfatpekatsehinggamenjadiunsur-unsurnya. Elemenkarbondanhidrogenteroksidasimenjadi CO, CO2dan H2O. Nitrogen akanberubahmenjadi (NH4)2SO4. UntukmempercepatreaksidapatditambahkankatalissepertiHgOdan Na2SO4, K2SO4atau
CUSO4.Denganpenambahankatalistitikdidihasamsulfatakannaiksehinggadestruksib erjalancepat. Selenium jugaseringdigunakansebagaikatalisuntukmempercepat proses oksidasi(Sudarmadji, dkk., 1989).
Padatahapdestilasi, ammonium sulfatdipecahmenjadi ammonia denganpenambahannatrium hidroksidasampai alkalis dandipanaskan. Ammonia yang dibebaskanselanjutnyaakanditangkapolehlarutanasamstandar, asamstandar yang digunakanadalahasamkloridaatauasamborat 4%. Destilasidiakhiribilasemua ammonia
12
Pada tahap titrasi apabila penampung destilat asam borat berlebih, maka asam borat yang bereaksi dengan ammonia dapat diketahui dengan dititrasi menggunakan asam klorida 0,1 N dengan indikator campuran metil merah dan metil biru, selisih jumlah titrasi sampel dan blanko merupakan jumlah ekuivalen nitrogen (Sudarmadji, dkk., 1989).
2. Metode Spektrofotometer
Kebanyakan protein mengabsorbansi sinar ultraviolet maksimum pada 200 nm. Hal ini terutama oleh adanya asam amino tirosin trip-tophan dan fenilalanin yang ada pada protein tersebut. Pengukuran protein berdasarkan absorbsi sinar ultraviolet cepat, mudah dan tidak merusak bahan (Sudarmadji, dkk., 1989).
3. Metode Lowry
Konsentrasi protein diukur berdasarkan optical density (OD) pada panjang gelombang 600 nm. Untuk mengetahui banyaknya protein dalam larutan, lebih dahulu dibuat kurva standar yang melukiskan hubungan antara konsentrasi dengan OD. Larutan Lowry ada dua macam yaitu larutan A yang terdiri dari fosfoturigstat-fosfomolibdat (1:1) dan larutan Lowry b yang terdiri dari Na2CO32% dalam NaOH 0,1 N, CuSO4 dan Na-K-tartrat 2%. Cara penetapannya adalah sebagai berikut: 1 ml larutan protein ditambahkan 5 ml Lowry B, digojok dan dibiarkan selama 10 menit. Kemudian ditambahkan 0,45 ml Lowry Adigojok dan biarkan 20 menit, selanjutnya diamati OD nya pada panjang gelombang 600 nm (Sudarmadji, dkk., 1989).