Jurusan Kimia FMIPA Universitas Negeri Surabaya, 20 September 2014
B - 111
PREPARASI, MODIFIKASI DAN KARAKTERISASI KATALIS Ni/ZSiA (PREPARATION, MODIFICATION AND CHARACTERIZATION CATALYST Ni/ZSiA)
D. Setyawan Purwo Handoko
FMIPA Kimia Universitas Jember Jl. Kalimantan 25 Jember Jawa Timur
Email : kreka_zeolit@yahoo.com atau desetyawanpeha@gmail.com
Abstrak. Modifikasi dan karakterisasi terhadap katalis Ni/ZSiA yang dipreparasi dari zeolit alam telah dilakukan. Katalis ZSiA dibuat melalui pencucian zeolit alam dengan akuades, perendaman dengan larutan HCl 2 M, penambahan Na2SiO3 5 % b/b, perendaman dengan
larutan NH4Cl 2 M, kalsinasi pada temperatur 500 o
C sambil dialiri gas nitrogen selama 2 jam dengan laju alir nitrogen 20 mL/menit, oksidasi sambil dialiri oksigen selama 2 jam dengan laju alir oksigen 20 mL/menit dan impregnasi logam Ni ke permukaan sampel katalis dengan menggunakan logam Ni(NO3)2٠6H2O 2 % b/b. Selanjutnya dilakukan reduksi sambil dialiri
gas hidrogen dengan laju alir 20 mL/menit selama 2 jam. Katalis hasil dianalisis terhadap kandungan kation logam dengan AAS, keasaman dengan metode gravimetri, luas permukaan spesifik dengan surface area analyzer NOVA 1000 dan kristalinitas dengan difraktometer sinar-X (XRD, shimadzu-6000). Perlakuan asam pada zeolit alam mengakibatkan terjadinya peristiwa pelepasan logam Ca dan Fe yang terdapat dalam zeolit alam sehingga zeolit mengalami peningkatan keasaman. Disamping itu, perlakuan asam pada zeolit alam juga mengakibatkan terjadinya peristiwa dealuminasi sehingga meningkatkan rasio Si/Al zeolit dan secara kuantitas meningkatkan jumlah pada pori 10 hingga 20 angstrom.
Kata kunci : zeolit, rasio Si/Al, keasaman, pori-pori
ABSTRACT. Modification and characterization of the catalyst Ni / ZSiA are prepared from natural zeolite have been carried out. ZSiA catalyst was prepared by washing zeolite with aquadest, followed by dipping in HCl 2M solution, adding Na2SiO3 5% b/b, dipping in NH4Cl
2M, calcination at 500 oC under nitrogen with flow rate of 20 mL/min for 2 hours, oxydation under oxygen flow rate of 20 mL/min and impregnation of Ni metal into catalyst surface using Ni(NO3)2٠6H2O 2% b/b. The catalyst was then oxydized under oxygen flow rate of 20 mL/min
for 2 hours and reduced under hydrogen flow rate of 20 mL/min for 2 hours. Characterization of the catalyst included determination of metal content using AAS, acidity using gravimetric method, surface area using Gas Sorption Analyzer NOVA 1000, and crystallinity using XRD.
Acid treatment on natural zeolite resulted in the release events Ca and Fe metals contained in the natural zeolite that zeolite acidity increased. In addition, the acid treatment also resulted in a natural zeolite dealumination events thus increasing the Si / Al ratio of zeolite and the quantity increases in the number of pores of 10 to 20 angstroms.
Jurusan Kimia FMIPA Universitas Negeri Surabaya, 20 September 2014
B - 112 PENDAHULUAN
Hubungan antara temperatur dengan tekanan uap adsorbat pada kesetimbangan antara fasa terkondensasi (teradsorpsi) dengan fasa fluida dapat dijelaskan dengan persamaan Clausius-Clapeyron (Gaser, 1987) sebagai berikut :
2 ln RT L dT P d
dimana P adalah tekanan uap dan L adalah entalpi penguapan adsorbat. Untuk sistem kesetimbangan cair-uap, L adalah panas penguapan dari proses penguapan (evaporasi). Proses tersebut seringkali disebut sebagai persamaan Clausius-Clapeyron. Jika persamaan tersebut diterapkan pada kesetimbangan antara adsorbat teradsorpsi dan gas, maka persamaan tersebut harus dimodifikasi sehingga perubahan entalpi bukan dalam konstanta pada
umumnya, tetapi bergantung pada fraksi penutupan pada permukaan,
coverage (). Keadaan ini biasanya
untuk mendifinisikan saat membahas entalpi adsorpsi. Perubahan entalpi pada nilai tertentu disebut entalpi adsorpsi isosterik, Hist. Dengan asumsi bahwa Hist
adalah tidak bergantung pada temperature (pada rentang yang kecil), sehingga persamaan hubungan antara tekanan dengan temperatur pada fraksi penutupan permukaan tertentu adalah sebagai berikut ,
2 1 1 2 1 1 ln T T R H P P ist Banyaknya adsorbat teradsorpsi atau fraksi penutupan permukaan sebagai fungsi tekanan pada dua temperatur, T1 dan T2 akan
dihasilkan kurva yang disajikan pada Gambar 1.
Jurusan Kimia FMIPA Universitas Negeri Surabaya, 20 September 2014
B - 113
Gambar 1. Adsorpsi, (a) isotermis, (b) isobar (Satterfield, 1980)
Dari Gambar 1 (a) dapat ditunjukkan bahwa semakin tinggi temperatur semakin besar tekanan yang dibutuhkan untuk menghasilkan fraksi penutupan permukaan dengan nilai tertentu (θ = x, dimana 0 < x < 1) dan panas adsorpsi ditentukan sebagai fungsi .
Menurut Gasser (1987), fraksi penutupan pada permukaan, ditentukan pada tekanan yang konstan dan pada temperatur yang bervariasi. Panas adsorpsi isosterik ditentukan dari kurva isobar dengan membaca hubungan P dan T pada harga tertentu. Dengan demikian dapat disimpulkan bahwa Hist = f
(P,T) . Pada adsorpsi isobar berlaku
bahwa = f (T)P dan adsorpsi
isotermis = f (P)T dimana,
kapasitas
jumlah
adsorben
permukaan
pada
situs
jumlah
si
mengadsorp
yang
situs
jumlah
Interaksi antara adsorbat – adsorben dengan gaya Van der Waals antara molekul gas dengan permukaan katalis disebut fisisorpsi. Fisisorpsi yang berlanjut sehingga melibatkan orbital elektron untuk membentuk suatu ikatan pada permukaan katalis maka akan menghasilkan kemisorpsi. Dasar dari pengukuran luas permukaan suatu padatan (katalis) adalah fisisorpsi yang merupakan dasar dari prosedur BET, dimana secara umum digunakan untuk menentukan luas permukaan suatu padatan (LPP).
Jurusan Kimia FMIPA Universitas Negeri Surabaya, 20 September 2014
B - 114
Gambar 2. Penentuan volume lapis tunggal pada permukaan padatan (Augustine, 1996)
Pada Gambar 2, dapat dijelaskan bahwa pada keadaan awal, perubahan tekanan yang sangat sedikit menyebabkan peningkatan volume gas (nitrogen) yang teradsorpsi. Volume lapis tunggal adsorpsi dapat ditentukan melalui ekstrapolasi bagian multilayer dari kurva hingga saat tekanan relatif mendekati nol.
Persamaan BET menurut Augustine (1996), adalah sebagai berikut:
m m o o ads P P C V C C V P P V P . . 1 . 1 ) (
dimana Vads = volume gas
teradsorp pada tekanan P
Po = tekanan uap
jenuh
Vm = Volume gas
teradsorp pada fraksi penutupan permukaan
monolayer C = konstanta BET yang berhubungan dengan entalpi adsorpsi
dan entalpi penguapan
dengan membuat grafik hubungan
antara ) ( 0 P P V P o ads lawan
oP
P
.
maka akan diperoleh garis lurus dengan, Slope (S) = . . 1 C V C m
, dan Intersep (I)
= C Vm 1 , maka Vm = ( S + I ) -1
Luas permukaan yang diperoleh melalui metode BET dinyatakan dalam m2/g. Diketahui bahwa N(bilangan Avogadro) = 6,02.1023 molekul dan Am
adalah luas penampang lintang molekul adsorbat nitrogen yaitu 16,2 Å persegi dan V volume molar adsorbat. Maka Luas permukaan padatan ditentukan sebagai berikut,
LPP = Vm . N . Am . 10
V ( )
METODOLOGI
Preparasi Katalis Ni/ZSiA
Zeolit dengan ukuran lolos 100 mesh direndam dalam akuades dan dicuci sambil diaduk. Kemudian direndam dengan HF 2 % selama 30 menit selanjutnya dicuci dengan akuades diulang hingga 3 kali, kemudian dikeringkan dalam oven pada temperatur 120 oC selama 3 jam.
Jurusan Kimia FMIPA Universitas Negeri Surabaya, 20 September 2014 [Type text]
B - 115
Selanjutnya dioksidasi dengan oksigen pada temperatur 500 oC selama 2 jam dan dikalsinasi dengan nitrogen pada temperatur 500 oC selama 2 jam dengan laju alir gas 20 mL/menit sehingga diperoleh katalis Z (Handoko, 2001).
Selanjutnya katalis Z dicuci dengan menggunakan larutan HCl 2 M dengan perbandingan volume antara zeolit : larutan HCl = 1 : 2, sambil diaduk selama 20 hingga 30 menit (Zhang, 1999). Selanjutnya sampel zeolit dicuci dengan menggunakan akuades hingga pH = 6 dan dikeringkan dalam oven pada temperatur 120 oC selama 3 jam dan dilanjutkan dengan oksidasi menggunakan gas oksigen dengan laju alir 20 mL/menit pada temperatur 500 oC selama 2 jam dan kalsinasi dengan gas nitrogen dengan laju alir 20 mL/menit pada temperatur 500 oC selama 2 jam. Kemudian ke dalam katalis Z dalam gelas beker ditambahkan Na-Silikat (Na2SiO3)
sebanyak 5 % (w/w) yang dilarutkan ke dalam akuades dan selanjutnya dipanaskan pada temperatur antara 80 oC hingga 90 oC selama 24 jam sambil diaduk menggunakan pengaduk magnet. Kemudian sampel
didinginkan dan dilanjutkan oksidasi dengan gas oksigen pada temperatur 500 oC selama 2 jam dengan laju alir gas 20 mL/menit dan diteruskan kalsinasi dengan gas nitrogen pada temperatur 500 oC selama 2 jam dengan laju alir gas 20 mL/menit sehingga diperoleh katalis ZSi.
Katalis ZSi didinginkan dan ditambahkan larutan NH4Cl 2 M ke
dalam gelas beker dengan perbandingan 1 : 2 (v/v) dan campuran dipanaskan kembali pada temperatur 90 oC selama 4 jam dengan pengaduk magnet (Zhang, 1999). Kemudian didinginkan dan dilanjutkan dengan proses oksidasi menggunakan gas oksigen pada temperatur 500 oC selama 2 jam dengan laju alir gas 20 mL/menit dan diteruskan kalsinasi dengan gas nitrogen pada temperatur 500 oC selama 2 jam dengan laju alir gas 20 mL/menit sehingga diperoleh katalis
ZSiA.
Impregnasi logam Ni (Ni 2 % (w/w)) pada permukaan katalis ZSiA dilakukan dengan metode impregnasi basah (wet impregnation). Garam Ni(NO3)2٠6H2O sebanyak 9,91 g
dilarutkan ke dalam 100 mL akuades sambil diaduk hingga homogen,
Jurusan Kimia FMIPA Universitas Negeri Surabaya, 20 September 2014 [Type text]
B - 116
selanjutnya ditambahkan sampel (katalis ZSiA) sebanyak 100 g. Kemudian dipanaskan dan diuapkan pada temperatur 80 oC hingga 90 oC (pada 1 atm) sambil diaduk sehingga komponen air secara perlahan-lahan akan teruapkan. Setelah komponen air teruapkan kemudian sampel dimasukkan ke dalam oven pada temperatur 120oC selama 2 jam dan dilanjutkan proses oksidasi dengan gas oksigen pada temperatur 500 oC selama 2 jam dengan laju alir gas 20 mL/menit dan reduksi pada temperatur 500 oC dengan gas hidrogen yang dialirkan 20 mL/menit sehingga diperoleh katalis Ni/ZSiA (Handoko, 2001).
Setiap tahap perlakuan dilakukan analisis kandungan logam dengan AAS, keasaman dengan metode gravimetri, kristalinitas dengan XRD dan luas permukaan dengan menggunakan metode BET.
HASIL PENELITIAN DAN PEMBAHASAN
Hasil Karakterisasi Katalis
Katalis Ni/ZSiA dipreparasi melalui beberapa tahap perlakuan yaitu: perlakuan asam, perlakuan
dengan Na2SiO3, perlakuan
hidrotermal, kalsinasi, oksidasi, reduksi dan impregnasi Ni. Pada masing-masing tahap perlakuan dilakukan analisis kandungan logam dengan AAS, keasaman dengan metode gravimetri, kristalinitas dengan XRD dan luas permukaan dengan menggunakan metode BET.
Kristalinitas Katalis
Menurut Harber (1991), persyaratan material zeolit sebagai katalis yaitu luas permukaan, rasio Si/Al, keasaman, kandungan kation dan kristalinitas. Sifat tersebut sangat berhubungan dengan jari-jari pori, volume pori dan keasaman yang terdapat dalam zeolit. Kristalinitas zeolit merupakan suatu ukuran kekuatan kisi kristal dalam mempertahankan bentuk kristalnya. Sifat kristal zeolit dapat juga berpengaruh terhadap kemampuannya dalam proses adsorpsi. Jika suatu zeolit memiliki sifat kristal yang rendah maka kisi kristal zeolit tersebut akan mudah rusak dan akan menyebabkan penyumbatan terhadap mulut pori, pengurangan volume pori, penurunan jumlah asam. Akibat lebih jauh maka
Jurusan Kimia FMIPA Universitas Negeri Surabaya, 20 September 2014 [Type text]
B - 117
zeolit tersebut akan mengalami penurunan aktivitasnya sebagai
katalis.
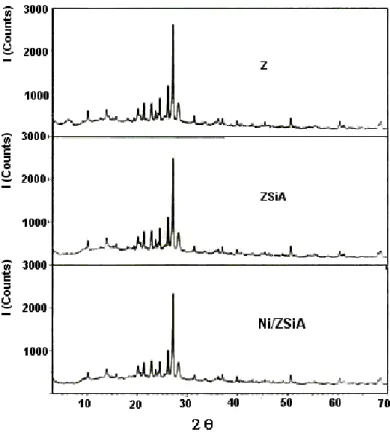
Gambar 3. Difraktogram katalis Z, ZSiA, Ni/ZsiA
Metode yang digunakan untuk menganalisis struktur kristal katalis yang dibuat adalah difraksi sinar-X (XRD). Prinsip dasar analisis kimia yang digunakan dalam XRD adalah jarak antar bidang (d) yang karakteristik. Posisi sudut difraksi (2) dan jarak antar bidang menggambarkan jenis kristal, sedangkan intensitas menunjukkan kristalinitas suatu padatan (West, 1984; Sibilia, 1996).
Berdasarkan Tabel 1 dapat disimpulkan bahwa zeolit alam yang dipakai sebagai pengemban logam aktif Ni (ZSiA) mempunyai kandungan tipe campuran antara lain mordenit, klinoptilolit dan kuarsa. Keadaan tersebut dibuktikan dengan mencocokkan pola difraktogram XRD dari zeolit alam standar menurut Treacy dan Higgins (2001), dengan zeolit alam sampel.
Jurusan Kimia FMIPA Universitas Negeri Surabaya, 20 September 2014
B - 118
Tabel 1. Identifikasi posisi sudut difraksi (2θ) pada difraktogram XRD katalis yang dibuat dengan zeolit alam standar
Jenis zeolit
2θ
Zeolit alam sampel Zeolit alam menurut Treacy dan Higgins (2001) Mordenite 6,54; 13,81; 18,03; 24,42; 25,64; 25,99; 27,00; 35,58; 36,90; 39,83; 45,33; 47,91; dan 48,70 6,51; 13,83; 18,19; 24,43; 25,63; 26,04; 27,09; 35,61; 36,87; 39,82; 45,28; 47,97; dan 48,70 Clinoptilolite 19,19; 20,40; 22,38; 25,32; 25,99; 28,08; 29,81; 36,22; 45,34; dan 48,92 19,10; 20,40; 22,36; 25,35; 26,04; 28,15; 29,79; 36,19; 45,38; dan 48,92
Quartz 20,86; dan 26,70 20,86; dan 26,65
Berdasarkan Tabel 2 terlihat bahwa katalis hasil mengalami peningkatan intensitas dari Z menjadi ZSiA, keadaan ini disebabkan adanya proses aktivasi dengan larutan HCl dan NH4Cl, penambahan Na2SiO3
serta pemanasan pada temperatur 500 oC. Keadaan tersebut berdampak pada peningkatan kristalinitasnya, yaitu 300, 1429, 259 menjadi 342, 1560 dan 284.
Tabel 2 Intensitas difraktogram dengan puncak terbesar dari katalis hasil 2θ (derajat) d (Å) Jenis Intensitas (counts) Z ZSiA Ni/ZSiA 24,39 2,26 Mordenite 300 342 264 25,99 2,99 Clinoptilolite 472 - - 26,70 3,18 Quartz 270 200 164 27,00 3,30 Mordenite 1429 1560 1411 28,08 3,34 Clinoptilolite 259 284 253 29,82 3,43 Clinoptilolite 192 - - 39,83 3,65 Mordenite 161 95 105
Pada saat impregnasi logam Ni dengan garam Ni(NO3)2٠6H2O
menyebabkan sifat kristal zeolit menjadi turun, yaitu 200, 1560 dan 284 menjadi 164, 1411 dan 254. Zeolit alam yang digunakan sebagai katalis
setelah dibandingkan dengan zeolit alam standar menurut Treacy dan Higgins (2001) memiliki indeks kemiripan dengan jenis mordenite,
clinoptilolite dan quartz, sehingga
Jurusan Kimia FMIPA Universitas Negeri Surabaya, 20 September 2014 [Type text]
B - 119
struktur kristal jenis mordenite, clinoptilolite dan quartz.
Kandungan Logam dalam Katalis Hasil
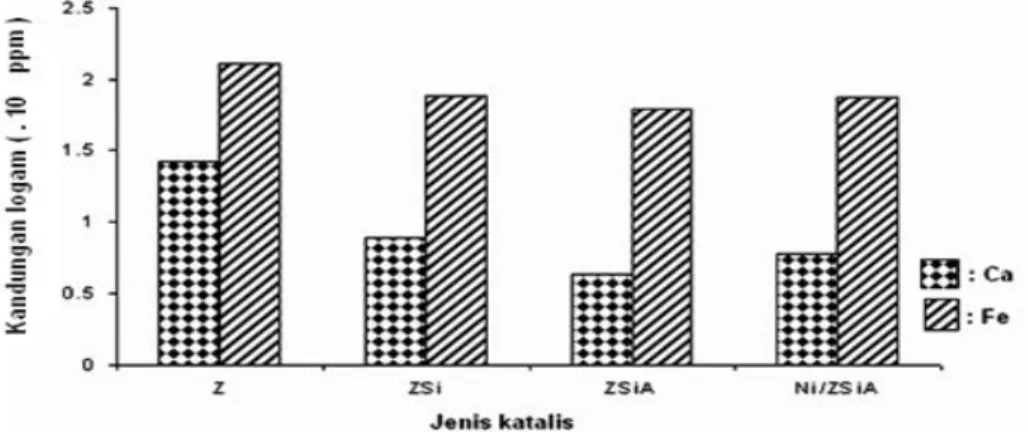
Pada perlakuan kalsinasi dan pengayaan Si terhadap zeolit hingga perlakuan asam terjadi penurunan kandungan logam Ca dan Fe. Pada katalis Ni/ZSiA terjadi peningkatan kandungan Ca dan Fe meskipun relatif sangat sedikit tetapi tidak terlalu signifikan.
Ketika perendaman dan pengadukan saat impregnasi logam Ni dari garam Ni(NO3)2٠6H2O tersebut
terjadi peningkatan logam Ca dan Fe. Peningkatan yang relatif sedikit tersebut kemungkinan disebabkan saat impregnasi logam Ni dari garam Ni(NO3)2٠6H2O digunakan pelarut air
yang mengandung Ca dan Fe sehingga logam Ca dan Fe teradsorpsi kembali oleh zeolit meskipun relatif sangat sedikit.
Gambar 4. Kandungan logam Ca dan Fe dari berbagai jenis katalis , Z : katalis zeolit, ZSi : katalis zeolit pengkayaan dengan Si (Na2SiO3), ZSiA : katalis ZSi yang diberi perlakuan asam,
Ni/ZSiA : katalis ZSiA yang diimpregnasi logam Ni Selain alasan tersebut,
kemungkinan yang lain adalah karena garam Ni(NO3)2٠6H2O pada bahan
dasarnya mengandung Ca sebanyak 50 mg/kg dan Fe sebanyak 50 mg/kg, sehingga saat impregnasi logam Ni dari garam Ni(NO3)2٠6H2O kandungan
Ca dan Fe dalam zeolit menjadi naik kembali.
Keasaman Katalis Hasil
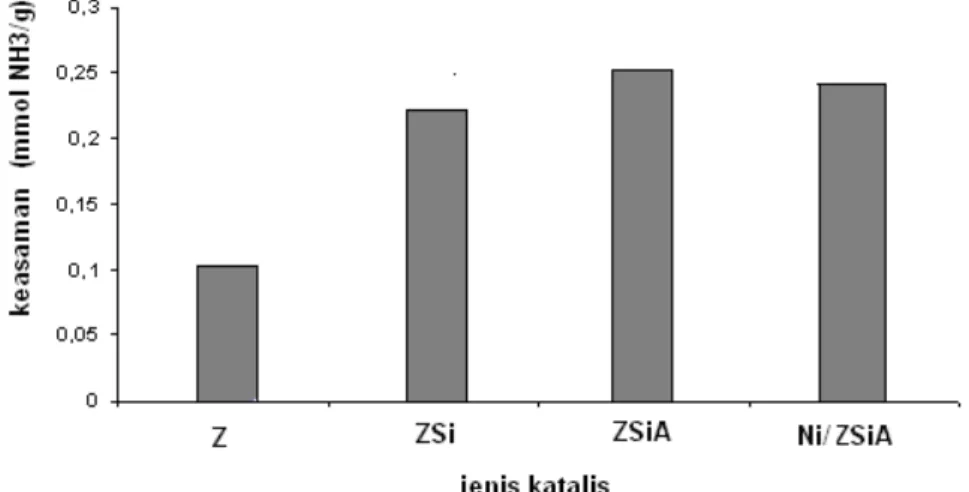
Berdasarkan Gambar 5 dapat dijelaskan bahwa keasaman meningkat mulai dari perlakuan dengan Na2SiO3 hingga perlakuan
asam. Peningkatan keasaman tersebut mengindikasikan terjadi pembentukkan situs asam Bronsted
Jurusan Kimia FMIPA Universitas Negeri Surabaya, 20 September 2014 [Type text]
B - 120
pada permukaan zeolit melalui pertukaran ion. Pengukuran keasaman zeolit dilakukan dengan metode adsorpsi basa amoniak pada permukaan katalis.
Menurut Satterfield (1980) dan Van Santen (1995), keasaman (acid
amount) suatu katalis didefinisikan
sebagai banyaknya mmol basa
(amoniak) yang teradsorpsi oleh situs asam Bronsted maupun situs asam Lewis per gram pada permukaan katalis. Semakin banyak basa amoniak yang dapat teradsorpsi pada permukaan katalis maka keasaman katalis semakin tinggi, menurut Satterfield (1980),
Gambar 5. Keasaman beberapa katalis hasil
Z : katalis zeolit, ZSi : katalis zeolit pengkayaan dengan Si, ZSiA : katalis ZSi yang diberi perlakuan asam, Ni/ZSiA : katalis ZSiA yang diimpregnasi logam Ni
Rasio Si/Al dan Dealuminasi Katalis Hasil
Peningkatan rasio Si/Al menggambarkan adanya pelepasan Al dalam framework (Al framework) menjadi Al diluar framework.
Keberadaan Al dalam kerangka zeolit membawa muatan negatif yang distabilkan dengan keberadaan ion
logam seperti Na+, Ca2+, K+, Mg2+, Fe3+ atau ion H+, sehingga saat perlakuan asam terhadap zeolit baik dengan HF maupun dengan HCl disamping menyebabkan keluarnya Al
framework menjadi Al diluar
framework juga berdampak secara
langsung terhadap peristiwa berkurangnya kandungan ion logam
Jurusan Kimia FMIPA Universitas Negeri Surabaya, 20 September 2014 [Type text]
B - 121
yang terdapat dalam zeolit. Peningkatan rasio Si/Al menyebabkan zeolit semakin bersifat non polar dan zeolit yang semakin bersifat non polar akan lebih mudah berinteraksi dengan senyawa-senyawa non polar (Twaiq, 2003).
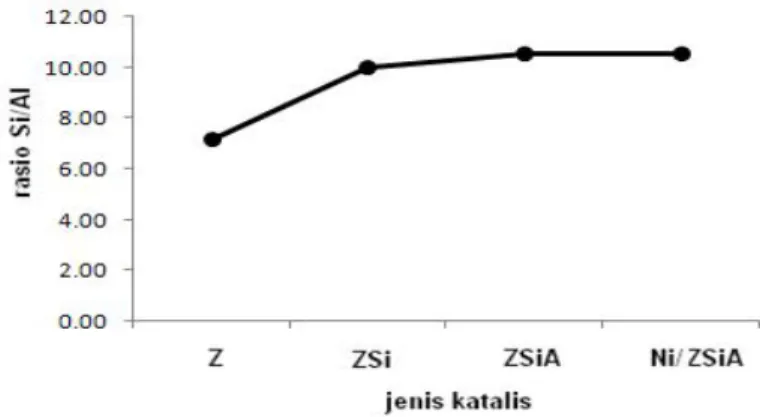
Rasio Si/Al pada jenis katalis Ni/ZSiA mengalami penurunan sedikit, tetapi tidak signifikan (0,19 %). Kemungkinan yang terjadi adalah saat
impregnasi logam Ni dari garam Ni(NO3)2٠6H2O relatif tidak terjadi
perubahan kandungan Si dan relatif tidak terjadi perubahan kandungan Al, sehingga kandungan rasio Si/Al dari Ni/ZSiA relatif tetap. Pada perlakuan penyisipan logam Si dari jenis katalis Z sehingga menjadi ZSi terjadi peningkatan rasio Si/Al sebesar 40,17 %
Gambar 6. Rasio Si/Al dari berbagai jenis katalis, Z : katalis zeolit, ZSi : katalis zeolit pengkayaan dengan Si, ZSiA : katalis ZSi yang diberi perlakuan asam, Ni/ZSiA : katalis ZSiA yang diimpregnasi logam Ni
Jurusan Kimia FMIPA Universitas Negeri Surabaya, 20 September 2014 [Type text]
B - 122
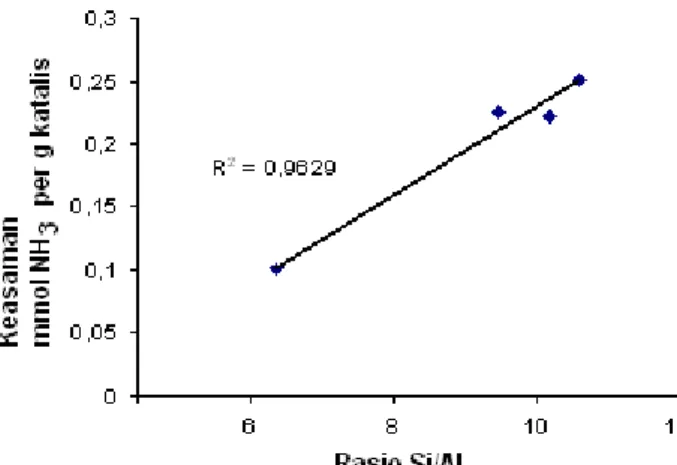
Gambar 7. Hubungan antara keasaman dan rasio Si/Al katalis
Semakin tinggi rasio Si/Al maka zeolit semakin asam dan semakin bersifat non polar. Zeolit yang semakin asam memiliki indikator semakin banyak ion H+ yang terbentuk pada permukaan zeolit. Ion H+ pada permukaan zeolit, yang berarti situs asam Bronsted yang semakin banyak maka kemampuan dalam mengadsorpsi basa amoniak semakin banyak pula.
Luas Permukaan Katalis
Berdasarkan hasil penelitian, luas permukaan spesifik zeolit sesudah diimpregnasikan logam Ni mengalami penurunan sedikit. Keadaan ini dapat dijelaskan bahwa impregnasi logam Ni relatif merata tetapi terdapat sebagian kecil akumulasi pada mulut pori atau
sebagian permukaan zeolit, sehingga luas permukaan zeolit saat dianalisis dengan menggunakan metode BET menunjukkan sedikit penurunan. Hasil analisis dengan AAS kandungan logam Ni ke dalam katalis Ni/ZSiA adalah 1,06 % dari 2,00 % yang ditargetkan. Jadi tingkat keberhasilan impregnasi logam Ni ke dalam sampel zeolit adalah 53,00 %.
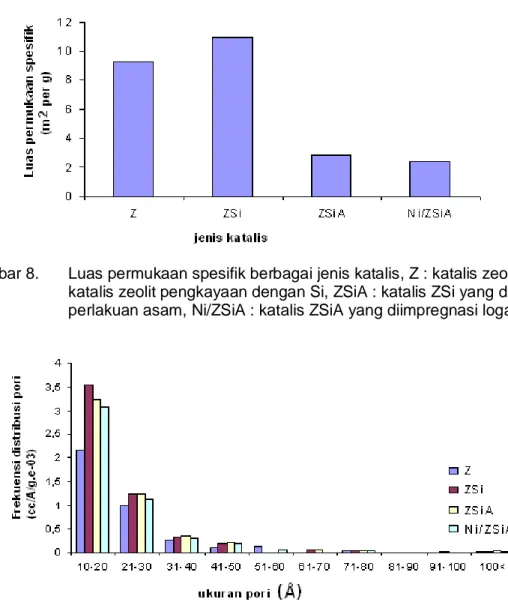
Berdasarkan hasil penelitian yang ditunjukkan Gambar 8 dapat dijelaskan bahwa perlakuan dengan Na2SiO3 menaikan luas permukaan
katalis. Sementara perlakuan asam menyebabkan terjadinya penurunan luas permukaan spesifik katalis yang cukup signifikan. Penurunan luas permukaan katalis dapat disebabkan karena terjadinya perusakan pada kerangka zeolit saat terjadinya
Jurusan Kimia FMIPA Universitas Negeri Surabaya, 20 September 2014 [Type text]
B - 123
dealuminasi dan pengotor hasil dealuminasi kemungkinan dapat menutupi pori-pori katalis. Keadaan ini berakibat saat dilakukan analisis dengan metode BET maka gas nitrogen yang diadsorpsikan tidak mampu masuk ke dalam pori-pori katalis, sehingga yang terdeteksi adalah permukaan luar dan beberapa permukaan bagian dalam dari katalis. Frekuensi Distribusi Ukuran Pori Katalis
Frekuensi distribusi ukuran pori suatu katalis menggambarkan banyaknya atau jumlah pori pada rentang ukuran pori tertentu. Menurut Augustine (1995), pori-pori katalis dibedakan menjadi 3, yaitu mikropori (kurang dari 0,5 nm), mesopori (1,0 – 3,0 nm) dan makropori (lebih besar dari 5,0 nm). Pori-pori pada daerah makro pori relatif tidak dijumpai. Berdasarkan hasil analisis frekuensi distribusi ukuran pori hasil analisis menggunakan peralatan surface analyzer NOVA (metode BET) dapat
dijelaskan bahwa zeolit sesudah diberi
perlakuan dengan asam, Na2SiO3 dan
impregnasi logam Ni mengalami peningkatan jumlah ukuran pori pada daerah 10 hingga 20 angstrom yang cukup signifikan.
Pori-pori zeolit pada daerah 10 hingga 20 angstrom memperlihatkan bahwa terjadi peningkatan jumlah ukuran pori yang cukup signifikan dari jenis katalis Z ke jenis katalis ZSi, ZSiA dan Ni/ZSiA. Peningkatan jumlah ukuran pori tersebut jugaterjadi pada daerah 21 hingga 50 angstrom, dimana semakin besar ukuran pori maka peningkatan jumlah ukuran pori semakin kecil. Zeolit alam yang digunakan sebagai pengemban logam Ni mayoritas memiliki pori-pori pada daerah 10 hingga 30 Å yang sangat dominan. Perlakuan kimia dan fisika terhadap zeolit berdampak mayoritas pada daerah pori-pori tersebut, seperti pembukaan pori-pori katalis, pelebaran mulut pori dan penutupan mulut pori akibat abrasi serta penutupan saluran pori bagian dalam.
Jurusan Kimia FMIPA Universitas Negeri Surabaya, 20 September 2014 [Type text]
B - 124
Gambar 8. Luas permukaan spesifik berbagai jenis katalis, Z : katalis zeolit, ZSi : katalis zeolit pengkayaan dengan Si, ZSiA : katalis ZSi yang diberi perlakuan asam, Ni/ZSiA : katalis ZSiA yang diimpregnasi logam Ni
Gambar 9. Frekuensi distribusi pori berbagai jenis katalis, Z : katalis zeolit, ZSi : katalis zeolit pengkayaan dengan Si, ZSiA : katalis ZSi yang diberi perlakuan asam, Ni/ZSiA : katalis ZSiA yang diimpregnasi logam Ni
KESIMPULAN
Perlakuan asam pada zeolit alam mengakibatkan terjadinya peristiwa pelepasan logam Ca dan Fe yang terdapat dalam zeolit alam sehingga zeolit mengalami
peningkatan keasaman. Disamping itu, perlakuan asam pada zeolit alam juga mengakibatkan terjadinya peristiwa dealuminasi sehingga meningkatkan rasio Si/Al zeolit.
Jurusan Kimia FMIPA Universitas Negeri Surabaya, 20 September 2014 [Type text]
B - 125 DAFTAR PUSTAKA
Augustine, R.L., 1996, Heterogeneous
Catalysis for Chemist, Marcel
Dekker Inc., New York.
Gasser, R.P.H., 1987, An Introduction
to Chemisorption and Catalysis by Metal, Oxford Science
Publication, Oxford.
Handoko. D., S., P., 2001, Modifikasi
Zeolit Alam dan
Karakterisasinya Sebagai
Katalis Perengkahan Asap
Cair Kayu Bengkirah, Program
Pasca Sarjana Kimia UGM, Jogjakarta.
Harber, J., 1991, Manual on Catalyst
Characterization, Pure and
Appl. Chem., 63, 9,
1227-1246.
Satterfield, C.N., 1980, Heterogenous
Catalysis in Practices,
McGraw-Hill Book Co., New York.
Sibilia, J.P., 1996, A Guide to
Materials Characterization and Chemical Analysis, 2nd Edition. VCH Publishers, Inc., New York.
Treacy, M.M.J., and Higgins, J.B., 2001, Collection of Simulated
XRD Powder Patternsfor
Zeolite, Elsevier, Amsterdam.
Twaiq, F.A.A., Asmawati Noor M. Zabidi, Abdul Rahman Mohamed and Subhash Bhatia, 2003, Catalytic Conversion of Palm Oil Over Meso Porous Aluminosilicate MCM 41 for The Production of Liquid Hydrocarbon Fuel, Fuel Process Technol, 84, 1-3, 105
– 120.
Van Santen, R.A. and Kramer, G.J., 1995, Reactivity Theory of
Zeolitic Bronsted Acidic Sites, J. Am. Chem. Soc : Chem. Rev, 95, 637-669.
West, A.R., 1984, Solid State Chemistry and It’s Application,
John Willey & Sons, New York. Zhang, W. and Smirniotis, P.G., 1999,
Effect of Zeolite Structure and
Acidity on the Product
Selectivity and Reaction
Mechanism for n-Octane
Hydroisomerization and
Hydrocracking, J. Catal., 182,