PRODUKSI XILOSA DARI TONGKOL JAGUNG (Zea mays L.)
DENGAN HIDROLISIS ASAM KLORIDA
Oleh Yani Darliah
F34104079
2008
FAKULTAS TEKNOLOGI PERTANIAN
INSTITUT PERTANIAN
YANI DARLIAH. F34104079. Produksi Xilosa dari Tongkol Jagung (Zea mays L.) dengan Hidsrolisis Asam Klorida. Di bawah bimbingan Liesbetini Hartoto dan Ani Suryani. 2008.
RINGKASAN
Tongkol jagung merupakan salah satu limbah lignoselulosik yang banyak terdapat di Indonesia, tercatat pada tahun 2008 tongkol jagung yang dihasilkan sebesar 4.456.215 ton (BPS, 2008). Namun, tongkol jagung tersebut belum dimanfaatkan secara optimal terutama bagi keperluan industri.
Tongkol jagung mengandung selulosa 40 %, hemiselulosa 36 %, lignin 16 % dan 8 % bahan lainnya (Anonimous, 1981). Kandungan hemiselulosa yang tinggi merupakan potensi tongkol jagung untuk dikembangkan menjadi bahan baku industri pemanis seperti xilosa dan xilitol yang dihasilkan dari hidrolisis xilan (hemiselulosa). Xilosa digunakan dalam industri pangan dan juga dapat disintesis menjadi xilitol, etanol dan asam-asam organik. Selain itu, xilosa dalam bentuk kristal banyak dimanfaatkan sebagai gula rendah kalori pengganti sukrosa terutama bagi penderita diabetes mellitus.
Hidrolisis xilan dapat dilakukan secara enzimatis maupun secara asam. Akan tetapi, hidrolisis secara asam lebih aplikatif karena biaya produksinya lebih rendah dibandingkan dengan hidrolisis enzimatis. Pada penelitian ini digunakan hidrolisis asam dengan menggunakan katalis asam klorida karena HCl mempunyai pH yang stabil, dan mempunyai sifat melarutkan yang baik. Efektifitas hidrolisis xilan menggunakan asam dipengaruhi oleh suhu, konsentrasi asam, tekanan, kekuatan asam dan lama hidrolisis (Sjostrom, 1995).
Penelitian ini bertujuan untuk menentukan varietas tongkol jagung (BISMA, BISI dan P-21) yang menghasilkan rendemen xilan tertinggi dan menentukan kondisi hidrolisis xilan yang optimal. Hidrolisis xilan dilakukan pada suhu 105oC, tekanan 0,05 mPa, konsentrasi xilan 20 %, konsentrasi HCl 0,3 %; 0,5 %; 0,7 % dan hidrolisis dilakukan selama 1, 2, 3, 4, dan 5 jam. Analisis yang dilakukan terhadap hasil hidrolisis adalah kadar bahan kering, rendemen, total gula, gula pereduksi dan derajat polimerisasi.
Hasil analisis proksimat menunjukan bahwa kadar serat kasar tongkol jagung sekitar 34,02-35,42 % bk. Kandungan serat terendah diperoleh dari tongkol jagung varietas BISMA (34,02 %) dan yang tertinggi diperoleh dari varietas P-21 (35,42 %). Serat kasar ini terdiri dari hemiselulosa, selulosa dan lignin. Analisis serat menunjukan bahwa kandungan serat dari varietas BISMA terdiri dari 41,66 % bk hemiselulosa, 43,66 % bk selulosa, dan 13,10 % bk lignin, varietas BISI terdiri dari 29,40 % bk hemiselulosa, 52,66 % bk selulosa dan 13,10 % bk lignin, sedangkan varietas P-21 terdiri dari 61,41 % bk selulosa, 16,89 % bk hemiselulosa dan 19,89 % bk lignin. Hasil ekstraksi dan purifikasi xilan memperlihatkan bahwa rendemen xilan tertinggi diperoleh dari tongkol jagung varietas BISMA (12,24 % bk) dengan efisiensi ekstraksi dari persentase hemiselulosa sebesar 29,38 % dan rendemen terendah diperoleh dari varietas P-21 (7,75 % bk) dengan efisiensi ekstraksi dari persentase hemiselulosa sebesar 45,89 %.
Berdasarkan keseluruhan hasil hidrolisis, diketahui bahwa kondisi optimal hidrolisis xilan dengan HCl tercapai pada konsentrasi HCl 0,3 % (v/v) dan waktu hidrolisis selama 4 jam. Pada kondisi tersebut dihasilkan xilosa dengan rendemen sebesar 57,36 %, kadar bahan kering 19,74 %, total gula 101,43 mg/ml, gula pereduksi 99,82 mg/ml dan derajat polimerisasi 1,01.
YANI DARLIAH. F34104079. Production of Xylose From Corncob (Zea mays L.) by Hydrochloride Acid Hydrolysis. Under the Guidance of Liesbetini Hartoto and Ani Suryani. 2008.
SUMMARY
Corncob is a waste of lignocellulose which is abundant in Indonesia, recorded by BPS, corncob reaches 4.456.215 tons in 2008. But, the corncob has not been exploited optimally especially for industry.
Corncob consists of 40 % cellulose, 36 % hemicellulose, 16 % lignin and 8 % of other substances (Anonimous, 1981). High content of hemicellulose represents the potency of corncob as the raw material of sweetener industry, such as xylose and xylitol which is produced from xylan (hemicellulose) hydrolysis. Xylose is used for food industry and can be converted into xylitol, etanol, and organic acids. Besides that, xylose in crystal form is used for substitute of sucrose as low sugar calorie especially for diabetes mellitus patients.
Hydrolysis of xylan can be done by enzymatic and acid hydrolysis. However, acid hydrolysis is more applicable because the production cost is lower than the enzymatic hydrolysis. In this research acid hydrolysis method was used with chloride acid as catalyst because HCl has stable pH, and has the nature of dissolving good. The effectiveness of acid hydrolysis of xylan is influenced by temperature, acid concentration, pressure, acid strength and hydrolysis time (Sjostrom, 1995).
The purpose of this research were to determine the varieties of corncob (BISMA, BISI and P-21) which produce the highest yield of xylan and to determine the optimal condition of xylan hydrolysis. Xylan hydrolysis was done at temperature 105 oC, pressure 0,05 mPa, xylan concentration 20 %, HCl concentration 0,3 %; 0,5 %; 0,7 % and hydrolysis time for 1, 2, 3, 4, and 5 hours. The analysis which was done to hydrolysis result were dry substance, yield, total of sugar, reducing sugar value and polymerization degree.
The result of proximate analysis showed that crude fiber of corncob is about 34,02-35,42 % db. A lower crude fiber was given from corncob BISMA (34,02 %) and highest crude fiber was given from corncob P-21 (35,42 %). This Crude fiber consisted of hemicellulose, lignin and cellulose. Analyze of fiber showed that crude fiber content from corncob BISMA contained 41,66 % db hemicellulose, 43,66 % db cellulose, and 13,10 % db lignin, BISI variety contained 29,40 % db hemicellulose, 52,66 % db cellulose and 13,10 % db lignin, while P-21 varieties contained 61,41 % db cellulose 16,89 % db hemicellulose and lignin fraction 19,89 % db. The result of xylan extraction and purification from corncob showed that the highest yield of xylan came from corncob BISMA variety (12,24 % db) with extraction efficiency of 29,38 % from hemicellulose percentage and the lowest P-21 variety (7,75 % db) with extraction efficiency of 45,89 % from hemicellulose percentage.
According to the result of hydrolysis, the optimal condition of xylan hydrolysis by HCl was reached at HCl concentration 0,3 % (v/v) and hydrolysis time for 4 hours. It produced 57,36 % xylose, 19,74 % dry substance, 101,43 mg/ml total of sugar, 99,82 mg/ml of reducing sugar and 1,01 of polymerization degree.
FAKULTAS TEKNOLOGI PERTANIAN INSTITUT PERTANIAN BOGOR
PRODUKSI XILOSA DARI TONGKOL JAGUNG (Zea mays L.) DENGAN HIDROLISIS ASAM KLORIDA
SKRIPSI
Sebagai salah satu syarat untuk memperoleh gelar
SARJANA TEKNOLOGI PERTANIAN
Pada Departemen Teknologi Industri Pertanian Fakultas Teknologi Pertanian
Institut Pertanian Bogor
Oleh YANI DARLIAH
F34104079
2008
FAKULTAS TEKNOLOGI PERTANIAN INSTITUT PERTANIAN BOGOR
FAKULTAS TEKNOLOGI PERTANIAN INSTITUT PERTANIAN BOGOR
PRODUKSI XILOSA DARI TONGKOL JAGUNG (Zea mays L.) DENGAN HIDROLISIS ASAM KLORIDA
SKRIPSI
Sebagai salah satu syarat untuk memperoleh gelar
SARJANA TEKNOLOGI PERTANIAN
Pada Departemen Teknologi Industri Pertanian Fakultas Teknologi Pertanian
Institut Pertanian Bogor
Oleh YANI DARLIAH
F34104079
Dilahirkan pada tanggal 22 Juli 1986 Di Majalengka
Tanggal lulus : Menyetujui,
Bogor, September 2008
Dr. Ir. Liesbetini Hartoto, MS Dosen Pembimbing I
Dr. Ir. Ani Suryani, DEA Dosen Pembimbing II
SURAT PERNYATAAN
Saya yang bertanda tangan di bawah ini menyatakan dengan sebenar-benarnya bahwa skripsi dengan judul “Produksi Xilosa dari Tongkol Jagung
(Zea mays L.) dengan Hidrolisis Asam klorida” adalah hasil karya saya sendiri
dengan arahan dosen pembimbing akademik, kecuali yang dengan jelas ditunjukan rujukannya.
Bogor, Agustus 2008
Yani Darliah F34104079
RIWAYAT HIDUP
Penulis dilahirkan di Majalengka, Jawa Barat pada tanggal 22 Juli 1986. Penulis adalah anak kedua dari dua bersaudara dari pasangan Eman dan (Alm) Uun. Pada tahun 1998, penulis menyelesaikan pendidikan sekolah dasar di SDN 1 Cibeureum. Penulis menyelesaikan pendidikan sekolah menengah di SLTPN 1 Talaga dan lulus pada tahun 2001. Kemudian penulis melanjutkan pendidikan di SMUN 11 Bandung dan lulus pada tahun 2004. Tahun 2004 penulis melanjutkan pendidikan di Perguruan Tinggi Negeri, Institut Pertanian Bogor melalui jalur USMI (Undangan Seleksi Masuk IPB).
Selama kuliah di IPB, penulis pernah menjadi asisten praktikum pada mata kuliah Bioproses periode 2006/2007 dan 2007/2008. Penulis juga aktif dalam organisasi kemahasiswaan dengan menjadi pengurus HIMALOGIN pada tahun 2005/2006 serta pernah menjadi panitia dalam beberapa acara.
Pada tahun 2007 penulis melaksanakan praktek lapangan di PTPN. VIII Goalpara-Sukabumi dengan topik “Mempelajari Teknologi Proses Produksi dan Pengawasan Mutu Teh Hitam Orthodoks di PTP. Nusantara VIII Goalpara, Sukabumi “. Untuk menyelesaikan tugas akhir ini, penulis melakukan penelitian yang dituangkan dalam skripsi berjudul “Hidrolisis Xilan dari Tongkol Jagung
KATA PENGANTAR
Alhamdulillah, Puji Syukur tak terhingga penulis haturkan ke hadirat Allah SWT yang telah memberikan rahmat dan karunia-Nya, sehingga penulis dapat menyelesaikan penyusunan skripsi yang berjudul “Produksi Xilosa dari Tongkol Jagung (Zea mays L.) dengan Hidrolisis Asam Klorida” ini dengan baik. Skripsi ini disusun sebagai salah satu syarat untuk memperoleh gelar Sarjana di Departemen Teknologi Industri Pertanian, Fakultas Teknologi Pertanian, Institut Pertanian Bogor.
Penulis sepenuhnya menyadari bahwa penulisan skripsi ini tidak akan selesai tanpa adanya bimbingan dan dukungan yang penuh ketulusan baik secara moril maupun materil dari semua pihak. Oleh karena itu, dalam kesempatan ini penulis mengucapkan banyak terimakasih kepada pihak-pihak yang turut membantu dalam penyusunan skripsi ini.
Penghargaan dan ucapan terimakasih penulis haturkan kepada :
1. Ibu Dr. Ir. Liesbetini Hartoto, MS selaku dosen pembimbing I dan Dr. Ir. Ani Suryani, DEA selaku dosen pembimbing II atas bimbingan dan saran-saran yang diberikan selama penulis menyelesaikan skripsi.
2. Ir. Sugiarto, MSi selaku dosen penguji atas kritik dan saran yang diberikan kepada penulis.
3. Kedua orang tua yang telah memberikan motivasi dan do’a serta kasih sayang dan dukungan kepada penulis.
4. Nenek, kakek (alm), paman, tante dan kakakku yang telah memberikan motivasi dan do’a serta kasih sayang dan dukungan kepada penulis.
5. PT. Lautan Luas yang telah menyediakan dana penelitian ini.
6. Bu Rini, Pak Gunawan, Bu Sri, Bu Ega, Pak Edi, Pak Agus, Pak Sugi dan seluruh pegawai jurusan TIN yang juga sangat membantu dalam kelancaran pelaksanaan penelitian penulis.
7. Teman-teman anggota ”Pondok Ami” dengan segala kehangatan dan persahabatan yang tak pernah terlupakan.
8. Seluruh teman-teman TIN 41 yang selalu memberikan semangat kepada penulis.
Penulis menyadari masih banyak kekurangan di berbagai sisi baik dari penyajian isi maupun penulisan dan penyusunan skripsi ini. Oleh sebab itu saran dan kritik akan menjadi masukan yang terbaik untuk lebih membangun, memperbaiki dan menyempurnakannya untuk saat ini maupun masa mendatang. Semoga segala sesuatu yang tertuang dalam skripsi ini akan bermanfaat bagi yang memerlukannya. Amien.
Bogor, Agustus 2008
DAFTAR ISI
Halaman
KATA PENGANTAR ...i
DAFTAR ISI...iii
DAFTAR TABEL...v
DAFTAR GAMBAR ...vi
DAFTAR LAMPIRAN...vii
I. PENDAHULUAN ...1
A. LATAR BELAKANG...1
B. TUJUAN ...2
II. TINJAUAN PUSTAKA ...3
A. JAGUNG ...3
B. TONGKOL JAGUNG...5
C. KOMPONEN SERAT TONGKOL JAGUNG ...6
1. Selulosa...7 2. Hemiselulosa ...8 3. Lignin...9 D. XILAN...10 E. EKSTRAKSI XILAN...12 1. Delignifikasi ...12 2. Ekstraksi ...13 F. PURIFIKASI XILAN...13 G. XILOSA ...14
H. HIDROLISIS HEMISELULOSA (XILAN) ...15
III. METODOLOGI PENELITIAN...18
A. BAHAN DAAN ALAT...18
B. METODE PENELITIAN ...18
1. Analisa Proksimat ...18
2. Ekstraksi Xilan dari Tongkol Jagung...18
a. Delignifikasi ...19
Halaman
c. Purifikasi Xilan...21
3. Hidrolisis Xilan ...21
C. RANCANGAN PERCOBAAN ...23
IV. HASIL DAN PEMBAHASAN...25
A. ANALISA PROKSIMAT ...25
B. EKSTRAKSI DAN PURIFIKASI XILAN...27
C. HIDROLISIS XILAN ...29 1. Bahan Kering...31 2. Rendemen ...32 3. Total Gula ...34 4. Gula Pereduksi...35 5. Derajat Polimerisasi...37
D. PERBANDINGAN HASIL HIDROLISIS HCl DENGAN KONTROL...39
V. KESIMPULAN DAN SARAN...40
A. KESIMPULAN ...40
B. SARAN ...40
DAFTAR PUSTAKA ...41
LAMPIRAN...46
DAFTAR TABEL
Halaman
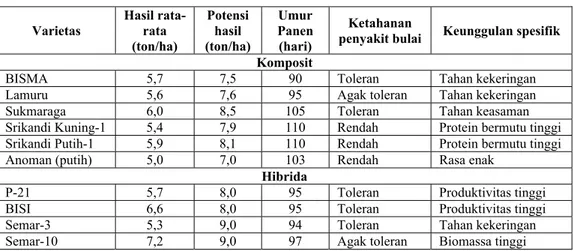
Tabel 1. Varietas Jagung Unggul ...4
Tabel 2. Rencana Pergeseran Penggunaan Varietas Jagung ...4
Tabel 3. Areal Panen Jagung di Empat Propinsi Utama Penghasil... Jagung di Indonesia...5
Tabel 4. Komposisi Kimia Tongkol Jagung ...6
Tabel 5. Kadar Xilan Berbagai Limbah Industri Pertanian...11
Tabel 6. Perbandingan Karakteristik antara HCl dan H2SO4...17
Tabel 7. Hasil Analisa Proksimat Tongkol Jagung...25
Tabel 8. Komposisi Serat Tongkol Jagung ...25
Tabel 9. Rendemen Xilan Hasil Ekstraksi dan Purifikasi ...29
DAFTAR GAMBAR
Halaman
Gambar 1. Kemungkinan Pemanfaatan Bahan Lignoselulosik...6
Gambar 2. Struktur Molekul Selulosa...7
Gambar 3. Penampang Membujur Hemiselulosa dalam Jaringan Tanaman ...8
Gambar 4. Struktur Molekul Monosakarida Penyusun Hemiselulosa ...9
Gambar 5. Struktur Molekul Lignin dan Monomer Penyusunnya...10
Gambar 6. Struktur Kimia Xilan...10
Gambar 7. Struktur Kimia D-Xilosa ...14
Gambar 8. Reaksi Hidrogenasi Xilosa menjadi Xilitol...14
Gambar 9. Struktur Molekul Furfural ...16
Gambar 10. Diagram Alir Proses Ekstraksi Xilan Metode Asidifikasi ...20
Gambar 11. Diagram Alir Proses Purifikasi Xilan...22
Gambar 12. Diagram Alir Proses Hidrolisis Xilan Secara Asam ...23
Gambar 13. Xilan Tongkol Jagung Kering...30
Gambar 14. Tahap Pemurnian Xilosa ...31
Gambar 15. Grafik Hubungan antara Konsentrasi HCl dengan Waktu Hidrolisis terhadap Bahan Kering Xilosa...32
Gambar 16. Grafik Hubungan antara Konsentrasi HCl dengan Waktu Hidrolisis terhadap Rendemen Xilosa...33
Gambar 17. Grafik Hubungan antara Konsentrasi HCl dengan Waktu Hidrolisis terhadap Total Gula ...34
Gambar 18. Grafik Hubungan antara Konsentrasi HCl dengan Waktu Hidrolisis terhadap Gula Pereduksi...36
Gambar 19. Grafik Hubungan antara Konsentrasi HCl dengan Waktu Hidrolisis terhadap Derajat Polimerisasi...37
Gambar 20. Kurva Standar Total Gula ...64
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Prosedur Analisa Karakteristik Tongkol Jagung...47
Lampiran 2. Prosedur Analisa Xilosa ...51
Lampiran 3. Neraca Massa Proses Ekstraksi Xilan ...53
Lampiran 4. Neraca Massa Proses Hidrolisis Xilan...56
Lampiran 5. Analisa Keragaman terhadap Bahan Kering Xilosa ...57
Lampiran 6. Analisa Keragaman terhadap Rendemen Xilosa ...58
Lampiran 7. Analisa Keragaman terhadap Total Gula...59
Lampiran 8.Analisa Keragaman terhadap Gula Pereduksi ...61
Lampiran 9.Analisa Keragaman terhadap Derajat Polimerisasi ...63
Lampiran 10. Kurva Standar Total Gula (480 nm) ...64
I. PENDAHULUAN
A. LATAR BELAKANG
Tongkol jagung merupakan salah satu limbah lignoselulosik yang banyak tersedia di Indonesia. Berdasarkan data Badan Pusat Statistik, ketersediaan tongkol jagung di Indonesia pada tahun 2006 adalah sebesar 3.482.839 ton, pada tahun 2007 sebesar 3.986.258 ton, dan berdasarkan perkiraan, pada tahun 2008 tongkol jagung ada sekitar 4.456.215 ton.
Tongkol jagung selama ini baru dimanfaatkan sebagai pakan ternak, sedangkan pemanfaatan untuk bahan baku industri belum banyak dilakukan. Oleh karena itu, diperlukan adanya diversifikasi pemanfaatan limbah tongkol jagung yang ada, salah satunya adalah dengan memanfaatkan fraksi hemiselulosa. Hemiselulosa adalah polisakarida dimana sebagian besar monomernya adalah pentosan (xilosa). Menurut Annonimous (1981), tongkol jagung pada umumnya mengandung hemiselulosa sebesar 36 %, kandungan hemiselulosa tersebut berbeda-beda tergantung varietasnya. Tingginya kandungan hemiselulosa tongkol jagung tersebut mengakibatkan tongkol jagung berpotensi untuk diolah menjadi xilosa.
Xilosa memiliki aplikasi yang cukup luas dalam beberapa industri pangan dan dapat disintesis menjadi xilitol, etanol, asam-asam organik (butanol, aseton, asam asetat dan asam laktat) serta protein sel tunggal. Selain itu, xilosa dalam bentuk kristal banyak dimanfaatkan sebagai gula rendah kalori pengganti sukrosa terutama bagi penderita diabetes melitus. Hingga saat ini seluruh kebutuhan xilosa dalam negeri diperoleh melalui impor. Impor terbesar diperoleh dari Cina yang saat ini menguasai pasar xilosa dunia.
Xilosa dapat dihasilkan dari proses hidrolisis hemiselulosa (xilan) baik secara enzimatis maupun secara asam. Hidrolisis hemiselulosa secara enzimatis tidak menghasilkan produk yang beracun, namun proses ini tidak efektif dalam memproduksi xilosa, selain karena harga enzim xilanase sangat mahal, proses hidrolisis xilan secara enzimatis hanya menghasilkan monosakarida (xilosa) dalam jumlah yang sedikit dan menghasilkan oligosakarida dalam jumlah yang lebih tinggi (rendemen rendah), serta
membutuhkan waktu hidrolisis yang lama, yaitu pada umumnya lebih dari 24 jam.
Hidrolisis secara asam lebih efisien karena biaya produksinya lebih rendah, waktu hidrolisis relatif singkat dan menghasilkan rendemen yang lebih tinggi dibandingkan dengan hidrolisis enzimatis. Namun meskipun demikian, hidrolisis hemiselulosa secara asam mempunyai kelemahan yaitu, larutan gula yang dihasilkan kemungkinan mempunyai rasa yang asin karena pada saat penetralan dihasilkan garam dalam jumlah yang cukup banyak, sehingga memerlukan pemurnian lebih lanjut.
Penelitian ini menggunakan metode hidrolisis asam karena metode ini lebih efisien dari segi biaya, waktu dan rendemen. Asam yang digunakan adalah asam klorida (HCl). Selain harganya murah, HCl mempunyai pH yang stabil, dan mempunyai sifat melarutkan yang baik.
Dalam pelaksanaannya, keberhasilan hidrolisis hemiselulosa secara asam tidak hanya ditentukan oleh jenis asam (katalis) yang digunakan, tetapi juga dipengaruhi oleh konsentrasi asam yang digunakan dan lamanya hidrolisis hemiselulosa tersebut. Berdasarkan hal inilah maka kajian mengenai pengaruh faktor-faktor di atas dalam produksi xilosa sangat diperlukan agar hasil yang diperoleh optimal.
B. TUJUAN
Penelitian ini bertujuaan untuk :
1. Menentukan varietas tongkol jagung (BISMA, BISI dan P-21) yang menghasilkan rendemen xilan tertinggi.
2. Menentukan konsentrasi HCl dan waktu hidrolisis terbaik dalam konversi xilan menjadi xilosa.
II. TINJAUAN PUSTAKA
A. JAGUNG
Tanaman jagung (Zea mays L.) merupakan tanaman biji-bijian yang termasuk ke dalam famili rumput-rumputan (Graminae). Tanaman jagung terdiri atas akar, batang, daun, bunga, dan biji. Biji jagung berkeping tunggal, tersusun dalam tongkol dengan susunan teratur memanjang dan ditutup oleh seludang atau kelobot (Sumadi dan Rasyid, 2002). Sistematika tanaman jagung adalah sebagai berikut.
Kingdom : Plantae Divisio : Spermatophyta Sub Divisio : Angiospermae Classis : Monocotyledone Ordo : Graminae
Familia : Graminaceae Genus : Zea
Species : Zea mays L. (http://id.wikipedia.org/wiki/Jagung)
Varietas jagung dibedakan menjadi dua golongan yaitu, varietas unggul dan lokal. Varietas unggul adalah varietas jagung yang mempunyai sifat berproduksi tinggi, umur pendek, tahan terhadap serangan penyakit dan sifat-sifat lainnya yang menguntungkan. Varietas unggul ini dibedakan menjadi dua, yaitu jagung hibrida dan komposit (http://www.puslittan.bogor.net) Varietas-varietas jagung unggul komposit dan hibrida yang telah dihasilkan oleh Badan Litbang Pertanian disajikan dalam Tabel 1.
Jagung hibrida adalah varietas jagung generasi pertama hasil persilangan dua galur murni, sedangkan varietas jagung komposit adalah varietas jagung hasil persilangan dari beberapa varietas jagung. Pada umumnya, varietas jagung hibrida memberikan hasil yang lebih baik daripada varietas jagung komposit, yaitu mampu berproduksi lebih tinggi 15-20% dan menghasilkan biji yang lebih besar dibandingkan varietas komposit. Namun varietas hibrida ini tidak dapat bertahan di lahan kering, sebaliknya varietas komposit dapat ditanam di lahan yang tidak subur (http://www.puslittan.bogor.net).
Tabel 1. Varietas Jagung Unggul
Varietas Hasil rata-rata (ton/ha) Potensi hasil (ton/ha) Umur Panen (hari) Ketahanan
penyakit bulai Keunggulan spesifik Komposit
BISMA 5,7 7,5 90 Toleran Tahan kekeringan
Lamuru 5,6 7,6 95 Agak toleran Tahan kekeringan
Sukmaraga 6,0 8,5 105 Toleran Tahan keasaman
Srikandi Kuning-1 5,4 7,9 110 Rendah Protein bermutu tinggi Srikandi Putih-1 5,9 8,1 110 Rendah Protein bermutu tinggi
Anoman (putih) 5,0 7,0 103 Rendah Rasa enak
Hibrida
P-21 5,7 8,0 95 Toleran Produktivitas tinggi
BISI 6,6 8,0 95 Toleran Produktivitas tinggi
Semar-3 5,3 9,0 94 Toleran Tahan kekeringan
Semar-10 7,2 9,0 97 Agak toleran Biomassa tinggi
Sumber : http://www.puslittan.bogor.net
Produksi jagung, terutama jagung varietas hibrida setiap tahun semakin meningkat. Hal ini disebabkan oleh adanya rencana pemerintah yang akan melakukan pergeseran penggunaan varietas jagung lokal secara nasional ke jenis hibrida dan komposit (Tabel 2) agar hasil produksi jagung dalam negeri semakin meningkat. Dengan demikian dapat diperkirakan juga bahwa ketersediaan tongkol jagung dari varietas jagung hibrida dan komposit (BISI, BISMA dan P-21) akan semakin banyak, sehingga ketiga varietas tersebut sangat berpotensi untuk digunakan sebagai bahan baku untuk industri xilosa. Pada umumnya, varietas jagung komposit dan hibrida banyak ditanam di Indonesia seperti di daerah Jawa Tengah, Jawa Timur, Lampung dan Sumatra Utara (Tabel 3).
Tabel 2. Rencana Pergeseran Penggunaan Varietas Jagung
Tahun Hibrida (%) Komposit (%) Lokal (%)
2008 40 40 20 2010 50 35 15 2015 60 30 10 Sumber: Departemen Pertanian (2008).
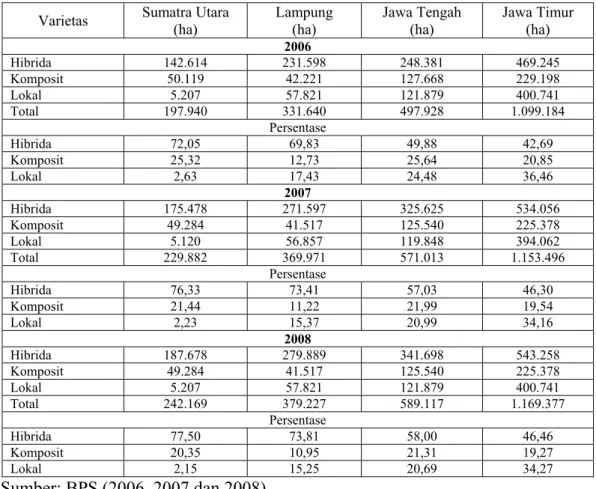
Tabel 3. Areal Panen Jagung di Empat Provinsi Utama Penghasil Jagung di Indonesia
Varietas Sumatra Utara (ha) Lampung (ha) Jawa Tengah (ha) Jawa Timur (ha)
2006 Hibrida 142.614 231.598 248.381 469.245 Komposit 50.119 42.221 127.668 229.198 Lokal 5.207 57.821 121.879 400.741 Total 197.940 331.640 497.928 1.099.184 Persentase Hibrida 72,05 69,83 49,88 42,69 Komposit 25,32 12,73 25,64 20,85 Lokal 2,63 17,43 24,48 36,46 2007 Hibrida 175.478 271.597 325.625 534.056 Komposit 49.284 41.517 125.540 225.378 Lokal 5.120 56.857 119.848 394.062 Total 229.882 369.971 571.013 1.153.496 Persentase Hibrida 76,33 73,41 57,03 46,30 Komposit 21,44 11,22 21,99 19,54 Lokal 2,23 15,37 20,99 34,16 2008 Hibrida 187.678 279.889 341.698 543.258 Komposit 49.284 41.517 125.540 225.378 Lokal 5.207 57.821 121.879 400.741 Total 242.169 379.227 589.117 1.169.377 Persentase Hibrida 77,50 73,81 58,00 46,46 Komposit 20,35 10,95 21,31 19,27 Lokal 2,15 15,25 20,69 34,27 Sumber: BPS (2006, 2007 dan 2008) B. TONGKOL JAGUNG
Menurut Koswara (1991), tongkol jagung adalah tempat pembentukan lembaga dan gudang penyimpanan makanan untuk pertumbuhan biji. Jagung mengandung kurang lebih 30 persen tongkol jagung sedangkan sisanya adalah kulit dan biji.
Menurut Maynard dan Loosli (1993), tongkol jagung terdiri dari 35,5 % serat kasar, 2,5 % protein, 0,12 % kalsium, 0,04 % fosfor dan zat-zat lainnya sebesar 38.16 %. Lebih lanjut, Annonimous (1981) menyatakan bahwa tongkol jagung mengandung selulosa (40 %), hemiselulosa (36 %) dan lignin (16 %) serta at-zat lainnya (8 %). Komposisi kimia tongkol jagung disajikan pada Tabel 4.
Tabel 4. Komposisi Kimia Tongkol Jagung Komponen (% bk) a b Glukan 34,40 ± 0,40 39,40 Xilan 31,30 ± 0,30 28,40 Arabinan 3,01 ± 0,07 3,60 Galaktan - 1,10 Lignin 18,80 ± 0,10 7,00 Abu 1,30 ± 0,03 1,70 Protein 4,30 ± 0,09 3,20 Lemak kasar - 0,70 Gugus Asetil 3,08 ± 0,01 -
Bahan lainnya (by diff.) 0,46 -
Asam Uronat 3,36 ± 0,09 -
a : Parajo et al. (2003)
b : White dan Johnson (2003)
C. KOMPONEN SERAT TONGKOL JAGUNG
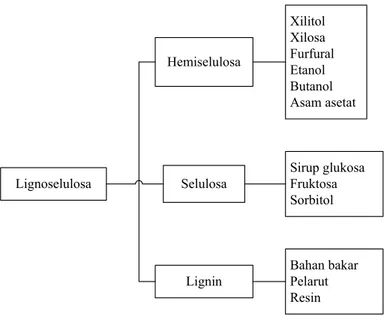
Tongkol jagung merupakan limbah padat yang dapat dikategorikan dalam limbah lignoselulosik. Limbah lignoselulosik adalah limbah pertanian yang mengandung selulosa, hemiselulosa dan lignin. Menurut Humprey (1979), pemanfaatan limbah lignoselulosik adalah melalui proses degradasi, baik secara kimiawi maupun secara enzimatis. Kemungkinan pemanfaatan lignoselulosik disajikan pada Gambar 1.
Lignoselulosa Lignin Selulosa Hemiselulosa Xilitol Xilosa Furfural Etanol Butanol Asam asetat Sirup glukosa Fruktosa Sorbitol Bahan bakar Pelarut Resin
Gambar 1. Kemungkinan Pemanfaatan Bahan Lignoselulosik (Humprey, 1997)
1. Selulosa
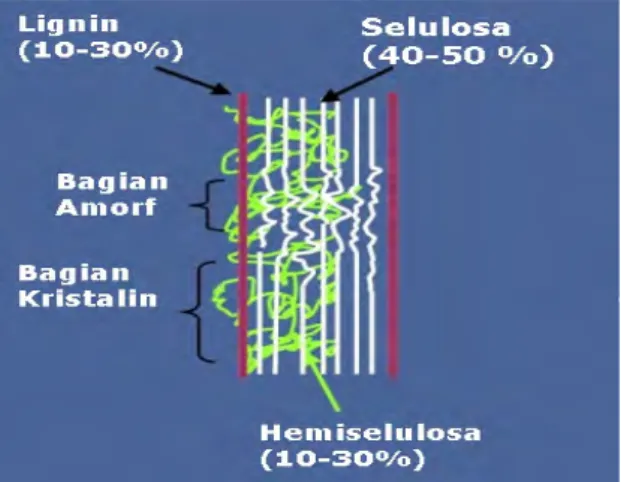
Selulosa merupakan homopolisakarida yang tersusun atas unit-unit D-glukopiranosa yang terikat satu sama lain dengan ikatan β-1,4 glikosidik (Sjostrom,1998). Menurut Achmadi (1989), selulosa mempunyai dua macam ikatan hidrogen, yaitu ikatan hidrogen intramolekul dan ikatan hidrogen intermolekul. Struktur fibril dan kuatnya ikatan hidrogen, menyebabkan selulosa bersifat tidak larut dalam berbagai pelarut. Struktur molekul selulosa diperlihatkan pada Gambar 2.
Gambar 2. Struktur Molekul Selulosa (http://prs.files.wordpress.com) Menurut Fengel dan Wegener (1995), selulosa jika direaksikan dengan alkali akan membengkak sampai batas tertentu tergantung konsentrasi alkali dan suhu reaksi. Ada beberapa tipe pereaksi yang menyebabkan selulosa membengkak, yaitu hidroksida logam alkali, garam-garam dalam larutan basa kuat, beberapa garam dari asam anorganik, senyawa amina dan sejenisnya. Hidroksi logam alkali seperti NaOH merupakan pereaksi yang paling banyak digunakan industri untuk membengkakan selulosa (Achmadi, 1989).
Selulosa terbagi ke dalam tiga jenis, yaitu alfa selulosa, beta selulosa dan gama selulosa. Alfa selulosa adalah bagian selulosa yang tidak larut dalam larutan alkali kuat (NaOH). Beta selulosa adalah bagian selulosa yang larut dalam media alkali dan mengendap jika larutan dinetralkan, sedangkan gama selulosa adalah bagian selulosa yang larut dalam alkali dan tetap larut jika larutan dinetralkan (Fengel dan Wegener, 1995).
2. Hemiselulosa
Hemiselulosa merupakan salah satu komponen lignoselulosa yang sering diartikan sebagai selulosa dengan bobot molekul rendah. Hemiselulosa bersifat tidak tahan terhadap perlakuan panas (Fengel dan Wegener, 1995), strukturya amorf dan mudah dimasuki pelarut (Sjostrom, 1995), dapat diekstraksi menggunakan alkali dan ikatannya lemah sehingga mudah dihidrolisis (Winarno, 1984).
Gong et al. (1991) menyatakan bahwa hemiselulosa bergabung dengan selulosa dalam jaringan lignin untuk membangun dinding sel tanaman yang keras dan kuat. Hemiselulosa tergolong polisakarida yang terdiri dari berbagai jenis heksosa, pentosa dan asam heksuronat. Oleh sebab itu, hemiselulosa didefinisikan sebagai ikatan pendek rantai heteropolisakarida dari campuran heksosa dan pentosa. Penampang membujur hemiselulosa dalam jaringan tanaman dapat dilihat pada Gambar 3.
Gambar 3. Penampang Membujur Hemiselulosa dalam Jaringan Tanaman (http://isroi.files.wordpress.com)
Menurut Wenzl (1990), komponen-komponen monomer hemiselulosa dapat dibagi dalam beberapa tipe sebagai berikut:
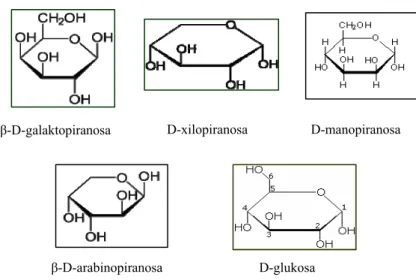
1. Glukomanan, yaitu hemiselulosa dimana monomer penyusunnya terdiri dan β-D-glukopiranosa dan β-D-manopiranosa.
2. Arabinogalaktan, yaitu hemiselulosa dimana monomer penyusunnya adalah β-D-galaktopiranosa dan L-arabinosa.
β-D-galaktopiranosa D-xilopiranosa D-manopiranosa
β-D-arabinopiranosa D-glukosa
3. Xilan, yaitu hemiselulosa dimana monomer penyusunnya adalah β-D-xilopiranosa.
Hemiselulosa tanaman Angiospermae pada umumnya terdiri dari komponen glukomanan (2-5 %), xilan (15-30 %) dan sejumlah kecil asam galakturonat (Fengel dan Wegener, 1995). Struktur molekul monosakarida sebagai monomer penyusun hemiselulosa diperlihatkan pada Gambar 4.
Gambar 4. Struktur Molekul Monosakarida Penyusun Hemiselulosa (Sjostrom, 1995).
3. Lignin
Lignin adalah polimer tiga dimensi yang terdiri dari unit fenil propana yang diikat dengan ikatan eter (C-O-C) dan ikatan karbon (C-C). Lignin bersifat tahan terhadap hidrolisis karena adanya ikatan arilalkil dan ikatan eter (Judoamidjojo et al., 1989), serta tidak larut dalam air, dalam larutan asam dan larutan hidrokarbon (Krik dan Othmer 1952).
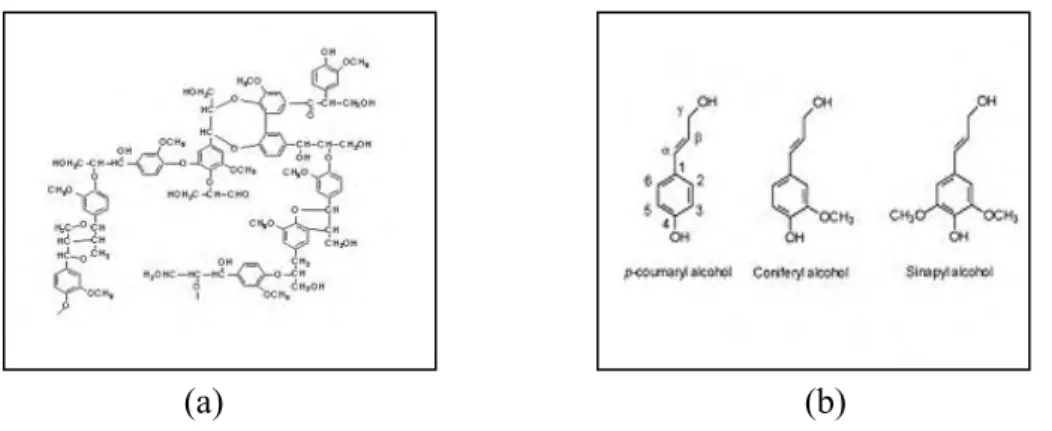
Sjostrom (1995) menyatakan reaktivitas lignin sangat dipengaruhi oleh gugus-gugus fungsi yang terdapat pada polimer lignin itu sendiri. Polimer lignin mengandung gugus metoksil, gugus hidroksil fenol dan beberapa gugus aldehid pada rantai sampingnya. Menurut Achmadi (1989), gugus fungsi yang sangat mempengaruhi reaktivitas lignin adalah gugus hidroksil fenolik dan gugus karbonil. Struktur molekul lignin dan monomer penyusunnya diperlihatkan pada Gambar 5.
(a) (b)
Gambar 5. Struktur Molekul Lignin (a) dan monomer penyusunnya (b) (http://id.wikipedia.org/wiki/Lignin)
D. XILAN
Xilan atau polimer xilosa adalah komponen yang paling banyak terdapat dalam hemiselulosa tanaman (Whistler, 1950). Menurut Sjostrom (1995), xilan merupakan polimer dari xilosa yang berikatan β-1,4-xilopiranosa dengan jumlah monomer 150 hingga 200 unit. Rantai xilan bercabang dan strukturnya tidak berbentuk kristal sehingga lebih mudah dimasuki pelarut dibanding selulosa. Struktur asli xilan sangat kompleks dan dapat disubstitusi dengan grup asetil, L-arabinofuranosil dan glukoronosil pada rantai sampingnya (Whistler, 1950). Struktur kimia xilan dapat dilihat pada Gambar 6.
Gambar 6. Struktur Kimia Xilan (Eriksson et al., 1990)
Pada umumnya, xilan diklasifikasikan atau disebut sebagai hemiselulosa karena diperoleh melalui prosedur ekstraksi hemiselulosa dan xilan adalah komponen pokok dari hemiselulosa (Whistler, 1950). Hemiselulosa (xilan) yang dihasilkan dari proses ekstraksi ada 2 jenis, yaitu hemiselulosa A (55 %)
dan hemiselulosa B (45 %). Hemiselulosa A yang identik dengan nama xilan adalah endapan yang diperoleh dari pengasaman filtrat alkali hingga pH-nya sekitar 4,5-5,0. Hemiselulosa A mengandung xilosa (88,5 %), arabinosa 9,1 % dan galaktosa 2,4 %. Hemiselulosa B adalah endapan yang diperoleh dari penambahan etanol pada filtrat dari hemiselulosa A. Hemiselulosa B terdiri atas xilosa (61,2 %), galaktosa 27,8 % dan arabinosa 11,0 % (Soltes, 1983).
Menurut Whistler (1950), xilan bersifat dapat larut dalam larutan alkali (NaOH atau KOH 2-15 persen) dan larut dalam air. Sedangkan berdasarkan hasil penelitian Richana (2006), xilan bersifat larut sempurna dalam alkali (NaOH 1 %), larut dalam air panas dan sedikit larut dalam air dingin, serta tidak larut dalam asam (HCl 1 N).
Xilan banyak dijumpai pada limbah pertanian seperti tongkol jagung, bagas tebu, jerami padi, dedak gandum, dan biji kapas. Menurut Whistler (1950), kandungan xilan dalam bahan-bahan tersebut berkisar antara 15-30 persen bobot kering. Kayu keras (hardwood) dan kayu lunak (softwood) juga merupakan bahan-bahan yang kaya akan xilan. Kayu keras mengandung 20-25 persen xilan, sedangkan kayu lunak mengandung 7-12 persen (Sjostrom, 1995).
Berdasarkan penelitian Agustina (2002) dan Richana (2006), kadar xilan dalam tongkol jagung adalah yang tertinggi dibandingkan kadar xilan pada limbah angiospermae lainnya. Oleh karena itu, tongkol jagung sangat potensial untuk digunakan sebagai sumber xilan dalam produksi xilosa. Kadar xilan dalam berbagai limbah industri pertanian dapat dilihat pada Tabel 5.
Tabel 5. Kadar Xilan Berbagai Limbah Hasil Pertanian
Limbah/bahan Kadar xilan (%)
Tongkol jagung 31,94 *
Ampas umbi garut 6,86 *
Onggok 0,40 * Sekam 29,91 * Bekatul 10,25 * Bagas tebu 9,60 ** Oat hulls 12,30 ** Kulit kacang 6,30 **
Kulit biji kapas 10,2 **
Sumber: *) Agustina (2002) **) Richana (2006)
E. EKSTRAKSI XILAN
Proses ekstraksi xilan terbagi menjadi dua tahap yaitu tahap delignifikasi dan ekstraksi (Widyani, 2002; Adam, 1965 dan Soltes, 1983).
1. Delignifikasi
Menurut Soltes (1983), isolasi hemiselulosa dari limbah pertanian bisa dilakukan dengan dua cara yaitu pertama, mengekstraksi hemiselulosa secara langsung dengan alkali dan yang kedua adalah melakukan delignifikasi terlebih dahulu dengan menggunakan pelarut yang bersifat oksidator.
Menurut Fridia (1989), proses delignifikasi merupakan perlakuan pendahuluan terhadap bahan baku sehingga mempermudah pelepasan hemiselulosa. Delignifikasi dapat dilakukan dengan menggunakan bahan kimia alkali dan bahan kimia yang bersifat oksidator. Bahan kimia yang bersifat oksidator diantaranya adalah klor, oksigen, hipoklorit, peroksida, ozon dan nitrogen dioksida. Sedangkan alkali yang bisa digunakan untuk delignifikasi adalah NaOH (Batubara, 2006).
Menurut Fengel dan Wegener (1995), pada umumnya proses delignifikasi dilakukan dengan menggunakan pelarut natrium hipoklorit (NaOCl) karena pelarut tersebut mengandung ion-ion hipoklorit yang mampu memecah ikatan eter dalam struktur lignin.
Bahan yang telah dikenai proses delignifikasi selain mengalami penyusutan kandungan ligninnya juga mengalami penyusutan selulosa dan hemiselulosa. Proses delignifikasi yang baik adalah yang menghasilkan holoselulosa dengan kandungan sisa lignin yang rendah, hilangnya polisakarida minimal serta terjadi degradasi oksidatif dan hidrolitik selulosa minimal (Fengel dan Wegener, 1995).
2. Ekstraksi Xilan
Hespell et al. (1997) menyatakan bahwa ekstraksi xilan dapat dilakukan dengan menggunakan beberapa pelarut seperti natrium hidroksida (NaOH), amonium hidroksida (NH4OH) dan kalium hidroksida
adalah natrium hidroksida, karena NaOH merupakan alkali yang paling kuat dalam mendegradasi struktur dinding sel. Hal ini sesuai dengan pernyataan Soltes (1983) bahwa hemiselulosa sangat mudah diekstraksi dengan menggunkan NaOH. Laju ekstraksi hemiselulosa meningkat secara bertahap dengan peningkatan konsentrasi NaOH yang digunakan.
Selain itu, menurut Fengel dan Wegener (1995), garam NaCl yang terbentuk dari proses penetralan larutan alkali (NaOH) oleh HCl mempunyai kelarutan yang tinggi dalam etanol, sehingga memudahkan proses pemurnian xilan. Menurut Somaatmadja (1981), syarat pelarut yang digunakan pada proses ekstraksi adalah tidak berbahaya bagi pekerja, tidak bersifat racun dan dapat melarutkan xilan dengan cepat dan sempurna, murah serta mudah diusahakan sebagai pertimbangan ekonomi.
F. PURIFIKASI XILAN
Purifikasi atau pemurnian merupakan tahapan yang dilakukan dengan tujuan agar hemiselulosa yang diperoleh dari tahap ekstraksi lebih murni dan homogen. Purifikasi xilan dapat dilakukan dengan beberapa metode seperti dialisis, kromatografi kolom dan metode pengendapan (Fengel dan Wegener, 1995).
Metode pengendapan merupakan metode yang paling banyak digunakan karena metode ini relatif sederhana dan menghasilkan xilan dengan kemurnian yang tinggi. Proses pemurnian ini meliputi beberapa tahap pengendapan ekstrak, yaitu dengan cara pengasaman dan penambahan pelarut organik netral seperti etanol, metanol, atau aseton ke dalam larutan ekstrak hemiselulosa (Fengel dan Wegener, 1995).
Sama halnya dengan Fengel dan Wegener (1995), Sjostrom (1995), menyatakan bahwa pelarutan bertingkat ekstrak hemiselulosa pada konsentrasi alkali rendah dapat digunakan untuk memisahkan komponen-komponen hemiselulosa secara kasar. Hemiselulosa dapat diendapkan dari larutan alkali dengan pengasaman. Penambahan pelarut organik netral seperti etanol akan menghasilkan pengendapan yang lebih sempurna.
G. XILOSA
Xilosa (C5H10O5) merupakan gula (monomer) yang paling banyak
ditemukan dari seluruh gula dalam hemiselulosa (Whistler, 1950). D-xilosa dapat diperoleh melalui hidrolisis tongkol jagung atau xilan (hemiselulosa A) secara asam maupun enzimatis. Gonzales et al. (1985) menyebutkan bahwa hidrolisis hemiselulosa akan menghasilkan tiga jenis monosakarida yaitu xilosa dan arabinosa dalam jumlah yang lebih banyak serta glukosa dalam jumlah yang lebih sedikit. Struktur kimia xilosa dapat dilihat pada Gambar 7.
Gambar 7. Struktur Kimia D-Xilosa (http://es.wikipedia.org/wiki/Xilosa) Xilosa sebagai produk hidrolisis xilan dapat digunakan dalam pembuatan tablet dan artificial low calorie sweeteners (Kulkarni, 1999). Selain itu ditinjau dari sifatnya yang tidak dapat dimetabolisme, xilosa sangat sesuai digunakan sebagai pemanis pada permen karet karena disamping tidak menyebabkan kegemukan juga tidak merusak gigi. Kegunaan lainnya dari xilosa adalah sebagai bahan campuran pasta gigi karena dapat memperkuat gusi (Ramirez et al., 2002). Melalui proses secara bertahap, xilosa dapat dikonversi menjadi xilitol, etanol, dan produk organik lainnya (Thompson, 1983). Menurut Eiteman et al. (1978), xilosa dapat dikonversi menjadi xilitol melalui proses hidrogenasi (Gambar 8) pada tekanan dan suhu tinggi yaitu pada tekanan 40-70 atm dan suhu antara 80-140°C.
+ H2
H. HIDROLISIS HEMISELULOSA (XILAN)
Hidrolisis adalah pemecahan kimiawi suatu molekul karena pengikatan air, sehingga menghasilkan molekul-molekul yang lebih kecil (Gaman dan Sherrington, 1981). Reaksi hidrolisis dapat dipercepat dengan penambahan asam ataupun enzim sebagai katalis.
Hemiselulosa dapat didegradasi menjadi xilosa dengan menggunakan asam dan enzim. Hidrolisis hemiselulosa secara asam dapat dilakukan dengan dua cara yaitu, hidrolisis dengan menggunakan temperatur yang tinggi atau menggunakan asam konsentrasi tinggi (Kosaric, et al., 1983).
Menurut Elander dan Hsu (1995), hidrolisis hemiselulosa menjadi xilosa menggunakan asam lebih efisien daripada secara enzimatis. Kombinasi yang tepat antara pH, suhu dan lama reaksi dapat menghasilkan rendemen gula (xilosa) yang tinggi.
Hidrolisis hemiselulosa secara enzimatis tidak menghasilkan produk yang beracun, namun proses ini tidak efektif dalam memproduksi gula sederhana, selain karena harga enzim sangat mahal, proses hidrolisis xilan secara enzimatis hanya menghasilkan monosakarida dalam jumlah yang sedikit dan menghasilkan oligosakarida dalam jumlah yang lebih tinggi (Hespell et al., 1997). Hidrolisis sempurna xilan memerlukan aktivitas sinergis kelompok enzim hemiselulosa (hidrolitik), di antaranya adalah enzim endo-b-xilanase dan exo-b-xilosidase (Saddler, 1993). Enzim endo-b-endo-b-xilanase berperan dalam memutus ikatan β-1,4 pada bagian dalam dari rantai xilan sehingga dihasilkan xilooligosakarida (baik bercabang maupun tidak) yang meliputi xilopentosa, xilotetraosa, xilotriosa dan xilobiosa. Sedangkan enzim exo-b-xilosidase berfungsi dalam menghidrolisis xilooligosakarida rantai pendek menjadi xilosa. Enzim ini bekerja dengan memutus ujung-ujung non-pereduksi dari rantai xilooligosakarida (Saha, 2000).
Sama halnya dengan Hespell et al., Wayman (1986), menyebutkan bahwa gula yang dihasilkan dari hemiselulosa terutama xilosa lebih mudah diperoleh melalui hidrolisis asam yang biasanya dilakukan pada suhu 100-160 oC, meskipun pada proses ini dapat dihasilkan produk samping
seperti furfural. Hemiselulosa (xilan) jika dihidrolisis dengan asam akan terurai menjadi molekul-molekul yang lebih kecil, yaitu sebagai berikut.
Xilan xilooligosakarida xilosa furfural produk dekomposisi Pada umumnya, komponen terlarut yang terdapat pada hasil hidrolisis xilan adalah xilosa, glukosa dan arabinosa. Namun, jika proses hidrolisis tidak terkontrol maka selain tiga komponen gula tersebut juga dihasilkan furfural atau 5-hidroksimetilfurfural dan asam-asam organik seperti asam format dan asam asetat (Soltes, 1983). Untuk mencegah terjadinya degradasi xilosa menjadi furfural dan asam organik, hidrolisis sebaiknya dilakukan pada suhu di bawah 180 oC dan konsentrasi asam di bawah 1 % (Pessoa et al., 1997). Sedangkan menurut Sjostrom (1995), hidrolisis hemiselulosa agar tidak terbentuk furfural adalah pada suhu di bawah 130 oC.
Furfural (C5H4O2) merupakan senyawa organik turunan dari golongan
furan. Senyawa ini berfasa cair berwarna kuning hingga kecoklatan dengan titik didih 161.7oC, densitas (20oC) adalah 1.16 g/cm3. Furfural merupakan senyawa yang kurang larut dalam air namun larut dalam alkohol, eter, dan benzena (http://www.chem-is-try.org). Gambar 9. menunjukkan struktur molekul furfural.
Gambar 9. Struktur Molekul Furfural (http://www.chem-is-try.org) Menurut Ladish (1989) dan Cao et al. (1995), hemiselulosa jika dihidrolisis sempurna secara asam akan menjadi D-xilosa 50-70 % b/b dan L-arabinosa 5-15 % b/b. Secara umum, asam yang digunakan dalam proses hidrolisis xilan menjadi xilosa adalah asam kuat seperti asam sulfat dan asam klorida dengan konsentrasi antara 0,1-6,0 persen. Proses hidrolisis tersebut berlangsung selama 30 sampai 240 menit dan suhu 100-180 oC (Buckl et al., 1976).
Hidrolisis xilan dari tongkol jagung berdasarkan hasil penelitian Anggraini (2003) yang menggunakan asam sulfat 0,3; 0,5 dan 1 % (v/v) dengan dihidrolisis selama 60 menit diperoleh konsentrasi asam optimal sebesar 0,3 % yang menghasilkan rendemen xilosa sekitar 83,12 %, gula pereduksi 89,23 mg/ml, total gula 94,57 mg/ml, derajat polimerisasi 1,06, kadar bahan kering 15,33 % dan kejernihan 46,99 %T.
Selain asam sulfat, asam kuat lainnya yang dapat digunakan dalam proses hidrolisis xilan menjadi xilosa adalah asam klorida. Perbandingan karakteristik asam sulfat dan asam klorida disajikan pada Tabel 4.
Tabel 6. Perbandingan Karakteristik HCl dan H2SO4
Parameter HCl (Asam Klorida) H2SO4 (Asam Sulfat)
Keasaman (pKa) −8,0 *) -3,0 **)
Bahaya utama Korosif *) membakar bahan organik**) Sangat korosif dan bersifat Harga/l Rp. 11.000,- Rp. 12.000,-
*) http://en.wikipedia.org/Hydrochloric_acid **) http://en.wikipedia.org/Sulfuric_acid
pKa sebagaimana pH digunakan untuk menunjukkan kekuatan suatu
asam. pKa mempunyai rumus sebagai berikut. pKa = - log Ka
Nilai Ka untuk asam kuat adalah sangat besar, sehingga akan dihasilkan nilai pKa yang rendah. Semakin kecil nilai pKa suatu asam maka asam tersebut semakin kuat (Staf Pengajar Kimia dasar I, 2004).
Berdasarkan karakteristiknya tersebut, maka HCl sangat berpotensi untuk digunakan dalam menghidrolisis xilan menjadi xilosa. Hal ini telah dibuktikan oleh Kurakake et al. (2005) yang menghidrolisis xilan dari kulit biji jagung dengan HCl 0,2 M. Berdasarkan penelitiannya, hidrolisis pada suhu 125 oC selama 20 menit menghasilkan xilosa sebanyak 290 mg/g dan rendemen sebesar 99 %.
III. METODOLOGI PENELITIAN
A. BAHAN DAN ALAT
Bahan baku yang digunakan dalam penelitian ini adalah tongkol jagung dan xilan hasil ekstraksi. Tongkol jagung yang digunakan dalam penelitian berasal dari jagung varietas BISMA berasal dari daerah kediri (Jawa Timur), BISI dan P-21 yang berasal dari Cina. Tongkol jagung tersebut digiling sampai ukuran kurang lebih 10 mesh.
Bahan kimia yang dipergunakan dalam penelitian ini dibagi menjadi dua bagian, yaitu bahan kimia untuk ekstraksi dan bahan kimia untuk hidrolisis xilan. Bahan kimia untuk ekstraksi xilan terdiri dari NaOCl 1 %, NaOH 15 %, HCl 6 N dan etanol 95 %. Bahan kimia untuk hidrolisis xilan terdiri dari HCl dengan konsentrasi 0,3; 0,5; 0,7 % (v/v), Na2CO3 30 %, arang aktif, serta
bahan-bahan kimia untuk analisis.
Peralatan yang diperlukan diantaranya adalah timbangan analitik, sentrifus, otoklaf, penyaring vakum, oven, alat-alat gelas, dan spektofotometer. Peralatan ini digunakan untuk proses ekstraksi, hidrolisis xilan serta analisis xilosa yang dihasilkan.
B. METODE PENELITIAN 1. Analisis Proksimat
Tongkol jagung sebelum diekstraksi kandungan hemiselulosanya (xilan) terlebih dahulu dianalisis komposisi kimianya, yaitu meliputi kadar air, abu, lemak, serat kasar, protein, karbohidrat (by difference), hemiselulosa, selulosa dan lignin. Prosedur analisis proksimat tongkol jagung dapat dilihat pada Lampiran 1.
2. Ekstraksi dan Purifikasi Xilan dari Tongkol Jagung
Proses ekstraksi dan purifikasi xilan dari tongkol jagung dilakukan berdasarkan penelitian Widyani (2002) dan Adam (1965).
a. Delignifikasi (Widyani, 2002)
Delignifikasi dilakukan dengan memasukan sampel ke dalam wadah plastik dan direndam dalam larutan NaOCl 1 % selama 5 jam pada suhu ruang. Setelah 5 jam, sampel dibilas dengan air dan disaring. Sampel kemudian dikeringkan pada suhu 50 0C selama 48 jam dan sampel selanjutnya siap untuk diekstraksi.
b. Ekstraksi Xilan Metode Asidifikasi (Widyani, 2002)
Ekstraksi xilan dilakukan dengan menggunakan metode asidifikasi, yaitu xilan diperoleh dari proses pemisahan larutan hemiselulosa yang bersifat alkali setelah diasamkan hingga pH 4,5-5,0. Metode ekstraksi ini didasarkan pada sifat xilan yang tidak larut dalam asam tetapi larut dalam alkali.
Pada penelitian ini, ekstraksi dilakukan dengan merendam bubuk tongkol kering hasil delignifikasi dalam larutan NaOH 15 % selama 24 jam pada suhu ruang. Setelah 24 jam perendaman, dilakukan penyaringan untuk memperoleh filtrat. Filtrat yang dihasilkan ditampung untuk diukur pH-nya dan selanjutnya diasamkan dengan HCl 6 N hingga pH 4,5-5,0. Sedangkan ampasnya (fraksi selulosa) dibuang karena tidak terpakai.
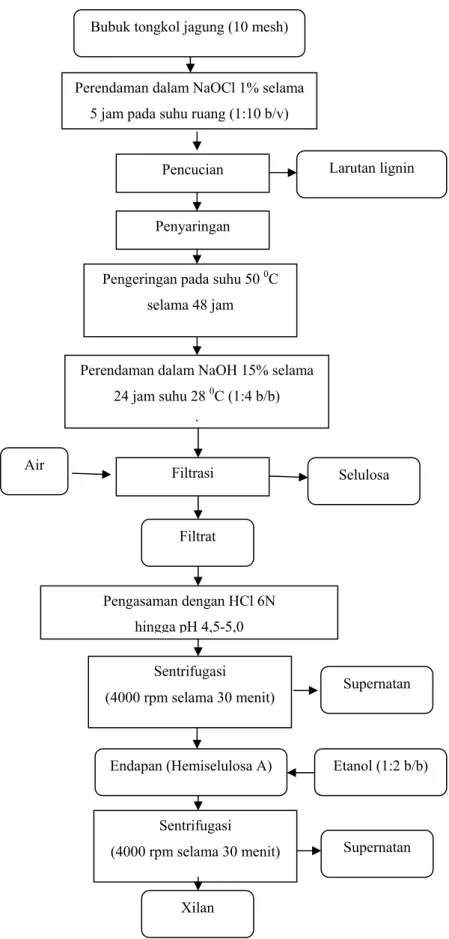
Filtrat hasil pengasaman selanjutnya disentrifugasi dengan kecepatan 4000 rpm selama 30 menit untuk memisahkan endapan (xilan kasar) dengan cairannya (supernatan). Kemudian, xilan didispersikan dalam etanol 95 %, dan disentrifugasi kembali dengan kecepatan dan waktu yang sama dengan sebelumnya. Diagram alir proses ekstraksi xilan metode asidifikasi dapat dilihat pada Gambar 10.
Bubuk tongkol jagung (10 mesh)
Perendaman dalam NaOCl 1% selama 5 jam pada suhu ruang (1:10 b/v)
Larutan lignin Pencucian
Penyaringan Pengeringan pada suhu 50 0C
selama 48 jam
:
Selulosa
Filtrat Filtrasi
Perendaman dalam NaOH 15% selama 24 jam suhu 28 0C (1:4 b/b) Air hingga pH 4,5-5,0 Pengasaman dengan HCl 6N Supernatan Etanol (1:2 b/b) Endapan (Hemiselulosa A) Sentrifugasi (4000 rpm selama 30 menit) Supernatan Xilan (4000 rpm selama 30 menit) Sentrifugasi
Gambar 10. Diagram Alir Proses Ekstraksi Xilan Metode Asidifikasi (Widyani, 2002)
c. Purifikasi Xilan (Adam, 1965)
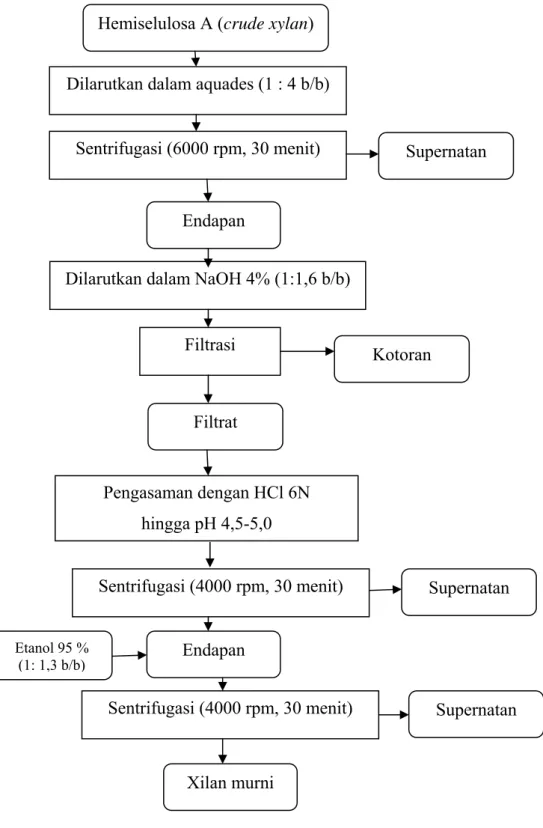
Endapan xilan (hemiselulosa A) yang diperoleh dari tahap ekstraksi dilarutkan dalam air, kemudian disentrifus dengan kecepatan putaran 6000 rpm selama 30 menit. Endapan yang diperoleh dilarutkan dalam NaOH 4 %. Larutan alkali yang mengandung xilan tersebut kemudian disaring untuk memisahkan kotoran-kotoran yang terdapat di dalamnya. Filtrat yang diperoleh diasamkan kembali dengan HCl 6 N hingga pH 4,5-5,0, kemudian dilakukan sentrifugasi pada kecepatan 4000 rpm selama 30 menit untuk memperoleh endapan (xilan murni). Diagram alir proses purifikasi xilan dapat dilihat pada Gambar 11. Analisis yang dilakukan terhadap xilan hasil purifikasi meliputi kadar air (Lampiran 1) dan rendemen. Rendemen dinyatakan dalam persentase berat kering (%bk) dan dihitung berdasarkan rumus berikut (Anggraini, 2003). 100% b) x (ka -b a bk) (% Rendemen = x dimana : a = bobot xilan (g)
b = bobot tongkol jagung yang diekstraksi (%) ka = kadar air xilan (%)
3. Hidrolisis Xilan Secara Asam (Arifin, 1990)
Hidrolisis xilan menjadi xilosa dilakukan dengan menggunakan metode hidrolisis asam. Xilan tongkol jagung dilarutkan dalam HCl berkonsentrasi 0,3; 0,5 dan 0,7 % (v/v) dengan perbandingan 1 : 4 (b/v). Larutan kemudian diotoklaf pada suhu 105°C, tekanan 0,05 mPa selama 1, 2, 3, 4 dan 5 jam. Filtrat hasil hidrolisis yang diperoleh dinetralkan dengan Na2CO3 30 % hingga pH-nya mencapai 5, selanjutnya filtrat dijernihkan
dengan arang aktif (2 % b/v larutan), dipanaskan pada suhu 80-90°C selama 15 menit, dan filtratnya disaring dengan kertas saring Whatman nomor 41. Diagram alir proses hidrolisis xilan secara asam dapat dilihat pada Gambar 12. Analisis yang dilakukan terhadap xilosa hasil hidrolisis
meliputi kadar bahan kering, rendemen, total gula metode Fenol, kadar gula pereduksi metode DNS dan derajat polimerisasi. Prosedur Analisis disajikan pada Lampiran 2.
Hemiselulosa A (crude xylan) Dilarutkan dalam aquades (1 : 4 b/b)
Sentrifugasi (6000 rpm, 30 menit)
Endapan
Supernatan
Filtrasi
Dilarutkan dalam NaOH 4% (1:1,6 b/b)
Sentrifugasi (4000 rpm, 30 menit) Pengasaman dengan HCl 6N hingga pH 4,5-5,0 Sentrifugasi (4000 rpm, 30 menit) Kotoran Filtrat Supernatan Supernatan Endapan Etanol 95 % (1: 1,3 b/b) Xilan murni
Xilan bubuk (20 mesh)
Dilarutkan dalam HCl 0,3%; 0,5%; 0,7% v/v (1:4 b/v)
Hidrolisis dalam otoklaf , 105 0C,
0,05 mPa selama 1, 2, 3,4 & 5 jam Penetralan dengan Na2CO3 30 %
sampai pH 5
Penambahan arang aktif sebanyak 2% (b/v larutan)
Pemanasan pada suhu 85-90 0C
Selama 15 menit
Filtrat jernih (xilosa)
Filtrasi dengan kertas Whatman nomor 41 Kotoran
Gambar 12. Diagram Alir Proses Hidrolisis Xilan Secara Asam (Arifin, 1990)
C. RANCANGAN PERCOBAAN
Rancangan percobaan yang digunakan pada penelitian ini adalah Rancangan Acak Lengkap Faktorial 5 x 3 (Walpole, 1992). Faktor pertama menunjukkan waktu hidrolisis dengan 5 taraf faktor (1, 2, 3, 4 dan 5 jam) sedangkan faktor kedua menunjukkan konsentrasi HCl dengan 3 taraf faktor (0,3 %; 0,5 % daan 0,7 %), sehingga rancangan percobaan yang dilakukan memiliki 15 unit percobaan dengan replikasi sebanyak 2 kali. Model yang digunakan untuk desain Rancangan Percobaan Acak Lengkap tersebut adalah sebagai berikut.
Yijk = u + Ai + Bj + ABij + Єk(ij)
Dengan i = 1, 2, 3, 4, 5 ; j = 1, 2, 3, 4, 5 ; k = 1, 2 Dimana
Yijk = variabel respon dari hasil observasi ke-k yang terjadi karena pengaruh
taraf ke-i faktor waktu hidrolisis dan taraf ke-j konsentrasi HCl. u = nilai tengah populasi.
Ai = efek dari taraf ke-i faktor waktu hidrolisis.
BBj = efek dari taraf ke-j faktor konsentrasi HCl.
ABij = efek interaksi antara taraf ke-i faktor waktu hidrolisis dan taraf ke-j
faktor konsentrasi HCl.
Єk(ij) = galat percobaan dari perlakuan waktu hidrolisis ke-i dan perlakuan
IV. HASIL DAN PEMBAHASAN
A. ANALISIS PROKSIMAT
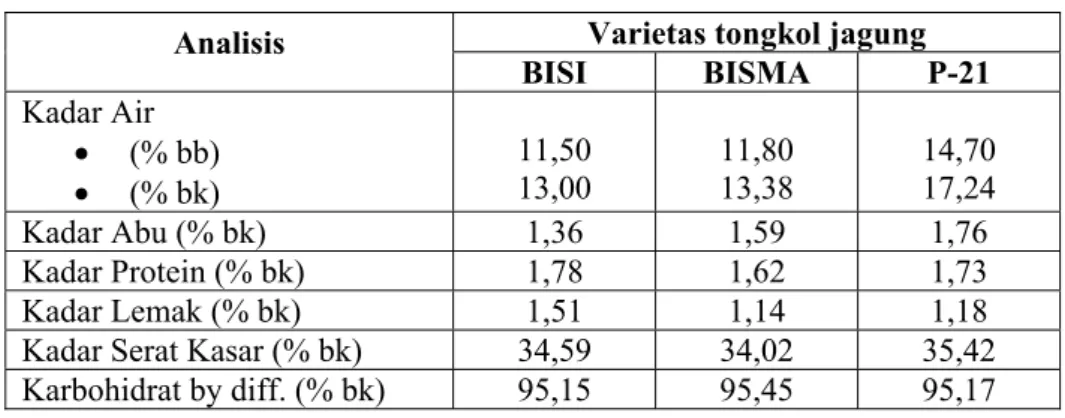
Analisis proksimat tongkol jagung terdiri dari analisis kadar air, abu, protein, lemak, serat kasar, karbohidrat (by diff.), hemiselulosa, selulosa, dan lignin. Hasil analisis proksimat ketiga varietas tongkol jagung tersebut dapat dilihat pada Tabel 7 dan 8.
Tabel 7. Hasil Analisis Proksimat Tongkol Jagung Varietas tongkol jagung Analisis BISI BISMA P-21 Kadar Air • (% bb) • (% bk) 11,50 13,00 11,80 13,38 14,70 17,24 Kadar Abu (% bk) 1,36 1,59 1,76 Kadar Protein (% bk) 1,78 1,62 1,73 Kadar Lemak (% bk) 1,51 1,14 1,18
Kadar Serat Kasar (% bk) 34,59 34,02 35,42
Karbohidrat by diff. (% bk) 95,15 95,45 95,17
Tabel 8. Komposisi Serat Tongkol Jagung
Varietas tongkol jagung Analisis (% bk)
BISI BISMA P-21
Kadar Hemiselulosa 29,40 41,66 16,89
Kadar Selulosa 52,66 43,66 61,41
Kadar Lignin 13,10 8,55 19,89
Kadar Bahan lainnya 17,84 19,51 19,04
Kadar air perlu dianalisis karena kadar air sangat berpengaruh terhadap mutu dan daya simpan bahan. Semakin tinggi kadar air suatu bahan maka daya simpannya semakin rendah. Berdasarkan hasil analisis, tongkol jagung varietas BISI mempunyai kadar air 11,50 %, BISMA 11,80 %, dan P-21 14,70 % (bb). Hal ini menunjukkan bahwa tongkol jagung varietas BISI dan BISMA yang digunakan dalam penelitian ini relatif kering, sehingga tongkol jagung dapat disimpan dalam jangka waktu yang lama. Sedangkan tongkol jagung varietas P-21 dengan kadar air sebesar 14,70 % bb (± aw : 0,97) sangat rentan dalam penyimpanannya karena kadar air yang tinggi memberikan peluang
yang cukup besar bagi pertumbuhan mikroorganisme terutama kapang yang dapat hidup pada substrat dengan kadar air yang cukup rendah. Menurut Fardiaz (1989), batas kadar air minimum dimana mikroba masih dapat tumbuh adalah 14-15 % bb.
Abu merupakan zat organik dalam bahan yang tidak mudah terbakar selama proses pembakaran. Kadar abu menunjukkan besarnya kandungan zat organik atau unsur mineral suatu bahan. Kadar abu sangat dipengaruhi oleh jenis bahan yang dianalisis, umur bahan, dan lain-lain. Berdasarkan hasil analisis, kadar abu tongkol jagung adalah 1,36-1,76 % bk. Kadar abu tertinggi diperoleh dari tongkol jagung varietas P-21 dan terendah adalah varietas BISI. Perbedaan kandungan abu ketiga varietas tongkol jagung tersebut dapat disebabkan oleh perbedaan penambahan pupuk dan kondisi tanah tempat tumbuh jagung tersebut.
Lemak merupakan zat ekstraktif, yaitu senyawa yang larut dalam pelarut organik seperti dietil eter, petroleum eter, aseton dan lain-lain (Fengel dan Wegener, 1995). Berdasarkan hasil analisis, ketiga varietas tongkol jagung tersebut mempunyai kadar lemak antara 1,14-1,51 % bk. Kandungan lemak dalam tongkol jagung sangat berpengaruh terhadap efektifitas proses ekstraksi xilan. Kadar lemak tongkol jagung yang tinggi dapat menghambat proses delignifikasi, yaitu menghambat masuknya larutan NaOCl 1 % ke dalam struktur lignin, karena lemak bersifat tidak larut dalam NaOCl, sehingga lignin yang dihilangkan tidak maksimal dan hal ini dapat mengakibatkan proses ekstraksi xilan juga berlangsung tidak optimal.
Kadar protein merupakan parameter analisis yang juga penting karena dapat mempengaruhi mutu produk (xilosa) yang dihasilkan. Hasil analisis menunjukan bahwa kadar protein dari ketiga varietas tongkol jagung tersebut berkisar 1,62-1,78 % bk. Kadar protein yang tinggi dapat menyebabkan xilosa yang dihasilkan berwarna gelap akibat terjadinya reaksi Maillard, yaitu reaksi antara xilosa (gula pereduksi) dengan gugus amino pada suhu tinggi dan menimbulkan warna kecoklatan. Pada proses pemanasan suhu tinggi dengan katalis asam atau basa, gula pereduksi akan mengalami karamelisasi atau reaksi Maillard (Winarno, 1984).
Kadar serat kasar adalah residu dari bahan makanan atau pertanian setelah diperlakukan dengan asam atau alkali mendidih (Fardiaz dan Rambitan, 1989). Kadar serat kasar terdiri dari selulosa, hemiselulosa dan sebagian kecil lignin. Menurut Maynard dan Loosli (1993), tongkol jagung terdiri dari 35,5 % serat kasar dan menurut Anonimous (1981), tongkol jagung mengandung selulosa (40 %), hemiselulosa (36 %), lignin (16 %) dan zat-zat lainnya (8 %).
Berdasarkan hasil penelitian, kadar serat kasar tongkol jagung sekitar 34,02-35,42 % bk. Kandungan serat dari tongkol jagung varietas BISMA adalah paling rendah (34,02 %) dan varietas P-21 yang paling tinggi (35,42 %). Analisis lebih lanjut dari kandungan serat ketiga varietas tongkol jagung tersebut menunjukkan bahwa kandungan serat dari varietas BISMA terdiri dari 41,66 % bk hemiselulosa, 43,66 % bk selulosa, dan 8,55 % bk lignin, varietas BISI terdiri dari 29,40 % bk hemiselulosa, 52,66 % bk selulosa, dan 13,10 % bk lignin, sedangkan varietas P-21 terdiri dari selulosa yaitu sebesar 61,41 % bk, 16,89 % bk hemiselulosa, dan 19,89 % bk lignin.
Berdasarkan hasil analisis kandungan hemiselulosa, diperkirakan bahwa tongkol jagung varietas BISMA adalah varietas tongkol jagung yang akan menghasilkan rendemen xilan tertinggi, sedangkan varietas P-21 akan menghasilkan xilan dalam jumlah yang relatif sedikit.
B. EKSTRAKSI DAN PURIFIKASI XILAN
Ekstraksi merupakan proses pemisahan atau pengisolasian suatu komponen tertentu dari suatu bahan. Pada proses ekstraksi xilan, tongkol jagung yang digunakan berupa bubuk berukuran 10 mesh. Hal ini dilakukan agar proses ekstraksi dapat berlangsung dengan optimal. Proses ekstraksi xilan dari tongkol jagung terdiri atas dua tahapan utama, yaitu tahap delignifikasi dan ekstraksi. Neraca massa proses ekstraksi xilan disajikan pada Lampiran 3.
Tahap awal proses ekstraksi adalah delignifikasi. Menurut Fridia (1989), proses delignifikasi merupakan perlakuan pendahuluan terhadap bahan baku yang berfungsi untuk membebaskan lignin dan selulosa. Pada penelitian ini, proses delignifikasi dilakukan dengan menggunakan pelarut NaOCl 1 %, karena ion-ion hipoklorit yang terkandung dalam pelarut tersebut mampu
memecah ikatan eter yang terdapat pada lignin. Menurut Sjostrom (1995), ion-ion hipoklorit tersebut akan mendorong terjadinya pemecahan ikatan-ikatan eter dan meningkatkan hidrofilitas lignin karena adanya pelepasan gugus-gugus hidroksi fenol. Lignin yang terdegradasi tersebut larut pada media delignifikasi dalam bentuk senyawa keton.
Ekstraksi xilan dilanjutkan dengan merendam bahan dalam larutan NaOH 15 %. Larutan NaOH 15 % ini dipilih karena berdasarkan penelitian Anggraini (2003) dan Widyani (2002), ekstraksi xilan dengan NaOH 15 % menghasilkan rendemen yang tinggi, xilan yang dihasilkan berwarna lebih putih, relatif bersih dari pengotor, dan mudah larut dalam air.
Tahap berikutnya dari ekstraksi xilan ini adalah purifikasi, karena xilan yang diperoleh dari tahap ekstraksi masih mengandung material lain yang ikut terendapkan selama proses asidifikasi, seperti β-selulosa dan garam. Oleh karena itu diperlukan tahap purifikasi untuk memperoleh fraksi xilan yang lebih murni. Menurut Anggraini (2003), untuk memperoleh xilan dengan kemurnian yang tinggi maka xilan perlu dimurnikan dengan menggunakan etanol 95 %.
Xilan hasil pemurnian selanjutnya dikeringkan pada suhu 50 oC selama 12 jam sampai kadar airnya kurang dari 10 % agar xilan lebih mudah dan aman untuk disimpan. Suhu 50 oC dipilih karena hemiselulosa (xilan) tidak tahan terhadap suhu tinggi (Sjostrom, 1995). Berdasarkan hasil penelitian, rendemen xilan dari tongkol jagung yang diekstraksi (1 kg) adalah sekitar 7,75-12,24 % bk. Nilai rendemen tersebut sesuai dengan Whistler (1950) yang menyatakan bahwa rendemen xilan hasil ekstraksi dari bahan-bahan yang mengandung xilan rata-rata adalah 10 %. Rendemen xilan tertinggi diperoleh dari varietas BISMA (12,24 % bk) dan terendah adalah P-21 (7,75 % bk).
Berdasarkan perhitungan efisiensi ekstraksi xilan terhadap kandungan hemiselulosa masing-masing varietas tongkol jagung tersebut, diperoleh nilai efisiensi antara 29,32-45,89 %. Efisiensi ekstraksi xilan terhadap kandungan hemiselulosa tertinggi diperoleh dari tongkol jagung varietas P-21 yaitu 45,89% bk, dan yang terendah adalah BISI sebesar 29,32 % bk (Tabel 9). Efisiensi ekstraksi xilan tersebut dipengaruhi oleh banyaknya fraksi
hemiselulosa yang dapat larut dalam pelarut alkali. Hemiselulosa tidak dapat diekstraksi seratus persen karena beberapa hal diantaranya adalah adanya sebagian kecil hemiselulosa yang terikat pada alfa selulosa sehingga tidak larut dalam alkali, larutnya sebagian hemiselulosa selama proses delignifikasi dan tidak semua hemiselulosa mengendap pada saat purifikasi dengan etanol (Whistler, 1950).
Berdasarkan data tersebut, maka dapat disimpulkan bahwa varietas BISMA merupakan varietas yang paling baik digunakan dalam menghasilkan xilan. Hal ini dikarenakan dari bobot tongkol jagung yang sama (1 kg) untuk semua varietas, varietas BISMA menghasilkan rendemen xilan tertinggi. Meskipun varietas P-21 mempunyai efisiensi ekstraksi xilan dari persentase hemiselulosa yang tertinggi, namun rendemen xilan yang dihasilkan dari 1 kg bahan (tongkol jagung) lebih rendah daripada varietas lain, yaitu 7,75 % bk.
Tabel 9. Rendemen Xilan Hasil Ekstraksi dan Purifikasi
Parameter BISMA BISI P-21
Rendemen xilan dari tongkol jagung (%bk) 12,24 8,62 7,75
Efisiensi ekstraksi xilan dari persentase
hemiselulosa (%) 29,38 29,32 45,89
Kadar air (% bb) 3,64 4,61 4,61
C. HIDROLISIS XILAN
Hidrolisis merupakan proses pemecahan molekul substrat di dalam air. Xilan yang merupakan polisakarida akan terpecah menjadi xilan yang rantainya lebih pendek dengan media air dan katalis asam. Reaksi dasar dalam hidrolisis xilan menjadi xilosa dengan asam adalah pemotongan ikatan β-1,4-D-xilopiranosa dari xilan. Xilan jika dihidrolisis dengan asam akan terurai menjadi molekul-molekul yang lebih kecil, yaitu sebagai berikut.
Xilan xilooligosakarida xilosa furfural produk dekomposisi Pada umumnya, komponen terlarut yang terdapat pada hasil hidrolisis xilan adalah xilosa, glukosa, dan arabinosa. Namun, jika proses hidrolisis tidak terkontrol maka selain tiga komponen gula tersebut juga dihasilkan
furfural atau 5-hidroksimetilfurfural dan asam-asam organik seperti asam format dan asam asetat (Soltes, 1983). Oleh karena itu, kondisi hidrolisis seperti suhu, konsentrasi asam dan lama hidrolisis harus terkontrol agar tidak dihasilkan produk yang tidak diinginkan.
Pada penelitian ini hidrolisis xilan dilakukan dengan menambahkan asam klorida. Xilan yang telah digiling dengan ukuran 20 mesh (Gambar 13) dimasukkan ke dalam labu erlenmeyer dan ditambahkan larutan HCl 0,3; 0,5 dan 0,7 % (v/v) dengan perbandingan 1: 4 (b/v), kemudian dihidrolisis dengan menggunakan otoklaf pada suhu 105 oC selama 1, 2, 3, 4 dan 5 jam. Neraca
massa proses hidrolisis xilan dapat dilihat pada Lampiran 4.
Gambar 13. Xilan Tongkol Jagung Kering
Proses hidrolisis xilan dihentikan dengan penetralan yaitu dengan menambahkan alkali, pada penelitian ini digunakan larutan natrium karbonat 30 %. Proses netralisasi ini akan menghasilkan garam dan air. Reaksi antara natrium karbonat dan HCl yang terjadi pada proses penetralan ini adalah sebagai berikut.
Setelah proses penetralan, kemudian dilakukan proses pemucatan dengan menggunakan arang aktif agar dihasilkan larutan xilosa yang jernih. Dalam indusri xilosa yang sebenarnya, larutan xilosa jernih yang dihasilkan dari proses hidrolisis ini akan dimurnikan dan dikristalisasi sehingga didapatkan produk akhir berupa xilosa murni dalam bentuk bubuk kristal putih (Gambar 14). Namun dalam penelitian ini, tahapan pemurnian dan krisalisasi tidak dilakukan sehingga hasil akhir yang diperoleh adalah xilosa dalam bentuk
larutan. Larutan xilosa ini kemudian dianalisis untuk mengetahui kualitas dan kuantitasnya, yaitu meliputi kadar bahan kering, rendemen, total gula, gula pereduksi dan derajat polimerisai.
Filtrat xilosa jernih Ion exchange Evaporasi Kristalisasi Sentrifugasi Pengeringan Penyaringan Serbuk kristal xilosa Dekolorisasi Sentrifugasi Etanol 50 % v/v
Gambar 14. Tahap Pemurnian Xilosa (Nicoletta et al., 2002)
1. Bahan Kering
Kadar bahan kering xilosa adalah semua komponen dalam larutan xilosa selain air dan bahan volatil. Kadar bahan kering yang tinggi dapat menunjukkan tingkat kesempurnaan proses hidrolisis. Kadar bahan kering yang tinggi disebabkan oleh banyaknya kandungan monosakarida (xilosa) dalam larutan.
Kadar bahan kering xilosa hasil hidolisis rata-rata adalah 16,17-20,00%. Kadar bahan kering cenderung meningkat seiring dengan meningkatnya waktu hidrolisis dan konsentrasi HCl yang digunakan. Kadar bahan kering tertinggi diperoleh dari perlakuan hidolisis dengan menggunakan HCl 0,5 % dan dihidrolisis selama 4 jam (20,00 %). Sedangkan bahan kering terendah diperoleh dari hasil hidrolisis selama 1 jam pada konsentrasi 0,3 % (16,17 %). Grafik hubungan antara konsentrasi
9.00 14.00 19.00 24.00
1 2 3 4 5 6
Waktu Hidrolisis (jam ke-)
B a ha n K e ri ng ( % ) 0.30% 0.50% 0.70%
HCl dan waktu hidrolisis terhadap bahan kering xilosa dapat dilihat pada Gambar 15.
Gambar 15. Grafik Hubungan antara Konsentrasi HCl dengan Waktu Hidrolisis terhadap Bahan Kering Xilosa.
Hasil analisis ragam pada taraf α = 0,05 menunjukkan bahwa, konsentrasi asam dan interaksi antara waktu hidrolisis dengan konsentrasi asam tidak berpengaruh nyata terhadap nilai bahan kering xilosa. Sedangkan waktu hidrolisis memberikan pengaruh yang nyata terhadap tingginya bahan kering xilosa. Hal ini menunjukan bahwa peningkatan waktu hidrolisis akan meningkatkan kadar bahan kering xilosa secara signifikan. Uji lanjut Duncan terhadap waktu hidrolisis menunjukkan bahwa hidrolisis selama 4 jam (bahan kering rata-rata : 19,25 %) merupakan perlakuan yang menghasilkan bahan kering tertinggi. Analisis keragaman terhadap bahan kering dapat dilihat pada Lampiran 5.
Lama hidrolisis mempengaruhi kadar bahan kering xilosa karena semakin lama suatu bahan dihidrolisis maka pemutusan rantai β-xilopiranosil yang terjadi akan semakin banyak pula, sehingga xilosa yang diperoleh semakin tinggi.
2. Rendemen
Rendemen merupakan salah satu parameter keberhasilan proses hidrolisis. Besarnya nilai rendemen salah satunya ditentukan oleh bobot xilosa yang dihasilkan dan kadar bobot kering xilosa. Dengan demikian, apabila bobot xilosa dan bobot bahan kering tinggi maka rendemen xilosa pun tinggi.
38.00 46.00 54.00 62.00
0 1 2 3 4 5 6
Waktu Hidrolis is (jam ke -)
Ren d em en X il o s a ( % ) 0.30% 0.50% 0.70%
Berdasarkan hasil penelitian, rendemen xilosa hasil hidrolisis dengan menggunakan HCl berkisar antara 40,51-60,37 %. Rendemen xilosa tertinggi didapatkan dari perlakuan menggunakan HCl 0,5 % dan dihidrolisis selama 4 jam (60,37 %), sedangkan rendemen terendah didapatkan dari perlakuan menggunakan HCl 0,3 % dan dihidrolisis selama 1 jam (40,51 %). Grafik hubungan antara Konsentrasi HCl dan waktu hidrolisis terhadap rendemen xilosa dapat dilihat pada Gambar 16.
Gambar 16. Grafik Hubungan antara Konsentrasi HCl dengan Waktu Hidrolisis terhadap Rendemen Xilosa.
Rendemen xilosa hasil hidrolisis dipengaruhi oleh kondisi hidrolisis seperti konsentrasi asam yang digunakan, jenis asam, suhu, dan lamanya hidrolisis. Pada umumnya semakin tinggi konsentrasi asam, semakin kuat asam yang digunakan, semakin tinggi suhu dan semakin lama hidrolisis rendemen xilosa yang dihasilkan semakin tinggi. Berdasarkan grafik di atas terlihat bahwa rendemen cenderung meningkat seiring meningkatnya konsentrasi HCl dan waktu hidrolisis. Hasil analisis ragam pada taraf α = 0,05 menunjukkan bahwa waktu hidrolisis berpengaruh nyata terhadap rendemen xilosa. Peningkatan waktu hidolisis akan mempengaruhi besarnya rendemen xilosa secara signifikan.
Waktu reaksi yang lama memungkinkan xilan terhidrolisis sempurna. Reaksi yang berlangsung lama akan memberikan kesempatan yang besar untuk terjadinya penetrasi asam ke bagian dalam struktur xilan yang amorf sehingga pemutusan rantai β-D-xilopiranosil semakin banyak. Hasil pemutusan ikatan rantai β-D-xilopiranosil ini akan menghasilkan gula-gula sederhana terutama xilosa.
Hasil uji lanjut Duncan pada taraf α = 0,05 menunjukkan perlakuan terbaik adalah hidrolisis selama 4 jam (rendemen rata-rata : 56,813 %). Perlakuan tersebut menghasilkan rendemen yang tertinggi dibandingkan dengan perlakuan hidrolisis selama 5 jam (rendemen rata-rata 55,283 %). Analisis keragaman terhadap rendemen xilosa dapat dilihat pada Lampiran 6. 60.0 70.0 80.0 90.0 100.0 0 2 4 6
Waktu Hidrolisis (jam ke-)
T o ta l G u la ( m g /m l) 0.30% 0.50% 0.70% 3. Total Gula
Total gula merupakan seluruh gula bebas yang dilepaskan dari hidrolisis xilan menggunakan asam. Total gula hasil hidrolisis ditetapkan berdasarkan Metode Fenol dengan prinsip bahwa gula sederhana, oligosakarida, polisakarida dan turunannya dapat bereaksi dengan fenol dalam asam sulfat pekat menghasilkan warna orange yang stabil. Nilai absorbansi yang diperoleh dihitung dengan menggunakan kurva standar fenol (Lampiran 10).
Berdasarkan penelitian, total gula rata-rata yang dihasilkan berkisar antara 68,85 mg/ml sampai 101,98 mg/ml. Total gula tertinggi diperoleh dari perlakuan hidrolisis xilan menggunakan HCl 0,5 % dan dihidrolisis selama 4 jam, sedangkan perlakuan yang memberikan total gula terendah adalah perlakuan hidrolisis dengan menggunakan HCl 0,3 % dan waktu hidrolisis selama 1 jam. Grafik hubungan antara Konsentrasi HCl dengan waktu hidrolisis terhadap total gula dapat dilihat pada Gambar 17.
Gambar 17. Grafik Hubungan antara Konsentrasi HCl dengan Waktu Hidrolisis terhadap Total Gula.