IDENTIFIKASI PEMBELAJARAN EKSPERIMEN PADA MATA PELAJARAN KIMIA SMA KELAS XII
Tugas Kelompok
Disusunoleh :
1. Alfaruq Chandra Kusuma 2016063608 2. Andi Zulkarnain 2016065973 3. Marlinda Damayanti Nifu 2016079686 4. Muhammad Khaerudin 2016080396 5. Muhammad Sodikin 2016067130
6. Ratiningrum 2016063296
PENDIDIKAN PROFESI GURU
DEPARTEMEN PENDIDIKAN KIMIA
FAKULTAS PENDIDIKAN MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS PENDIDIKAN INDONESIA
▸ Baca selengkapnya: proses pembuatan unsur gas mulia
(2)ANALISIS KEBUTUHAN PEMBELAJARAN EKSPERIMEN PADA KELAS XII
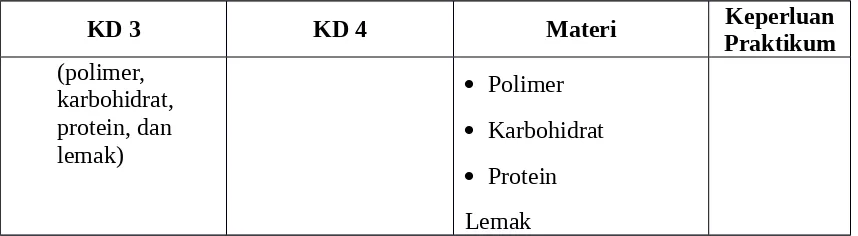
KD 3 KD 4 Materi Keperluan
Praktikum 3.1 Menganalisis penyebab adanya fenomena sifat koligatif larutan pada penurunan tekanan uap, kenaikan titik didih, penurunan titik beku dan tekanan osmosis.
4.1 Menyajikan hasil analisis berdasarkan data percobaan terkait penurunan tekanan uap, kenaikan titik didih, penurunan titik beku, dan tekanan osmosis larutan.
Sifat Koligatif Larutan. Diagram P-T Penurunan tekanan
uap jenuh
Kenaikan titik didih Penurunan titik beku Osmosis dan tekanan
osmosis Ada 3.2 Membedakan sifat koligatif larutan elektrolit dan larutan nonelektrolit.
4.2 Mengolah dan menganalisis data percobaan untuk
membandingka n sifat koligatif larutan elektrolit dengan sifat koligatif larutan nonelektrolit yang konsentrasinya sama.
Sifat koligatif larutan elektrolit dan larutan nonelektrolit Ada 3.3 Mengevaluasi gejala atau proses yang terjadi dalam contoh sel elektrokimia (sel volta dan sel elektrolisis) yang digunakan dalam
kehidupan.
4.3 Menciptakan ide/gagasan produk sel elektrokimia.
Redoks dan Sel Elektrokimia
Penyetaraan persamaan reaksi redoks
Sel Volta dan potensial sel
Tidak ada
3.4 Menganalisis proses yang terjadi dalam sel Volta dan menjelaskan
4.4 Mengajukan ide/gagasan untuk mencegah dan mengatasi terjadinya Penyetaraan persamaan reaksi redoks
Sel Volta dan
KD 3 KD 4 Materi PraktikumKeperluan kegunaannya korosi potensial sel
3.5 Menganalisis faktor-faktor yang
mempengaruhi terjadinya korosi dan cara mengatasinya 4.5 Memecahkan masalah terkait dengan perhitungan sel elektrokimia
Korosi Ada
3.6 Menerapkan stoikiometri reaksi redoks dan hukum Faraday untuk menghitung besaran-besaran yang terkait sel elektrolisis.
4.6 Menalar dan menganalisis kelimpahan, kecenderungan sifat fisik dan sifat kimia, manfaat, dampak, proses pembuatan unsur-unsur golongan utama (gas mulia, halogen, alkali dan alkali tanah, periode 3) serta unsur golongan transisi (periode 4) dan senyawanyadal am kehidupan sehari-hari.
Sel Elektrolisis dan Hukum Faraday
Ada
3.7 Menganalisis kelimpahan, kecenderungan sifat fisik dan sifat kimia, manfaat, dampak, proses pembuatan unsur-unsur golongan utama (gas mulia, halogen, alkali, dan alkali tanah) 4.7 Melakukan percobaan pembuatan unsur halogen dan mengidentifikas i sifat fisika dan kimia unsur golongan utama (halogen, alkali, atau alkali tanah) Kimia Unsur
Kelimpahan unsur-unsur golongan utama, unsur-unsur periode 3, dan unsur transisi periode 4. Sifat fisis dan sifat
kimia unsur-unsur golongan
utama,periode 3, dan unsur transisi periode 4.
KD 3 KD 4 Materi PraktikumKeperluan 3.8 Menganalisis
kelimpahan, kecenderungan sifat fisik dan sifat kimia, manfaat, dampak, dan proses pembuatan unsur periode 3 dan unsur golongan transisi (periode 4).
4.8 Merancang dan melakukan percobaan untuk menunjukkan sifat amfoter aluminium (Al3+)
Ekstraksi unsur-unsur halogen, alkali, alkali tanah, aluminium, nitrogen, oksigen, belerang, silikon, besi, kromium, tembaga, dan senyawanya. Manfaat unsur dan
senyawa golongan utama, periode ke-3 dan transisi (periode 4) Ada 3.9 Menganalisis struktur, tatanama, sifat, sintesis, dan kegunaan senyawa karbon
4.9 Menalar dan menganalisis struktur, tata nama, sifat dan kegunaan makromolekul (polimer, karbohidrat, dan protein)
Struktur, Tata Nama, Sifat, Isomer,
Identifikasi dan Kegunaan Senyawa: Haloalkana Amina
Alkanol dan Alkoksi Alkana
Alkanal dan Alkanon Asam alkanoat dan
alkil alkanoat Ada 3.10 Menganalisis struktur, tata nama, penggolongan, sifat, dan kegunaan lemak
4.10 Menalar dan menganalisis struktur, tata nama, penggolongan, sifat, dan pengaruh lemak bagi tubuh manusia. Benzena dan Turunannya Struktur Tata Nama Sifat Kegunaan
Tidak Ada
3.11Menganalisis struktur, tata nama, sifat dan penggolongan makromolekul 4.11 Menalar pembuatan suatu produk dari makromolekul
Struktur, tata nama, sifat, penggunaan dan penggolongan
KD 3 KD 4 Materi PraktikumKeperluan (polimer,
karbohidrat, protein, dan lemak)
Polimer Karbohidrat Protein Lemak
PERENCANAAN PEMBELAJARAN EKSPERIMEN
Kompetensi Dasar :
3.2 Membedakan sifat koligatif larutan elektrolit dan larutan nonelektrolit
4.2 Mengolah dan menganalisis data percobaan untuk membandingkan sifat koligatif larutan elektrolit dengan sifat koligatif larutan nonelektrolit yang konsentrasinya sama.
Materi Pokok:
Sifat Koligatif Larutan Topik :
Kenaikan titik didih dan penurunan titik beku JudulPraktikum :
Penentuan Titik Didih dan Titik Beku Larutan Elektrolit dan Nonelektrolit Prosedur Kerja :
Kegiatan 1 : Kenaikan titik didih larutan (∆Tb)
1. Masukkan 100 ml air suling ke dalam gelas kimia 200 ml, lalu panaskan. Celupkan termometer ke dalam air yang mendidih, catat berapa suhunya.
2. Ulangi langkah 1 dan 2 dengan larutan gula dan larutan NaCl sebagai pangganti air suling. Kemudian catat kembali suhu yang ditunjukkan pada saat larutan mendidih.
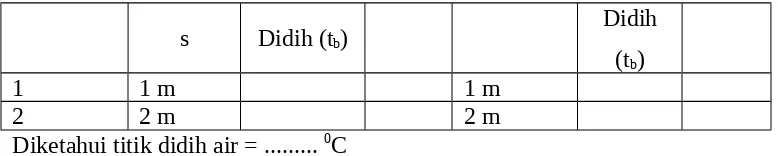
3. Berdasarkan hasil pengamatan, isilah tabel berikut ini dan hitunglah perubahan titik didih larutan dibandingkan titik didih air.
Tabel hasil pengamatan No
Percobaan
Larutan Gula Larutan NaCl
s Didih (tb) Didih (tb)
1 1 m 1 m
2 2 m 2 m
Diketahui titik didih air = ... 0C
Kegiatan 2: Penurunan titik beku larutan (∆tf)
1. Sediakan gelas kimia 1000 ml, masukkan ke dalamnya es batu yang telah dihancurkan sampai volume 700 ml, tambahkan 8 sendok garam dapur.
2. Isilah tabung reaksi dengan air suling setinggi 4 cm. Masukkan tabung reaksi tersebut ke dalam campuran pendingin, aduk campuran pendingin. Masukkan pengaduk kaca ke dalam tabung reaksi dann gerakkan pengaduk dalam air sampai air membeku seluruhnya.
3. Keluarkan tabung itu dari campuran pendingin, biarkan es dalam tabung mencair sebagian. Ganti pengaduk dengan termometer. Aduk hati-hati air dalam tabung dengan thermometer (hati-hati resevoir termometer mudah pecah). Bacalah termometer dan catat berapakah suhunya!
4. Ulangi langkah 2 dan 3 dengan larutan urea dan NaCl sebagai pengganti air suling, catat suhu masing-masing larutan pada saat membeku!
5. Berdasarkan hasil percobaan, isilah tabel berikut ini dan hitunglah perubahan titik beku larutan dibandingkan titik beku air.
Tabel Hasil Pengamatan
No Percobaan
Larutan Gula Larutan NaCl
Molalita s
Titik
Beku (tf) ∆ Tf Molalitas
Tititk Didih (tf)
∆ Tf
1 1 m 1 m
2 2 m 2 m
Alat dan bahan :
3. Kaki tiga + kassa 1 buah 4. Gelas kimia 1000 ml 1 buah
5. Statif +Klem 1 buah
6. Termometer 1 buah
7. Pembakar spirtus 1 buah
8. Air suling Secukupnya
9. Larutan NaCl I m dan 2 m 200 ml 10. Larutan gula 1 m dan 2 m 200 ml 11. Larutan urea 1m dan 2m 200 ml
12. Benang secukupnya
13. Es Batu secukupnya
14. Batang Pengaduk 1 buah 15. Garam Dapur secukupnya
Sumber:
DESAIN OPTIMASI
1. Kenaikan titik didih
Variabel Bebas : Larutan Urea Larutan garam Larutan cuka Variabel Terikat :Perubahan Suhu
Variabel Kontrol : Larutan Uji dibuat dengan konsentrasi 1, 2 dan 3 molal Volume Larutan 20 mL
Ukuran Gelas Kimia 50 ml dan 500 mL Thermometer skala Celcius
Ukuran tinggi kaki tiga, kasa dan Bunsen 2. Penurunan titik beku
Variabel Bebas :Larutan Urea Larutan garam Larutan cuka Variabel Terikat :Perubahan Suhu
Variabel Kontrol :Larutan Uji dibuat dengan konsentrasi 1,2dan 3 molal Volume Larutan 8 mL (tinggi larutan sekitar 5,2 cm)
Ukuran Gelas Kimia 50 ml dan 500 mL Thermometer skala Celcius
Tabung reaksi diameter (ukuran t=15 cm, d=2 cm) 3. Prosedur Optimasi
a. Kegiatan 1 : Kenaikan Titik Didih Larutan ( ΔTb )
1) Masukkan 20 ml air ke dalam gelas kimia 50 ml, lalu panaskan. Celupkan termometer ke dalam air yang mendidih, catat berapa suhunya.
2) Ulangi langkah 1 dengan larutan urea, larutan NaCl, dan larutan cuka 2m sebagai pangganti air suling. Kemudian catat kembali suhu yang ditunjukkan pada saat larutan mendidih.
Tabel hasil pengamatan
No Percobaan
Larutan Urea Larutan NaCl Larutan Cuka Molalitas
(m)
Titik Didih
(tb)
∆ tb
Molal itas (m)
Tititk Didih (tb)
∆ tb Molalitas
(m)
Tititk Didih (tb)
∆ tb
1 1 m 1 m 1 m
2 2 m 2 m 2 m
3 3 m 3 m 3 m
Diketahui titik didih air = ... 0C
b. Kegiatan 2: Penurunan titik beku larutan (∆tf)
1) Sediakan gelas kimia 500 ml, masukkan ke dalamnya es batu yang telah dihancurkan sampai volume 350 ml, tambahkan 4 sendok garam dapur.
2) Isilah tabung reaksi dengan air suling setinggi 5 cm. Masukkan tabung reaksi tersebut ke dalam campuran pendingin, aduk campuran pendingin. Masukkan termometer ke dalam tabung reaksi.kemudian tunggu sampai air suling membeku.
3) Keluarkan tabung itu dari campuran pendingin, biarkan es dalam tabung mencair sebagian. Bacalah termometer dan catat berapakah suhunya!
4) Ulangi langkah 2 dan 3 dengan larutan urea, larutan NaCl, dan larutan Cuka sebagai pengganti air suling, catat suhu masing-masing larutan pada saat membeku!
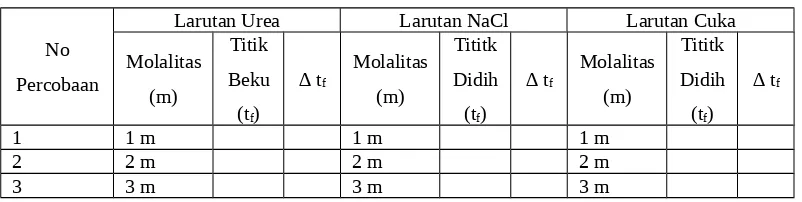
5) Berdasarkan hasil percobaan, isilah tabel berikut ini dan hitunglah perubahan titik beku larutan dibandingkan titik beku air.
Tabel Hasil Pengamatan
No Percobaan
Larutan Urea Larutan NaCl Larutan Cuka
Molalitas (m)
Titik Beku (tf)
∆ tf
Molalitas (m)
Tititk Didih (tf)
∆ tf
Molalitas (m)
Tititk Didih (tf)
∆ tf
1 1 m 1 m 1 m
2 2 m 2 m 2 m
4. Alat dan Bahan
Nama Alat Jumlah Nama Bahan Jumlah
Gelas kimia 50 ml 4 buah Air suling Secukupnya Pembakar spirtus 1 buah Larutan Urea 1 m 28 mL
Kaki tiga 1 buah Larutan Urea 2m 28 mL
Kassa 1 buah Larutan Urea 3 m 28 mL
Statif +Klem 1 buah Larutan Garam 1 m 28 mL
Benang secukupnya Larutan Garam 2m 28 mL
Termometer 1 buah Larutan Garam 3 m 28 mL Gelas kimia 500 ml 1 buah Larutan Cuka 1 m 28 mL
Sendok 1 buah Larutan Cuka 2 m 28 mL
Tabung reaksi 4 buah Larutan Cuka 3 m 28 mL
Batang pengaduk 1 buah Es batu Secukupnya
Garam Secukupnya
ALAT DAN BAHAN YANG DIBUTUHKAN SESUAI PROSEDUR STANDAR Jumlah siswa dalam 1 kelas = 30 siswa
A. Kebutuhan Alat dan Bahan dalam Satu Kelompok 1. Kenaikan Titik Didih
Alat :
Gelas kimia 250 ml 2 buah Kaki tiga + kassa 1 buah
Statif +Klem 1 buah
Termometer 1 buah
Pembakar spirtus 1 buah
Benang secukupnya
Bahan :
Air suling Secukupnya
Larutan NaCl I m dan 2 m 200 ml Larutan gula 1 m dan 2 m 200 ml Larutan urea 1m dan 2m 200 ml 2. Penurunan Titik Beku
Alat :
Tabung reaksi 3 buah Gelas kimia 1000 ml 1 buah
Statif +Klem 1 buah
Termometer 1 buah
Sendok 1 buah
Benang secukupnya
Batang Pengaduk 1 buah Bahan :
Air suling Secukupnya
Larutan NaCl I m dan 2 m 10 ml Larutan gula 1 m dan 2 m 10 ml Larutan urea 1m dan 2m 10 ml
Es Batu secukupnya
B. Kebutuhan Alat dan Bahan dalam Satu Kelas 1. Kenaikan Titik Didih
Alat :
Gelas kimia 250 ml 20 buah Kaki tiga + kassa 10 buah
Statif +Klem 10 buah
Termometer 10 buah
Pembakar spirtus 10 buah
Benang secukupnya
Bahan :
Air suling Secukupnya
Larutan NaCl I m dan 2 m 2 L Larutan gula 1 m dan 2 m 2 L Larutan urea 1m dan 2m 2L
2. Penurunan Titik Beku Alat :
Tabung reaksi 30 buah Gelas kimia 1000 ml 10 buah
Statif +Klem 10 buah
Termometer 10 buah
Sendok 10 buah
Benang secukupnya
Batang Pengaduk 10 buah Bahan :
Air suling Secukupnya
Larutan NaCl I m dan 2 m 100 ml Larutan gula 1 m dan 2 m 100 ml Larutan urea 1 m dan 2m 100 ml