Fondasi
Evolusi
Studi
Genomik
Algae
1
Catatan‐Catatan Kritis untuk Studi Genomik Algae dan Implikasinya pada Studi Molekuler Rumput Laut di Indonesia
Ferry Fredy Karwur
Universitas Kristen Satya Wacana
Abstrak
Indonesia adalah negara pantai, kaya akan algae. Tulisan berikut memberikan perpektif evolusi akan pentingnya studi genomik algae di Indonesia. Dan sebagai demikian, perkembangan-perkembangan muktahir studi genomik algae menjadi titik berangkatnya sebagai genome tools untuk membangun mainstream Indonesia sendiri berdasarkan keunikan spesies, lingkungan, kekayaan hayati, dan kepentingan nasional. Pemanfaatan genome tools ini dan pengembangan mainstream baru itu harus bersifat kolaboratif-konsorsium dengan prinsip “strategic pooling and sharing of resources”.
Kata Kunci: algae, evolusi, eukariota, genomik
Pengantar
Algae adalah kumpulan organisme fotosintetik yang muncul dalam garis pewarisan
tertentu yang berevolusi secara bebas dan yang dapat hidup dalam lingkungan
terestrial, namun terutama pada lingkungan perairan (Popper, et al., 20111).
1 Bahan yang disampaikan dalam Seminar Nasional dan Workshop Rumput Laut 2014 oleh UKK
Algae memiliki peran hayati yang sangat fundamental. Mereka menyusun dan
membangun diversitas perairan, mempengaruhi perubahan-perubahan evolusi biosfer,
dan melalui layanan ekologisnya berperan fundamental dalam kemantapan, adaptasi,
serta perubahan iklim dan lingkungan. Algae juga memiliki kemanfaatan manusia yang
hakiki. Algae merupakan faktor penting dalam pengelolaan sumberdaya perairan;
sumber pangan, pakan, zat gizi, bahan bioaktif untuk kesehatan, bahan baku industrial,
serta sumber energi kini dan masa depan (Radmer, 19962; U.S. Department of Energy,
20103)
Estimasi kekayaan spesies makroalgae laut saja sekitar 6,200 s/d 13,248, dan
terbanyak adalah algae merah (3,900 – 9.500 spesies), diikuti oleh algae coklat (1500 –
2151 spesies), dan algae hijau (>800 – 1597) (lihat: Guillermo Diaz-Pulido & Laurence,
2008)4. Jika ditambah dengan kekayaan spesies dari divisi Chrysophyta yang
berjumlah lebih dari 12,500 spesies (Wilson, 1986)5 maka total spesies algae mencapai
27.000 (termasuk Dinoflagellates dan Euglenoids, yang berjumlah sekitar 1,900
spesies). Jumlah ini tentu tidak besar ketimbang jumlah spesies Fungi (46,000 spesies)
atau Plantae (248.428 spesies).
Walaupun jumlah spesiesnya tidak sebanyak plantae, diktum Theodosius
Dobzhansky, bahwa, “nothing in biology makes sense except in the light of evolution”
--tiada yang bermakna dalam alam hayati kecuali dalam terang evolusi-- berlaku dalam
menjelaskan hubungan antar kelas algae, dan hubungan antara algae dengan
algae dalam peran fundamental di dalam biosfer, kita tidak bisa mengelak untuk
menemukan jawabannya di dalam terang dan cahaya evolusi akan bagaimana algae itu
hadir dan mengikuti arus sejarah evolusi, karena dari sejarah (evolusi) kita belajar
kehidupan, sebagaimana ungkapan: “historia magistra vitae” atau sejarah adalah guru
kehidupan (Cicero, 106-43 SM, sebagaimana disetir oleh Gultom, 2014).
Landasan Evolusi
Lebih dari tiga milyar tahun lampau, fotosintesis [dengan fotosistem I] telah
beroperasi namun tidak menghasilkan oksigen. Oksigen atmosfer praktis belum ada.
Fotosistem II (oksigenik) tampil dalam sejarah evolusi ≈ 2.8 milyar tahun lalu. Ia
memanfaatkan air sebagai sumber elektron2 untuk memanen cahaya matahari dengan
hasil samping O2. Kehadiran fotosistem II pada sianobakteri menjadi “biang” perubahan
dunia anoxic ke dunia oxic3. Bukti kehadiran sianobakteri pada lebih dari 2 milyar tahun
lalu antara lain adanya fosil sianobakteri Eoentophysalis belcherensis pada batuan
Belcher di Kanada (Knoll, 19926).
Sejak itu, dunia berubah dan tidak balik lagi ke dunia anoxic. Kehadiran oksigen
yang terus merangkak naik meningkatkan efisiensi produksi energi seluler. Oksigen
menjadi umpan-balik positif bagi ribuan rentetan reaksi aerobik dan bagi kemunculan
organisme yang lebih kompleks. Hal tersebut menjadi kunci dari munculnya eukarion
2 Dihasilkannya O
2 oleh fotosistem II karena terseleksinya kompleks mangan (Mn) pada sistem enzim “katalase
purba”, yang awalnya hanya dapat menghancurkan H2O2 menjadi dapat memotong air (H-O-H) dan menghasilkan
O2.
3 Bukti kehadiran sianobakteri pada lebih dari 2 milyar tahun lalu antara lain dibuktikan dengan adanya fosil
fotosintetik, dan memicu transformasi dunia uniseluler ke dunia multiseluler (Karwur,
20137).
Dari sianobakteri yang adalah prokarion mulailah perjalanan panjang evolusi
organisme fotosintetik eukariota; dan dalam hal ini, algae menempati tempat yang khas
dan menentukan bagi kemunculan beragam strategi pemanenan cahaya,
pengembangan mekanisme proteksi keracunan oksigen, dan mengawali kemunculan
organisme fotosintetik terestrial.
Fosil mirip protista (Valeria lophostriata), berbentuk bola dan berdiameter 240
μM, bersalutkan membran organik, telah terdeteksi pada era Paleoproterozoic (2.5 s/d
1.6 milyar tahun lalu) di China (Yan & Liu, 19938; Javaux et al., 20049). Pada era
Mesoproterozoic (1.6 s/d 1 milyar tahun lalu), organisme eukariotik awal mulai
berdiversifikasi dan mengambil alih relung hidup yang lebih luas, mungkin sekali ini
sebagai akibat dari naiknya kadar oksigen di atmosfer. Mereka antara lain:
Shuiyousphaeridium macroreticulatum (dengan umur lebih dari 1,250 milyar tahun lalu),
Tappania plana, Valeria lophostriata, Satka favosa, Grypania spiralis, dan Horodyskia
moniliformis (Knoll et al., 200610).
Fosil-fosil yang ditemukan pada era ini memberikan petunjuk kuat organisme
eukariotik dengan kompleksitas genetik dan sitologis telah ada pada sekitar 1,5 s/d 1,3
milyar tahun lalu. Pada tahapan ini, keanekaragaman eukariota dan heterogenitas
ekologis semakin tinggi. Di penghujung era Mesoproterozoic dan pada awal
Neoproterozoic, organisme multiseluler muncul. Sayangnya bahwa hampir semua
pohon eukariotik, kecuali beberapa dari mereka dapat dikaitkan dengan cabang-cabang
taksonomik yang lebih jauh, seperti algae merah Bangiophyte, algae Vaucheriales, dan
fungi.
Kepastian bahwa algae merah adalah titik singgung evolutif antara prokariotik,
eukariotik uniseluler, dan dengan eukarion multiseluler disokong oleh fosil algae merah
purba Bangiomorpha pubescence. Bangiomorpha pubescence adalah fosil berumur 1,2
milyar, ditemukan pada formasi Hunting Mesoproterozoic di arctic Canada (Butterfield,
2000). Ia menyerupai sianobakteri filamentous uniseriat dimana sel-selnya tersusun
berderet dalam satu baris bagaikan barisan kacang di dalam sebuah polong) namun
berbeda dalam sejumlah karakter kunci. Rangkaian berantai sel-sel yang membentuk
filament-filamen dari Bangiomorpha mempunyai organ jangkar (holdfasts) bagaikan
akar untuk menempelkan dirinya pada substrat. Jangkar tersebut tersusun atas sel-sel
yang telah berdiferensiasi. Bangiomorpha juga memiliki zona-zona sel-sel discoidal
(disc-shaped) yang memelar dan membelah secara radial pada sejumlah arah dan
menghasilkan sel-sel berbentuk baji yang khas (distinctive wedge-shaped cells).
Ciri-ciri tersebut tidak dikenal pada sianobakteri tetapi justru terdapat pula bersama-sama
dengan karakter lain-- pada algae merah bangiofita lain (Butterfield et al., 199011;
Butterfield 200012).
Lebih lanjut, ciri-ciri fosilisasi(taphonomic) Bangiomorpha lebih menyerupai yang
ditemukan pada eukariota awal lainnya yang berbedah dengan yang ada pada
sianobakteri filamentous yang telah diketahui pada fosil Proterozoic. Bangiomorpha
menunjukkan keterawetan dinding-dinding sel bagian luar dan bagian dalam, kecuali
lembaran-lembaran menunjukkan keterawetan lembaran-lembaran-lembaran-lembaran itu namun secara parsial atau
seluruhnya mengalami kehancuran bagian isi sel (Bartley 1996). Gejalah ontogenik
Bangiomorpha mencakup kehadiran tahapan sel-sel 1, 2, 3, 4 dan 8. Pendugaan umur
(radiometrik) dan stratigrafi menunjukkan umur fosil Bangiomorpha pubescens sekitar
1.2 milyar tahun (Butterfield, 200013).
Yang menjadi pertanyaan ialah, “kapan algae lain seperti algae hijau, hadir
dalam panggung sejarah evolusi?” Studi-studi menggunakan penanda hayati
(biomarker) menunjukkan bahwa algae merah dan algae hijau ada dalam keadaan
berlimpah dalam ekosistem Neoproterozoic (Summons and Walter, 199014). Hal ini
diperkuat dengan temuan fosil algae hijau multiseluler (‘rumput laut”) pada era
Neoproterozoic (1000 s/d 540 juta tahun lampau), yang ciri-ciri mirip dengan algae
hijau Cladophora dan Coelastrum (Butterfield et al., 198815). Diduga, algae hijau telah
ada sebelumnya karena kedua spesies ini muncul dalam percabangan lanjut dalam
pohon filogeni algae hijau. Demikian pula bahwa fosil mirip algae Chrysophyta berumur
610 s/d 750 juta tahun, terdeteksi di daerah Yukon dekat Alaska. Algae hijau air tawar
hadir kemudian dalam era lebih mudah, pada era Proterozoic akhir.
Bukti-bukti fosil di atas menjelaskan fakta adanya sesuatu, tetapi kurang dapat
membantu menjelaskan mekanisme terjadinya keanekaragaman hayati, yang dalam
konteks algae adalah soal diferensiasi sel dan plastida, konsekuensi-konsekuensi yang
ditimbulkannya kemudian, serta revolusi quantum hayati lain pada dunia algae, seperti
perubahan membran dan dinding sel. Dan yang fundamental ialah bahwa tentunya
bahwa fosil akan terbatas dalam menjelaskan mekanisme endosimbiosis –primer,
usul eukariota, eukariota plastidial, serta pemencaran spesiesnya (Palmer et al.,
200416; Keeling, 200417;Falkowski et al., 200418). Studi morfologi, biokimia, seluler, dan
molekuler menjadi sentral dalam menyumbangkan kekurangan ini.
Dalam latar-belakang seperti yang telah disampaikan di atas maka pada bagian
berikut kita akan memahami dan mengkritisi studi molekuler genomik dari
organisme-organisme yang telah dirunut urutan basa DNA genomiknya dari sejumlah algae yang
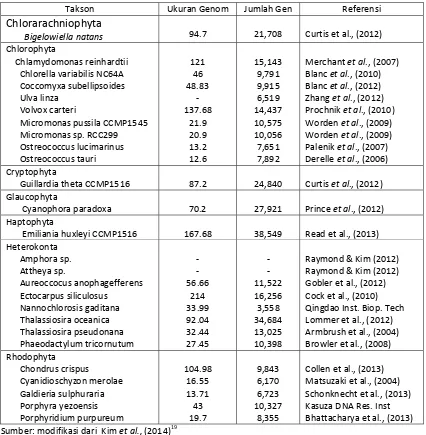
Tabel 1:
Kompilasi Projek Perunutan DNA Genomik Algae yang Dilaporkan Melalui Bank Genom (NCBI)
Takson Ukuran Genom Jumlah Gen Referensi
Chlorarachniophyta
Chlorella variabilis NC64A
Coccomyxa subellipsoides
Ulva linza
Volvox carteri
Micromonas pussila CCMP1545
Micromonas sp. RCC299
Studi Genom Algae Merah, Coklat, dan Hijau
Perunututan (sequencing) DNA genomik pada sejumlah spesies algae telah
kritis terhadap 3 spesies algae yang DNA genomiknya telah dirunut yang mewakili tiga
kelas besar, yakni algae hijau uniselular Chlamydomonas reinhardtii (121 MB)
(Merchant et al., 200720), algae coklat Ectocarpus siliculosus (214 MB) (Cock et al.,
201021), dan Chondrus crispus (104,98 MB) (Collen et al., 201322). Dua spesies
terakhir tergolong rumput laut. Perbandingan karakteristik genom Chlamydomonas
reinhardtii, Ectocarpus siliculosus, dan Chondrus crispus ditampilkan pada Tabel 2.
Tabel 2
Perbandingan karakteristik genom antara Chlamydomonas reinhardtii, Ectocarpus siliculosus dan Chondrus crispus
Ciri Genom C. reinhardtii E. siliculosus C.crispus
Ukuran genom (Mb) 121 214 104.98
Jumlah gen 15,143 16,256 9,606
Gen per genom (%) 16 12 11,3
G/C (%) 64 53,6 ?, 28,7 (Plastida)
Intron per gen 7,4 6,98 0,32
Ukuran Intron (bp) 174 704 123
a. Chlamydomonas reinhardtii (Merchant et. al., 200723)
C. reinhardtii adalah algae hijau uniseluler berukuran ~ 10 μm. Ia memiliki kromosom
ganda dengan 2 flagella anterior untuk motilitas dan untuk kawin serta sebuah
kloroplast tempat berdiam piranti fotosintetik dan lintasan-lintasan metabolik penting. C.
reinhardtii adalah organisme model yang penting dengan sejumlah alasan, antara lain:
(a) Penting dalam menguak pertanyaan di sekitar fotosintesis eukariotik karena algae
ini dapat hidup dengan sumber karbon yang disuplai sambil tetap menjaga piranti
fotosintetiknya fungsional, termasuk biogenesis kloroplast (Lohr et al., 200524; (b)
Penting untuk menyingkap rahasia kehadiran flagella eukariotik dan fungsi dasar tubuh,
memahami lebih baik aspek-aspek hayati fundamental lain (circadian rhythms,
pengendalian siklus sel, respirasi tumbuhan, transporter metal, (Ball, 200525) serta
menjawab pertanyaan-pertanyaan praktikal manusia, bioremediasi dan produksi bahan
bakar hayati (Merchant et al., 2007, dan pustaka lain yang disitasinya). Sejumlah piranti
riset genomik (prosedu pengujian genomik fungsional, microarray, prosedur rutin
peminakan berbasis peta fisik –map-based cloning) telah pula dibangun pada
organisme model ini. DNA genomik algae hijau uniselular ini telah dirunut tahun 2007
oleh kelompok peneliti Arthur Grossman.
Ukuran genom C. reinhardtii sebesar 121 Mb menyusun 17 kromosom.
Genomnya memiliki gen-gen dengan kerapatan homogen, DNA berulang sederhana,
dan transposable elements (TE). rRNA-nya tersusun dalam tandem pada tautan 1, VII,
dan XV. Teridentifikasi pula 259 tRNA, 16 kelas DNA berulang sederhana, 100 keluarga
TE, dan SINE (short interspersed elements) yang terhubung tRNA. Terdapat pula
dompolan-dompolan tRNA dan dan adanya duplikasi tRNA yang belum lama terjadi,
serta dompolan gen-gen dengan fungsi hayati spesifik. Potongan genom kloroplast dan
mitokondria sedikit saja terdeteksi di DNA genom. Gen pengkode protein memiliki
rata-rata 8,3 exon per gen serta kaya akan intron. 30% panjang intron karena DNA
berulang.
Pada Chlamydomonas tercatat 1226 keluarga gen yang mengkode 2 atau lebih
protein. 317 dari 798 keluarga gen yang mengkode 2 gen terancang dalam tandem.
Walaupun terdapat proporsi besar keluarga kinase dan sitokrom P-450 (seperti pada
Arabidopsis), tetapi yang terbesar justru keluarga klas III guanylyl dan adenylyl cyclase.
keluarga protein yang penting dalam akuisisi hara juga ditemukan. Beragam transporter
pada tumbuhan dan hewan juga kebanyakan ada pada Chlamydomonas. Namun
teradapat juga gen yang ada pada Chlamydomonas dan tumbuhan, tetapi tidak ada
pada hewan; dan sebaliknya. Tercatat pula transporter-transporter substrat spesifik,
yang penting dalam aklimatisasi. Yang perlu dicatat pula adalah kehadiran gen-gen
plastidial, regulator-regulator redoks fotosintetik (thioredoxin), gen-gen terkait respons
fototaktik, serta gen-gen terkait fungsi flagellar dan gen-gen basal body tempat
berjangkarnya flagella.
b. Ectocarpus siliculosus (Cock, et al., 201026)
Algae coklat adalah organisme dengan lintasan sejarah evolusi tersendiri, yang sangat
berbedah dengan kelas algae lain, sehingga menunjukkan sejumlah ciri asali (novel):
metabolisme (termasuk metabolism karbohidrat, lipid, dan halogen), fisiologi,
karakteristik seluler, dan karakteristik ekologis. Dinding selnya mengandung banyak
polisakarida “aneh” serta memiliki kedayatahanan yang tinggi terhadap cekaman
osmotik. Algae coklat filamentous Ectocarpus siliculosus adalah rumput laut yang
memiliki perangkat fotosintetik kompleks. Algae ini terutama tumbuh di ekosistem pantai
berbatu dan menunjukkan daya adaptasi yang luarbiasa pada lingkungannya itu, dan
bahkan pada lingkungan yang sukar. Piranti riset genomik, analisis gen fungsional,
telah terbangun pula pada organisme ini. Genomnya telah dirunut tahun 2010 (Charrier
et al., 200827).
Genom algae coklat Ectocarpus siliculosus berukuran 214 Mb dan mengkode
(rata-rata 845 pb) dan sering terletak sangat dekat satu dengan yang lain dalam kromosom.
Urutan DNA berulang mencakup transposon, retrotransposon, dan helitron (total 22,7%)
RNA cilik cenderung berada dekat dengan transposon. Ditemukan pula potongan besar
virus DNA yang mirip dengan Ectocarpus phaeovirus (319,4 kb). Gen-gen yang terkait
dengan adaptasi pada lingkungan hidup yang sangat dinamis dan berat. Terdapat
keluarga besar LHC (Light Harvesting Complex) sebanyak 523 loci. Diantaranya adalah
1 dompolan dengan 11 gen yang terkait dengan adaptasi cekaman cahaya terkait LHC.
Terdapat pula gen pensintesis klorofil dalam kehadiran cahaya yang lemah (DPOR).
Jadi, Ectocarpus memiliki sistem fotosintesis kompleks yang memampukannya
beradaptasi dengan variasi cahaya yang berubah-ubah. Demikian pula bahwa kadar
fenol yang tinggi pada algae coklat mungkin penting untuk pertahanan radiasi UV
(terdapat gen-gen pensintesis flavanoid, yang tidak ada pada diatom dan algae hijau),
gen-gen metabolisme ROS, dan gen-gen yang terlibat dalam proteksi terhadap halida.
Hadir pula pada algae coklat ini gen-gen khas pensintensis polisakarida khusus
(seperti alginate, fucan) disamping selulosa, dan gen-gen pemodifikasi polisakarida.
Enzim-enzim yang dikodenya penting dalam mengubah sifat fisika kimia dinding sel,
yang mempengaruhi rigiditas, pertukaran ion, dan resistensi cekaman abiotik.
Algae coklat ini juga memiliki gen-gen pengkode protein kinase (dan protein lain,
seperti integrin dan ion channel yang penting dalam pensinyalan kalsium) yang penting
dalam perkembangan, diferensiasi, dan evolusi multiseluler, bahkan ada yang berbeda
sekali dengan yang ada pada hewan dan tumbuhan. Keluasan ragam faktor
sejumlah microRNA (sebagaimana pula teridentifikasi pada eukariotik lain)
menunjukkan bahwa molekul pengatur ini telah ada pada fase awal evolusi eukariotik.
c. Chondrus crispus (Collen et al., 201328)
Ada sejumlah alasan mengapa perunutan genom pada algae merah layak dilakukan.
Pertama, algae merah menempati posisi penting dalam sejarah evolusi eukariota
fotosintetik dan eukariota lain. Kedua, kekayaan spesies algae merah yang sangat
tinggi memainkan penting dalam ekosistem perairan. Ketiga, antena pemanen cahaya
fotosintetiknya tersusun atas fikobiliprotein, dengan tilakoidnya yang tidak tersusun
dalam tumpukan, dan sama sekali tidak memiliki flagella dan sentriola. Keempat, algae
merah menyimpan karbon tersimpan sebagai butiran pati di dalam sitoplasma (pati
floridean). Kelima, dinding selnya merupakan susunan kompleks antara selulosa,
berbagai ragam hemiselulosa, dan galaktan-galaktan yang tersulfatasi (sulfated
galactans) yakni agar dan carrageenas (Popper et al., 201129). Algae merah yang DNA
genomiknya telah dirunut adalah Chondrus crispus (atau Irish moss) yang adalah
anggota dari florideofita (Gigartinales). Chondrus crispus adalah rumput laut merah
intertidal, yang berukuran mencapai 20 cm, dan ditemukan di daerah pantai berbatu di
lautan atlantik utara Spesies ini memiliki nilai penting baik secara ekonomis maupun
ekologis. Ia mendiami ekosistem pantai dan merupakan sumber pangan dan polimer.
Dibandingkan dengan algae merah lain, informasi ilmiah dari spesies ini jauh lebih
banyak (lihat Collen et al., 2013 dan pustaka di dalamnya).
Genom Chondrus crispus berukuran 104,98 Mb, dengan jumlah gen 9,606.
monoexonik. Intron-intronnya berukuran kecil (182 nt; median, 123). Gen-gen pada
algae ini bergerombol di daerah kaya gen yang tersebar dengan runutan yang
mengandung banyak elemen-elemen DNA berulang, sehingga jarak antar gen cukup
rapat (0,8 kb) (bandingkan dengan eukariotik umumknya, yang 6,9 kb). Jadi walaupun
kerapan gennya rendah tetapi dengan pendompolan gen yang sangat tinggi. Ada bukti
kuat terjadinya penyederhanaan genom –kandungan gen berkurang- dan hilangnya
intron.
Genom Chondrus crispus kaya dengan urutan DNA berulang (73%) (terutama
LTR retrotransposon, dan sedikit non-LTR retrotransposon; inverted repeated elements,
dan sedikit helitron). Jadi LTR retroelement merupakan penyetir utama struktur dan
ekspansi ukuran genom Chondrus.
Menarik dari pemetaan genom Chondrus, diketahui bahwa ada sekitar 52% gen
yang teridentifikasi tidak memiliki counterpartnya di bank gen. Jadi banyak gen yang
belum diketahui/baru. Teridentifikasi pula gen-gen yang khas terlibat dalam metabolism
karbohidrat, termasuk gen-gen pensintesis carrageenan, yang memiliki kemiripan
dengan yang ada pada hewan dan algae coklat, tetapi telah hilang pada tumbuhan.
Terdapat pula gen pengkode 12 galactose-6-sulfurylase yang bertanggung-jawab pada
tahapan akhir sintesisn karagenan, adalah khas untuk algae merah. Algae ini juga
memiliki enzim yang khas terkait metabolism primer dan sekunder, termasuk gen-gen
untuk metabolism halogen.
a. Dari ketiga runutan genom ketiga algae yang mewakili lintasan sejarah evolusi yang
berbeda dan khas sebagaimana dideskripsikan di atas, maka bangunan dan struktur
genomik dari masing-masing spesies yang mewakili kelasnya menunjukkan peran
dari determinasi lingkungan evolusioner dan adaptasi aktif dari masing-masing algae
tersebut. Interaksi lingkungan evolusioner dan adaptasi aktif itu menyeleksi (a)
bangunan dan struktur genomik, serta gen-gen dari masing-masing spesies, serta
(b) menyeleksi gen-gen yang telah ada sebelumnya sebagai wujud adaptasi pada
lingkungan khasnya, termasuk di dalamnya penciptaan inovasi baru melalui
penciptaan gen baru/khas atau penemuan fungsi baru gen lama pada setiap
organisme.
b. Indonesia, negara pantai, kaya sekali dengan sumberdaya algae. Genome tools
yang telah tersedia tersebut di atas perlu dimanfaatkan oleh peneliti muda Indonesia
sambil membangun mainstream sendiri berdasarkan keunikan spesies, lingkungan,
kekayaan hayati, dan kepentingan nasional. Pemanfaatan genome tools ini dan
pengembangan mainstream baru itu harus bersifat kolaboratif-konsorsium dengan
prinsip “strategic pooling and sharing of resources”.
Referensi
1. Popper ZA, Gurvan M, Herve C, Domozych DS, Willats WGT, Tuohy MG, Kloareg B, and Stengel DB, 2011. Evolution and Diversity of Plant Cell Walls: From Algae to Flowering Plants. Annu. Rev. Plant Biol. 62:567-590
2. Richard J. Radmer RJ, 1996. Algal Diversity and Commercial Algal Products (Marine Biotechnology). BioScience 46(4), 263-270.
3. U.S. DOE 2010. National Algal Biofuels Technology Roadmap. U.S. Department of
Energy, Office of Energy Efficiency and Renewable Energy, Biomass Program. 4. Guillermo Diaz-Pulido & Laurence J. McCook, 2008. Macroalgae (Seaweeds) in
Chin. A, (ed) The State of the Great Barrier Reef On Line, Great Barrier Reef
Marine Park Authority, Townsville.
5. Wilson, E.O., 1986. The current state of biological diversity. In E.O. Wison, ed.
Biodiversity. Proceedings of a Biodiversity Forum held in Washington DC.
September 1986, pp3-18. National Academy of Science, Washington, DC. 6. Knoll AH, 1992. The Early Evolution of Eukaryotes: A Geological Perspective.
Science 256, 622-627.
7. Karwur F, 2012. Paradoks Oksigen. BioS 6(1),5-17.
8. Yan Y, Liu Z, 1993. Significance of eukaryotic organisms in the microfossil flora of Changcheng System. Acta Micropalaeontologica Sinica 10, 167-180.
9. Javaux EJ, Knoll AH, Walter MR, 2004. TEM Evidence for Eukaryotic diversity in mid-Proterozoic oceans. Geobiology 2, 121-132.
10. Knoll, AH, Javaux EJ, Hewitt D, and P Cohen, Eukaryotic organisms in Proterozoic oceans. Phil. Trans. R. Soc. B (2006) 361, 1023–1038.
11. Butterfield, N.J., Knoll, A.H. & Swett, K. 1990 A bangiophyte red alga from the Proterozoic of Arctic Canada. Science 250, 104-107.
12. Butterfield, N.J. (2000) Bangiomorpha pubescens n. gen., n. sp.: implications for the evolution of sex, multicellularity, and the Mesoproterozoic/Neoproterozoic radiation of eukaryotes. Paleobiology 26: 386–404.
14. Summons, R.E., and Walter, M.R., 1990, Molecular fossils and microfossils of prokaryotes and protists from Proterozoic sediments: Am. J. Sci., v. 290-A, p. 212-244.
15. Butterfield NJ, Knoll AH, and Swett K, 1988. Exceptional preservation of fossils in an Upper Proterozoic shale. Nature 334, 424 – 427.
16. Palmer JD, Soltis DE, Chase MW, 2004. The Plant Tree of Life: An Overview and Some Points of View. American Journal of Botany 91: 1437-1445.
17. Keeling PJ, 2004. Diversity and Evolutionary History of Plastids and Their Hosts.
American Journal of Botany 91:
18. Falkowski PG, Katz ME, Knoll AH, Quigg A, Raven JA, Schofield O, & Taylor FJR, 2004.The Evolution of Modern Eukaryotic Phytoplankton. Science 305:354-360.
19. Kim KM, Park J-H, Bhattacharya & Yoon HS, 2014. Application of Next-Generation Sequencing to Unraveling the Evolutionary History of Algae. International Journal of Systematic and Evolutionary Microbiology 64, 333-345.
20. Merchant SS (and other 16 researchers), 2007. The Chlamydomonas Genome Reveals the Evolution of Key Animal and Plant Functions. Science 318: 245-251.
21. Cock JM, (and other 77 researchers), 2010. The Ectocarpus genome and the
independent evolution of multicellularity in brown algae. Nature 465:617-621.
22. Collen J., (other 57 researchers), 2013. Genome structure and metabolic features in the red seaweed Chondrus crispus shed light on evolution of the Archaeplastida. PNAS 110, 5347-5252.
23. –idem 20--.
24. Martin Lohr M, Im C-S, & Grossman AR, 2005. Genome-Based Examination of Chlorophyll and Carotenoid Biosynthesis in Chlamydomonas reinhardtii. Plant Physiol. 138: 490–515
25. Ball SG, 2005. Eukaryotic Microalgae Genomic. The Essence of Being a Plant.
Plant Physiol., 137: 397-398.
26. –idem 20--.
Ectocarpus siliculosus: two centuries of research. New Phytologist (2008) 177:
319–332.