BAB 2
TINJAUAN PUSTAKA
2.1. Jahe(Zingiberaceae Officinale)
Jahe merupakan salah satu bumbu yang paling penting dan luas penggunaannya di seluruh dunia. Disebabkan permintaan yang tinggi, jahe tersebar sampai negara-negara tropis maupun subtropis dari wilayah Cina-India. Negara-negara-negara penghasil jahe yakni : India, Cina, Thailand, Nigeria, Indonesia, Brasil, Jepang, Malaysia, Srilanka dan negara-negara kepulauan pasifik lainnya dan Indonesia sendiri merupakan penghasil penting lainnya, dimana mempunyai luas penanaman sampai 10.000 hektar dan produksi sekitar 77.000 ton dan penanamannya dipusatkan di kepulauan Jawa-Sumatra (Ravindran, 2005).
Jahe secara botani dikenal sebagai Zingiber Officinale Roscoe, dengan subkingdom Tracheobionta, subdivisi Spermatophyta, klas Monocotyledons, subklas Zingiberidae, ordo Zingiberales, sub-ordo Scimitae, family Zingiberaceae, genus Zingiber, spesies Officinale (Butt, 2011 ; Ravindran, 2005 ; Zachariah, 2008). Jahe juga merupakan tanaman khas yang memiliki gabungan dari banyak sifat dan ciri, dimana mengandung minyak volatil, minyak non-volatil, senyawa pedas, resin, pati, protein dan mineral. Komponen tertentu dari kelimpahan relatif dapat sangat bervariasi antara sampel jahe dalam kondisi segar maupun kering.
Komposisi rimpang segar dipengaruhi oleh jenisnya, kondisi lingkungan tumbuh dan tingkat kematangan hasil panen. Perubahan lebih lanjut dalam kelimpahan relatif dari beberapa komponen dapat juga karena pasca panen selama preparasi dan kemudian penyimpanan hingga kering (Zachariah, 2008).
2.1.2.Komponen Kimia pada Jahe
meliputi sebagian hidrokarbon seskuiterpen, hidrokarbon monoterpen dan monoterpen teroksigenasi.
Komponen monoterpen dipercaya memberikan kontribusi yang sangat penting terhadap aroma jahe dan ketergantungan yang relatif besar dalam minyak alami dari rimpang segar daripada minyak atsiri yang didestilasi dari jahe kering. Seskuiterpen teroksigenasi merupakan komponen yang relatif sedikit dalam minyak volatil tetapi tampaknya penting sebagai penyumbang sifat rasa. Hasil minyak yang didestilasi dipengaruhi oleh sejumlah faktor, yang mencakup jenis jahe, tingkat kematangan saat panen, metode untuk preparasi, umur, dan termasuk metode destilasi (Zachariah, 2008).
2.1.2. Manfaat Jahe
Adapun manfaat yang terkandung dalam jahe itu sendiri antara lain : A.Jahe sebagai penyedap rasa
Rempah-rempahyang digunakan dalammakanan untukempat tujuandasar : 1. Untuk penyedap
2. untuk menutupi atau penghilangan bau 3. untuk menyampaikan kepedasan 4. untuk menambahkanwarna
Komponenfungsionalyang signifikanpadajahe yang utama aroma dan kedua rasa pedasnya.Banyak studi yang dipublikasikan terhadap komponen kimia yang berkontribusiterhadap kualitasfungsional.Salzer telah menyarankanfaktor penentukualitasjahe, yakni :
1. Sitral dan sitronellil asetat adalah yang penting dalam faktor pendukung bau 2. Zingiberen dan β-seskuifelandren merupakan komponenutamaminyak
yangbaru diperoleh
3. komponen inidikonversi kear-kurkumendengan penyimpanan
4. rasio zingiberene + β-seskuifelandren menjadi ar-kukurmen merupakan indikasi dari usia minyak
B. Jahe sebagai antioksidan
Jahememiliki kandunganantioksidanyang tinggidan telahdikelompokkansebagai salah saturempah-rempahdengan aktivitasantioksidanyang baik. Hal ini membuatnya sebagai peredam radikal bebas.Sethi dan Aggarwal melaporkan bahwa jahe kering memiliki sifat antioksidan yang lemah.
jahe yang mempunyai aktivitas antioksidan.Aktivitas antioksidan dari jahe bergantung pada struktur sisi-rantai dan pola substitusi pada cincin benzen terutama,aktivitas antioksidan yang diberikan oleh gingerol dan heksahidrokurkumen. Pada hewan percobaan, diet yang mengandung jahe menunjukkan efek yang sangat protektif, terhadap kerusakan oksidatif yang disebabkan malathion menunjukkan aktivitas antioksidan. Penggabungan garam dan ekstrak jahe pada daging sapi tanpa lemak tengik selama penyimpanan, meningkatkan kelembutan dan menambah jangka waktu simpan.
C. Jahe sebagai antimikroba
Meskipun digunakan dalam pengawetan makanan, jahe sangat tidak efektif dalam mencegah pembusukan makanan karena kontaminasi mikroba dan degradasi oksidatif. Jahe hanya memiliki aktivitas antimikroba ringan.
Nilai MIC (Minimum Inhibitory Concentration) dari jahe yang melawan Clostridium botulinum (bakteriyang menyebabkan keracunan makanan berat) ditunjukkan sekitar kira-kira 2000µg/ml. Minyak atsiri jahe ditunjukkan untuk menghambat kedua bakteri kolera dan tifus. Komponen minyak yang berperan dalam memberikan efek antimikroba yakni gingeron dan gingerol. Studi lainnya juga melaporkan sifat antimikroba dari gingerol terhadap Bacillus subtilis, Escherihia colidan Mycrobacterium.
Jahe merangsang nafsu makan, bertindak sebagai antioksidan, antimikroba dan antiflatulant, dan karenanya memiliki penggunaan yang luar biasa dalam produk makanan olahan (Ravindran, 2005).
2.2. Ikan
Ikan bisa ditemukan di hampir semua “genangan” air yang cukup besar baik air tawar, air payau, dan air asin pada kedalaman yang bervariasi, dari dekat permukaan sampai beberapa ribu meter dari permukaan. Ikan terdiri dari ikan air tawar dan air laut. Salah satu ikan dari air tawar adalah ikan nila. Keduanya adalah sumber protein yang sangat penting bagi pertumbuhan. Ikan mengandung 18% protein yang terdiri dari asam-asam amino esensial yang tidak rusak pada waktu dimasak. Kandungan lemaknya 1 - 20% lemak yang mudah dicerna dan bisa langsung digunakan oleh jaringan tubuh. Kandungan lemaknya sebagian besar adalah asam lemak tak jenuh yang dibutuhkan pada masa pertumbuhan dan dapat menurunkan kolesterol yang ada dalam darah (Hamid, 2010).
2.2.1. Ikan nila
Klasifikasi ikan nila adalah sebagai berikut :
kelas : Osteichthyes
Sub-kelas : Acanthoptherigii
Ordo : Percomorphi
Sub-ordo : Percoidea
Familia : Cichilidae
Genus : Oreochromis
Spesies : Oreochromis niloticus
Ikan nila merupakan spesies yang berasal dari kawasan Sungai Nil dan danau-danau sekitarnya di Afrika. Bentuk tubuh memanjang, pipih kesamping dan warna putih kehitaman. Jenis ini merupakan ikan konsumsi air tawar yang banyak dibudidayakan setelah ikan mas (Cyrprinus Carpio) dan telah dibudidayakan di lebih dari 85 negara. Saat ini, ikan ini telah tersebar ke negara beriklim tropis dan subtropis, sedangkan pada wilayah beriklim dingin tidak dapat hidup dengan baik. Bibit nila didatangkan ke Indonesia secara resmi oleh Balai Peneliti Perikanan Air Tawar (Balitkanwar) dari Taiwan pada tahun 1969. Setelah melalui masa penelitian dan adaptasi, ikan ini kemudian disebarluaskan kepada petani di seluruh Indonesia. Nila adalah nama khas Indonesia yang diberikan oleh pemerintah melalui Direktur Jenderal Perikanan (Dinas kelautan dan perikanan, 2010).
pasar domestik, nila merupakan salah satu sumber protein hewani yang saat ini cukup diminati pasar dunia terutama dalam bentuk fillet (potongan daging tanpa tulang). Permintaan pasar dunia terhadap jenis fillet nila semakin meningkat. Indonesia merupakan salah satu negara pemasok fillet nila terbesar di dunia selain Thailand, Cina, Taiwan dan Fillipina (Direktorat Pemasaran Dalam Negeri, 2010).
Produksi ikan nila di Indonesia tersebar di seluruh wilayah dan produsen utamanya Jawa Barat, Sumatera Selatan, Sumatera Utara danSumatera Barat.Volume produksi dunia diperkirakan 3 juta ton pertahun. Produksi Indonesia tahun 2008 sebesar 306.527 ton berasaldari tangkapan di perairan umum (5,05%) dan budidaya (94,95%)(Direktorat Pemasaran Dalam Negri, 2010).
2.2.2. Bagian-bagian dari Ikan yang Bermanfaat
Berikut merupakan informasi yang diperoleh dari Direktorat Jenderal Pengolahan dan Pemasaran Hasil Perikanan mengenai bagian-bagian dari ikan yang memiliki manfaat yang kaya akan gizi.
- Kepala dan mata
Kepala dan mata ikan mengandung polisakarida yang berfungsi mengontrol aliran darah.
- Duri
Duri ikan mengandung kalsium dan kolagen yang sangat bermanfaat membantu pertumbuhan tulang dan gigi
- Minyak ikan
Minyak ikan mengandung DHA (Doca Hexaenoic Acid) yang sangat penting bagi pertumbuhan otak dan retina
- Daging
Daging ikan mengandung protein berkualitas tinggi dan vitamin yang sangat berguna untuk pertumbuhan dan ketahanan tubuh
- Kulit
Kulit ikan mengandung vitamin A dan B12 yang sangat bermanfaat untuk kesehatan mata dan kekebalan tubuh (Hamid,2010).
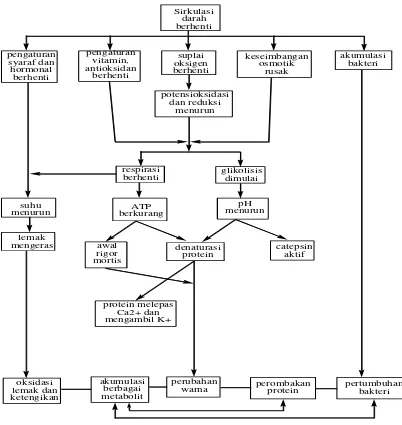
Sirkulasi
Gambar 2.1. Perubahan-perubahan yang terjadi Setelah Kematian Ikan
Ikan mengandung lemak dengan persentase yang berbeda dan sebagian besar berupa lemak tidak jenuh yang memiliki beberapa ikatan rangkap. Lemak dengan ikatan rangkap demikian bersifat tidak stabil dan relatif mudah mengalami proses oksidasi. Selama penyimpanan, reaksi oksidasi yang terjadi akan menghasilkan senyawa-senyawa yang berperan pada pembentukan aroma, cita rasa dan penampakan.
2.3. Oksidasi Lipida
Minyak dan lemak pada makanan memburuk melalui beberapa reaksi degradasi baik pada pemanasan dan penyimpanan jangka panjang. Proses kerusakan utama adalah reaksi oksidasi dan dekomposisi dari produk oksidasi yang mengakibatkan penurunan nilai gizi dan kualitas sensorik. Dengan adanya proses-proses oksidasi adalah penting bagi produsen makanan dan, memang, untuk semua orang yang terlibat dalam seluruh rantai pangan dari pabrik ke konsumen. Oksidasi dapat dihambat oleh berbagai metode termasuk pencegahan akses oksigen, penggunaan suhu rendah, inaktivasi enzim mengkatalisis oksidasi, reduksi tekanan oksigen dan penggunaan kemasan yang cocok (Pokorny, 2001).
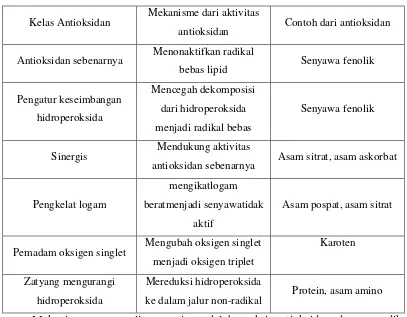
Metode lain perlindungan terhadap oksidasi adalah dengan menggunakan aditif spesifik yang menghambat oksidasi. Inhibitor ini mewakili kelas zat yang sangat bervariasi dalam struktur kimia, dan memiliki mekanisme yang beragam (Tabel 2.1.)
Tabel 2.1. Mekanisme Aktivitas Antioksidan
Kelas Antioksidan Mekanisme dari aktivitas
antioksidan Contoh dari antioksidan
Antioksidan sebenarnya Menonaktifkan radikal
bebas lipid Senyawa fenolik
Pengatur keseimbangan
antioksidan sebenarnya Asam sitrat, asam askorbat
Pengkelat logam
mengikatlogam
beratmenjadi senyawatidak
aktif
Asam pospat, asam sitrat
Pemadam oksigen singlet Mengubah oksigen singlet menjadi oksigen triplet
Karoten
Zatyang mengurangi
hidroperoksida
Mereduksi hidroperoksida
ke dalam jalur non-radikal Protein, asam amino
hidroperoksida lipida. Inhibitor lain menstabilkan hidroperoksida lipida, mencegah dekomposisi mereka menjadi radikal bebas.
Dekomposisi hidroperoksida dikatalisi soleh logam berat, dan akibatnya logam agen pengkelat juga menghambat oksidasi. Beberapa zat yang disebut sinergis menunjukkan tidak ada aktivitas antioksidan dalam diri mereka, tetapi mereka dapat meningkatkan aktivitas antioksidan sebenarnya. Kelompok lain zat mendekomposisi hidroperoksida lipida oleh jalur non-radikal, sehingga mengurangi kandungan radikal bebas. Akhirnya, oksigen singlet mengoksidasi lipida lebih cepat dari oksigen triplet pada umumnya, dan akibatnya pemadam oksigen singlet juga memiliki efek penghambatan penting pada oksidasi lipida.
Aktivitas antioksidan tergantung pada banyak faktor seperti komposisi lipida, konsentrasi antioksidan, suhu, tekanan oksigen, dan adanya antioksidan lain serta banyak komponen makanan umum, misalnya protein dan air. Antioksidan pertama kali digunakan sebelum Perang Dunia II untuk mengawetkan makanan. Antioksidan pertama sekali adalah bahan alami. Bahan alamiah ini akan segera digantikan oleh zat sintetis, yang lebih murah, kemurnian lebih konsisten, dan memiliki sifat antioksidan lebih seragam.
Bahan sintetis diuji toksisitasnya dengan berbagai metode pada konsentrasi 100-200 dari konsentrasi yang lazim dikonsumsi, untuk konfirmasi penggunaan yang aman sebagai penggunaan bahan aditif. Kemudian ada tantangan dari konsumen untuk penggunaan bahan sintetis, sehingga konsumen ingin bahan aditif ini digantikan oleh bahan-bahan alami, yang dianggap lebih diterima sebagai komponen makanan.
Produsen industritelah mencoba untuk mematuhi keinginan konsumen, dan telah pindah kepeningkatan penggunaan antioksidan alami. Antioksidan paling alami adalah komponen makanan umum, dan telah memiliki penggunaan dalam makanan selama ribuan tahun sehingga manusia menyesuaikan dengan konsumsi mereka.
merupakan trigliserida, dan inilah komponen yang paling signifikansi sebagai sumber potensial oksidatif pemutus-rasa dalam makanan tersebut (Pokorny, 2001).
2.3.1. Jalur Menuju Oksidasi Lipida
Reaksi spontan oksigen atmosfer dengan lipida, yang dikenal sebagai autoksidasi, adalah proses yang paling umum yang menyebabkan kerusakan oksidatif. Asam lemak tak jenuh ganda memiliki potensi untuk membusuk oleh proses ini, apakah dalam bentuk asam lemak bebas atau dalam bentuk trigliserida (atau digliserida atau monogliserida) atau fosfolipida.
Ketika cahaya dan klorofil (sensitizer) berada pada saat yang bersamaan, aktivasi oksigen ke oksigen singlet mungkin memainkan peran dalam inisiasi kerusakan oksidatif. Senyawa logam seperti besi atau tembaga, atau enzim lipoksigenase, mungkin memainkan peran dalam proses awal kerusakan oksidatif.
Lipoksigenase ada pada jaringan tanaman termasuk pada kedelai, kacang dan enzim tomat. Hal ini dapat menyebabkan kerusakan oksidatif lipida selama isolasi minyak dari minyak sayur, tetapi juga memainkan peran dalam pembentukan rasa positif dalam sayuran selama pengunyahan (Pokorny, 2001).
2.3.2. Produk Oksidasi Lipida
Komponen dibentuk pada tahap awal autoksidasi adalah hidroperoksida, dan ini juga produk dibentuk pada oksidasi katalisis lipoksigenase. Meskipun hidroperoksida adalah tidak mudah menguap dan tidak berbau, mereka adalah senyawa yang relatif tidak stabil dan mereka baik secara spontan untuk mendekomposisi atau dalam reaksi katalis untuk membentuk senyawa aroma yang mudah menguap, yang dianggap aroma-tak sedap. Sifat aroma-tak sedap terdeteksi terutama tergantung pada komposisi asam lemak dari substrat dan tingkat oksidasi, meskipun kondisi oksidasi juga dapat mempengaruhi volatil yang dihasilkan dan sifat sensorik dari minyak teroksidasi.
pigmen, terutama karotenoid, dengan intermediet reaktif, disebut radikal bebas, yang dibentuk selama oksidasi lipida. Radikal bebas juga dapat menyebabkan pengurangan kualitas gizi melalui reaksi dengan vitamin, khususnya vitamin E, yang hilang dari makanan selama aksinya sebagai antioksidan.
Dalam minyak goreng, konsentrasi radikal bebas meningkat menjadi jauh tingkat lebih tinggi dari pada makanan disimpan atau diproses pada suhu yang sedang. Pada temperatur tinggi pada saat penggorengan, yang biasanya sekitar 180°C, radikal bebas akan bergabung untuk membentuk dimer hingga konsentrasi tertentu. Hal ini menyebabkan peningkatan viskositas minyak, pembentukan asam lemak bebas, warna minyak menjadi gelap dan peningkatan busa dan terbentuknya asap selama penggorengan. Sesuai dengan rekomendasi Masyarakat Jerman untuk Penelitian Lemak (DGF), minyak goreng dianggap tidak baik jika mengandung lebih dari 24% materi polar dan material polimer 12%. Saat terbentuknya zat tersebut maka sebagian besar dari tokoferol bersama-sama dengan asam lemak tak jenuh ganda yang terdapat di dalam minyak akan hilang.
Aroma-tak sedap yang berkembang selama oksidasi lipida secara umum merupakan peringatan bahwa makanan tersebut tidak lagi dapat dimakan, meskipun hal ini tidak berlaku untuk suplemen lemak tak jenuh ganda yang diambil dalam bentuk kapsul. Ada beberapa kekhawatiran bahwa asupan berlebihan hidroperoksida lipid dapat menyebabkan efek merugikan kesehatan. Secara teori, jika hidroperoksida diserap konsumen yang merupakan potensial sumber radikal maka akan dapat menyebabkan kerusakan secara in vivo. Radikal bebas yang dihasilkan oleh dekomposisi hidroperoksida dapat menyebabkan kerusakan pada protein, enzim, atau DNA dan juga dapat menghasilkan karsinogen.
Hidroperoksida juga bisa terbentuk oleh foto-oksidasi jika cahaya bekerja pada lemak dengan kehadiran sebuah sensitizer. Namun, dekomposisi hidroperoksida adalah reaksi energi rendah untuk inisiasi autoksidasi, dan komposisi dari volatil aroma-tak sedap yang terbentuk biasanya merupakan karakteristik produk autoksidasi (Pokorny, 2001).
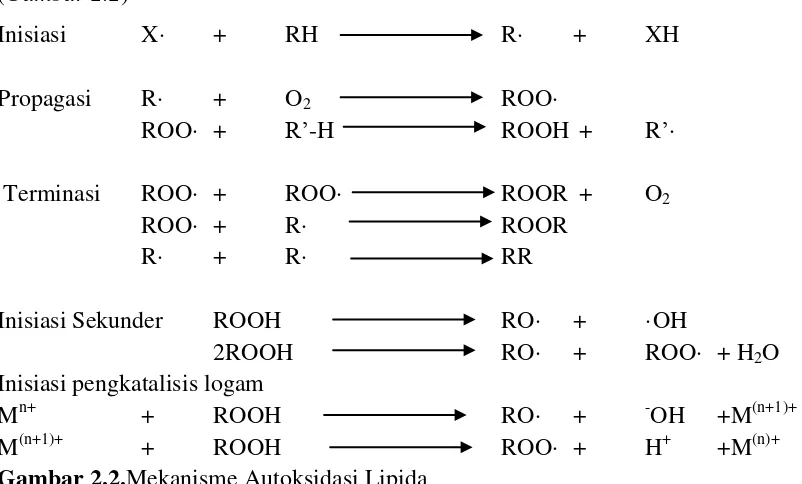
2.3.3. Mekanisme Autoksidasi
Sebagai reaksiradikal bebas, autoksidasiberlangsung dalam tigalangkah yang berbeda. (Gambar 2.2)
Inisiasi X· + RH R· + XH
Propagasi R· + O2 ROO·
ROO· + R’-H ROOH + R’·
Terminasi ROO· + ROO· ROOR + O2
ROO· + R· ROOR
R· + R· RR
Inisiasi Sekunder ROOH RO· + ·OH
2ROOH RO· + ROO· + H2O
Inisiasi pengkatalisis logam
Mn+ + ROOH RO· + -OH +M(n+1)+
M(n+1)+ + ROOH ROO· + H+ +M(n)+
Gambar 2.2.Mekanisme Autoksidasi Lipida
Langkah pertama adalah inisiasi di mana radikal lipida terbentuk dari lipida molekul. Abstraksi atom hydrogen oleh spesies reaktif seperti radikal hidroksil dapat menyebabkan inisiasi oksidasi lipida. Namun, dalam minyak sering kali ada jejak hidroperoksida, yang mungkin telah dibentuk oleh aksi lipoksigenase sebelum dan selama ekstraksi minyak. Inisiasi sekunder dengan pemecahan homolitik dari hidroperoksida berlangsung pada energi reaksi yang relatif rendah dan biasanya reaksi inisiasi utama terdapat dalam minyak yang dimakan. Reaksi ini biasanya dikatalisis oleh ion logam.
reaksi tersebut relatif rendah dibandingkan dengan reaksi inisiasi, sehingga reaksi propagasi terjadi dengan cepat dibandingkan dengan reaksi inisiasi.
Padatekananatmosfer, reaksi radikal alkildengan oksigen sangat cepat, sehingga konsentrasi radikal peroksi lebih tinggi dari radikal alkil. Abstraksi hydrogen terjadi secara istimewa pada atom karbon yang energi disosiasinya rendah. Karena energi disosiasi ikatan C-H dikurangi dengan tetangga fungsi alkena, maka abstraksi hidrogen terjadi paling cepat pada kelompok metilen antara dua kelompok alkenadalam asam lemak tak jenuh ganda (PUFA).
Para radikal yang terbentuk awalnya dari sebuah PUFA yang terdelokalisasi di lima atom karbon dari bagian 1,4-pentadienil, dan reaksi dengan oksigen terjadi secara istimewa dengan penambahan pada satu dari karbon akhir struktur ini. Ini mengarah pada pembentukan 9- dan 13-hidroperoksida dari asam linoleat seperti ditunjukkan pada (Gambar 2.3).
Gambar 2.3. Pembentukan13-hidroperoksida dari Asam Linoleat (senyawa 9-hidroperoksida merupakan produk utama yang terbentuk melalui jalur seperti diatas)
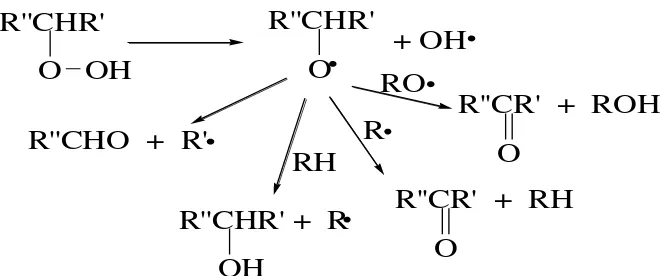
Radikal alkoksi dibentuk oleh dekomposisi hidroperoksida dapat terurai untuk melepaskan hidrokarbon yang mudah menguap, seperti alkohol atau. Alkohol dan keton yang non volatil juga dapat terbentuk seperti yang ditunjukkan pada Gambar
CH3CH2CH2CH2CH2CH=CH-CH2-CH=CH(CH2)7COOH
CH3CH2CH2CH2CH2CH=CH-CH-CH=CH(CH2)7COOH
CH3CH2CH2CH2CH2CH-CH=CH-CH=CH(CH2)7COOH
CH3CH2CH2CH2CH2CH-CH=CH-CH=CH(CH2)7COOH OO
CH3CH2CH2CH2CH2CH-CH=CH-CH=CH(CH2)7COOH OOH
Asam Linoleat
Radikal Linoleil
Radikal peroksil
13-hidroperoksida O2
Gambar 2.4. Pembentukan Produk Sekunder dari Dekomposisi Hidrokperoksida
Aldehida volatil sangat penting sebagai kontributor aroma minyak teroksidasi, dan heksanal biasanya dimonitor dalam menilai pembentukan produk oksidasi sekunder selama oksidasi lipida. Heksanal biasanya terbentuk dalam jumlah yang relatif besar selama oksidasi lipida melalui 13-hidroperoksida (Gambar 2.5).
Gambar 2.5. Dekomposisi 13-Hidroperoksida dari Asam Linoleat Membentuk Heksanal
Selain heksanal juga terbentuk produk lain yang mudah menguap dapat berkontribusi lebih dari heksanal untuk rasa aroma-tak sedap dalam penilaian sensorik minyak teroksidasi. Ambang batas rasa dari beberapa aldehida terbentuk pada autoksidasi asam linoleat ditampilkan pada (Tabel 2.2).
R''CHR'
+ OH
O
R''CHR'
O OH
R''CHO + R'
R''CHR' + R
OH
R''CR' + RH
O
R''CR' + ROH
O
R
RH
RO
CH3CH2CH2CH2CH2CH-CH=CH-CH=CH(CH2)7COOH
O-OH 13-hidroperoksida
CH3CH2CH2CH2CH2CH-CH=CH-CH=CH(CH2)7COOH -OH
O
CH3CH2CH2CH2CH2CHO + CH=C-CH=CH(CH2)7COOH
Radikal alkoksil
Tabel 2.2. Ambang Batas Aroma Asam Linoleat yang mungkin dari Oksidasi Produk dalam Minyak Parafin
Senyawa Ambang batas (mg. Kg-1)
Heksanal 0.08 - 0.6
Heptanal 0.04 - 0.055
Oktanal 0.04 - 0.6
Trans-2-nonenal 0.04 - 0.4
Cis-2-dekenal 0.1
Trans,trans-2,4-nonadienal 0.46
Trans,cis -2,4- dekadienal 0.02
Selain dekomposisi untuk membentuk produk oksidasi sekunder, hidroperoksida yang terbentuk dari asam lemak tak jenuh ganda dapat mengalami oksidasi lanjut dari dihidroperoksida dan molekul yang memiliki oksigen yang menghasilkan cincin seperti hidroperoksi epidioksida dan bisiklo-endoperoksida. Mekanisme untuk pembentukan hidroperoksi epidioksida dari-linolenat ditunjukkan pada Gambar 2.6.
Gambar 2.6. Reaksi 12-Hidroperoksida dari α- Asam Linolenat membentuk 9-Hidroperoksi Endoperoksida
OOH
12
OO
12
O
12
O
12
O
10
-H
O2 , H
O
10 9
OOH Hidroperoksi epidioksida
Radikal Linolenil Asam Linolenat COOH
COOH
COOH
2.3.4. Titik Kritis Oksidasi
Oksidasi umumnya merupakan sebagai bentuk reaksi yang paling sering menyebabkan kerusakan lipida, yang menghasilkan ketengikan, senyawa aroma-tak sedap, polimerisasi, dan reaksi lainnya yang menyebabkan kerusakan dan nilai gizi dari produk pangan. Lipida terdapat pada hampir semua bahan makanan, dan sebagian besar (lebih dari 90%) adalah dalam bentuk triasilgliserol yang merupakan este rasam lemak dan gliserol.
Dua komponen utama terlibat dalam oksidasi lipida yaitu asam lemak tak jenuh dan oksigen. Degradasi oksidatif lipida dapat dimulai oleh oksigen aktif dan terkait spesies (Tabel 2.3.), yang lebih aktif dari oksigen triplet yang ada diudara, dan juga oleh agen eksogen (UV, ionisasiradiasi,panas).
Tabel 2.3.Oksigen Aktif dan Spesies yang terkait
Radikal Non radikal
LOOH lipida hidroperoksida Fe=O kompleks besi-oksigen HOCl hipoklorit
Asam-asam lemak bebas juga memberikan pengaruh pro-oksidatif. Dimana akan terbentuk kompleks antara hidroperoksida dan kelompok karboksil melalui ikatan hydrogen yang mempercepat terjadinya dekomposisi hidroperoksida menjadi radikal bebas. Serangkaian senyawa hidroksilipida seperti alkohol lemak yang lebih tinggi, sterol, mono- dan diasilgliserol adalah komponen dari lipida alam yang mungkin mempengaruhi tingkat oksidasi mereka. Efeknya tergantung pada jenis substrat lipida dan kondisi oksidasi. Franzke dkk menemukan bahwa mono-dan diasilgliserol tidak terpengaruh pada proses ini, sedangkan penulis lain telah mengamati adanya pengaruh pro-oksidatif.
tidak-OH
ROOH O O O O
ROO
menghambat oksidasi lipida, telah terbukti menjadi akibat percepatan dekomposisi hidroperoksida menjadi radikal. Oksidasi secara termal senyawa lipida juga menunjukkan efekpro-oksidan pada penghalusan dan pemurnian minyak kedelai (Pokorny, 2001).
2.3.5. MenghambatAutoksidasi
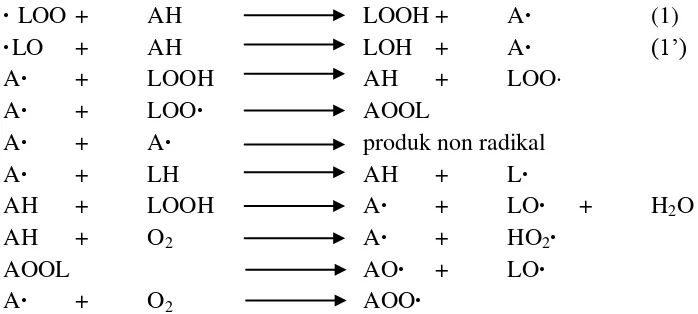
Proses rantai radikal bebas dari autoksidasi dapat dihambat oleh dua kategori inhibitor: rantai-melanggar inhibitor (atau antioksidan) dan inhibitorpencegahan. Rantai-melanggar / antioksidan AH menangkap radikal bebas (·LOO, ·LO) mengganggu reaksi propagasi [reaksi (1)dan (1’) pada Gambar2.7] dan membentuk sebuah antioksidan radikal A· semacam reaktivitas rendah yang selanjutnya tidak bereaksi dengan lipida terjadi.
Peredam radikal biasanya menyumbangkansatu electron dengan electron tidak berpasangan dari radikal bebas. Polifenolsangat aktif untuk hal tersebut.
· LOO + AH LOOH + A· (1)
·LO + AH LOH + A· (1’)
A· + LOOH AH + LOO·
A· + LOO· AOOL
A· + A· produk non radikal
A· + LH AH + L·
AH + LOOH A· + LO· + H2O
AH + O2 A· + HO2·
AOOL AO· + LO·
A· + O2 AOO·
Gambar 2.7. Penghambatan Autoksidasi Lipida oleh Antioksidan
Senyawa fenolik tersebut juga memiliki kestabilan dalam radikal fenoksinya pada Gambar 2.7.1.(Shahidi, 2005)
2.3.6. Pengaruh Antioksidan
Antioksidan dalam makanan dapat didefinisikan sebagai zat yang mampu menunda, memperlambat atau mencegah pengembangan ketengikan dan rasa dalam makanan atau kerusakan lainnya akibat oksidasi. Antioksidan menunda pergembangan aroma-tak sedap dengan memperpanjang periode induksi. Penambahan antioksidan setelah akhir periode ini cenderung tidak efektif dalam memperlambat pengembangan ketengikan.
Antioksidandapat menghambat ataumemperlambatoksidasidalam dua cara: baik dengan peredaman radikal bebas, dalam hal ini senyawa tersebut digambarkan sebagai antioksidan primer,atau dengan mekanisme yang tidak melibatkan peredaman radikal bebas langsung, dalam hal ini senyawa tersebut adalah antioksidan sekunder. Antioksidan primer termasuk senyawa fenolik. Komponen ini dikonsumsi selama periode induksi. Antioksidan sekunder beroperasi dengan berbagai mekanisme termasuk mengikat ion logam, peredaman oksigen, mengubah hidroperoksida untuk spesi non-radikal, menyerap radiasi UV atau menonaktifkan oksigen singlet.
Biasanya, antioksidan sekunder hanya menunjukkan aktivitas antioksidan ketika komponen minor keduanya ada. Hal ini dapat dilihat dalam kasus eksekusi agen seperti asam sitrat yang efektif hanya di hadapan ion logam, dan mengurangi agen seperti asam askorbat yang efektif dalam kehadiran tokoferol atau antioksidan primer lainnya (Pokorny, 2001).
2.3.7. Pengukuran Aktivitas Antioksidan dengan DPPHRadikal Bebas
Peredaman radikal merupakan suatu mekanisme utama dari antioksidan yang berperan dalam makanan. Beberapa metode yang telah dikembangkan dalam perhitungan nilai aktivitas antioksidan oleh peredaman radikal sintetis dalam pelarut organik polar, pada suhu kamar. Yang dipergunakan yakni radikal 2,2 diphenyl-1-picrylhydrazyl / DPPH dan2,2'-azino-bis(3-ethylbenzothiazoline-6-sulphonic acid)/ABTS.
Dalam pengujian DPPH, peredaman radikal-radikal DPPH diikuti dengan memantau penurunan absorbansi yang disebabkan karena reduksi oleh antioksidan (AH) atau reaksi dengan spesi radikal (R·)
DPPH· + AH DPPH-H + A·
DPPH· + R· DPPH-R
karena itu, keadaan dasar tidak akan tercapai untuk beberapa jam. Kebanyakan dokumentasi untuk penggunaan metode DPPH adalah peredaman setelah 15 atau 30 menit waktu reaksi. Hasil yang dituliskan berupa IC50, yang merupakan suatu
konsentrasi sampel antioksidan yang diuji mampu melakukan peredaman 50% terhadap radikal DPPH dalam jangka waktu tertentu.
Metode ini hanya berguna untuk skrining antioksidan, tetapi efektivitas antioksidan dalam makanan harus selalu dipelajari dengan metode lainnya karena aktivitas antioksidan dalam bermacam makanan tergantung pada banyak faktor yang meliputi polaritas, kelarutan dan aktivitas pengkelat logam (Pokorny, 2001)
2.4. Antioksidan
Senyawa antioksidan saat ini bermanfaat untuk berbagai bidang, seperti dalam bidang pangan, industri tekstil, minyak bumi, bahan pewarna dan lain-lain. Riset tentang perkembangan senyawa berkhasiat antioksidan telah banyak dikembangkan baik senyawa alam maupun senyawa sintetis. Senyawa antioksidan adalah senyawa yang berperanan untuk menghambat proses autooksidasi dalam minyak atau lemak (Ketaren, 1986).
Sebenarnya tubuh sendiri mempunyai sistem antioksidan termasuk superoksid dismutase, katalase, dan glutation, akan tetapi jika terjadi paparan oksidan yang berlebihan, antioksidan tubuh ini tidak akan mampu untuk mengatasinya. Sehingga tubuh memerlukan pasokan antioksidan dari luar (Nordmann,1993).
Antioksidan tubuh dikelompokkan menjadi tiga, yaitu : 1. Antioksidan primer
berfungsi untuk mencegah pembentukan senyawa radikal bebas baru. Antioksidan primer mengubah radikal bebas yang ada menjadi molekul yang berkurang dampak negatifnya sebelum radikal bebas ini sempat bereaksi. contoh : enzim SOD yang berfungsi sebagai pelindung hancurnya sel-sel dalam tubuh serta mencegah proses peradangan karena radikal bebas.
Enzim SOD sebenarnya sudah ada dalam tubuh kita. Namun, bekerjanya membutuhkan bantuan zat-zat gizi mineral seperti mangan, seng,dan tembaga. Selenium juga berperan sebagai antioksidan. Jadi, jika ingin menghambat gejala dan penyakit degeneratif, mineral -mineral tersebut hendaknya tersedia cukup mdalam makanan yang dikonsumsi tiap hari
2. Antioksidan sekunder
3. Antioksidan tersier
berfungsi memperbaiki kerusakan sel-sel dan jaringan yang disebabkan radikal bebas. Contoh : enzim yang memperbaiki DNA pada inti sel adalah metionin sulfoksidan reduktase. Adanya enzim-enzim perbaikan DNA ini berguna untuk mencegah penyakit kanker.
Untuk mencegah atau memperlambat kerusakan oksidatif makanan, antioksidan banyak digunakan sebagai aditif dalam lemak dan minyak, dan dalam pengolahan makanan. Jenis antioksidan yang dapat digunakan antara lain : antioksidan sintetis dan antioksidan alami (Ensofas, 2010).
2.4..1. Antioksidan Sintetis
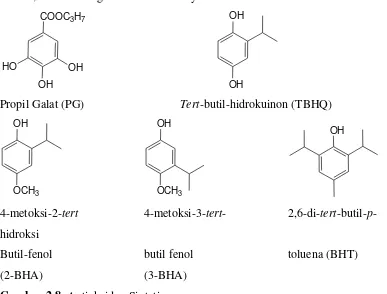
Beberapa antioksidan sintetis lebih popular digunakan adalah senyawa fenolik seperti butylatedhydroxyanisol, (BHA) butylatedhidroksi-toluen (BHT), tersierButyl hydro quinone (TBHQ) ,dan ester dari asam galat, misalnya propilgalat (PG) . Antioksidan fenolik sintetis selalu diganti dengan alkil untuk meningkatkan kelarutannya dalam lemak dan minyak. Keempat antioksidan sintetis pada prakteknya digunakan pada batas 0,02% kandungan lemak atau minyak dari makanan.
OH
OH HO
COOC3H7 OH
OH
Propil Galat (PG) Tert-butil-hidrokuinon (TBHQ)
OH
OCH3
OH
OCH3
OH
4-metoksi-2-tert 4-metoksi-3-tert- 2,6-di-tert-butil-p-hidroksi
Butil-fenol butil fenol toluena (BHT)
(2-BHA) (3-BHA)
Gambar 2.8. Antioksidan Sintetis
untuk membentuk endapan gelap dengan ion besi dan sensitivitas panas. Beberapa antioksidan, seperti BHA dan BHT, digunakan secara kombinasi akan dapat bersinergis, demikian juga BHA sinergis dengan PG.
Antioksidan sintetis sudah sangat benar-benar diuji untuk perilaku toksikologi-nya, tetapi beberapa dari perilakutoksikologi-nya, setelah lama penggunaan, di bawah tekanan berat sebagai data toksikologi baru yang memaksakan beberapa penggunaan yang hati-hati. Dalam konteks ini, produk antioksidan alami muncul sebagai antioksidan yang sehat dan lebih aman daripada sintetis. Sejak sekitar tahun 1980 antioksidan alami telah muncul sebagai alternatif antioksidan sintetis (Pokorny, 2001).
2.4.2. Antioksidan Alami
Penggunaan senyawa alami sebagai antioksidan sudah sangat lama. Hal itu meliputi pengasapan dan pembumbuan untuk pengawetan daging, ikan, dan makanan lain yang kaya lemak. Perlakuan tersebut diakui dapat memberi efek penghambat-tengik.
Hal ini tidak lazim untuk mencoba mendefinisikan antioksidan alami dapat mempengaruhi zat yang terbentuk sebagai konsekuensi dari memasak atau pengolahan bahan nabati atau hewani untuk makanan. Antioksidan alami hamper ditemukan pada semua mikroorganisme, jamur,dan bahkan di jaringan hewan dan tumbuhan ini sebagian besar adalah senyawa fenolik dan yang merupakan beberapa dari kelompok antioksidan alamiadalah flavonoid, asamfenolik dan minyak atsiri.
Flavonoid merupakan kelompok besar fenolat yang terdapat dalam tanaman yang dicirikan dengan rangka karbon C6-C3-C6. Dasar struktur dari senyawa ini terdiri
dari dua cincin aromatic dihubungkan oleh tiga-karbon rantai alifatik yang biasanya telah terkondensasi untuk membentuk piran atau cincin furan.
Kemampuan flavonoid menghambat oksidasi lipida didokumentasikan dengan baik, untuk produk lipida alami. Flavonoid dapat bertindak sebagai antioksidan dengan peredaman radikal yang mencakup superoksida anion, radikal lipida peroksil dan radikal hidroksil. Mekanisme lain dari flavonoid yang dipilih meliputi pendinginan singlet oksigen, logam khelasi, serta penghambatan lipoksigenase.
Turunan-turunan asam sinamat merupakan antioksidan lebih aktif daripada turunan
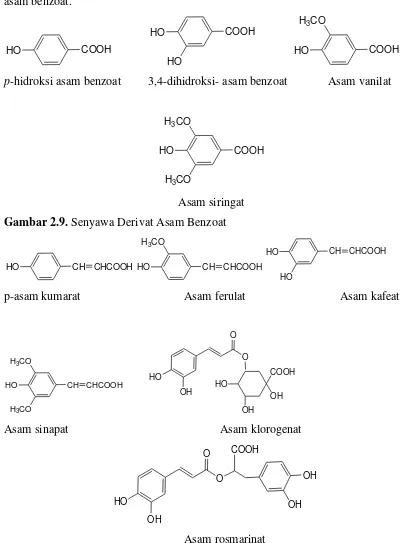
p-hidroksi asam benzoat 3,4-dihidroksi- asam benzoat Asam vanilat
HO COOH
H3CO
H3CO
Asam siringat Gambar 2.9. Senyawa Derivat Asam Benzoat
HO CH CHCOOH HO CH CHCOOH H3CO
Asam sinapat Asam klorogenat
OH
Gambar 2.9.1.Senyawa Derivat Asam Sinamat
aktivitas antioksidannya, misalnya asam klorogenat kurangefektif daripada asam kafeat (Pokorny, 2001).
Minyak atsiri merupakan senyawa yang volatil, alami dan dengan bau yang kuat dimana terdapat pada setiap bagian dari tanaman sepertu bunga, daun, biji, akar, rimpang, kayu dan resin sebagai metabolit sekunder yang biasanya diperoleh dengan destilasi air ataupun uap. Minyak atsiri sering dianalisis dengan tujuan utama antara lain : (i) untuk mengidentifikasi dan mengetahui banyaknya komponen senyawa yang mungkin terdapat didalamnya. (ii) untuk mengevaluasi kualitas dari minyak dan mendeteksi adanya kemungkinan bahwa komponen didalamnya memiliki pengaruh yang bermanfaat. Analisis minyak atsiri umumnya dilakukan menggunakan kromatografi gas-spekstroskopi massa.
Kebanyakan komponen minyak atsiri merupakan kelompok besar dari terpen (Hamid, 2011). Terpen yang juga dikenal sebagai terpenoid atau isoprenoid membentuk kelompok terbesar dari produk tanaman alam. Dalam ilmu medis, terpen biasanya digunakan sebagai agen antiseptik, anti-inflamasi, untuk penyakit kanker dan malaria serta antioksidan (Degenhardt, 2003).
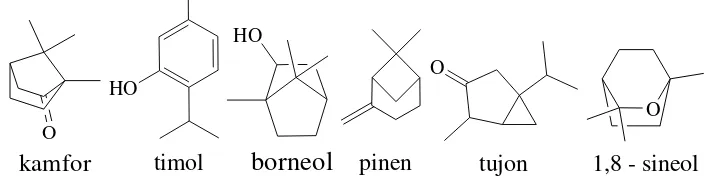
Komponen senyawa yang tidak jenuh dan teroksigenasi lebih stabil dalam melawan pengaruh oksidasi dibandingkan komponen lainnya, yakni golongan monoterpen dan seskuiterpen (Handa, 2008). Monoterpen juga merupakan komponen primer dari minyak atsiri dan mempunyai pengaruh medis didalamnya. Beberapa komponen senyawa yang mempunyai aktivitas antioksidan yaitu karvakrol, timol, ɤ
-terpinen (Bakkali, 2008), α-pinen (Gundidza, 2008), α-tujon, kamfor, 1,8-sineol, β -tujon dan borneol (Kadri,2011).
O
kamfor
HO
timol
HO
borneol
pinenO
tujon
O
1,8 - sineol Gambar 2.9.2. Senyawa-senyawa komponen dalam minyak atsiri
mutagenik, tetapi banyak senyawa bahan alami belum pernah diuji. Adapun keuntungandan kerugian dari antioksidan sintetis dan alami dirangkum dalam (Tabel2.4).
Tabel 2.4.Keuntungandan Kerugian dariAntioksidanSintetis dan Alami Antioksidan sintetis Antioksidan alami
murah mahal
Banyak diterapkan Kegunaan terbatas padabeberapa produk
menengahdengan aktivitasantioksidan yang tinggi
Aktivitas antioksidan dengan rentang yang luas
meningkatkan soal keselamatan dianggap sebagaizatberbahaya
Penggunaan dilarang untuk beberapa dari mereka
Meningkatkan dan memperluas penggunaan aplikasi
Kelarutan rendah dalam air Jangkauan kelarutan luas Menurunkan keuntungan Menaikkan keuntungan
Tidak ada argument ilmiah atau teknis rasional dapat diberikan untuk antioksidan alami: antioksidan alami lebih diterima oleh konsumen terutama berdasarkan alasan emosional. Kebanyakan antioksidanyang umumnya ditambahkan pada makanan (misalnya propel galat, flavonoid, tokoferol-a, asam karnosat, karnosol, katekin, vitamin C) merupakan yang mampu menstimulasi radikal bebas kerusakan pada komponen nonlipida, karbohidrat dan DNA dalam makanan.
Namun,manfaat menggunakan antioksidan lebih besar daripada risiko. Tanpa antioksidan dalam makanan, produk oksidasi yang terbentuk dapat menyebabkan resiko yang lebih besar untuk kesehatan (Pokorny, 2001). Bahan-bahan alami yang kaya akan antioksidan dapat diperoleh dengan ekstraksi.
2.5. Ekstraksi
Metode ekstraksi dilakukan tergantung pada beberapa faktor, antara lain : - tujuan dilakukan ekstraksi
- skala ekstraksi
Ekstraksi merupakan istilah yang paling umum untuk mendapatkan suatu senyawa yang berasal dari suatu campuran yang didapat dari kontak antara pelarut dengan senyawa terlarut di dalam bahan yang kita inginkan. Campuran itu bisa saja berupa padatan ataupun cairan, dan berbagai teknik dan alat ukur yang digunakan untuk situasi yang berbeda. (Rodig, 1997)
Ragam ekstraksi yang tepat sudah tentu bergantung pada tekstur dan bahan kandungan air dalam bahan tumbuhan yang diekstraksi. Umumnya kita perlu menghidrolisis jaringan tumbuhan untuk mencegah terjadinya oksidasi enzim. Mencelupkan jaringan daun segar atau bunga (bila perlu dipotong-potong) kedalam metanol mendidih yang mana merupakan suatu cara yang baik untuk mencapai tujuan itu. Alkohol merupakan pelarut serbaguna yang baik untuk ekstraksi pendahuluan. Selanjutnya bahan dapat dimaserasi dalam suatu pelumat, lalu disaring. Tetapi hal ini hanya betul-betul diperlukan bila kita ingin mengekstraksi habis. (Harbone,1987)
2.5.1. Ekstraksi Lipida dari Makanan dan Bahan Biologis Lipida dalam hal sifat yang terkait dengan molekul lain melalui
(a) interaksi Van der Waals
contoh : interaksi beberapa lipida dengan protein (b) ikatan elektrostatis dan hidrogen
terutama antara lipida dengan protein
(c) ikatan kovalen antara lipida, karbohidrat dan protein
Karena itu, untuk memisahkan dan mengisolasi lipida dari matriks seluler yang kompleks,penanganan secara kimia dan fisis yang berbeda harus diberikan.
Ketidaklarutan dalam air secara umum digunakan untuk pemisahan lipida dari komponen lainnya. Ekstraksi lengkap mungkin memerlukan waktu ekstraksi yang lama atau seri atau kombinasi pelarut sehingga lipida dapat dilarutkan dari matriks. Prosedur dalam ekstraksi lipida dari jaringan hewan atau tumbuhan biasanya meliputi beberapa langkah :
(a) penyediaan sampel, yang meliputi: pengeringan, pengecilan ukuran atau hidrolisis
(b) homogenisasi jaringan dengan adanya pelarut
(c) pemisahan cairan (organik dan larutan) dan fase padat (d) penghilangan kontaminasi non-lipida
A. Penyediaan Sampel
Persiapan sampel untuk analisis lipida tergantung pada jenis makanan dan sifat lipidanya. Analisis yang efektif membutuhkan pengetahuan tentang kimia, struktur dan konstituennya. Oleh karena itu, tidak mungkin merancang metode standar tunggal untuk ekstraksi semua jenis lemak dalam makanan yang berbeda.
Ekstraksi lipida harus dilakukan sesegera mungkin setelah pelepasan jaringan dari organisme hidup sehingga untuk meminimalkan perubahan berikutnya. Ekstraksi langsung tidak selalu mungkin, namun sampel biasanya disimpan pada suhu yang sanga trendah dalam wadah tertutup, di bawah suasana (nitrogen) inert atau di atas es kering. Namun, proses pembekuanitu sendiri secara permanen dapat merusak jaringan sebagai akibat dari kejutan osmotik.
Pencairan sampel diambil dari penyimpanan beku sebelum ekstraksi dapat meningkatkan kerusakan ini. Oleh karena itu, sampel jaringan harus homogen dan diekstraksi dengan pelarut tanpa diperbolehkan untuk mencair. Enzim lipolitik jaringan hewan dan tumbuhan biasanya dinonaktifkan ireversibel oleh homogenisasi dengan pelarut polar. Penggunaan suhu tinggi harus dihindari, melainkan juga dianjurkan, bila mungkin, untuk menjaga suasana inert selama persiapan sampel dan ekstraksi yang dapat meminimalkan reaksi oksidasi lipida tak jenuh.
B. Perlakuan 1. Pengeringan
Kadang-kadang pelarut nonpolar, seperti dietil eter dan heksana, tidak mudah menembus jaringan lembab (kelembaban > 8%); Oleh karena itu, ekstraksi lipida efektif tidak terjadi. Dietil eter adalah higroskopis dan menjadi jenuh dengan air sehingga tidak efisien untuk ekstraksi lipida. Pengeringan oven vakum pada suhu rendah atau liofilisasi biasanya dianjurkan.
2. Pengecilan ukuran partikel
Efisiensi ekstraksi lipida dari sampel kering juga tergantung pada ukuran partikel. Oleh karena itu, pengecilan ukuran partikel dapat meningkatkan luas permukaan, yang memungkinkan lebih banyak kontak langsung dengan pelarut, dan meningkatkan ekstraksi lipida.
Untuk membuat lipida yang tersedia bagi pelarut ekstraksi, matriks makanan sering dihidrolisis dengan asam atau alkali sebelum ekstraksi. Hidrolisis asam atau alkali diperlukan untuk melepaskan kovalen dan ionic terikat lipida dengan protein dan karbohidrat serta untuk memecah emulsi lemak. Digesti sampel dengan asam (biasanya3-6M HCl) dalam kondisi refluks mengubah lipida terikat tersebut untuk bentuk yang mudah diekstrak.
C. Ekstraksi lipida dengan pelarut
Ketidaklarutan lipida dalam air membuat kemungkinan pemisahan mereka dari protein, karbohidrat dan air dalam jaringan. Dalam analisis makanan rutin, kandungan lemak (kadang-kadang disebut ekstrak eter, lemak netral, atau lemak kasar) mengacu pada konstituen lipida “bebas” yang dapat diekstraksi ke dalam pelarut kurang polar, seperti petroleum eter atau dietil eter. Konstituen lipida yang “terikat” memerlukan pelarut lebih polar, seperti alkanol, untuk ekstraksi mereka.
Oleh karena itu, penggunaan pelarut universal tunggal untuk ekstraksi lipida dari jaringan tidak mungkin. Selama ekstraksi pelarut, ikatan VanderWaals dan interaksi elektrostatik serta ikatan hidrogen rusak sampai batas yang berbeda, namun ikatan kovalen tetap utuh.
Lipida netral terikat secara hidrofobik dandapat diekstraksi dari jaringan oleh pelarut nonpolar, sedangkan lipida polar, yang terikat secara dominan oleh gaya elektrostatik dan ikatan hidrogen, memerlukan pelarut polar untuk mampu memecah ikatan tersebut (Akoh, 2002).
Lipida yang terikat secara kovalen kelompok polipeptida dan polisakarida tidak akan diekstrak sama sekali oleh pelarut organik dan akan tetap dalam residu nonlipida. Oleh karena itu, langkah hidrolisis mungkin diperlukan untuk melepaskan lipida kovalen terikat untuk membuat mereka sepenuhnya diekstrak :
1. Sifat pelarut ekstraksi
Pelarut ekstraksi juga dapat mencegah hidrolisis lemak secara enzimatis, sehingga memastikan tidak adanya reaksi samping. Pelarut harus siap menembus partikel sampel dan harus memiliki titik didih yang relatif rendah untuk menguap dengan mudah tanpa meninggalkan residu ketika memperoleh lipida kembali.
Pelarut yang banyak digunakan untuk isolasi lipida adalah alkohol (metanol, etanol, isopropanol, n-butanol), aseton, asetonitril,eter (dietil eter, isopropil eter, dioksan, tetrahidrofuran), halokarbon (kloroform, diklorometan), hidrokarbon (heksana, benzena, sikloheksana, isooktana) atau campurannya. Meskipun pelarut seperti benzena berguna dalam ekstraksi lipida, disarankan untuk mencari pelarut alternatif karena sifat potensial kanker dari produk tersebut, mudah terbakar dan toksisitas pelarut juga menjadi pertimbangan penting untuk meminimalkan potensi bahaya serta biaya dan sifat nonhigroskopis.
2. Metode ekstraksi dengan pelarut tunggal
Dietil eter dan petroleum eter merupakan yang paling umum digunakan untuk ekstraksi lipida. Di samping itu, heksana dan kadang-kadang pentana lebih disukai untuk mendapatkan lipida dari minyak sayur Dietil eter mempunyai kemampuan solvasi yang lebih baik untuk lipida dibandingkan dengan petroleum eter.
3. Metode ekstraksi dengan kombinasi pelarut
Suatu pelarut tunggal nonpolar tidak dapat mengekstrak lipida polar dari jaringan untuk memastikan secara lengkap dan kuantitatif lipida dari jaringan, sistem pelarut terdiri dari berbagai perbandingan komponen polar dan nonpolar dapat digunakan seperti campuran ekstrak lipida total lebih mendalam dan ekstrak ini cocok untuk karakterisasi lipida lebih lanjut.
dengan atau tanpa air telah berhasil digunakan untuk mengekstrak jaringan. Heksana-isopropanol (3:2), heptana-etanol-air-natrium dodesilsulfat (1:1:1), metilen klorida-metanol (2:1) dan heksana-aseton (1:1) merupakan pelarut kombinasi digunakan untuk mengekstrak lipida dari bahan biologis
4. Metode ekstraksi dengan pelarut non-organik
Karena masalah lingkungan dan bahaya kesehatan potensial dari pelarut organik, pelarut nonorganic telah menjadi populer. Penggunaan gelombang mikro untuk mengisolasi lipida. Disarankan bahwa energi gelombang mikro dengan meningkatkan kekuatan rotasi yang menghubungkan molekul dipol pada molekul yang berdekatan, mengurangi energi yang dibutuhkan untuk mengganggu asosiasi hidrofobik. Ikatan hydrogen dan interaksi elektrostatis, sehingga membantu untuk melarutkan semua jenis lipida.
D. Penghapusan kontaminan nonlipida dari ekstrak lipida dan pertimbangan praktis lainnya
Penghapusan kontaminan nonlipida dari ekstrak lipida diperlukan karena sebagian besar pelarut yang digunakan juga melarutkan sejumlah besar minyak yang larut dalam rasa, pigmen, gula, asam amino, peptida rantai pendek, garam anorganik dan urea. Penggunaan larutan garam memiliki keuntungan mencegah atau meminimalkan pembentukan fase menengah.
E. Penghilangan pelarut dari ekstrak lipida
Penghilangan pelarut dari ekstrak lipida harus dikondisikan secara vakum dalam rotari evaporator, larutan harus dipekatkan dan dipindahkan ke dalam botol kecil. Lipida harus disimpan segera dalam pelarut non-alkoho linert seperti kloroform, n-heksana bukannya dibiarkan tetap dalam keadaan kering untuk waktu yang lama.