BAB 1
BAB 1
PENDAHULUAN
PENDAHULUAN
1.1 Latar Belakang 1.1 Latar BelakangUrin atau air seni atau air kencing adalah cairan sisa yang diekskresikan oleh ginjal Urin atau air seni atau air kencing adalah cairan sisa yang diekskresikan oleh ginjal yang kemudian akan dikeluarkan dari dalam tubuh melalui proses urinasi. Eksreksi yang kemudian akan dikeluarkan dari dalam tubuh melalui proses urinasi. Eksreksi urin diperlukan untuk membuang molekul-molekul sisa dalam darah yang disaring urin diperlukan untuk membuang molekul-molekul sisa dalam darah yang disaring oleh ginjal dan untuk menjaga homeostasis cairan tubuh. Dalam mempertahankan oleh ginjal dan untuk menjaga homeostasis cairan tubuh. Dalam mempertahankan homeostasis tubuh peranan urin sangat penting, karena sebagian pembuangan cairan homeostasis tubuh peranan urin sangat penting, karena sebagian pembuangan cairan oleh tubuh adalah melalui sekresi urin. Selain urin juga terdapat mekanisme oleh tubuh adalah melalui sekresi urin. Selain urin juga terdapat mekanisme berkeringat
berkeringat dan dan juga juga rasa rasa haus haus yang yang kesemuanya kesemuanya bekerja bekerja sama sama dalamdalam mempertahankan homeostasis ini.
mempertahankan homeostasis ini.
Urin yang kita keluarkan terdiri dari berbagai unsur seperti : air, protein, amoniak, Urin yang kita keluarkan terdiri dari berbagai unsur seperti : air, protein, amoniak, glukosa, sedimen, bakteri, epitel dsb. Unsur-unsur tersebut sangat bervariasi glukosa, sedimen, bakteri, epitel dsb. Unsur-unsur tersebut sangat bervariasi perbandingannya
perbandingannya pada pada orang orang yang yang berbeda berbeda dan dan juga juga pada pada waktu waktu yang yang berbeda berbeda dandan dipengaruhi oleh makanan yang kita konsumsi. Kandungan urin inilah yang dipengaruhi oleh makanan yang kita konsumsi. Kandungan urin inilah yang menentukan tampilan fisik air urin seperti kekentalannya, warna, kejernihan, bau, menentukan tampilan fisik air urin seperti kekentalannya, warna, kejernihan, bau, busa, dsb.
busa, dsb.
Untuk mengetahui aktivitas enzim diastase dalam menghidrolisis amilum oleh karena Untuk mengetahui aktivitas enzim diastase dalam menghidrolisis amilum oleh karena itu kita akan melakukan praktikum kali ini. Enzim diastase dapat ditemukan di dalam itu kita akan melakukan praktikum kali ini. Enzim diastase dapat ditemukan di dalam air liur di mulut yang dikeluarkan dari kelenjar air liur dan di dalam usus halus yang air liur di mulut yang dikeluarkan dari kelenjar air liur dan di dalam usus halus yang dikeluarkan dari pankreas.
dikeluarkan dari pankreas.
1.2 Tujuan Praktikum 1.2 Tujuan Praktikum
Setelah dilaksankan praktikum, mahasiswa diharapkan mampu: Setelah dilaksankan praktikum, mahasiswa diharapkan mampu:
1.
1. Memahami pengertian dari urinMemahami pengertian dari urin 2.
2. Memahami komponen urin normalMemahami komponen urin normal 3.
3. Mengetahui kadar atau aktivitas enzim diastase normal yang terdapat dalamMengetahui kadar atau aktivitas enzim diastase normal yang terdapat dalam urin
BAB II
TINJAUAN PUSTAKA
2.1 Urine
Urine adalah cairan sisa yang diekskresikan oleh ginjal yang kemudian akan dikeluarkan dari dalam tubuh melalui proses urinasi. Urine disaring didalam ginjal, dibawa melalui ureter menuju kandung kemih, akhirnya dibuang keluar tubuh melalui uretra. Cairan dan materi pembentuk urine berasal dari darah atau cairan interstisial. Komposisi urine berubah sepanjang proses reabsorbsi ketika ada molekul yang masih dibutuhkan oleh tubuh. Cairan yang tersisa mengandung urea dalam kadar yang tinggi dan berbagai senyawa yang berlebih atau berpotensi racun yang akan dibuang keluar dari tubuh (Poedjiadi, 2005).
Urine atau air seni atau air kencing adalah cairan sisa yang diekskresikan oleh ginjal yang kemudian akan dikeluarkan dari dalam tubuh melalui urinalisasi. Ekskresi urine diperlukan untuk membuang molekul-molekul sisa dalam darah yang disaring oleh ginjal dan menjaga homeostasis cairan tubuh. Dalam mempertahankan homeostasis tubuh peranan urine sangat penting, karena sebagian pembuangan cairan oleh tubuh adalah melalui sekresi urine (Soendoro, 1985).
2.1.1 Proses Pembentukan Urine Manusia
Urine berasal dari darah yang dibawa arteri renalis masuk ke dalam ginjal dengan melalui glomerulus berfungsi sebagai ultrafiltrasi pada simpai Bowman, berfungsi untuk menampung hasil filtrasi dari glomerulus. Pada tubulus ginjal akan terjadi penyerapan kembali zat-zat yang sudah disaring pada glomerulus, sisa cairan akan diteruskan ke piala ginjal terus berlanjut ke
Ada tiga tahap dalam pembentukan urine:
1. Proses Filtrasi
Proses ini terjadi di glomerulus, proses filtrasi terjadi karena permukaan aferen lebih besar dari permukaan eferen sehingga terjadi penyerapan darah. Sedangkan sebagian tersaring adalah bagian cairan darah kecuali protein. Cairan yang tersaring ditampung oleh simpai Bowman yang terdiri dari glukosa, air, natrium, klorida, sulfat, bikarbonat, dan lain-lain yang diteruskan ke tubulus ginjal (Ganong, 2003).
2. Proses Reabsorbsi
Fungsi utama tubulus proksimal adalah reabsorbsi, yaitu proses dikembalikannya air bersama dengan glukosa, asam amino, asam urat dan protein yang berhasil menembus filter glomerulus ke aliran darah. Tubulus proksimal juga mengembalikan elektrolit, natrium, klorida dan bikarbonat. Simpai henle mereabsorbsi air dan natrium. Tubulus distal secara halus mengatur konsentrasi ion-ion ntrium, kalium, bikarbonat, fosfat dan hidrogen (Ganong, 2003).
3. Proses Sekresi
Proses ini adalah proses penyerapan urine sisa dari filtrasi dan reabsorbsi. Proses penyerapan urine ini terjadi pada tubulus dan diteruskan ke piala ginjal selanjutnya diteruskan ke ureter masuk ke vesika urinaria. Pada proses sekresi ini menghasilkan urine yang sesungguhnya (Ganong, 2003).
2.2 Metode Wohlgemuth
Diastase adalah enzim yang bekerja memecah amilum. Tahap awal enzim bekerja mengubah amilum menjadi dekstrin yang berwarna ungu dengan iodium. Kemudian menjadi eritrodekstrin yang memberikan perubahan warna iodium. Akhirnya diubah menjadi maltosa yang juga tidak memberikan warna dengan Iodium. Cara penentuan aktivitasnya dapat dilakukan dengan mengencerkan enzim tersebut agar dapat diketahui aktivitasnya. Hasilnya dinyatakan dalam satuan unit. Satu Unit diastase, diartikan dengan banyaknya mL amilum yang dapat diuraikan oleh enzim yang terdapat dalam 1 mL sampel (serum atau urin) pada suhu 37 derajat Celsius selama 30 menit. Kadar atau aktivitas enzim diastase normal yang terdapat dalam urin adalah 32 U/L, sedangkan dalam serum adalah 16 U/L.
Kata enzim berarti “dalam ragi”. Suatu enzim adalah suatu katalis biologis. Hewan tingkat tinggi memiliki ribuan enzim. Hamper semua reaksi kimia dikatalis oleh enzim. Bahkan kesetimbangan CO2 + H2O ↔ H2CO3 dikatalis oleh enzim karena laju penyetimbangan tanpa katalis tidak menghasilkan asam karbonat yang cukup cepat untuk keperluan hewan. Enzim merupakan katalis yang lebih efisien daripada kebanyakan katalis laboratorium atau industri (seperti Pd pada reaksi dehidrogenasi). Reaksi biologis dalam tubuh berlangsung pada 37o C dan dalam medium air. Enzim suatu pengendali laju reaksi yang yang tidak dimungkinkan oleh kelas katalis lain. Suatu enzyme adalah protein.
Enzim adalah sekelompok protein yang berperan sebagai pengkatalis dalamreaksi-reaksi biologis. Enzim dapat juga didefenisikan sebagai biokatalisator yangdihasilkan oleh jaringan yang berfungsi meningkatkan laju reaksi dalam jaringan itusendiri. Semua enzim yang diketahui hingga kini hampir seluruhnya adalah protein.Berat molekul enzim pun sangat beraneka ragam, meliputi rentang yang sangat luas (Suhtanry & Rubianty, 1985).
Beberapa memiliki struktur yang sederhana, namun sebagian besar memiliki struktur yang rumit. Banyak enzim yang strukturnya tidak diketahui. Untuk aktivitas biologis. Beberapa enzim memerluakan gugus-gugus prostetik ddan kofaktor. Kofaktor ini merupakan bagian non-protein dari enzim itu. Suatu kofaktor dapat brupa ion logam sederhana, ion tembaga misalnya merupakan suatu kofaktor bagi enzim suatu asam askorbat oksidase. Enzim lain mengandung molekul organic non-protein sebagai kofaktor. Gugus prostetik organic biasanya sering kali dirujuk sebagai suatu koenzim. Jika suatuorganisme tidak dapat mensintesis suatu kofaktor yang diperlukan maka kofaktor itu harus terdapat dalam makanan dalam jumlah kecil. Satuan-satuan aktif dari banyak kofaktor adalah vitamin (Fessenden, 1989: 396).
Dalam pengolongan enzim berdasarkan reaksi yang dikatalis ada 6 kelas utama enzim. Tiap-tiap enzim ditetapkan dalam empat tingkat nomor kelas dan di beri suatu nama sistematik yang mengidentifikasi reaksi yang dikatalis. Kebanyakan enzyme mangatalis pemindahan electron, atom, atau gugus fungsional.
Dalam dunia biokimia sering kita mendengar enzim amylase. Amylase merupakan enzyme yang termasuk dalam kelas hidrolase, yang menghidrolisis amilum menjadi monosakaridanya. Enzime amilum memecah ikatan-ikatan amilum hingga membentuk maltosa. Ada 3 macam enzim amylase yaitu α-amilase, β-amilase, dan γ-amilase. α-amilase terdapat pada saliva dan pancreas. Enzyme ini memecah ikatan 1-4 yang terdapat pada amilum dan disebut endoamilase sebab enzim ini memecah bagian dalam atau bagian tengah molekul amilum. β-amilase teutama terdapat pada tumbuhan dan dinamakan ekso-amilase sebab memecah dua unit glukosa yang terdapat pada ujung molekul amilum secara berurutan sehingga terbentuk maltosa. γ-amilase telah diketahui terdapat dalam hati. Enzim ini dapat memecah ikatan 1-4 dan 1-6 pada glikogen dan menghasilkan glokosa (Poedjiadi, 1994: 155).
Enzim -amilase mengkatalisis hidrolisis ikatan 1,4 pati menghasilkan maltodekstrin linear pendek. Enzim ini digunakan secara luas dalam industri makanan dan deterjen. Penggunaan amilase dari bakteri halofil dapat memberikan keuntungan karena memiliki aktivitas optimum di kadar garam tinggi (Ventosa & Nieto 1995). Baru sedikit informasi yang ada mengenai amilase dari bakteri halofil. Acinetobacter sp. (Onishi & Hidaka 1978), Nesterenkonia halobia (Onishi & Sonoda 1979), Micrococcus varianssubsp. Halophilus (Kobayashi et al. 1986), dan isolat Micrococcus spp. (Onishi 1972, Khire 1994) dilaporkan memiliki aktivitas amilolitik, tetapi tidak tersedia informasi mengenai karakteristik molekulernya. Satu-satunya bakteri halofil yang telah dikarakterisasi amilasenya secara molekuler ialah Halomonas meridiana. Hasil analisis protein dari gen penyandi amilasenya menunjukkan homologi yang cukup tinggi dengan amylase dari bakteri lain, streptomycetes, serangga, dan mamalia (Coronado et al. 2000).
BAB III
METODOLOGI PRAKTIKUM
3.1 Waktu dan Tempat
Hari, Tanggal : Kamis, 28 September 2017 Waktu : 08.00 s.d. selesai
Tempat : Laboratorium Terpadu Poltekkes Tanjung Karang
3.2 Alat dan Bahan
Alat : 1. Tabung-tabung reaksi 2. Maat pipet 1, 2, 5, 10 3. Water bath
Bahan : 1. Larutan NaCl 0,9% 2. Larutan amilum 1% 3. Larutan Iodium 0,1 N 4. Air seni
3.3 Prosedur Kerja
Menyediakan 12 tabung reaksi, beri nomor secara berurutan.
Ke dalam tabung nomor 1 dan 2, masukkan 1 mL urin dan ke dalam tabung nomor 2 sampai 12 masukkan masing-masing 1 mL larutan NaCl 0,9%
Mencampur tabung 2 sampai homogen, dipindahkan sebanyak 1 mL dari tabung 2 ke tabung ke 3.
Mencampur tabung 3 sampai homogen, dipindahkan sebanyak 1 mL dari tabung 3 ke tabung ke 4, dan seterusnya sampai tabung 12. Dari tabung 12
buan seban ak 1 mL.
Ke dalam tiap tabung ditambahkan masing-masing 2 mL larutan amilum 1% dan 2 mL larutan buffer phosphat pH 6,8 kocok sampai homogen.
Memasukkan semua tabung ke dalam penangas air dengan suhu 37o Celsius selama 30 menit.
Didinginkan, kemudian pada tabung 1 dan 2 tambahkan 3 tetes larutan iodium 0,1 N, sedangkan pada tabung lainnya masing-masing ditambahkan 2
tetes larutan iodium 0,1 N.
Mengamati perubahan warna yang terjadi.
BAB IV
HASIL DAN PEMBAHASAN
4.1 Hasil Praktikum
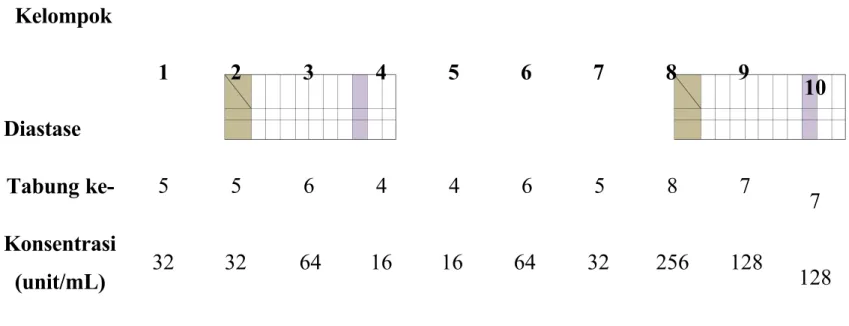
Tabel diastase urine.
Kelompok Diastase 1 2 3 4 5 6 7 8 9 10 Tabung ke- 5 5 6 4 4 6 5 8 7 7 Konsentrasi (unit/mL) 32 32 64 16 16 64 32 256 128 128 4.2 Pembahasan
Dalam praktikum ini, kami hanya memakai satu sample urine, tetapi masih belum diketahui probandus mempunyai penyakit apa, karena tidak pernah melakukan uji urine atau tes lab yang lainnya. Urin yang kita keluarkan terdiri dari berbagai unsur seperti : air, protein, amoniak, glukosa, sedimen, bakteri, epitel dsb. Unsur-unsur tersebut sangat bervariasi perbandingannya pada orang yang berbeda dan juga pada waktu yang berbeda dan dipengaruhi oleh makanan yang kita konsumsi. Kandungan urin inilah yang menentukan tampilan fisik air urin seperti kekentalannya, warna, kejernihan, bau, busa, dsb.
karena ketika itu sampel masih belum terkontaminasi apapun. Menurut para dokter dalam Medicinenet pun begitu, sampel yang optimal cenderung menjadi sampel urin pagi hari karena seringkali yang paling terkonsentrasi urin diproduksi dalam sehari. Warna urine yang kami amati berwarna kuning tua. Menurut MedlinePlus yang merupakan Medical Encyclopedia Air kencing kuning terang masuk dalam kategori warna normal menunjukkan bahwa tubuh terdihidrasi dengan baik.
Berikut terdapat tabel warna air seni:
Bau urin dapat bervariasi karena kandungan asam organik yang mudah menguap. Diantara bau yang berlainan dari normal seperti: bau oleh makanan yang mengandung zat-zat atsiri seperti jengkol, petai, durian, asperse dll. Bau obat-obatan seperti menthol, dbs.
Pada buku Biokimia Harper dinyatakan bahwa bau amoniak biasanya terjadi kalau urin dibiarkan tanpa pengawet atau karena reaksi oleh bakteri yang mengubah ureum di dalam kantong kemih.Bau keton sering pada penderita kencing manis, dan bau busuk sering terjadi pada penderita keganasan (tumor) di saluran kemih.Pada urine probandus terdapat bau amonia hal ini karena kami tidak memakai pengawet pada urine ini. Bau amonia ini dikarenakan amonnium yang terkandung di dalm urine menguap atau terlepas ke udara.Ini berarti urin sampel mengandung garam
amonium.Reaksi utama pada tubuh yang menghasilkan NH4+ terjadi di dalam sel, yaitu perubahan glutamin menjadi glutamat yang dikatalisis oleh enzim glutaminase yang terdapat di dalam sel tubulus renalis. Glutamat dehidrogenase mengkatalisis perubahan glutamat menjadi α-ketoglutarat.
Glutamin → glutamat + NH4+Glutamate → α-ketoglutarat + NH4+
Urin mengandung: 1. Air dan garam-garam dalam jumlah sedemikian rupa sehingga terdapat keseimbangan antara cairan ekstrasel dan cairan intrasel.
2. Asam dan basaSisa-sisa metabolisme yang tidak berguna lagi bagi tubuh.
3. Zat-zat yang dikeluarkan dari darah karena kadarnya berlebihan.
Menurut Eni dalam websitenya “Enifreaks”, urine normal biasanya bersifat sedikit asam dengan pH antara 5 – 7, pernyataan ini diambil dari Kimber. Dari pernyataan tersebut dapat diketahui bahwa urine probandus meskipun tidak netral dan dapat dikatakan bersifat asam masih merupakan urine normal karena memang urine normal bersifat sedikit asam. Lain halnya dengan urine orang yang vegetarian. Bagi urine
orang yang vegetarian nantinya akan didapat urine yang bersifat alkali. Menurut Biokimia Harper, dalam cairan interstisial dan urin tubulus, NH3 bergabung dengan H+ membentuk NH4+ yang menyingkirkan NH3 dan mempertahankan perbedaan konsentrasi yang memudahkan difusi NH3 keluar sel. Bila pH urin7,0 maka rasio NH3 : NH4+ = 1 : 100. Bila urin lebih asam, maka keseimbangan berubah lebih lanjut ke NH4+. Proses NH3 disekresikan disebut difusi non-ionik. Salisilat dan sejumlah obat lain yang merupakan basa lemah atau asam lemah juga disekresi oleh difusi non ionik. Ion ammonium berasal dari makanan, obat-obatan dan hasil hidrolisa urea.
Enzyme adalah suatu protein yang memiliki fungsi sebagi katalis suatu reaksi pada organisme., baik tumbuhan maupun hewan. Enzyme sering disebut sebagai biokatalis karena hal diatas. Suatu enzyme sendiri hanya mengkatalis satu arah reaksi saja. Sehingga di dalam tubuh memiliki banyak sekali enzyme. Dalam struktur enzyme sendiri dibagi menjadi 2 bagian yaitu sisi protein dan sisi non-protein. Enzyme diberi nama berdasarkan subtratnya dan berakhiran – ase. Contohnya amilum = amylase. Enzyme sendiri di golongkan menjadi 6 macam golongan utama antara lain Oksireduktase, Transferase, hidrolase, liase, isomerase dan ligase (Lehningger, 1988).
Pada praktikum ini kita hanya membahas enzyme amylase yang termasuk sebagai golongan enzyme hidrolase. Enzyme ini menghidrolisis amilum menjadi maltosa secara bertahap . tahapan hidrolisis amilum adalah sebagai berikut. Amilum-amilum terlarut amilodekstrin-eritodekstrin-akrodekstrin-maltosa. Masing-masing tahap ini akan menghasilkan warna yang berbeda jika larutan ditambahkan larutan iod, yang awalnya biru karena terbentuknya kompleks antara amilosa dengan iod, dan semakin kecil seperti eritodekstrin akan memberikan warna merah dengan larutan iod (Poedjiadi,1994).
Enzyme amylase sendiri hanya memecah ikatan (1-4) glikosida bukan memecah ikatan (1-6) glikosida, jadi untuk memecahkanya di perlukan suatu enzyme lain yang disebut glokusidase. Dekstrin sendiri yang dapat di identifikasi dalam praktikum ini adalah berupa campuran oligosakarida yang memiliki ikatan (1-4) dan (1-6) glikosida (Fessenden, 1989).
Enzyme amylase sendiri dapat di peroleh dari saliva atau pancreas. Pada air seni juga terdapat sedikit amylase, maka untuk mengetahuinya pada praktikum ini dilakukan uji dengan penambahan urin pada 10 tabung reaksi dengan kosentrasi yang berbeda. Sebagai indikatornya kita mengunakan larutan iod, sedangkan untuk larutan ujinya kita mengunakan larutan amilum 0,1% yang mengandung NaCl. NaCl ini berfungsi agar larutan tahan (awet), karena amilum cepat rusak saat penyimpanan terlalu lama,
amilum mudah rusak karena adanya bakteri di udara bebas. Karena reaksi ini cukup lambat maka kita melakukan pemanasan tetapi dengan suhu tertentu agar diperoleh suhu maksimum sehingga enzyme berjalan cukup cepat. Pemanasan dilakukan pada suhu 37o C selama 30 menit pada temperatur ruangan atau sampai terjadi ada perubahan warna.
Setelah pemanasan tabung reaksi di dinginkan agar reaksi langsung berhenti sehingga diharapkan hasil dapat diamati dengan jelas. Dan pada hasil pengamatan yang didapat terjadi perubahan pada tabung ke- 8 tersebut. Hal ini dikarenakan amilum akan memberikan warna biru, dan eritodekstrin akan memberikan warna merah. Jumlah iod yang paling sedikit diperlukan untuk mengubah 2 mL larutan amlium (berisi urine pula) terlarut menjadi erythrodextrine merupakan petunjuk tentang kadar amilase yang terdapat pada urine. Indeks diastase dari urine normal berkisar antara 5-20. Bila melebihi ambang tersebut maka terdapat penyakit pankreas atau kerusakan fungsi sekresi ginjal. Tetapi pada percobaan kali ini indeks diastasenya sebesar 258 sehingga kerja pankreas melebihi batas normal. Reaksi yang terjadi pada percobaan kali ini adalah:
Indeks diastasenya ditentukan dari perubahan warna yang terjadi pada tabung. Adanya perbedaan hasil kelompok kami dengan kelompok pembanding dapat dikarenakan human error bias pada saat penetesan iodium atau juga pada saat
pengambilan urin dari hasil pengenceran, karena pipet volume yang digunakan sama dari tabung 1 hingga tabung 12.
BAB V
PENUTUP
5.1 Kesimpulan
Dari praktikum yang telah dilakukan dapat disimpulkan bahwa:
1. Urine adalah cairan sisa yang diekskresikan oleh ginjal yang kemudian akan dikeluarkan dari dalam tubuh melalui proses urinasi. Urine disaring didalam ginjal, dibawa melalui ureter menuju kandung kemih, akhirnya dibuang keluar tubuh melalui uretra.
2. Urin yang kita keluarkan terdiri dari berbagai unsur seperti : air, protein, amoniak, glukosa, sedimen, bakteri, epitel ,dsb.
3. Kadar atau aktivitas enzim diastase normal yang terdapat dalam urin adalah 32 U/L, sedangkan dalam serum adalah 16 U/L.
5.2 Saran
Diharapkan selama melaksanakan praktikum untuk mengenakan peralatan praktikum di laboratorium secara lengkap seperti jas lab, sepatu lab, handscoon, masker dan menyediakan tissue.
DAFTAR PUSTAKA
Coronado MJ, Vargas C, Mellado E, Tegos G, Drainas C, Nieto JJ, Ventosa A. 2000. The -amylase gene amyH of the moderate halophile Halomonas meridiana: cloning and molecular characterization. Microbiology 146:861-868.
Fessenden, Ralph J dan Joan S. Fessenden. 1989. Kimia Organik edisi ketiga. Jakarta: Erlangga.
Ganong. 2003. Fisiologi Kedokteran. Yogyakarta: Gadjah Mada University Press Kobayashi T, Kamekura M, Kamlayakrit W, Onishi H. 1986. Production, purification, haracterization of an amylase of the moderate halophile Micrococcus
varians subsp. Halophilus. Microbiology 46:165-170.
Lehningger, Albert L. 1988. Dasar-dasar Biokimia. Jakarta: Erlangga.
Onishi H. 1972. Halophilic amylase from a moderately halophilic Micrococcus. J Bacteriol 109:570-574.
Onishi H, Hidaka O. 1978. Purification and properties of amylase produced by a moderately halophilic Acinetobacter sp. Can J Microbiol 24:1017- 1023.
Poedjiadi, Anna, dan F.M. Titin Supriyanti. 1994. Dasar-dasar Biokimia. Jakarta: UIPress.
Poedjiadi, Anna dkk. 2005. Dasar-dasar Biokimia. Jakarta: UIPress Soendoro. 1985. Prinsip-prinsip Biokimia. Surabaya: Erlangga
Suhtanry, rubianto, 1985. Kimia pangan.Badan Kerja Sama Perguruan Tinggi Indonesia Bagian Timur, Makassar.
Ventosa A, Nietto JJ. 1995. Biotechnology application and potentialities of halophilic microorganisms. W J Microbiol Biotechnol 11:85-94.
Hasil Pemeriksaan:
Tabung 1 (pengenceran: 1/1): bening Tabung 2 (pengenceran: 1/2): bening Tabung 3 (pengenceran: 1/4): bening Tabung 4 (pengenceran: 1/8): bening Tabung 5 (pengenceran: 1/16): bening Tabung 6 (pengenceran: 1/32): bening Tabung 7 (pengenceran: 1/64): ungu tua Tabung 8 (pengenceran: 1/128): ungu Tabung 9 (pengenceran: 1/256): ungu Tabung 10 (pengenceran: 1/512): biru Tabung 11 (pengenceran: 1/1024): biru Tabung 12 (pengenceran: 1/2048): biru
Perhitungan:
konsentrasi = 1 x 2 unit
(1/128)
LAPORAN PRAKTIKUM BIOKIMIA GIZI
“PENENTUAN KADAR DIASTASE URIN”
OLEH:
KELOMPOK B III
1. VISCA ANDINI (1613411036)
2. JIHAN CAHYANI (1613411037)
3. M. IRVAN PERDANA (1613411038)
4. ANNISA KURNIAWATI (1613411039)
POLTEKKES TANJUNG KARANG JURUSAN GIZI