BAB2
TINJAUAN PUSTAKA
2.1 Preeklampsia
Preeklampsia (PE) merupakan gangguan multisistem pada kehamilan
yang mempengaruhi keadaan ibu dan janin.Perubahan yang terjadi pada ibu
meliputi hipertensi dan proteinuria dengan onset setelah minggu ke-20 pada
kehamilan. Hal ini juga mempengaruhi kondisi janin sehingga janin berisiko
tinggi mengalami gangguan pertumbuhan intrauterin atau bahkan kematian
dalam kandungan (Wagner, 2004).
Insiden Preeklampsia di dunia sekitar 3% sampai 5% dari seluruh
kehamilandan diperkirakan menyebabkan 60 000 kematian ibusetiap tahun.
Dalam laporanterakhirdariDepartemen Kesehatan Iran, angka kematian ibu
diperkirakan menjadi 22,18 per 100 000 (Zibaeenezhad et al, 2010). Di Amerika
Serikat, 18% penyebab kematian ibu adalah preeklampsia (Savaj and Vaziri,
2012). Di Indonesia, kasus preeklampsia terjadi 5-10 % dari kehamilan dan masih
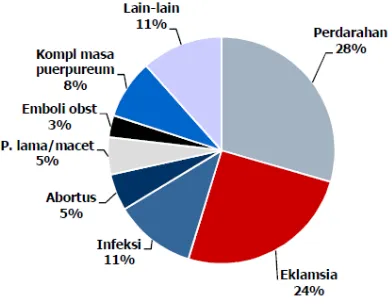
Gambar 2.1 Diagram Penyebab Kematian Ibu Hamil (Kemenkes RI, 2011)
Beberapa faktor risiko terjadinya preeklampsia pada kehamilan adalah
riwayat kehamilan, usia ibu terlalu muda (kurang dari 20 tahun ) atau terlalu tua
(lebih dari 35 tahun), riwayat keluarga, riwayat penyakit ibu dan obesitas.
Frekuensi preeklampsia pada primigravida lebih tinggi dibandingkan pada
multigravida, terutama primigravida pada usia muda (Uzan et al, 2011; Mikat et
al, 2012; Eiland et al, 2012; ACOG, 2002). Menurut rozhikan (2007), risiko
terjadi preeklampsia pada kehamilan pertama sebesar 3,9 % sedangkan pada
kehamilan kedua sebesar 1,7% dan kehamilan ketiga sebesar 1,8%.
Faktor risiko preeklampsia yang lain adalah obesitas. Wanita yang
memiliki indeks massa tubuh lebih dari 35 sebelum hamil memiliki risiko empat
kali lebih tinggi mengalami preeklampsia. Begitu juga dengan wanita yang
memiliki indeks massa tubuh kurang dari 20. Kehamilan kembar juga merupakan
faktor risiko terjadinya preeklampsia. Ibu hamil dengan penyakit penyerta
dengan ibu hamil tanpa penyakit penyerta (Matsubara, 2009). Beberapa penyakit
penyerta lainnya juga meningkatkan risiko terjadinya preeklampsia pada
kehamilan, seperti hipertensi, gangguan fungsi ginjal, kelainan hematologi,
penyakit imunodefisiensi seperti SLE. (Jido and Yakasai, 2013)
Tabel 2.1 Faktor Risiko terjadinya Preeklampsia (ACOG, 2002)
Berdasarkan onsetnya, preeklampsia dibagi dua yaitu early onset yaitu
preeklampsia yang terjadi sebelum usia kehamilan 34 minggu dan late onset, yaitu
preeklampsia yang terjadi setelah kehamilan 34 minggu (Grill, 2009).
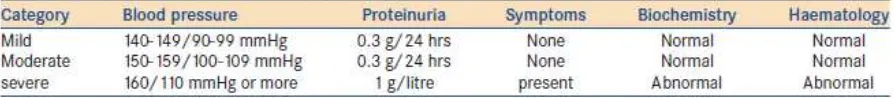
Berdasarkan gejala klinis, preeklamsia dapat dibedakan dalam bentuk
ringandan berat.Preeklamsiaringan didefinisikan oleh sistolikTekanan darah> 140
pengukuran terpisahdiambilsetidaknya6 jam terpisah.Preeklampsia berat
didiagnosis jika ada peningkatan tekanan darah sistolik > 160 mmHg atau tekanan
darah diastolik > 110 mmHg disertai dengan disfungi organ lainnya. Kriteria
spesifik yang disepakati dalam American Congress Obstetricians and
Gynecologists (ACOG)ditunjukkan pada tabel di bawah ini.
Tabel 2.2 Klasifikasi Preeklampsia (ACOG, 2002)
Sindrom HELLP merupakan varian tertentu dari preeklampsia berat.
HELLP adalahakronim untuk hemolisis, peningkatan hatienzim dan nilai
trombosit yang rendah.Kriteria dari sindrom HELLP diantaranya adalah anemia
mikroangiopati, nilai Aspartat Aminotransferase (AST) > 70, nilai
laktatdehidrogenase (LDH)> 600, atau nilai totalbilirubin>1.2,
dantrombosit<100.000(Sibai, 2004; Cunningham, 2002).
Beberapa kriteria untuk diagnosispreeklampsia berat digambarkan
munculnya berbagai gangguan fungsi organ. Peningkatan proteinuria dan oliguria
merupakan gambaran dari disfungsi ginjal. Sakit kepala dan perubahan fugsi
hati digambarkan dengan nilai ASTataualanine aminotransferase(ALT)yang
melebihi dua kali batas atas normal(ACOG, 2002).
Table 2.3 Kriteria Preeklampsia Berat (ACOG, 2002)
2.2 Patogenesis Preeklampsia
Saat ini telah terdapat kemajuan dalam pemahaman
kitatentangpatogenesispreeklampsia. Secara historis, preeklampsia
dikenalsebagai"the disease of theory", tetapi baru-baru ini
misteritentangpatogenesismolekulpreeklampsiamulaiteruraidenganditemukan
kunci tentangperubahan
faktorantiangiogenikplasenta. Molekuldasar sebagai faktor patogen
untukdisregulasiplasentainimasih belum diketahui, dan
trofoblasmulaidieksplorasi.Faktor antiangiogenik sepertisFLT-1dansoluble
endoglin(sEng)menyebabkan disfungsi endotelsistemik, sehingga akhirnya
muncullah manifestasi klinis sepertihipertensi, proteinuria, danmanifestasi
sistemiklainnya
daripreeklampsia (Gilbert et al, 2008; Karumanchi and Epstein, 2007; Noris,
2005; Robert and Ecsudero, 2012; Wang et al, 2009)
Keadaan Hipoksiajuga dianggap menjadiregulatorpenting. Selain
itu,aksis renin-aldosteron-angiotensinII, stresoksidatifyang
berlebihandanpuing-puing sinsitiotrofoblas, maladaptasikekebalan tubuh, dan faktor genetik
mungkinjugasemua memilikiperan dalampatogenesis
preeklampsia (Rolfo et al, 2013; Savaj and Vaziri, 2012; Uzan et al, 2012; Zhou
et al, 2011)
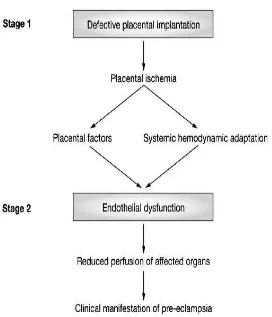
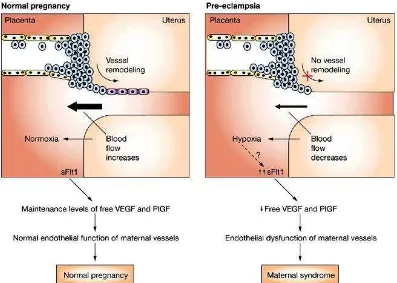
Patogenesis preeklampsia secaraumum terdiri dari dua tahapan proses.
Tahap yang pertama ditandai dengan perkembangan plasenta yang abnormal
selama trimester pertama yang mengakibatkan insufisiensi plasenta dan pelepasan
beberapa material plasenta ke dalam sirkulasi maternal. Tahap ini merupakan
tahapan asimptomatik. Tahapan selanjutnya merupakan tahapan simptomatik atau
tahap sindrom maternal yang ditandai dengan hipertensi, gangguan ginjal dan
proteinuria (Mutter and Karumanchi, 2008; Gilbert et al, 2008; Jido, 2013;
Pennington et al, 2012)
Suplai darah uterus difasilitasi oleh arteri uterina yang bercabang menjadi
arteri arkuata. Arteri arkuata segera terbagi ke arah anterior dan posterior yang
berjalan secara melingkar. Arteri arkuata berlanjut ke arteri radialis menuju ke
arah lumen uterus. Arteri ini memperdarahi lapisan basal endometrium dan
bagian arteriol spiralis memasok lapisan fungsional endometrium. Arteri spiralis
adalah arteri kecil yang memasok darah ke lapisan endometrium uterus (Harris,
2011; Kapiteijn, 2006)
Dalam keadaan tidak hamil dinding arteri spiralis dan arteri radialis
berisi jumlah darah yang cukup banyak. Dindingnya terdiri atas otot polos yang
dipersarafi oleh saraf otonom. Oleh karena itu, arteri spiralis sangat responsif
terhadap rangsangan adrenergik eksogen dan endogen yang akan menimbulkan
vasodilatasi ataupun vasokonstriksi (Kapiteijn, 2006)
Sel-sel trofoblas terus menginvasi jaringan desidua (trofoblas interstitial)
dan arteri spiralis (trofoblas endovaskular) maternal. Pada awalnya invasi sel-sel
trofoblas endovaskuler pada arteri spiralis menyebabkan arteri spiralis tersumbat,
sehingga plasenta mengalami hipoksia (Murphy et al, 2012; Rolfo et al, 2013).
Keadaan hipoksia ini merangsang se-sel trofoblas memproduksi dan
mensekresikan faktor-faktor proangiogenik, diantaranya adalah VEGF dan PLGF.
VEGF berikatan dengan reseptornya, yaitu KDR untuk merangsang peningkatan
permeabilitas kapiler vili, proliferai dan migrasi sel endotel kapiler vili. Selain
itu VEGF berikatan dengan reseptor FLT-1, yang mengatur laju proliferasi sel
endotel dan mengorganisasikan pembentukan cabang-cabang kapiler vili baru
selama trimester pertama kehamilan dan sampai akhir trimester pertama terbentuk
tangkai vili dan cabang-cabang vilinya.
Setelah minggu ke-12 sumbatan trofoblas endovaskuler pada arteri
spiralis mulai terbuka. Invasi sl-sel trofoblas endovaskuler ke dalam arteri spiralis
terus berlanjut, pada akhir trimester kedua invasi sel-sel tersebut mencapai
sepertiga bagian arteri radialis miometrium. Sel-sel trofoblas endovaskuler
menyerupai dan menggantikan sel-sel endotel spiralis maternal.
Selamainvasiendovaskular, endoteliumdansel-selotot polos pembuluh darahakan
diganti dengantrofoblas (Harris, 2011; Andraweera et al, 2012).
Remodelingarterispiralinimenghasilkan pembuluh darah dengan diameter lebih
besar dan lebar sehingg mampumemasokcukupdarah maternalke plasentauntuk
mengakomodasipeningkatan kebutuhan janin(Knofler, 2012; Uzan et al, 2011).
Selainremodeling arteri spiralis yang dimediasi oleh trofoblas, perubahan
halus dalamstrukturarterispiraldiamatidi awalkehamilan padadesidua(Harris,
2011).Pada saat ini dikaitkandenganmasuknyaleukositke
dalamdesiduauterustermasuksel Natural Killer(NK) seldan makrofag.
SelNKrahimyang terisolasi daridesidua pada saat trimesterpertama,
mensekresikanbanyak faktorpertumbuhan angiogeniktermasukVEGF-A, VEGF-
C, danPLGF (Neufeld et al, 1999; Knofler, 2012; Levine, 2006; Noris et al,
2005).Mekanisme molekuler yangmengontrolremodelingarterispiralmasih
belumjelas, tetapi diketahuibahwaselamainvasi, sitotrofoblaskehilangan
kemampuan mereka untukmembagi danbahwasel-selyanginterdigitateantara
sel-selendotelibukehilangankarakteristikepitelmereka
danmemperolehfenotipendoteldalamtransisiproses yang
disebutpseudovaskulogenesis. Dalam hal Ini termasukjuga
perubahanekspresipadamolekul(Andraweera et al, 2012).
Selamadiferensiasi, sitotrofoblasmengurangi regulasimolekul
adhesidiantaranyaintegrina6b4, a5b6dancadherinepitel danmeningkatkan regulasi
molekul adhesi yangdiekspresikan padasel-selendoteltermasukintegrinavb3,
A1B1, pembuluh darahcadherinendotel, Vascular Cel adhesion Molekul-1
(VCAM-1)danadhesi selendoteltrombosit (Robert and Hubel, 2008; Pennington et
al, 2012; Noris, 2005; Harris, 2011).
Arteri spiralis mengalami remodeling menjadi arteri yang kehilangan otot
maka aliran darah uteropalsenta meningkat dan suasana plasenta menjadi
normoksia. Pada keadaan ini sekresi VEGF sebagai proangiogenik menurun,
sedangkan PLGF meningkat. Ikatan PLGF dengan reseptornya yaitu FLT-1
diketahui dapat meningkatkan efek yang diperantarai oleh ikatan VEGF dengan
reseptor KDR. Ikatan ini akan menginduksi proliferasi dan migrasi sel endotel,
juga menginduksi pemanjangan cabang-cabang kapiler vili sebelumnya disertai
pematangan vili. Vili-vili menajdi tipis dengan ujung yang berdilatasi menjadi
vili intermedier matur dan vili terminal. Proses ini berlangsug dari trimester
kedua sampai masa aterm (Eiland et al, 2012; Harris, 2011)
Perubahan fisiologis arteri spiralis ibu adalah kunci keberhasilan
kehamilan. Pada kehamilan, dinding otot pembuluh darah arteri spiralis
mengalami penghilangan sebagian otot polos dan lamina elastis hingga mencapai
kedalaman sepertiga lapisan miometrium sehingga diameter pembuluh darah
arteri spiralis menjadi berdilatasi, 5-10 kali lipat dari ukuran sebelumnya.
Kegagalan perubahan fisiologis ini akan menimbulkan beberapa komplikasi
dalam kehamilan. (Cunningham et al.,2008; Harris, 2011; Noris, 2005; Mutter,
2008; Romero and chaiworapongsa, 2013)
2.2.2 Plasentasi Abnormal
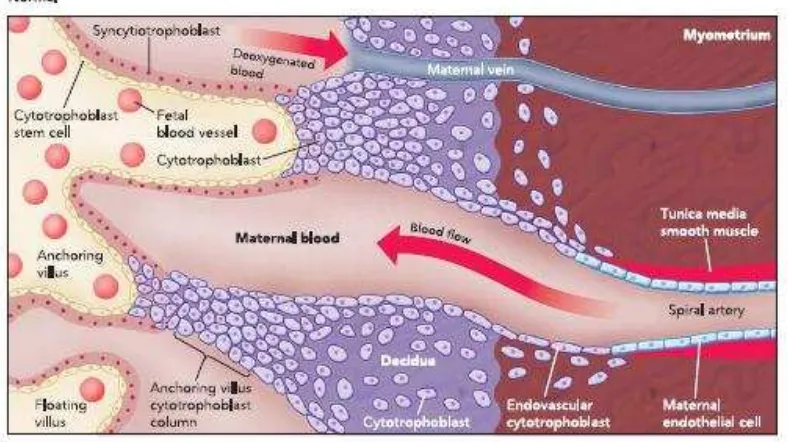
Pada implantasi normal, arteri spiralis mengalami remodeling ekstensif
karena diinvasi oleh trofoblas endovaskuler (Andraweera et al, 2012; Noris
2005;Savaj and Vajiri, 2012). Sel-sel ini menggantikan lapisan otot dan endotel
spiralis mengalami transformasi dari pembuluh darah kecil dengan resistensi yang
tinggi menjadi pembuluh darah dengan kapasitas kapiler yang tinggi sehingga
mampu memenuhi perfusi plasenta yang adekuat untuk pertumbuhan janin.
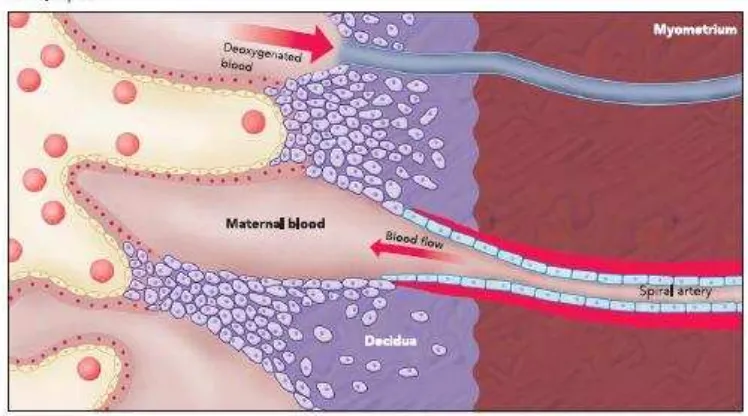
Pada preeklampsia, transformasi ini berjalan tidak sempurna. Diduga
invasi sitotrofoblas ke dalam arteri spiralis hanya terbatas pada desidua
superfisialis dan hanya melibatkan sedikit segmen pada area miometrium. Selama
proses invasi, vaskular sitotrofoblas berubah dari fenotip epitel menjadi fenotip
endotel (pseudovaskulogenesis/vascular mimicry). Pada preeklampsia,
sitotrofoblas gagal melakukan invasi tersebut dan selanjutnya menyebabkan
diameter pembuluh darah menjadi kecil dan pembuluh darah menjadi resisten
(Mutter and Karumanchi, 2008; Matsubara et al, 2009; Sibai, 2005; )
Gambar 2.3 Arteri Spiralis pada Kehamilan dengan Preeklampsia
Kegagalan perubahan arteri spiralis inimenyebabkan plasentasi yang
abnormal dan iskemia plasenta. Hal ini menimbulkan keadaan hipoksia (stress
oksidatif. Hipoksia plasenta menyebabkan pelepasan berbagai faktor terlarut dari
plasenta. Plasenta yang mengalami stres oksidatif menghasilkan protein
anti-angiogenik yaitu SFLT-1, prostaglandin dan sitokin seperti NK- cell, TNF- α, IL-1,
IL-2, IL-6, IL-8 ke dalam sirkulasi ibu (Gilbert et al, 2007; Andraweera et al,
2012; Murphy et al, 2012; ).
Sementara, keadaan hipoksia plasenta sendiri menyebabkan pengurangan
produksi faktor proangiogenik termasuk faktor pertumbuhan plasenta (PLGF) dan
faktor pertumbuhan endotel vaskular (VEGF). Keadaan ini mempengaruhi fungsi
endotel (Mutter and Karumanchi, 2008; Shibuya, 2013).
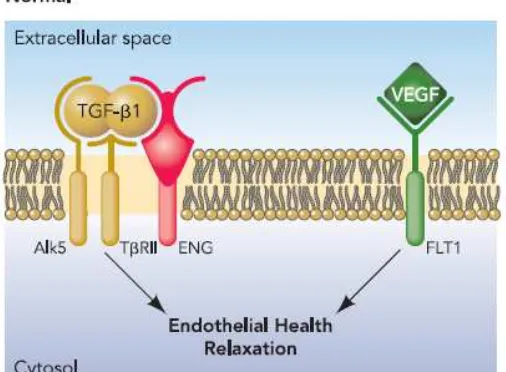
Target organ pertama yang dipengaruhi adalah endotel maternal.
Perubahan ini menyebabkan disfungsi endotel dan aktivasi respon inflamasi
sitemik. Substansi vasoaktif yang dikeluarkan endotel antara lain nitric oxide
(NO), bradikinin, asetilkolin, endothelial-derived relaxing factor (EDRF),
Gambar 2.4 Diagram Mekanisme Patofisiologi Preeklampsia (Sumber: Norris, 2005)
Respon inflamasi sistemik yang terjadi akibat disfungsi endotel
mempengaruhi banyak fungsi organ, diantaranya peningkatan resistensi pembuluh
darah sistemik, yang akhirnya terjadi vasokonstriksi, aktivasi kaskade koagulasi
sampai akhirnya menimbulkan manifestasi klinis seperti hipertensi, proteinuria,
gangguan fungsi hati, gangguan hematologi, gangguan sistem saraf dan gangguan
2.3 Faktor Angiogenik dan Anti Angiogenik pada Preeklampsia
Pada preeklampsia terjadi ketidakseimbangan faktor proangiogenik dan
antiangiogenik. Barton (2008) menyatakan adanya faktor-faktor proangiogenik
dan antiangiogenik yang beredar dalam sirkulasi pada saat sebelum onset
preeklampsia.
Angiogenesis adalah pembentukan pembuluh darah kapiler baru dari
pembuluh darah yangsudah ada sebelumnya. Proses ini melibatkan interaksi
kompleks antara berbgai olekul seperti faktor-faktor proangiogenik dan
reseptornya (Kapitejn, 2006; Knofler, 2012).
Tahapan angiogenesis diawali dengan respon jaringan. Jaringan yang
rusak memproduksi dan melepaskan faktor pertumbuhan (GF) yang berdifusi ke
jaringan sekitarnya. Faktor pertumbuhan angiogenik akan berikatan dengan
reseptor spesifik yang terdapat pada sel endotel pembuluh darah terdekat. Setelah
itu sel endotel menjadi aktif, memberikan sinyal pertumbuhan. Sel-sel endotel
mulai membentuk molekul-molekul baru, termasuk juga mengaktifkan enzim.
Enzim akan melarutkan protein dan membentuk lubang-lubang kecil pada
membran basal. Melalui lubang-lubang yang dibentuk, sel endotel mulai
berproliferasi dan bermigrasi menuju jaringan yang rusak. Dalam proses ini juga
diperlukan molekul adhesi atau integrin yang akan berfungsi sebagai kait sehingga
pembuluh darah yang baru dibentuk dapat bergerak maju. Enzim lainnya seperti
matriks metaloproteinase (MMP) juga diperlukan untuk menghancurkan jaringan
di depan ujung mbuluh darah baru yang sedang tumbuh. Sel-sel endotel yang
darah berhubungan satu dengan yang lain supaya darah dapat mengalir.
Selanjutnya dengan bantuan sel-sel otot, pembuluh darah yang baru akan
mengalami stabilisasi (Kapitejn, 2006; Knofler and Pollheimer, 2012)
Proses angiogenesis pada kehamilan berperan untuk memastikan suplai
oksigen dan nutrisi sampai ke janin. Angiogenesis melibatkan berbagai macam
faktor proangiogenik dan antiangiogenik yang bekerja sama dalam plasenta.
Faktor proangiogenik yang berperan diantaranya adalah VEGF, PLGF dan Tissue
Growth Factor β-1 (TGF β-1)
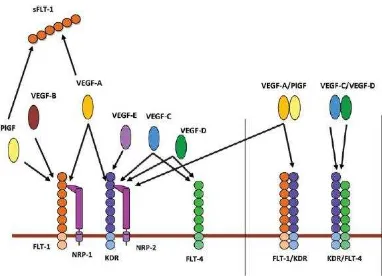
Gambar 2.5 Family VEGF beserta Reseptornya ( Andraweera, 2012)
Pada preeklampsia terdapat dua protein antiangiogenik yang diproduksi
secara berlebihan diantaranya adalah sFLT-1 dan sEng. SFLT-1 merupakan
menghambat penandaan Transforming Growth Factor β-1 (TGF β-1) di dalam
sirkulasi.
Pada Plasenta wanita dengan preeklampsia ditemukan peningkatan
produksi protein sFLT-1. Hal ini memberikan kontribusi pada preeklampsia
(Levine et al, 2006; Jacobs, 2011; Karumanchi, 2007).
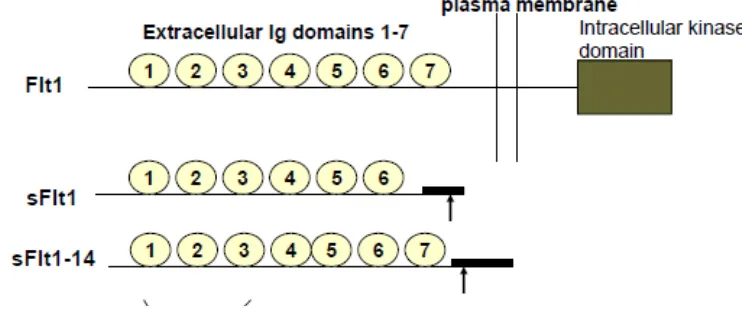
2.3.1 Soluble Fms Like Tyrosine Kinase -1
SFLT-1 juga dikenal dengan soluble vascular endothelial growth factor
reseptor -1 (sVEGFR-1), merupakan variasi bentuk dari reseptor FLT-1. Reseptor
Flt-1 mengikat VEGF-A, VEGF-B dan PLGF dengan kuat dan diekspresikan pada
banyak jaringan, termasuk monosit / makrofag dan trofoblas plasenta. Gen Flt-1
berlokasi di kromosom ke-13. Hasil alternative splicing dari pre-mRNA yang
mengkode Flt-1adalah bentuk Flt-1yang kehilangan domain sitoplasmik dan
transmembran tetapi masih memiliki domain ligand-binding yaitu bentuk soluble
dari Flt-1. Bentuk soluble ini disebut sFLT-1, disekresikan oleh sel endotel,
monosit dan plasenta (Shibuya, 2006; Neufeld et al, 1999).
Protein sFLT-1ini merupakan suatu faktor anti angiogenik yang bekerja
sebagai antagonis VEGF-A dan PLGF, menghambat ikatannya dengan reseptor di
permukaan sel. Hal ini mengakibatkan fungsi PLGF dan VEGF sebagai faktor
proangiogenik terhambat, dan pertumbuhan pembuluh darah tidak terjadi (Rolfo et
al, 2013; Romero and Chaiworapongsa, 2013).
Banyak penelitian yang menyatakan bahwa peningkatan ekspresi dan
sekresi sFLT-1 pada sirkulasi maternal memiliki kontribusi terhadap patogenesis
preeklampsia. Penelitian yang dilakukan oleh Boyd et al (1987) menyatakan
bahwa adanya peningkatan insiden preeklampsia pada ibu hamil dengan janin
trisomi 13. Hal ini dikaitkan dengan lokasi gen Flt-1 di kromosom ke-13.
Dengan adanya trisomi kromosom ke-13, maka terjadi peningkatan ekspresi gen
sFLT-1 sehingga sFLT-1 dalam sirkulasi ibu meningkat. peningkatan sFLT-1
pada serum ibu hamil berhubungan dengan disfungsi endotel yang terjadi pada
preeklampsia, yang ditandai dengan timbulnya manifestasi klinis (Maynard et al,
2003; Levine, 2006).Menurut Levine et al (2006), sFLT-1 dalam serum ibu hamil
dengan preeklampsia tinggit pada usia kehamilan 20 minggu dan meningkat
secara signifkan dalam 5 minggu sebelum timbul hipertensi dan preeklampsia.
Mekanisme molekuler yang berperan dalam peningkatan sFLT-1 plasenta
pada preeklampsia dan perannya dalam plasentasi belum jelas diketahui. Banyak
faktor yang dikaitkan dengan mekanisme molekuler pelepasan sFLT-1 pada
preeklampsia. Saat ini dipercaya bahwa keadaan hipoksia merupakan salah satu
penyebab mayor lepasnya sFLT-1 (Gu et al, 2008; ). Namun Redman dan Sargent
adanya stres oksidatif dibandingkan dengan hipoksia. Mereka menyatakan bahwa
stimulus inflamasi yang menyebabkan lepasnya sFLT-1 ke dalam sirkulasi
maternal memiliki efek yang lebih besar dibandingkan dengan keadaan hipoksia.
2.3.2 Placental Growth Factor
Faktor pertumbuhan plasenta (PLGF) adalah anggota dari faktor
pertumbuhan endotel vaskular (VEGF), yaitu sebuah molekul yang terlibat dalam
proses angiogenesis dan vaskulogenesis, khususnya selama embriogenesis.
(Levine, 2004; Karumanchi, Maynard, Stillman, 2005)
PLGF berada pada kromosom manusia ke -14 dan terdiri dari tujuh
ekson. Alternatif mRNA splicing dari PLGF menghasilkan empat bentuk isoform,
diantaranya PLGF-1 (PLGF131), PLGF-2 (PLGF152), PLGF-3 (PLGF203) dan
PLGF-4 (PLGF224) (Maglione et al., 1993) yang berbeda dalam ukuran, sifat
dan sekresi serta afinitas ikatannya (Ribatti, 2008). Namun PLGF-1 dan PLGF-2
diyakini merupakan isoform utama. PLGF-1 dan PLGF-2 masing-masing terdiri
dari 131 dan 152 residu asam amino. PLGF homodimers mengikat FLT-1 dan
Beberapa mekanisme yang dilakukan PLGF dalam proses angiogenesis adalah
dengan merangsang sel-sel endotel melalui ikatannya dengan reseptor FLT 1,
berkompetisi denganVEGF-A untuk berikatan dengan FLT-1, sehingga
memungkinkan VEGF-A berperan untuk mengaktifkan KDR, merekrut monosit /
makrofag yang berperan dalam pertumbuhan pembuluh darah (Ribatti, 2008) dan
menginduksi sekresi VEGF-A dari monosit.
Dilaporkan bahwa peningkatan PLGF dalam sirkulasi maternal terjadi
dari awal kehamilan sampai kepada akhir trimester dua kehamilan selanjutnya
mulai dari minggu ke-30 sampai kepada persalinan, PLGF akan mengalami
penurunan. Penurunan yang terjadi pada ibu hamil dengan preeklampsia
ditemukan lebih banyak dibandingkan pada ibu hamil normal (Schmidtet al, 2009;
Lim et al, 2008; Mcelrath et al, 2012).
Selama kehamilan normal, ada peningkatan PLGF yang stabil dalam
serum pada dua trimester pertama, puncaknya pada 29-32 minggu dan akan
mengalami penurunan sesudahnya (Levine et al, 2004). Pada wanita yang
kemudian mengalami pre-eklampsia, konsentrasi PLGF serum tidak mengalami
peningkatan bila dibandingkan pada usia 10-13 minggu kehamilan (Levine et al,
2004) dan mengalami penurunan yang cukup besar 5 minggu sebelum munculnya
Gambar 2.8 Proses Mekanisme Disfungsi Endotel pada Preeklampsia (Norris, 2005)
Serum PLGF pada 21-32 minggu kehamilan diketahui lebih rendah pada
kasus pre-eklampsia jenis early onset (sebelum 34 minggu) dibandingkan dengan
jenis late onset. Begitu juga dengan kasus penyakit berat dibandingkan dengan
penyakit ringan dan kasus preeklampsia yang disertai dengan bayi kecil untuk
masa kehamilan dibandingkan dengan ukuran yang sesuai untuk bayi usia
kehamilan (Levine et al., 2004).
Pada pemeriksaan PLGF urin, hasilnya menunjukkan nilai yang paralel
dengan pemeriksaan pada serum dengan kenaikan dua trimester pertama,
Tetapi bagaimana pun juga perkembangan preeklampsia tidak didahului dengan
perubahan pada nilai PLGF urin (Savvidouet al., 2009)
2.4 SFLT,PLGF dan Preeklampsia
Keseimbangan antara faktor angiogenik dan faktor antiangiogenik dinilai
memegang peranan penting dalam regulasi vaskulogenesis plasenta. Adanya
ketidakseimbangan antara VEGF, PLGF sebagai faktor angiogenik poten dalam
perkembangan plasenta dengan sFLT-1 sebagai antiangiogenik yang beredar
dalam sirkulasi maternal ditunjukkan pada sirkulasi ibu hamil dengan
preeklampsia. PLGF serum ibu dikenal sebagai kebalikan dari sFLT-1; semakin
tinggi-sFLT-1, semakin rendah PLGF.Didapati adanya peningkatan sFLT-1 dalam
serum maternal yang diikuti dengan penurunan kadar VEGF dan PLGF bebas
Gambar 2.9: Gambar Ikatan sFLT-1 dengan PLGF pada Kehamilan Eklampsia (Hagmannet al, 2012)
Ketidakseimbangan faktor angiogenik dengan anti angiogenik yang
terjadi memiliki hubungan dengan manifestasi klinik yang timbul pada
preeklampsia. Levine (2004) menyatakan bahwa peningkatan sFLT-1 dan
penurunan PLGFberhubungan dengan perkembangan preeklampsia. Ohkuchi et
al (2010) melakukan pemeriksaan kadar sFLT-1 dan PLGF dalam plasma wanita
jepang yang hamil dengan preeklampsia. Didapati bahwa nilai ratiosFLT-1
dengan PLGFdapat digunakan untuk menggambarkan perjalanan penyakit pada
nilai kadar sFLT-1, PLGF serta ratio sFLT-1/PLGF dianggap dapat digunakan
sebagai prediktor pada kasus preeklampsia dan kasus hipertensi kronis yang akan
berkembang menjadi preeklampsia (Verlohren, 2010). Dalam penelitian yang
dilakukan oleh Kim et al (2007), preeklampsia memiliki hubungan yang kuat
dengan peningkatan sFLT-1 dan penurunan PLGF dalam plasma ibu hamil
trimester dua, bahkan ratio sFLT-1/PLGF dapat digunakan sebagai prediktor
preeklampsia.
Disfungsi Endotel
Kegagalan invasi trofoblas ke dalam arteri spiralis maternal
2.6 Kerangka Konsep
PLGF
sFlt-1
PREEKLAMPSIA BERAT/ EKLAMPSIA