i
SINTESIS SENYAWA
2,2´-(1,4 FENILENA bis (METANILILIDENA)) DISIKLOHEKSANADION DARI 1,3 SIKLOHEKSANADION DAN TEREPHTHALALDEHID
DENGAN KATALIS NATRIUM HIDROKSIDA
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Farmasi
Oleh : Petrus Wicaksono
NIM: 078114136
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
ii
SINTESIS SENYAWA
2,2´-(1,4 FENILENA bis (METANILILIDENA)) DISIKLOHEKSANADION DARI 1,3 SIKLOHEKSANADION DAN TEREPHTHALALDEHID
DENGAN KATALIS NATRIUM HIDROKSIDA
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Farmasi
Oleh : Petrus Wicaksono
NIM: 078114136
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
v
HALAMAN PERSEMBAHAN
Kebanggaan terbesar bukanlah tidak pernah
mengalami kegagalan,
tetapi bangkit kembali setiap kali jatuh
(Confusius)
vi
LEMBAR PERNYATAAN PERSETUJUAN PUBLIKASI KARYA ILMIAII
UNTUK KEPENTINGAN AKADEMIS
Yang bertanda tangan di bawah ini, saya mahasiswa Universitas Sanata Dharma: Nama : Petrus Wicaksono
Nomor Mahasiswa : 07 8114 136
Demi perkembangan ilmu pengetahuan, saya memberikan kepada Perpustakaan Universitas Sanata Dharma karya ilmiah saya yang berjudul:
SINTESIS SENYAWA 2,2´-(1,4 FENILENA bis (METANILILIDENA)) DISIKLOHEKSANADION DARI 1,3 SIKLOHEKSANADION DAN TEREPHTHALALDEHID DENGAN KATALIS NATRIUM HIDROKSIDA
beserta perangkat yang diperlukan (bila ada). Dengan demikian saya memberikan kepada Perpustakaan Universitas Sanata Dharma hak untuk menyimpan, mengalihkan dalam bentuk media lain, mengelolanya dalam bentuk pangkalan data, mendistribusikan secara terbatas, dan mempublikasikannya di internet atau media lain untuk kepentingan akademis tarpa perlu meminta ijin dari saya ataupun memberi royalti kepada saya selamatetap mencantumkan nama saya sebagai penulis.
Demikian pernyataan ini yang saya buat dengan sebenamya. Dibuat di Yogyakarta
Pada tanggal: 8 Februari 2011 Yang menyatakan
vii
PRAKATA
Puji dan syukur kepada Tuhan Yesus Kristus atas segala berkat, kasih, karunia, rahmat dan penyertaan-Nya sehingga penulis dapat menyelesaikan skripsi yang berjudul “Sintesis Senyawa 2,2´-(1,4 Fenilena bis (Metanililidena)) Disikloheksanadion dari 1,3 Sikloheksanadion dan Terephtalaldehid dengan Katalis Natrium Hidroksida” dengan baik. Skripsi ini disusun untuk memenuhi salah satu syarat dalam memperoleh gelar Sarjana Strata Satu Program Studi Farmasi di Fakultas Farmasi Universitas Sanata Dharma.
Dalam menyelesaikan penelitian dan penyusunan skripsi ini tidak lepas dari dukungan dan bantuan berbagai pihak. Oleh karena itu, pada kesempatan ini penulis ingin mengucapkan terima kasih secara khusus kepada:
1. Ipang Djunarko, M. Sc., Apt. selaku Dekan Fakultas Farmasi Universitas Sanata Dharma Yogyakarta
2. Jeffry Julianus, M.Si. selaku dosen pembimbing yang telah bersedia memberikan pengarahan dan bimbingan selama penelitian hingga terselesaikannya penyusunan skripsi ini
3. Dra. M. M. Yetty Tjandrawati, M. Si. dan Prof. Dr. Sri Noegrohati, Apt. selaku dosen penguji atas ketersediaannya meluangkan waktu dan memberikan berbagai masukan, kritik dan saran.
4. Dr. Pudjono, S.U. Apt. atas saran dan bantuan yang telah diberikan
viii
6. Bapak dan Ibu dosen Fakultas Farmasi Universitas Sanata Dharma yang telah memberi ilmu dan pengalaman yang membantu dalam penyelesaian skripsi ini.
7. Rini Dwiastuti, M. Sc., Apt. selaku kepala laboratorium farmasi, terima kasih atas ijin yang diberikan untuk melakukan penelitian.
8. Pak Parlan, Pak Kunto, Mas Bimo, Pak Wagiran dan yang telah membantu selama penelitian.
9. Teman-teman satu payung sintesis senyawa antiangiogenesis: Fandri, Ardi, dan Anin atas bantuan, kebersamaan, dan dukungannya selama penelitian.
10.Teman-teman skripsi lantai 4 yang memberikan semangat dan dukungan selama penelitian.
11.Teman-teman angkatan 2007 yang telah berbagi kebersamaan dan keceriaan selama ini.
12.Semua pihak yang telah membantu selama penyelesaian skripsi ini yang tidak dapat disebutkan satu per satu
Penulis menyadari sepenuhnya bahwa skripsi ini masih jauh dari sempurna. Oleh karena itu, penulis dengan senang hati menerima segala kritik dan saran yang membangun demi kesempurnaan skripsi ini. Semoga skripsi ini dapat memberikan manfaat bagi pembaca dan bagi perkembangan ilmu pengetahuan.
ix
PERNYATAAN KEASLIAN KARYA
Saya menyatakan dengan sesungguhnya bahwa skripsi yang saya tulis ini tidak memuat karya atau bagian karya orang lain, kecuali yang telah disebutkan dalam kutipan dan daftar pustaka, sebagaimana layaknya karya ilmiah.
Apabila di kemudian hari ditemukan indikasi plagiarisme dalam naskah ini, saya bersedia menanggung segala sanksi sesuai peraturan perundang-undangan yang berlaku
Yogyakarta, 15 Januari 2011 Penulis
x
INTISARI
Pengobatan kanker dapat dilakukan dengan menggunakan senyawa inhibitor angiogenesis. Kurkumin berpotensi sebagai senyawa anti angiogenesis
karena memiliki dua gugus α,β-unsaturated keton. Namun tauromerisasi kurkumin menyebabkan penurunan aktivitasnya. Senyawa 2,2´-(1,4 fenilena bis
(metanililidena)) disikloheksanadion memiliki dua gugus α,β-unsaturated keton sehingga diharapkan lebih poten dibandingkan kurkumin.
Penelitian ini merupakan penelitian eksperimental deskriptif non-analitik. Sintesis 2,2´-(1,4 fenilena bis (metanililidena)) disikloheksanadion dilakukan dengan mereaksikan 7,46 mmol 1,3 sikloheksanadion dan 0,5 mmol terephthalaldehid berdasarkan reaksi kondensasi aldol silang menggunakan katalis natrium hidroksida. Sintesis dianalisis dengan uji organoleptis, uji kelarutan, kromatografi lapis tipis (KLT), uji titik lebur, kromatografi gas (GC) serta dilakukan elusidasi struktur dengan spektrometri massa (MS) dan spektrofotometri infra merah (IR).
Senyawa hasil sintesis berupa serbuk putih berbau khas dengan crude product sebesar 0,474 gram, 0,682 gram, dan 0,785 gram. Hasil uji kelarutan menunjukkan senyawa hasil sintesis larut dalam dimetil sulfoksida dan piridin, agak sukar larut dalam aseton, sukar larut dalam etanol dan kloroform, dan tidak larut dalam air. Hasil uji KLT menunjukkan senyawa hasil sintesis memiliki bercak tunggal. Titik lebur senyawa hasil sintesis 218-220°C. Elusidasi struktur menggunakan GC-MS dan spektrofotometri IR menunjukkan senyawa hasil sintesis adalah 2,2´-(1,4 fenilena bis (metanililidena)) disikloheksanadion.
Kata kunci: inhibitor angiogenesis, kondensasi aldol silang, 2,2´-(1,4 fenilena bis
xi ABSTRACT
Cancer treatment can be performed using angiogenesis inhibitor compound. Curcumin has potent anti angiogenesis activity because it has two
clusters α, β-unsaturated ketone. But curcumin’s tauromerism lowering its
activity. Therefore the 2,2'- (1,4 phenylene bis (metanililidene)) dicyclohexanedione which have two clusters α, β-unsaturated ketone expected to have more potent angiogenesis inhibitor than curcumin.
This study is a descriptive non-experimental non-analytic. Synthesis of 2,2'- (1,4 phenylene bis (metanililidene)) dicyclohexanedione carried out by reacting 7.46 mmol of 1,3 cyclohexanedione and 0.5 mmol of terephthalaldehyde based cross aldol condensation reaction with sodium hidroxyde catalyst. The synthesis was analyzed by organoleptic test, solubility test, thin layer chromatography (TLC), melting point test, gas chromatography (GC) and performed structure elucidation with mass spectrometry (MS) and infrared (IR).
The obtained synthesized compounds is a white powder with distinctive smell with crude product amounts 0,474 gram, 0,682 gram, and 0,785 gram. Solubility of synthesized compound is soluble in dimethyl sulfoxide and pyridine, slightly soluble in acetone, difficult soluble in ethanol and chloroform, and insoluble in water. In TLC test synthesized compound has a single spot. Compound melting point is 218-220°C. The structure elucidation using GC-MS and IR spectrometry indicated synthesized compound is 2,2'- (1,4 phenylene bis (metanililidene)) dicyclohexanedione.
xii
DAFTAR ISI
Halaman
HALAMAN JUDUL ii
HALAMAN PERSETUJUAN PEMBIMBING iii
HALAMAN PENGESAHAN iv
HALAMAN PERSEMBAHAN v
PERNYATAAN PERSETUJUAN PUBLIKASI vi
PRAKATA vii
PERNYATAAN KEASLIAN KARYA ix
INTISARI x
ABSTRAK xi
DAFTAR ISI xii
DAFTAR GAMBAR xv
DAFTAR TABEL xvii
DAFTAR LAMPIRAN xviii
BAB I PENDAHULUAN 1
A. Latar Belakang 1
1. Permasalahan 3
2. Keaslian Penelitian 4
3. Manfaat Penelitian 4
B. Tujuan Penelitian 4
BAB II PENELAAHAN PUSTAKA 5
A. Kurkumin 5
xiii
C. Uji Pendahuluan 9
1. Uji Organoleptis 10
2. Uji Kelarutan 10
3. Uji Titik Lebur 10
4. Uji Kemurnian Menggunakan Kromatografi Lapis Tipis (KLT) 11
5. Kromatografi Gas 12
D. Elusidasi Struktur Senyawa Hasil Sintesis 13
1. Spektroskopi Massa 13
2. Spektrofotometri Inframerah 13
E. Landasan Teori 14
F. Hipotesis 14
BAB III METODE PENELITIAN 15
A. Jenis dan Rancangan Penelitian 15
B. Definisi Operasional 15
C. Bahan Penelitian 15
D. Alat Penelitian 16
E. Tata Cara Penelitian 26
1. Sintesis 2,2´-(1,4 fenilena bis(metanililidena)) disikloheksanadion
dengan katalis NaOH 1,0 N 16
2. Uji Pendahuluan 16
a. Organoleptis 16
b. Uji Kelarutan Senyawa Hasil Sintesis 17
xiv
d. Uji Kemurnian Menggunakan Kromatografi Lapis Tipis (KLT)17
e. Kromatografi Gas 18
3. Elusidasi Struktur Senyawa Hasisl Sintesis 18
a. Spektroskopi Massa 18
b. Spektrofotometri Inframerah 19
F. Analisis Hasil 19
1. Rendemen 19
2. Analisis Pendahuluan 19
3. Elusidasi Struktur 19
BAB IV HASIL DAN PEMBAHASAN 20
G. Sintesis 2,2´-(1,4 fenilena bis(metanililidena)) disikloheksanadion
dengan katalis NaOH 1,0 N 20
H. Analisis Senyawa Hasil Sintesis 25
1. Organoleptis 25
2. Uji Kelarutan Senyawa Hasil Sintesis 26
3. Uji Titik Lebur 27
4. Uji Kemurnian Menggunakan Kromatografi Lapis Tipis (KLT) 28 5. Kromatografi Gas-Spektroskopi Massa (GC-MS) 32
6. Spektrofotometri Inframerah 36
BAB V KESIMPULAN DAN SARAN 40
DAFTAR PUSTAKA 41
LAMPIRAN 44
xv
DAFTAR GAMBAR
Halaman
Gambar 1. Struktur kurkumin 6
Gambar 2. Tautomerisasi kurkumin 6
Gambar 3. Resonansi ion enolat 7
Gambar 4. Reaksi aldol silang 7
Gambar 5. Struktur sikloheksanadion 8
Gambar 6. Struktur terephthalaldehid 9
Gambar 7. Hidrogen alfa pada 1,3 dikloheksanadion 21
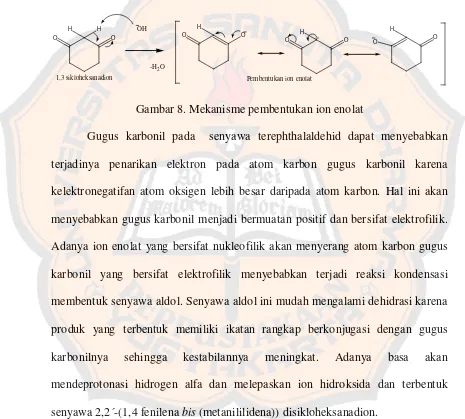
Gambar 8. Mekanisme pembentukan ion enolat 22
Gambar 9. Mekanisme sintesis 2,2´-(1,4 fenilena bis (metanililidena))
disikloheksanadion 23
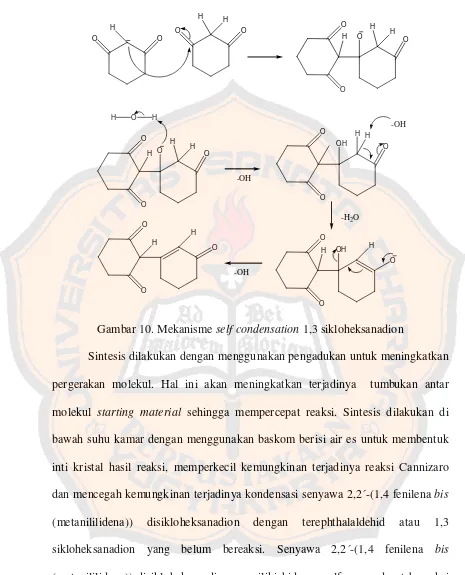
Gambar 10. Mekanisme self condensation 1,3 sikloheksanadion 24 Gambar 11. Hidrogen alfa senyawa 2,2´-(1,4 fenilena bis (metanililidena))
disikloheksanadion 25
Gambar 12. Senyawa hasil sintesis 26
Gambar 13. Interaksi hidrogen senyawa 2,2´-(1,4 fenilena bis
(metanililidena)) disikloheksanadion 30 Gambar 14. Kromatogram hasil elusi senyawa hasil sintesis, 1,3
xvi
Gambar 17. Usulan mekanisme fragmentasi senyawa 2,2´-(1,4 fenilena bis
(metanililidena)) disikloheksanadion 35 Gambar 18. Spektra massa peak 1 senyawa hasil sintesis 35 Gambar 19. Struktur senyawa 2-(4-(dietoksimetil) benzilidena)
-1,3-sikloheksanadion 36
xvii
DAFTAR TABEL
Halaman
Tabel I. Data Uji Organoleptis Senyawa Hasil Sintesis dan Starting
Material 27
Tabel II. Data uji kelarutan senyawa hasil sintesis, 1,3 sikloheksanadion,
dan terephthalaldehid 27
Tabel III. Data uji titik lebur senyawa hasil sintesis, 1,3 sikloheksanadion,
dan terephthalaldehid 28
xviii
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Perhitungan Rendemen Senyawa Hasil Sintesis 44
Lampiran 2. Foto Senyawa Hasil Sintesis 47
Lampiran 3. Uji KLT 48
Lampiran 4. Kromatogram GC senyawa hasil sintesis 49 Lampiran 5. Spektra MS senyawa hasil sintesis 50 Lampiran 6. Spektra IR senyawa hasil sintesis 52
1
BAB I
PENDAHULUAN
A. Latar Belakang
Kanker merupakan suatu penyakit yang disebabkan karena sel dalam tubuh telah kehilangan sifat normalnya sehingga mengalami pertumbuhan yang sangat cepat dan tidak terkendali. Perkembangan sel yang tidak normal ini dapat mengganggu dan bahkan dapat mengancam jiwa penderitanya. Kanker dapat terjadi di semua bagian tubuh manusia dan dapat menyerang siapa saja, tidak mengenal usia atau jenis kelamin. Sulitnya menangani penyakit kanker disebabkan karena pengobatan kemoterapi kurang selektif terhadap sel kanker (Wu, Huang, dan Chang, 2008).
Terapi pengobatan penyakit kanker dapat dilakukan dengan menggunakan senyawa inhibitor angiogenesis. Angiogenesis adalah proses pembentukan pembuluh darah baru dari pembuluh darah yang telah ada (Plank dan Sleeman, 2003). Adanya pembuluh darah baru yang terbentuk akibat proses angiogenesis
berfungsi mensuplai oksigen dan nutrisi yang penting bagi perkembangan sel kanker. Terapi anti angiogenesis dilakukan dengan cara menghambat sintesis protein angiogenesis yang dihasilkan sel kanker, menetralkan protein
angiogenesis, menghambat reseptor endotelial protein angiogenesis, atau secara langsung menginduksi apoptosis sel endotelial (Wu et al., 2008).
kerusakan sedikit saja pada microvessel sel kanker dapat menyebabkan sel kanker kekurangan nutrisi dan mati (Hou, Tian, dan Wei, 2004).
Kurkumin merupakan senyawa aktif dalam rhizoma tanaman Curcuma longa L yang telah diteliti berpotensi sebagai senyawa antiangiogenesis(Gururaj, Belakavad, Venkatesh, Marm, Salimatha, 2002). Robinson et al. (2003) merancang senyawa-senyawa enon aromatik dan dienon aromatik yang merupakan analog kurkumin sebagai inhibitor angiogenesis. Senyawa-senyawa tersebut dilaporkan aktif sebagai inhibitor angiogenesis dengan penghambatan antara 87,1-98,2% pada konsentrasi 3 µg/mL dan antara 90,4-98,1% pada konsentrasi 6 µg/mL.
Struktur kurkumin memiliki dua gugus α,β-unsaturated keton yang dapat menghambat aktivasi NF-κB (Moos et al., 2004). NF-κB merupakan faktror transkripsi yang diperlukan untuk ekspresi gen-gen yang terlibat pada proses proliferasi, invasi sel, metastasis, angiogenesis dan dapat pula menekan proses apoptosis pada berbagai sel tumor (Aggarwal et al., 2003). Namun adanya tautomerisasi menyebabkan berkurangnya aktivitas kurkumin karena gugus keton berubah ke bentuk enol sehingga hanya memiliki satu gugus α,β-unsaturated
keton. Stabilisasi struktur keto bertanggung jawab terhadap peningkatan aktivitas turunan kurkumin (Suparjan dan Da’i, 2005). Selain itu, menurut penelitian yang dilakukan oleh Goel, Kunnumakkara, dan Aggarwal (2008) dengan menggunakan buffer fosfat, sebagian besar (lebih dari 90%) kurkumin dapat terdegradasi dalam
Senyawa 2,2´-(1,4 fenilena bis (metanililidena)) disikloheksanadion merupakan senyawa turunan kurkumin yang memiliki dua bagian dua gugus α,β -unsaturated keton yang dapat bekerja sebagai inhibitor angiogenesis. Senyawa 2,2´-(1,4 fenilena bis (metanililidena)) disikloheksanadion diharapkan dapat digunakan sebagai inhibitor angiogenesis yang lebih poten dibandingkan kurkumin.
Senyawa 2,2´-(1,4 fenilena bis (metanililidena)) disikloheksanadion dapat disintesis dari senyawa sikloheksana-1,3-dion dan terephtalaldehid berdasarkan reaksi kondensasi aldol silang. Prinsip reaksi kondensasi aldol silang adalah reaksi adisi dimana dua molekul atau lebih bergabung menjadi satu molekul yang lebih besar, dengan atau tanpa hilangnya suatu molekul kecil. Produk reaksi kondensasi aldol silang adalah senyawa enon berkonjugasi alfa
-beta (Fessenden dan Fessenden, 1986).
Katalis digunakan untuk menurunkan energi aktifasi suatu reaksi sehingga dapat mempercepat suatu reaksi. Pada sintesis 2,2´-(1,4 fenilena bis
(metanililidena)) disikloheksanadion digunakan katalis natrium hidroksida karena merupakan basa kuat sehingga diharapkan mudah untuk mengambil hidrogen alfa dari 1,3 sikloheksanadion untuk membentuk ion enolat karena adanya halangan sterik gugus karbonil pada 1,3 sikloheksanadion.
1. Permasalahan
2. Keaslian Penelitian
Sejauh pengamatan peneliti, penelitian mengenai sintesis senyawa 2,2´-(1,4 fenilena bis (metanililidena)) disikloheksanadion dari 1,3 sikloheksanadion dan terephtalaldehid belum pernah dilakukan.
3. Manfaat Penelitian
1. Manfaat teoritis
Untuk memberikan informasi mengenai sintesis 2,2´-(1,4 fenilena bis
(metanililidena)) disikloheksanadion dari sikloheksana-1,3-dion dan terephtalaldehid dengan katalis natrium hidroksida (NaOH).
2. Manfaat metodologi
Untuk memberikan pengetahuan tentang cara sintesis 2,2´-(1,4 fenilena
bis (metanililidena)) disikloheksanadion dengan menggunakan reaksi kondensasi aldol silang.
3. Manfaat praktis
Untuk memberikan informasi adanya senyawa yang berpotensi sebagai inhibitor angiogenesis.
B. Tujuan Penelitian
5
BAB II
PENELAAHAN PUSTAKA
A. Angiogenesis
Angiogenesis adalah proses pembentukan pembuluh darah baru dari pembuluh darah yang telah ada (Plank dan Sleeman, 2003). Adanya pembuluh darah baru yang terbentuk akibat proses angiogenesis berfungsi mensuplai oksigen dan nutrisi yang penting bagi perkembangan sel kanker. Terapi anti
angiogenesis dilakukan dengan cara menghambat sintesis protein angiogenesis
yang dihasilkan sel kanker, menetralkan protein angiogenesis, menghambat reseptor endotelial protein angiogenesis, atau secara langsung menginduksi apoptosis sel endotelial. (Wu, Huang, dan Chang, 2008).
Terapi anti angiogenesis memiliki toksisitas kecil, dapat digunakan dalam berbagai jenis tumor primer termasuk tumor metastasis, dan efektif karena kerusakan sedikit saja pada microvessel sel kanker dapat menyebabkan sel kanker kekurangan nutrisi dan mati. Selain itu sel-sel endotel yang secara genetik stabil sehingga kecil kemungkinannya untuk mengalami mutasi yang memungkinkan mereka mengembangkan resistansi terhadap obat (Hou, Tian, dan Wei, 2004).
B. Kurkumin
Kurkumin (1,7-bis(4’-hidroksi-3’-metoksifenil)-1,6-heptadiena-3,5-dion) yang merupakan komponen aktif dari rhizoma Curcuma longa L. Kurkumin dapat menghambat inisiasi, promosi, dan metastasis tumor. Kurkumin juga telah diteliti dan berpotensi sebagai anti angiogenesis (Gururaj et al., 2002). Robinson et al.
merupakan analog kurkumin sebagai inhibitor angiogenesis. Senyawa-senyawa tersebut dilaporkan aktif sebagai inhibitor angiogenesis dengan penghambatan antara 87,1-98,2% pada konsentrasi 3 µg/mL dan antara 90,4-98,1% pada konsentrasi 6 µg/ml.
H3CO
Gambar 1. Struktur kurkumin
Struktur kurkumin memiliki dua gugus α,β-unsaturated keton yang dapat menghambat aktivasi NF-κB (Moos et al., 2004). NF-κB merupakan faktror transkripsi yang diperlukan untuk ekspresi gen-gen yang terlibat pada proses proliferasi, invasi sel, metastasis, angiogenesis dan dapat pula menekan proses apoptosis pada berbagai sel tumor (Aggarwal et al., 2003).
Stabilitas kurkumin dapat dipengaruhi oleh tautomerisasinya. Bentuk tautomeri tersebut berpengaruh terhadap sebaran muatan positif struktur kurkumin. Semakin bertambah sebaran muatan positif, menunjukkan aktivitas yang semakin meningkat. Stabilisasi struktur keto bertanggung jawab terhadap peningkatan aktivitas turunan kurkumin (Suparjan dan Da’i, 2005).
H3CO
C. Senyawa 2,2´-(1,4 fenilena bis (metanililidena)) disikloheksanadion
Suatu reaksi kondensasi ialah reaksi di mana dua molekul atau lebih bergabung menjadi satu molekul yang lebih besar, dengan atau tanpa hilangnya suatu molekul kecil seperti air. Bila suatu aldehida diolah dengan basa seperti NaOH dalam air, ion enolat yang terjadi dapat bereaksi pada gugus karbonil dari molekul aldehid lain yang disebut suatu reaksi kondensasi aldol. Kata ”aldol” diturunkan dari aldehida dan alkohol, memerikan produk itu, yang merupakan suatu aldehida β-hidroksi (Fessenden dan Fessenden, 1986).
CH3CH OH Gambar 3. Resonansi ion enolat
Prinsip reaksi kondensasi aldol silang adalah suatu senyawa karbonil dengan sedikitnya satu hidrogen α mengalami reaksi kondensasi dengan senyawa karbonil lain yang tidak memiliki hidrogen α dalam suasana basa. Suatu kondensasi aldol silang sangat berguna bila hanya satu senyawa karbonil yang
memiliki hidrogen α, kalau tidak akan diperoleh produk campuran. Keton dapat
digunakan dalam kondensasi aldol silang dengan aldehida yang tidak mengandung
hidrogen α.
Senyawa 2,2´-(1,4 fenilena bis (metanililidena)) disikloheksanadion diduga dapat disintesis dari starting material 1,3 sikloheksanadion dan terephtalaldehida. Reaksi yang mendasari sintesis senyawa 2,2´-(1,4 fenilena bis
(metanililidena)) disikloheksanadion adalah reaksi kondensasi aldol silang. Dalam suasana basa, hidrogen alfa pada 1,3 sikloheksanadion akan terdeprotonasi dan terbentuk ion enolat yang berperan sebagai nukleofil. Pembentukan ion enolat akan meningkatkan nukleofilisitas C alfa pada 1,3 sikloheksanadion dan dapat beresonansi membentuk karbanion yang kemudian menyerang atom C karbonil dari terephtalaldehida. Kemudian dari reaksi tersebut akan terbentuk produk senyawa aldol yang mudah terdehidrasi sehingga menghasilkan senyawa 2,2´-(1,4 fenilena bis (metanililidena)) disikloheksanadion.
Nama lain dari 1,3-sikloheksandion adalah dihidroresorsinol. Senyawa ini berupa kristal, dengan rumus molekul C8H6O2 dan berat molekul 112,12. Titik lebur senyawa ini adalah 105°C. Dihidroresorsinol larut dalam air, kloroform, aseton dan benzena panas. Tidak larut dalam eter, karbondioksida dan petroleum eter (Budavari, O’Neil, Smith, dan Heckelman, 1989).
O
O
Gambar 5. Struktur 1,3-sikloheksanadion (Budavari, 1989).
gram/mol. Titik lebur senyawa ini adalah 114-116°C. Titik didih senyawa ini adalah 246°C. Terephthalaldehyde larut dalam air dan alkohol (Lide, 2010).
O
H O
H
Gambar 6. Terephthalaldehid
Katalis adalah suatu senyawa kimia yang dapat meningkatkan kecepatan suatu reaksi tanpa diubah dalam reaksi keseluruhan, tetapi bukan berarti katalis tidak terlibat dalam reaksi. Pada saat reaksi berlangsung, katalis akan berada dalam bentuk yang sama sebelum dan sesudah reaksi (Bruice, 1998).
Ada beberapa mekanisme yang dapat dilakukan oleh katalis:
1. Meningkatkan kemampuan elektrofil untuk diserang oleh nukleofil 2. Meningkatkan reaktifitas dari suatu nukleofil
3. Meningkatkan kemampuan gugus pergi (leaving group) untuk meninggalkan senyawa (Bruice,1998).
Natrium hidroksida, pemerian berupa putih, massa melebur, berbentuk pellet, serpihan atau batang atau bentuk lain. Keras, rapuh, dan menunjukkan pecahan hablur. Bila dibiarkan di udara, dapat menyerap CO2 dan lembab. Kelarutan natrium hidroksida, mudah larut dalam air dan dalam ethanol Direktorat Jendral Pengawasan Obat dan Makanan, 1995).
D. Uji Pendahuluan
1. Pemeriksaan organoleptis
Uji ini merupakan uji yang paling sederhana dan memuat paparan mengenai suatu zat secara umum meliputi bentuk, warna, dan bau. Pernyataan dalam pemeriksaan organoleptis tidak cukup kuat dijadikan syarat baku. Namun secara tidak langsung dapat membantu dalam penilaian pendahuluan terhadap zat yang bersangkutan (Direktorat Jendral Pengawasan Obat dan Makanan, 1995)
2. Uji Kelarutan
Kelarutan suatu zat sebagian besar disebabkan oleh polaritas dari pelarut yaitu oleh momen dipolnya. Pelarut polar dapat melarutkan zat terlarut ionik dan zat polar lain. Pelarut semipolar seperti alkohol dapat dapat menginduksi suatu derajat polaritas tertentu dalam molekul pelarut non polar, sehingga menjadi dapat larut dalam alkohol. Maka pelarut semipolar ini dapat bertindak sebagai pelarut perantara yang dapat menyebabkan bercampurnya cairan polar dan nonpolar. Pelarut nonpolar dapat melarutkan zat terlarut non polar melalui interaksi dipol induksi. Selain momen dipol, faktor lain yang berpengaruh terhadap kelarutan zat antara lain tetapan dielektrik, asosiasi, solvasi, tekanan dalam, reaksi asam-basa dan faktor-faktor lainnya (Martin dan Bustamante, 1993).
3. Uji titik lebur
sehingga bila energi yang diserap cukup besar maka akan terjadi vibrasi dan rotasi dari molekul tersebut. Bila suhu tetap dinaikkan terus maka ikatan antar molekul akan rusak dan berubah menjadi cairan (Bradstatter, 1971).
Penelitian titik lebur dapat memberikan informasi mengenai kemurnian dari suatu produk hasil sintesis. Pada umumnya suatu senyawa mempunyai kemurnian yang baik bila jarak leburnya tidak lebih dari 2°C. Rentangan lebih besar dari harga ini dapat dikatakan senyawa kurang murni (MacKenzie, 1967).
4. Uji kemurnian menggunakan Kromatografi Lapis Tipis (KLT)
KLT merupakan metode pemisahan komponen-komponen atas dasar perbedaan adsorbsi atau partisi oleh fase diam di bawah pergerakan fase gerak. Pemilihan fase gerak sangat dipengaruhi oleh macam dan polaritas senyawa kimia yang dipisahkan (Mulja dan Suharman,1995).
Kromatografi lapis tipis dapat digunakan untuk mengidentifikasi komponen tertentu. Teknik ini sering dilakukan dengan lempeng kaca atau plastik yang dilapisi dengan fase diam. Senyawa yang akan dianalisis ditotolkan pada dasar lempengan yang dilapisi fase diam dan dielusi dengan fase gerak yang akan bergerak naik oleh karena gaya kapilaritas (Bresnick, 2004).
disimpulkan bahwa jarak rambat senyawa pada lempengan dapat digunakan sebagai cerminan polaritas suatu senyawa (Bresnick, 2004).
Untuk mengidentifikasi bercak yang ada pada lempeng KLT dapat dilakukan dengan menempatkan lempeng KLT dibawah sinar UV atau dengan menyemprotkan larutan yang dapat bereaksi dengan senyawa sehingga dapat menimbulkan warna (Bresnick, 2004).
Kromatografi Lapis Tipis (KLT) dapat digunakan untuk menguji kemurnian secara kualitatif dari campuran suatu senyawa. Hal ini berkaitan untuk pembuktian ada atau tidaknya komponen yang dicari dan apakah komponen tersebut murni atau tidak. (Gasparic dan Churacek, 1978).
5. Kromatografi Gas
Kromatografi gas merupakan instrumen analitis yang memberikan informasi baik kualitatif maupun kuantitatif mengenai komponen suatu sampel. Sampel akan mengalami proses pemisahan dalam kolom, kemudian dideteksi dan direkam sebagai pita elusi (Day and Underwood, 1996).
E. Elusidasi Struktur
1. Spektroskopi Massa
Metode kromatografi gas dan spektrometri massa memberikan keuntungan saat keduanya digunakan secara bersamaan. Proses pemisahan dilakukan oleh kromatografi gas, sedangkan proses identifikasi dan kuantitatif dilakukan oleh spektrometri massa. Keuntungan dari kromatografi gas-spektrometri massa antara lain metode ini dapat digunakan untuk hampir semua jenis analit, memiliki batas deteksi yang rendah, dan memberi informasi penting tentang spektra massa dari suatu senyawa organik (Dean, 1995).
2. Spektrofotometri Inframerah
Spektrofotometri inframerah biasanya digunakan untuk mengetahui gugus fungsional yang terdapat dari suatu senyawa (Bresnick, 2004). Radiasi yang digunakan untuk analisis instrumental adalah radiasi inframerah dengan rentang bilangan gelombang 4000 sampai 670 cm-1 atau panjang gelombang 2,5 sampai 15 µm. Radiasi tersebut terbagi lagi menjadi 2 daerah yaitu gugus fungsi pada rentang bilangan gelombang antara 4000 cm-1 hingga 6000 cm-1 dan darah fingerprint pada rentang bilangan gelombang 1600 hingga 670 (Muljadan Suharman, 1995).
akan diserap. Serapan inilah yang dapat direkam oleh detektor pada spektrofotometri inframerah (Bresnick, 2004).
F. Landasan Teori
Prinsip reaksi kondensasi aldol silang adalah suatu senyawa karbonil dengan sedikitnya satu hidrogen α mengalami reaksi kondensasi dengan senyawa karbonil lain yang tidak memiliki hidrogen α dalam suasana basa. Senyawa 1,3 sikloheksanadion memiliki hidrogen yang berposisi alfa terhadan dua gugus karbonil sehingga bersifat asam. Adanya katalis natrium hidroksida dapat menyebabkan terbentuknya ion enolat. Hal ini disebabkan karena ion OH- akan mengambil hidrogen alfa yang bersifat asam sehingga akan terbentuk ion enolat. Pembentukan ion enolat akan meningkatkan nukleofilisitas dari karbon alfa 1,3 sikloheksanadion dan dapat beresonansi membentuk karbanion yang kemudian menyerang atom karbon gugus karbonil senyawa terephtalaldehid yang bersifat elektrofil untuk membentuk senyawa aldol yang mudah terdehidrasi dan menghasilkan senyawa 2,2´-(1,4 fenilena bis (metanililidena)) disikloheksanadion.
G.Hipotesis
15
BAB III
METODE PENELITIAN
A. Jenis dan Rancangan Penelitian
Penelitian ini termasuk dalam penelitian eksperimental deskriptif non-analitik. Pada penelitian ini tidak ada perlakuan pada subjek uji dan hanya dipaparkan fenomena yang terjadi yang tidak terdapat hubungan sebab akibat.
B. Definisi Operasional
1. Reaktan adalah bahan yang digunakan untuk penelitian. Reaktan yang digunakan dalam penelitian ini adalah terephtalaldehid dan 1,3-sikloheksandion.
2. Katalis adalah suatu senyawa yang digunakan dalam reaksi untuk meningkatkan laju reaksi kimia. Dalam penelitian ini digunakan katalis natrium hidroksida.
3. Senyawa target adalah senyawa yang diharapkan terbentuk dari reaksi. Senyawa target yang diharapkan terbentuk adalah senyawa 2,2´-(1,4 fenilena
bis (metanililidena)).
C. Bahan Penelitian
Sikloheksana-1,3-dion (p.a., Nacalai), Aquades, Terephtalaldehid (p.a., Nacalai), Etanol (p.a., Merck), Natrium hidroksida (p.a., Merck), Metanol (p.a.,
D. Alat Penelitian
Pengaduk Magnetik, Pemanas Listrik (Herdolph MR 2002), Pengering (Memmert Oven Model 400), Neraca analitik (Mextler PM 100), Thermophan (Electrothermal 9100), Seperangkat alat gelas, klem, statif, corong Buchner, spektrofotometer IR (IR Shimadzu Prestige-21), kromatografi gas-spektrometer massa (Shimadzu QP 2010S), lampu UV254 nm, mikropipet, baskom, kertas saring, dropple plate.
E. Tata Cara Penelitian
1. Sintesis 2,2´-(1,4 bis(metanililidena)) disikloheksanadion dengan katalis NaOH
1,3-Sikloheksanadion 7,46 mmol (0,84 g) dimasukkan ke dalam labu erlenmeyer 500 mL dan dilarutkan dengan etanol 22 mL. Terephtalaldehid 3,73 mmol (0,50 g) ditambahkan dalam larutan tersebut. Natrium hidroksida 1,0 N sebanyak 2 ml dilarutkan dalam 10 mL aquadest, ditambahkan ke dalam campuran tersebut kemudian digojog. Campuran diaduk dengan pengaduk magnetik pada kecepatan 250 putaran per menit pada suhu di bawah suhu kamar selama 60 menit. Aquadest ditambahkan hingga volume 400 mL. Endapan yang terbentuk disaring kemudian dikeringkan di dalam oven.
2. Uji Pendahuluan a. Organoleptis
digunakan dalam penelitian yaitu 1,3-sikloheksanadion dan terephtalaldehid.
b. Uji Kelarutan Senyawa Hasil Sintesis
Senyawa hasil sintesis sebanyak 10 mg dimasukkan ke dalam beberapa tabung reaksi, kemudian ditambahkan dengan akuades tetes demi tetes, amati kelarutannya. Pelarut lain yaitu etanol, metanol dan kloroform dilakukan dengan prosedur yang sama. Kemudian dibandingkan dengan reaktan yang digunakan dalam penelitian yaitu 1,3-sikloheksanadion dan terephtalaldehid
c. Uji Titik Lebur
Sejumlah kristal hasil sintesis dimasukkan ke dalam
electrothermal capillary tubes, kemudian dimasukkan ke dalam alat pengukur titik lebur (thermophan). Amati peleburan kristalnya dan catat suhu waktu pertama kali melebur hingga kristal melebur seluruhnya dengan kenaikan suhu 0,2°C tiap menitnya.
d. Uji Kemurnian Menggunakan Kromatografi Lapis Tipis (KLT)
e. Kromatografi Gas
Pemisahan dan pemeriksaan kemurnian senyawa hasil sintesis dilakukan menggunakan instrumen kromatografi gas dengan kondisi alat: suhu injektor 300°C, jenis kolom Rtx-5MS, panjang kolom 30 meter, suhu kolom diprogram 100-300°C, gas pembawa helium, tekanan 22 kPa, kecepatan alir fase gerak 0,5 ml/menit, dan detektor ionisasi nyala. Cuplikan senyawa hasil sintesis dilarutkan dalam aseton, kemudian diinjeksikan kedalam injektor pada alat kromatografi gas. Aliran gas dari gas pengangkut helium akan membawa cuplikan yang sudah diuapkan masuk kedalam kolom Rtx-5MS yang dilapisi fase cair
dimethylpolysiloxane. Selanjutnya cuplikan diukur oleh detektor hingga diperoleh suatu kromatogram.
1. Elusidasi Struktur Senyawa Hasil Sintesis
Elusidasi struktur senyawa hasil sintesis dilakukan dengan cara: a. Spektroskopi Massa
dengan kelimpahan relatif setiap fragmennya. Kelimpahan relatif setiap fragmen akan dicatat dan menghasilkan data spektra massa.
b. Spektrofotometri Inframerah
Senyawa hasil sintesis sebanyak kurang lebih 0,5-1 mg dicampur homogen dengan kurang lebih 10 mg KBr, kemudian dikempa dan dibuat tablet. Cahaya inframerah dari sumber dilewatkan melalui cuplikan, kemudian dipecah menjadi frekuensi-frekuensi individunya dalam monokromator dan intensitas relatif dari frekuensi individu diukur oleh detektor hingga didapat spektra inframerah dari senyawa yang bersangkutan. Bilangan gelombang yang digunakan 400-4000 nm.
F. Analisis Hasil
1. Crude Product
Penimbangan crude product dilakukan setelah senyawa hasil sintesis diisolasi dan dikeringkan.
2. Analisis Pendahuluan
Analisis pendahuluan senyawa hasil sintesis berdasarkan data organoleptis, data kromatografi lapis tipis, kelarutan, titik lebur, dan data kromatografi gas. 3. Elusidasi Struktur
20
BAB IV
HASIL DAN PEMBAHASAN
A. Sintesis senyawa 2,2´-(1,4 fenilena bis (metanililidena))
disikloheksanadion
Penelitian ini bertujuan untuk mensintesis senyawa 2,2´-(1,4 fenilena bis
(metanililidena)) disikloheksanadion dari 1,3 sikloheksanadion dan terephthalaldehid berdasarkan reaksi kondensasi aldol silang. Proses sintesis dilakukan dengan menggunakan katalis natrium hidroksida untuk pembentukan ion enolat yang berperan sebagai nukleofil sehingga dapat bereaksi dengan karbon pada gugus karbonil senyawa terephthalaldehid membentuk suatu produk aldol yang mudah terdehidrasi menjadi 2,2´-(1,4 fenilena bis (metanililidena)) disikloheksanadion.
Hidrogen alfa pada senyawa 1,3 sikloheksanadion bersifat asam sehingga dengan penambahan natrium hidroksida dapat mendeprotonasi hidrogen alfa membentuk ion enolat. Adanya 2 gugus karbonil pada 1,3 sikloheksanadion dapat menimbulkan halangan sterik yang menghambat proses deprotonasi hidrogen alfa pada 1,3 sikloheksanadion sehingga digunakan katalis natrium hidroksida yang merupakan basa kuat.
O
Hidrogen alfa di antara 2 gugus karbonil memiliki keasaman yang lebih tinggi dibandingkan hidrogen alfa yang lain karena sifat elektronegatif 2 gugus karbonil menyebabkan proses deprotonasi cenderung terjadi pada hidrogen alfa di antara gugus karbonil tersebut. Ion enolat yang terbentuk dapat beresonansi membentuk suatu karbanion yang berperan sebagai nukleofilik.
O
1,3 sikloheksanadion Pembentukan ion enolat
H
O O
Gambar 8. Mekanisme pembentukan ion enolat
H
2,2'-(1,4 fenilenabis(metanilidena)) disikloheksanadion
Pembentukan produk aldol
Gambar 9. Mekanisme sintesis 2,2´-(1,4 fenilena bis (metanililidena)) disikloheksanadion
O O
Gambar 10. Mekanisme self condensation 1,3 sikloheksanadion
Sintesis dilakukan dengan menggunakan pengadukan untuk meningkatkan pergerakan molekul. Hal ini akan meningkatkan terjadinya tumbukan antar molekul starting material sehingga mempercepat reaksi. Sintesis dilakukan di bawah suhu kamar dengan menggunakan baskom berisi air es untuk membentuk inti kristal hasil reaksi, memperkecil kemungkinan terjadinya reaksi Cannizaro dan mencegah kemungkinan terjadinya kondensasi senyawa 2,2´-(1,4 fenilena bis
(metanililidena)) disikloheksanadion dengan terephthalaldehid atau 1,3 sikloheksanadion yang belum bereaksi. Senyawa 2,2´-(1,4 fenilena bis
disikloheksanadion dengan 1,3 sikloheksanadion lebih kecil dibandingkan dengan terephthalaldehid karena gugus karbonil 1,3 sikloheksanadion kurang elektronegatif dibandingkan gugus karbonil terephthalaldehid.
O
H
O H
O
O
Gambar 11. Hidrogen alfa senyawa 2,2´-(1,4 fenilena bis (metanililidena)) disikloheksanadion
Untuk mendesak molekul senyawa 2,2´-(1,4 fenilena bis (metanililidena)) disikloheksanadion agar dapat terpisah dari campuran, maka perlu dilakukan penambahan air. Hal ini dikarenakan berdasarkan strukturnya, senyawa 2,2´-(1,4 fenilena bis (metanililidena)) disikloheksanadion memiliki kelarutan yang kurang baik dalam air. Bobot molekul yang besar, banyak mengandung hidrokarbon, dan bentuknya yang simetris dapat menyebabkan senyawa 2,2´-(1,4 fenilena bis
(metanililidena)) disikloheksanadion cenderung bersifat hidrofob. Air akan mendesak senyawa 2,2´-(1,4 fenilena bis (metanililidena)) disikloheksanadion dari etanol sehingga dapat membentuk kristal sehingga dapat dilakukan pemisahan terhadap starting material dengan menggunakan penyaringan karena 1,3 sikloheksanadion dan terephthalaldehid dapat terlarut dalam air.
gugus karbonil terephthalaldehid mulai terjadi saat proses pengadukan untuk melarutkan senyawa terephthalaldehid. Hal ini menyebabkan terjadinya perbedaan jumlah crude product hasil sintesis karena waktu pelarutan terephthalaldehid yang berbeda. Jumlah senyawa hasil sintesis tidak maksimal kemungkinan disebabkan karena pembentukan ion enolat oleh natrium hidroksida yang kurang optimal sehingga menyebabkan jumlah nukleofil yang menyerang elektrofil kurang optimal dan proses kristalisasiyang kurang sempurna.
B. Analisis Senyawa Hasil Sintesis
1. Uji Organoleptis
Uji organoleptis dilakukan dengan cara membandingkan senyawa hasil sintesis dengan 1,3 sikloheksanadion dan terephthalaldehid berdasarkan pengamatan secara langsung terhadap bentuk, warna, dan bau. Senyawa hasil sintesis dapat dilihat pada gambar berikut:
Gambar 12. Senyawa hasil sintesis
Tabel I. Data Uji Organoleptis Senyawa Hasil Sintesis dan Starting Material
Pengamatan Senyawa Hasil Sintesis
Starting Material
1,3
sikloheksanadion terephthalaldehid
Bentuk Serbuk kristal kristal
Warna putih Putih kecoklatan Putih mengkilat
Bau khas khas khas
Berdasarkan uji organoleptis di atas, ada perbedaan antara senyawa hasil sintesis dengan starting materialnya yang menunjukkan bahwa telah terbentuk suatu senyawa baru hasil reaksi. Senyawa hasil sintesis berupa serbuk yang berwarna putih, berbeda dengan starting material yang berupa kristal berwarna putih kecoklatan dan putih mengkilat. Selain itu senyawa hasil sintesis memiliki bau yang khas, berbeda dengan starting material.
2. Uji Kelarutan
Hasil uji kelarutan senyawa hasil sintesis dibandingkan dengan kelarutan
starting materialnya yaitu 1,3 sikloheksanadion dan terephthalaldehid, dapat dilihat pada tabel berikut:
Tabel II. Data uji kelarutan senyawa hasil sintesis, 1,3 sikloheksanadion, dan terephthalaldehid
Pelarut
Kelarutan Senyawa
Hasil Sintesis Terephthalaldehid
1,3-Sikloheksanadion Aquadest praktis tidak larut agak sukar larut Larut
Dimetil sulfoksida Larut larut larut
Etanol sukar larut Larut mudah larut
Aseton agak sukar larut larut larut
Piridin mudah larut larut mudah larut
Berdasarkan data tersebut dapat diketahui senyawa hasil sintesis dapat larut dalam pelarut kurang polar dan basa. Senyawa hasil sintesis memiliki kelarutan yang berbeda dengan starting material yang menunjukkan telah terbentuk suatu senyawa baru.
3. Uji Titik Lebur
Uji titik lebur dapat digunakan untuk mengetahui terbentuknya senyawa baru hasil sintesis dengan cara membandingkannya dengan 1,3 sikloheksanadion dan terephthalaldehid. Selain itu uji titik lebur juga dapat digunakan untuk mengetahui kemurnian senyawa hasil sintesis berdasarkan rentang titik leburnya.
Tabel III. Data uji titik lebur senyawa hasil sintesis, 1,3 sikloheksanadion, dan terephthalaldehid
No Senyawa Titik Lebur (°C)
1 hasil sintesis 218 -220
2 1,3 sikloheksanadion
(Budavari et al., 1989) 105 3 Terephthalaldehid (Lide,
2004) 114-116
4. Uji Kemurnian Senyawa Hasil Sintesis Menggunakan Kromatografi
Lapis Tipis (KLT)
Pengujian dengan kromatografi lapis tipis (KLT) dilakukan untuk mengidentifikasi dan mengetahui kemurnian senyawa hasil sintesis. Senyawa 1,3 sikloheksanadion dan terephthalaldehid digunakan sebagai pembanding untuk mengidentifikasi adanya senyawa baru yang terbentuk.
Elusi dilakukan menggunakan 2 jenis fase gerak yang berbeda untuk mengetahui kemurnian senyawa hasil sintesis. Perbedaan polaritas fase gerak dapat dilihat pada tabel di bawah ini:
Tabel IV. Indeks polaritas n-heksan:etil asetat dan kloroform:etil asetat
Fase Gerak Indeks Polaritas
n-heksan:Etil Asetat (1:1) 2,2
Kloroform:Etil Asetat (1:9) 4,3
Uji menggunakan KLT ini menggunakan sistem kromatografi fase normal dimana fase diamnya bersifat lebih polar dibandingkan fase geraknya. Fase diam yang digunakan adalah silika gel GF254. Silika gel bersifat polar karena pada strukturnya mengandung gugus hidroksi dan terdapat atom oksigen yang letaknya berselang-seling dengan atom silika. Senyawa 2,2´-(1,4 fenilena bis
O
O
O
O
Si
O Si
O Si
O Si
O O O O
H H H H
keterangan: = interaksi hidrogen
Gambar 13. Interaksi hidrogen senyawa 2,2´-(1,4 fenilena bis (metanililidena)) disikloheksanadion dengan fase diam silika gel
Kloroform:Etil Asetat (1:9) n-heksan:Etil Asetat (1:1)
n-heksan:Etil Asetat (1:1)
Gambar 14. Kromatogram hasil elusi senyawa hasil sintesis, 1,3 sikloheksanadion dan terephthalaldehid
keterangan:
A = senyawa hasil sintesis replikasi I B = 1,3 sikloheksanadion
C = terephthalaldehid
31
Berdasarkan data kromatogram tersebut dapat diketahui nilai Rf masing-masing bercak.
Tabel V. Data nilai Rf masing-masing bercak Senyawa Hasil
Sintesis Terephthlaldehid
1,3-Berdasarkan data tersebut dapat diketahui bahwa senyawa hasil sintesis merupakan senyawa baru karena memiliki nilai Rf yang berbeda dengan 1,3 sikloheksanadion dan terephthalaldehid. Elusi senyawa hasil sintesis menggunakan fase gerak n-heksan:Etil Asetat (1:1) menghasilkan nilai Rf 0,20 sedangkan elusi menggunakan fase gerak n-heksan:Etil Asetat (1:1) menghasilkan nilai Rf 0,66.
Untuk menguji apakah senyawa hasil sintesis replikasi I, II, dan III merupakan senyawa yang sama, elusi senyawa hasil sintesis replikasi I, II, dan III dilakukan dalam 1 plat KLT menggunakan fase gerak n-heksan:Etil Asetat (1:1) karena berdasarkan nilai Rf, proses pemisahannya lebih baik. Berdasarkan data tersebut dapat diketahui senyawa hasil sintesis replikasi I, II, dan III merupakan senyawa yang sama karena memiliki profil KLT yang mirip.
4. Kromatografi Gas-Spektroskopi Massa (GC-MS)
Pengujian senyawa hasil sintesis dengan menggunakan kromatografi gas-spektroskopi massa (GC-MS) dilakukan untuk mengetahui kemurnian senyawa hasil sintesis dan bobot molekul senyawa tersebut.
Gambar 16. Spektra massa peak 3 senyawa hasil sintesis
Berdasarkan spektra massa di atas, dapat diketahui bahwa senyawa pada
peak 3 memiliki bobot molekul 322 gram/mol diketahui dari ion molekulnya yang mempunyai nilai m/z 322. Hal ini sesuai dengan bobot molekul senyawa target hasil sintesis yaitu 2,2´-(1,4 fenilena bis (metanililidena)) disikloheksanadion yang memiliki bobot molekul 322 gram/mol. Fragmen ini memiliki intensitas yang cukup tinggi, yaitu sekitar 50% menunjukkan bahwa fragmen ini cukup stabil. Dalam spektroskopi massa, fragmen-fragmen yang terdeteksi hanyalah fragmen dengan muatan positif, sedangkan fragmen dengan muatan netral atau radikal tidak akan terdeteksi.
294 m/z
Gambar 17. Usulan mekanisme fragmentasi senyawa 2,2´-(1,4 fenilena bis
(metanililidena)) disikloheksanadion
Fragmen dengan nilai m/z 217 memiliki intensitas yang paling tinggi yaitu 100% menunjukkan bahwa fragmen ini adalah yang paling stabil.
Gambar 18. Spektra massa peak 1 senyawa hasil sintesis
Pada kromatogram GC, berdasarkan nilai AUC, kandungan senyawa peak
senyawa ini adalah 2-(4-(dietoksimetil) benzylidene) -1,3-sikloheksanadion yang merupakan reaksi samping pada proses sintesis. Senyawa 2- (4- (dietoksimetil) benzilidena) -1,3-sikloheksanadion berasal dari adisi ion enolat ke salah satu sisi gugus karbonil terephthalaldehid menjadi 4-((2,6-dioksosikloheksilidena) metil) benzaldehid. Senyawa 4-((2,6-dioksosikloheksilidena) metil) benzaldehid bereaksi dengan etanol membentuk senyawa asetal, yaitu 2-(4-(dietoksimetil) benzilidena) -1,3-sikloheksanadion.
Gambar 19. Struktur senyawa 2-(4-(dietoksimetil) benzilidena) -1,3-sikloheksanadion
Fragmentasi senyawa 2-(4-(dietoksimetil) benzylidena) -1,3-sikloheksanadion belum dapat diketahui. Fragmen dengan nilai m/z 108 memiliki intensitas yang paling tinggi yaitu 100% menunjukkan bahwa fragmen ini adalah yang paling stabil.
Berdasarkan data uji GC-MS dapat diketahui bahwa dalam senyawa hasil sintesis mengandung senyawa 2,2´-(1,4 fenilena bis (metanililidena)) disikloheksanadion dan produk reaksi samping yaitu 2-(4-(dietoksimetil) benzilidena) -1,3-sikloheksanadion. Kemurnian senyawa 2,2´-(1,4 fenilena bis
5. Spektrofotometri inframerah
Spektroskopi inframerah (IR) digunakan untuk mengetahui gugus-gugus fungsional penyusun senyawa hasil sintesis.
Gambar 20. Spektra IR senyawa hasil sintesis
Spektra inframerah di atas digunakan sebagai dasar interpretasi gugus-gugus fungsional penyusun senyawa hasil sintesis. Struktur aromatis ditunjukkan pada bilangan gelombang 3093 cm-1. Ikatan C-H sp3 ditunjukkan pada bilangan gelombang 2947 cm-1, 2870 cm-1, 2831 cm-1. Struktur alkena yang mengalami efek konjugasi ditunjukkan pada bilangan gelombang 1604 cm-1 (Pavia, Lampman, Kriz, dan Vyvyan, 2009). Gugus karbonil pada β-diketon bentuk keto ditunjukkan pada serapan doublet bilangan gelombang 1720 cm-1 dan 1689 cm-1 (Pretsch, Buhlmann, dan Badertscher, 2009)
serapan kuat pada bilangan gelombang 1120 cm-1 yang menunjukkan adanya gugus eter alifatik. Senyawa 2-(4-(dietoksimetil) benzilidena) -1,3-sikloheksanadion tidak terlihat dalam spektra IR disebabkan karena kandungan senyawa senyawa 2-(4-(dietoksimetil) benzilidena) -1,3-sikloheksanadion dalam senyawa hasil sintesis terlalu sedikit.
Tabel VI. Analisis spektra IR senyawa hasil sintesis Bilangan Gelombang
(cm-1) Intensitas Gugus Fungsional
3093 sedang-melebar C=C-H aromatis
2947 Sedang-tajam -C-H sp3
2870 Sedang-tajam -C-H sp3
2831 Sedang-tajam -C-H sp3
1720 Kuat-tajam C=O β-diketon bentuk
keto
1689 Kuat-tajam C=O β-diketon bentuk
keto
1604 Kuat-tajam C=C terkonjugasi dengan
C=O
Gambar 21. Spektra IR senyawa terephthalaldehid (Anonim, 2010 a) Spektra IR senyawa hasil sintesis tidak menunjukkan adanya gugus karbonil yang berikatan dengan gugus fenil sehingga dapat diketahui bahwa senyawa hasil sintesis tidak mengandung senyawa terephthalaldehid. Hal ini juga menunjukkan bahwa reaksi adisi ion enolat terjadi pada kedua gugus karbonil terephthalaldehid.
Dalam spektra IR senyawa 1,3 sikloheksanadion terlihat serapan pada bilangan gelombang dan 1570 cm-1 yang menunjukkan adanya gugus karbonil 1,3 diketon bentuk enol (Bruno dan Svonoros, 2006). Ikatan O-H pada gugus enol ditunjukkan oleh serapan lebar pada bilangan gelombang 2557 cm-1(Pretsch, Buhlmann, dan Badertscher, 2009). Adanya bentuk enol ini disebabkan karena adanya tautomeri pada struktur β-diketon senyawa 1,3 sikloheksanadion.
Pada spektra IR senyawa hasil sintesis tidak ditemukan serapan yang menunjukkan ikatan O-H tidak terdapat gugus enol dan tidak terdapat serapan pada bilangan gelombang 1570 cm-1yang menunjukkan adanya gugus karbonil 1,3 diketon bentuk enol. Hal ini menunjukkan bahwa senyawa hasil sintesis tidak mengandung senyawa 1,3 sikloheksanadion. Selain itu hal ini juga memperkuat dugaan bahwa gugus karbonil terephthalaldehid bereaksi hanya dengan hidrogen alfa yang diapit oleh dua gugus karbonil karena senyawa hasil sintesis tidak berada dalam bentuk enol.
Data spektra IR tersebut menujukkan bahwa senyawa hasil sintesis memiliki gugus-gugus fungsional seperti yang diharapkan. Sehingga memperkuat dugaan bahwa senyawa hasil sintesis merupakan 2,2´-(1,4 fenilena bis
40
BAB V
KESIMPULAN DAN SARAN
A. Kesimpulan
Berdasarkan penelitian dapat disimpulkan bahwa senyawa 2,2´-(1,4 fenilena bis (metanililidena)) disikloheksanadion dapat disintesis dari 1,3 sikloheksanadion dan terephthalaldehid berupa crude product sebesar 0,474 gram, 0,682 gram, dan 0,785 gram dengan kemurnian 90,35%.
B. Saran
Daftar Pustaka
Aggarawal, BB., Kumar, A. Aggarawal, MS., and Shishodia, S., 2003, Curcumin derived from Turmeric (Curcuma longa): A Spice for All Seasons,
Phytochemical in Cancer Chemoprevention, 8 (28), 1-9.
Anwar, C., Pranowo, H. D., dan Wahyuni, T. D., 1994, Pengantar Praktikum Kimia Organik, UGM Press, Yogyakarta, pp. 73, 189.
Anonim, 2010 a http://riodb01.ibase.aist.go.jp/sdbs/cgi-bin/cre_frame_disp.cgi? spectrum_type=ir&sdbsno=3580 diakses tanggal 12 desember 2010
Anonim, 2010 http://riodb01.ibase.aist.go.jp/sdbs/cgi-bin/cre_frame_disp.cgi? spectrum_type=ir&sdbsno=10165 diakses tanggal 12 desember 2010
Bradstatter, M. K., 1971, Thermomicroscopy’s Analysis of Pharmaceutical, Pergamon Press, London, pp.1-10.
Bresnick, S. D., 2004, Intisari Kimia Organik, Hipokrates Jakarta, pp. 96-99, 101-107.
Bruno T. J. dan Svonoros P. D. N., 2006, Handbook of Fundamental Spectroscopic Correlation Charts, CRC Press, New York, pp. 7-13.
Budavari, S., O’Neil, M., J., Smith A., dan Heckelman, 1989, The Merck Index, Merck and CO Inc., USA, pp. 7635
Day, Jr., R. A. And Underwood, A. L., Analisis Kimia Kuantitatif, diterjemahkan oleh Pudjaatmaka, A. H., Edisi IV, Penerbit Erlangga, Jakarta, pp. 519. Dean, J. A., 1995, Analytical Chemistry Handbook, McGraw-Hill, Inc., New
York, pp. 13, 26.
Direktorat Jendral Pengawasan Obat dan Makanan, 1995, Farmakope Indonesia, edisi IV, Departemen Kesehatan RI, Jakarta, pp. 589.
Fessenden, R.J, Fessenden, J.S., 1986, Kimia Organik, Jilid 2, , Penerbit Erlangga, Jakarta, pp. 179-183.
Gasparic, J., and Churacek J., 1978, Laboratory Handbook of Paper and Thin Layer Chromatography, Ellis Horwood Limited, England, pp. 63
Goel, A., Kunnumakkara, A. B., dan Aggarwal, B. B., 2008, Curcumin as "Curecumin": From kitchen to clinic. Biochemical Pharmacology, pp. 75, 787-809
Gururaj, A. E., Belakavadi M., Venkatesh, D. A., Marm, D., and Salimatha, B. P., 2002, Molecular mechanisms of anti-angiogenic efect of curcumin,
Biochem. Biophys. Res. Commun., pp. 297, 934–942
Hou, J., Tian, L., dan Wei, Y., 2004, Cancer Immunotherapy of Targeting Angiogenesis, Cellular & Molecular Immunology, 1(3),161-166
Lide D. R., 2004, Handbook of Chemistry dan Physics, 84th Edition, CRC Press, Boston, pp. 157
MacKenzie, 1967, Experimental Organic Chemistry, 3rd Edition, Prentice-Hall Inc., Englewood Cliffs, New Jersey
Martin, A., and Bustamante, P., 1993, Physical Pharmacy Chemical Principles in the Pharmaceutical Sciences, 4th Edition, Lea and Febriger, Philadelphia, pp. 272-275.
Moos, P. J., Edes, K., Mullally, J. E., and Fitzpatrick, F. A., 2004, Curcumin Impairs Tumor Suppressor p53 Function In Colon Cancer Cells,
Carcinogenesis, 25(9), 1611-1617.
Mulja H. M. dan Suharman, 1995, Analisis Instrumental, Airlangga University Press, Surabaya, pp. 104.
Plank, M.J., Sleeman, B.D. 2003. Tumour-induced angiogeneis: a review. Journal of Theoretical Medicine. Vol. 5(3-4), 137-153
Pavia, D. L., Lampman, G. M., Kriz, G. S., Vyvyan, J. R., 2009, Introduction to Spectroscopy, Fourth Edition, Brooks/Cole, USA, pp.16-84
Pretsch E., Buhlmann P., dan Badertscher M., 2009, Structure Determination of Organic Compound, 4th Completely Revised Edition, 269-234, Springer-Verlag, Berlin
Suparjan dan Da’i M., 2005, Hubungan Struktur dan Aktivitas Sitotoksik Turunan Kurkumin Terhadap Sel Myeloma, Majalah Farmasi Indonesia, 16(2), 100-104
LAMPIRAN
Lampiran 1. Perhitungan Crude Product Senyawa Hasil Sintesis
O
Replikasi I
Penimbangan 1,3 sikloheksanadion
Berat Kertas : 0,244 gram
Penimbangan Crude Product :
Berat Kertas + Zat : 0,854 gram Berat Kertas : 0,380 gram
Berat Zat : 0,474 gram
Replikasi II
Penimbangan 1,3 sikloheksanadion
Berat Kertas : 0,410 gram
Penimbangan Crude Product :
Berat Kertas + Zat : 1,156 gram Berat Kertas : 0,495 gram
Replikasi III
Penimbangan 1,3 sikloheksanadion
Berat Kertas : 0,422 gram Berat Kertas + Zat : 1,271 gram Berat Kertas + Sisa : 0,424 gram
Berat Zat : 0,847 gram
Penimbangan Terephthalaldehid
Berat Kertas : 0,413 gram Berat Kertas + Zat : 0,915 gram Berat Kertas + Sisa : 0,414 gram
Berat Zat : 0,501 gram
Penimbangan Crude Product :
Berat Kertas + Zat : 1,288 gram Berat Kertas : 0,503 gram
Lampiran 2. Foto Senyawa Hasil Sintesis
Senyawa Hasil Sintesis
Lampiran 3. Uji KLT
Perhitungan Kepolaran Fase Gerak
Fase Gerak Indeks Polaritas
n-heksan:Etil Asetat (1:1) 2,2
Kloroform:Etil Asetat (1:9) 4,3
Rumus perhitungan kepolaran senyawa :
P′ AB = ΦAPA+ ΦBPB
Keterangan : ΦA = fraksi pelarut A
ΦB = fraksi pelarut B P = polaritas fraksi
P′ = polaritas campuran pelarut Indeks polaritas: n-heksan : 0,0
Etil asetat : 4,4 Kloroform : 4,1
Pada lempeng silika gel GF254 ditotolkan senyawa hasil sintesis dan
starting material yaitu 1,3 sikloheksanadion dan terephthtalaldehid. Setelah dielusi dengan jarak pengembangan 10 cm diperoleh semua bercak berwarna ungu. Dengan menggunakan rumus perhitungan Rf, didapat nilai Rf masing-masing bercak:
Rf = 𝑗𝑗𝑗𝑗𝑗𝑗𝑗𝑗𝑗𝑗 𝑏𝑏𝑏𝑏𝑗𝑗𝑏𝑏𝑗𝑗𝑗𝑗 𝑦𝑦𝑗𝑗𝑦𝑦𝑦𝑦 𝑑𝑑𝑑𝑑ℎ𝑗𝑗𝑎𝑎𝑑𝑑𝑎𝑎𝑗𝑗𝑗𝑗𝑦𝑦 𝑎𝑎𝑏𝑏𝑠𝑠𝑏𝑏𝑎𝑎𝑗𝑗ℎ 𝑏𝑏𝑎𝑎𝑒𝑒𝑎𝑎𝑑𝑑𝑗𝑗𝑗𝑗𝑗𝑗𝑗𝑗𝑗𝑗 𝑏𝑏𝑎𝑎𝑒𝑒𝑎𝑎𝑑𝑑 Senyawa Hasil
Sintesis Terephthlaldehid
Lampiran 7. Spektra IR starting material
Spektra IR 1,3 sikloheksanadion
BIOGRAFI PENULIS