UJI ANGKA KAPANG/KHAMIR (AKK) DAN ANGKA LEMPENG TOTAL (ALT) DALAM JAMU SERBUK TEMULAWAK (Curcuma xanthorrhiza Roxb.) YANG DIJUAL DI PASAR BERINGHARJO
YOGYAKARTA
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Farmasi
Oleh :
Florensia Rika Cristianty NIM : 168114154
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
2021
ii
HALAMAN PERSETUJUAN PEMBIMBING
UJI ANGKA KAPANG/KHAMIR (AKK) DAN ANGKA LEMPENG TOTAL (ALT) DALAM JAMU SERBUK TEMULAWAK (Curcuma xanthorrhiza
Roxb.) YANG DIJUAL DI PASAR BERINGHARJO YOGYAKARTA
Skripsi yang diajukan oleh:
Florensia Rika Cristianty NIM : 168114154
telah disetujui oleh:
Pembimbing Utama
(Dr. apt. Erna Tri Wulandari) Tanggal, 21 Mei 2021
iii
Pengesahan Skripsi Berjudul
UJI ANGKA KAPANG/KHAMIR (AKK) DAN ANGKA LEMPENG TOTAL (ALT) DALAM JAMU SERBUK TEMULAWAK (Curcuma xanthorrhiza
Roxb.) YANG DIJUAL DI PASAR BERINGHARJO YOGYAKARTA
Oleh:
Florensia Rika Cristianty NIM : 168114154
Dipertahankan di hadapan Panitia Penguji Skripsi Fakultas Farmasi
Universitas Sanata Dharma Pada tanggal 23 Maret 2021
Mengetahui Fakultas Farmasi Universitas Sanata Dharma
Dekan
(Dr. apt. Yustina Sri Hartini)
Panitia Penguji Tanda Tangan
1. Dr. apt. Erna Tri Wulandari ………….
2. Dr. apt. Yustina Sri Hartini ………….
3. apt. Maywan Hariono, Ph.D.
iv
PERNYATAAN KEASLIAN KARYA
Saya menyatakan dengan sesungguhnya bahwa skripsi yang saya tulis ini tidak memuat karya atau bagian karya orang lain, kecuali yang telah disebutkan dalam kutipan dan daftar pustaka, dengan mengikuti ketentuan sebagaimana layaknya karya ilmiah.
Apabila dikemudian hari ditemukan indikasi plagiarism dalam naskah ini, maka saya bersedia menanggung segala sanksi sesuai peraturan perundang-undangan yang berlaku.
Yogyakarta, 12 Januari 2021 Penulis,
Florensia Rika Cristianty
v
LEMBAR PERNYATAAN PERSETUJUAN
PUBLIKASI KARYA ILMIAH UNTUK KEPENTINGAN AKADEMIS
Yang bertanda tangan dibawah ini, saya mahasiswa Universitas Sanata Dharma:
Nama : Florensia Rika Cristianty Nomor Mahasiswa : 168114154
Demi pengembangan ilmu pengetahuan, saya memberikan kepada Perpustakaan Universitas Sanata Dharma karya ilmiah saya yang berjudul:
”UJI ANGKA KAPANG/KHAMIR (AKK) DAN ANGKA LEMPENG TOTAL (ALT) DALAM JAMU SERBUK TEMULAWAK (Curcuma
xanthorrhiza Roxb.) YANG DIJUAL DI PASAR BERINGHARJO YOGYAKARTA”
beserta perangkat yang diperlukan (bila ada). Dengan demikian saya memberikan kepada Perpustakaan Universitas Sanata Dharma hak untuk menyimpan, mengalihkan dalam bentuk media lain, mengelolanya dalam bentuk pangkalan data, mendistribusikan secara terbatas, dan mempublikasikannya di Internet atau media lain untuk kepentingan akademis tanpa perlu meminta ijin dari saya maupun memberikan royalti kepada saya selama tetap mencantumkan nama saya sebagai penulis.
Demikian pernyataan ini saya buat dengan sebenarnya.
Dibuat di Yogyakarta
Pada tanggal : 12 Januari 2021
Yang menyatakan
Florensia Rika Cristianty
vi
HALAMAN PERSEMBAHAN
Karya ini penulis persembahkan untuk Tuhan Yesus Kristus,
Bapak, Mamak, Adek, sahabat-sahabatku, teman-teman seperjuanganku FSMD16 Almamaterku Universitas Sanata Dharma Yogyakarta.
vii
PRAKATA
Puji syukur kehadirat Tuhan Yang Maha Esa atas berkat dan rahmat-Nya penulis dapat menyelesaikan penelitian dan penyusunan naskah skripsi yang berjudul
“Uji Angka Kapang/Khamir (AKK) dan Angka Lempeng Total (ALT) dalam Jamu Serbuk Temulawak (Curcuma Xanthorrhiza Roxb.) yang dijual di Pasar Beringharjo Yogyakarta”. Penulisan skripsi inini bertujuan untuk memenuhi salah satu syarat dalam memperoleh gelar Sarjana Farmasi (S.Farm.) Fakultas Famarsi Universitas Sanata Dharma Yogyakarta.
Penyelesaian skripsi ini tentunya tidak lepas dari bimbingan, bantuan, dukungan dan doa dari berbagai pihak. Oleh karena itu, dengan tulus hati penulis ingin mengucapkan terima kasih kepada :
1. Ibu Dr. apt. Yustina Sri Hartini, selaku Dekan Fakultas Farmasi Universitas Sanata Dharmma Yogyakarta, serta dosen penguji yang kerap kali memberikan masukan dan saran dalam proses penyelesaian skripsi ini sehingga menjadikan skripsi ini lebih baik.
2. Ibu Dr. apt. Christine Patramurti, selaku Ketua Program Studi Fakultas Farmasi Universitas Sanata Dharma Yogyakarta.
3. Ibu apt. Dina Christin Ayuning Putri, M.Sc., selaku Dosen Pembimbing Akademik.
4. Ibu Dr. apt. Erna Tri Wulandari, selaku dosen pembimbing skripsi yang telah meluangkan waktunya untuk membantu penulis, membimbing, selalu mengingatkan, memberi saran, serta dukungan kepada penulis selama penyusunan skripsi.
5. Bapak apt. Maywan Hariono, Ph.D. selaku dosen penguji yang telah memberi saran dan masukan dalam proses penyelesaian skripsi ini sehingga menjadikan skripsi ini lebih baik.
6. Bapak Kunto selaku laboran mikrobiologi Fakultas Farmasi Sanata Dharma Yogyakarta atas segala bantuan yang diberikan selama proses pengambilan data skripsi ini.
7. Keluarga tercinta Mamak Veronika Rina, Bapak Kangin dan Adek Julisa Friska Cristiani yang selalu mendukung penulis melalui doa, cinta, kasih
viii
sayang, dukungan, semangat dan wejangan yang tidak pernah habis, sehingga menjadi semangat dan kekuatan bagi penulis dalam menyelesaikan skripsi ini.
8. Andry Purnomo, selaku support system yang telah menemani, membantu, memberi dukungan, bagi penulis dari masa SMA hingga sekarang.
9. Ciwi-ciwi yang masih solid hingga sekarang, Veli dan Sopiya yang selalu menjadi tempat curhat penulis dari masa SMA hingga sekarang, yang selalu memberi wejangan, motivasi, tawa dan mendukung penulis dari jarak jauh.
10. EXCELSONE dan EXCELSONE cabang jogja yang masih solid hingga sekarang, Asri, Saras, Mbak Rizka, Meidy, Veli, Sopiya, Yayan, Andry, Katok, Fadly dan yang lainnya, atas kegajean yang selalu mendatangkan keceriaan, kerecehan, cerita, motivasi, dukungan dan waktu dari masa SMA hingga sekarang.
11. Teman-teman seperjuangan di masa perkuliahan, Fany, Nona dan Agista yang menjadi tempat curhat penulis dan selalu menemani, membantu, memberi dukungan, tawa, warna, kasih sayang dan motivasi pada masa perkuliahan penulis.
Penulis menyadari bahwa penulisan skripsi ini masih banyak terdapat kekurangan. Oleh karena itu penulis mengharapkan kritik dan saran yang membangun demi kebaikan penelitian di kemudian hari. Semoga naskah skripsi ini dapat bermanfaat dan menambah ilmu pengetahuan serta wawasan bagi pembaca.
Yogyakarta, 12 Januari 2021
Penulis
ix
DAFTAR ISI
HALAMAN JUDUL ...i
HALAMAN PERSETUJUAN PEMBIMBING ... ii
HALAMAN PENGESAHAN ... iii
PERNYATAAN KEASLIAN KARYA ...iv
HALAMAN PERSEMBAHAN ...vi
PRAKATA ... vii
DAFTAR ISI ...ix
DAFTAR TABEL ... x
DAFTAR GAMBAR ...xi
DAFTAR LAMPIRAN ... xii
ABSTRAK ...xiv
ABSTRACT ... xv
PENDAHULUAN ... 1
METODE PENELITIAN ... 4
Alat dan Bahan ... 4
Pemilihan dan pengumpulan sampel ... 4
Persiapan Sampel ... 5
Homogenisasi Sampel ... 5
Uji Angka Kapang/Khamir ... 6
Uji Angka Lempeng Total ... 7
Pengumpulan Data dan Analisis Hasil ... 8
HASIL DAN PEMBAHASAN ... 12
KESIMPULAN DAN SARAN ... 22
DAFTAR PUSTAKA ... 23
LAMPIRAN ... 26
BIOGRAFI PENULIS ... 75
x
DAFTAR TABEL
Tabel I. Hasil rata-rata nilai ALT pada ketiga sampel ... 17 Tabel II. Hasil rata-rata nilai AKK pada ketiga sampel ... 21
xi
DAFTAR GAMBAR
Gambar 1. Kontrol Pengencer dan Kontrol Media Uji ALT……….…16 Gambar 2. Kontrol Pengencer dan Kontrol Media Uji AKK………..……..20
xii
DAFTAR LAMPIRAN
Lampiran 1. Sampel jamu serbuk temulawak dalam wadah ... 27
Lampiran 2. Nilai ALT sampel A ... 27
Lampiran 3. Perhitungan ALT sampel A Replikasi 1 ... 28
Lampiran 4. Perhitungan ALT sampel A Replikasi 2 ... 29
Lampiran 5. Perhitungan ALT sampel A Replikasi 3 ... 30
Lampiran 6. Perhitungan SD dan CV ALT Sampel A ... 31
Lampiran 7. Nilai ALT sampel B ... 32
Lampiran 8. Perhitungan ALT sampel B Replikasi 1 ... 33
Lampiran 9. Perhitungan ALT sampel B Replikasi 2 ... 34
Lampiran 10. Perhitungan ALT sampel B Replikasi 3 ... 35
Lampiran 11. Perhitungan SD dan CV ALT Sampel B ... 36
Lampiran 12. Nilai ALT sampel C ... 37
Lampiran 13. Perhitungan ALT sampel C Replikasi 1 ... 38
Lampiran 14. Perhitungan ALT sampel C Replikasi 2 ... 39
Lampiran 15. Perhitungan ALT sampel C Replikasi 3 ... 40
Lampiran 16. Perhitungan SD dan CV ALT Sampel C ... 41
Lampiran 17. Nilai AKK sampel A ... 42
Lampiran 18. Perhitungan AKK sampel A Replikasi 1 ... 43
Lampiran 19. Perhitungan AKK sampel A Replikasi 2 ... 44
Lampiran 20. Perhitungan AKK sampel A Replikasi 3 ... 45
Lampiran 21. Perhitungan SD dan CV ALT Sampel A ... 46
Lampiran 22. Nilai AKK sampel B... 47
Lampiran 23. Perhitungan AKK sampel B Replikasi 1 ... 48
Lampiran 24. Perhitungan AKK sampel B Replikasi 2 ... 49
Lampiran 25. Perhitungan AKK sampel B Replikasi 3 ... 50
Lampiran 26. Perhitungan SD dan CV ALT Sampel B ... 51
Lampiran 27. Nilai AKK sampel C... 52
Lampiran 28. Perhitungan AKK sampel C Replikasi 1 ... 53
Lampiran 29. Perhitungan AKK sampel C Replikasi 2 ... 54
Lampiran 30. Perhitungan AKK sampel C Replikasi 3 ... 55
Lampiran 31. Perhitungan SD dan CV ALT Sampel A ... 56
Lampiran 32. Hasil ALT sampel A Replikasi 1 ... 57
Lampiran 33. Hasil ALT sampel A Replikasi 2 ... 58
Lampiran 34. Hasil ALT sampel A Replikasi 3 ... 59
Lampiran 35. Hasil ALT sampel B Replikasi 1 ... 60
Lampiran 36. Hasil ALT sampel B Replikasi 2 ... 61
Lampiran 37. Hasil ALT sampel B Replikasi 3 ... 62
Lampiran 38. Hasil ALT sampel C Replikasi 1 ... 63
Lampiran 39. Hasil ALT sampel C Replikasi 2 ... 64
Lampiran 40. Hasil ALT sampel C Replikasi 3 ... 65
Lampiran 41. Hasil AKK sampel A Replikasi 1 ... 66
Lampiran 42. Hasil AKK sampel A Replikasi 2 ... 67
Lampiran 43. Hasil AKK sampel A Replikasi 3 ... 68
Lampiran 44. Hasil AKK sampel B Replikasi 1 ... 69
xiii
Lampiran 45. Hasil AKK sampel B Replikasi 2 ... 70
Lampiran 46. Hasil AKK sampel B Replikasi 3 ... 71
Lampiran 47. Hasil AKK sampel C Replikasi 1 ... 72
Lampiran 48. Hasil AKK sampel C Replikasi 2 ... 73
Lampiran 49. Hasil AKK sampel C Replikasi 3 ... 74
xiv
ABSTRAK
Jamu serbuk temulawak merupakan jamu yang memiliki banyak manfaat dan dapat digunakan untuk mengobati banyak penyakit, termasuk memiliki efek antimikroba, anti inflamasi. Kandungan minyak astiri pada temulawak juga bersifat antibakteri dan antipiretik. Selain itu temulawak juga mempunyai khasiat yaitu, untuk memperlancar ASI, mengobati asma dan meredakan nyeri haid. Penelitian ini bertujuan untuk mengetahui Angka Kapang Khamir (AKK) dan Angka Lempeng Total (ALT) dalam jamu serbuk temulawak dari tiga penjual jamu dengan merk yang sama, pengambilan sampel dilakukan dengan sistem kluster, dimana dipilih tiga penjual jamu dari beberapa penjual jamu di pasar Beringharjo Yogyakarta dan mengetahui apakah nilai AKK dan ALT jamu serbuk temulawak yang dijual di pasar Beringharjo Yogyakarta memenuhi persyaratan berdasarkan KaBPOM Nomor 12 tahun 2014 yang menyatakan bahwa AKK yang diperbolehkan ≤ 104 koloni/g dan ALT yang diperbolehkan ≤ 106 koloni/g. Penelitian ini merupakan penelitian non eksperimental dengan rancangan penelitian deskriptif komparatif. Tahapan penelitian yang dilakukan meliputi penentuan dan pemilihan tempat pengambilan sampel, pengambilan sampel, pengujian AKK, pengujian ALT dan analisis hasil pengujian dilakukan sesuai dengan ketentuan pada PPOMN tahun 2006. Hasil penelitian yang dilakukan pada jamu serbuk temulawak yang dijual di pasar Beringharjo Yogyakarta diperoleh nilai ALT sebesar 2,9 x 102 sampai dengan 1,8 x 102 koloni/g dan nilai AKK <10 koloni/g. Berdasarkan nilai tersebut ALT dan AKK pada sampel jamu serbuk temulawak memenuhi syarat Peraturan Kepala Badan Pengawasan Obat Dan Makanan Republik Indonesia Nomor 12 Tahun 2014 Tentang Persyaratan Mutu Obat Tradisional.
Kata kunci : Angka Kapang Khamir, Angka Lempeng Total, Obat Tradisioanl, Jamu serbuk, (Curcuma xanthorrhiza Roxb.).
xv
ABSTRACT
Jamu serbuk temulawak is medicine has many benefits and can be used to treat many diseases, including having antimicrobial and anti-inflammatory effects. The essential oil content in ginger is also antibacterial and antipyretic. Temulawak also has properties to facilitate breastfeeding, treat asthma and relieve menstrual pain. This study aims to determine the value of Mold/Yeast Count (MYC) and Total Plate Count (TPC) in jamu serbuk temulawak from three herbal medicine sellers with the same brand, sampling is done using a cluster system, where three herbal medicine sellers are selected from several herbal medicine sellers in the Beringharjo market in Yogyakarta and find out whether the Mold/Yeast Count (MYC) and Total Plate Count (TPC) values of the jamu serbuk temulawak that are sold in the Beringharjo market in Yogyakarta meet the requirements based on KaBPOM Number 12 of 2014 which states that the allowable MYC is ≤ 104 colonies / g and the allowed TPC is ≤ 106 colonies / g. This research is an experimental study with a comparative descriptive research design. The stages of the research carried out included determining and selecting a sampling site, sampling, MYC testing, TPC testing and analysis of the test results carried out in accordance with the provisions of the 2006 PPOMN. The results of research conducted on jamu serbuk temulawak sold in the Beringharjo market in Yogyakarta obtained TPC values of 2.9 x 102 to 1.8 x 102 colonies/g and MYC values <10 colonies/g. Based on these values, TPC and MYC in the sample of jamu serbuk temulawak meet the requirements of the Regulation of the Head of the Food and Drug Administration of the Republic of Indonesia Number 12 of 2014 concerning Quality Requirements for Traditional Medicines.
Keywords: jamu serbuk temulawak, total plate count, mold / yeast count
1
PENDAHULUAN
Indonesia merupakan negara yang memiliki kekayaan hayati yang cukup besar yang dapat dikembangkan terutama untuk obat tradisional, obat tradisional merupakan bahan atau ramuan bahan berupa bahan tumbuhan, bahan hewan, bahan mineral, sediaan sarian atau galenik, atau campuran dari bahan tersebut, yang secara turun temurun telah digunakan untuk pengobatan berdasarkan pengalaman. Obat tradisional telah diterima secara luas di negara berkembang dan di negara maju.
Faktor pendorong peningkatan penggunaan obat herbal di negara maju diantaranya adalah usia harapan hidup yang lebih panjang terus meningkat, adanya kegagalan dalam penggunaan obat sintetik atau modern untuk penyakit tertentu seperti kanker, serta semakin luasnya akses informasi mengenai obat tradisional (Wasito, 2011).
Menurut Riskesdas 2018, pada tahun 2009 penduduk Indonesia melakukan pengobatan sendiri menggunakan obat tradisional sebesar 15,04%, sedangkan pada tahun 2010 mengalami peningkatan sebanyak dua kali lipat, yaitu 31,7% dan meningkat menjadi 41,7% pada tahun 2012. Pada tahun 2013 dari 294.692 rumah tangga di Indonesia yang memanfaatkan pelayanan kesehatan tradisional (yankestrad) dalam satu tahun terakhir berjumlah 30,4% (89.753). Sedangkan pada tahun 2018 berjumlah 31,4%. Pada tahun 2018 proporsi jenis pelayanan kesehatan tradisional yang dimanfaatkan khususnya ramuan jadi menurut data rata-rata dari tiap provinsi di Indonesia sebesar 48% (MENKES RI, 2018).
Obat Bahan Alam Indonesia berdasarkan perbedaan cara pembuatan serta jenis klaim penggunaan dan tingkat pembuktian khasiat dapat dikelompokkan menjadi tiga golongan, yaitu jamu, obat herbal terstandar, dan fitofarmaka (BPOM RI, 2004). Jamu merupakan sebagian besar produk obat tradisional yang terdaftar di Badan POM RI dimana khasiat dan keamanannya hanya didasarkan pada penggunaan empiris secara turun-temurun. Jamu masih banyak digunakan untuk pengobatan alternatif karena pembuatannya berasal dari bahan herbal dan harganya pun masih relatif murah (Wasito, 2011).
Jamu harus memenuhi kriteria aman sesuai dengan persyaratan yang ditetapkan, klaim khasiat dibuktikan berdasarkan data empiris dan memenuhi persyaratan umum mutu yang berlaku. Jamu sudah menjadi budaya masyarakat
2
Indonesia dibuktikan dengan perkembangan pelayanan kesehatan tradisional menggunakan ramuan saat ini semakin pesat, terbukti dari hasil Riskesdas 2010, bahwa persentase penduduk Indonesia yang pernah mengonsumsi jamu sebanyak 59,12 % yang terdapat pada semua kelompok umur, baik laki-laki maupun perempuan, di pedesaan maupun di perkotaan. Data Riskesdas ini menunjukkan bahwa, jamu sebagai bagian dari pengobatan tradisional, telah diterima oleh masyarakat Indonesia (MENKES RI, 2016).
Masyarakat Indonesia sudah lama menggunakan ramuan obat tradisional sebagai upaya pemeliharaan kesehatan, pencegahan penyakit, dan perawatan kesehatan. Ramuan obat tradisional Indonesia tersebut umumnya berasal dari tumbuhan dengan bentuk sediaan yang paling banyak disukai adalah cairan, diikuti berturut-turut seduhan/serbuk, rebusan/rajangan, dan bentuk kapsul/pil/tablet (MENKES RI, 2016). Bentuk sediaan kering dari obat tradisional yang banyak beredar di pasaran adalah dalam bentuk serbuk yang merupakan sediaan obat tradisional berupa butiran homogen dengan derajat halus yang sesuai, terbuat dari simplisia atau campuran dengan ekstrak yang cara penggunaannya diseduh dengan air panas (BPOM RI, 2019). Jamu serbuk memiliki kelebihan yaitu bersifat praktis dan cepat dalam penyajiannya, serta memiliki daya simpan yang relatif lama (Ismono, Suyanto, Hidajati, 2018).
Salah satu komoditas rimpang yang banyak digunakan sebagai pengobatan, bahan baku dalam industri jamu dan farmasi karena memiliki banyak manfaat dan khasiat adalah temulawak (Curcuma xanthorrhiza Roxb.). Beberapa penelitian yang telah dilakukan menemukan bahwa di dalam temulawak terdapat senyawa curcuminoids (terdiri dari kurkumin dan demetoksikurkumin) dan minyak astiri yang diketahui mempunyai aktivitas antioksidan (Nurcholis et al., 2012). Selain itu, temulawak juga mengandung senyawa minyak astiri seperti isofuranogermakren, trisiklin, germakren, allo-aromadendren dan xanthorrizol. Temulawak berkhasiat sebagai penurun kolesterol, nyeri haid, penambah nafsu makan, perut kembung, demam, kanker, wasir, jerawat dan diare (Wasito, 2011). Kandungan minyak astiri pada temulawak juga bersifat antibakteri dan antipiretik (Latief, 2009). Selain itu,
3
temulawak juga mempunyai khasiat yaitu untuk memperlancar ASI, mengobati asma dan meredakan nyeri haid (Nurmalia, 2012).
Proses pembuatan jamu yang meliputi pemilihan bahan baku, pencucian, pengolahan dan penyajian dengan cara yang masih sangat sederhana tidak menutup kemungkinan apabila jamu-jamu tersebut tercemar oleh mikroorganisme (Susanti, Emma, Riza, 2017). Adanya kontaminasi kapang toksik pada jamu serbuk dapat memberikan efek negatif bagi penggunanya. Salah satunya yaitu adanya mikotoksin yang dihasilkan oleh kapang kontaminan pada jamu serbuk. Mikotoksin sebagai racun dapat bersifat teratogenik, karsinogenik dan mutagenik (Dion dan Susiana, 2020).
Jamu serbuk yang beredar dan dikonsumsi oleh masyarakat harus memenuhi standar kualitas dan keamanannya secara mikrobiologis untuk dikonsumsi. Persyaratan mutu termasuk bahan baku dan produk jadi, sebagaimana termasuk dalam Farmakope Herbal Indonesia, Materia Medika Indonesia, standar persyaratan farmakope negara lain atau referensi ilmiah yang diakui. Sesuai Peraturan Kepala Badan Pengawas Obat dan Makanan Republik Indonesia Nomor 12 Tahun 2014 tentang Persyaratan Mutu Obat Tradisional yang menyatakan bahwa persyaratan mutu dalam jamu serbuk seduhan yaitu cemaran mikroba ALT yang diperbolehkan adalah ≤ 𝟏𝟎𝟔 koloni/g dan AKK yang diperbolehkan adalah ≤ 𝟏𝟎𝟒 koloni/g (BPOM RI, 2014). Angka Lempeng Total dan Angka Kapang Khamir digunakan sebagai perameter keamanan produksi dari obat tradisional. Semakin kecil ALT dan AKK dalam sebuah sediaan jamu menunjukkan semakin aman jamu tersebut dan semakin tinggi nilai penerapan Cara Pembuatan Obat Tradisional yang Baik dalam pembuatan obat tradisional tersebut (Wasito, 2011).
Berdasarkan beberapa uraian di atas, peneliti ingin melakukan penelitian lebih lanjut terhadap nilai ALT dan AKK pada sediaan jamu serbuk temulawak, dengan tempat pengambilan sampel yang berbeda di pasar Beringharjo Yogyakarta.
Penelitian ini bertujuan untuk meneliti nilai cemaran mikroba yang meliputi ALT dan AKK pada jamu serbuk temulawak yang di jual oleh penjual jamu di pasar Beringharjo Yogyakarta, sehingga dapat diketahui apakah produk jamu serbuk
4
temulawak yang dijual oleh penjual jamu tersebut sudah memenuhi persyaratan mikrobiologis antara lain ALT dan AKK.
METODE PENELITIAN Bahan
Bahan-bahan yang digunakan dalam penelitian ini antara lain jamu serbuk temulawak yang dijual oleh penjual jamu di pasar tradisional Beringharjo Yogyakarta, Potato Dextrose Agar (PDA), Plate Count Agar (PCA), Kloramfenikol 1%, Buffered Peptone Water (BPW), aquades steril, alkohol 70%
Alat
Autoklaf, laminar air flow (LAF), bio safety cabinet (BSC), inkubator, oven, stomacher 400 circulator, alat-alat gelas (Pyrex®) berupa gelas beker, corong, gelas ukur, pipet tetes, tabung reaksi dilengkapi tabung durham, cawan petri, pipet volume, erlenmeyer, batang pengaduk, bunsen, stirer magnetik, neraca analitik (Mettler AE 200), micropipette, pipette tipcone, bunsen, neraca analitik, colony counter, hot plate.
Tata Cara Penelitian
1. Pemilihan dan pengumpulan sampel
Sampel jamu serbuk yang dipilih diambil dari jamu serbuk temulawak yang dijual di pasar Beringharjo Yogyakarta. Di pasar Beringharjo terdapat blok yang khusus menjual obat tradisional, dalam blok tersebut terdapat 3 baris toko dengan total 24 toko yang menjual obat tradisional dalam bentuk rajangan simplisia, serbuk simplisia, jamu serbuk seduhan, dan kemasan obat tradisional lainnya. Dari total 24 toko tersebut terdapat 12 toko yang menjual jamu serbuk temulawak yang diproduksi oleh produsen X. Kemudian diambil 9 sampel jamu serbuk temulawak dari 3 toko obat tradisional, dari masing-masing baris dipilih 1 toko obat tradisional yang berbeda. Pengambilan sampel dilakukan dengan sistem kluster, dimana penarikan sampel secara acak pada individu dalam populasi.
Dipilih sejumlah tiga sampel karena dalam pasar tersebut terdapat tiga baris toko untuk penjual jamu serbuk. Sehingga untuk setiap baris toko diambil
5
satu sampel untuk mewakili keseluruhan penjual jamu yang berada pada baris toko tersebut, kemudian dilakukan replikasi sebanyak tiga kali.
Sampel jamu serbuk selanjutnya disimpan dalam wadah yang sebelumnya telah dibersihkan menggunakan alkohol, kering dan tertutup rapat serta dimasukkan dalam coolbox dan dibawa ke laboratorium untuk diteliti.
2. Sterilisasi Alat, Media dan Ruangan
Sterilisasi dilakukan menggunakan autoklaf pada suhu 121°C selama 15 menit. Pada penelitian ini steriliasi media dan peralatan yang digunakan seperti benda-benda kaca atau cawan petri yang sebelumnya telah dibungkus menggunakan kertas coklat dilakukan secara terpisah menggunakan autoklaf (Radji, 2009). Sterilisasi meja kerja dilakukan dengan menyemprotkan alkohol 70% kemudian dilap satu arah menggunakan tissue/lap.
3. Persiapan Sampel
Persiapan sampel sampai dengan Uji ALT dan AKK dilakukan di Biological Safety Cabinet (BSC). Sebanyak 9 botol plastik jamu serbuk temulawak dibersihkan dengan kapas beralkohol 70% kemudian dibuka secara aseptis.
4. Uji Angka Kapang Khamir
a. Homogenisasi sampel untuk uji AKK
Diambil sebanyak tiga per empat sendok sampel dari masing- masing botol jamu serbuk temulawak, kemudian masing-masing serbuk temulawak dilarutkan dengan 100 ml aquadest panas dan dihomogenkan. Sebanyak 1 ml jamu temulawak diambil dan dimasukkan kedalam labu ukur 10 ml kemudian ditambah larutan pengencer BPW hingga tanda batas sehingga diperoleh pengenceran 10-1.
b. Pembuatan pengencer BPW (Buffered Pepton Water)
Sebanyak 6,37 g serbuk BPW ditimbang dan dilarutkan dalam 250 mL aquadest steril, kemudian dipanaskan dan diaduk dengan hot
6
plate dan magnetic stirer hingga larutan jernih. Sterilisasi dengan autoklaf selama 15 menit pada suhu 121oC.
c. Pengenceran sampel untuk uji AKK
Tiga buah labu ukur 10 ml disiapkan, masing-masing telah diisi dengan 9 ml BPW. Dipipet 1 ml sampel pengenceran 10-1 dan dimasukkan kedalam tabung pertama yang telah berisi BPW hingga diperoleh pengenceran 10-2 lalu dikocok homogen dengan vortex.
Dibuat pengenceran berikutnya sampai 10-4. d. Pembuatan Larutan Kloramfenikol
Sebanyak 1 gram kloramfenikol dilarutkan ke dalam 100 ml aquadest steril.
e. Pembuatan Larutan Media Potato Dextrose Agar (PDA)
Sebanyak 29 gram serbuk PDA disuspensikan dalam 1000 mL aquadest steril, kemudian dilarutkan dengan pemanasan menggunakan hot plate dan magnetic steerer diaduk hingga larutan jernih, kemudian dimasukkan dalam tabung reaksi steril. Sterilisasi dengan autoklaf selama 15 menit pada suhu 121oC.
f. Uji Angka Kapang Khamir
Dari masing-masing pengenceran dipipet 1 ml ke dalam cawan petri steril secara duplo. Selanjutnya sebanyak 20 mL media PDA dituangkan ke dalam cawan petri yang sebelumnya telah ditambah dengan 1 ml larutan kloramfenikol dan diputar ke depan dan ke belakang agar dapat tercampur merata dan didiamkan hingga memadat. Setelah memadat cawan petri dibalik dan diinkubasikan pada suhu 35 - 37oC atau pada suhu kamar selama 5 hari. Koloni kapang dan khamir dihitung setelah 5 hari. Uji sterilitas media dilakukan dengan menuangkan media PDA dalam cawan petri dan dibiarkan memadat. Uji sterilitas pengencer dilakukan dengan cara menuangkan media PDA dan 1 ml pengencer (BPW) lalu dibiarkan memadat.
7
5. Uji Angka Lempeng Total
a. Pembuatan Media Plate Count Agar (PCA)
Sebanyak 29 g PCA ditimbang dan di campurkan dengan 1650 ml aquadest, dipanaskan hingga larutan jernih. Kemudian disterilkan dengan autoklaf selama 15 menit pada suhu 121oC.
b. Pembuatan Larutan Pengencer Buffered Pepton Water (BPW) Sebanyak 6,37 g serbuk BPW dilarutkan dalam 250 ml aquadest steril, kemudian dilarutkan ke dalam Erlenmeyer menggunakan magnetic steerer. Sterilisasi dengan menggunakan autoklaf selama 15 menit pada suhu 121oC.
c. Homogenisasi sampel untuk uji ALT
Secara aseptis diambil sebanyak 1 ml sampel kedalam labu ukur 10 ml, lalu ditambahkan 9 ml BPW dan homogenkan hingga diperoleh pengenceran 10-1.
d. Pengenceran sampel untuk uji ALT
Sebanyak 5 buah labu ukur 10 ml disiapkan masing-masing telah diisi dengan 9 ml pengencer BPW. Dipipet 1 ml pengenceran 10-1 dari hasil homogenisasi pada penyiapan sampel dan dimasukkan ke dalam tabung pertama yang telah diisi 9 ml BPW hingga diperoleh pengenceran 10-2 dan dihomogenkan dengan menggunakan vortex. Kemudian dibuat pengenceran selanjutnya hingga 10-6 (PPOMN, 2006).
e. Uji Angka Lempeng Total
Dari masing-masing pengenceran dipipet 1 ml kedalam cawan petri steril secara duplo. Dalam setiap cawan petri dituangkan sebanyak 15 ml media PCA yang masih cair. Cawan petri digoyangkan membentuk angka delapan dengan hati-hati agar sampel tersebar merata kemudian dibuat duplo. Dilakukan pula uji kontrol untuk mengetahui sterilitas media dan pengencer. Uji sterilitas media dilakukan dengan cara menuangkan media PCA dalam suatu cawan petri dan biarkan memadat.
8
Seluruh cawan petri diinkubasi terbalik pada suhu 37oC selama 24 jam hingga 48 jam. Jumlah koloni yang tumbuh diamati dan dihitung.
(PPOMN, 2006).
6. Teknik Pengumpulan Data dan Analisis Hasil a.) Uji Angka Kapang Khamir
Cara menganalisis hasil pengujian untuk nilai AKK sesuai dengan ketentuan PPOMN (2006), yaitu : cawan petri yang menunjukkan jumlah koloni antara 10-150 dari satu pengenceran dipilih dan dihitung jumlah koloni dari kedua cawan lalu dikalikan dengan faktor pengencerannya. Bila pada cawan petri dari dua tingkat pengenceran yang berurutan menunjukkan jumah antara 10-150, maka dihitung jumlah koloni dan dikalikan dengan faktor pengenceran, kemudian diambil anhka rata-rata. Hasil dikalikan sebagai AKK dalam tiap gram atau mililiter sampel.
Beberapa kemungkinan lain yang berbeda dari pernyataan diatas, maka diikuti petunjuk sebagai berikut :
a. Bila hanya salah satu diantara kedua cawan petri dari pengenceran yang menunjukkan jumlah antara 10-150 koloni, dihitung jumlah koloni dari kedua cawan dan dikalikan dengan faktor pengenceran.
b. Bila pada tingkat pegenceran yang lebih tinggi didapat jumlah koloni lebih besar dari dua kali jumlah koloni pada pengenceran dibawahnya, maka dipilih tingkat pengenceran terendah (Misal:
pada pengenceran 10−2 diperoleh 60 koloni dan pada pengenceran 10−3 diperoleh 30 koloni, maka dipilih jumlah koloni pada pengenceran 10−2 yaitu 60 koloni. Bila pada pengenceran yang lebih tinggi didapat jumlah koloni kurang dari dua kali jumlah koloni pengenceran dibawahnya, maka diambil angka rata-rata dari jumlah koloni kedua pengenceran tersebut. Hasil dinyatakan sebagai AKK dalam tiap gram sampel
9
(Misal pada pengenceran 10−2 diperoleh 60 koloni dan pada pengenceran 10−3 diperoleh 10 koloni, maka AKK adalah:
6+10
2 x 103 = 8 x 103)
c. Bila dari seluruh cawan petri tidak ada satupun yang menunjukkan jumlah antara 10-150 koloni, maka dicatat angka sebenarnya dari tingkat pengenceran terendah dan dihitung sebagai AKK perkiraan.
d. Bila tidak ada pertumbuhan pada semua cawan dan bukan disebabkan karena faktor inhibitor, maka AKK dilaporkan sebagai kurang dari satu dikalikan faktor pengenceran terendah (<1 x faktor pengenceran terendah)
b.) Uji Angka Lempeng Total
Cara menganalisis hasil pengujian sesuai untuk nilai ALT sesuai dengan ketentuan PPOMN (2006), yaitu :
a. Pilih cawan petri dari satu pengenceran yang menunjukkan jumlah koloni antara 25-250 setiap cawan. Semua koloni dalam cawan petri dihitung dengan menggunakan alat penghitung koloni (Colony counter). Jumlah koloni dihitung rata-rata dan dikalikan dengan faktor pengenceran. Hasilnya dinyatakan sebagai jumlah bakteri per mililiter atau gram.
b. Jika salah satu dari dua cawan petri terdapat jumlah koloni lebih kecil dari 25 atau lebih besar dari 250, dihitung rata-rata jumlah koloni dan dikalikan dengan faktor pengenceran. Hasilnya dinyatakan sebagai jumlah bakteri per mililiter atau gram.
c. Jika hasil dari dua pengenceran jumlahnya berturut-turut terletak antara 25-250 koloni, jumlah koloni dari masing-masing pengenceran dihitung seperti yang pada poin a dan poin b diatas, dan dihitung rata-rata jumlah koloni dari kedua pengenceran tersebut. Jika jumlah yang tertinggi lebih besar dari dua kali jumlah yang terkecil, dinyatakan jumlah yang lebih kecil sebagai jumlah bakteri per mililiter atau gram.
10
d. Jika rata-rata jumlah koloni masing-masing cawan petri tidak terletak antara 25-250 koloni, dihitung jumlah koloni seperti pada poin a dan poin b diatas, dan dinyatakan sebagai jumlah bakteri per mililiter atau gram
e. Jika jumlah koloni dari semua pengenceran lebih dari 250 koloni, maka setiap dua cawan petri dengan pengenceran tertinggi dibagi ke dalam 2, 4, atau 8 sektor. Jumlah koloni dihitung dalam satu bagian atau lebih. Untuk mendapatkan jumlah koloni dalam satu cawan petri, dihitung rata-rata jumlah koloni dan dikalikan dengan faktor pembagi dan pengencer. Hasil dinyatakan sebagai jumlah bakteri perkiraan per mililiter atau gram.
f. Jika dalam 1/8 bagian cawan petri terdapat lebih dari 200 koloni, maka jumlah koloni yang didapat = 8 x 200 (1600), dikalikan dengan faktor pengenceran dan hasilnya dinyatakan sebagai jumlah bakteri perkiraan per mililiter atau gram lebih besar dari jumlah yang didapat (>1600 x faktor pengenceran).
g. Jika tidak ada koloni yang tumbuh dalam cawan petri, dinyatakan jumlah bakteri perkiraan lebih kecil dari satu dikalikan dengan faktor pengenceran yang terendah (<10).
h. Menghitung koloni perambat (spreader)
Ada 3 macam koloni perambatan pada koloni, yaitu : i. Merupakan rantai yang tidak terpisah-pisah
ii. Perambatan yang terjadi diantara dasar cawan petri dan perbenihan
iii. Perambatan yang terjadi pada pinggir atau permukaan perbenihan
Jika terjadi hanya 1 perambatan (seperti rantai) maka koloni dianggap 1. Tetapi jika 1 atau lebih rantai terbentuk dan yang berasal dari sumber yang terpisah-pisah, maka setiap sumber dihitung sebagai 1 koloni. Bila (2) dan (3) terjadi maka sebaiknya
11
pemeriksaan diulangi karena koloni dalam keadaan semacam ini agak sulit dihitung
i. Menghitung dan membulatkan angka
Dalam melaporkan jumlah koloni atau jumlah koloni perkiraan hanya 2 angka penting yang digunakan, yaitu angka yang pertama dan kedua (dimulai dari kiri), sedangkan angka ketiga diganti dengan 0, apabila < 5 dan apabila 5 atau lebih dijadikan 1 yang ditambah pada angka yang kedua.
Contoh : 523.000 dilaporkan sebagai 520.000 (5,2 x 105) 86.300 dilaporkan sebagai 84.000 (8,4 x 104)
(PPOMN, 2006).
12
HASIL DAN PEMBAHASAN
Jamu telah dikenal masyarakat secara turun temurun, umumnya jamu dimanfaatkan sebagai preventif untuk menjaga kesehatan dan pengobatan suatu penyakit, karena efek samping yang ditimbulkan relatif kecil, praktis, aman dan harga yang terjangkau (Afifi, 2016). Jamu serbuk yamg beredar dan dikonsumsi oleh masyarakat harus memenuhi standar kualitas dan keamanannya secara mikrobiologis untuk dikonsumsi. Salah satu parameter jaminan keamanan dan mutu dari cairan obat dalam adalah nilai Angka Lempeng Total (ALT) dan Angka Kapang Khamir (AKK). Hal tersebut diatur dalam Peraturan Kepala Badan Pengawas Obat dan Makanan Republik Indonesia Nomor 12 Tahun 2014 tentang Persyaratan Mutu Obat Tradisional menyatakan bahwa persyaratan mutu untuk nilai ALT jamu serbuk seduhan adalah ≤ 106 koloni/g, sedangkan untuk nilai AKK jamu serbuk seduhan yaitu ≤ 104 koloni/g.
Pemilihan dan Pengambilan Sampel
Sampel jamu serbuk yang digunakan dalam penelitian ini adalah jamu serbuk temulawak produksi X yang dijual di pasar Beringharjo Yogyakarta. Jamu temulawak dipilih berdasarkan persentasi penggunaan tanaman obat di Indonesia dalam Formularium Obat Herbal Asli Indonesia yang menunjukkan bahwa temulawak masuk dalam daftar tanaman obat yang paling diminati untuk dikonsumsi. Temulawak berkhasiat sebagai penambah nafsu makan, penurun kolesterol, untuk memperlancar ASI, perut kembung, mengobati asma dan meredakan nyeri haid (Wasito, 2011).
Pasar Beringharjo dipilih sebagai tempat pengambilan sampel karena merupakan pasar pusat penjualan bahan baku jamu seperti rimpang, simplisia dan serbuk simplisia. Selain itu Pasar Beringharjo berada di pusat kota dan merupakan pasar terbesar di Yogyakarta. Pasar Beringharjo memiliki blok yang khusus menjual obat tradisional, dalam blok tersebut terdapat 3 baris toko yang menjual obat tradisional, kemudian diambil 9 sampel jamu serbuk temulawak dari 3 toko obat tradisional secara acak. Pengambilan sampel dilakukan dengan sistem kluster, dimana penarikan sampel secara acak pada individu dalam populasi. Dipilih sejumlah tiga sampel karena dalam pasar tersebut terdapat tiga baris toko untuk
13
penjual jamu serbuk. Sehingga untuk setiap baris toko diambil satu sampel untuk mewakili keseluruhan penjual jamu yang berada pada baris toko tersebut, kemudian dilakukan replikasi sebanyak tiga kali yang dianggap dapat mempresentasikan penjual obat tradisional di pasar tersebut. Sampel jamu serbuk selanjutnya disimpan dalam wadah yang sebelumnya telah dibersihkan menggunakan alkohol, kering dan tertutup rapat serta dimasukkan dalam coolbox dan dibawa ke laboratorium untuk diteliti.
Sterilisasi Alat, Media, dan Ruangan
Sterilisasi adalah proses penghilangan atau membunuh mikroorganisme (protozoa, fungi, bakteri, mycoplasma, virus) dalam benda/peralatan untuk menjaga peralatan dilaboratorium tetap bersih/steril, serta mencegah terjadinya kontaminasi (Istini, 2020). Peralatan yang digunakan dalam penelitian ini seperti benda-benda kaca atau cawan dibungkus menggunakan kertas coklat kemudian disterilisasi menggunakan autoklaf pada suhu 121°C selama 15 menit (Radji, 2009). Media yang telah dicampur dengan aquadest dan dihomogenkan hingga jernih diatas hotplate menggunakan stirrer, disterilisasi menggunakan autoklaf pada suhu 121°C selama 15 menit.
Sterilisasi menggunakan panas lembab (tekanan uap dalam autoklaf) dapat membunuh mikroorganisme karena dapat menyebabkan denaturasi protein, termasuk enzim-enzim didalam sel (Istini, 2020). Autoklaf adalah alat untuk mensterilkan berbagai macam alat dan bahan yang digunakan dalam mikrobiologi menggunakan uap air panas bertekanan. Autoklaf ditujukan untuk membunuh endospora, karena sel ini dapat dibunuh pada suhu 100oC yang merupakan titik didih air pada tekanan atmosfer normal. Pada suhu 121oC, endospora dapat dibunuh dalam waktu 4-5 menit (Djais dan Theodorea, 2019). Tekanan yang digunakan pada umumnya 15 Psi atau sekitar 2 atm dan dengan suhu 121oC. Mekanisme kerusakan oleh panas ini ditandai dengan rusaknya produksi rantai tunggal DNA akibat tekanan tinggi yang menyebabkan penetrasi uap air ke dalam sel-sel mikroba menjadi optimal sehingga langsung mematikan mikroba (Dewi dkk, 2017).
Sterilisasi ruangan dilakukan dengan menyemprotkan alkohol 70% pada meja kerja kemudian dilap satu arah menggunakan tissue/lap.
14
Persiapan Sampel
Kemasan jamu serbuk temulawak dibersihkan dengan alkohol 70%
kemudian dibuka secara aseptis. Jamu serbuk temulawak kemudian diambil dan dilarutkan dengan aquadest steril.
Homogenisasi Sampel
Homogenisasi sampel merupakan tahap awal dalam pengujian yang berguna untuk membebaskan sel bakteri yang mungkin terlindung partikel sampel dan untuk memperoleh distribusi bakteri sebaik mungkin (Afifi dan Sugiarti, 2016).
Homogenisasi sampel dilakukan dengan mencampur 1 ml larutan jamu temulawak dan dimasukkan kedalam labu ukur 10 ml kemudian ditambah larutan pengencer BPW hingga tanda batas sehingga diperoleh pengenceran 10-1 .
Pengenceran Sampel
Pengenceran adalah proses melarutkan atau melepaskan mikroba dari substratnya kedalam air sehingga penanganannya lebih mudah. Pengenceran dilakukan untuk menurunkan atau memperkecil konsentrasi larutan dengan menambah zat pelarut kedalam larutan sehingga volume larutan menjadi berubah (Afifi dan Sugiarti, 2016).
Pada penelitian ini pengenceran dilakukan dengan mengambil 1 ml dari pengenceran 10-1 dan ditambahkan 9 ml larutan pengencer, sehingga diperoleh pengenceran 10-2 lalu dihomogenkan menggunakan vortex. Pengenceran pada uji ALT dilakukan sampai 10-4, sedangkan pengenceran pada uji AKK dilakukan sampai 10-6. Pengencer yang digunakan pada uji ALT dan AKK adalah BPW (Buffered Peptone Water). BPW memiliki kandungan utama berupa peptone yang merupakan protein yang berperan sebagai sumber nutrisi. BPW juga berfungsi sebagai buffer yang digunakan untuk mempertahankan pH optimum untuk pertumbuhan bakteri yaitu pada pH 6,5-7,5. Kandungan pepton pada larutan BPW ini berfungsi sebagai sumber karbon, nitrogen, vitamin dan mineral bagi pertumbuhan bakteri. Selain itu kandungan NaCl pada larutan BPW berfungsi dalam menjaga keseimbangan osmotik medium pertumbuhan (Soesetyaningsih, Azizah, 2020).
15
Uji Angka Lempeng Total
Uji ALT merupakan suatu metode yang digunakan untuk menumbuhkan sel-sel mikroorganisme hidup pada media agar, sehingga mikroorganisme tersebut akan berkembang biak dan membentuk koloni yang dapat dilihat secara langsung dengan mata tanpa menggunakan mikroskop (Tyas, 2018). Prinsip dari ALT adalah menghitung pertumbuhan koloni bakteri aerob mesofil setelah sampel ditanam pada media yang sesuai dengan cara tuang (metode pour plate) kemudian diinkubasi selama 24-48 jam pada suhu 35-37oC. Angka Lempeng Total dapat dipergunakan sebagai indikator proses higine sanitasi produk, analisis mikroba lingkungan pada produk jadi, indikator proses pengawasan, dan digunakan sebagai dasar pertimbangan dapat atau tidak diterimanya suatu produk berdasarkan kualitas mikrobiologinya (Puspandari dan Isnawati, 2015). Nilai ALT yang melebihi ambang batas juga dapat membahayakan bagi konsumen, karena jika nilai ALT tinggi kemungkinan terdapat bakteri patogen diantaranya adalah Salmonella, E.coli dan Shigella. Salah satu penyakit yang disebabkan oleh bakteri patogen Salmonella adalah salmonelosis. Kaum lanjut usia dan orang yang memiliki sistem kekebalan tubuh yang kurang baik beresiko menderita salmonelosis. Manifestasi klinik salmonelosis antara lain deman enteric(demam thypoid), gastroenteritis dan septisema (Radji, 2010;Yonathan, 2013).
Kelangsungan hidup dan pertumbuhan mikroorganisme yang berkelanjutan tergantung pada suplai nutrisi yang memadai dan lingkungan pertumbuhan yang menguntungkan (Cappucino, 2011). Nutrisi yang dibutuhkan mikroorganisme untuk pertumbuhannya meliputi karbon, nitrogen, unsur non logam seperti sulfur dan fosfor, unsur logam seperti Ca, Zn, Na, K, Cu, Mn, Mg, dan Fe, vitamin, air, dan energi (Cappucino, 2014). Menurut Cappuccino (2011) media pertumbuhan dapat berupa media cair, semi-padat, ataupun padat. Proses pembuatan media harus dilakukan sterilisasi dan selalu menerapkan perilaku aseptis agar tidak ada kontaminan yang berasal dari media.
Media yang digunakan dalam uji ALT adalah Plate Count Agar (PCA).
Media PCA mengandung tryptone, yeast extract, glukosa dan agar dengan pH
16
7,0±0,2 yang berfungsi sebagai nutrisi untuk pertumbuhan bakteri dalam media.
Menurut Radji (2010), bakteri tumbuh optimum pada pH 6,5-7,5.
Pada uji ALT seri pengenceran dibuat hingga 10-6 dengan tujuan untuk mendapatkan koloni bakteri yang tumbuh terpisah dengan jumlah antara 25-250 yang tampak pada cawan petri setelah inkubasi, sehingga mempermudah perhitungan koloni. Jika pengenceran tidak dilakukan, maka koloni bakteri akan sangat pekat, sehingga perhitungan koloni akan sulit dilakukan. Masing-masing pengenceran dibuat duplo yang bertujuan untuk meningkatkan akurasi dalam perhitungan.
Pada penelitian ini juga dibuat kontrol media dan kontrol pengencer untuk mengetahui sterilitas media dan pengencer serta keaseptisan selama pengujian.
Kontrol media hanya berisi media PCA dengan tujuan untuk memastikan bahwa bakteri yang tumbuh nantinya murni berasal dari sampel dan bukan dari media.
Kontrol pengencer berisi media PCA dan pengencer BPW yang bertujuan untuk memastikan bahwa tidak terdapat kontaminan yang berasal dari pengencer BPW.
Gambar 1. Gambar Kontrol Pengencer dan Kontrol Media Uji ALT
Pada gambar 1 yaitu pada kontrol media dan kontrol pengencer tidak terdapat koloni bakteri yang tumbuh setelah diinkubasi pada suhu 37oC selama 24 jam. Hasil pengujian tersebut menunjukkan bahwa media PCA dan pengencer BPW yang digunakan tidak terkontaminsi mikroba, sehingga koloni bakteri yang tumbuh pada cawan petri selama penelitian bukan berasal dari media PCA dan pengencer BPW yang digunakan.
Setelah inkubasi selama 24 jam, pada pengenceran 10-1 hingga 10-6 tampak koloni bakteri tumbuh pada beberapa seri pengenceran. Koloni yang tumbuh pada media kemudian dihitung menggunakan colony counter menurut cara perhitungan
17
ALT yang tercantum dalam PPOMN tahun 2006. Jumlah koloni yang tumbuh dinyatakan sebagai jumlah koloni per mL sampel. Hasil perhitungan nilai ALT dari ketiga replikasi sampel jamu serbuk temulawak ditunjukkan pada lampiran 2, lampiran 7 dan lampiran 12. Sedangkan hasil dari perhitungan rata-rata nilai ALT pada ketiga replikasi sampel jamu serbuk temulawak ditunjukkan pada tabel I.
Tabel I. Hasil perhitungan rata-rata nilai ALT pada ketiga sampel Sampel ALT (koloni/g) SD CV A (Penjual A) 2,9 x 102 15,3 5,1%
B (Penjual B) 3,3 x 102 30,5 9,1 %
C (Penjual C) 1,8 x 102 10 5,5%
Berdasarkan hasil perhitungan ALT pada tabel I (tabel perhitungan lengkap pada lampiran 2 dengan mengacu pada MA PPOMN tahun 2006) menunjukkan bahwa ketiga sampel jamu serbuk temulawak berturut-turut seluruhnya masuk dalam kriteria ambang batas yang diperbolehkan atau masuk dalam range normal ALT seperti yang tercantum dalam BPOM RI 2014 yang menyatakan bahwa persyaratan mutu untuk nilai ALT jamu serbuk seduhan adalah ≤ 106 koloni/g.
Pada penjual A, pengenceran yang dipilih untuk perhitungan koloni adalah pengenceran 10-1 karena jumlah koloni yang tumbuh pada pengenceran ini masuk dalam range 25-250 koloni dan nilai ALT penjual A adalah 2,9 x 102 koloni/g. Pada penjual B, pengenceran yang dipilih untuk perhitungan koloni adalah pengenceran 10-1 karena jumlah koloni yang tumbuh pada pengenceran ini masuk dalam range 25-250 koloni dan nilai ALT penjual B adalah 3,3 x 102 koloni/g.Pada penjual C, pengenceran yang dipilih untuk perhitungan koloni adalah pengenceran 10-1 karena pada kedua cawan petri pada setiap replikasi hanya terdapat kurang dari 25 koloni.
Sehingga bila hasil koloni kurang dari 25, hitung jumlah yang ada pada cawan dari tiap pengenceran lalu rerata jumlah koloni tiap cawan dan kalikan dengan faktor pengencernya (SNI, 2008) dan nilai ALT penjual C adalah 1,8 x 102 koloni/g.
Nilai Standar Deviasi (SD) yang didapatkan pada penelitian ini untuk masing-masing sampel A, B dan C adalah 15,3; 30,5; dan 10. Nilai SD pada
18
penelitian ini menunjukkan bahwa presisi data yang didapat bagus. Selain itu.
Coefisien Variansi (CV) untuk masing-masing sampel A, B dan C adalah 5,1%;
9,1%; dan 5,5%. Tingginya nilai SD dan CV menunjukkan kemungkinan tempat penyimpanan sampel tiap toko yang berbeda, pengukuran yang dilakukan hanya sekali, pengambilan sampel hanya dari 3 toko. Presisi data yang didapat kurang bagus juga dikarenakan jumlah sampel yang diteliti kurang mencukupi, karena semakin besar sampel semakin tinggi pula tingkat presisi yang didapatkan, namun pada sampel B dan C sudah menunjukkan tingkat presisi yang cukup baik.
Sehingga dapat dikatakan bahwa jamu serbuk temulawak yang dijual oleh ketiga pedagang jamu serbuk tersebut layak untuk dikonsumsi masyarakat. Nilai ALT yang tidak melebihi batas dipengaruhi oleh berbagai faktor, yaitu kebersihan bahan baku yang digunakan, tempat pengolahan jamu, proses pengolahan jamu, pengemasan yang baik, cara penyimpanan bahan baku ataupun jamu yang diproduksi, serta proses pencucian bahan baku hingga bersih menggunakan air mengalir secara berulang dalam proses pengolahannya juga dapat menjadi salah satu faktor minimnya kontaminasi mikroorganisme. Hal tersebut diketahui berdasarkan hasil observasi yang dilakukan peneliti terhadap ketiga penjual jamu saat pengambilan sampel di pasar Beringharjo Yogyakarta.
Uji Angka Kapang Khamir
Uji AKK merupakan suatu metode untuk menghitung jumlah koloni kapang dan khamir yang tumbuh dari cuplikan yang diinokulasikan pada media yang sesuai setelah inkubasi selama 3-5 hari dalam suhu 20-25oC. Tujuan dilakukannya uji AKK adalah memberikan jaminan bahwa sediaan obat tradisional tidak mengandung cemaran fungi yang melebihi batas yang ditetapkan karena dapat mempengaruhi stabilitas dan alfatoksin yang berbahaya bagi kesehatan (Radji, 2010).
Kapang atau mold adalah mikroba bersel tunggal berupa benang-benang halus yang disebut hifa, kumpulan hifa disebut miselium, berkembang biak dengan spora atau membelah diri (SNI, 2009). Adanya kapang dalam makanan dan minuman sangat berbahaya karena kapang menghasilkan mitotoksin. Mitotoksin adalah metabolit sekunder dari kapang yang bersifat sitotoksik, merusak struktur
19
sel, seperti membran dan merusak proses pembentukan sel yang penting bagi tubuh.
Penyakit berbahaya yang disebabkan oleh mitotoksin disebut mikotoksis. Terdapat 5 jenis mikotoksin yang berbahaya bagi kesehatan yaitu, alfatoksin, fumonisin, okratoksin, trikotesena dan zearalenon. Alfatoksin terutama dihasilkan oleh Apergilus flavus dan Aspergilus parasiticus. Alfatoksin B1, B2, G1, G2 merupakan alfatoksin yang paling sering dijumpai dan bersifat toksik (Ahmad, 2009).
Khamir atau yeast adalah fungi uniseluler, tidak berfilamen, berbentuk oval atau bulat, tidak berflagela, dan berukuran lebih besar jika dibandingkan dengan sel bakteri. Khamir bereproduksi dengan pertunasan, beberapa khamir menghasilkan tunas yang tidak dapat melepaskan diri sehingga membentuk sel-sel rantai pendek yang disebut pseudohifa. Khamir mampu hidup dalam keadaan aerob maupun anaerob (Pratiwi, 2008). Beberapa kelompok khamir yang dominan ditemukan dalam air dan ekosistem tanah adalah genus Cryptococcus, Candidia, dan Debaryomyces. Candida albicans merupakan flora normal di permukaan membran mukosa, saluran pencernaan, dan saluran genitalia wanita. Candida albicans akan menjadi patogen apabila ada beberapa faktor risiko penyebab infeksi, seperti penurunan sistem imunitas dan terjadi perubahan fisiologis pada tubuh (Jayanti dan Nyoman, 2018). Apabila jumlahnya berlebihan di dalam tubuh, Candida akan mengkolonisasi saluran pencernaan dan membentuk struktur seperti rizoid. Rizoid dapat menembus mukosa atau dinding usus dan menyebabkan terbentuknya lubang sehingga dapat masuk ke sistemik Candida yang berada dalam sirkulasi sistemik akan menyebar ke berbagai organ tubuh seperti mulut, sinus, tenggorokan, dan saluran reproduksi sehingga menyebabkan infeksi penyakit (Pratiwi, 2008).
Kapang/ khamir dapat tumbuh selama proses penyimpanan bahan baku jamu, serta dalam kondisi tanah lembab (SNI, 2009).
Media yang akan digunakan untuk pengujian AKK adalah Potato Dextrose Agar (PDA). Potato Dextrose Agar merupakan media yang umum untuk pertumbuhan jamur di laboratorium karena memilki pH yang rendah (pH 4,5 - 5,6) sehingga dapat menghambat pertumbuhan bakteri yang membutuhkan lingkungan yang netral dengan pH 7,0 dan suhu optimum untuk pertumbuhan antara 25-30° C (Cappucino, 2014). Potato Dextrose Agar tersusun atas bahan alami (kentang) dan
20
bahan sintesis (dextrose dan agar), sehingga termasuk media semi sintetik. Kentang merupakan sumber karbon (karbohidrat), vitamin dan energi, dextrose sebagai sumber gula dan energi, selain itu komponen agar berfungsi untuk memadatkan medium PDA, komponen ini sangat diperlukan bagi pertumbuhan dan perkembangbiakkan mikroorganisme terutama jamur (Octavia, 2017).
Dalam uji AKK homogenisasi sampel bertujuan untuk meratakan distribusi kapang/khamir dan dibuat seri pengenceran yang bertujuan untuk mendapatkan koloni yang tumbuh terpisah, sehingga memudahkan pengamatan dan perhitungan hasil, serta menghindari pertumbuhan koloni yang saling bertumpuk, yang nantinya akan sulit untuk diamati dan dihitung.
Pada penelitian ini juga dibuat kontrol media yang berisi media PDA dan kontrol pengencer yang berisi media PDA dan pengencer BPW yang bertujuan untuk memastikan bahwa mikroorganisme yang tumbuh bukan berasal dari media PDA atau pengencer BPW.
Gambar 2. Gambar Kontrol Pengencer dan Kontrol Media Uji AKK Pada gambar 2 yaitu pada kontrol media dan kontrol pengencer tidak terdapat koloni bakteri yang tumbuh setelah diinkubasi pada suhu 20-25oC selama 5 hari. Hasil pengujian tersebut menunjukkan bahwa media PDA dan pengencer BPW yang digunakan tidak terkontaminsi mikroba, sehingga koloni bakteri yang tumbuh pada cawan petri selama penelitian bukan berasal dari media PDA dan pengencer BPW yang digunakan.
Pada uji AKK seri pengenceran dibuat hingga 10-4 yang bertujuan sebagai orientasi untuk mendapatkan tingkat pengenceran yang paling efektif, koloni mudah dihitung dan sesuai range. Dibuat seri pengenceran agar memperoleh individu fungi yang tumbuh terpisah dan tidak menumpuk.
Hasil perhitungan nilai AKK dari ketiga replikasi sampel jamu serbuk temulawak ditunjukkan pada lampiran 17, lampiran 22 dan lampiran 27. Sedangkan
21
hasil dari perhitungan rata-rata nilai AKK pada ketiga replikasi sampel jamu serbuk temulawak ditunjukkan pada tabel II.
Tabel II. Hasil rata-rata nilai AKK pada ketiga sampel Sampel AKK (koloni/g) SD CV
A (Penjual A) <10 0 0
B (Penjual B) <10 0 0
C (Penjual C) <10 0 0
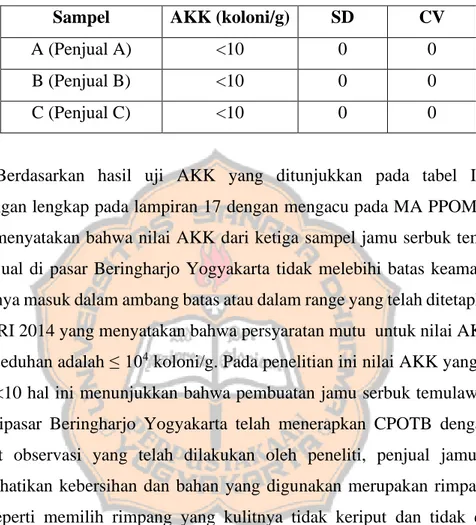
Berdasarkan hasil uji AKK yang ditunjukkan pada tabel II (tabel perhitungan lengkap pada lampiran 17 dengan mengacu pada MA PPOMN tahun 2006), menyatakan bahwa nilai AKK dari ketiga sampel jamu serbuk temulawak yang dijual di pasar Beringharjo Yogyakarta tidak melebihi batas keamanan dan seluruhnya masuk dalam ambang batas atau dalam range yang telah ditetapkan oleh BPOM RI 2014 yang menyatakan bahwa persyaratan mutu untuk nilai AKK jamu serbuk seduhan adalah ≤ 104 koloni/g. Pada penelitian ini nilai AKK yang didapat adalah <10 hal ini menunjukkan bahwa pembuatan jamu serbuk temulawak yang dijual dipasar Beringharjo Yogyakarta telah menerapkan CPOTB dengan baik.
Menurut observasi yang telah dilakukan oleh peneliti, penjual jamu serbuk memperhatikan kebersihan dan bahan yang digunakan merupakan rimpang yang segar seperti memilih rimpang yang kulitnya tidak keriput dan tidak dimakan serangga, bahan baku yang digunakan diletakkan ditempat yang sejuk dan kering sehingga terhindar dari pertumbuhan jamur, mencuci bahan-bahan yang akan diproses menjadi jamu serbuk, serta menyimpan jamu dalam kemasan khusus jamu serbuk dan ditutup rapat sehingga kemungkinan untuk tercemar sangat rendah.
Nilai Standar Deviasi (SD) yang diperoleh pada penelitian ini memiliki keterulangan yang baik karena ketiga replikasi dari sampel A, B dan C masing- masing tidak menunjukkan pertumbuhan koloni.untuk masing-masing sampel A, B dan C.
22
KESIMPULAN DAN SARAN I. KESIMPULAN
1. Nilai ALT pada jamu serbuk temulawak di pasar Beringharjo Yogyakarta sebesar 2,7 x 102 koloni/g, maka jamu serbuk temulawak memenuhi persyaratan keamanan KaBPOM RI No. 12 Tahun 2014 yang menyatakan bahwa nilai ALT jamu serbuk yang diperbolehkan yaitu ≤ 106 koloni/g.
2. Nilai AKK pada jamu serbuk temulawak di pasar Beringharjo Yogyakarta sebesar < 10 koloni/g, maka jamu serbuk temulawak memenuhi persyaratan keamanan KBPOM RI No. 12 Tahun 2014 yang menyatakan nilai AKK jamu serbuk yang diperbolehkan yaitu ≤ 104 koloni/g.
II. SARAN
1. Perlu dilakukan pengujian terhadap parameter-parameter persyaratan mutu obat lainnya yang telah diatur dalam Peraturan KBPOM RI Nomor 12 Tahun 2014 mengenai cemaran alfatoksin, cemaran logam berat dan cemaran mikroba seperti bakteri patogen yang terdapat dalam sediaan jamu serbuk temulawak di pasar Beringharjo yang berada di Yogyakarta sehingga dapat diketahui koloni bakteri apa yang terdapat didalam sampel jamu tersebut, misal E.coli, Salmonella dan Pseudomonas.
23
DAFTAR PUSTAKA
Afifi, C. dan Sugiarti, L., 2016. Analisis Mikrobiologis Jamu Tujuh Angin dan Sari Asih PT. Jamu Air Mancur Surakarta dengan metode ALT dan AKK. Jurnal Keperawatan dan Kesehatan Masyarakat STIKES Cendikia Utama Kudus, 1(5),65-71.
Ahmad, R. Z., 2009. Cemaran Kapang Pada Pakan dan Pengendaliannya. Balai Besar Penelitian Veteriner. Bogor. 15
Badan Penelitian dan Pengembangan Kesehatan Kementrian Kesehatan RI, 2018.
Riset Kesehatan Dasar 2010. Badan Penelitian dan Pengembangan Kesehatan Kementrian Kesehatan RI. Jakarta.
Badan Pengawas Obat dan Makanan RI, 2006. Metode Analisis PPOMN. MA PPOMN nomor 97/mik/00. Uji Angka Kapang/Khamir dalam Obat Tradisional. Jakarta. 108-110.
Badan Pengawas Obat dan Makanan RI, 2014. Peraturan Kepala Badan Pengawas Obat dan Makanan RI nomor 12 Tahun 2014 tentang Persyaratan Mutu Obat Tradisional. Kepala Badan Pengawas Obat dan Makanan RI. Jakarta.
Badan Standarisasi Nasional, 2008. Metode Pengujian Cemaran Mikroba. SNI 2897:2008. Jakarta. 14-32.
Badan Standarisasi Nasional, 2009. Batas Maksimum Cemaran Mikroba dalam Pangan. SNI 7388:2009. Jakarta. 6
Cappuccino, J. G., Sherman, N., 2011. Microbiology : A Laboratory Manual 9th edition. Pearson Education, Inc., USA.
Cappuccino, J. G., Sherman, N., 2014. Microbiology : A Laboratory Manual 10th edition. Pearson Education, Inc., USA.
Departemen Kesehatan Republik Indonesia, 2016. Peraturan Menteri Kesehatan nomor 006 tahun 2016 tentang Formularium Obat Herbal Asli Indonesia, Departemen Kesehatan Republik Indonesia. Jakarta.
Dion, R., Susiana, P., 2020. Analisis Cemaran Kapang dan Khamir pada Jamu Serbuk Instan Jahe Merah dan Temulawak. Jurnal Bioteknologi, 3(2).
Djais, A. A., Theodorea, C, F., 2019. The Effect of Presto Cooker as an Alternative Sterilizer Device for Dental Equipment. Journal of Indonesian Dental Association. 2(1), 2-13.
24
Ismono, I., Suyatno, S., Hidajati, N. 2018. Pelatihan pembuatan serbuk minuman herbal instan untuk Warga desa jajar, kecamatan talun, kabupaten blitar.
Jurnal Abdi: Media pengabdian kepada masyarakat, 3(2), 76-83.
Istini, 2020. Pemanfaatan Plastik Polipropilen Standing Pouch Sebagai Salah Satu Kemasan Sterilisasi Peralatan Laboratorium. Indonesian Journal Of Laboratory, 2(3), 41-46.
Jayanti, N. K. S., Nyoman, J., 2018. Isolasi Candida albicans dari Swab Mukosa Mulut Penderita Diabetes Melitus Tipe 2. Jurnal Teknologi Laboratorium.
7(1): 01-07.
Latief, A., 2009. Obat Tradisional. Penerbit Buku Kedokteran EGC. Jakarta, 48- 49, 259.
Nurcholis, W., Laksmi, A., Ni Luh, P. E. K. S., Latifah,K.D., 2012. Curcuminoid Contents Antioxidant and Anti-Inflammatory Activities of Curcuma xanthorrhiza RoxB. and Curcuma domestica Val. Promising Lines From Sukabumi of Indonesia. Prosiding Seminar Nasional Kimia Unesa 2012.
978–979.
Nurmalia, R., 2012. 24 Herbal Legendaris Untuk Kesehatan Anda. Gramedia, Jakarta, 329-335.
Octavia, A. dan Wantini, S., 2017. Perbandingan Pertumbuhan Jamur Aspergillus flavus Pada Media PDA (Potato Dextrose Agar) dan Media Alternatif dari Singkong (Manihot esculenta Crantz). Jurnal Analis Kesehatan, 6(2), 625- 631.
Pratiwi, S.T., 2008. Mikrobio Farmasi. Fakultas Universitas Gajah Mada, Yogyakarta, 38, 135-140, 206-207.
Puspandari, N., Ani, I.,2015. Deskripsi Hasil Uji Angka Lempeng Total (ALT) Pada Beberapa Susu Formula Bayi. Jurnal Kefarmasian Indonesia. 5(2)00 106-112.
Radji, M., 2009. Buku Ajar Mikrobiologi : Panduan Mahasiswa Farmasi dan Kedokteran. Penerbit Buku Kedokteran EGC. Jakarta.
Radji, M., 2010. Buku Ajar Mikrobiologi : Panduan Mahasiswa Farmasi dan Kedokteran. Penerbit Buku Kedokteran EGC. Jakarta.
Dewi, T. M., Nurbaity, A., Suryatmana, P., Sofyan, E.T., 2017. Effect Of Sterilization And Medium Composition For Mycorrhizal Fungi On Root Colonisation, Length And Weight Of Sorghum Root. Jurnal Agro, 4(1).
25
Soesetyaningsih, E. dan Azizah, 2020. Berkala Sainstek, 8(3), 76-78.
Susanti., Emma., Riza, A., 2017. Uji Cemaran Mikroba Pada Jamu Keliling Yang Dijual Di Kelurahan Simpang Baru Panam Pekanbaru Dengan Metode Mpn (Most Probable Number). Jurnal Penelitian Farmasi Indonesia, 6(2), 56-60.
Tyas, D. E., Niniek, W., Anhar, S., 2018. Perbedaan Jumlah Bakteri Dalam Sedimen Pada Kawasan Bermangrove Dan Tidak Bermangrove Di Perairan Desa Bedono, Demak. Journal Of Maquares. 7(2), 189-196.
Wasito, H., 2011. Obat Tradisional Kekayaan Indonesia. Graha Ilmu. Yogyakarta.
13-15, 29, 41-42, 51.
Yonathan, D. Y., 2013. Hubungan Antara Kualitas Sarana & Prasarana Rumah dan Perilaku Sehat dengan Kejadian Demam Typhoid di Wilayah Kerja Puskesmas Ngaliyan Kota Semarang. Jurnal Kesehatan Masyarakat. 2(1), 1
26
LAMPIRAN
27
Lampiran 1. Sampel jamu serbuk temulawak
Sampel jamu serbuk temulawak
Lampiran 2. Nilai ALT dan perhitungan ALT sampel jamu serbuk temulawak sampel A inkubasi 24 jam
Sampel Replikasi Pengenceran Jumlah Koloni Nilai ALT (koloni/g) Cawan
1
Cawan 2
Rata-rata
A 1 10-1 30 32 31 3,1 x 102
10-2 15 17 16
10-3 6 8 7
10-4 1 1 1
10-5 0 0 0
10-6 0 0 0
2 10-1 25 31 28 2,8 x 102
10-2 13 15 14
10-3 4 6 5
10-4 0 0 0
10-5 0 0 0
10-6 0 0 0
3 10-1 33 27 30 3 x 102
10-2 17 13 16
10-3 7 5 6
10-4 0 0 0
10-5 0 0 0
10-6 0 0 0
Keterangan :
: angka yang masuk dalam perhitungan ALT
28
Lampiran 3. Perhitungan ALT sampel A Replikasi 1
Pengenceran 10-1
⟶30 + 32
2 x101 = 310 koloni/g
Pengenceran 10-2
⟶Tidak dapat dihitung karena koloni bakteri kurang dari range 25-250
Pengenceran 10-3
⟶Tidak dapat dihitung karena koloni bakteri kurang dari range 25-250
Pengenceran 10-4
⟶ Tidak dapat dihitung karena koloni bakteri kurang dari range 25-250
Pengenceran 10-5
⟶Tidak dapat dihitung karena tidak terdapat koloni bakteri yang tumbuh
Pengenceran 10-6
⟶Tidak dapat dihitung karena tidak terdapat koloni bakteri yang tumbuh
Jumlah ALT replikasi 1 = 310 ~ 3,1 x 102 koloni/g
29
Lampiran 4. Perhitungan ALT sampel A Replikasi 2
Pengenceran 10-1
⟶25 + 31
2 x101 = 280 koloni/g
Pengenceran 10-2
⟶Tidak dapat dihitung karena koloni bakteri kurang dari range 25-250
Pengenceran 10-3
⟶Tidak dapat dihitung karena koloni bakteri kurang dari range 25-250
Pengenceran 10-4
⟶Tidak dapat dihitung karena tidak terdapat koloni bakteri yang tumbuh
Pengenceran 10-5
⟶Tidak dapat dihitung karena tidak terdapat koloni bakteri yang tumbuh
Pengenceran 10-6
⟶Tidak dapat dihitung karena tidak terdapat koloni bakteri yang tumbuh
Jumlah ALT replikasi 2 = 280 ~ 2,8x 102 koloni/g
30
Lampiran 5. Perhitungan ALT sampel A Replikasi 3
Pengenceran 10-1
⟶33 + 27
2 x101 = 300 koloni/g
Pengenceran 10-2
⟶Tidak dapat dihitung karena koloni bakteri kurang dari range 25-250
Pengenceran 10-3
⟶Tidak dapat dihitung karena koloni bakteri kurang dari range 25-250
Pengenceran 10-4
⟶Tidak dapat dihitung karena tidak terdapat koloni bakteri yang tumbuh
Pengenceran 10-5
⟶Tidak dapat dihitung karena tidak terdapat koloni bakteri yang tumbuh
Pengenceran 10-6
⟶Tidak dapat dihitung karena tidak terdapat koloni bakteri yang tumbuh
Jumlah ALT replikasi 3 = 300 ~ 3 x 102 koloni/g
Rata − rata ALT Sampel A =310 + 280 + 300
3 = 296 ~ 2,9 x 102 koloni/g
31
Lampiran 6. Perhitungan Standar Deviasi (SD) dan Koefisien Variasi (CV) ALT Sampel A
Replikasi X X̅ X -X̅ (X -X̅)2
1 310 296 14 196
2 280 296 -16 256
3 300 296 4 16
∑(X − X̅)2 468
n=3
SD =
√
∑(X −X̅)2𝑛−1
=
√
4682 = 15,3
CV = 𝑆𝐷 X̅
= 15,3296 x 100%
= 5,1%