KUALITAS BIOETANOL LIMBAH TAPIOKA PADAT KERING DIHALUSKAN (TEPUNG) DENGAN PENAMBAHAN RAGI DAN
H2SO4 PADA LAMA FERMENTASI YANG BERBEDA
SKRIPSI
Untuk Memenuhi Sebagian Persyaratan Guna Mencapai Derajat Sarjana S-1 Pendidikan Biologi
Disusun Oleh : Septina Dwi Prasetyana
A. 420.050.026
FAKULTAS KEGURUAN DAN ILMU PENDIDIKAN UNIVERSITAS MUHAMMADIYAH SURAKARTA
PERSETUJUAN
KUALITAS BIOETANOL LIMBAH TAPIOKA PADAT KERING DIHALUSKAN (TEPUNG) DENGAN PENAMBAHAN RAGI DAN H2SO4 PADA LAMA FERMENTASI YANG BERBEDA
Yang dipersiapkan dan disusun oleh :
SEPTINA DWI PRASETYANA A. 420050026
Disetujui untuk dipergunakan dihadapan Dewan Penguji Skripsi S1
Pembimbing I Pembimbing II
Dra. Hj. Suparti, M.Si. Dra. Hj. Aminah Asngad, M.Si.
PENGESAHAN
KUALITAS BIOETANOL LIMBAH TAPIOKA PADAT KERING DIHALUSKAN (TEPUNG) DENGAN PENAMBAHAN RAGI DAN H2SO4 PADA LAMA FERMENTASI YANG BERBEDA
Yang dipersiapkan dan disusun oleh :
SEPTINA DWI PRASETYANA A. 420050026
Telah dipertahankan di depan Dewan Penguji Pada tanggal : 9 Juni 2009
dan dinyatakan telah memenuhi syarat
Susunan Dewan Penguji
1. Dra. Hj. Suparti, M.Si ( )
2. Dra. Hj. Aminah Asngad, M.Si ( )
3. Mukhlissul Faatih, S.Si, M. Biotech ( )
Surakarta, Juni 2009
UNIVERSITAS MUHAMMADIYAH SURAKARTA FAKULTAS KEGURUAN DAN ILMU PENDIDIKAN
Dekan
PERNYATAAN
Dengan ini saya menyatakan bahwa dalam skripsi ini tidak terdapat karya yang pernah diajukan untuk memperoleh gelar kesarjanaan S1 suatu perguruan tinggi dan sepanjang pengetahuan saya juga tidak terdapat karya atau pendapat yang pernah ditulis atau diterbitkan oleh orang lain, kecuali yang secara tertulis diacu dalam naskah dan disebutkan dalam daftar pustaka.
Apabila ternyata kelak di kemudian hari terbukti ada ketidakbenaran dalam pernyataan saya di atas, maka saya akan bertanggung jawab.
Surakarta, Juni 2009
MOTTO
!
"
"
PERSEMBAHAN
Kupanjatkan puji syukur kepada Allah SWT atas rahmadNya hingga terselesainya skripsi ini dan kupersembahkan karya sederhana ini, untuk :
Bapak dan ibuku tercinta yang selalu setia mendoakan dan memberi dorongan motivasi kepadaku.
Adikku (Sevian), kakakku (Agustin – Eddy) dan keponakanku (dhek Hana) tersayang yang turut memberikan doa dan semangat hingga skripsi ini selesai.
Teman-temanku team Bioetanol (Ilma, Triya, Mus, Rina, Nurul, Umi, Phe, Linda, Tatik) terima kasih atas kerjasama dan kebersamaannya.
Sahabat sejatiku (Fitri, Danang HS, Heni dan A. Maryanto) yang turut memberikan doa dan motivasi kepadaku.
KATA PENGANTAR
Puji syukur penulit panjatkan kehadirat Allah SWT yang telah memberikan rahmad dan hidayahNya sehingga penulis dapat menyelesaikan penyusunan naskah skripsi ini tepat pada waktunya. Juga tidak lupa sholawat serta salam senantiasa kepada Nabi Muhammad SAW beserta keluarga dan sahabat-sahabatnya.
Naskah skripsi yang berjudul ”KUALITAS BIOETANOL LIMBAH
TAPIOKA PADAT KERING DIHALUSKAN (TEPUNG) DENGAN
PENAMBAHAN RAGI DAN H2SO4 PADA LAMA FERMENTASI YANG BERBEDA” ini disusun berdasarkan hasil penelitian yang telah dilakukan sebagai syarat dalam memperoleh derajat Sarjana Fakultas Keguruan dan Ilmu Pendidikan pada Jurusan Pendidikan Biologi Universitas Muhammadiyah Surakarta.
Selama penelitian dan penyusunan naskah skripsi, penulis mendapatkan banyak bimbingan dan petunjuk serta nasehat dari berbagai pihak, oleh karena itu pada kesempatan ini penulis mengucapkan banyak terima kasih kepada:
1. Bapak dan ibuku tercinta yang selalu setia mendoakan, memberikan motivasi dan membiayaiku hingga terselesainya skripsi ini.
2. Dra. Hj. Suparti, M.Si., selaku Pembimbing I atas segala bimbingan, pengarahan, dorongan dan masukan yang telah diberikan dengan segenap kebesaran hati sejak penyusunan proposal, awal penelitian hingga selesainya penyusunan naskah ini. 3. Dra. Hj. Aminah Asngad, M.Si., selaku pembimbing II yang telah memberikan
4. Dra. Hj. Tuti Rahayu, M.Pd, selaku pembimbing akademik dan bapak ibu dosen yang senantiasa memberikan bimbingan serta kritikan yang senantiasa memacu semangat penulis untuk menyelesaikan studi di Fakultas Keguruan dan Ilmu Pendidikan Jurusan Biologi.
5. Ibu Siti Mardiyah, selaku Laboran Laboratorium Kimia Fakultas Ilmu Kesehatan yang telah membantu dalam melaksanakan penelitian.
6. Kakakku (Agustin), adikku (Sevian), yang senantiasa memberikan kasih sayang dan doanya.
7. Teman-teman team Bioetanol dan angkatan 2005.
8. Sahabat-sahabat yang tidak dapat penulis sebutkan semua disini karena suatu hal. 9. Semua pihak yang telah banyak membantu yang tidak dapat penulis sebutkan
satu persatu.
Dalam penyusunan skripsi ini, masih jauh dari kesempurnaan, sehingga penulis harapkan segala kritik dan saran yang membangun. Semoga karya sederhana ini bermanfaat bagi dunia pendidikan dan pembaca pada umumnya. Terima kasih.
Surakarta, Mei 2009
DAFTAR ISI
HALAMAN JUDUL ... i
HALAMAN PERSETUJUAN ... ii
HALAMAN PENGESAHAN... iii
HALAMAN PERNYATAAN ... iv
DAFTAR LAMPIRAN ... xiii
ABSTRAK ... xiv
6. Saccharamyces cerevisieae... 20
7. Asam Sulfat... 21
8. Etanol ... 22
B. Kerangka Pemikiran ... 23
BAB III. METODE PENELITIAN... 24
A. Tempat dan Waktu Penelitian ... 25
B. Alat dan Bahan ... 25
C. Prosedur Penelitian ... 25
1. Pembuatan Fermentasi ... 25
2. Destilasi Alkohol... 26
3. Analisis Kadar Alkohol... 26
D. Rancangan Percobaan ... 27
E. Teknik Pengumpulan Data ... 28
F. Analisis Data ... 29
BAB IV. HASIL DAN PEMBAHASAN ... 33
A. Hasil ... 33
B. Pembahasan... 34
BAB V. KESIMPULAN DAN SARAN ... 38
A. Kesimpulan ... 38
B. Saran... 38 DAFTAR PUSTAKA
DAFTAR TABEL
Tabel Halaman
3.1. Kombinasi perlakuan pada limbah tapioka padat kering
dihaluskan ... 27 3.2. Data Perlakuan Kadar Alkohol ( % ) ... 28 4.1. Data Pengamatan Kadar Alkohol Limbah Tapioka Padat
Kering Dihaluskan Dengan Penambahan Ragi dan H2SO4
Pada Lama Fermentasi yang Berbeda ... 33 4.2. Hasil Uji Anava Dua Jalur Kualitas Bioetanol Limbah
Tapioka Padat Kering Dihaluskan Dengan Penambahan Ragi
DAFTAR GAMBAR
Gambar Halaman
2.1. Diagram Alir Tahapan Proses Pengolahan Tapioka ... 10 2.2. Urutan Proses Pengeringan Tapioka ... 16 3.1. Kerangka Pemikiran ... 23 4.1. Histogram Kadar Alkohol Limbah Tapioka Padat Kering
Dihaluskan Dengan Penambahan Ragi dan H2SO4
DAFTAR LAMPIRAN
1. Anava Dua Jalur untuk Kadar Alkohol 2. Foto-foto Hasil Penelitian
3. Daftar Nilai Baku F pada Taraf Kritis 5 dan 1 % untuk Analisis Sidik Ragam (Analysis of Variance)
4. Daftar Nilai Baku P (Significant Studentized Ranges (R) X Q Pada Taraf Kritis 5 dan 1 Persen untuk Uji Jarak Nyata Duncan
KUALITAS BIOETANOL LIMBAH TAPIOKA PADAT KERING DIHALUSKAN (TEPUNG) DENGAN PENAMBAHAN RAGI DAN H2SO4
PADA LAMA FERMENTASI YANG BERBEDA
SEPTINA DWI PRASETYANA, A 420 050 026, PROGRAM STUDI PENDIDIKAN BIOLOGI FAKULTAS KEGURUAN DAN ILMU
PENDIDIKAN, UNIVERSITAS MUHAMMADIYAH SURAKARTA, 2009, 38 HALAMAN
ABSTRAK
Indonesia sebagai negara berkembang dengan jumlah penduduk sekitar dua ratus juta jiwa menghadapi masalah energi yang cukup mendasar , sebagai contoh minyak bumi. Sehingga bioetanol sebagai energi alternatif. Tumbuhan yang potensial untuk menghasilkan bioetanol adalah ketela pohon, tebu, jagung. Indonesia merupakan sentra tanaman pangan terutama Manihot utilissima pohl sebagai bahan baku pembuatan tepung tapioka.Penelitian ini bertujuan untuk mengetahui kadar bioetanol hasil fermentasi limbah tapioka padat kering dihaluskan dengan penambahan ragi dan H2SO4. Bioetanol ini merupakan salah satu alternatif energi di Indonesia. Pembuatan bioetanol menggunakan limbah tapioka padat kering dihaluskan diproses dengan cara fermentasi dan destilasi sehingga menghasilkan bahan bakar yang berupa bioetanol.
Penelitian dilakukan di Laboratorium Kimia Fakultas Ilmu Pendidikan UNS dan Laboratorium Kima Fakultas Ilmu Kesehatan UMS pada bulan Desember 2008-Januari 2009. Metode yang digunakan adalah metode eksperimen dengan menggunakan Rancangan Acak Lengkap (RAL) pola faktorial yang terdiri dari 2 faktor yaitu waktu fermentasi (W) dan dosis ragi (D). Analisis data yang digunakan adalah Anava dua jalur dan Uji DMRT (Duncan’s Multiple Range Test). Dari penelitian tersebut diperoleh hasil yaitu kadar alkohol tertinggi 14,43% pada W2D3 (7 hari/75 gr),sedangkan kadar alkohol terendah 3,70% pada W3D1 (9hari/25 gr). Berdasarkan hasil analisis data dapat diperoleh bahwa limbah tapioka padat kering dihaluskan mempunyai kadar alkohol tertinggi pada W2D3 dengan waktu fermentasi 7 hari dan dosis ragi 75 gr.
BAB I PENDAHULUAN
A. Latar Belakang Masalah
Indonesia sebagai negara berkembang dengan jumlah penduduk sekitar dua ratus jiwa menghadapi masalah energi yang cukup mendasar. Sebagai contoh, terjadinya penurunan produksi minyak bumi Indonesia perhari. Disisi lain kebutuhan masyarakat terhadap minyak bumi semakin tinggi. Sehingga bioetanol sebagai bentuk energi alternatif. Tumbuhan yang potensial untuk menghasilkan bioetanol adalah tanaman yang mempunyai karbohidrat tinggi, misalnya : ketela pohon, tebu, jagung, jerami.
Industri tapioka merupakan salah satu industri pertanian (agroindustri) yang cukup banyak terdapat di Indonesia, salah satunya di Kabupaten Sukoharjo. Merupakan daerah sentra tanaman pangan terutama ketela pohon (Manihot utilissima pohl) sebagai bahan baku pembuatan tepung tapioka. Untuk menopang ketersediaan bahan pangan yang melimpah tersebut, di Kecamatan Polokarto ada sebuah pabrik yaitu industri pengolahan tepung tapioka. Industri tersebut menampung bahan baku yang berasal dari para petani di daerah Polokarto berkapasitas antara 2-5 ton per hari.
apabila tidak ditangani dengan seksama onggok dapat menimbulkan potensi besar mencemari lingkungan. Sebagian besar industri topioka berlokasi dekat pemukiman penduduk padat dan ditepi sungai sehingga onggok yang dibuang disekitar lokasi industri akan berakibat fatal bagi lingkungan dan makhluk hidup yang mendiami daerah sekitar.
Proses pengolahan singkong menjadi tepung tapioka, menghasilkan limbah sekitar 2/3 bagian atau sekitar 75% dari bahan mentahnya, limbah ini biasa disebut onggok. Warga sekitar pabrik tapioka PT. Sukoharjo Makmur Abadi, Polokarto sudah sangat akrab dengan onggok. Dalam keadaan kering onggok mengeluarkan bau tidak sedap, apalagi dalam keadaan basah saat musim hujan. Bau tidak sedap ini muncul akibat terjadinya proses pembusukan onggok yang sangat cepat. Meskipun merupakan limbah tetapi kandungan karbohidrat onggok masih tinggi yaitu mencapai 63%-68%, sementara kadar airnya 20%. Tingginya kandungan karbohidrat dan kadar air inilah yang mempermudah akitifitas mikroba pengurai. Proses penguraian bisa bersifat aerob (membutuhkan oksigen) dan bisa pula bersifat anaerob (tidak membutuhkan oksigen). Dalam proses penguraian ini dihasilkan bau berupa H2S dan NH3 serta berbagai gas berbau menyengat lainnya. Meskipun disimpan dalam tempat khusus, bau tidak sedap ini tetap sulit dicegah penyebarannya.
karbohidrat sebesar 68%, protein sebesar 1,57%, lemak sebesar 0,26%, serat kasar sebesar 10% dan kadar air 20% (Winarno, 1988).
Karbohidrat merupakan sumber energi utama manusia. Kabohidrat yang kita makan adalah tepung atau pati yang ada dalam gandum, jagung, beras, kentang, padi-padian dan juga umbi ketela pohon (Fessenden, 1997). Glukosa suatu gula monokarida merupakan salah satu karbohidrat penting yang digunakan sebagai sumber tenaga bagi hewan dan tumbuhan.
Upaya minimalisasi limbah dari proses pembuatan tepung singkong salah satunya dengan memanfaatkan kembali limbah. Teknologi biokonversi merupakan konversi bahan secara enzimatik melalui fermentasi yang dapat dimanfaatkan untuk meningkatkan nilai onggok. Dalam hal tersebut, fermentasi merupakan proses perubahan-perubahan kimia dalam suatu substrat organik yang berlangsung karena aksi katalisator biokimiawi yaitu enzim yang dihasilkan oleh mikroba hidup tertentu. Pada proses ini, Saccharomyces cerevisiae merupakan organisme aerob. Organisme ini mempunyai ciri-ciri yaitu sel-selnya bundar, lonjong, memanjang dan menghasilkan pseudomiselium (Pelczar dan Chan, 1988).
Bioetanol merupakan biokimia dari proses fermentasi gula dari sumber karbohidrat menggunakan bantuan mikroorganisme (Anonim, 2008).
Pada dasarnya untuk menunjang pembangunan yang berwawasan lingkungan, semua industri tapioka diharuskan menyusun dokumen penyajian evaluasi lingkungan (PEL), sesuai keputusan menteri lingkungan hidup No. 51/MENKLH/6/1987 tentang pedoman teknis penyusunan amdal. Sehingga belum dapat beroperasi optimal dan cenderung berpotensi menimbulkan pencemaran lingkungan.
Perbedaan waktu fermentasi dan dosis ragi berpengaruh terhadap kadar alkohol sari umbi ketela pohon. Kadar alkohol tertinggi sebesar 51%, yaitu pada lama fermentasi 15 hari dan dosis ragi 8 gr. Sedangkan kadar alkohol terendah adalah 14,303% pada lama fermentasi 9 hari dan dosis ragi 2 gr. (Sugiarti, 2007). Hasil penelitian Indah (2007), tentang pengaruh waktu fermentasi dan dosis ragi terhadap kadar alkohol hasil fermentasi ampas umbi ketela karet (Manihot glaziovii muell), menunjukkan bahwa kadar alkohol tertinggi pada waktu fermentasi selama 18 hari dan dosis ragi 11 gr dengan kadar alkohol mencapai 13,8%, sedangkan kadar alkohol terendah adalah 5,933 % pada waktu fermentasi 12 hari dengan dosis ragi 5 gr.
Berdasarkan hasil penelitian Tatik (2008), kadar bioetanol pada tepung umbi ketela pohon dengan penambahan H2SO4 yang tinggi adalah pada waktu fermentasi 7 hari dengan dosis ragi 100 gr yaitu 30,60%, sedangkan kadar bioetanol terendah adalah waktu fermentasi 7 hari dengan dosis ragi 50gr yaitu 13,13%.
bahan alternatif dalam pembuatan alkohol karena limbah tapioka mengandung karbohidrat. Sehingga diadakan penelitian lebih lanjut dengan judul “KUALITAS BIOETANOL LIMBAH TAPIOKA PADAT KERING DIHALUSKAN (TEPUNG) DENGAN PENAMBAHAN RAGI DAN H2SO4 PADA LAMA FERMENTASI YANG BERBEDA”.
B. Pembatasan Masalah
Untuk menghindari meluasnya suatu permasalahan penelitian, maka perlu ada pembatasan masalah. Adapun batasan-batasan masalah adalah :
1. Subyek dalam penelitian ini adalah waktu fermentasi (5 hari, 7 hari dan 9hari) dosis ragi (25gr, 50gr, 75gr) dan H2 SO4 (20ml)
2. Obyek dalam penelitian ini adalah kadar alkohol pada fermentasi limbah tapioka padat kering dihaluskan.
3. Parameter penelitian adalah kadar alkohol. C. Perumusan Masalah
Berdasarkan latar belakang dan pembatasan diatas, maka perumusan masalah dalam penelitian ini adalah :
1. Bagaimana pengaruh waktu fermentasi dan dosis ragi dengan penambahan H2SO4 terhadap kadar alkohol pada fermentasi limbah tapioka padat kering dihaluskan ?
D. Tujuan Penelitian
Adapun tujuan penelitian ini adalah :
1. Mengetahui pengaruh waktu fermentasi, dosis ragi dengan penambahan H2SO4 terhadap kadar alkohol pada fermentasi limbah tapioka padat kering dihaluskan.
2. Mengetahui waktu fermentasi, dosis ragi dan H2SO4 yang efektif untuk mendapatkan kadar alkohol yang optimum.
E. Manfaat Penelitian
Manfaat yang diharapkan dalam penelitian ini adalah adalah :
1. Memberikan informasi mengenai keefektifan perbandingan waktu fermentasi, dosis ragi dan H2SO4 yang dapat digunakan untuk memperoleh kadar alkohol pada fermentasi ampas umbi ketela pohon yang optimum.
2. Dapat menambah pengetahuan penelitian terutama dalam pengemabangan teknologi pengolahan limbah tapioka padat kering dihaluskan.
BAB II
LANDASAN TEORI
A. Tinjauan Pustaka 1. Umbi Ketela Pohon
Ketela pohon disebut pula ubi kayu, casava singkong. Ketela pohon merupakan salah satu tanaman penghasil makanan. Di Indonesia tanaman ini tersebar luas dan tumbuh di pulau Jawa, Madura dan Sumatra. Singkong di Indonesia menduduki urutan ke III diantara empat produksi pangan yang utama antara lain : padi, jagung, singkong dan ubi jalar. Klasifikasi ketela pohon yaitu sebagai berikut :
Divisio : Spermatophyta Sub divisio : Angiospermae Classis : Dicotyledoneae Ordo : Euphorbiales Famili : Euphorbiaceae Genus : Manihot
Species : Manihotutilissima pohl (Steenis, 2005) 2. Industri Tapioka
a. Bahan Baku Produksi Tapioka
diharapkan dari pedagang-pedagang singkong yang sudah ada, maka terkadang terjadi kekosongan proses produksi 1-2 hari apabila bahan baku singkong yang ada habis diolah (Susanto, 2000).
b. Produk Tapioka
Tapioka adalah pati yang diperoleh dari umbi tanaman ubi kayu (Manihot utilissima). Dalam perdagangan lebih dikenal sebagai “tapioca Flour” atau tepung tapioka. Nama lain dari tapioka adalah pati kanji, pati ubi kayu, pati cassava, pati singkong, pati pohong sesuai dengan sebutan untuk ubi kayu dibeberapa daerah. Pati merupakan polisakarida yang tersusun oleh molekul glukoza yang terdiri dari molekul amilosa dan amilopektin. Seperti pati antara lain berbentuk makromolekul, tidak bermuatan, berbentuk granula yang padat dan tidak larut dalam air dingin. Jika dipanaskan akan mengalami gelatinasi dalam keadaan kering berwarna putih dan dalam bentuk gelatin berwarna opak (Mulyoharjo,1987).
c. Tahap-tahap produksi
1) Penghancuran sel-sel dan pemisahan butiran-butiran pati dari benda lain yang tidak larut. Fase ini meliputi: pengupasan, pencucian umbi dan pemarutan.
2) Pemisahan susu pati dari air dengan penyaringan menggunakan kain saring atau kawat kasa halus.
3) Pengurangan sebagian besar air yang terkandung pada pati basah 4) Penggilingan pati yang masih kasar kemudian dilakukan pengayakan.
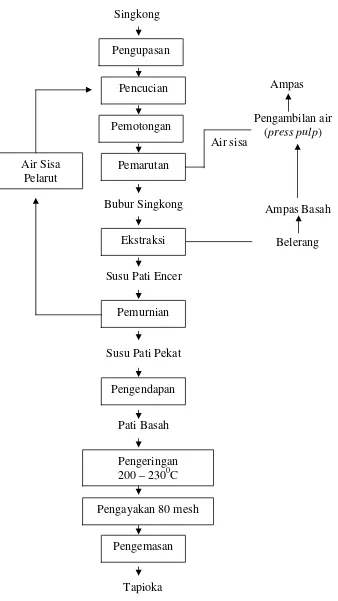
Gambar 2.1 : Diagram Alir Tahapan Proses Pengolahan Tapioka (Sumber PT. Sukoharjo Makmur Abadi)
Singkong
Pengupasan
Pencucian
Pemotongan
Pemarutan
Bubur Singkong
Ekstraksi
Susu Pati Encer
Pemurnian
Susu Pati Pekat Pengendapan
Pati Basah Pengeringan 200 – 2300C Pengayakan 80 mesh
Pengemasan
Tapioka Air Sisa
Pelarut
Pengambilan air (press pulp) Air sisa
Ampas
Diagram alir proses pembuatan pati tapioka akan diuraikan lebih lanjut dibawah ini :
1) Pengupasan
Bahan baku singkong yang telah dibongkar dari muatan kendaraan pengangkut, kemudian dimasukkan ke dalam happer yang berkapasitas sekitar 4 m dengan excavator sebagai tempat penampungan sementara singkong-singkong yang akan diproses lebih lanjut. Dari happer singkong dibawa naik dengan menggunakan konveyor menuju mesin pengupas (root peller). Pada mesin pengupas ini kulit ari atau kulit luar singkong dikupas dan dibersihkan dari kotoran-kotoran yang menempel pada permukaan singkong seperti tanah, batu-batuan kecil, plastik dan kotoran lainnya dengan cara diputar secara terus-menerus.
2) Pencucian
Singkong yang telah bersih dari kulit ari maupun kotoran, kemudian dicuci dengan menggunakan air yang disemprotkan sehingga menimbulkan tekanan terhadap singkong-singkong tersebut sambil diputar oleh pedal (peddle) pada mesin pencuci (root washer). Proses pencucian ini berlangsung melalui 3 tahapan yang berulang secara berturut-turut dan diharapkan singkong akhirnya akan benar-benar dalam keadaan bersih.
3) Sortasi
mengambil dan memotong bagian pangkal singkong yang keras (benggol), kayu-kayu yang terikut serta mengambil benda-benda keras seperti batu-batuan kecil yang terkadang masih sering ikut terbawa. Bagian pangkal singkong dan benda-benda keras ini adalah faktor yang menyebabkan mesin pemotong atau mesin pemarut sering rusak ataupun tumpul.
4) Pemotongan
Tahapan selanjutnya, singkong yang telah disortasi diangkut dengan konveyor menuju mesin pemotong (root chapper). Pada proses ini singkong dipotong menjadi bagian yang kecil-kecil yang siap diparut. 5) Pemarutan
Singkong yang telah dipotong kecil-kecil turun kebawah menuju mesin pemarut (roor rasper) yang terletak dibawah mesin pemotong, aluran yang digunakan untuk menghubungkan antara mesin pemotong dan mesin pemarut berupa pipa besar berbentuk segi empat yang bercabang dua sehingga apabila terdapat gangguan berupa benda keras atau batu yang masuk kedalam mesin pemarut dapat dikeluarkan dengan mengambil dari salah satu pipa tersebut, tanpa harus menghentikan kerja mesin pemarut apabila mesin ini membutuhkan waktu yang lama untuk stabil kembali.
berupa bubur cair, selain itu air parutan ini juga dapat berfungsi untuk menjaga ketajaman dan keawetan dari mata pisau parutan.
6) Ekstrasi
Ekstrasi adalah proses pembuatan ekstrak pati dari bahan parutan berupa bubur singkong menjauh ekstrak pati yang terpisah dari ampasnya. Proses ekstraksi dilakukan dalam tiga bagian, setiap bagiannya terdapat enam buah mesin ekstraktor ditambah enam buah pulp ekstraktor, sehingga keseluruhannya berjumlah dua puluh empat buah. Proses penambahan belerang terjadi didalam tahapan ekstraksi ini. Penambahan belerang pada proses ini dimaksudkan sebagai penghambat pencoklatan dan untuk mengawetkan pati. Mekanisme kerja belerang dalam menghambat pencoklatan adalah Ion bisulfit bereraksi dengan enzym dalam sel membentuk ion kompleks enzym sulfat sehingga enzym tidak dapat mengkatalisa terjadinya reaksi pencoklatan. Sulfat menghambat hidroksilasi oksidatif sehingga mencegah pembentukan senyawa melanoidin (penyebab warna coklat).
pelarutnya. Dari hasil olahan separator I, II kemudian dialirkan menuju ekstraktor III (final extractor) untuk disaring dan dipisahkan kembali dari ampasnya yang masih tersisa dengan ukuran saringan 250 mesh. Ekstraktor III merupakan proses penyaringan terakhir, dengan hasil akhir berupa susu pati berwarna putih.
Hasil samping (limbah padat) yang didapatkan dari proses ekstraksi kemudian akan diolah kembali didalam bubur ekstraktor (pulp ectractor) untuk dipisahkan antara air dengan ampas. Air yang didapatkan akan dialirkan menuju mesin pemarut sedangkan ampasnya kemudian akan dipress dengan mesin pengepres (pulp press) dan akan dihasilkan hasil akhir berupa limbah padat.
7) Pemurnian (refining)
Pemisahan sari pati dari pelarutnya dilakukan dengan tujuan agar susu pati hasil penyaringan dari ekstraktor lebih kental sehingga kandungan pati pada susu pati tersebut lebih besar. Sebenarnya selain terjadi pemisahan sari pati, pada proses pemurnian ini juga dilakukan proses pembersihan terhadap susu pati yang kental dan bersih. Semakin kental susu pati yang dihasilkan maka akan semakin banyak pati basah yang diperoleh.
penyaringan ekstraktor III (final extractor) kemudian dialirkan menuju mesin separator III dan IV (final separator).
8) Pengendapan (de-hidrating)
Sari pati dihasilkan dari pemisahan sari pati oleh separator III, IV yang masih berbentuk susu pati tersebut kemudian diendapkan pada mesin centrifuge dengan perlakuan pemusingan sehingga saripati terpisah dari seluruh pelarutnya, akhirnya yang tertinggal hanya endapan berupa pati basah yang siap dikeringkan. Proses pengendapan ini berlangsung sekitar empat menit untuk selanjutnya dilakukan penghamburan dengan mengikis seluruh endapan pati basah yang menempel pada seluruh permukaan bagian dalam mesin centrifuge.
Hasil penghamburan tersebut menghasilkan sekitar 50 kg pati basah setiap empat menitnya. PT Sukoharjo Makmur Abadi dalam proses pengolahannya menggunakan empat mesin centrifuge.
9) Pengeringan (drying)
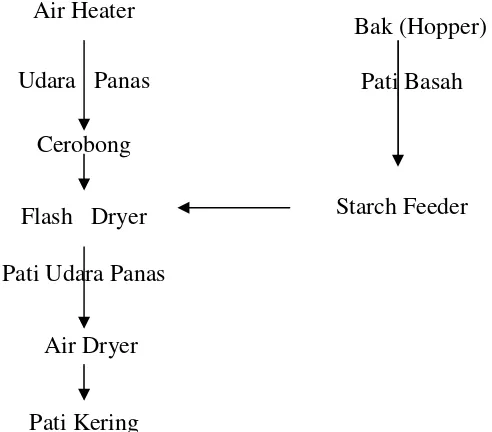
Gambar 2.2 Urutan Proses Pengeringan Tapioka Sumber PT. Sukoharjo Makmur Abadi
Maksud dari bagan proses pengeringan tapioka diatas yaitu udara panas yang diperlukan untuk proses pengeringan dihasilkan pada air heater, selanjutnya udara panas tersebut akan dibawa oleh flash dryer
melalui cerobong air heater. Pati yang akan dikeringkan masuk ke flash dryer dengan starch feeder sehingga udara panas dan pati basah akan tercampur, selama pati tersebut menuju air dryer merupakan tempat pengeringan pati yang terakhir, dalam tahapan ini pati dapat diatur tingkat kekeringan dengan mengatur banyaknya masukan pati tiap detiknya.
Air Heater Udara Panas
Cerobong Flash Dryer Pati Udara Panas
Air Dryer
Pati Kering
Flash Dryer Starch Feeder
10)Pengayakan dan Pengepakan (grading and packing)
Tujuan pengayakan adalah untuk memisahkan fraksi pati yang halus dengan fraksi yang kasar, sesuai dengan tingkat kualitas yang diharapkan. Untuk kualitas A dan B adalah 99% harus melewati saringan 140 mesh dan untuk kualitas C adalah 99% harus melalui saringan 80 mesh.
Pati yang sudah dikeringkan dalam oven tersebut masih dalam keadaan panas sehingga diperlukan proses pendinginan terhadap pati pada mesin pendingin (cooling syclone). Kemudian pati tersebut diayak dengan menggunakan saringan berukuran 80 mesh supaya lebih halus dan bersih. Sementara itu, sebelum dilakukan pengemasan diadakan pengujian terlebih dahulu uji kontrol terhadap kualitas pati yang meliputi uji kadar air dan uji warna.
Pengepakan dilakukan pada karung-karung yang terbuat dari bahan plastik dengan ukuran 50 kg. setelah dilakukan pengepakan dilanjutkan dengan sistem penggundangannya, yaitu produk tapioka yang siap dipasarkan diatur secara bersusun diatas balok kayu untuk menghindari kontak langsung dengan lantai sehingga kelembatan pati tetap terjaga.
d. Limbah Industri Tapioka
organik, ada 3 macam limbah, yaitu limbah cair, limbah cair, limbah padat dan limbah gas. Limbah cair industri tapioka banyak mengandung pati terlarut, asam hidrosianat (HCN) yang mudah terurai menjadi sianida, nitrogen, fosfor dan senyawa organik. Menurut Mahida (1995), pada prinsipnya penangangan limbah industri pangan adalah meredoksi kandungan bahan organik yang terlarut berdasarkan penanganan secara fisika, kimia, biologis.
1) Limbah padat
Limbah padat terdiri dari dua jenis yaitu :
a) Limbah kulit yang didapatkan dari proses pembersihan singkong. Adapun penanganannya dengan dijual kepada konsumen untuk pakan ternak.
b) Limbah dari ampas atau onggok yang didapat proses pemarutan dan pengepresan.
2) Limbah cair
Limbah cair ini dihasilkan dari proses pencucian bahan sebelum pemarutan, air hasil kerja separator yang memisahkan pati kental dari air pelarutnya maupun dari pembersihan peralatan. Masalah yang ditimbulkan dari limbah cair adalah pencemaran bau dan keasaman.11 3. Karbohidrat
gandum, jagung, beras, kentang dan padi-padian lainnya, buah serta sayuran. (Fessenden, 1997).
Karbohidrat merupakan sumber tenaga utama untuk semua fungsi tubuh gerakan-gerakan otot, pencernaan dan asimilasi makanan. Bilamana karbohidrat itu terikat dengan oksigen maka itu akan menghasilkan panas yang diperlukan untuk mempertahakan suhu tubuh yang stabil. Karbohidrat terdapat dalam berbagai jenis makanan seperti gula, tepung, padi-padian dan selulosa (Simorangkir, 1994).
4. Glukosa
Pengubahan glukosa menjadi asam laktat atau etanol berlangsung dalam beberapa tahap yang masing-masing tahapnya dikatalis oleh enzim jalur glikolisa dan fermentasi alkohol itu disusun oleh embeden, menyerhof dan parnas yang kemudian dikenal dengan jalur EMP (Winarno, 1997).
Glukosa suatu gula monosakarida merupakan salah satu karbohidrat penting yang digunakan sebagai sumber tenaga bagi hewan maupun tumbuhan. Proses penguraian glukosa menjadi piruvat, alkohol, CO2 dan air dapat berlangsung melalui beberapa jalan metabolisme, tergantung dari keadaan lingkungan, keadaan dalam sel atau macam jasadnya satu macam jasad dapat melakukan atau lebih jalur metabolisme penguraian tersebut. (Wirahadikusuma, 1995).
5. Fermentasi
yaitu enzim yang dihasilkan oleh mikroba hidup tertentu. Untuk berlangsungnya proses fermentasi oleh suatu mikroba perlu adanya medium fermentasi yang mengandung nutrien untuk pertumbuhan, bahan pembentuk sel, dan biosintesis produk-produk metabolisme (Rahman, 1989). Berdasarkan produk yang difermentasi digolongkan menjadi 2 macam yaitu sebagai berikut:
a. Fermentasi alkoholis adalah fermentasi yang menghasilkan alkohol sebagai produk akhir disamping produk lainnya misalnya pada pembuatan wine, tape.
b. Fermentasi non alkoholis adalah fermentasi yang tidak menghasilkan alkohol sebagai produk akhir selain bahan lainnya misalnya pembuatan tempe, antibiotika dan lain-lain (Rukmana dan Yuniarsih, 2001).
6. Saccharomyces cerevisieae
Produsen utama alkohol adalah ragi terutama dari strain Saccharomyces cerevisieae. Ragi-ragi seperti juga kebanyakan fungi merupakan organisme yang bersifat aerob. Dalam lingkungan terisolasi dari udara, organisme ini meragika karbohidrat menjadi etanol dan CO2. ragi sendiri merupakan organisme aerob pada kondisi an aerob. Dengan mengalirkan udara, maka peragian dapat dihambat sempurna dengan memasukkan banyak udara (Schlegel, 1994).
penguncupan multiteral. Konjugasi isogami atau heterogami dapat mendahului atau dapat terjadi setelah pembentukan askus. Dapat berbentuk tonjolan, setiap askus dapat mengandung satu sampai empat spora dengan berbagai bentuk, spora dapat berkonjugasi. Disimilasi berlangsung dari oksidatif yang disukai sampai kepada fermentasi yang dominan. Dalam biakan cair biasanya terjadi pertumbuhan didasar cincin dan partikel dapat berbentuk dengan waktu yang lebih panjang. Senyawa-senyawa gula yang umum biasanya difermentasikan dengan kuat, nitrat tidak diasimilasikan kebanyakan Khamir Industri tergolong dalam genos Saccharmyces contohnya adalah Saccharomyces cerevisiae (Pelczar dan Chan, 1988).
7. Asam Sulfat
Asam sulfat (H2SO4) sangat penting dalam industri dan dibuat dalam jumlah yang lebih besar daripada asam lain. Asam sulfat adalah cairan yang tidak berwarna seperti minyak dan higroskopik dengan berat jenuh 1,838 gr/mL. Asam pekat yang murni dan komersial adalah suatu campuran bertitik didik konstan, dengan titik didih 3380C dan mengandung asam kira-kira 98%. Cairan dapat bercampur dengan air dalam semua perbandingan dengan melepaskan panas yang banyak sekali (Setiono dan Pudjaatmaka, 1985).
8. Etanol
Etanol disebut alkohol karena dapat diperoleh dengan cara fermentasi dari padi-padian. Sebenarnya fermentasi dari semua bahan yang mengandung karbohidrat seperti anggur dan kentang juga padi menghasilkan etanol. Etanol yang dipakai untuk minuman dan gosohol masih dibuat secara fermentasi, Etanol yang dipakai sebagai pelarut dibuat dengan hidrasi dari etilen suatu zat petrokimia yang didapat dari reaksi pemecahan minyak bumi (Fessenden, 1997).
Alkohol merupakan cairan bening, mudah menguap mudah bergerak, tidak berwarna, bau khas dan rasa panas. Alkohol mudah terbakar dengan memberikan nyala berwana biru dan tidak berasap. Nama lain dari alkohol adalah aethanol, etanol, aethyl alkohol (Wresniwiro, 1999).
B. Kerangka Pemikiran
Gambar 3.1 Kerangka Pemikiran
C. Hipotesis
Dosis ragi dan waktu fermentasi yang berbeda berpengaruh terhadap dan kadar bioetanol pada fermentasi tepung umbi ketela pohon (Manihot utilissima pohl) dengan penambahan H2SO4.
Dihidrolisis + H2SO4
Fermentasi Destilasi Bioetanol
Ragi / khamir Sisa pengolahan tepung kanji
BAB III
METODE PENELITIAN
A. Tempat dan Waktu Penelitian 1. Tempat Penelitian
Penelitian lapangan dilakukan di Desa Sawur Kecamatan Polokarto Kabupaten Sukoharjo sedangkan destilasi dilaksanakan di Laboratorium Kimia Fakultas Ilmu Pendidikan Universitas Sebelas Maret. Uji kadar alkohol dilaksanakan di Laboratorium Kimia Fakultas Ilmu Kesehatan Universitas Muhammadiyah Surakarta.
2. Waktu Penelitian
Penelitian dilaksanakan pada bulan Desember 2008 sampai dengan Februari 2009.
B. Alat dan Bahan
1. Alat yang digunakan dalam penelitian ini adalah :
a. Alat yang digunakan untuk membuat tepung dan fermentasi antara lain pisau, tampah, mesin penggiling tepung, kompor, baskom, panci, sendok, gelas ukur, timbangan analitik, penyaring, toples, plastik.
b. Alat untuk mengukur kadar alkohol antara lain tabung reaksi, spektrofotometer, waterbath, pipet volume, gelas ukur, alat destilasi, tiang statis, labu ukur 100 mL dan 250 ml, termometer.
2. Bahan yang digunakan untuk penelitian ini adalah :
b. Bahan yang digunakan untuk uji etanol antara lain limbah padat tapioka kering dihaluskan hasil fermentasi dan alkohol hasil destilasi, kalium karbonat (K2CO3), alkohol 90% dan kalium dikarbonat K2 (CO3)2.
C. Prosedur Penelitian
1. Pembuatan Fermentasi Ketela Pohon
a. Menyiapkan ampas umbi ketela pohon, kemudian mengeringkan ampas umbi ketela pohon.
b. Menggiling ampas umbi ketela pohon yang telah kering untuk dijadikan tepung dan ditimbang masing-masing 500 gr. Untuk masing-masing perlakuan ada 12 perlakuan, jadi ampas yang dibutuhkan ada 6.000 gr. c. Mencampurkan limbah tapioka padat kering dihaluskan dengan
perbandingan 1 : 5 dan menambahkan H2SO4 8%.
d. Merebus campuran pada panci dengan api sedang dan mengaduknya secara terus menerus sampai campuran berwarna kecoklatan.
e. Membiarkan limbah tapioka padat kering dihaluskan yang telah direbus tadi selama 1-2 jam hingga benar-benar dingin.
f. Setelah dingin, sebelumnya pH dari bahan dinetralkan dengan penambahan NaOH, setelah itu pH diturunkan kembali dengan menggunakan H2SO4 sampai pH menjadi 4,5 – 5,5.
h. Mencampur bahan ragi NKL yang sudah dibuat starter, masing-masing
dengan dosis yang telah ditentukan
gr
i. Memasukkan bahan ke dalam toples, lalu menutup toples dengan plastik. j. Menginkubasi bahan masing-masing selama 5, 7 dan 9 hari.
2. Destilasi alkohol
a. Mengambil sampel atau bahan hasil fermentasi lalu memasukkan ke dalam alat destilasi alkohol.
b. Mendestilasi alkohol dengan cara memanaskan masing-masing bahan hasil fermentasi sampai mendidih pada suhu 70-800C.
c. Mengembunkan uap hasil destilasi tersebut dan menampungnya dalam tabung penampung.
d. Apabila uap sudah tidak menetes lagi, kemudian mengambil hasil destilasi tersebut dan menyimpannya dalam botol.
3. Analisis Kadar Alkohol
a. Menyiapkan larutan dari hasil destilasi fermentasi limbah tapioka padat kering dihaluskan.
b. Menuang alkohol pada tabung reaksi dan mengukurnya dengan alokolmeter.
c. Memasukkan larutan alkohol tersebut sebanyak 1mL kedalam tabung reaksi yang telah diberi kalium karbonat, kalium dikarbonat dan etanol. d. Memasukkan tabung reaksi tersebut kedalam waterbath selama 2 jam
e. Setelah diinkubasi selama 2 jam kemudian diujikan pada spektrofotometer dan membaca kadar alkohol yang tertera.
D. Rancangan Percobaan
Rancangan percobaan yang dilakukan dalam penelitian ini adalah menggunakan RAL (Rancangan Acak Lengkap) pola faktorial yang terdiri dari 2 faktor yaitu waktu fermentasi dan dosis ragi dengan syarat perlakuan:
Faktor I : Waktu fermentasi (W) W1 : Waktu fermentasi 5 hari W2 : Waktu fermentasi 7 hari W3 : Waktu fermentasi 9 hari Faktor 2 : Dosis Ragi (D)
D0 : Dosis tanpa ragi dan H2SO4 D1 : Dosis ragi 25/500gr
D2 : Dosis Ragi 50/500 gr D3 : Dosis ragi 75/500gr
Tabel 3.1 Kombinasi perlakuan pada tepung umbi ketela pohon. D
W D0 D1 D2 D3
W1 W1D0 W1D1 W1D2 W1D3
W2 W2D0 W2D1 W1D2 W2 D3
W3 W3D0 W3D1 W1D3 W3 D3
Keterangan :
W1D1 : Waktu fermentasi 5 hari dengan dosis ragi 25gr/500gr ( 5%)
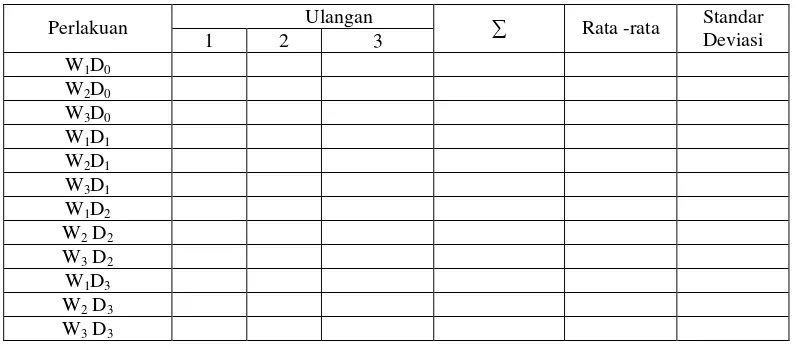
Dari Kombinasi Perlakuan Sehingga Diperoleh 12 Kombinasi Tabel 3.2 Data Perlakuan Kadar Alkohol (%)
Ulangan
E. Teknik Pengumpulan Data
2. Observasi, yaitu melakukan pengamatan langsung dilapangan pada proses pengolahan tepung tapioka dan limbahnya.
3. Studi pustaka, yaitu dengan mengumpulkan referensi dan kepustakaan sebagai dasar penelitian dan untuk memperkuat hasil penelitian.
F. Analisis Data
Analisis data yang digunakan adalah analisis deskriptif kuantitatif yaitu berupa angka atau data kadar alkohol hasil fermentasi limbah tapioka padat kering dihaluskan. Pengolahan data dilakukan dengan menggunakan analisis varian dua jalur untuk mengetahui perbedaan antara perlakuan. Adapun langkah-langkah analisis varian dua jalur yaitu sebagai berikut:
1. Menghitung faktor korelasi (FK)
(
)
2. Menghitung Jumlah Kuadrat total (KT)
=
3. Menghitung jumlah kuadrat perlakuan (JKp)
(
)
FK r
X
JKp= ij −
4. Menghitung jumlah kuadrat variabel A (JKA)
5. Menghitung jumlah kuadrat variabel B (JKB)
6. Menghitung jumlah kuadrat variabel A dan B (JKAB) JK AB= JKp - JKA – JKB
7. Mencari jumlah kuadrat galad (JKG) JKG = JKT - JKA- JKB- JKAB
14.Menghitung kuadrat tengah perlakuan (KTp)
15.Menghitung kuadrat tengah variabel A (KTA)
16.Menghitung kuadrat tengah variabel B (KTB)
B
17.Menghitung kuadrat tengah variabel A dan B (KTAB)
G
18.Menghitung kuadrat tengah galat (KTG)
G
19.Menghitung F hitung Variabel perlakuan (FP)
Untuk selanjutnya dari masing-masing harga Fhitung yang diperoleh dikonsultasikan dengan harga F pada tabel sehingga sebaran bebas F adalah (K-1) (n-K) dan pada taraf nyata = 0,05. bila Fhitung ternyata lebih besar dari F tabel maka Ho ditolak.
BAB IV
HASIL DAN PEMBAHASAAN
A. Hasil
Berdasarkan hasil penelitian yang dilakukan tentang kualitas bioetanol limbah tapioka padat kering dihaluskan (tepung) dengan penambahan ragi dan H2S04 pada lama fermentasi yang berbeda dapat disajikan sebagai berikut:
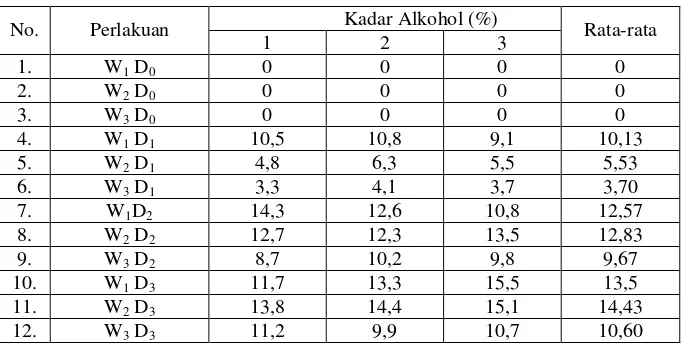
Tabel 4.1 Kadar Alkohol (%), Limbah tapioka padat kering dihaluskan dengan penambahan ragi dan H2S04 pada lama fermentasi yang berbeda.
Kadar Alkohol (%)
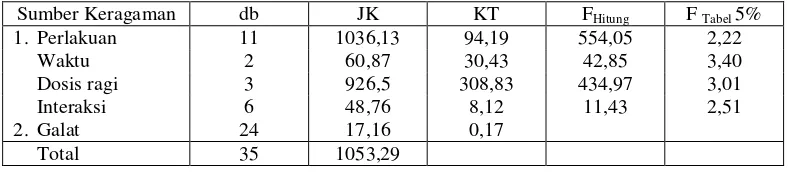
Tabel 4.2 : Hasil uji Anava dua jalur diatas bioetanol limbah tapioka padat kering dihaluskan dengan penambahan ragi dan H2 SO4 pada lama Fermentasi yang berbeda
Sumber Keragaman db JK KT FHitung F Tabel 5%
1. Perlakuan 11 1036,13 94,19 554,05 2,22
Waktu 2 60,87 30,43 42,85 3,40
Dosis ragi 3 926,5 308,83 434,97 3,01
Interaksi 6 48,76 8,12 11,43 2,51
2. Galat 24 17,16 0,17
Total 35 1053,29
Keputusan Uji Anava dua jalur adalah :
1. FHitung > Ftabel (42,85 > 3,40), berarti signifikan yaitu waktu fermentasi (5, 7, 9 hari berpengaruh terhadap kadar alkohol. Limbah tapioka padat kering dihaluskan.
2. FHitung > Ftabel (434,97 > 3,01), berarti signifikan yaitu dosis ragi yang berbeda (25 gr, 50 gr dan 75 gr) berpengaruh terhadap kadar alkohol limbah tapioka padat kering dihaluskan.
3. Fhitung > Ftabel (11,43 > 2,51), berarti signifikan yaitu diinteaksi antara waktu fermentasi dan dosis ragi terhadap kadar alkohol. Limbah tapioka padat kering dihaluskan.
Karena hasil Fhitung > Ftabel maka dapat data tersebut adalah signifikan sehingga dilanjutkan dengan uji Duncan’s Multiple Range Test (DMRT) untuk mengetahui beda nyata antar perlakuan
B. Pembahasaan
0 5 10 15
1 2 3 4 5
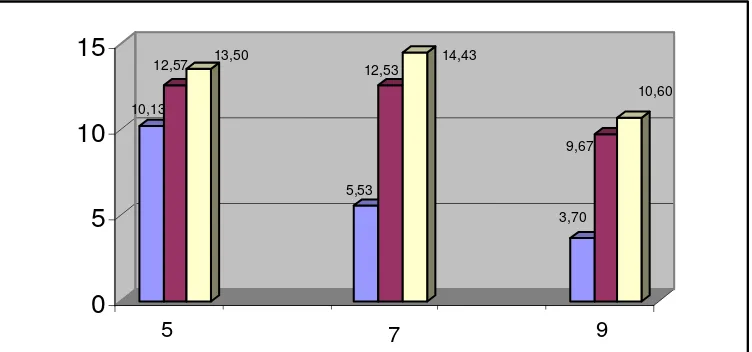
menunjukkan bahwa kadar alkohol tertinggi terdapat pada W2D3 ( 7 hari/75 gr) dengan kadar alkohol mencapai 14,43%. Ditinjau dari segi waktu fermentasi (W) dan dosis ragi (D), limbah tapioka padat kering dihaluskan yang difermentasikan selama 7 hari dan dosis ragi 75 gram (W2D3) menghasilkan kadar alkohol tertinggi yaitu 14,43%, kemudian waktu 7 hari dan dosis ragi 5 gr/500 gr (W1D2) yaitu 12,83%, terendah pada hari dengan dosis ragi 25 gr/500gr (W3D1) yaitu 3,70%. Data hasil penelitian tersebut juga dapat digambarkan dalam histogram berikut:
Waktu Fermentasi (Hari) : dosis ragi 25 gr/500 gr
: dosis ragi 50 gr/500 gr : dosis ragi 75 gr/500 gr
Gambar 4.1 Histrogram kadar alkohol limbah tapioka padat kering dihaluskan dengan penambahan ragi dan H2S04 pada lama fermentasi yang berbeda.
5 7 9
10,13
12,57 13,50
5,53 12,53
14,43
3,70 9,67
Untuk mengetahui hasil penelitian tersebut signifikan atau tidak maka dilakukan uji anava dua jalur dan dilanjutkan dengan uji DMRT. Berdasarkan uji anava dua jalur dengan taraf signifikan 5% (tabel 4.1), menunjukkan bahwa waktu fermentasi, dosis ragi dan interaksi antara waktu fermentasi dengan dosis ragi adalah signifikan, sehingga berpengaruh terhadap kadar alkohol pada lama fermentasi yang berbeda. Kadar alkohol yang dihasilkan dipengaruhi oleh waktu atau lama fermentasi. Dari lama fermentasi 5,7, dan 9 hari dapat diketahui bahwa perbedaan kadar alkohol ditunjukkan dari hasil uji anava dua jalur tabel (4.2), bahwa Fhitung > Ftabel (42,85 > 3,40) pada taraf signifikan 5%.
Hasil pengukuran kadar alkohol pada fermentasi 7 hari adalah yang paling tinggi mencapai 14,43%. Dibandingkan dengan waktu fermentasi 5 hari dan 9 hari. Hal ini dikarenakan proses fermentasi pada limbah tapioka padat kering dihaluskan mencapai titik waktu yang optimum untuk menghasilkan kadar alkohol tertinggi pada hari ke-7.
Hasil penghitungan Fhitung > ftabel yaitu 434,97 > 3,01 pada taraf signifikansi 5%. Hal ini menunjukkan bahwa dosis ragi yang berbeda yaitu 25 gr, 50 gr, dan 75 gr sangat berpengaruh terhadap kadar alkohol limbah tapioka padat kering dihaluskan. Hasil penghitungan Fhitung > Ftabel yaitu 11,43 > 2,51 pada taraf signifikan 5%. Hal ini menunjukkan bahwa ada interaksi antara waktu fermentasi (5 hari, 7 hari dan 9 hari) dan dosis ragi terhadap kadar alkohol limbah tapioka padat kering dihaluskan.
berbeda-beda yaitu ragi, ragi dan asam sulfat (H2S04). Sehingga penambahan inokulum yang tersebut juga dapat mempengaruhi tinggi rendahnya kadar bioetanol yang dihasilkan. Selain itu, juga dipengaruhi oleh cepat lambatnya pertumbuhan sel ragi yang digunakan dalam fermentasi bahan. Cepat lambatnya pertumbuhan khamir dapat dipengaruhi oleh faktor, yaitu komposisi media yang digunakan sebagai media pengembangbiakan mikroba mulai persiapan sampai fermentasi dapat berjalan optimum. Suhu yang baik untuk fermentasi maksimum adalah 300C. semakin rendah suhu fermentasi maka semakin banyak alkohol yang dihasilkan, karena pada suhu rendah fermentasi akan lebih kompleks dan kehilangan alkohol yang terbawa gas CO2 akan lebih sedikit.
Dari hasil penelitian uji kadar bioetanol ini juga ditambahkan asam sulfat (H2S04) yang bersifat sebagai katalisator. Katalisator merupakan zat yang ditambahkan kedalam suatu reaksi dengan maksud memperbesar reaksi.
Khamir Saccharomyces cerevisieae tidak memerlukan O2 dalam proses pengubahan organik yang satu menjadi organik yang lain yaitu gula menjadi alkohol. Dalam lingkungan terisolasi udara, organisme ini meragikan karbohidrat menjadi etanol dan CO2.
BAB V
KESIMPULAN DAN SARAN
A. Kesimpulan
Berdasarkan hasil penelitian dan pembahasan dalam penelitian ini dapat diambil kesimpulan sebagai berikut:
1. Ada interaksi antara waktu fermentasi (5 hari, 7 hari dan 9 hari) dan dosis ragi terhadap kadar alkohol limbah tapioka padat kering dihaluskan.
2. Kualitas bioetanol limbah tapioka padat kering dihaluskan (tepung) dengan penambahan ragi dan H2S04 pada lama fermentasi yang berbeda yang tertinggi adalah pada waktu fermentasi 7 hari dengan dosis ragi 75 gram/500 gram yaitu 14,43 %.
3. Kualitas bioetanol terendah adalah waktu fermentasi 9 hari dengan dosis ragi 25 gram/500 gram yaitu 3,70%.
4. Proses fermentasi limbah tapioka padat kering dihaluskan mencapai titik waktu yang optimum dalam menghasilkan kadar alkohol tertinggi adalah pada hari ke-7.
B. Saran
DAFTAR PUSTAKA
Amos, Simorangkir, 1994. Terapi Gizi Untuk Penyakit Kardiovaskuler. Bandung: Universal Offset Bandung.
Anonim, 2008. http://id.wikipedia.org/wiki/asamsulfat (Diakses tanggal 20 Nopem ber 2008).
, 2008. http://id. Wikipedia. Org/Wiki/Dehidrasi Alkohol
Indah, Sari, Pramesti. 2007. Pengaruh Waktu Fermentasi dan Dosis Ragi Terhadap Kadar Alkohol Hasil Fermentasi Ampas Umbi Ketela Karet (Manihot Glaziovii Muell). Skripsi. Jurusan Pendidikan Biologi FKIP. Surakarta: Universitas Muhammadiyah Surakarta.
Fessenden RJ dan Fessenden Js. 1997. Dasar-dasar Kimia Organik Jakarta: Binapura Aksara.
Mahida, U N. 1995. Pencemaran Air Dan Pemanfaatan Limbah Industri. Jakarta: CV Rajawali.
Mulyohardjo, M. 1987. Teknologi Pengolahan Pati, Yogyakarta: UGM Muhammad, Pelczar. M.J, dan Chan, E.C.S. 1988. Dasar-dasar Mikrobiologi. Jakarta: UI Press. Rahmat Rukmana dan Yuniarsih. 2001. Aneka Olahan Ubi Kayu. Yogyakarta:
Kanisius.
Schlegel, H.G. 1994. Mikrobiologi Umum. Yogyakarta: Gadjah Mada University Press.
Setiono, L.A dan Hadyana. P.1985. Buku Analisis Anorgonik Kualitatif Makro dan Semimikro Jilid II Edisi ke-5, Jakarta: PT Kalman Media Pustaka.
Steenis, Van, J. 2005. Flora, Jakarta: PT. Pradnya Paramita
Sugiarti. 2007. Pengaruh Waktu Fermentasi Dan Dosis Ragi Terhadap Kadar Alkohol Pada Fermentasi Sari Umbi Ketela Pohon (Manihot Utilissima Poh) Varietas Randu. Surakarta: Universitas Muhammadiyah Surakarta.
Tatik Kristiyaningsih. 2008. Kadar Glukosa dan Kadar Bioetanol Pada fermentasi Tepung Umbi Ketela Pohon (Manihot utiltssima Pohl) Dengan penambahan H2SO4. Surakarta: Universitas Muhammadiyah Surakarta.
Winarno. 1997. Kimia Pangan dan Gizi. Jakarta: PT Gramedia Pustaka.
LAMPIRAN
TWO WAY ANOVA/DUA JALUR Tabel satu arah dengan perlakuan kombinasi dua faktor
Ulangan (%) No. Perlakuan
1 2 3 Jumlah Rata-rata
1. W1Do 0 0 0 0 0
2. W1D1 10,5 10,8 9,1 30,4 10,13
3. W1D2 14,3 12,6 10,8 37,7 12,57
4. W1D3 11,7 13,3 15,5 40,5 13,5
5. W2Do 0 0 0 0 0
6. W2D1 4,8 6,3 5,5 16,6 5,53
7. W2 D2 12,7 12,3 13,5 38,5 12,83
8. W2D3 13,8 14,4 15,1 43,3 14,43
9. W3 Do 0 0 0 0 0
10. W3 D1 3,3 4,1 3,7 11,1 3,70
11. W3D2 8,7 10,2 9,8 28,7 9,67
12. W3 D3 11,2 9,9 10,7 31,8 10,60
278,6: 36 = 7,73
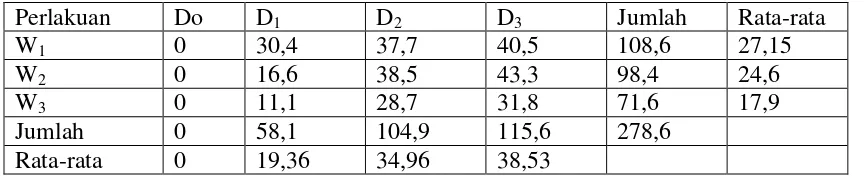
Data tersebut kemudian dapat diringkas dalam tabel 2 arah sebagai berikut :
Perlakuan Do D1 D2 D3 Jumlah Rata-rata
W1 0 30,4 37,7 40,5 108,6 27,15
W2 0 16,6 38,5 43,3 98,4 24,6
W3 0 11,1 28,7 31,8 71,6 17,9
Jumlah 0 58,1 104,9 115,6 278,6
PERHITUNGAN ANALISIS RAGAM 1. Menghitung Jumlah Kuadrat (JK)
a. (Faktor Koreksi)
b. Jumlah Kuadrat Total (JKT)
c. Jumlah Kuadrat Perlakuan (JKP)
e. Jumlah Kuadrat Variabel B (Dosis Ragi)
f. Jumlah Kuadrat Interaksi antar Variabel A dengan Variabel B JKAB= JKp - JKA- JKB
= 1036,13 – 60,87 – 926,5 = 48,76
g. Jumlah Kuadrat Galat JKG = JKT – JKp
= 1053,29 – 1036,13 = 17,16
j. dbB = Macam Dosis ragi -1
3. Menghitung Kuadrat Tengah (KT) a. (Kuadrat Tengah Perlakuan)
p
b. Kuadrat Tengah Variabel A
A
c. Kuadrat Tengah Variabel B
d. Kuadrat Tengah Variabel A dengan Variabel B
e. Kuadrat Tengah Galat
G
4. Menghitung F. Hitung
d.
Dari perhitungan diatas kemudian diringkas dalam tabel Anova sebagai berikut: Sumber Keragaman db JK KT FHitung F Tabel 5%
UJI DUNCAN’S
1. Rata-rata setiap perlakuan berdasarkan ranking
Ragam Rata-rata
2. Menghitung Standar error rata-rata perlakuan
r
3. Nilai Rp (P,V) pada tabel Duncan’s
5. Membandingkan Setiap Perbedaan rata-rata perlakukan dengan SSD masing-masing
Rerata Beda Jarak Nyata
GAMBAR BAHAN DAN ALAT-ALAT PENELITIAN
Limbah tapioka padat kering dihaluskan Singkong
Asam sulfat NaOH
Timbangan analitik Gelas ukur, pipet, termometer
Hasil Pemasakan Proses Peragian
Proses Destilasi