Indonesia Chimica Acta, , ISSN 2085 014X Vol. 3. No. 2, December 2010
Cd2+
! "# $$! % " " &&'(# (& ) #
1
Prodi PGSD FIP Universitas Negeri Makassar, Sulawesi Selatan JL. Monumen Emmy Saelan III Makassar
2
Jurusan Kimia FMIPA Universitas Hasanuddin, Makassar, Sulawesi Selatan Jl. Perintis Kemerderkaan Tamalanrea Makassar
* +! Pola pertumbuhan fitoplankton nannochloris dalam medium conwy yang terpapar ion logam Cd2+. Dalam penelitian ini, telah diselidiki interaksi ion logam Cd2+ yang dipaparkan dalam medium conwy pada kultur fitoplankton jenis nannochloris. Seri kultur dilakukandengan dan tanpa penambahan ion logam Cd2+. Pengamatan terhadap pola pertumbuhan nannochloris akan ditentukan parameter laju pertumbuhan spesifik, persentasi hambatan pertumbuhan, dan uji toksisitas. Hasil penelitian menunjukkan bahwa pola pertumbuhan nannochloris pada medium conwy tanpa penambahan ion logam Cd2+ (kontrol) mempunyai kurva pertumbuhan paling tinggi. Pada medium kultur yang ditambahkan ion logam Cd2+0,25 mg/L memperlihatkan grafik pola pertumbuhan yang relatif sama dengan kontrol. Pada penambahan konsentrasi ion logam Cd2+ di atas 0,25 mg/L, dapat menurunkan laju pertumbuhan spesifik nannochloris yang diperkuat dengan meningkatnya harga hambatan pertumbuhan spsifiknya (PGI). Hasil analisis statistik uji beda terhadap blanko pada pemaparan ion logam Cd2+ terhadap nannochloris mengindikasikan bahwa konsentrasi ion logam Cd2+yang tidak mempengaruhi pertumbuhan nannochloris adalah pada konsentrasi 0,01 hingga 0,25 ppm; dan harga konsentrasi tertinggi yang dapat ditoleransi (MTC) oleh nannochloris pada konsentrasi 0,25 ppm dan konsentrasi ion logam Cd2+ yang menyebabkan penurunan laju pertumbuhan sebesar 50 % relatif terhadap blanko EC50 = 0,849 ppm.
Kata Kunci: Nannochloris, ion logam Cd2+, laju pertumbuhan spesifik.
* +! ,+ The pattern of phytoplankton growth in the medium Conwy nannochloris exposed metal ions Cd2+ In this research, has investigated the interaction of metal ions Cd
2 +
are presented in Conwy in the medium culture of phytoplankton nannochloris types.The series of Culture have been done with and without addition of metal ions Cd2+.. Observation of growth patterns nannochloris using parameters to be determined specific growth rate, percentage of growth inhibition, and toxicity test. The results showed that the pattern of growth in the medium Conwy nannochloris without the addition of metal ions Cd 2 + (Control) had the highest growth curve. In the medium culture which added with the metal ions Cd 2 + 0,25 mg/L the curve of relative growth patterns similar to controls. In addition the concentration of metal ions Cd 2 + above 0.25 mg / L, can decrease the specific growth rate nannochloris reinforced by rising prices spsifiknya growth inhibition (PGI). The result of statistical analysis of differencial test against the standart at the exposure of metal ion Cd 2 + to nannochloris indicate that the concentration of metal ions Cd 2 + which does not affect the growth nannochloris is the concentration of 0.01 to 0.25 ppm, and the number of the highest concentration that can be tolerated by nannochloris at a concentration of 0.25 ppm and the concentration of metal ions Cd2+ which causes a decrease in growth rate of 50% relative to the standart at EC50 at 0.849 ppm.
Key Words: Nannochloris, Metal ion Cd2+, spesific growth inhibition (PGI).
*
Fitoplankton merupakan tumbuhan renik, terdiri dari berbagai jenis dengan sifat sifat yang berbeda. Dalam siklus makanan di perairan, fitoplankton berperan sebagai "primary producer" yang merupakan sumber makanan bagi zooplankton, kemudian zooplankton ini dimangsa oleh hewan hewan yang lebih besar dan selanjutnya ke manusia. Di sisi lain, keberadaan ion logam berat di perairan adalah sebagai partikel terlarut. Karena ukuran fitoplankton relatif kecil, maka interaksi antara fitoplankton dan ion logam berat di perairan akan berlangsung efektif. Oleh karena itu, fitoplankton merupakan faktor terpenting dalam transfer bahan bahan biologi, sebab mereka mewakili pion pertama masuknya pencemar ke dalam rantai makanan dan merupakan biomassa terbesar di perairan.
Meskipun efektifitas interaksi antara fitoplankton dan ion logam berat menghasilkan penyerapan yang tinggi, namun fitoplankton juga mempunyai kemampuan untuk bertahan hidup pada perairan yang tercemar ion logam berat. Hal ini menjadi petunjuk bagi beberapa
peneliti untuk memanfaatkan
fitoplankton sebagai fitoremediasi logam berat.
Kadmium (Cd) mempunyai
nomor atom 48, massa atom relatif 112,40 gram permol, dalam Tabel Periodik terdapat dalam golongan IIB bersama dengan Zn dan Hg. Di alam, keadaan stabil ditemui sebagai ion logam Cd2+, bergabung dengan ion logam Zn2+ dalam bentuk mineral karbonat dan sulfat. Dalam industri pertambangan logam Pb dan Zn, proses
pelumas, dan bahan bakar (Palar, 1994).
Moore dan Ramamoorthy (1984) mengungkapkan bahwa ion logam kadmium berikatan secara kovalen dan mempunyai afinitas yang tinggi terhadap gugus tiol, mendorong peningkatan kelarutan lemak, dapat terakumulasi dan bersifat racun.
Ion logam Cd2+ dapat
menghasilkan tekanan oksidatif terhadap produksi spesies oksigen reaktif (ROS) (Olmos, 2003), dan dapat memproduksi radikal bebas in vitro
dengan hadirnya H2O2 (Keyhani et al., 2006). Ion logam Cd2+ dalam konsentrasi tinggi, secara in vitro dapat juga merusak reaksi dapat balik protein (Keyhani et al., 2003) melalui pembentukan ikatan logam tiolat (Dafre
et al., 1996) dan terjadinya perubahan dinding sel atau permeabilitas membran oleh pengikatan terhadap gugus nukleofil (Ramos et al., 2002). Lebih lanjut, ion logam Cd2+ dapat mempengaruhi tanggapan antioksi dan dalam semua organ tumbuhan (Iannelli
et al., 2002), menyebabkan
pembentukan ROS secara langsung atau tidak langsung, sehingga mengganggu reaksi redoks dan mempengaruhi hilangnya produksi khlorofil (Baryla et al., 2001; Schutzendubel et al., 2002). Keberadaan ROS merupakan zat antara yang sangat beracun (cytotoxic) dan dapat bereaksi dengan lemak, protein dan asam asam nukleat sehingga menyebabkan peroksidasi lemak, kerusakan membrane, dan tidak aktifnya enzim.
Indonesia Chimica Acta, , ISSN 2085 014X Vol. 3. No. 2, December 2010
( & ( " + -(-"'+' (
Bahan yang digunakan dalam penelitian ini adalah sebagai berikut:
a. Bibit fitoplankton nannochloris dari kultur murni Balai Penelitian Perikanan dan Kelautan Maros, Sulawesi Selatan.
b. Bahan bahan kimia yang digunakan semua berkualitas analitik (analytical grade) meliputi: NaCl; MgSO4
Peralatan yang digunakan dibedakan atas: neraca analitik, mikroskop, haemocitometer
c. Alat lainnya meliputi: pompa vakum, oven, lumpang porselin, aerator, refirigator, selang plastik, balon Neon, thermometer, panel saringan diameter 47 mm, magnetik stirer,
Bibit murni fitoplankton
Nannochloris dikultur dalam gelas
Erlenmeyer 500 mL dengan
menggunakan medium Conwy. Selama pelaksanaan kultur, parameter fisika kimia dipertahankan meliputi penerangan lampu Neon 40 watt
diberikan secara terus menerus, gas CO2 dari aerator pompa udara, suhu antara 22 – 25oC, pH medium antara 8 – 9, dan salinitas 30 ‰. Seluruh peralatan dan bahan yang digunakan dalam kultur disterilkan terlebih dahulu.
Setelah pelaksanaan kultur 11 hari, bibit fitoplankton selanjutnya dikultur dalam botol kultur 1 liter. Merujuk pada hasil penelitian
Nurhamsiah, (2010) pada
Laboratorium kimia anorganik Universitas Hasanuddin Makassar, bahwa fitoplankton laut jenis
Nannochloris mempunyai
pertumbuhan yang optimum jika dikultur dengan kepadatan awal inokulasi sebesar 1.000.000 sel/mL.
Untuk mengetahui pola
pertumbuhan fitoplankton, dilakukan penghitungan jumlah sel per mililiter medium setiap hari. Sampel medium yang telah ditumbuhkan fitoplankton diambil dengan pipet tetes steril, diteteskan sekitar 0,5 mL pada
Haemocytometer, kemudian diamati melalui mikroskop (Seafdec, 1985). Bila kepadatan sel masih normal,
Pengamatan pengaruh ion logam Cd2+ pada pertumbuhan Nannochloris
spesifik untuk setiap variasi
konsentrasi dihitung dengan
menggunakan persamaan (2);
sedangkan untuk menentukan
persentasi hambatan pertumbuhan (Prosen Growth Inhibition, PGI) pada fitoplankton dengan menggunakan persamaan (3). spesifik; dan t adalah waktu (hari).
Dimana, PGI = Persentasi hambatan pertumbuhan, (i = Tetapan laju
pertumbuhan spesifik ke i, dan (0 =
Tetapan laju pertumbuhan spesifik kontrol.
' +$ ' '+ $( $1 . / & '+$/" ( +$(
Uji toksisitas ion logam Cd2+ terhadap pertumbuhan fitoplankton
nannochloris dilakukan dengan mengkultur fitoplankton pada kondisi optimum pada volume kultur 1000 mL. Parameter yang diamati meliputi uji (i)
Non Effect Concentration (NEC), yakni menentukan konsentrasi ion logam Cd2+ yang tidak mempengaruhi pertumbuhan fitoplankton; (ii)
Maximum Tolerable Concentration
(MTC), yakni menentukan konsentrasi maksimum ion logam Cd2+ yang dapat ditolerir oleh fitoplankton; dan Effect Concentration 50 % (EC50), yakni
menentukan konsentrasi ion logam Cd2+ yang menyebabkan penurunan laju pertumbuhan sebesar 50 % relatif terhadap blanko.
Berdasarkan hasil penghitungan kepadatan sel yang diperoleh,
ditentukan dan PGI setiap
konsentrasi ion logam Cd2+ yang dipaparkan, lalu dilakukan uji beda terhadap blanko pada tingkat konfidensi 99 %, maka akan diperoleh harga t '+ (1 untuk setiap nilai variasi konsentrasi ion logam Cd2+; lalu dibandingkan terhadap nilai ttabel.
Untuk nilai: t '+ (1 < t+ *-", maka: Nilai diperoleh dari harga terendah hingga tertinggi, Nilai diperoleh dari harga tertinggi dari nilai t '+ (1 < t+ *-" Nilai 45 diperoleh dengan meregresikan harga PGI terhadap konsentrasi ion logam Cd2+ yang dipaparkan.
-!+ .* ( '+$/" ( +$(
Hasil pengamatan pola
pertumbuhan fitoplankton laut
Nannochloris dalam medium Conway pada kondisi parameter fisika kimia dipertahankan meliputi penerangan 2 buah lampu TL 20 watt yang diberikan secara terus menerus pada jarak sekitar 75 cm, gas CO2 dari aerator pompa udara, suhu antara 20 – 22oC, pH medium antara 8 – 9 dan salinitas
medium 30 ‰ seperti yang
Indonesia Chimica Acta, , ISSN 2085 014X Vol. 3. No. 2, December 2010
Gambar 1. Pola pertumbuhan Nannochloris pada kondisi tanpa penambahan ion logam Cd2+
Berdasarkan Gambar 1
menunjukkan bahwa fitoplankton
Nannochloris mempunyai empat tahap
pertumbuhan. Nannochloris
membutuhkan waktu relatif singkat (sekitar 3 hari) untuk penyesuaian
terhadap medium pertumbuhan
Conway; sehingga pembelahan sel berlangsung optimal mulai hari ke 3 sampai hari ke 10. Dapat diungkapkan bahwa penggunaan medium Conway untuk mengkultur fitoplankton laut
Nannochloris pada kepadatan awal
1.000.000 sel/mL medium dapat
meningkat sekitar 28 kali
kepadatannya hanya dalam waktu 10 hari kultur.
Berdasarkan perhitungan
kepadatan sel dalam tiap mililiter
medium, dengan menggunakan
persamaan (2) diperoleh nilai tetapan laju pertumbuhan spesifik (O) fitoplankton Nannochloris yang dikultur dengan medium Conway seperti disajikan pada Tabel 1:
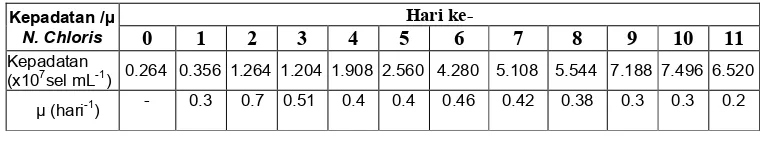
Tabel 1. Kepadatan sel dan tetapan laju pertumbuhan spesifik ( ) Nannochloris yang dikultur dengan menggunakan medium Conway
Kepadatan / !' -6
5 # 7 8 4 9 : ; < 5
Kepadatan
(x107sel mL1) 0.264 0.356 1.264 1.204 1.908 2.560 4.280 5.108 5.544 7.188 7.496 6.520
(hari1) 0.3 0.7 0.51 0.4 0.4 0.46 0.42 0.38 0.3 0.3 0.2
Berdasarkan Tabel 1, penebaran bibit Nannochloris dalam medium Conway mempunyai pola pertumbuhan yang relatif baik yakni kepadatan sel meningkat seiring dengan pemaparan hari kultur hingga hari ke 10. Karena masa pertumbuhan sel dibatasi oleh ketersediaan nutrien yang diberikan, maka pada hari ke 11 terjadi penurunan
jumlah sel dalam medium. Ditinjau dari laju pertumbuhan spesifik Nannochloris
memperlihatkan bahwa pertumbuhan yang cepat terjadi pada hari ke 3 masa kultur; setelah itu kecepatan pertumbuhannya berangsur angsur menurun. Nampak pada Tabel 1, kenaikan tetapan laju pertumbuhan
Nannochloris berlangsung progresif.
Hal ini berakibat pada cepatnya tercapai
pertumbuhan optimum untuk
fitoplankton. Dengan demikian bahwa parameter tetapan laju pertumbuhan spesifik dapat digunakan untuk memprediksi waktu (hari) tercapainya kepadatan optimum suatu kultur.
Pola pertumbuhan Nannochloris
dengan penambahan ion logam Cd2+ sebesar 0,10 hingga 10,00 ppm sebagai kadmium klorida pada medium kultur fitoplankton laut disajikan pada Gambar 2 berikut:
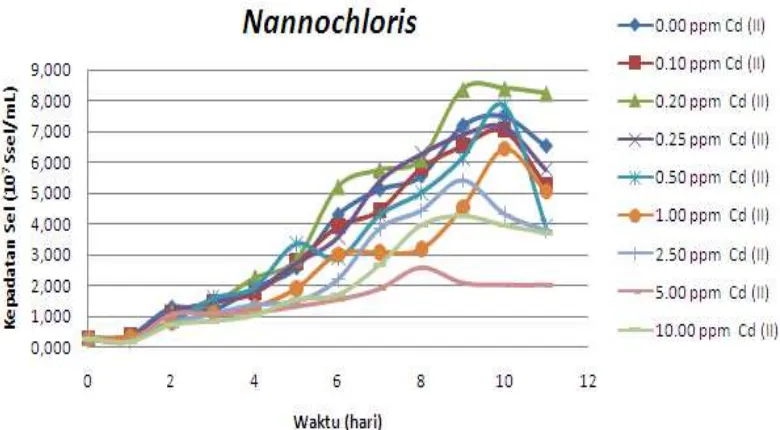
Gambar 2 Pola pertumbuhan Nannochloris pada kondisi tanpa dan dengan penambahan ion logam Cd2+pada berbagai tingkat konsentrasi
Berdasarkan Gambar 1, meskipun grafik pola pertumbuhan Nannochloris
pada medium Conway tanpa
penambahan ion logam Cd2+ (kontrol)
bukan merupakan grafik pola
pertumbuhan yang paling tinggi, tetapi pemaparan ion logam Cd2+ pada konsentrasi 0,10 mg/L hingga konsentrasi 0.25 mg/L memperlihatkan grafik pola pertumbuhan yang relatif sama dengan kontrol. Semakin besar konsentrasi ion logam Cd2+ yang
dipaparkan, semakin rendah grafik pola
pertumbuhannya. Fenomena ini
A.Makkasau et al. ISSN 2085 014X
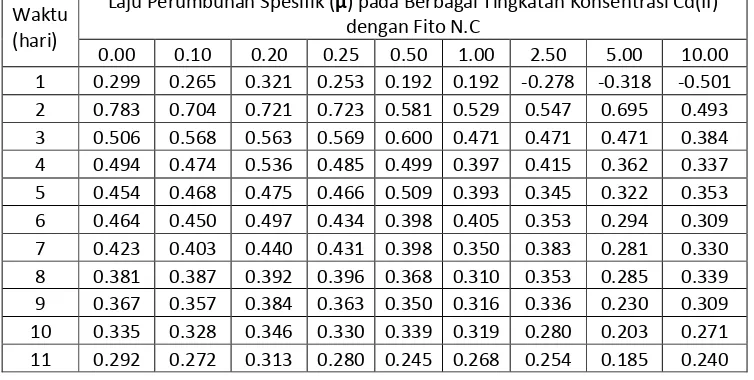
2 Tabel 2. Tetapan laju pertumbuhan spesifik ( ) Nannochloris tanpa dan dengan
penambahan ion logam Cd2+ pada berbagai tingkat konsentrasi
Waktu (hari)
Laju Perumbuhan Spesifik (µ) pada Berbagai Tingkatan Konsentrasi Cd(II)
dengan Fito N.C
0.00 0.10 0.20 0.25 0.50 1.00 2.50 5.00 10.00
1 0.299 0.265 0.321 0.253 0.192 0.192 -0.278 -0.318 -0.501
2 0.783 0.704 0.721 0.723 0.581 0.529 0.547 0.695 0.493
3 0.506 0.568 0.563 0.569 0.600 0.471 0.471 0.471 0.384
4 0.494 0.474 0.536 0.485 0.499 0.397 0.415 0.362 0.337
5 0.454 0.468 0.475 0.466 0.509 0.393 0.345 0.322 0.353
6 0.464 0.450 0.497 0.434 0.398 0.405 0.353 0.294 0.309
7 0.423 0.403 0.440 0.431 0.398 0.350 0.383 0.281 0.330
8 0.381 0.387 0.392 0.396 0.368 0.310 0.353 0.285 0.339
9 0.367 0.357 0.384 0.363 0.350 0.316 0.336 0.230 0.309
10 0.335 0.328 0.346 0.330 0.339 0.319 0.280 0.203 0.271
11 0.292 0.272 0.313 0.280 0.245 0.268 0.254 0.185 0.240
Berdasarkan Tabel 2, secara umum untuk perlakuan variasi konsentrasi ion logam Cd2+ 0.00 ppm hingga 1.00 ppm, pertambahan waktu kultur menyebabkan peningkatan laju pertumbuhan spesifik hingga hari ke 6, selanjutnya terjadi penurunan kecepatan laju pertumbuhan spesifik. Hal ini karena ketersediaan nutrien yang cukup dalam medium untuk pertumbuhan fitoplankton. Meskipun demikian, pengaruh racun ion logam Cd2+ yang semakin meningkat menyebabkan laju pertumbuhan spesifik Nannochloris
semakin menurun. Hal ini terlihat pada
hari ke 1 dengan perlakuan konsentrasi ion logam Cd2+ dalam medium sebesar
2.50 ppm hingga 10.00 ppm,
menyebabkan sebagian sel telah mengalami kematian yang ditandai dengan nilai tetapan laju pertumbuhan yang bernilai negative. Pada hari ke 2 secara umum terjadi kenaikan laju pertumbuhan spesifik dan selanjutnya di hari ke 3 terjadi penurunan laju pertumbuhan spesifik.
Tabel 3. Persentasi Hambatan Pertumbuhan (PGI) Nannochloris tanpa dan dengan penambahan ion logam Cd2+ pada berbagai tingkat konsentrasi
Time (day)
Hambatan Pertumbuhan (PGI %)
0.00 0.10 0.20 0.25 0.50 1.00 2.50 5.00 10.00
1 0.00 11.47 -7.43 15.38 35.66 35.66 192.86 206.51 267.49
2 0.00 10.05 7.95 7.72 25.79 32.48 30.17 11.24 37.01
3 0.00 -12.34 -11.24 -12.52 -18.57 6.92 6.92 6.92 24.04
4 0.00 4.08 -8.38 1.94 -0.95 19.71 16.09 26.75 31.86
5 0.00 -3.06 -4.44 -2.67 -11.97 13.59 24.12 29.16 22.26
6 0.00 3.15 -6.99 6.61 14.22 12.76 23.89 36.69 33.40
7 0.00 4.73 -4.01 -1.75 5.91 17.30 9.56 33.59 21.97
8 0.00 -1.57 -3.01 -4.07 3.29 18.42 7.26 25.12 11.05
9 0.00 2.84 -4.60 1.20 4.73 14.04 8.50 37.47 15.80
10 0.00 1.88 -3.40 1.34 -1.33 4.61 16.36 39.25 19.10
11 0.00 6.77 -7.29 3.82 15.80 7.98 12.72 36.60 17.53
Meskipun pada konsentrasi 1,00 hingga 5 ppm ion logam Cd2+ mengalami peningkatan laju spesifik yang sangat lambat. Penurunan nilai tetapan laju pertumbuhan spesifik fitoplankton akibat peningkatan konsentrasi ion logam Cd2+ yang
dipaparkan, diperkuat dari
meningkatnya harga PGI.
Berdasarkan data laju
pertumbuhan spesifik dan persentasi hambatan pertumbuhan membuktikan bahwa ketersediaan nutrien yang cukup tidak mampu mengimbangi semakin tingginya pengaruh racun ion logam Cd2+ yang ditambahkan pada medium kultur. Seperti yang dikemukakan oleh Wang dan Evangelou, (1995) bahwa secara umum dinding sel fitoplankton mengandung 25–30% selulosa, 15–25% hemiselulosa, 35% pektin dan 5–10% glikoprotein. Gugus fungsi yang
yang akan terikat kuat oleh ion logam Cd2+, sedangkan dalam setiap sel terdapat 260 jenis enzim yang membutuhkan ion logam Zn2+ (Liljas et al., 1972) yang dapat digantikan oleh ion logam Cd2+ sehingga dapat merusak kerja enzim dan mengganggu jaringan sel fitoplankton.
' $ ' '+ $( $1 .  +-! & /
Hasil analisis statistik uji beda terhadap blanko pada pengaruh penambahan ion logam Cd2+ terhadap
nannochlorisuntuk konsentrasi 0,1; 0,2; 0,25; 0,5; 1,0; 2,5; 5; dan 10 ppm; mempunyai nilai thitung berturut turut
3.844; -10.257; 1.038; 13.587; 33.555;
40.327; 154.695 dan 66.562. Sedang nilai
A.Makkasau et al. ISSN 2085 014X
2
ion logam Cd2+ 0,01 hingga 0,25 ppm; dan harga konsentrasi tertinggi yang dapat ditolerir (Maximum Tolerable Concentration) oleh fitoplankton
nannochloris pada konsentrasi ion logam Cd2+ sebesar 0,25 ppm. Fenomena tersebut mengindikasikan
bahwa nannochloris mempunyai
toleransi yang tinggi terhadap pencemar ion logam Cd2+.
Berdasarkan pada batas
maksimum kandungan ion logam Cd2+ yang diperbolehkan di perairan sebesar 0,01 ppm, maka dapat dinyatakan bahwa fitoplankton nannochloris dapat tumbuh normal pada perairan laut yang tercemar ion logam Cd2+. Hal ini membuktikan bahwa nannochloris
dapat dipertimbangkan sebagai bioindikator perairan laut yang tercemar ion logam Cd2+.
Data persentasi hambatan pertumbuhan (PGI) nannochloris
dialurkan terhadap konsentrasi ion logam Cd2+ yang dipaparkan dapat
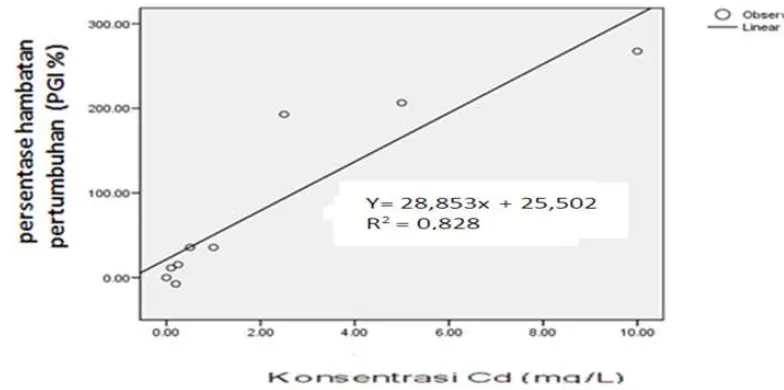
dilihat pada Gambar 2. Berdasarkan Gambar 2, harga EC50 dapat dicari dengan meregresikan harga PGI terhadap konsentrasi ion logam Cd2+ yang ditambahkan. Persamaan garis regresi yang diperoleh yaitu y = 28,853x + 25,502, dengan harga EC50 yang diperoleh adalah 0,849 ppm.
Tingginya konsentrasi ion logam Cd2+ yang dapat ditolerir oleh
nannochloris menunjukkan bahwa fitoplankton berperan dalam proses detoksifikasi ion logam Cd2+. Detoksifikasi ion logam Cd2+ oleh fitoplankton sedikitnya melibatkan dua langkah: (i) pengaktifan fitokelatin sinthase (PC sinthase) (menggunakan glutation, GSH, sebagai substrat), yang terjadi sebagai hasil peningkatan konsentrasi ion logam Cd2+ pada intraselular; dan (ii) pengomplekan dan inaktivasi ion logam Cd2+ untuk dimasukkan ke sitosol oleh molekul fitokelatin.
Gambar 2. Hubungan antara konsentrasi ion logam Cd2+ dengan persentasi hambatan pertumbuhan (PGI) pada nannochloris
Ketika ion logam Cd2+ telah masuk ke dalam sitosol, suatu sistem yang berhubungan dengan metabolisme belerang diaktifkan yang menyebabkan produksi fitokelatin (PC). Dengan
adanya gugus tiolik sistein yang mengkelat ion logam Cd2+, PC membentuk kompleks dengan ion
logam Cd2+, (PC Cd) yang
ion logam Cd2+ bebas di dalam sitosol. Kompleks PC Cd ini menjadi 1000 kali kurang beracun bagi banyak enzim tumbuhan dibanding ion logam Cd2+ dalam keadaan bebas (Kneer dan Zenk, 1992). Dalam beberapa menit setelah ion logam Cd2+ mensuplai enzim, terjadi proses pengaturan diri dan sintesis PC berlanjut sampai ion logam Cd2+ tidak tersedia (Loeffler et al., 1989). Sintesis PC berlangsung cepat sehingga terbentuk suatu kompleks molekul berbobot rendah (low molecular weight, LMW) dengan ion logam Cd2+. Ketersediaan ion logam Cd2+ membentuk kompleks molekul berbobot sedang (medium molecular weight, MMW) ke tingkatan yang lebih tinggi. Dua kompleks ini memperoleh S2 pada tonoplas dalam rangka membentuk kompleks molekul berbobot tinggi (high molecular weight, HMW) yang mempunyai afinitas lebih tinggi terhadap ion logam Cd2+ untuk proses detoksifikasi ion logam Cd2+. Karena di dalam vakuola mempunyai pH asam,
maka kompleks HMW terurai
menghasilkan kompleks baru dengan asam asam organik vakuola seperti; asam sitrat, asam oksalat, asam malat dan asam amino. Hidrolase pada vakuola dapat menghasilkan kembali apofitokelatin dalam reaksi balik menuju sitosol (Sanita di Toppi dan Gabbrielli, 1999; dan Burcu, 2006).
Berdasarkan hasil penelitian dan
pembahansan yang telah
dikemukakan di atas dapat
disimpulkan sebagai berikut:
1. Penggunaan medium conwy untuk
pada medium kultur fitoplankton
nannochloris dapat menurunkan laju pertumbuhan spesifik, penurunan jumlah sel dan berat kering nannochloris.
3. Konsentrasi ion logam Cd2+ yang tidak mempengaruhi pertumbuhan fitoplankton nannochloris (NEC)
sebesar (0,1 0,25) ppm,
konsentrasi maksimum ion logam Cd2+ yang dapat ditolerir oleh fitoplankton nannochloris adalah 0,25 ppm, dan konsentrasi ion logam Cd2+ yang menyebabkan penurunan laju pertumbuhan sebesar 50 % relatif terhadap blanko EC50 = 0,849 ppm.
Ucapan terima kasih disampaikan kepada Laboratorium Kimia Anorganik Devisi Bioremidiasi Logam Berat Jurusan Kimia FMIPA Universitas Hasanuddin dan pemberi beasiswa BPPS Dikti yang telah memberikan fasilitas untuk kelancaran penelitian.
1. Asada, K., 1999, The water cycle in chloroplast: Scavenging of active oxygen and dissipation of excess photons. Annual Review of Plant Physiology and Plant Molecular Biology 45: 601 639
2. Asada, M. and Takashaki M.,1987, Production and scavenging of active oxygen in photosynthesis. In
Photoinhibition: Topics in photosynthesis (Kyle DJ, Osmond CB, Arntzen CJ)
Indonesia Chimica Acta, , ISSN 2085 014X Vol. 3. No. 2, December 2010
durum wheat cultivars in respon to increasing Cd application, Thesis, School of Engineering and Natural Sciences, Sabancı University 5. Dafre´ AL, Sies H, Akerboom T.,
1996, Protein S thiolation and regulation of microsomal
glutathione transferase activity by the glutathione redox couple. Arch Biochem Biophys, 77#: 288–294 6. Dat J.F., Van Breusegem F.,
Vandenabeele S., Vranova E., Van Montagu M., Inze D., 2000, Dual action of active oxygen species during plant strees responses, Cell Mol. Life Sci. 4:: 779 795. 7. Foster P.L., 1977, Copper exlusion
as a mechanism of heavy metal tolerance in a greean alga. Nature, Lond., #9<: 322 323.
8. Gadallah, M.A., 1995, Effects of cadmium and kinetin on
chlorophyll content, saccahrides and dry matter accumulation in sunflower plants. Biol. Plant., 7:: 233 240.
9. Halliwell B, Gutteridge, JMC, 1995, Free Radicals in Biology and Medicine. London: Clarendon Press 10. Hastuti W. dan Djunaidah, 1991,
Spirolina dalam dunia perikanan,
BPAP, Jepara.
11. Iannelli MA, Pietrini F, Fiore L, Petrilli L, Massacci A. 2002, Antioxidant response to cadmium in Phragmites australis plants. Plant Physiol Biochem85: 977–982 12. Keyhani, E., Abdi Oskoui, F.,
Attar, F. and Keyhani, J., 2006,
DNA strand breaks by metal9 induced oxygen radicals in purified Salmonella typhimurium DNA. Ann. N.Y. Acad. Sci. in Press. 13. Keyhani, J., Keyhani, E., Einollahi,
N., Minai Tehrani, D., and Zarchipour, S., 2003, Heterogeneous inhibition of horseradish peroxidase activity bya
cadmium. Biochim. Biophys. Acta.
9# : 140 148.
14. Kneer, R. and Zenk, M.H., 1992, Phytochelatins protect plant enzymes from heavy metals poisioning, Phytochemistry,
7 =;>:2663 2667.
15. Liljas, A., 1972, Crystal structure of human carbonic anhydrase C. Nature New Biol.#74: 131–137.
16. Loiffler Hochberger A, Grill E, Gekeler W, Winnacker E L, Zenk MH, 1989, Termination of the phytochelatin synthase reaction through sequestration of heavy metals by the reaction product.
FEBS Letters 258:42 46
17. Lue Kim, H., Wozniak, P.C., dan Fletcher, R.A., 1980, "Cd Toxicity on Synchronous Populations Chlorella ellipsoidea", Can. J. Bot.,
4;: 1781 1788
18. Moore J.W. and Ramamoorthy S., 1984, Heavy metals in natural waters, applied monitoring and impact assessment; Springer Verlag New York Inc.
19. Nurhamsiah. 2010. Bioakumulasi Ion Cr6+ oleh Fitolankton Laut Nannochloris dan Tetraselmis Chuii dengan Penambahan Glutation. Unhas,Tesis
20. Olmos E, Martínez Solano JR, Piqueras A, Hellín E., 2003, Early steps in the oxidative burst induced by cadmium cultured tobacco cells
(BY 2 line). Journal of
Experimental Botany, 48:291 301 21. Palar, H., 1994 : Pencemaran dan
Toksikologi Logam Berat, PT. Rineka Cipta, Jakarta
22. Parsons, T. R., Y. Maita and C. M. Lalli (1984): A Manual of Chemical and Biological Methods for
Seawater Analysis. Pergamon Press, Oxford.
plants of Lactica sp. Cd Mn interaction. Plant Sci, 9#: 761– 767
24. Rochaix J. D.,1995,
Chlamydomonas reinhardtii as the photosynthetic yeast. Annu Rev Genet, #<: 209–230
25. Romero Puertas MC, Rodriguez Serrano M, Corpas FJ, Gomez M, Del Rio LA., 2004, Cadmium induced subcellular accumulation of O2. and H2O2 in pea leaves.
Plant Cell and Environment. #::1122 1134
26. Sanita` di Toppi L, Gabbrielli R., 1999, Response to cadmium in higher plants. Environmental and Experimental Botany 8 :105 130 27. Schüendübel A, Nikolova P,
Rudolf C, Polle A., 2002, Cadmium and H2O2 induced oxidative stress in Populus canescens roots. Plant
Physiology and Biochemistry 85: 577 584
28. Schutzendubel A, Schwanz P, Teichmann T, Gross K,
Langenfeld Heyser R, Godbold DL, Polle A., 2001, Cadmium induced changes in antioxidative systems, hydrogen peroxide
content, and differentiation in Scots pine roots. Plant Physiol, #:: 887– 898
29. Seafdec,1985, Prawn Hatchery design and Operational,
Aquaculture Extention Manual No. 9, Aquaculture Department, Tigbauan, Iliolo, Philippines. 30. Wang J, and Evangelou VP., 1995,