i
PENETAPAN KADAR KLORAMFENIKOL DAN LIDOKAIN
HIDROKLORIDA DALAM OBAT TETES TELINGA COLME® DENGAN METODE KROMATOGRAFI LAPIS TIPIS DENSITOMETRI
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Farmasi
Oleh: Prasilya NIM : 088114032
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
2011
ii
Persetujuan Pembimbing
PENETAPAN KADAR KLORAMFENIKOL DAN LIDOKAIN
HIDROKLORIDA DALAM OBAT TETES TELINGA COLME® DENGAN METODE KROMATOGRAFI LAPIS TIPIS DENSITOMETRI
Skripsi yang diajukan oleh: Prasilya
NIM : 088114032
iii
iv
HALAMAN PERSEMBAHAN
v
PERNYATAAN KEASLIAN KARYA
Saya menyatakan dengan sesungguhnya bahwa skripsi yang saya tulis ini tidak memuat karya atau bagian karya orang lain, kecuali yang telah disebutkan dalam kutipan dan daftar pustaka, sebagaimana layaknya karya ilmiah.
Apabila di kemudian hari ditemukan indikasi plagiarism dalam naskah ini, maka saya bersedia menanggung segala sanksi sesuai peraturan perundang-undangan yang berlaku.
Yogyakarta, 5 September 2011 Penulis
Prasilya
vi
LEMBAR PERNYATAAN PERSETUJUAN
PUBLIKASI KARYA ILMIAH UNTUK KEPENTINGAN AKADEMIS
Yang bertanda tangan di bawah ini, saya mahasiswa Sanata Dharma:
Nama : Prasilya
Nomor mahasiswa : 088114032
Demi pengembangan ilmu pengetahuan, saya memberikan kepada Perpustakaan Universitas Sanata Dharma karya ilmiah saya yang berjudul:
“PENETAPAN KADAR KLORAMFENIKOL DAN LIDOKAIN
HIDROKLORIDADALAM OBAT TETES TELINGA COLME® DENGAN METODE KROMATOGRAFI LAPIS TIPIS DENSITOMETRI”
Beserta perangkat yang diperlukan (bila ada), dengan demikian saya memberikan kepada Perpustakaan Universitas Sanata Dharma hak untuk menyimpan, mengalihkan dalam bentuk media lain, mengelolanya dalam bentuk pangkalan data, mendistribusikan secara terbatas, dan mempublikasikannya di Internet atau media lain untuk kepentingan akademis tanpa perlu meminta ijin dari saya maupun memberikan royalti kepada saya selama tetap mencantumkan nama saya sebagai penulis.
Demikiann pernyataan ini saya buat dengan sebenarnya. Dibuat di Yogyakarta
Pada tanggal: 5 September 2011 Yang menyatakan
vii
PRAKATA
Puji dan syukur kepada Tuhan Yang Maha Esa atas segala rahmat yang
dilimpahkan sehingga penulis dapat menyelesaikan skripsi berjudul “Penetapan
Kadar Kloramfenikol dan Lidokain Hidroklorida Dalam Obat Tetes Telinga Colme®
Dengan Metode Kromatografi Lapis Tipis Densitometri”. Skripsi ini disusun sebagai salah satu syarat untuk meraih gelar Sarjana Farmasi (S.Farm) di Fakultas Farmasi, Universitas Sanata Dharma, Yogyakarta.
Dalam pelaksanaan penelitian hingga selesainya penyusunan skripsi, penulis mendapat banyak bantuan dari berbagai pihak. Oleh karena itu, penulis mengucapkan terima kasih kepada:
1. Ipang Djunarko, M.Si.,Apt. selaku Dekan Fakultas Farmasi Sanata Dharma 2. Jeffry Julianus, M.Si. selaku dosen pembimbing yang telah membimbing penulis,
memberi masukan, semangat, dan motivasi selama perkuliahan, penelitian maupun penyusunan skripsi.
3. Christine Patramurti, M.Si.,Apt. yang ikut mengarahkan penulis, memberi masukan, dan memberi dukungan selama penyusunan skripsi.
4. Dra. M.M. Yetty Tjandrawati M.Si. selaku dosen penguji yang memberikan arahan, masukan dan saran untuk skripsi ini.
5. dr. Fenty M. Kes., SpPK selaku dosen pembimbing akademik yang selalu mendukung dan memberikan saran selama penulis menyelesaikan masa studi.
viii
6. Siswanto Tanuadmojo dan PT. Interbat yang telah memberikan baku dan sampel untuk penelitian ini.
7. Rini Dwiastuti, M.Sc.,Apt. selaku Kepala Laboratorium Fakultas Farmasi Universitas Sanata Dharma.
8. Semua dosen-dosen yang telah memberikan ilmu selama penulis menempuh pendidikan di Fakultas Farmasi Universitas Sanata Dharma.
9. Seluruh staf laboratorium di Fakultas Farmasi Universitas Sanata Dharma Yogyakarta terutama Mas Otok, Mas Bimo, Pak Farlan dan Mas Kunto yang telah membantu dan mendukung berlangsungnya skripsi ini.
10.Aphing, Edi, Ayus, Devi, Awang, dan Dea yang selalu memberikan kasih sayang, semangat, dan doa.
11.Felicia dan Sasa selaku rekan kerja penulis yang selalu member dukungan dan semangat selama penelitian dan penyusunan skripsi, melewati suka dan duka bersama.
12.Wiwi, Tere, Sari, Susi, Susan, Nona, Novi, Citra, Cure, Amel, Ayesa, Dina sebagai teman seperjuangan di Laboratorium Kimia Analisis Instrumental atas semangat dan kebersamaannya.
13.Bravo, Rika, Elia, Lala, Siska, Yessi, Metri, atas dukungan, semangat dan doa yang diberikan.
ix
15. Semua pihak yang telah membantu dan mendukung yang tidak dapat disebutkan satu per satu.
Penulis menyadari bahwa masih terdapat banyak kekurangan dalam penyusunan skripsi ini. Oleh karena itu penulis sangat mengharapkan masukan, kritik, dan saran yang membangun. Akhir kata, semoga skripsi ini bermanfaat bagi pembaca.
Penulis
x
DAFTAR ISI
halaman
HALAMAN JUDUL ... i
HALAMAN PERSETUJUAN PEMBIMBING ... ii
HALAMAN PENGESAHAN ... iii
HALAMAN PERSEMBAHAN ... iv
PERNYATAAN KEASLIAN KARYA ... v
LEMBAR PERSETUJUAN PUBLIKASI KARYA ... vi
PRAKATA ... vii
2. Keaslian penelitian ... 4
3. Manfaat penelitian ... 4
B. Tujuan Penelitian ... 5
xi
A. Kloramfenikol ... 6
B. Lidokain Hidroklorida ... 7
C. Obat Tetes Telinga ... 8
D. Larutan ... 9
E. Kromatografi Lapis Tipis ... 10
1. Definisi dan instrumentasi ... 10
2. Pemisahan dan resolusi ... 13
3. Sistem KLT ... 15
4. Analisis kualitatif dan kuantitatif ... 18
F. Densitometri ... 19
G. Landasan Teori ... 20
H. Hipotesis ... 22
BAB III METODE PENELITIAN... 23
A. Jenis dan Rancangan Penelitian ... 23
B. Variabel Penelitian ... 23
1. Variabel bebas ... 23
2. Variabel tergantung ... 23
3. Variabel pengacau terkendali ... 23
C. Definisi Operasional... 24
D. Bahan Penelitian... 24
E. Alat Penelitian ... 25
F. Tata Cara Penelitian ... 25
xii
1. Pemilihan dan pengambilan sampel ... 25
2. Pembuatan fase gerak ... 25
3. Penetapan panjang gelombang pengamatan... 26
4. Pembuatan larutan baku klormfenikol ... 26
5. Pembuatan larutan baku lidokain HCl ... 27
6. Pembuatan kurva baku kloramfenikol dan lidokain hidroklorida ... 27
7. Preparasi sampel... 28
8. Penetapan kadar ... 28
G. Analisis Hasil ... 29
BAB IV HASIL DAN PEMBAHASAN ... 30
A. Pemilihan Sampel ... 30
B. Fase Gerak ... 32
C. Larutan Baku ... 33
D. Penetapan Panjang Gelombang Pengamatan ... 34
E. Analisis Kualitatif ... 37
F. Kurva Baku Kloramfenikol dan Lidokain HCl ... 43
G. Penetapan Kadar Kloramfenikol dan Lidokain HCl Dalam Sampel ... 46
BAB V KESIMPULAN DAN SARAN ... 49
A. Kesimpulan ... 49
B. Saran ... 49
DAFTAR PUSTAKA ... 50
xiii
BIOGRAFI PENULIS ... 78
xiv
DAFTAR TABEL
Tabel I. Persyaratan uji keseragaman volume ... 10 Tabel II. Nilai indeks polaritas pelarut ... 17 Tabel III. Keseragaman volume sampel Colme® ... 31 Tabel IV. Data nilai Rf baku kloramfenikol, baku lidokain HCl, dan sampel .. 42 Tabel V. Data persamaan kurva baku kloramfenikol ... 44 Tabel VI. Data persamaan kurva baku lidokain HCl ... 44 Tabel VII. Hasil penetapan kadar campuran kloramfenikol dan lidokain HCl
xv
DAFTAR GAMBAR
Gambar 1. Struktur kimia kloramfenikol ... 6
Gambar 2. Struktur kimia lidokain HCl ... 7
Gambar 3. Obat tetes telinga Colme® ... 9
Gambar 4. Ilustrasi perhitungan nilai Rf ... 14
Gambar 5. Ilustrasi resolusi pada KLT ... 15
Gambar 6. Struktur silika gel ... 16
Gambar 7. Scanner KLT ... 19
Gambar 8. Gugus kromofor dan gugus auksokrom kloramfenikol ... 34
Gambar 9. Gugus kromofor dan gugus auksokrom lidokain HCl ... 35
Gambar 10. Spektra kloramfenikol 300 ng dan lidokain HCl 3000 ng ... 35
Gambar 11. Spektra kloramfenikol 600 ng dan lidokain HCl 6000 ng ... 36
Gambar 12. Spektra kloramfenikol 900 ng dan lidokain HCl 9000 ng ... 36
Gambar 13. Interaksi kloramfenikol dengan fase diam ... 38
Gambar 14. Interaksi lidokain dengan fase diam ... 39
Gambar 15. Interaksi kloramfenikol dengan fase gerak heksana:toluena:dietilamin:metanol (15:79:6:20) ... 40
Gambar 16. Interaksi lidokain dengan fase gerak heksana:toluena:dietilamin:metanol (15:79:6:20) ... 40
Gambar 17. Kromatogram pemisahan kloramfenikol dan lidokain HCl ... 41
Gambar 18. Kurva baku kloramfenikol ... 45
xvi
xvii
DAFTAR LAMPIRAN
Lampiran 1. Sertifikat analisis kloramfenikol ... 54
Lampiran 2. Sertifikat analisis lidokain HCl ... 55
Lampiran 3. Sistem KLT densitometri yang digunakan ... 56
Lampiran 4. Data penimbangan baku kloramfenikol dan lidokain HCl ... 57
Lampiran 5. Spektra panjang gelombang pengamatan ... 58
Lampiran 6. Kromatogram blanko plat kosong dan fase gerak ... 59
Lampiran 7. Kromatogram baku kloramfenikol replikasi 2 ... 60
Lampiran 8. Kromatogram baku lidokain HCl replikasi 2 ... 62
Lampiran 9. Contoh perhitungan jumlah analit teoritis ... 64
Lampiran 10. Data persamaan kurva baku kloramfenikol dan lidokain HCl .. 65
Lampiran 11. Data pengukuran berat jenis sampel ... 66
Lampiran 12. Data hasil uji keseragaman volume... 67
Lampiran 13. Kromatogram campuran kloramfenikol dan lidokain HCl dalam sampel Colme® ... 68
Lampiran 14. Data kadar kloramfenikol dan lidokain HCl dalam sampel Colme® ... 75
Lampiran 15. Contoh perhitungan kadar kloramfenikol dan lidokain HCl dalam sampel Colme® ... 76
Lampiran 16. Perhitungan KV kloramfenikol dan lidokain HCl dalam sampel Colme® ... 77
xviii
xix
INTISARI
Otitis Media Supratif Kronik merupakan salah satu penyakit yang memiliki prevalensi cukup tinggi di Indonesia. Colme® merupakan salah satu obat tetes telinga yang dapat digunakan untuk mengobati Otitis Media Supratif Kronik. Colme® mengandung kloramfenikol dan lidokain HCl. Tujuan penelitian ini adalah untuk mengetahui kesesuaian kadar kloramfenikol dan lidokain HCl dengan yang tertera pada etiket obat tetes telinga Colme® dalam rangka penjaminan mutu suatu produk obat.
Penelitian ini bersifat non-eksperimental diskriptif karena tidak dilakukan manipulasi dan perlakuan terhadap subjek uji. Penetapan kadar kloramfenikol dan lidokain HCl dilakukan dengan metode kromatografi lapis tipis densitometri. Fase gerak yang digunakan adalah heksana:toluena:dietilamin:metanol (15:79:6:20) dan fase diam yang digunakan adalah lempeng silika gel 60 F254. Kelebihan metode kromatografi lapis tipis-densitometri adalah dapat dilakukan analisis kualitatif dan kuantitatif campuran dalam waktu yang besamaan.
Kadar kloramfenikol adalah 9,94-10,79% (b/v) dan kadar lidokain HCl adalah 3,68-3,84% (b/v). Kadar kloramfenikol sesuai dengan kadar yang tertera pada etiket, dan kadar lidokain HCl tidak sesuai dengan kadar yang tertera pada etiket.
Kata kunci: kloramfenikol, lidokain HCl, obat tetes telinga, KLT, densitometri, penetapan kadar
xx
ABSTRACT
Chronic otitis media suprative is one of the disease that has highly prevalence in Indonesia. Colme® is one of the ear drops that can be used to treat chronic otitis media suprative. Colme® contained chloramphenicol and lidocaine HCl. The purpose of this study was to determine the suitability levels of chloramphenicol and lidocaine HCl obtained as stated on the label Colme® ear drops in order to guarantee the quality of a medicinal product.
This study is non experimental descriptive because it does not have any manipulation and treatment of the test subjects. Assay of chloramphenicol and lidocaine HCl performed by thin layer chromatography densitometry method. The mobile phase used is hexan:toluene:diethylamine:methanol (15:79:6:20) and stationary phase used is silica gel 60 F254. Advantage method thin-layer chromatography densitometry is can be used as qualitative and quantitative analysis of the mixture in concequtive time.
Level of chloramphenicol is 9.94 to 10.79% (w/v) and the level of lidocaine HCl is 3.68 to 3.84% (w/v). Level of chloramphenicol is suitable with level indicated on the label, and the level of lidocaine HCl is not suitable with level indicated on the label.
1
BAB I
PENGANTAR
A. Latar Belakang
Penyakit infeksi Otitis Media Supratif Kronik (OMSK) memiliki prevalensi yang cukup tinggi di Indonesia yaitu mencapai 3% (Anonimc, 2010). Colme® merupakan salah satu obat tetes telinga yang dapat digunakan untuk mengobati Otitis Media Supratif Kronik. Colme® mengandung kloramfenikol 10% dan lidokain HCl 4% dengan cairan pembawa propilenglikol. Menurut Farmakope Indonesia IV (1995), obat tetes telinga adalah obat tetes yang digunakan dengan cara meneteskan ke dalam telinga. Kecuali dinyatakan lain, dibuat dengan menggunakan pembawa bukan air.
2
Kloramfenikol sukar larut dalam air, mudah larut dalam etanol, propilenglikol, aseton, dan etil asetat (Direktorat Jendral Badan Pengawasan Obat dan Makanan, 1995). Kloramfenikol berbentuk jarum, serbuk kristal, atau memanjang, berwarna putih, abu-abu atau kekuningan. Titik leleh kloramfenikol adalah 150,5°C-151,5°C, dan bobot molekul 323,13g/mol. Kloramfenikol memiliki koefisien partisi 12; pH 4-7,5. Dalam air, kloramfenikol memiliki panjang gelombang maksimum pada 278 nm ( =298) (Clarke,1986).
Lidokain HCl sangat mudah larut dalam air dan dalam etanol, larut dalam kloroform dan tidak larut dalam eter. Lidokain HCl berbentuk serbuk kristal, tidak berbau, dan rasa sedikit pahit (Direktorat Jendral Badan Pengawasan Obat dan Makanan, 1995). Bobot molekul lidokain adalah 234,34g/mol dengan titik leleh 66°C -69°C. Dalam larutan asam, lidokain HCl memiliki serapan maksimum 263 nm ( = 19) (Clarke,1986).
Penelitian ini merupakan suatu rangkaian penelitian yang diawali dengan tahap optimasi yang telah dilakukan oleh Felicia dan validasi metode yang telah dilakukan oleh Regina. Pada penelitian ini, peneliti mengambil bagian penetapan kadar. Fase gerak yang diperoleh dari hasil optimasi adalah heksana:toluena:dietilamin:metanol (15:79:6:20) dengan fase diam silika gel 60 F254. Hasil validasi menunjukkan bahwa validitas yang baik untuk kloramfenikol dan lidokain HCl adalah pada seri tengah yaitu 600 ng untuk kloramfenikol dan 6000 ng untuk lidokain HCl.
Penetapan kadar kloramfenikol dan lidokain HCl dilakukan dengan metode kromatografi lapis tipis densitometri. Metode KLT densitometri dipilih karena dengan metode ini dapat dilakukan analisis kualitatif dan kuantitatif untuk campuran obat. KLT biasanya merupakan metode pilihan pertama dalam memisahkan suatu campuran. Hal ini disebabkan karena KLT merupakan metode yang sederhana dan cepat (Dean,1995). Kloramfenikol dan lidokain HCl dapat dipisahkan dengan KLT karena kedua senyawa tersebut memiliki sifat kepolaran yang berbeda. Dari hasil pemisahan dengan KLT dapat dilanjutkan analisis kuantitatif dengan densitometri karena kloramfenikol dan lidokain HCl memiliki gugus kromofor dan gugus auksokrom. Densitometri merupakan suatu analisis kuantitatif yang berdasarkan pada interaksi radiasi elektromagnetik dengan analit yang merupakan bercak KLT. Densitometri lebih banyak digunakan untuk megukur analit dengan kadar kecil yang mana perlu dilakukan pemisahan terlebih dahulu dengan kromatografi lapis tipis (Rohman, 2009).
1. Permasalahan
a. Berapakah kadar kloramfenikol dan lidokain HCl dalam obat tetes telinga Colme® yang ditetapkan dengan metode kromatografi lapis tipis densitometri? b. Apakah kadar kloramfenikol dan lidokain HCl yang ditetapkan dengan metode
4
2. Keaslian penelitian
Penetapan kadar kloramfenikol dan lidokain HCl secara tunggal menggunakan metode kromatografi lapis tipis sudah pernah dilakukan. Penelitian mengenai penetapan kadar lidokain HCl dilakukan oleh Kiszka dan Madro (2011). Fase gerak optimum yang digunakan adalah heksana:toluena:dietilamin (60:20:5), dengan nilai Rf 0,48. Penelitian mengenai penetapan kadar kloramfenikol juga sudah pernah dilakukan oleh Vovk dan Simonovska (2005). Fase gerak yang digunakan pada penelitian tersebut adalah heksana:etil asetat (35:65), dan fase diam yang digunakan adalah silika gel F254 dengan reflektansi absorbansi pada panjang gelombang 280 nm. Pada penelitian ini akan dilakukan penetapan kadar campuran kloramfenikol dan lidokain HCl dalam sampel obat tetes telinga Colme® dengan metode kromatografi lapis tipis densitometri dimana penelitian ini belum pernah dilakukan sebelumnya.
3. Manfaat penelitian
a. Manfaat metodologis. Dapat memberikan sumbangan ilmiah mengenai metode kromatografi lapis tipis densitometri yang digunakan untuk pemisahan dan penetapan kadar kloramfenikol dan lidokain HCl.
b. Manfaat praktis. Dapat memberikan informasi mengenai kadar kloramfenikol dan lidokain HCl pada obat tetes telinga Colme® yang ditetapkan dengan metode kromatografi lapis tipis densitometri.
B. Tujuan Penelitian
1. Mengetahui kadar kloramfenikol dan lidokain HCl dalam obat tetes telinga Colme® dengan metode kromatografi lapis tipis densitometri.
6
BAB II
PENELAAHAN PUSTAKA
A. Kloramfenikol
Kloramfenikol dalam tetes telinga mengandung tidak kurang dari 90,0% dan tidak lebih dari 130,0% C11H12Cl2N2O5 dari jumlah yang tertera pada etiket. Kloramfenikol berbentuk serbuk hablur halus berbentuk jarum atau lempeng memanjang, berwarna putih hingga putih kelabu, atau putih kekuningan. Kloramfenikol stabil dalam larutan netral atau larutan agak asam (Direktorat Jendral Badan Pengawasan Obat dan Makanan, 1995). Kloramfenikol memiliki berat molekul 323,1g/mol; memiliki titik lebur 150°C-153°C; kelarutan dalam air 1:400; kelarutan dalam etanol 1:2,5; agak larut dalam eter; dan kloroform (Clarke, 1969). Kloramfenikol memiliki koefisien partisi 12; pH 4-7,5. Kloramfenikol memiliki panjang gelombang maksimum pada 278 nm ( =298) dalam pelarut air (Clarke, 1986).
[
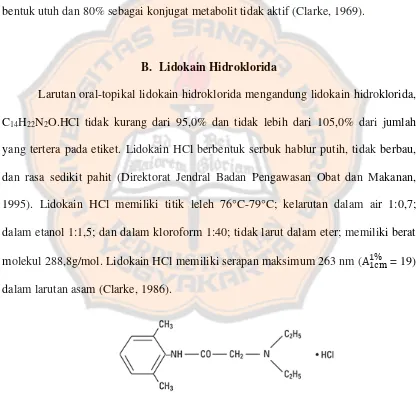
Gambar 1. Struktur kimia kloramfenikol (Anonima, 2010)
Kloramfenikol merupakan antibiotik yang semula berasal dari sejenis
Streptomyces, namun kemudian dibuat secara sintesis. Kloramfenikol dapat
berkhasiat sebagai bakteriostatis dan bakterisid. Mekanisme kerjanya dengan menghambat sintesis protein pada bakteri (Tjaya dan Rahardja, 2010).
Secara luas kloramfenikol di distribusikan ke jaringan tubuh dan diekskresikan melalui empedu dan urin. Proporsi terbesar disekresikan melalui urin selama 6 jam pertama setelah setelah dicerna, kurang lebih 10% disekresikan dalam bentuk utuh dan 80% sebagai konjugat metabolit tidak aktif (Clarke, 1969).
B. Lidokain Hidroklorida
Larutan oral-topikal lidokain hidroklorida mengandung lidokain hidroklorida, C14H22N2O.HCl tidak kurang dari 95,0% dan tidak lebih dari 105,0% dari jumlah yang tertera pada etiket. Lidokain HCl berbentuk serbuk hablur putih, tidak berbau, dan rasa sedikit pahit (Direktorat Jendral Badan Pengawasan Obat dan Makanan, 1995). Lidokain HCl memiliki titik leleh 76°C-79°C; kelarutan dalam air 1:0,7; dalam etanol 1:1,5; dan dalam kloroform 1:40; tidak larut dalam eter; memiliki berat molekul 288,8g/mol. Lidokain HCl memiliki serapan maksimum 263 nm ( = 19) dalam larutan asam (Clarke, 1986).
8
Lidokain (otopain) adalah zat pemati rasa lokal yang pada kulit dan selaput lendir mampu menghalangi rasa nyeri, perasaan terbakar, dan gatal. Terdapat dalam tetes telinga 0,5%, tetapi tidak digunakan pada perforasi selaput gendang dan pada radang telinga atau congek. Berhubung tidak mengakibatkan hipersensitasi, lidokain banyak digunakan dalam banyak sediaan topikal (Tjayb dan Rahardja, 2010).
C. Obat Tetes Telinga
Menurut Farmakope Indonesia IV (1995), obat tetes telinga adalah obat tetes yang digunakan dengan cara meneteskan ke dalam telinga. Guttae, obat tetes telinga adalah sediaan cair berupa larutan, emulsi atau suspensi, dimaksudkan untuk obat dalam atau obat luar, digunakan dengan cara meneteskan menggunakan penetes yang menghasilkan tetesan setara dengan tetesan yang dihasilkan penetes baku yang disebutkan dalam Farmakope Indonesia (Direktorat Jendral Badan Pengawasan Obat dan Makanan, 1979). Kecuali dinyatakan lain, tetes telinga dibuat menggunakan cairan pembawa bukan air. Obat tetes telinga biasanya mengandung antibiotik seperti kloramfenikol, gentamisin, atau ofloxacin dengan tambahan zat pemati rasa lokal seperti lidokain dan benzokain (Anonimb, 2011).
Cairan pembawa yang digunakan harus mempunyai kekentalan yang cocok agar obat mudah menempel pada dinding telinga, umumnya digunakan gliserol dan propilenglikol. Dapat juga digunakan etanol, heksilenglikol, dan minyak lemak nabati. Keasaman-kebasaan kecuali dinyatakan lain, pH 5,0 sampai 6,0. Penyimpanan kecuali dinyatakan lain, dalam wadah tertutup rapat.
Tetesan (guttae) adalah sediaan cair yang mengandung bahan obat atau sediaan obat atau bahan obat dan sediaan obat terlarut, teremulsi, atau tersuspensi, ditakar berdasar jumlah tetesan, digunakan untuk diminum dan diisikan ke dalam wadah bertakaran ganda. Untuk tetesan tertentu yang digunakan di telinga, dinamakan tetes telinga (otoguttae) (Voigt, 1994).
Gambar 3. Obat tetes telinga Colme (Anonimb, 2010)
Colme® merupakan salah satu obat tetes telinga yang mengandung kloramfenikol 10% dan lidokain HCl 4% dengan propilenglikol sebagai pembawa. Colme tetes telinga memiliki indikasi pengobatan infeksi superficial pada telinga luar oleh bakteri Gram-negatif dan bakteri Gram-positif yang peka terhadap kloramfenikol. Colme® disimpan dalam kondisi tertutup, di bawah 25oC, jangan disimpan dalam lemari pembeku, terlindung dari cahaya matahari, hindari terjadinya kontaminasi, dan jauhkan dari jangkauan anak-anak (Anonimb, 2010).
D. Larutan
10
secara merata, maka penggunaan larutan sebagai bentuk sediaan, umumnya memberikan jaminan keseragaman dosis dan memiliki ketelitian yang baik jika larutan diencerkan atau dicampur.
Farmakope menyatakan sediaan yang mungkin ada dalam bentuk larutan antara lain obat tetes, sediaan injeksi dan infus, minyak-minyak obat, tetes mata, pembilas mata, spiritus obat, ekstrak, tingtur, sirup, dan dispersi udara (Voigt, 1994). Keseragaman volume, volume isi netto tiap wadah harus sedikit berlebih dari volume yang ditetapkan. Kelebihan volume yang dianjurkan tertera dalam tabel di bawah ini:
Tabel I. Persyaratan uji keseragaman volume (Direktorat Jendral Pengawasan Obat dan Makanan RI, 1979)
Volume tertera dalam penandaan Kelebihan volume yang dianjurkan
Untuk cairan encer Untuk cairan kental
0,5 ml 0,10 ml 0,12 ml
1. Definisi dan instrumentasi
Kromatografi didefinisikan sebagai prosedur pemisahan zat terlarut oleh suatu proses migrasi diferensial dinamis dalam sistem yang terdiri dari dua fase atau lebih, salah satu diantaranya bergerak secara berkesinambungan dalam arah tertentu dan di
dalamnya zat-zat itu menunjukkan perbedaan dalam adsorpsi, partisi, kelarutan, tekanan uap, ukuran molekul, atau kerapatan muatan ion. Dengan demikian masing-masing zat dapat diidentifikasi atau ditetapkan dengan metode analitik (Direktorat Jendral Badan Pengawasn Obat dan Makanan, 1995).
Kromatografi dapat dibedakan atas berbagai macam tergantung pada pengelompokannya. Berdasarkan pada mekanisme pemisahannya, kromatografi dibedakan menjadi kromatografi adsorbsi, kromatografi partisi, kromatografi pasangan ion, kromatografi penukar ion, kromatografi eksklusi ukuran, dan kromatografi afinitas (Gandjar dan Rohman, 2007).
Teknik kromatografi umum membutuhkan zat terlarut terdistribusi diantara dua fase, satu diantaranya diam (fase diam), yang lainnya bergerak (fase gerak). Fase gerak membawa zat terlarut melalui media, hingga terpisah dari zat terlarut lainnya, yang terelusi lebih awal atau lebih akhir. Umumnya zat terlarut dibawa melalui media pemisah oleh aliran suatu pelarut berbentuk cairan atau gas yang disebut eluen. Fase diam dapat berfungsi sebagai penjerap, seperti halnya penjerap alumina yang diaktifkan, silika gel, resin penukar ion, atau dapat bertindak melarutkan zat terlarut, sehingga terjadi partisi antara fase diam dan fase gerak ((Direktorat Jendral Badan Pengawasn Obat dan Makanan, 1995).
12
merupakan kromatografi planar yang digunakan secara luas untuk analisis kualitatif dan dapat juga digunakan untuk analisis kuatitatif (Christian, 2004). KLT biasanya merupakan metode pilihan pertama dalam memisahkan suatu campuran. Pada kromatografi lapis tipis, fase diam berada pada pelat gelas, plastik atau logam dan sampel akan ditotolkan di atas pelat fase diam. Sampel melewati pelat fase diam bersama dengan fase gerak dengan daya kapilaritas. Volume sampel yang dapat digunakan pada kromatografi lapis tipis adalah 1 sampai 5 µL (Dean, 1995).
Fase diam, fase gerak dan material lain yang dibutuhkan dalam persiapan lapis tipis harus memenuhi persyaratan spesifik yang ditentukan mengenai kemurnian, ukuran partikel dan sifat-sifat yang menentukan untuk adsorpsi, distribusi cair-cair, dan proses lainnya. Keuntungan besar dari KLT adalah kecepatan analisis sampel karena jarak elusi yang pendek (sekitar 10 sampai 15 cm) dan waktu elusi yang singkat (Dean, 1995).
Bejana kromatografi harus tertutup rapat dan sedapat mungkin volume fase gerak sedikit mungkin (akan tetapi harus mampu mengelusi lempeng sampai ketinggian lempeng yang telah ditentukan). Untuk melakukan penjenuhan fase gerak, biasanya bejana dilapisi dengan kertas saring. Jika fase gerak telah mencapai ujung atas kertas saring, maka dapat dikatakan bahwa fase gerak telah jenuh. Selama proses elusi, bejana kromatografi harus ditutup rapat, misalkan dengan lembar alumunium dan sebagainya (Gandjar dan Rohman, 2007).
2. Pemisahan dan resolusi
Koefisien Rf merupakan kuantitas dasar yang digunakan untuk menunjukkan posisi dari solut pada pengembangan kromatogram. Retardation factor (Rf) merupakan perbandingan antara jarak yang ditempuh solut dengan jarak yang ditempuh fase gerak (Dean, 1995). Pemisahan kromatografi planar (kromatografi lapis tipis dan kromatografi kertas) pada umumnya dihentikan sebelum semua fase gerak melewati seluruh permukaan fase diam (Rohman, 2009).
Rf = (1) (Dean, 1995). Nilai Rf antara 0 (solut berada pada batas awal pengembangan) dan 0,999 (solut bermigrasi ke atas bersama dengan fase gerak). Perhitungan nilai Rf dapat dilakukan dengan simbol yang ditunjukkan pada gambar 4.
Rf = (2)
dengan : z = jarak yang ditempuh analit
14
Gambar 4. Ilustrasi perhitungan nilai Rf (Kowalska, 1996)
Tujuan utama dari kromatografi adalah dapat memisahkan campuran solut. Walaupun demikian, tidak menutup kemungkinan bahwa dua spot akan saling berdampingan dan bertumpang tindih baik pada derajat kecil maupun derajat besar. Maka dari itu diperlukan suatu pengukuran pada pemisahan tersebut. Pemisahan pengukuran tersebut dapat dihitung sebagai Rs, disebut resolusi. Pemisahan didefinisikan sebagai perbedaan antara waktu retensi 2 puncak yang saling
berdekatan (Δz = z2-z1) dibagi dengan rata-rata lebar puncak (w1+w2)/2 sebagaimana diilustrasikan pada gambar berikut:
Rs =
(3)
Gambar 5. Ilustrasi resolusi pada KLT: (a) kromatogram; (b) profil kromatografi masing-masing bercak (Kowalska, 1996)
Jika R=1 maka pemisahan yang terjadi adalah 98%. Untuk pemisahan yang baik, nilai
R≥1,5 hal ini berarti pemisahan ≥99,7% (Sastrohamidjojo, 2002).
3. Sistem KLT
16
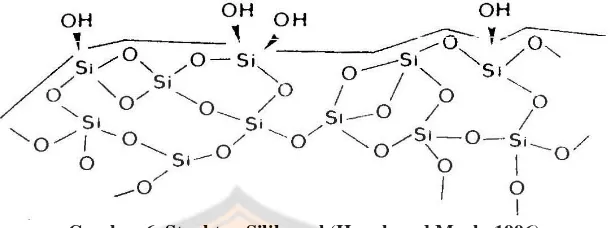
Gambar 6. Struktur Silika gel (Hauck and Mack, 1996)
Partikel-partikel silika gel terdiri dari gugus-gugus hidroksil pada permukaan, gugus hidroksil tersebut akan berinteraksi hidrogen dengan molekul yang bersifat polar. Kandungan air dalam silika gel dapat mecegah molekul polar lainnya untuk mencapai permukaan dan berinteraksi hidrogen dengan gugus hidroksil, sehingga gel harus diaktifkan dengan pemanasan untuk menghilangkan kandungan air. Pemanasan dilakukan dengan meletakkan lempeng silika gel pada oven dengan suhu 110°C selama beberapa jam (Christian, 2004).
Adsorpsi solut oleh fase diam atau oleh adsorben sangat tergantung pada struktur kimia solut atau adanya gugus aktif tertentu yang berinteraksi dengan adsorben, ukuran partikel adsorben, kelarutan solut dalam fase gerak. Semakin kecil ukuran partikel adsorben, maka luas permukaannya semakin luas sehingga interaksinya dengan solut juga semakin luas. Solut yang makin mudah larut dalam fase gerak akan semakin mudah lepas dari fase diam (Gandjar dan Rohman, 2007).
b. Fase gerak. Pelarut yang digunakan harus memiliki kemurnian yang tinggi. Adanya sejumlah kecil air atau campuran lain yang tidak murni dapat menghasilkan kromatogram yang tidak reprodusibel (Christian, 2004). Pemilihan
pelarut yang digunakan untuk senyawa yang akan dianalisis dengan metode KLT, harus dapat melarutkan analit dengan sempurna, mudah menguap, viskositas rendah, serta dapat membasahi lapisan penyerap (Sherma, 1996).
Fase gerak adalah medium angkut yang terdiri atas satu atau beberapa pelarut. Fase gerak bergerak di dalam fase diam yaitu lapisan berpori karena ada gaya kapiler. Apabila diperlukan sistem pelarut multi komponen, maka harus berupa suatu campuran sederhana yang mungkin terdiri dari tiga komponen (Stahl, 1985).
Berikut ini merupakan tabel beberapa nilai indeks polaritas dari beberapa pelarut yang sering digunakan:
Tabel II. Nilai indeks polaritas pelarut (Snyder and Kirkland, 1997)
Solvent Indeks
18
terlalu kuat pada permukaan fase diam senyawa akan tetap di tempat (tidak terelusi). Disisi lain, jika terikat lemah pada permukaan fase diam tidak akan terjadi pemisahan dan semua campuran senyawa akan melewati fase diam bersama dengan fase gerak. Fase diam dan fase gerak tidak boleh bereaksi satu sama lain. Misalnya asam organik tidak digunakan sebagai fase gerak bila karbonat sebagai fase diam (Stahl, 1985).
4. Analisis kualitatif dan kuantitatif
Kromatografi lapis tipis dapat digunakan untuk uji identifikasi senyawa baku. Parameter pada KLT yang digunakan untuk identifikasi adalah nilai Rf. Dua senyawa dikatakan identik jika mempunyai nilai Rf yang sama jika diukur pada kondisi KLT yang sama. Pemisahan pada kromatografi lapis tipis yang optimal akan diperoleh hanya jika menotolkan sampel dengan ukuran bercak sekecil mungkin dan sesempit mungkin. (Gandjar dan Rohman, 2007).
Ada 2 metode yang digunakan untuk analisis kuantitatif dengan KLT. Pertama, bercak diukur langsung pada lempeng dengan menggunakan ukuran luas atau dengan teknik densitometri. Cara kedua adalah dengan mengerok bercak lalu menetapkan kadar senyawa yang terdapat dalam bercak tersebut dengan metode analisis yang lain, misalkan dengan metode spektrofotometri (Munson, 1991).
Untuk menjamin kondisi yang digunakan dalam analisis kuantitatif stabil dan reprodusibel, baik pada penyiapan sampel atau proses kromatografi, berikut beberapa syarat yang harus dipenuhi dalam analisis kuantitatif:
a. Analit (solut) harus telah diketahui dan terpisah sempurna dari komponen-komponen lain di dalam kromatogram
b. Baku dengan kemurnian yang tinggi dan telah diketahui harus tersedia c. Prosedur kalibrasi yang sudah diketahui harus digunakan
Analisis kuantitatif dari suatu senyawa yang telah dipisahkan dengan KLT biasanya dilakukan dengan densitometer langsung pada lempeng KLT (atau secara in situ). Densitometer dapat bekerja secara serapan atau fluoresensi. Kebanyakan densitometer mempunyai sumber cahaya, monokromator untuk memilih panjang gelombang yang cocok, sistem untuk memfokuskan sinar pada lempeng, pengganda foton, dan rekorder. Pada sistem serapan dapat dilakukan dengan model pantulan atau transmisi. Pada cara pantulan, yang diukur adalah sinar yang dipantulkan, yang dapat menggunakan sinar tampak maupun ultraviolet. Sementara itu, cara transmisi dilakukan dengan menyinari bercak dari satu sisi dan mengukur sinar yang diteruskan pada sisi lain. Pada kenyataannya, hanya sinar tampak yang dapat digunakan untuk metode ini (Gandjar dan Rohman, 2007).
F. Densitometri
20
Densitometri merupakan suatu analisis kuantitatif yang berdasarkan pada interaksi radiasi elektromagnetik dengan analit yang merupakan bercak KLT. Densitometri lebih banyak digunakan untuk megukur analit dengan kadar kecil yang mana perlu dilakukan pemisahan terlebih dahulu dengan KLT (Rohman, 2009).
Pengukuran secara in situ suatu area dengan scanning densitometer adalah teknik yang digunakan untuk kuantitatif KLT. Jumlah senyawa yang dipisahkan dengan kromatografi lapis tipis dapat ditentukan kadarnya secara langsung pada lempeng kromatografi dengan pengukuran serapan UV/Vis maupun fluoresensi (Sherma, 1996).
Pada densitometri serapan, bercak pada lempeng kromatografi lapis tipis dideteksi oleh sinar monokromatik dibentuk menjadi gambar celah dengan panjang celah dipilih sesuai dengan diameter dari spot terbesar. Karena respon deteksi dari reflektansi-absorbansi tidak linier dengan konsentrasi, maka standar kalibrasi disertakan dalam setiap sampel. Batas deteksi minimum untuk pengukuran dengan UV atau visible antara 100 pg sampai 100 ng setiap bercak (Dean, 1995).
G. Landasan Teori
Colme® merupakan obat tetes telinga yang mengandung kloramfenikol 10% dan lidokain HCl 4% dengan cairan pembawa propilenglikol. Dalam rangka penjaminan mutu obat maka perlu dilakukan penetapan kadar untuk mengetahui kesesuain kadar yang tertera pada etiket.
Kloramfenikol dalam tetes telinga mengandung tidak kurang dari 90,0% dan tidak lebih dari 130,0% C11H12Cl2N2O5 dari jumlah yang tertera pada etiket. Kloramfenikol sukar larut dalam air, larut dalam etanol, agak larut dalam eter, dan kloroform. Kloramfenikol Memiliki pH 4-7,5, dan panjang gelombang maksimum pada 278 nm ( =298) dalam pelarut air. Kloramfenikol stabil dalam larutan netral atau larutan agak asam.
Larutan oral-topikal lidokain hidroklorida mengandung lidokain hidroklorida, C14H22N2O.HCl tidak kurang dari 95,0% dan tidak lebih dari 105,0% dari jumlah yang tertera pada etiket. Lidokain HCl larut dalam air, etanol dan koroform, tidak larut dalam eter. Dalam larutan asam, lidokain HCl memiliki serapan maksimum 263 nm ( = 19).
22
H. Hipotesis
1. Kadar kloramfenikol dan lidokain HCl yang diperoleh dengan metode kromatografi lapis tipis densitometri secara berturut-turut adalah 10% dan 4%. 2. Kadar kloramfenikol dan lidokain HCl yang ditetapkan dengan metode
kromatografi lapis tipis densitometri sesuai dengan kadar yang tertera pada etiket.
23
BAB III
METODE PENELITIAN
A. Jenis dan Rancangan Penelitian
Penelitian ini termasuk jenis penelitian non eksperimental diskriptif karena tidak dilakukan manipulasi dan perlakuan terhadap subjek uji.
B. Variabel Penelitian
1. Variabel bebas
Variabel bebas pada penelitian ini adalah tempat pengambilan sampel obat tetes telinga Colme®.
2. Variabel tergantung
Variabel tergantung penelitian ini adalah kadar dan reprodusibilitas kadar pada obat tetes telinga Colme®.
3. Variabel pengacau terkendali
24
C. Definisi Operasional
1. Obat tetes telinga adalah obat tetes yang digunakan dengan cara meneteskan ke dalam telinga. Kecuali dinyatakan lain, dibuat dengan menggunakan pembawa bukan air.
2. Colme® merupakan obat tetes telinga yang mengandung kloramfenikol 10%, lidokain HCl 4% dengan cairan pembawa propilenglikol.
3. Kadar kloramfenikol dan lidokain hidroklorida dalam obat tetes telinga Colme® dinyatakan dalam % b/v.
4. Kromatografi lapis tipis (KLT) yang digunakan yaitu fase normal dengan fase diam silika gel 60 F254 dan fase gerak heksana:toluena:dietilamin:metanol (15:79:6:20).
D. Bahan Penelitian
Bahan-bahan yang digunakan adalah baku kloramfenikol dari Chemo Lugano Branch dengan nomor batch 80002250001 dan baku lidokain HCl dari
Megafine Pharma dengan nomor batch ALH/449/10, lempeng KLT silika gel 60 F254 (E. Merck), etanol p.a (E. Merck), toluena p.a (E. Merck), heksana p.a (E. Merck), metanol p.a (E. Merck), dietilamin p.a (E. Merck), aquadest, obat tetes telinga Colme® kemasan 8 mL produksi Interbat dengan nomor batch D 016102.
E. Alat Penelitian
Alat-alat yang digunakan dalam penelitian ini adalah seperangkat alat densitometer (Camag TLC Scanner 3 CAT. No. 027.6485 SER. No.160602) autosampler (Linomat 5 No.170610), neraca analitik (OHAOUS Carat Series PAJ 1003, max 60/120 g, min 0,0001 g, d = 0,01/0,1 mg, e = 1 mg), neraca analitik (Scaltec SBC 22 max 60/210 g; min 0,001 g; d=0,01/0,1mg; e=1mg), mikro pipet
Scorex, bejana kromatografi (Camag), alat-alat gelas (Pyrex), kertas saring.
F. Tata Cara Penelitian
1. Pemilihan dan pengambilan sampel
Sampel yang dipilih adalah obat tetes telinga Colme® yang mencantumkan kloramfenikol dan lidokain HCl pada kemasan dengan nomor batch yang sama. Sebanyak 20 buah sampel Colme® dicampur hingga homogen kemudian ditetapkan kadarnya dengan dilakukan 10 kali replikasi.
2. Pembuatan fase gerak
26
3. Penetapan panjang gelombang pengamatan
Larutan baku kloramfenikol 300 ppm dan lidokain HCl 3000 ppm masing-masing ditotolkan sebanyak 1, 2, dan 3 µ L pada lempeng silika gel 60 F254 dengan jarak antar totolan 1 cm. Kemudian dikembangkan di dalam bejana kromatografi yang telah dijenuhi dengan fase gerak. Setelah mencapai jarak pengembangan 10 cm, lempeng dikeluarkan dan dikeringkan. Penentuan panjang gelombang pengamatan dilakukan dengan merekam pola spektra absorbsi masing-masing seri jumlah pada daerah panjang gelombang 200-400 nm menggunakan densitometer. Overlapping
spektra kloramfenikol dan lidokain HCL diukur pada level rendah, sedang, dan tinggi. Untuk kloramfenikol pada seri jumlah 300; 600; dan 900 ng. Untuk lidokain HCl pada seri jumlah 3000; 6000; dan 9000 ng.
4. Pembuatan larutan baku kloramfenikol
a. Pembuatan larutan stok. Baku kloramfenikol lebih kurang 10,0 mg ditimbang seksama dan dimasukkan ke dalam labu takar 10 ml, kemudian dilarutkan dengan etanol sampai tanda batas sehingga diperoleh larutan stok kloramfenikol 1000 ppm.
b. Pembuatan seri jumlah baku. Larutan stok diambil sebanyak 1,5 mL menggunakan mikro pipet, lalu dimasukkan ke dalam labu ukur 5 mL dan diencerkan dengan etanol hingga batas. Larutan digojog hingga diperoleh konsentrasi larutan baku kloramfenikol 300 ppm. Larutan baku kloramfenikol 300 ppm ditotolkan sejumlah 1; 1,5; 2; 2,5; 3 µL pada lempeng silika gel 60 F254 sehingga diperoleh seri jumlah 300; 450 ; 600; 750; dan 900 ng.
5. Pembuatan larutan baku lidokain HCl
a. Pembuatan larutan stok. Baku lidokain HCl lebih kurang 30,0 mg ditimbang seksama dan dimasukkan ke dalam labu takar 10 ml, kemudian dilarutkan dengan etanol sampai tanda batas sehingga diperoleh larutan stok kloramfenikol 3000 ppm.
b. Pembuatan seri jumlah baku. Larutan stok lidokain HCl 3000 ppm ditotolkan dengan volume 1; 1,5; 2; 2,5; 3 µL pada lempeng silika gel 60 F254 sehingga diperoleh seri jumlah 3000; 4500; 6000; 7500; dan 9000 ng.
6. Pembuatan kurva baku kloramfenikol dan lidokain hidroklorida
Larutan baku kloramfenikol dengan kadar 300 ppm ditotolkan pada lempeng silika gel 60 F254 dengan jarak totolan 1 cm sejumlah 1; 1,5; 2; 2,5; 3 µ L sehingga diperoleh seri jumlah 300; 450; 600; 750; dan 900 ng, kemudian segera dikembangkan dalam bejana kromatografi yang telah dijenuhkan dengan fase gerak. Pengembangan dilakukan setinggi 10 cm. Lempeng silika gel 60 F254 segera dikeluarkan dan dikeringkan setelah pengembangan selesai.
28
Bercak seri kloramfenikol dan lidokain HCl diukur AUC-nya dengan densitometri pada panjang gelombang pengamatan yang telah diperoleh. Puncak kromatogram dan nilai AUC yang muncul diamati. Dengan metode regresi linear, nilai seri jumlah (ng) diplotkan terhadap nilai AUC masing-masing seri larutan baku sehingga diperoleh persamaan y = bx + a dimana y merupakan nilai respon (AUC), x merupakan konsentrasi senyawa baku, a adalah intersept, dan b adalah slope. Pembuatan kurva baku direplikasi sebanyak 3 kali dan dipilih persamaan kurva baku kloramfenikol dan lidokain HCl paling baik berdasarkan nilai koefisien korelasi (r).
7. Preparasi sampel
Dua puluh sampel obat tetes telinga Colme®dengan nomor batch yang sama dikeluarkan isinya dan dicampur hingga homogen. Sebanyak 0,75 mL sampel diambil dengan mikro pipet dan dimasukkan ke dalam labu takar 5 mL, kemudian diencerkan dengan etanol hingga batas dan gojog hingga homogen (Larutan A). Sebanyak 0,2 mL larutan A diambil dengan mikro pipet dan dimasukkan ke dalam labu takar 5 mL, kemudian diencerkan dengan etanol hingga tanda dan gojog sampai homogen (Larutan B). Larutan A dan larutan B siap ditotol.
8. Penetapan kadar
Sebanyak 1 µL larutan sampel (larutan A) dan (larutan B) ditotolkan pada lempeng silika gel 60 F254, kemudian dikembangkan dalam bejana kromatografi yang telah dijenuhkan dengan fase gerak heksana:toluene:dietilamin:metanol (15:79:6:20). Pengembangan dilakukan setinggi 10 cm, lempeng silika kemudian dikeluarkan,
dikeringkan, dan scanning pada panjang gelombang pengamatan dengan densitometri.
G. Analisis Hasil
Analisis kualitatif dilakukan dengan membandingkan nilai Rf sampel dengan nilai Rf baku. Analisis kuantitatif yang dilakukan adalah penetapan kadar kloramfenikol dan lidokain HCl berdasarkan data AUC dari masing-masing baku sehingga diperoleh persamaan regresi linear y = bx + a yang merupakan hubungan antara kadar dengan luas area yang dihasilkan. Data AUC sampel kemudian dimasukkan dalam persamaan regresi masing-masing baku sebagai y sehingga diperoleh kadar kloramfenikol dan lidokain HCl dalam % b/v.
Parameter yang digunakan untuk melihat reprodusibilitas kadar dalam obat tetes telinga Colme® adalah nilai KV. Nilai KV dapat dihitung dengan cara :
KV =
30
BAB IV
HASIL DAN PEMBAHASAN
Metode kromatografi lapis tipis densitometri dapat digunakan untuk menetapkan kadar kloramfenikol dan lidokain HCl dalam obat tetes telinga Colme® yang diawali dengan tahap optimasi dan validasi. Pada tahap optimasi diperoleh komposisi fase gerak yang optimal untuk pemisahan kloramfenikol dan lidokain HCl yaitu heksana:toluena:dietilamin:metanol (15:79:6:20). Fase gerak tersebut dapat menghasilkan pemisahan baku campuran yang baik dengan nilai Rf kloramfenikol 2,4 dan nilai Rf lidokain HCl 4,7.
Pada tahap validasi metode diperoleh hasil bahwa kloramfenikol memiliki rentang validitas yang memenuhi persyaratan presisi, akurasi, dan linearitas pada seri jumlah 300-600 ng. Untuk lidokain HCl memiliki presisi yang baik pada seri jumlah 3000-6000 ng dan akurasi yang baik pada seri jumlah 6000 ng.
A. Pemilihan Sampel
Sampel yang digunakan pada penelitian ini adalah sediaan obat tetes telinga Colme® yang memiliki nomor registrasi dan nomor batch yang sama serta mencantumkan komposisi zat aktif kloramfenikol dan lidokain HCl. Sampel diperoleh dari PT. Interbat sebanyak 30 buah dengan nomor batch D016102. Sampel tersebut kemudian dipilih sebanyak 20 buah secara acak untuk ditetapkan kadarnya
dengan dilakukan replikasi sebanyak 10 kali. Pada etiket kemasan tertera kandungan kloramfenikol 10% dan lidokain HCl 4% dengan volume 8 mL per kemasan. Untuk tahap awal identifikasi sebelum dilakukan penetapan kadar, dilakukan uji keseragaman volume sampel.
Kloramfenikol dan lidokain HCl yang akan dianalisis dalam sampel Colme® berada dalam cairan pembawa propilenglikol sehingga termasuk dalam kategori cairan kental. Persyaratan kelebihan volume yang dianjurkan untuk volume 8 mL yang tertera dalam penandaan pada kategori cairan kental adalah 0,8 mL (Direktorat Jendral Pengawasan Obat dan Makanan RI, 1995). Berikut ini adalah tabel hasil pengujian keseragaman volume sampel Colme® :
Tabel III. Keseragaman volume sampel Colme®
32
Volume sampel hasil pengujian diperoleh dari konversi berat sampel dalam kemasan yang dilakukan dengan menghitung berat jenis sampel menggunakan piknometer. Berat jenis sampel yang diperoleh adalah 1,0746 g/mL.
Uji keseragaman volume dilakukan pada 20 buah sampel. Dari tabel III, dapat dilihat bahwa semua sampel memenuhi persyaratan keseragaman volume karena tidak ada satupun dari sampel yang volumenya melebihi persyaratan yang ditentukan yaitu 0,8 mL.
B. Fase Gerak
Fase gerak yang digunakan pada penelitian ini adalah fase gerak yang diperoleh dari hasil optimasi yaitu heksana:toluena:dietilamin:metanol (15:79:6:20). Fase gerak yang digunakan memiliki nilai indeks polaritas 2,53. Fase gerak tersebut dapat menghasilkan pemisahan yang optimal untuk kloramfenikol dan lidokain HCl. Fase gerak yang digunakan bersifat non polar, sedangkan fase diam yang digunakan pada penelitian ini adalah silika gel 60 F254 yang bersifat polar, maka sistem kromatografi yang digunakan adalah kromatografi fase normal.
Adanya heksana dan toluena yang bersifat non polar berfungsi untuk menahan elusi kloramfenikol agar dapat terpisah dengan lidokain. Dietilamin dengan pKb 2,9 memberikan suasana basa. Suasana basa diperlukan untuk menjaga lidokain HCl yang merupakan garam tetap berada dalam bentuk basanya. Metanol yang digunakan berfungsi untuk meningkatkan elusi lidokain karena lidokain larut dalam metanol.
C. Larutan Baku
Larutan baku dibuat dengan seri jumlah tertentu. Pelarut yang digunakan adalah etanol karena kedua senyawa larut dalam etanol. Selain itu, etanol memenuhi syarat pelarut yang digunakan untuk kromatografi lapis tipis yaitu murni dan mudah menguap.
Perbandingan larutan baku antara kloramfenikol dan lidokain HCl adalah 1:10 yang diperoleh dari hasil optimasi dan validasi metode. Perbandingan tersebut tidak sesuai dengan perbandingan yang tertera pada sampel yaitu 5:2. Perbandingan yang tertera pada sampel tidak dapat digunakan pada penelitian ini karena serapan lidokain HCl yang sangat kecil. Hal tersebut dapat dilihat dari nilai untuk lidokain HCl adalah 19. Agar dapat terdeteksi maka lidokain HCl harus dalam kadar yang besar. Kloramfenikol memiliki nilai = 298 yang berarti bahwa kloramfenikol memiliki serapan yang lebih besar dari pada lidokain HCl, sehingga dalam jumlah yang kecil kloramfenikol dapat terdeteksi.
34
D. Penetapan Panjang Gelombang Pengamatan
Penetapan λ pengamatan bertujuan untuk mengetahui λ yang memberikan serapan optimal untuk kloramfenikol dan lidokain HCl. Penetapan λ pengamatan dilakukan dengan mengamati λ overlapping antara kloramfenikol dan lidokain HCl. Pengukuran λ kloramfenikol dan lidokain HCl dilakukan pada perbandingan 1:10 dengan tiga seri jumlah. Tiga seri jumlah yang digunakan merupakan level rendah, sedang, dan tinggi yang dapat mewakili seri jumlah pada kurva baku yang digunakan. Seri jumlah untuk kloramfenikol adalah 300; 600; dan 900 ng. Seri jumlah untuk lidokain HCl adalah 3000; 6000; dan 9000 ng. Pembacaan serapan dilakukan pada rentang λ 200-400 nm karena panjang gelombang kloramfenikol dan lidokain HCl berada pada rentang tersebut.
Pengukuran λ dilakukan dengan menggunakan densitometri yang memiliki detektor lampu D2 yang dapat menghasilkan sinar UV. Suatu senyawa dapat diukur serapannya pada daerah UV apabila senyawa tersebut memiliki gugus kromofor dan auksokrom. Berikut ini adalah gambar gugus kromofor dan auksokrom kloramfenikol dan lidokain HCl :
Gambar 8. Gugus kromofor dan gugus auksokrom kloramfenikol
auksokrom kromofor
Gambar 9. Gugus kromofor dan gugus auksokrom lidokain HCl
Berikut ini adalah hasil spektra panjang gelombang kloramfenikol dan lidokain HCl pada seri rendah, sedang dan tinggi:
Gambar 10. Spektra kloramfenikol 300 ng dan lidokain HCl 3000 ng Kloramfenikol
Lidokain HCl
36
Gambar 11. Spektra kloramfenikol 600 ng lidokain HCl 6000 ng
Gambar 12. Spektra kloramfenikol 900 ng dan lidokain HCl 9000 ng
Berdasarkan hasil yang diperoleh pada penelitian ini, panjang gelombang maksimum untuk kloramfenikol adalah 281 nm dan panjang gelombang maksimum untuk lidokain HCl adalah 263 nm. Secara teoritis kloramfenikol memiliki panjang gelombang maksimum pada 278 nm ( =298) dalam pelarut air, sedangkan
Kloramfenikol
Lidokain HCl
Kloramfenikol Lidokain
HCl
lidokain HCl memiliki serapan maksimum 263 nm ( = 19) dalam larutan asam (Clark, 1986). Berdasarkan hasil yang diperoleh, terjadi pergeseran 3 nm pada λ kloramfenikol dari hasil teoritis. Hal tersebut dikarenakan adanya perbedaan instrument yang digunakan. Untuk lidokain HCl hasil yang diperoleh sesuai dengan teoritis.
Dari spektra yang diperoleh dapat dilihat bahwa untuk seri rendah, sedang dan tinggi memiliki titik potong pada panjang gelombang 242 nm. Panjang gelombang pengamatan yang digunakan pada penelitian ini adalah λ perpotongan antara kloramfenikol dan lidokain HCl yaitu 242 nm. Panjang gelombang tersebut dipilih agar kloramfenikol dan lidokain HCl dapat memberikan serapan optimal. Lidokain HCl memiliki serapan yang kecil sehingga penentuan panjang gelombang pengamatan mengarah pada serapan dari lidokain HCl.
E. Analisis Kualitatif
38
Pemisahan kloramfenikol dan lidokain pada KLT dapat terjadi karena terdapat perbedaan interaksi antara kedua senyawa dengan fase gerak maupun fase diam. Interaksi kloramfenikol dengan fase diam lebih dominan dari pada interaksi lidokain dengan fase diam. Hal ini menyebabkan kloramfenikol akan tertahan lebih lama pada fase diam, sedangkan lidokain akan terelusi lebih dulu. Dari interaksi tersebut dapat dikatakan bahwa kloramfenikol bersifat lebih polar dari pada lidokain. Interaksi yang terjadi antara kloramfenikol dan lidokain HCl dengan fase diam adalah interaksi hidogen. Berikut ini adalah gambar interaksi kloramfenikol dan lidokain dengan fase diam:
Gambar 13. Interaksi kloramfenikol dengan fase diam
Interaksi hidrogen
N C
Gambar 14. Interaksi lidokain dengan fase diam
- - - -interaksi hidrogen
40
Gambar 15. Interaksi kloramfenikol dengan fase gerak heksana:toluene:dietilamin:metanol (15:79:6:20)
Interaki Van Der Waals Interaksi hidrogen
Gambar 16. Interaksi lidokain dengan fase gerak heksana:toluene:dietilamin:metanol (15:79:6:20)
Analisis kualitatif dilakukan dengan membandingkan Rf baku dengan Rf sampel. Berikut ini adalah kromatogram baku dan sampel:
A
B
42
D
Gambar 17. Kromatogram pemisahan kloramfenikol dan lidokain HCl A. Baku kloramfenikol seri tengah 600 ng
B. Baku lidokain HCl seri tengah 6000 ng C. Sampel Colme® (larutan A) D. Sampel Colme® (larutan B)
Dari kromatogram dapat dilihat bahwa terdapat perbedaan nilai Rf antara kloramfenikol dan lidokain. Perbedaan nilai Rf dikarenakan adanya perbedaaan interaksi antara kedua senyawa dengan fase diam dan fase gerak. Perbedaan nilai Rf tersebut menunjukkan terjadinya pemisahan antara kloramfenikol dan lidokain. Pemisahan yang optimal dapat diketahui dari nilai resolusi (resolusi yang baik adalah
lebih dari 1,5 dimana pemisahannya ≥99,7%) (Sastrohamidjojo, 2002). Resolusi
sampel yang diperoleh adalah 2,83. Hal tersebut menunjukkan bahwa terjadi pemisahan yang baik antara kloramfenikol dan lidokain.
Berikut ini adalah tabel perbandingan nilai Rf baku kloramfenikol, baku lidokain HCl, dan nilai Rf kedua senyawa dalam sampel :
Tabel IV. Data nilai Rf baku kloramfenikol, baku lidokain HCl dan sampel
Senyawa Rf baku Rf sampel (lar A) Rf sampel (lar B) Kloramfenikol 0,25 0,14 0,23
Lidokain HCl 0,47 0,48 -
Berdasarkan hasil yang diperoleh, nilai Rf baku kloramfenikol adalah 0,25. Nilai Rf kloramfenikol dalam sampel (larutan A) adalah 0,14. Perbedaan nilai Rf tersebut dikarenakan jumlah kloramfenikol yang ditotolkan pada sampel (larutan A) terlalu besar sehingga peak kloramfenikol tailing. Nilai Rf kloramfenikol dalam sampel (larutan B) adalah 0,23. Data AUC kloramfenikol pada larutan B yang akan digunakan untuk analisis kuantitatif selanjutnya. Nilai Rf pada sampel larutan B berbeda dengan nilai Rf pada baku dikarenakan adanya propilenglikol sebagai cairan pembawa pada sampel sehingga memperlambat elusi kloramfenikol. Untuk lidokain, nilai Rf baku adalah 0,47 dan nilai Rf sampel (larutan A) adalah 0,48. Data AUC lidokain pada sampel larutan A yang akan digunakan untuk analisis kuantitatif selanjutnya. Untuk sampel (larutan B) tidak terdeteksi adanya peak lidokain karena jumlah lidokain yang ditotolkan terlalu kecil. Dari data yang diperoleh, dapat disimpulkan bahwa sampel Colme® mengandung kloramfenikol dan lidokain HCl.
F. Kurva Baku Kloramfenikol dan Lidokain HCl
44
(Mulja dan Hanwar, 2003). Data persamaan kurva baku kloramfenikol dan lidokain HCl yang diperoleh adalah sebagai berikut:
Tabel V. Data persamaan kuva baku kloramfenikol Baku Kloramfenikol
Replikasi 1 Replikasi 2 Replikasi 3
Jumlah (ng) AUC Jumlah (ng) AUC AUC
Persamaan kurva baku kloramfenikol yang digunakan untuk penetapan kadar adalah replikasi 2, yaitu y = 3,8992 x + 392,5. Pada tabel V dapat dilihat bahwa untuk kurva baku replikasi 2 memiliki nilai koefisien korelasi paling tinggi yaitu 0,9998. Kurva baku tersebut memenuhi persyaratan linearitas yang baik dengan nilai r > 0,999.
Tabel VI. Data persamaan kurva baku lidokain HCl Baku Lidokain HCl
Replikasi 1 Replikasi 2 Replikasi 3
Persamaan kurva baku lidokain HCl yang digunakan untuk penetapan kadar adalah replikasi 2, yaitu y = 0,9181 x + 1310,74. Pada tabel VI dapat dilihat bahwa untuk kurva baku replikasi 2 memiliki nilai koefisien korelasi paling tinggi yaitu 0,9997. Kurva baku tersebut memenuhi persyaratan linearitas yang baik dengan nilai r > 0,999.
Gambar 18. Kurva baku kloramfenikol
Gambar 19. Kurva baku lidokain HCl
y = 0.975x + 98.04
0 2000 4000 6000 8000 10000 12000
AUC
46
Berdasarkan gambar 18 dan 19 dapat dilihat bahwa terjadi peningkatan respon AUC seiring dengan meningkatnya konsentrasi analit baik untuk kloramfenikol maupun lidokain HCl sehingga menghasilkan linearitas yang baik.
G. Penetapan Kadar Kloramfenikol dan Lidokain HCl Dalam Sampel
Analisis kuantitatif dilakukan dengan menghitung kadar kloramfenikol dan lidokain HCl dalam sampel. Pada penelitian ini digunakan 20 buah sampel dengan nomor batch yang sama dan dilakukan replikasi sebanyak 10 kali. Pada etiket sampel Colme® , perbandingan kloramfenikol dan lidokain HCl adalah 5:2. Perbandingan tersebut tidak digunakan pada penelitian ini karena respon lidokain HCl terlalu kecil sehingga tidak dapat terdeteksi. Maka pada penelitian ini digunakan perbandingan untuk kloramfenikol : lidokain HCl yaitu 1:10.
Pada penelitian ini dilakukan 2 tahap preparasi sampel. Tahap pertama diperoleh larutan A dengan konsentrasi kloramfenikol 15000 ppm dan lidokain HCl 6000 ppm. Tahap kedua diperoleh larutan B dengan konsentrasi kloramfenikol 600 ppm dan lidokain HCl 160 ppm. Dari preparasi pertama (larutan A) akan diperoleh data AUC lidokain HCl dan dari preparasi kedua (larutan B) akan diperoleh data AUC kloramfenikol yang digunakan untuk menghitung kadar masing-masing senyawa. Dilakukan 2 tahap preparasi bertujuan agar kloramfenikol dan lidokain HCl dapat terdeteksi pada konsentrasi yang ditentukan sesuai dengan perbandingan. Konsentrasi sampel diarahkan pada seri tengah yang memiliki validitas yang baik yaitu 600 ng untuk kloramfenikol dan 6000 ng untuk lidokain HCl.
Tabel VII. Hasil penetapan kadar campuran kloramfenikol dan lidokain HCl dalam sampel Colme®
No. Kloramfenikol Lidokain HCl
AUC Kadar (% b/v) AUC Kadar (% b/v)
Dalam etiket yang tertera pada kemasan menunjukkan kandungan kloramfenikol 10% dan lidokain HCl 4%. Rentang kadar yang diperbolehkan untuk kloramfenikol dalam tetes telinga adalah 90-130%, maka rentang kadar kloramfenikol yang diperbolehkan untuk kloramfenikol dalam sampel Colme® adalah 9-13%. Berdasarkan hasil yang diperoleh, rentang kadar kloramfenikol adalah 9,940-10,79% (b/v). Dari 10 replikasi sampel, tidak ada satupun sampel yang berada di luar rentang yang dipersyaratkan.
48
Hasil yang diperoleh menunjukkan bahwa kloramfenikol masuk dalam rentang persyaratan 90-130% dari rentang yang tertera pada etiket. Lidokain HCl tidak masuk dalam rentang persyaratan 95-105% dari yang tertera dalam etiket, hal tersebut dapat dikarenakan proporsi lidokain HCl yang terlalu kecil dalam campuran sehingga kurang homogen saat dicampur.
Nilai KV yang diperoleh untuk kloramfenikol adalah 3,00% dan untuk lidokain HCl adalah 1,33%. Nilai KV tersebut memenuhi persyaratan yang ditentukan yaitu 16% untuk kloramfenikol dan 5% untuk lidokain HCl. Dari nilai KV tersebut dapat disimpulkan bahwa kadar kloramfenikol dan lidokain HCl memiliki reprodusibilitas yang baik.
49
BAB V
KESIMPULAN DAN SARAN
A. KESIMPULAN
1. Kadar kloramfenikol adalah 9,940-10,79% (b/v) dan kadar lidokain HCl adalah 3,68-3,84% (b/v).
2. Kadar kloramfenikol sesuai dengan kadar yang tertera pada etiket, sedangkan kadar lidokain HCl yang diperoleh lebih kecil dari pada kadar yang tertera pada etiket.
B. SARAN
50
DAFTAR PUSTAKA
Anonima, 2010, Chloramphenicol, http://www.lookfordiagnosis.com/meshinfo. php?term=Chloramph%C3%A9nicol&lang=4, diakses tanggal 1 Mei 2011. Anonimb, 2010, Colme Tetes Telinga,
http://www.dechacare.com/COLME-Tetes-Telinga- P602.html , diakses tanggal 11 Agustus 2011.
Anonimc, 2010, Gangguan Pendengaran Masih Terabaikan, http: //www1.kompas.com/read/xml/2010/01/11/07584914/gangguan.penderan.mas ih.terabaikan, diakses tanggal 30 Maret 2011.
Anonima, 2011, Lidocaine Hidrochloride Solition, http://dailymed.nlm.nih.gov/ dailymed/drugInfo.cfm?id=9555, diakses tanggal 1 Mei 2011.
Anonimb, 2011, Obat Telinga, http://medicastore.com/apotik_online/obat_telinga .htm, diakses tanggal 26 April, 2011.
Christian, G. D., 2004, Analytical Chemistry, 6th ed, John Willey Sons, USA, pp. 627, 629.
Clarke, E.G.C., 1969, Isolation and Identification of Drug in Pharmaceuticals Body Fluid and Post-Material, The Pharmaceutical Press, London, pp. 246, 329. Clarke, E.G.C., 1986, Isolation and Identification of Drug in Pharmaceuticals Body
Fluid and Post-Material, The Pharmaceutical Press, London, pp. 160, 705. Dean, J., 1995, Analytical Chemistry Handbook, Mc Graw-Hill Companies Inc.,
USA, pp. 5.93, 5.106.
Direktorat Jendral Pengawasan Obat dan Makanan RI, 1979, Farmakope Indonesia,
edisi III, Departemen Kesehatan Republik Indonesia, Jakarta, hal. 9,10,19. Direktorat Jendral Pengawasan Obat dan Makanan RI, 1995, Farmakope Indonesia,
edisi IV, Departemen Kesehatan Republik Indonesia, Jakarta, hal. 15,16, 189, 497.
Gandjar, I. G., dan Rohman, A., Kimia Farmasi Analisis, 2007, Pustaka Pelajar, Yogyakarta, hal. 323-324, 353-354, 359-360.
Hauck, H. E., and Mack, M., 1996, Handbook of Thin Layer Chromatography :
Sorbents and Precoated Layer in Thin Layer Chromatography, 2nd ed, Marcel Dekker, USA, pp. 102.
Jaenchen, D. E., 1996, Handbook of Thin Layer Chromatography : Planar
Chromatography (Instrumental Thin-Layer Chromatography), 2nd ed, Marcel Dekker, USA, pp. 142.
Kiszka, M., Madro, R., 2011, The Usefulness of Thin-Layer Chromatography Method in the Identification of Cocaine and its Metabolite Benzoylecgonine in Autopsy Material, http://www.forensicscience.pl/component/option,com_ jbook/task,view/Itemid,9/catid,36/id,236/lang,en/, diakses tanggal 22 Agustus 2011.
Kowalska, T., 1996, Handbook of Thin Layer Chromatography : Theory and
Mechanism of Thin-Layer Chromatography, 2nd ed, Marcel Dekker, USA, pp. 55-57.
Mulja, M., dan Hanwar, D., 2003, Prinsip-prinsip Cara Berlaboratorium yang Baik (Good Laboratory Practice), Majalah Farmasi Airlangga, Vol III no 2, hal. 73.
Munson, J.W., 1991, Pharmaceutical Analysis Methods, diterjemahkan oleh Harjana, Parawa.B., Universitas Airlangga Press Surabaya, hal. 128.
Pescok, R. L., Shields, L. D., and Cains, T., 1976, Modern Methods of Chemical Analysis, 2nd ed, John Willey Sons, Inc, Canada, pp. 81.
Rohman, A., 2009, Kromatografi Untuk Analisis Obat, Graha Ilmu, Yogyakarta, hal. 53.
Sastrohamidjojo, H., 2002, Kromatografi, Penerbit Liberty, Yogyakarta, hal 68.
Sherma, J., 1996, Handbook of Thin Layer Chromatography: Basic Thechniques, Material, and Apparatus, 2nd ed, Marcel Dekker, USA, pp. 37.
Snyder, L.R., Kirkland, J.J., and Glajch, j.L., 1997, Practical HPLC Method Development, 2
nd
ed., Wiley & Sons, Inc., New York, pp. 208-209, 252. Stahl, E., 1985, Drug Analysis by Chromatography and Microscopy, diterjemahkan
52
Tjay a, T.H., dan Rahardja, K., 2010, Obat-Obat Penting : Khasiat, Penggunaan, dan Efek-Efek Sampingnya, PT Elex Media Komputindo Kelompok Kompas-Gramedia, Jakarta, hal. 82,388.
Tjay b, T.H., dan Rahardja, K., 2010, Obat-Obat Sederhana Untuk Gangguan Sehari-hari, PT Elex Media Komputindo Kelompok Kompas-Gramedia, Jakarta, hal. 135.
Voigt, R., 1994, Buku Pelajaran Teknologi Farmasi, Edisi V, Gadjah Mada University Press,
Yogyakarta, hal. 936, 939.
Vovk, I., Simonovska, B., 2005, Development and Validation of a Thin layer Chromathographic Method for Determination of Chloramphenicol residues on pharmaceutical equipment surfaces,http://www.ncbi.
nlm.nih.gov/pubmed/16386009, diakses tanggal 8 Mei 2011.
54
Lampiran 1. Sertifikat analisis kloramfenikol
56
Lampiran 3. Sistem KLT densitometri yang digunakan
Lampiran 4. Data penimbangan baku kloramfenikol dan lidokain HCl
1. Baku kloramfenikol
Kloramfenikol (g) Replikasi 1 Replikasi 2 Replikasi 3
Berat kertas 0,24247 0,24955 0,25342
Berat kertas + zat 0,25246 0,25956 0,26343
Berat kertas + zat 0,25240 0,25950 0,26340
Berat kertas + sisa 0,24240 0,24950 0,25340
Berat zat 0,0100 g 0,0100 g 0,0100 g
2. Baku lidokain HCl
Lidokain HCl (g) Rep 1 Rep 2 Rep 3
Berat kertas 0,24881 0,12844 0,12367
Berat kertas + zat 0,26381 0,14346 0,13861 Berat kertas + zat 0,26380 0,14340 0,13860 Berat kertas + sisa 0,24890 0,12840 0,12370
58
Lampiran 5. Spektra panjang gelombang pengamatan
1. Seri rendah
2. Seri sedang
3. Seri tinggi
Lampiran 6. Komatogram blanko plat kosong dan fase gerak
60
2. Fase gerak
Lampiran 7. Kromatogram baku kloramfenikol replikasi 2
1. 1 µL (297,30 ng)
2. 1,5 µL (445,95 ng)
3. 2 µL (594,60 ng)
4. 2,5 µL (743,25 ng)