PENETAPAN KADAR KLORAMFENIKOL DAN LIDOKAIN HIDROKLORIDA DALAM SEDIAAN TETES TELINGA COLME®
DENGAN METODE KROMATOGRAFI CAIR KINERJA TINGGI FASE TERBALIK
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm)
Program Studi Ilmu Farmasi
Oleh:
Efrida Lusia Sari Tambunan NIM: 088114033
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
PENETAPAN KADAR KLORAMFENIKOL DAN LIDOKAIN HIDROKLORIDA DALAM SEDIAAN TETES TELINGA COLME®
DENGAN METODE KROMATOGRAFI CAIR KINERJA TINGGI FASE TERBALIK
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm)
Program Studi Ilmu Farmasi
Oleh:
Efrida Lusia Sari Tambunan NIM: 088114033
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
2011
i
iii
Amsal 3: 12-14
“Karena TUHAN memberi ajaran kepada yang dikasihi-Nya, seperti seorang ayah kepada anak yang disayangi. Berbahagialah orang yang mendapat hikmat,
orang yang memperoleh kepandaian, karena keuntungannya melebihi keuntungan perak, dan hasilnya melebihi emas.”
Kupersembahkan karyaku ini untuk:
v
vii
PRAKATA
Puji dan syukur penulis panjatkan kepada Tuhan Yang Maha Kuasa atas
segala limpahan berkat dan kasih-Nya sehingga penelitian dan penyusunan skripsi
yang berjudul “Penetapan Kadar Kloramfenikol dan Lidokain Hidroklorida dalam
Sediaan Tetes Telinga Colme® dengan Metode KCKT Fase Terbalik” dapat
diselesaikan dengan baik. Skripsi ini disusun sebagai salah satu syarat untuk
meraih gelar Sarjana Farmasi (S.Farm) di Fakultas Farmasi, Universitas Sanata
Dharma, Yogyakarta.
Dalam pelaksanaan penelitian hingga selesainya penyusunan skripsi ini,
penulis mendapat banyak dukungan dan bantuan dari berbagai pihak. Oleh karena
itu, penulis mengucapkan terima kasih kepada:
1. Bapak Ipang Djunarko, M.Sc., Apt. selaku Dekan Fakultas Farmasi
Universitas Sanata Dharma Yogyakarta.
2. Ibu Christine Patramurti, M.Si., Apt. selaku dosen pembimbing yang
dengan sabar memberikan pengarahan, masukan, kritik dan saran baik
selama penelitian maupun penyusunan skripsi ini.
3. Bapak Jeffry Julianus, M.Si. selaku dosen penguji yang telah memberikan
saran dan kritik yang membangun dalam penyusunan skripsi.
4. Ibu Dra. M.M. Yetty Tjandrawati, M.Si. selaku dosen penguji yang telah
memberikan saran dan kritik yang membangun dalam penyusunan skripsi.
5. Ibu dr. Fenty, M. Kes., Sp.PK, selaku dosen pembimbing akademik atas
bimbingan dan semangat yang telah diberikan selama ini.
6. Ibu Rini Dwi Astuti, M.Sc, Apt. selaku Kepala Laboratorium Fakultas
Farmasi Universitas Sanata Dharma Yogyakarta.
7. Seluruh Dosen Fakultas Farmasi Universitas Sanata Dharma yang telah
memberikan ilmu yang bermanfaat demi kemajuan mahasiswa dalam
bidang farmasi.
8. Seluruh staf laboratorium kimia Fakultas Farmasi Universitas Sanata
Dharma: Mas Bimo, Mas Parlan, Mas Kunto, Mas Otok, dan Pak Timbul
yang telah banyak membantu selama penelitian di laboratorium.
9. Pak Siswanto selaku manager Research and Development PT. Interbat
yang telah membantu penulis dan tim penelitian dalam memperoleh baku
kloramfenikol dan lidokain hidroklorida serta sampel obat tetes telinga
Colme®.
10.Keluarga kedua sekaligus sahabat-sahabatku Ade Mauryn, Devi Sinaga,
Mariana, Melisa Darmawan, Monika Dika dan Novie Imoliana, Caroline
E. Daat, Eureka G. Letitia, Wiria S. Paiman, Rotua Silitonga, dan
Yoestenia. Terima kasih untuk kebersamaan, canda, tawa, suka, duka yang
telah kita lalui bersama.
11.Theresia Wijayanti dan Winarti H. Wibowo, teman seperjuangan dan
tempat berbagi keluh kesah selama penelitian dan penyusunan skripsi. I’ll
never forget you two, guys.
12.Tim “Kloramfenikol dan Lidokain Hidroklorida” Felicia Putri Hernat,
Regina Clarissa dan Prasilya. Terima kasih untuk diskusi, kebersamaan,
ix
13.Anasthasia Mardila, Theresia Wijayanti, Winarti Wibowo, teman
praktikum sejak semester pertama, tidak ada yang dapat menggantikan
posisi kalian.
14.Susi, Susan, Nona, Novi Chairio, Citra, Helena, Amel, Ayesa, dan Dina.
Terima kasih untuk diskusi dan kebersamaannya selama penelitian di
laboratorium.
15.Elya Findawati dan Margareth Henrika Silow sebagai teman bermain yang
selalu memberikan semangat kepada penulis dalam penyusunan skripsi ini.
16.Kelompok praktikum A2, Sasa, Yessi, Sin Lie, Lele, Tere, Lala, dan Wiwi
yang telah memberikan pengalaman yang berharga selama praktikum serta
telah memberikan semangat dalam penyusunan dan ujian skripsi.
17.Teman-teman kelompok praktikum A FST, dan teman-teman FST B atas
tawa, canda, kebersamaan dan kekompakan yang begitu indah dan tak
terlupakan.
18.Keluarga besar kost “Sari Ayu I”, Ibu Anti, Devi, Morin, Novi, Marjan,
Sasa, Monik, Kak Yanti, Kak Putri, Leza, Rotua, Yoestenia, Iness, Selly,
Kak Ade, Dwi, Jolina atas semangat yang diberikan kepada penulis dalam
penyusunan dan ujian skripsi.
19.Semua pihak yang tidak dapat disebutkan satu per satu yang telah
membantu penulis dalam mewujudkan skripsi ini.
Penulis menyadari bahwa masih banyak kekurangan dalam penyusunan
skripsi ini, sehingga segala kritik dan saran yang membangun sangat penulis
harapkan. Semoga skripsi ini membantu dan bermanfaat bagi pembaca pada
khususnya dan ilmu pengetahuan pada umumnya.
xi
DAFTAR ISI
Halaman
HALAMAN JUDUL………... i
HALAMAN PERSETUJUAN PEMBIMBING………. ii
HALAMAN PENGESAHAN………. iii
HALAMAN PERSEMBAHAN……….. iv
HALAMAN PERSETUJUAN PUBLIKASI……….. v
PERNYATAAN KEASLIAN KARYA……….. vi
PRAKATA……….. vii
DAFTAR ISI………... xi
DAFTAR TABEL………... xv
DAFTAR GAMBAR……….. xvi
DAFTAR LAMPIRAN………... xviii
INTISARI……… xix
ABSTRACT……….. xx
BAB I. PENGANTAR………
A. Latar Belakang………...
1. Permasalahan………...
2. Keaslian penelitian………..
3. Manfaat penelitian………...
B. Tujuan Penelitian………...
1
BAB II. PENELAAHAN PUSTAKA……….
A. Kloramfenikol………
5
5
B. Lidokain hidroklorida………
C. Obat tetes telinga………...
D. Obat tetes telinga Colme®……….
E. Spektrofotometri ultraviolet………..
F. Kromatografi Cair Kinerja Tinggi……….
1. Definisi dan instrumentasi………...
2. Kromatografi partisi fase terbalik………
3. Analisis kualitatif dan kuantitatif………
G. Landasan teori………...
H. Hipotesis………
BAB III. METODE PENELITIAN……….
A. Jenis dan rancangan penelitian………..
B. Variabel penelitian……….
C. Definisi operasional………...
D. Bahan penelitian………
E. Alat penelitian………...
F. Tata cara penelitian………
1. Pemilihan sampel………...
2. Pembuatan fase gerak……….
3. Pembuatan larutan baku kloramfenikol………..
4. Pembuatan larutan baku lidokain hidroklorida………...
5. Penetapan panjang gelombang pengamatan kloramfenikol
dan lidokain hidroklorida dengan spektrofotometer UV…
xiii
6. Pembuatan kurva baku kloramfenikol dan lidokain
hidroklorida………
7. Preparasi sampel……….
8. Penetapan kadar campuran kloramfenikol dan lidokain
hidroklorida……….
G. Analisis Hasil………
21
22
22
23
BAB IV. HASIL DAN PEMBAHASAN………
A. Pemilihan Sampel………..
B. Pembuatan Fase Gerak………..
C. Pembuatan Larutan Baku Kloramfenikol dan Lidokain
Hidroklorida………..
D. Penentuan Panjang Gelombang Pengamatan Kloramfenikol dan
Lidokain Hidroklorida dengan Spektrofotometer UV………….
E. Analisis Kualitatif Berdasarkan Waktu Retensi (tR)
Kloramfenikol dan Lidokain Hidroklorida………
F. Pembuatan Kurva Baku Kloramfenikol dan Lidokain
Hidroklorida………..
G. Penetapan Kadar Kloramfenikol dan Lidokain Hidroklorida
dalam Sediaan Tetes Telinga Colme® dengan Metode KCKT….
24
BAB V. KESIMPULAN DAN SARAN……….
A. Kesimpulan………
B. Saran ……….
44
44
44
DAFTAR PUSTAKA……….. 45
LAMPIRAN……… 48
xv
DAFTAR TABEL
Tabel I. Persyaratan keseragaman volume………... 8
Tabel II. Indeks polaritas beberapa pelarut………... 13
Tabel III. Keseragaman volume obat tetes telinga Colme®……... 25
Tabel IV. Data kurva baku kloramfenikol………. 38
Tabel V. Data kurva baku lidokain hidroklorida………... 39
Tabel VI. Data kurva baku kloramfenikol modifikasi…………... 39
Tabel VII. Data kurva baku lidokain hidroklorida modifikasi…… 39
Tabel VIII. Hasil penetapan kadar campuran kloramfenikol dan
lidokain hidroklorida dalam Colme®………... 42
DAFTAR GAMBAR
Gambar 1. Rumus struktur kloramfenikol………... 5
Gambar 2. Rumus struktur lidokain hidroklorida……… 6
Gambar 3. Obat tetes telinga Colme®……….. 8
Gambar 4. Diagram tingkat energi elektronik……… 10
Gambar 5. Peralatan KCKT………. 11
Gambar 6. Gugus kromofor dan auksokrom kloramfenikol……… 29
Gambar 7. Gugus kromofor dan auksokrom lidokain hidroklorida……… 29
Gambar 8. Spektra tumpang tindih kloramfenikol 13 ppm dan lidokain hidroklorida 300 ppm ………... 30
Gambar 9. Spektra tumpang tindih kloramfenikol 19,5 ppm dan lidokain hidroklorida 450 ppm……….. 30
Gambar 10. Spektra tumpang tindih kloramfenikol 26 ppm dan lidokain hidroklorida 600 ppm ………... 31
Gambar 11. Kromatogram baku kloramfenikol (500 ppm)………... 32
Gambar 12 Kromatogram baku lidokain hidroklorida (500 ppm)... 33
Gambar 13 Kromatogram sampel………. 33
Gambar 14 Kromatogram sampel adisi baku lidokain hidroklorida ………... 33
Gambar 15 Bagian polar dan non polar kloramfenikol……… 35
xvii
Gambar 17. Interaksi kloramfenikol dengan fase diam C18
(Oktadesilsilan) melalui interaksi Van Der Waals…… 36
Gambar 18. Interaksi lidokain hidroklorida dengan fase diam C18
(Oktadesilsilan) melalui interaksi Van Der Waals dan
interaksi ion-dipol……….. 36
Gambar 19. Interaksi kloramfenikol dengan fase gerak
metanol:aquabides (95:5)………... 37
Gambar 20. Interaksi lidokain dengan fase gerak
metanol:aquabides (95:5)………... 37
Gambar 21. Kurva hubungan antara jumlah kloramfenikol
vs AUC……….. 40
Gambar 22. Kurva hubungan antara jumlah lidokain hidroklorida
vs AUC……….. 40
DAFTAR LAMPIRAN
Lampiran 1 Sertifikat analisis kloramfenikol………... 49
Lampiran 2 Sertifikat analisis lidokain hidroklorida……… 50
Lampiran 3 Perhitungan bobot jenis sampel………. 51
Lampiran 4 Perhitungan keseragaman volume sampel…………. 52
Lampiran 5 Penimbangan baku dan contoh perhitungan kadar
baku……….... 53
Lampiran 6 Kromatogram baku……… 54
Lampiran 7 Kromatogram sampel………. 60
Lampiran 8 Kromatogram baku lidokain hidroklorida
300 ppm………. 65
Lampiran 9 Data kadar kloramfenikol dan lidokain
hidroklorida……… 70
Lampiran 10 Contoh perhitungan kadar kloramfenikol dan
lidokain hidroklorida………. 70
Lampiran 11 Perhitungan CV kloramfenikol dan lidokain
xix
INTISARI
Kloramfenikol dan lidokain hidroklorida merupakan kombinasi zat aktif yang terdapat dalam sediaan tetes telinga Colme®. Kombinasi zat aktif ditujukan untuk meningkatkan efek terapi bagi pasien sebagai pengguna obat. Penetapan kadar kloramfenikol dan lidokain hidroklorida perlu dilakukan sebagai pengawasan mutu dari jumlah obat karena berkaitan dengan dosis obat dalam sediaan tetes telinga Colme®.
Penelitian ini merupakan penelitian non eksperimental deskriptif. Kromatografi Cair Kinerja Tinggi (KCKT) fase terbalik yang digunakan adalah kondisi sistem yang optimal dan memenuhi parameter validasi. Sistem KCKT fase terbalik yang optimal menggunakan fase diam oktadesilsilan (C18), fase gerak
metanol:aquabides (95:5, v/v), kecepatan alir 1,0 ml/menit dengan detektor UV pada panjang gelombang 242 nm.
Kadar kloramfenikol dan lidokain hidroklorida dalam sediaan yang diteliti yaitu 11,01-12,21% untuk kloramfenikol dan 3,62-4,09% untuk lidokain hidroklorida. Kadar kloramfenikol yang diperoleh sesuai dengan yang tertera pada label kemasan, namun untuk kadar lidokain tidak sesuai dengan yang tertera pada label kemasan obat tetes telinga Colme®.
Kata kunci: kloramfenikol, lidokain hidroklorida, KCKT fase terbalik, penetapan kadar, sediaan tetes telinga Colme®
ABSTRACT
Chloramphenicol and lidocaine hydrochloride is a combination of active substances contained in Colme® ear drops. The combination of active substances intended to improve the theraupetic effects for patiens. The determination of chloramphenicol and lidocaine hydrochloride is needed to quality control of the drugs because it is associated with amount of the drug in Colme® ear drops.
This study is a non experimental descriptive. Reversed phase High Performance Liquid Chromatography (HPLC) is used optimum conditions and fulfill the validation parameters. The optimal conditions of HPLC system is used stationary phase octadecylsylane (C18), mobile phase methanol:aquabides (95:5,
v/v), flow rate 1,0 mL/min with UV detector at wavelength 242 nm.
The amount of chloramphenicol and lidocaine hydrochloride in the whole sample is 11,01%-12,21% for chloramphenicol and 3,62%-4,09% for lidocaine hydrochloride. The amount of cholramphenicol obtained is appropriate on the packaging label but the amount of lidocaine hydrochloride is inappropriate on the packaging label of Colme® ear drops.
Key words: chloramphenicol, lidocaine hydrochloride, reversed phase HPLC, determination, Colme® ear drops
BAB I
PENGANTAR
A. Latar Belakang
Kloramfenikol dan lidokain hidroklorida merupakan salah satu
kombinasi zat aktif yang terdapat di dalam sediaan obat tetes telinga. Kombinasi
zat aktif dalam suatu sediaan bertujuan untuk meningkatkan daya kerja terapeutis
dari sediaan. Sediaan obat tetes telinga yang mengandung zat aktif kloramfenikol
dan lidokain hidroklorida adalah obat tetes telinga Colme®. Obat tetes telinga
adalah obat tetes yang digunakan dengan cara meneteskan cairan obat ke dalam
telinga (Direktorat Jenderal Pengawasan Obat dan Makanan RI, 1979).
Kloramfenikol merupakan antibiotik bakteriostatik berspektrum luas
yang aktif terhadap organisme-organisme aerob dan anaerob gram positif maupun
gram negatif (Katzung, 2004). Lidokain hidroklorida yang ditambahkan ke dalam
obat tetes telinga diindikasikan sebagai zat pemati rasa lokal pada kulit yang
mampu menghalangi rasa nyeri yang sering menyertai infeksi pada telinga (Tan
dan Rahardja, 2010). Menurut Farmakope Indonesia IV sediaan obat tetes telinga
mengandung tidak kurang dari 90% dan tidak lebih dari 130% kloramfenikol dan
untuk lidokain hidroklorida tidak kurang dari 95% dan tidak lebih dari 105% dari
jumlah yang tertera pada etiket (Direktorat Jenderal Pengawasan Obat dan
Makanan RI, 1995). Pada sediaan obat tetes telinga Colme® tertera jumlah
kloramfenikol sebesar 10% dan lidokain hidroklorida sebesar 4%. Oleh karena itu
perlu dilakukan analisis penetapan kadar kloramfenikol dan lidokain hidroklorida
sebagai pengawasan mutu dari kandungan dalam sediaan obat tetes telinga
tersebut.
Pengawasan mutu dari jumlah obat adalah sangat penting karena
berkaitan dengan dosis obat. Apabila dosisnya lebih rendah dari yang tertera pada
etiket tidak akan menghasilkan efek terapi yang diinginkan sedangkan dosis yang
berlebih akan menyebabkan terjadinya toksisitas pada tubuh pasien sehingga hal
ini dapat merugikan pasien sebagai pengguna obat.
Untuk menetapkan kadar kloramfenikol dan lidokain hidroklorida dalam
sediaan tersebut diperlukan pemilihan metode analisis yang tepat karena metode
analisis tersebut yang selanjutnya akan digunakan sebagai alat untuk pengawasan
mutu dari jumlah obat apakah sesuai dengan yang tertera pada etiket. Penetapan
kadar kloramfenikol dan benzokain dalam sediaan topikal dengan metode KCKT
fase terbalik pernah dilakukan oleh Sadana dan Ghogare (1990). Kloramfenikol
dan lidokain hidroklorida dapat ditetapkan kadarnya dengan metode Kromatografi
Cair Kinerja Tinggi (KCKT) fase terbalik karena kloramfenikol dan lidokain
hidroklorida memiliki kepolaran yang berbeda, sehingga dapat dipisahkan karena
adanya perbedaan interaksi antara kloramfenikol dan lidokain hidroklorida
dengan fase diam yang bersifat non polar dan fase gerak yang bersifat polar.
Selain itu KCKT memiliki kelebihan yaitu cepat, sensitif, dan memiliki daya
pisah yang baik (Jhonson and Stevenson, 1978).
Penelitian ini merupakan tahap akhir dari rangkaian penelitian
“Penetapan Kadar Kloramfenikol dan Lidokain Hidroklorida dalam Sediaan Tetes
3
yang meliputi tahap optimasi, validasi, dan aplikasi. Dari hasil optimasi
didapatkan sistem KCKT yang optimum menggunakan fase gerak campuran
metanol:aquabides dengan komposisi 95:5 (v/v), fase diam oktadesilsilan (C18)
dengan kecepatan alir 1 mL/menit (Wibowo, 2011). Sistem ini juga memenuhi
syarat parameter validitas yang baik, meliputi selektivitas, linearitas, akurasi, dan
presisi (Wijayanti, 2011).
1. Permasalahan
a. Berapakah kadar kloramfenikol dan lidokain hidroklorida dalam sediaan obat
tetes telinga Colme®?
b. Apakah kadar kloramfenikol dan lidokain hidroklorida dalam sediaan obat
tetes telinga Colme® sesuai dengan yang tertera pada label kemasan?
2. Keaslian Penelitian
Penetapan kadar dari kloramfenikol dan benzokain secara simultan
dalam sediaan topikal dengan metode KCKT fase terbalik pernah dilakukan oleh
Sadana dan Ghogare (1990). Penetapan kadar kloramfenikol dalam sirup
kloramfenikol dengan menggunakan metode KCKT fase terbalik dengan
menggunakan kolom oktadesilsilan panjang 15 cm pernah dilakukan oleh
Bernadete Eko R. (2004). Penetapan kadar kloramfenikol dalam suspensi
kloramfenikol yang telah diisolasi menggunakan metode spektrofotometri
ultraviolet dilakukan oleh Fany Octavia (2005). Penerapan metode KCKT pada
penetapan kadar kloramfenikol dalam sediaan kapsul dengan nama dagang dan
generik dilakukan oleh Pasri (2010). Penetapan kadar lidokain HCl dalam sediaan
injeksi secara spektrofotometri serapan atom tidak langsung dilakukan oleh
Octaviana Manuhutu (2009). Penetapan kadar campuran hidrokortison asetat dan
kloramfenikol dalam sediaan krim topikal menggunakan metode KCKT fase
terbalik dilakukan oleh Octavianus Tri Harjanto (2009). Namun untuk penetapan
kadar kloramfenikol dan lidokain hidroklorida dalam sediaan tetes telinga Colme®
dengan metode KCKT fase terbalik belum pernah dilakukan.
3. Manfaat Penelitian
a. Manfaat Metodologis. Penelitian ini dapat menghasilkan prosedur
penggunaan metode KCKT fase terbalik untuk menetapkan kadar kloramfenikol
dan lidokain hidroklorida dalam sediaan tetes telinga Colme®.
b. Manfaat Praktis. Penelitian ini diharapkan dapat memberikan
informasi apakah kadar kloramfenikol dan lidokain hidroklorida dalam sediaan
tetes telinga Colme® sesuai dengan yang tertera pada label kemasan.
B. Tujuan Penelitian
1. Mengetahui kadar kloramfenikol dan lidokain hidroklorida yang terkandung
dalam sediaan obat tetes telinga Colme® menggunakan metode Kromatografi
Cair Kinerja Tinggi (KCKT) fase terbalik.
2. Mengetahui kesesuaian kadar kloramfenikol dan lidokain hidroklorida yang
ditetapkan kadarnya dengan jumlah yang tertera pada label kemasan sediaan
BAB II
PENELAAHAN PUSTAKA
A. Kloramfenikol
Kloramfenikol merupakan antibiotik dengan spektrum luas yang bersifat
bakteriostatik, mekanisme kerjanya menghambat sintesis protein bakteri dengan
cara berikatan pada ribosom 50s sehingga menghambat pembentukan rantai
peptida (Sukandar et al, 2008).
Kloramfenikol berbentuk serbuk hablur halus yang berbentuk jarum atau
lempeng memanjang, putih hingga putih kelabu atau putih kekuningan, dan stabil
dalam larutan netral atau larutan agak asam (Direktorat Jenderal Pengawasan
Obat dan Makanan RI, 1995). Kloramfenikol memiliki berat molekul 323
gram/mol; pKa 5,5; kelarutan dalam air 1:400; kelarutan dalam etanol 1:2,5;
λmaks kloramfenikol dalam air yaitu 278 nm ( 176) (Clarke, 1986).
Kloramfenikol termasuk senyawa antibiotik yang paling stabil. Larutan dalam air
pada pH 6 menunjukkan kecenderungan terurai yang paling rendah (Schunack et
al, 1990).
Gambar 1. Rumus struktur kloramfenikol (Hutt dan Graddy, 1996)
Tetes telinga kloramfenikol mengandung tidak kurang dari 90,0% dan
tidak lebih dari 130,0% kloramfenikol dari jumlah yang tertera pada etiket
(Direktorat Jenderal Pengawasan Obat dan Makanan RI, 1995).
B. Lidokain Hidroklorida
Lidokain hidroklorida adalah zat pemati rasa lokal yang pada kulit dan
selaput lendir mampu menghalangi rasa nyeri, perasaan terbakar atau gatal (Tan
dan Rahardja, 2010).
Lidokain hidroklorida berbentuk serbuk hablur putih, tidak berbau, rasa
sedikit pahit. Lidokain sangat mudah larut dalam air dan dalam etanol, larut dalam
kloroform dan tidak larut dalam eter (Direktorat Jenderal Pengawasan Obat dan
Makanan RI, 1995). Lidokain hidroklorida memiliki pKa 7,9. Lidokain
hidroklorida memiliki berat molekul sebesar 288,8 gram/mol. Lidokain dalam
etanol memiliki serapan maksimum pada daerah uv pada panjang gelombang 263
nm (E11cm% 13,5) (Clarke,1986).
Gambar 2. Rumus struktur lidokain hidroklorida (British Pharmacopeia Comission, 2009)
Larutan topikal lidokain hidroklorida mengandung lidokain hidroklorida
tidak kurang dari 95,0% dan tidak lebih dari 105,0% dari jumlah yang tertera pada
7
C. Obat Tetes Telinga
Obat tetes telinga adalah obat tetes yang digunakan dengan cara
meneteskan ke dalam telinga (Direktorat Jenderal Pengawasan Obat dan Makanan
RI, 1979). Tetesan adalah sediaan cair yang mengadung bahan obat atau sediaan
obat atau bahan obat dan sediaan obat terlarut, teremulsi atau tersuspensi, ditakar
berdasar jumlah tetesan. Untuk tetesan tertentu yang digunakan di telinga,
dinamakan tetes telinga (Otoguttae) (Voigt, 1995). Menurut Allen (2002) obat
tetes telinga yang berwujud cair dapat berupa bentuk larutan dan suspensi. Cairan
pembawa yang digunakan harus mempunyai kekentalan yang cocok agar obat
mudah menempel pada dinding telinga; umumnya digunakan gliserol dan
propilenglikol (Direktorat Jenderal Pegawasan Obat dan Makanan RI, 1979).
Pembawa yang kental memungkinkan kontak yang lebih lama antara obat dengan
jaringan telinga. Sifat higroskopis dari cairan pembawa juga memungkinkan
menarik kelembapan dari jaringan telinga sehingga mengurangi peradangan dan
membuang lembab yang tersedia untuk proses kehidupan mikroorganisme yang
ada (Ansel, 2008).
Berdasarkan Farmakope Indonesia edisi III, untuk sediaan tetes telinga
yang merupakan sediaan steril volume isi netto setiap wadah harus sedikit
berlebih dari volume yang ditetapkan. Kelebihan volume yang danjurkan tertera
dalam tabel berikut:
Tabel I. Persyaratan keseragaman volume
(Direktorat Jenderal Pengawasan Obat dan Makanan RI, 1979)
Volume pada etiket Volume tambahan yang dianjurkan
cairan encer cairan kental
0,5 ml 0,10 ml 0,12 ml
D. Obat Tetes Telinga Colme®
Gambar 3. Obat tetes telinga Colme® (Anonimb, 2011)
Obat tetes telinga Colme® diproduksi oleh PT. Interbat. Colme®
mengandung kloramfenikol 10%, lidokain HCl 4%, dan propilen glikol. Volume
8 mL untuk tiap kemasan. Obat tetes telinga Colme digunakan untuk indikasi
otitis eksterna, media akut dan kronis, neuro dermatitis, eksema pada meatus,
auditorius, nyeri telinga (Ikatan Sarjana Farmasi Indonesia, 2010). Kloramfenikol
merupakan antimikroba spektrum luas yang aktif terhadap bakteri gram-positif
dan bakteri gram-negatif, mekanisme kerjanya adalah menghambat sintesis
protein sel mikroba. Obat tetes telinga Colme® tidak dapat digunakan untuk
penderita yang hipersensitif terhadap kloramfenikol dan lidokain serta perforasi
9
terbakar, urtikaria, dermatitis vesikular, dan dermatitis makulopapular.
Penggunaan jangka panjang dapat menyebabkan pertumbuhan berlebihan dari
mikroorganisme yang tidak peka termasuk fungi, bila terjadi superinfeksi
pengobatan dihentikan. Aturan pakai untuk dewasa dan anak-anak yaitu 2-3 tetes,
2-3 kali sehari. Wadah disimpan dalam kondisi tertutup rapat, dihindari terjadinya
kontaminasi dan disimpan di bawah 25ºC terlindung dari cahaya matahari
(Anonimb, 2011).
E. Spektrofotometri Ultraviolet (UV)
Spektrofotometri ultraviolet adalah teknik analisis spektroskopik yang
memakai sumber radiasi elektromagnetik dekat (190-380 nm) dengan memakai
instrument spektrofotometer (Mulja dan Suharman, 1995). Spektrofotometer
menghasilkan sinar dari spektrum dengan panjang gelombang tertentu dan
fotometer adalah alat pengukur intensitas cahaya yang ditransmisikan atau
diabsorpsi (Khopkar, 1990). Prinsip kerja spektrofotometri berdasarkan atas
interaksi yang terjadi antara radiasi elektromagnetik dengan atom atau molekul.
Jika suatu molekul dikenai suatu radiasi elektromagnetik pada frekuensi yang
sesuai sehingga energi tersebut ditingkatkan ke level yang lebih tinggi, maka
terjadi peristiwa penyerapan (absorpsi) energi oleh molekul (Gandjar dan
Rohman, 2007).
Akibat adanya absorpsi radiasi elektromagnetik oleh molekul maka akan
terjadi eksitasi elektron ke tingkat energi yang lebih tinggi yang dikenal sebagai
elektron “anti bonding”. Terdapat empat jenis transisi elektronik yaitu σ→ σ*,
π→π*, n→σ*, dan n→π*. Eksitasi elektron σ→σ* memberikan energi terbesar
dan terjadi pada daerah ultraviolet jauh yang diberikan oleh ikatan tunggal,
sebagai contoh alkana. Eksitasi π→π* diberikan oleh ikatan rangkap dua dan tiga
(alkena dan alkana) juga terjadi pada daerah ultraviolet jauh. Eksitasi n→ σ*
terjadi pada gugus karbonil (dimetil keton dan asetaldehid) pada daerah ultraviolet
jauh (Mulja dan Suharman, 1995).
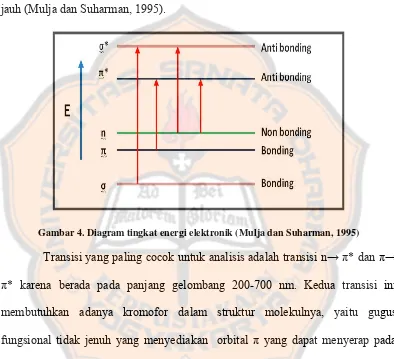
Gambar 4. Diagram tingkat energi elektronik (Mulja dan Suharman, 1995)
Transisi yang paling cocok untuk analisis adalah transisi n→π* dan π→
π* karena berada pada panjang gelombang 200-700 nm. Kedua transisi ini
membutuhkan adanya kromofor dalam struktur molekulnya, yaitu gugus
fungsional tidak jenuh yang menyediakan orbital π yang dapat menyerap pada
daerah ultraviolet (Skoog, 1985). Pada senyawa organik, selain kromofor dikenal
pula gugus auksokrom yaitu gugus fungsionil yang mempunyai elektron bebas
seperti -OH, -O, -NH2 dan -OCH3 yang memberikan transisi n→ σ*. Terikatnya
gugus auksokrom oleh gugus kromofor akan mengakibatkan pergeseran pita
absorpsi menuju ke panjang gelombang yang lebih panjang (batokromik) disertai
11
F. Kromatografi Cair Kinerja Tinggi
1. Definisi dan Instrumentasi
Kromatografi Cair Kinerja Tinggi (KCKT) merupakan salah satu metode
kromatografi cair yang fase geraknya dialirkan secara cepat dengan bantuan
tekanan, dan hasilnya dideteksi dengan instrumen (Willard et al, 1988). Pada
akhir tahun 1970, perkembangan instrument ini dapat menghasilkan pemisahan
yang baik atau menghasilkan penampilan peak yang baik sehingga sistem ini
lebih dikenal dengan KCKT (Kromidas, 2000). Pemisahan pada KCKT
merupakan hasil dari interaksi yang spesifik antara solut dengan fase diam dan
fase gerak (Dean, 1995). Instrumen KCKT dapat dilihat pada Gambar 5.
Gambar 5. Peralatan KCKT (Anonima, 2011)
2. Kromatografi Partisi Fase Terbalik
Konsep pengembangan kromatografi cair partisi yaitu perlakuan sampel
dalam kondisi cair-cair tergantung pada kelarutannya di dalam kedua cairan yang
terlibat. Jika solut ditambahkan ke dalam kondisi yang terdiri atas dua pelarut
yang tidak bercampur dan keseluruhan kondisi dibiarkan seimbang, solut akan
tersebar antara kedua fase itu menurut persamaan:
K =
K adalah koefisien distribusi, Cs adalah konsentrasi solute dalam fase diam dan
Cm adalah konsentrasi solut dalam fase gerak (Skoog et al, 1998).
Hal-hal yang harus diperhatikan dalam pemilihan metode kromatografi
partisi fase terbalik yaitu kolom, fase gerak, dan detektor.
a. Kolom. Kolom yang digunakan dalam pemilihan metode
kromatografi ini adalah kemasan fase terikat. Fase diam yang biasa digunakan
pada kromatografi partisi fase terbalik adalah oktadesilsilan (C18). Selain ODS,
dikenal pula silika dengan substitusi oktil (C8) (Munson, 1991). Oktadesilsilan
(C18) merupakan fase diam, yang paling banyak digunakan karena mampu
memisahkan senyawa-senyawa dengan kepolaran yang rendah, sedang, maupun
tinggi (Gandjar dan Rohman, 2007).
b. Fase gerak. Fase gerak pada KCKT sangat berpengaruh pada
tambatan sampel dan pemisahan komponen dalam campuran. Syarat fase gerak
yaitu murni, tidak bereaksi dengan kemasan,sesuai dengan detektor, dan dapat
melarutkan cuplikan (Johnson dan Stevenson, 1978). Pada fase terbalik
kandungan utama fase geraknya adalah air. Pelarut yang dapat campur dengan air
seperti metanol, etanol, asetonitril, dan tetrahidrofuran ditambahkan untuk
mengatur kepolaran fase gerak. Kepolaran dinyatakan dalam indeks polaritas (P’)
yang dapat dihitung dengan persamaan berikut:
13
Φa dan Φb adalah fraksi pelarut a dan b dalam campuran, sedangkan P’a
dan P’b adalah angka P’ pelarut murni (Gritter et al., 1991). Berikut adalah nilai
indeks polaritas (P’) dari beberapa pelarut pada KCKT fase terbalik:
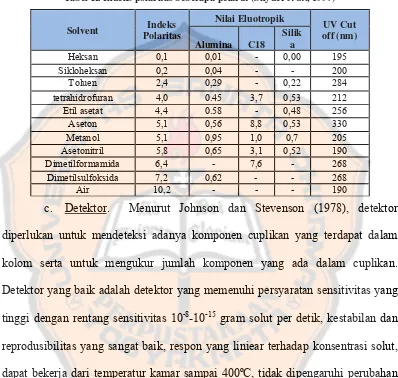
Tabel II. Indeks polaritas beberapa pelarut (Snyder et al., 1997)
Solvent Indeks
Polaritas
c. Detektor. Menurut Johnson dan Stevenson (1978), detektor
diperlukan untuk mendeteksi adanya komponen cuplikan yang terdapat dalam
kolom serta untuk mengukur jumlah komponen yang ada dalam cuplikan.
Detektor yang baik adalah detektor yang memenuhi persyaratan sensitivitas yang
tinggi dengan rentang sensitivitas 10-8-10-15 gram solut per detik, kestabilan dan
reprodusibilitas yang sangat baik, respon yang liniear terhadap konsentrasi solut,
dapat bekerja dari temperatur kamar sampai 400ºC, tidak dipengaruhi perubahan
temperatur dan kecepatan pelarut pengembang, mudah didapat, mudah dipakai
operator, selektif terhadap macam-macam linarut dalam pelarut pengembang dan
tidak merusak sampel (Mulja dan Suharman, 1995).
Secara umum detektor dibagi menjadi dua kategori, yaitu:
1) Bulk property detectors.
Jenis detektor ini mengukur perubahan sifat fisik gerak dan solut. Tipe ini
cenderung relatif tidak sensitive dan menghendaki suhu yang terkendali.
Contoh detektor jenis ini yaitu detektor indeks bias.
2) Solut property detectors.
Detektor tipe ini 100 kali lebih sensitive dan mampu mengukur solut sampai
satuan nanogram atau lebih kecil lagi. Contoh detektor jenis ini yaitu detektor
flurosensi, detektor penyerapan (UV-Vis), dan detektor elektrokimia (Munson,
1991).
3. Analisis kualitatif dan kuantitatif
KCKT dapat digunakan untuk analisis kualitatif dan kuantitatif dari suatu
sampel atau cuplikan. Hasil dari pemisahan adalah kromatogram yang
memberikan informasi mengenai waktu retensi suatu senyawa (Noegrohati,
1994).
Waktu retensi adalah selang waktu yang diperlukan oleh solut mulai saat
injeksi sampai keluar dari kolom dan sinyalnya ditangkap oleh detektor dan
dinyatakan sebagai tR (Mulja dan Suharman, 1995). Masing-masing senyawa
memiliki waktu retensi yang spesifik pada kondisi kolom, suhu, dan laju tertentu,
sehingga dapat digunakan sebagai salah satu dasar uji kualitatif. Analisis
kuantitatif dilakukan berdasarkan perbandingan tinggi atau luas puncak
15
G. Landasan Teori
Kloramfenikol dan lidokain hidroklorida merupakan kombinasi zat aktif
yang terdapat dalam sediaan obat tetes telinga. Sediaan obat tetes telinga yang
mengandung kedua zat aktif tersebut adalah Colme®. Kombinasi zat aktif
ditujukan untuk meningkatkan efek terapi bagi pasien sebagai pengguna obat.
Berdasarkan Farmakope Indonesia IV sediaan obat tetes telinga mengandung
tidak kurang dari 90% dan tidak lebih dari 130% kloramfenikol dan untuk
lidokain hidroklorida tidak kurang dari 95% dan tidak lebih dari 105% dari
jumlah yang tertera pada etiket.
Kloramfenikol dan lidokain hidroklorida memiliki panjang gelombang
pada daerah spektrofotometri UV dan sama-sama larut dalam etanol. Adanya
kromofor dan auksokrom serta gugus polar dan gugus non polar yang terdapat
pada kloramfenikol dan lidokain hidroklorida memungkinkan untuk melakukan
analisis kuantitatif dengan metode KCKT fase terbalik menggunakan detektor
UV.
Kelebihan dari metode KCKT yaitu memiliki sensitifitas dan selektifitas
yang tinggi dalam memisahkan campuran yang memiliki kepolaran yang sama.
Oleh karena itu, metode KCKT mempunyai daya pisah yang tinggi yang bisa
memisahkan kloramfenikol dan lidokain hidroklorida dari komponen lain yang
terkandung dalam sampel sediaan obat tetes telinga Colme®. Kloramfenikol dan
lidokain hidroklorida dapat dianalisis secara kualitatif dan dapat dilakukan
penetapan kadar kloramfenikol dan lidokain hidroklorida secara kuantitatif
dengan metode KCKT fase terbalik.
H. Hipotesis
Berdasarkan landasan teori di atas, dapat disusun hipotesis sebagai
berikut:
1. Kadar kloramfenikol dan lidokain hidroklorida yang diperoleh dari hasil
penetapan kadar dengan metode KCKT fase terbalik yaitu 10% untuk kadar
kloramfenikol dan 4% untuk kadar lidokain hidroklorida
2. Kadar kloramfenikol dan lidokain hidroklorida dalam sediaan tetes telinga
BAB III
METODE PENELITIAN
A. Jenis dan Rancangan Penelitian
Penelitian yang dilakukan merupakan jenis penelitian non eksperimental
dengan rancangan penelitian deskriptif, sebab pada penelitian ini tidak dilakukan
manipulasi pada subjek uji dan hanya mendeskripsikan keadaan yang ada.
B. Variabel Penelitian
1. Variabel bebas
Variabel bebas dalam penelitian ini adalah sediaan tetes telinga Colme® yang
mengandung kloramfenikol dan lidokain hidroklorida.
2. Variabel tergantung
Variabel tergantung dalam penelitian ini adalah kadar kloramfenikol dan
lidokain hidroklorida dalam sediaan tetes telinga.
3. Variabel pengacau terkendali
Variabel pengacau terkendali dalam penelitian ini adalah kemurnian pelarut
yang digunakan. Untuk mengatasinya digunakan pelarut yang memiliki
kemurnian tinggi yaitu pelarut pro analysis.
C. Definisi Operasional
1. Obat tetes telinga Colme® merupakan sediaan tetes telinga yang
mencantumkan kandungan kloramfenikol 10 % dan lidokain hidroklorida 4 %
pada labelnya dan memiliki nomor batch yang sama.
2. Lidokain hidroklorida yang digunakan adalah lidokain hidroklorida
monohidrat.
3. Sistem Kromatografi Cair Kinerja Tinggi (KCKT) fase terbalik yang
digunakan adalah fase diam kolom oktadesilsilan (C18), fase gerak
metanol:aquabides dengan perbandingan komposisi 95:5 (v/v), kecepatan alir
1,0 mL/menit, dan panjang gelombang pada detektor UV yaitu 242 nm.
4. Kadar kloramfenikol dan lidokain hidroklorida dalam sediaan obat tetes
telinga Colme® ditetapkan dalam % (b/v).
D. Bahan Penelitian
Bahan yang digunakan adalah baku kloramfenikol dan lidokain
hidroklorida kualitas working standar dengan Certificate of Analysis (CoA) dari
PT. Interbat, metanol (p.a., E. Merck), aquabidestilata (Pharmaceutical
laboratories, PT. Ikapharmindo Putramas), sediaan tetes telinga Colme® yang
diperoleh dari PT. Interbat dengan nomor batch D016102, dengan volume netto 8
19
E. Alat Penelitian
Alat yang digunakan adalah anorganic dan organic solvent membran
filter (Whatman) ukuran pori 0,45µm; diameter 47 mm, penyaring millipore,
indikator pH, mikropipet Socorex, neraca analitik (Ohaus PAJ1003),
ultrasonicator (Retsch tipe T460 no V935922013 Ey), pompa vakum (Gaast
model DOA-P104-BN), spektrofotometer UV/Vis (Optima SP 3000), sistem
KCKT (gradien, model LC-2010C HT, CAT No.228-46703-38, SERIAL No.
C21254706757 LP, Shimadzu Corporation), kolom oktadesilsilan (C18) berukuran
250 x 4,6 mm merk KNAUER No. 25EE181KSJ (B115Y620), seperangkat
computer (merk Dell B6RDZ1S Connexant System RD01-D850 A03-0382 JP
France S.A.S, printer HP Deskjet D2566 HP-024-000 625 730), dan alat-alat
gelas yang umum digunakan dalam analisis (Pyrex).
F. Tata Cara Penelitian
1. Pemilihan sampel
Sampel yang dipilih adalah sediaan tetes telinga Colme® yang
mencantumkan kloramfenikol dan lidokain hidroklorida pada kemasannya.
Sampel yang digunakan sebanyak 20 kemasan dengan nomor batch yang sama
dan dilakukan 10 kali replikasi.
2. Pembuatan fase gerak
Fase gerak yang digunakan dalam penelitian ini terdiri atas campuran
metanol:aquabidest dengan perbandingan 95:5 (v/v). Masing-masing komponen
fase gerak disaring menggunakan organic solvent membrane filter (Whatman)
untuk metanol, dan anorganic solvent membrane filter (Whatman) untuk
aquabides dengan bantuan pompa vakum. Fase gerak tersebut lalu diawaudarakan
selama 15 menit menggunakan ultrasonicator. Pencampuran kedua komponen
fase gerak dilakukan secara gradien di dalam instrument KCKT.
3. Pembuatan larutan baku kloramfenikol
a. Larutan stok kloramfenikol. Lebih kurang 10 mg baku kloramfenikol
ditimbang seksama, kemudian dilarutkan dengan metanol dalam labu takar 10,0
mL hingga tanda sehingga diperoleh konsentrasi 1000 ppm.
b. Larutan intermediet kloramfenikol. Larutan stok kloramfenikol dipipet
sebanyak 5 mL dan diencerkan dengan metanol dalam labu takar 10,0 mL hingga
tanda sehingga diperoleh konsentrasi 500 ppm. Larutan disaring dengan millipore
dan diawaudarakan selama 15 menit dengan ultrasonicator.
4. Pembuatan larutan baku lidokain hidroklorida
a.Larutan stok lidokain hidroklorida. Lebih kurang 10 mg lidokain
hidroklorida baku ditimbang seksama, kemudian dilarutkan dengan metanol
dalam labu takar 10,0 mL hingga tanda sehingga diperoleh konsentrasi 1000 ppm.
b.Larutan intermediet lidokain hidroklorida. Larutan stok lidokain
hidroklorida dipipet sebanyak 5 mL dan diencerkan dengan metanol dalam labu
takar 10,0 mL hingga tanda sehingga diperoleh konsentrasi 500 ppm. Larutan
disaring dengan millipore dan diawaudarakan selama 15 menit dengan
21
5. Penetapan panjang gelombang pengamatan kloramfenikol dan lidokain
hidroklorida dengan spektrofotometer UV.
Larutan stok kloramfenikol diambil sebanyak 0,130; 0,195; dan 0,260 ml
dan diencerkan dengan metanol dalam labu takar 10,0 mL hingga tanda sehingga
diperoleh konsentrasi sebesar 13; 19,5; dan 26 ppm. Larutan stok lidokain
hidroklorida diambil sebanyak 3; 4,5; dan 6 mL dan diencerkan dengan metanol
dalam labu takar 10,0 mL hingga tanda sehingga diperoleh konsentrasi sebesar
300; 450; dan 600 ppm. Masing-masing kadar kloramfenikol dan lidokain
hidroklorida tersebut dilakukan pengukuran absorbansi pada rentang panjang
gelombang 200-400 nm, sehingga dapat diketahui absorbansi masing-masing
senyawa. Dari spektra kloramfenikol dan lidokain hidroklorida yang dihasilkan
selanjutnya spektra tersebut ditumpangtindihkan untuk mengetahui panjang
gelombang pengamatan yang akan digunakan pada detektor dengan sistem KCKT
fase terbalik.
6. Pembuatan kurva baku kloramfenikol dan lidokain hidroklorida.
a.Pembuatan kurva baku kloramfenikol. Larutan intermediet
kloramfenikol 500 ppm yang telah disaring dengan millipore dan diawaudarakan
dengan ultrasonicator selama 15 menit diinjeksikan ke dalam sistem KCKT fase
terbalik dengan volume injeksi 12, 14, 16, 18, dan 20 µL. Replikasi dilakukan
sebanyak tiga kali.
b.Pembuatan kurva baku lidokain hidroklorida. Larutan intermediet
lidokain hidroklorida 500 ppm yang telah disaring dengan millipore dan
diawaudarakan dengan ultrasonicator diinjeksikan ke dalam sistem KCKT fase
terbalik dengan volume injeksi 12, 14, 16, 18, dan 20 µL. Replikasi dilakukan
sebanyak tiga kali.
7. Preparasi sampel
Sampel diambil 20 kemasan dari batch yang sama dan dicampur hingga
homogen. Sediaan tetes telinga Colme® diaduk selama 1 menit. Larutan sampel
kemudian dipipet seksama sebanyak 1,0 mL dan diencerkan dengan metanol
dalam labu takar 10,0 mL sehingga diperoleh konsentrasi 10000 ppm untuk
kloramfenikol dan 4000 ppm untuk lidokain hidroklorida. Larutan sampel diambil
sebanyak 0,5 ml kemudian 300 ppm larutan lidokain hidroklorida diadisi dengan
cara mengambil 3 mL larutan stok lidokain hidroklorida baku ke dalam labu takar
10,0 mL dan diencerkan dengan metanol hingga tanda. Larutan disaring dengan
millipore dan diawaudarakan selama 15 menit. Replikasi dilakukan 10 kali.
8. Penetapan kadar campuran kloramfenikol dan lidokain hidroklorida
Larutan sampel adisi dan larutan lidokain hidroklorida 300 ppm
diinjeksikan ke dalam sistem KCKT dengan fase diam oktadesilsilan (C18), fase
gerak metanol:air dengan komposisi 95:5 (v/v) serta kecepatan alir 1,0 mL/menit.
Volume injeksi 20 µL dan detektor diatur pada panjang gelombang pengamatan
hasil optimasi yaitu 242 nm. Amati kromatogram yang dihasilkan. Nilai AUC
sampel dimasukkan ke dalam persamaan kurva baku kloramfenikol dan lidokain
hidroklorida, maka akan didapatkan kadar kloramfenikol dan lidokain
hidroklorida dalam sampel. Data disajikan dengan satuan % (b/v). Replikasi
23
G. Analisis Hasil
Analisis kualitatif dilakukan dengan membandingkan waktu retensi (tR)
senyawa sampel dengan senyawa baku. Analisis kuantitatif yang dilakukan adalah
penetapan kadar kloramfenikol dan lidokain hidroklorida berdasarkan data AUC
sampel serta kurva baku masing-masing senyawa. Kadar kloramfenikol dan
lidokain hidroklorida dalam tetes telinga dinyatakan dalam (x+SD)% (b/v). Kadar yang diperoleh kemudian dibandingkan secara deskriptif dengan kadar yang
tertera pada label kemasan.
BAB IV
HASIL DAN PEMBAHASAN
A. Pemilihan Sampel
Kloramfenikol dan lidokain hidroklorida merupakan kombinasi zat aktif
yang terdapat dalam sediaan obat tetes telinga. Berdasarkan Informasi Spesialite
Obat Volume 45 2010-2011 sediaan tetes telinga yang mengandung kombinasi zat
aktif kloramfenikol dan lidokain hidroklorida yaitu tetes telinga Colme® (Ikatan
Sarjana Farmasi Indonesia, 2010). Sampel Colme® yang ditetapkan kadarnya
dengan metode KCKT fase terbalik tersebut diperoleh dari PT. Interbat.
Sampel yang diperoleh terdiri dari 20 botol kemasan dengan nomor
batch yang sama. Tujuan pengambilan sampel dari nomor batch yang sama yaitu
untuk mendapatkan kriteria homogenitas karena diasumsikan bahwa sampel
dengan nomor batch sama mengalami satu proses produksi yang sama. Selain itu,
sampel yang digunakan dalam analisis adalah tetes telinga yang berbentuk sediaan
larutan kental, molekul-molekul obat di dalam larutan terdispersi secara merata
sehingga memiliki homogenitas yang tinggi dan dapat memberikan jaminan
keseragaman dosis. Kriteria lainnya yang harus dipenuhi yaitu representatif, yakni
sampel yang dianalisis benar-benar mencerminkan populasi yang diwakilinya,
dengan 20 kemasan dan dilakukan replikasi 10 kali diharapkan telah memenuhi
persyaratan tersebut. Kriteria representatif pengambilan sampel dikendalikan
dengan pengadukan sampel hingga homogen dan pemipetan sampel dari berbagai
25
Tabel III. Keseragaman volume obat tetes telinga Colme®
No. Volume terukur (mL)
Volume pada label (mL)
Pada etiket obat tetes telinga Colme® tertera kandungan kloramfenikol
10% dan lidokain hidroklorida 4% dalam volume 8 mL. Keseragaman volume
dilakukan pada 20 kemasan obat tetes telinga Colme® sebagai tahap awal
identifikasi untuk mengetahui keseragaman kandungan dari obat tetes telinga
Colme®. Berdasarkan Farmakope Indonesia edisi III batas volume untuk sediaan
larutan kental adalah tidak lebih dari 0,80 mL dari volume larutan obat. Dari uji
keseragaman volume hasil yang diperoleh tidak ada satu botol kemasan yang
menyimpang dari persyaratan keseragaman volume. Hal ini menunjukkan dari 20
botol kemasan Colme® memiliki keseragaman volume yang baik.
B. Pembuatan Fase Gerak
Metode KCKT yang digunakan pada penelitian ini merupakan sistem
kromatografi fase terbalik, karena menggunakan fase gerak yang bersifat polar
dan fase diam oktadesilsilan (C18) yang bersifat non polar. Jenis dan komposisi
fase gerak yang digunakan pada penelitian yaitu campuran metanol dan aquabides
dengan perbandingan 95:5 (v/v).
Campuran fase gerak ini digunakan karena kloramfenikol dan lidokain
hidroklorida larut dalam metanol dan aquabides. Menurut Farmakope Indonesia
edisi IV (1995), kloramfenikol larut dalam lebih kurang 400 bagian air dan 2,5
bagian etanol, sedangkan lidokain hidroklorida sangat mudah larut dalam air dan
etanol. Karena kedua senyawa tersebut larut dalam pelarut alkohol, maka pada
penelitian ini digunakan metanol.
Sistem KCKT pada penelitian ini menggunakan metanol sebagai pelarut
maupun sebagai fase gerak dikarenakan viskositas metanol lebih kecil dibanding
viskositas etanol. Viskositas yang terlalu besar dapat meningkatkan tekanan
pompa pada KCKT dan mempengaruhi keawetan kolom yang digunakan. Selain
itu, juga digunakan aquabides untuk mendapatkan indeks polaritas yang sesuai,
sehingga dihasilkan profil kromatogram yang diinginkan dan memenuhi syarat
yang ditetapkan. Pencampuran masing-masing komponen fase gerak dilakukan di
dalam instrumen KCKT (sistem gradien). Pencampuran fase gerak menggunakan
sistem gradien karena dapat meningkatkan efisiensi waktu dalam proses analisis
dan didukung oleh kemampuan istrumen KCKT yang memadai. Pemilihan
27
pernah memisahkan kloramfenikol dan benzokain dengan fase gerak berupa
campuran metanol dan aquabides.
C. Pembuatan Larutan Baku Kloramfenikol dan Lidokain Hidroklorida
Larutan baku kloramfenikol dan lidokain hidroklorida dibuat dalam
konsentrasi tertentu dengan menggunakan pelarut metanol. Metanol digunakan
sebagai pelarut karena kedua senyawa tersebut larut dalam pelarut alkohol. Selain
itu digunakan metanol sebagai pelarut dikarenakan metanol merupakan komponen
terbesar fase gerak sehingga mudah terelusi dengan fase gerak. Pemilihan pelarut
sangat penting karena bertujuan untuk melarutkan analit yang akan dianalisis.
Syarat utama dari pelarut yang digunakan yaitu dapat melarutkan analit. Selain itu
pelarut harus murni, inert, dan dapat bercampur dengan fase gerak (Johnson dan
Stevenson, 1978).
Larutan baku kloramfenikol dan lidokain hidroklorida masing-masing
dibuat dengan pelarut metanol p.a. Larutan baku yang dibuat dalam penelitian ini
terdiri dari dua macam, yaitu larutan stok dan larutan intermediet. Larutan stok
kloramfenikol dan lidokain hidroklorida dibuat dengan konsentrasi
masing-masing sebesar 1000 ppm, sedangkan larutan intermediet dibuat dengan
konsentrasi masing-masing 500 ppm. Larutan seri baku kemudian dibuat dalam
lima volume injeksi yang berbeda, yaitu 12 µL, 14 µL, 16 µL, 18 µL, dan 20 µL
dengan mengambil dari larutan intermediet kloramfenikol 500 ppm dan larutan
intermediet lidokain hidroklorida 500 ppm. Sebelum dianalisis, larutan baku
disaring dengan millipore untuk menjamin bahwa tidak ada senyawa lain yang
dapat mengganggu pengukuran. Kemudian larutan baku diawaudarakan dengan
ultrasonicator untuk menghilangkan gelembung, karena adanya gelembung udara
dapat mengganggu tekanan pompa instrumen KCKT, akibatnya tekanan pompa
menjadi tidak stabil dan dapat mengganggu proses pembacaan sinyal dalam
instrumen KCKT. Hal yang sama juga dilakukan pada proses preparasi sampel.
D. Penentuan Panjang Gelombang Pengamatan Kloramfenikol dan
Lidokain Hidroklorida dengan Spektrofotometer UV
Penentuan panjang gelombang pengamatan bertujuan untuk mengetahui
panjang gelombang dimana kloramfenikol dan lidokain hidroklorida memiliki
serapan yang optimum secara bersamaan pada sistem KCKT. Detektor yang
digunakan pada sistem KCKT adalah spektrofotmeter UV.
Secara teoritis, panjang gelombang serapan maksimum kloramfenikol
dalam air adalah 278 nm dan panjang gelombang serapan maksimum lidokain
hidroklorida dalam etanol adalah 263 nm (Clarke, 1986). Oleh karena itu,
dilakukan pengamatan panjang gelombang pengamatan kloramfenikol dan
lidokain hidroklorida pada rentang panjang gelombang 200-400 nm menggunakan
spektrofotometer UV. Syarat suatu senyawa dapat dianalisis dengan
spektrofotometri UV yaitu memiliki gugus kromofor. Gugus kromofor merupakan
gugus atau atom yang mampu meyerap sinar ultraviolet. Gambar gugus kromofor
29
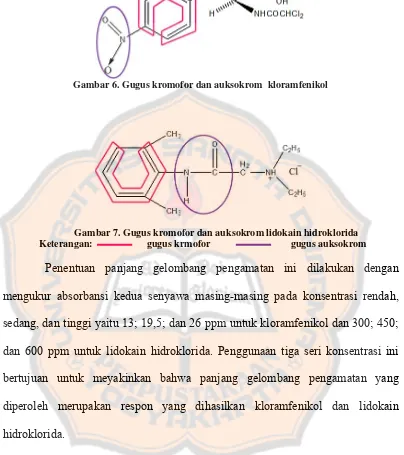
Gambar 6. Gugus kromofor dan auksokrom kloramfenikol
Gambar 7. Gugus kromofor dan auksokrom lidokain hidroklorida
Keterangan: gugus krmofor gugus auksokrom
Penentuan panjang gelombang pengamatan ini dilakukan dengan
mengukur absorbansi kedua senyawa masing-masing pada konsentrasi rendah,
sedang, dan tinggi yaitu 13; 19,5; dan 26 ppm untuk kloramfenikol dan 300; 450;
dan 600 ppm untuk lidokain hidroklorida. Penggunaan tiga seri konsentrasi ini
bertujuan untuk meyakinkan bahwa panjang gelombang pengamatan yang
diperoleh merupakan respon yang dihasilkan kloramfenikol dan lidokain
hidroklorida.
Hasil spektra serapan tumpang tindih kloramfenikol dan lidokain
hidroklorida dapat dilihat pada gambar berikut:
B
A
Gambar 8. Spektra tumpang tindih kloramfenikol 13 ppm (A) dan lidokain hidroklorida 300 ppm (B)
B
A
31
B
A
Gambar 10. Spektra tumpang tindih kloramfenikol 26 ppm(A) dan lidokain hidroklorida 600 ppm (B)
Dari hasil spektra menunjukkan bahwa panjang gelombang maksimum
kloramfenikol adalah 270 nm dan lidokain hidroklorida adalah 265 nm. Menurut
Clarke (1986) serapan maksimal untuk lidokain hidroklorida dalam etanol adalah
263 nm. Pergeseran panjang gelombang yang diijinkan adalah ±2 nm (Direktorat
Jenderal Pengawasan Obat dan Makanan RI, 1995). Oleh karena itu panjang
gelombang lidokain hidroklorida ini dapat diterima karena bergeser 1 nm dari
panjang gelombang teoritis. Berdasarkan Clarke (1986) serapan maksimal untuk
kloramfenikol dalam air adalah 278 nm, panjang gelombang ini bergeser lebih
dari 2 nm dari panjang gelombang teoritis. Hal ini dikarenakan penggunaan
pelarut yang digunakan berbeda dengan pelarut pada teori. Pada ketiga gambar
spektra di atas menunjukkan serapan antara kloramfenikol dan lidokain
hidroklorida saling tumpang tindih pada panjang gelombang 200 nm sampai 250
nm dan berpotongan pada panjang gelombang 242 nm. Berdasarkan spektra
tumpang tindih tersebut, maka panjang gelombang yang digunakan pada analisis
dengan sistem KCKT adalah 242 nm karena pada panjang gelombang ini
absorbansi kloramfenikol tidak terlalu besar dan absorbansi lidokain hidroklorida
juga tidak terlalu kecil, sehingga diharapkan pada analisis dengan sistem KCKT
didapatkan respon kloramfenikol dan lidokain hidroklorida yang tidak terlalu
berbeda jauh.
E. Analisis Kualitatif Berdasarkan Waktu Retensi (tR) Kloramfenikol dan
Lidokain Hidroklorida
Analisis kualitatif dilakukan dengan membandingkan waktu retensi
sampel (tR) dengan waktu retensi (tR) baku pembanding. Analisis kualitatif ini
dilakukan untuk membuktikan bahwa di dalam sampel Colme® yang diuji
terdapat kloramfenikol dan lidokain hidroklorida. Hal tersebut ditunjukkan
dengan adanya kemiripan waktu retensi sampel (tR) dengan waktu retensi (tR)
baku pembanding. Hasil kromatogram yang diperoleh sebagai berikut:
33
Gambar 12. Kromatogram baku lidokain hidroklorida (500 ppm)
Gambar 13. Kromatogram sampel
(kloramfenikol:lidokain hidroklorida = 500:200 ppm)
Gambar 14. Kromatogram sampel adisi baku lidokain hidroklorida (300 ppm) (kloramfenikol:lidokain hidroklorida = 500:500 ppm)
Dari kromatogram yang dihasilkan, antara baku kloramfenikol dan
lidokain hidroklorida memiliki waktu retensi yang tidak jauh berbeda dengan
sampel. Waktu retensi baku kloramfenikol adalah 2,576 menit dan waktu retensi
baku lidokain hidroklorida adalah 3,134 menit. Waktu retensi kedua senyawa
pada sampel adalah 2,493 menit untuk kloramfenikol dan lidokain hidroklorida
memiliki waktu retensi 3,338 menit. Namun pada kromatogram sampel (gambar
13) terlihat respon lidokain hidroklorida sangat rendah dan tidak berbentuk peak
kromatogram, sehingga dilakukan standard addition method yaitu dengan
penambahan sejumlah tertentu baku lidokain hidroklorida (300 ppm) ke dalam
sampel. Sesuai dengan rangkaian penelitian mengenai validasi metode KCKT
untuk penetapan kadar kloramfenikol dan lidokain hidroklorida dalam Colme®
perlu dilakukan standard addition method. Standard addition method dilakukan
bertujuan untuk meningkatkan respon lidokain hidroklorida dalam sistem KCKT
dan untuk mengetahui apakah pada waktu retensi lidokain hidroklorida pada
sampel benar merupakan peak dari lidokain hidroklorida. Pada kromatogram
sampel adisi (gambar 14) waktu retensi kloramfenikol adalah 2,577 menit dan
waktu retensi dari lidokain hidroklorida adalah 3,380 menit. Waktu retensi dari
kedua senyawa pada sampel identik dengan waktu retensi baku kloramfenikol
(gambar 11) dan waktu retensi lidokain hidroklorida (gambar 12) dan waktu
retensi kloramfenikol dan lidokain hidroklorida pada sampel adisi (gambar 14),
sehingga dapat dipastikan bahwa pada sampel terdapat kloramfenikol dan
lidokain hidroklorida.
Waktu retensi kloramfenikol dan lidokain hidroklorida dipengaruhi oleh
adanya perbedaan interaksi antara kedua senyawa dengan fase diam dan fase
35
sistem KCKT fase terbalik dimana fase gerak yang digunakan bersifat lebih polar
dibanding dengan fase diamnya. Fase gerak yang digunakan yaitu campuran
metanol dan aquabides dengan komposisi 95:5 (v/v). Sehingga senyawa yang
bersifat lebih polar akan terikut dalam fase gerak sehingga terelusi lebih cepat,
sedangkan senyawa yang bersifat lebih non polar akan tertambat lebih lama di
fase diam dan memiliki waktu retensi yang lebih lama daripada senyawa yang
bersifat lebih polar.
Gambar 15. Bagian polar dan non polar kloramfenikol
Gambar 16. Bagian polar dan non polar lidokain hidroklorida Keterangan: = gugus polar, = gugus non polar
Jika dilihat dari strukturnya, kloramfenikol dan lidokain hidroklorida
memiliki gugus non polar dan polar yang akan berinteraksi dengan fase diam dan
fase gerak. Gugus non polar akan berinteraksi dengan fase diam melalui interaksi
Van Der Waals, sedangkan gugus polar akan berinteraksi dengan fase gerak
melalui interaksi hidrogen. Berikut ini adalah gambar interaksi kloramfenikol dan
lidokain hidroklorida dengan fase diam oktadesilsilan dan fase gerak
Gambar 17. Interaksi kloramfenikol dengan fase diam C18(oktadesilsilan) melalui interaksi Van Der Waals
H3C Oktadesilsilan (C18)
Cl
Keterangan: Interaksi Van Der Waals Interaksi ion-dipol
Gambar 18. Interaksi lidokain hidroklorida dengan fase diam C18(Oktadesilsilan) melalui interaksi Van Der Waals dan interaksi ion-dipol
Pada gambar 17 dan 18 menunjukkan interaksi antara gugus non polar
dari kloramfenikol dan lidokain hidroklorida dengan fase diam oktadesilsilan
(C18). Dari gambar di atas terlihat lidokain hidroklorida lebih banyak memiliki
gugus non polar yang berinteraksi dengan fase diam oktadesisilan daripada
kloramfenikol. Pada kloramfenikol interaksi yang terjadi adalah interaksi Van Der
37
ion-dipol. Kedua interaksi ini menyebabkan lidokain hiroklorida tertahan lebih
lama di dalam kolom sehingga waktu retensi lidokain hidroklorida lebih lama
dibanding waktu retensi kloramfenikol.
Gambar 19. Interaksi kloramfenikol dengan fase gerak metanol:aquabides (95:5)
Gambar 20. Interaksi lidokain dengan fase gerak metanol:aquabides (95:5)
Dari gambar di atas dapat dilihat bahwa gugus polar kloramfenikol
(Gambar 19) memiliki kemungkinan interaksi hidrogen yang lebih banyak
daripada lidokain hidroklorida sehingga kloramfenikol memiliki waktu retensi
yang lebih singkat dibanding lidokain hidroklorida, karena semakin banyak
jumlah ikatan hidrogen maka ikatan antara solut dengan fase gerak akan semakin
kuat sehingga solut akan terelusi terlebih dahulu.
F. Pembuatan Kurva Baku Kloramfenikol dan Lidokain Hidroklorida
Pembuatan kurva baku bertujuan untuk memperoleh persamaan regresi
linear yang selanjutnya akan digunakan untuk menghitung kadar kloramfenikol
dan lidokain hidroklorida dalam sampel Colme®. Persamaan regresi linier yang
diperoleh menyatakan hubungan linier antara konsentrasi (jumlah) analit dengan
respon Area Under Curve (AUC). Parameter yang dilihat untuk menentukan
linearitas adalah keofisien korelasi (r). Koefisien korelasi menyatakan korelasi
antara jumlah analit dengan AUC yang dihasilkan. Pemilihan kurva baku yang
nantinya akan digunakan untuk perhitungan kadar dari kloramfenikol dan lidokain
hidroklorida didasarkan pada nilai koefisien korelasi (r) > 0,999 (Mulja dan
Hanwar, 2003). Persamaan kurva baku yang diperoleh yaitu:
Tabel IV. Data kurva baku kloramfenikol
Replikasi I Replikasi II Replikasi III
Jumlah (µg) AUC Jumlah (µg) AUC Jumlah (µg) AUC
6 4447920 5,9 4114603 6,06 3996431
7 5225652 6,9 4852908 7,07 4593295
8 5957832 7,9 5527894 8,08 5234015
9 6692209 8,9 6235642 9,09 5881656
39
Tabel V. Data kurva baku lidokain hidroklorida
Replikasi I Replikasi II Replikasi III
Jumlah (µg) AUC Jumlah (µg) AUC Jumlah (µg) AUC
5,9 1732820 6,01 1777099 5,89 2021719
6,9 2026936 7,01 2072133 6,87 2345544
7,9 2315898 8,02 2365937 7,86 2640648
8,9 2606270 9,02 2654677 8,84 3000499
9,9 2895505 10,02 2908162 9,82 3268629
A: 20769,64
Persamaan kurva baku kloramfenikol dan lidokain hidroklorida memiliki
nilai α = 89,990. Oleh karena itu, perlu dilakukan modifikasi kurva baku agar
menghasilkan nilai α yang mendekati 450 dan penampilan kurva yang dihasilkan
baik, sehingga dapat dilihat hubungan liniear antara jumlah analit dengan AUC.
Modifikasi dilakukan dengan AUC kloramfenikol dibagi 800000 dan lidokain
hidroklorida dibagi 300000. Hasil modifikasi dapat dilihat pada tabel VI dan VII.
Tabel VI. Data kurva baku kloramfenikol modifikasi
Replikasi I Replikasi II Replikasi III
Jumlah (µg) AUC Jumlah (µg) AUC Jumlah (µg) AUC
Tabel VII. Data kurva baku lidokain hidroklorida modifikasi
Replikasi I Replikasi II Replikasi III
Jumlah (µg) AUC Jumlah (µg) AUC Jumlah (µg) AUC
5,9 5,77607 6,01 5,92366 5,89 6,73906
6,9 6,75645 7,01 6,90711 6,87 7,81848
7,9 7,71966 8,02 7,88646 7,86 8,80216
8,9 8,68757 9,02 8,48892 8,84 10,00166
9,9 9,65168 10,02 9,69387 9,82 10,89543
A: 0,0692
Dari semua tabel di atas terlihat secara garis besar hampir semua kurva
baku yang dihasilkan memiliki nilai r > 0,999. Persamaan kurva baku yang
memiliki nilai koefisien korelasi terbesar digunakan untuk menetapkan kadar
kloramfenikol dan lidokain hidroklorida. Persamaan kurva baku yang digunakan
untuk menetapkan kadar kloramfenikol yaitu persamaan replikasi I yaitu y =
0,9299x + 1,08x10-4 yang memiliki nilai r = 0,9999. Untuk menetapkan kadar
lidokain hidroklorida digunakan persamaan replikasi I yaitu y= 0,9682x + 0,0692
yang memiliki nilai r = 0,9999.
Gambar 21. Kurva hubungan antara jumlah kloramfenikol vs AUC
Gambar 22. Kurva hubungan antara jumlah lidokain hidroklorida vs AUC
Dari kurva baku kloramfenikol dan lidokain hidroklorida di atas
41
tersebut menggambarkan terjadinya peningkatan respon AUC proporsional
dengan meningkatnya jumlah analit di dalam sampel.
G. Penetapan Kadar Kloramfenikol dan Lidokain Hidroklorida dalam
Sediaan Tetes Telinga Colme® dengan Metode KCKT
Dua puluh botol kemasan sampel dihomogenkan terlebih dahulu. Proses
homogenisasi dilakukan dengan mencampurkan semua sampel menjadi satu ke
dalam suatu wadah tertentu. Sampel dibuat menjadi larutan stok dengan
konsentrasi 10000 ppm lalu dibuat larutan intermediet yang didalamnya
mengandung 500 ppm kloramfenikol dan 200 ppm lidokain hidroklorida, hal ini
sesuai dengan perbandingan kandungan kloramfenikol dan lidokain hidroklorida
dalam sampel (10% : 4%) yaitu perbandingan 5:2.
Sesuai dengan rangkaian penelitian mengenai validasi metode KCKT
untuk penetapan kadar kloramfenikol dan lidokain hidroklorida dalam Colme®
untuk standard addition method memiliki akurasi dan presisi pada seri tinggi (10
µg) dengan volume injeksi 20 µL. Dari data yang diperoleh tersebut, maka sampel
diinjeksikan ke dalam sistem KCKT dengan volume injeksi 20 µL dari larutan
intermediet sampel yang sudah terkandung 500 ppm kloramfenikol, 200 ppm
lidokain hidroklorida, serta 300 ppm larutan baku hidroklorida yang telah
ditambahkan ke dalam sampel.
Analisis kuantitatif dilakukan dengan menghitung kadar tiap zat aktif
dalam obat tetes telinga Colme® yang memiliki komposisi kloramfenikol 10%
dan lidokain hidroklorida 4%. Larutan sampel diinjeksikan ke dalam sistem
KCKT. Hasil yang diperoleh sebagai berikut:
Tabel VIII. Hasil Penetapan Kadar Campuran Kloramfenikol dan Lidokain Hidroklorida dalam Colme®
Sampel
Kloramfenikol Lidokain Hidroklorida
AUC Kadar %
Di dalam etiket yang tertera pada kemasan obat tetes telinga Colme® ,
tertulis bahwa kandungan kloramfenikol dan lidokain hidroklorida adalah 10%
dan 4%. Rentang yang diperbolehkan untuk kloramfenikol pada obat tetes telinga
adalah 90-130% dan rentang untuk lidokain hidroklorida adalah 95-105%. Jadi
rentang kloramfenikol dalam sampel Colme® adalah 9-13% sedangkan untuk
lidokain hidroklorida adalah 3,8-4,2%. Hasil yang diperoleh menunjukkan bahwa
untuk kadar kloramfenikol berada pada rentang 11,01-12,21%, rentang ini masuk
dalam rentang persayaratan kadar kloramfenikol yaitu 9-13% dari yang tertera
dalam etiket. Kadar lidokain hidroklorida yang diperoleh berada pada rentang
3,62-4,09%, rentang ini tidak masuk dalam rentang persyaratan kadar lidokain
43
dari sepuluh replikasi, kadar lidokain hidroklorida untuk tujuh replikasi berada
dibawah batas terendah dari rentang yang dipersyaratkan (x < 3,8). Oleh karena
itu, perlu dilakukan pengawasan continue untuk homogenitas campuran dalam
proses produksi sediaan tetes telinga Colme®.
BAB V
KESIMPULAN DAN SARAN
A. Kesimpulan
1. Penetapan kadar kloramfenikol dan lidokain hidroklorida dalam sediaan tetes
telinga Colme® dengan metode KCKT fase terbalik diperoleh hasil yaitu
11,01-12,21% untuk kloramfenikol dan 3,62-4,09% untuk lidokain
hidroklorida. Coefficient of Variation (CV) kadar kloramfenikol yaitu 3,37%
dan CV kadar lidokain hidroklorida yaitu 3,95%
2. Kadar kloramfenikol yang diperoleh sesuai dengan yang tertera pada label
kemasan, namun untuk kadar lidokain tidak sesuai dengan yang tertera pada
label kemasan obat tetes telinga Colme®.
B. Saran
1. Perlu dilakukan penetapan kadar kloramfenikol dan lidokain hidroklorida
dalam sediaan obat tetes telinga Colme® dengan menggunakan sampling yang