i
VALIDASI METODE KROMATOGRAFI LAPIS TIPIS (KLT)-DENSITOMETRI PADA PENETAPAN KADAR KLORAMFENIKOL DAN LIDOKAIN HCl SEBAGAI ZAT AKTIF DI DALAM OBAT TETES
TELINGA COLME®
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Farmasi
Oleh: Regina Clarissa NIM : 088114029
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
2011
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
ii
VALIDASI METODE KROMATOGRAFI LAPIS TIPIS (KLT)-DENSITOMETRI PADA PENETAPAN KADAR KLORAMFENIKOL DAN LIDOKAIN HCl SEBAGAI ZAT AKTIF DI DALAM OBAT TETES
TELINGA COLME®
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Farmasi
Oleh: Regina Clarissa NIM : 088114029
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
2011
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
iii
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
iv
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
v
HALAMAN PERSEMBAHAN
Untuk yang tersayang,
Mami, Papa, Vania, Rio
Sahabat-sahabatku, serta
Almamaterku
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
vi
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
vii
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
viii
PRAKATA
Puji dan syukur penulis panjatkan kepada Tuhan Yang Maha Esa atas segala berkat dan anugerah yang telah diberikan-Nya, sehingga penulis dapat menyelesaikan skripsi yang berjudul Validasi Metode Kromatografi Lapis Tipis (KLT)-Densitometri pada Penetapan Kadar Kloramfenikol dan Lidokain HCl Sebagai Zat Aktif di dalam Obat Tetes Telinga Colme®. Skripsi ini disusun sebagai salah satu syarat untuk memperoleh gelar Sarjana Farmasi (S.Farm).
Selama perkuliahan, penelitian, dan penyusunan skrispsi ini, penulis mendapat banyak bantuan dari berbagai pihak yang berupa bimbingan, dukungan, semangat, kritik, dan saran yang membangun. Oleh karena itu, pada kesempatan ini penulis ingin menyampaikan ucapan terima kasih yang sebesar-besarnya kepada:
1. Bapak Ipang Djunarko, M.Sc., Apt. selaku Dekan Fakultas Farmasi Universitas Sanata Dharma.
2. Ibu Christine Patramurti, M.Si., Apt., selaku dosen pembimbing atas segala bimbingan, perhatian, semangat, kritik, dan saran selama penelitian dan penyusunan naskah.
3. Ibu Jeffry Julianus, M.Si., selaku dosen penguji atas segala arahan, masukan, kritik, dan saran yang telah diberikan kepada penulis.
4. Ibu Dra. M.M. Yetty Tjandrawati, M.Si., selaku dosen penguji atas segala arahan, masukan, kritik, dan saran yang telah diberikan kepada penulis.
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
ix
5. Ibu Rini Dwiastuti, M.Sc., Apt., selaku Kepala Laboratorium Universitas Sanata Dharma atas ijin yang diberikan untuk melakukan penelitian di laboratorium Kimia Analisis Intrumental.
6. Ibu dr. Fenty, M.Kes., Sp.PK, selaku dosen pembimbing akademik atas pendampingannya dari semester satu.
7. Segenap dosen dan karyawan atas ilmu dan pengalaman yang diberikan, sehingga berguna dalam penyusunan skripsi ini.
8. Bapak Siswanto Tanuatmojo, selaku Manager Research and Development PT. Interbat atas pemberian baku kloramfenikol, baku lidokain HCl, dan sampel obat tetes telinga Colme®.
9. Mas Bimo, Mas Parlan, Mas Kunto, selaku laboran yang telah banyak membantu penulis selama penelitian di laboratorium.
10. Pak Otok, atas bantuannya dalam pengadaan bahan-bahan yang diperlukan selama penelitian.
11. Lele dan Felicia sebagai teman seperjuangan satu judul dalam penyelesaian penelitian ini, atas kebersamaan, semangat, keceriaan, nasehat, dan dukungannya selama ini di laboratorium dan kuliah.
12. Sari, Tere, Wiwie sebagai teman satu kelompok skripsi kloram-lido atas kebersamaan, semangat, dan keceriaan selama di laboratorium maupun kuliah.
13. Novi, Cure, Citra, Susan, Susi, Nona, Ayesa, Amel, Dina, sebagai teman satu bimbingan skripsi atas kebersamaan, semangat, dan keceriaan selama ini.
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
x
14. Rika, Meimei, Bravo, Lala, Elya, Widi, Metri, Lisu untuk kebersamaan, keceriaan dan semangat selama ini.
15. Apostolos Family atas kebersamaan, keceriaan, dan persekutuan di PMK selama ini.
16. Teman-teman kelompok praktikum A, khususnya kelompok A2, dan teman-teman angkatan 2008 atas semangat, kerja sama, dan kebersamaannya selama ini.
17. Semua pihak yang tidak dapat disebutkan satu persatu oleh penulis, terima kasih atas segala bantuan yang telah diberikan selama ini, sehingga penulis dapat menyelesaikan skrispi ini.
Penulis menyadari masih banyak kekurangan di dalam penulisan skripsi ini. Oleh karena itu, penulis mengharapkan kritik dan saran yang membangun untuk perkembangan selanjutnya.
Penulis
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
xi
DAFTAR ISI
Halaman
HALAMAN JUDUL………... ii
HALAMAN PERSETUJUAN PEMBIMBING………...…... iii
HALAMAN PENGESAHAN………..…….. iv
HALAMAN PERSEMBAHAN………….………..…….. v
PERNYATAAN KEASLIAN KARYA………..……... vi
LEMBAR PERSETUJUAN PUBLIKASI KARYA………….………… vii
PRAKATA……….………… viii
A. Latar Belakang……… 1
1. Permasalahan……….…... 3
2. Keaslian Penelitian……… 3
3. Manfaat Penelitian……… 4
B. Tujuan………. 4
BAB II PENELAAHAN PUSTAKA………..………..…. 5
A. Kloramfenikol………... 5
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
xii
B. Lidokain HCl……….……….. 6
C. Obat Tetes Telinga……….. 7
D. Obat Tetes Telinga Colme®……… 7
E. Kromatografi Lapis Tipis……… 8
1. Tinjauan umum……….………… 8
2. Sistem kromatogfrafi lapis tipis……....………..………….. 12
F. Densitometer……….………….. 15
G. Validasi Metode……….………... 16
1. Tinjauan umum……….………… 16
2. Parameter validasi……….……… 18
H. Landasan Teori………... 21
I. Hipotesis………. 22
BAB III METODE PENELITIAN………....………….. 23
A. Jenis dan Rancangan Penelitian………. 23
B. Variabel Penelitian………. 23
C. Definisi Operasional………... 23
D. Bahan Penelitian………. 24
E. Alat Penelitian……… 24
F. Tata Cara Penelitian……… 25
1. Pembuatan fase gerak... 25
2. Pembuatan larutan baku kloramfenikol... 25
3. Pembuatan larutan baku lidokain HCl... 25 4. Pembuatan larutan baku campuran kloramfenikol:lidokain HCl
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
xiii
(1:10)... 25
5. Penentuan panjang gelombang pengamatan kloramfenikol dan lidokain HCl... 26
6. Pembuatan kurva baku... 26
7. Penentuan recovery dan Koefisien Variasi (KV) baku tunggal... 27
8. Penentuan recovery dan KV baku campuran kloramfenikol:lidokain HCl 300:3000 ng, 600:6000 ng, dan 900:9000 ng... 27
9. Penentuan recovery dan KV adisi baku dalam sampel... 28
G. Analisis Hasil... 30
1. Selektivitas... 30
2. Linearitas... 30
3. Akurasi... 30
4. Akurasi adisi baku dalam matriks sampel... 30
5. Presisi... 30
6. Range... 31
BAB IV HASIL DAN PEMBAHASAN... 32
A. Pembuatan Fase Gerak... 32
B. Pembuatan Larutan Baku... 32
C. Penentuan Panjang Gelombang Pengamatan... 33
D. Analisis Kualitatif... 36
E. Pembuatan Kurva Baku Kloramfenikol dan Lidokain HCl... 41
F. Validasi Metode Analisis... 44
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
xiv
1. Selektivitas... 44
2. Linearitas... 45
3. Akurasi... 46
4. Presisi... 48
5. Range... 50
6. Akurasi dan presisi adisi baku kloramfenikol dan lidokain HCl dalam sampel... 51
BAB V KESIMPULAN DAN SARAN... 56
A. Kesimpulan... 56
B. Saran... 56
DAFTAR PUSTAKA... 57
LAMPIRAN... 60
BIOGRAFI PENULIS... 101
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
xv
DAFTAR TABEL
Halaman
Tabel I. Nilai indeks polaritas pelarut... 14
Tabel II. Parameter analisis validasi metode... 18
Tabel III. Kriteria rentang recovery yang dapat diterima... 19
Tabel IV. Kriteria KV yang dapat diterima... 20
Tabel V. Data replikasi kurva baku kloramfeikol... 42
Tabel VI. Data replikasi kurva baku lidokain HCl... 42
Tabel VII. Nilai Rs sampel... 45
Tabel VIII. Data recovery baku tunggal... 46
Tabel IX. Data recovery baku campuran kloramfenikol:lidokain HCl (1:10)... 47
Tabel X. Data koefisen variasi (KV) baku tunggal... 48
Tabel XI. Data Koefisien Variasi (KV) baku campuran kloramfenikol:lidokain HCl (1:10)... 49
Tabel XII. Recovery dan KV adisi baku kloramfenikol dalam sampel.... 54
Tabel XIII. Recovery dan KV adisi baku lidokain HCl dalam sampel... 54
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
xvi
DAFTAR GAMBAR
Halaman
Gambar 1. Struktur kloramfenikol... 5
Gambar 2. Struktur lidokain HCl... 6
Gambar 3. Obat tetes telinga Colme®... 8
Gambar 4. Retardation Factor (Rf)... 12
Gambar 5. Struktur silika gel... 13
Gambar 6. Densitometer... 16
Gambar 7. Gugus kromofor dan auksokrom pada kloramfenikol (A) dan lidokain HCl (B)... 34
Gambar 8. Spektra kloramfenikol (300, 600, dan 900 ng) dan lidokain HCl (3000, 6000, dan 9000 ng)... 36
Gambar 9. Perbandingan nilai Rf baku kloramfenikol dan lidokain HCl dengan Rf sampel... 38
Gambar 10. Interkasi kloramfenikol dengan fase diam silika gel... 39
Gambar 11. Interkasi lidokain dengan fase diam silika gel... 39
Gambar 12. Interaksi kloramfenikol dengan fase gerak toluena: n-heksana:metanol:dietilamin (19,75;3,75;5;1,5)... 40
Gambar 13. Interaksi lidokain dengan fase gerak toluena: n-heksana:metanol:dietilamin (19,75;3,75;5;1,5)... 40
Gambar 14. Kurva hubungan antara jumlah kloramfenikol (ng) dan AUC (replikasi II hasil modifikasi)... 43 Gambar 15. Kurva hubungan antara jumlah lidokain HCl (ng) dan AUC
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
xvii
(replikasi II)... 43
Gambar 16. Kromatogram sampel... 45
Gambar 17. Range jumlah kloramfenikol... 50
Gambar 18. Range jumlah lidokain HCl... 51
Gambar 19. Kromatogram sampel tanpa penambahan baku kloramfenikol... 52
Gambar 20. Kromatogram sampel dengan penambahan baku kloramfenikol... 52
Gambar 21. Kromatogram sampel tanpa penambahan baku lidokain HCl... 53
Gambar 22. Kromatogram sampel dengan penambahan baku lidokain HCl... 53
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
xviii
DAFTAR LAMPIRAN
Halaman
Lampiran 1. CoA kloramfenikol... 60
Lampiran 2. CoA lidokain HCl... 61
Lampiran 3. Sistem densitometer... 62
Lampiran 4. Data penimbangan bahan... 62
Lampiran 5. Spektra kloramfenikol (300, 600, 900 ng) dan lidokain HCl (3000, 6000, 9000 ng)... 64
Lampiran 6. Kromatogram baku kloramfenikol 300 ppm (replikasi 2)... 66
Lampiran 7. Kromatogram baku lidokain HCl 3000 ppm (replikasi 2)... 68
Lampiran 8. Data kurva baku kloramfenikol dan lidokain HCl... 70
Lampiran 9. Kromatogram sampel dan perhitungan nilai resolusi sampel... 70
Lampiran 10. Kromatogram presisi dan akurasi baku tunggal kloramfenikol... 71
Lampiran 11. Kromatogram presisi dan akurasi baku tunggal lidokain HCl... 75
Lampiran 12. Presisi dan akurasi baku tunggal kloramfenikol... 78
Lampiran 13. Presisi dan akurasi baku tunggal lidokain HCl... 80
Lampiran 14. Kromatogram presisi dan akurasi baku campuran kloramfenikol:lidokain HCl (1:10)... 82
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
xix
Lampiran 15. Presisi dan akurasi baku campuran
kloramfenikol:lidokain HCl (1:10)... 87 Lampiran 16. Kromatogram sampel tanpa penambahan baku... 89 Lampiran 17. Kromatogram sampel dengan penambahan baku... 93 Lampiran 18. Presisi akurasi adisi baku kloramfenikol dalam sampel... 97 Lampiran 19. Presisi akurasi adisi baku lidokain HCl dalam sampel... 99
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
xx
INTISARI
Tujuan dari penelitian ini adalah melakukan validasi metode yang akan digunakan untuk melakukan penetapan kadar kloramfenikol dan lidokain HCl yang merupakan zat aktif di dalam obat tetes telinga Colme®. Penelitian ini merupakan penelitian non-eksperimental deskriptif. Metode yang digunakan adalah Kromatografi Lapis Tipis (KLT)-densitometri dengan fase diam silika gel 60 F254 dan fase gerak hasil optimasi yaitu toluena:n-heksana:metanol:dietilamin (19,75:3,75:5:1,5).
Parameter validasi yang diteliti meliputi selektivitas, linearitas, akurasi, presisi, dan range. Hasil penelitian menunjukkan bahwa metode KLT-densitometri telah memenuhi parameter selektivitas dengan nilai Rs = 2,95, linearitas dengan nilai r = 0,9998 (kloramfenikol) dan 0,9997 (lidokain HCl). Recovery untuk kloramfenikol 300 dan 600 ng masing-masing adalah 92,39-103,01% dan 91,29-1-3,13% , serta lidokain HCl 6000 ng dengan recovery 95,97-104,38% telah memenuhi parameter akurasi. KV untuk kloramfenikol 300, 600, dan 900 ng masing-masing adalah 4,66; 5,08; dan 4,92%, serta lidokain HCl 6000 ng dengan KV 3,78% telah memenuhi parameter presisi. Range 300-600 ng untuk kloramfenikol dan tidak ditemukan range untuk lidokain HCl, namun hanya pada satu titik yaitu 6000 ng untuk lidokain HCl.
Kata kunci: kloramfenikol, lidokain HCl, KLT-densitometri, validasi metode
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
xxi
ABSTRACT
The purpose of this study is to validate the method which will be used to perform the assay of chloramphenicol and lidocaine HCl which are the active substances in the Colme® ear drop. This study is a non-experimental descriptive study. The method that is used is Thin Layer Chromatography (TLC)-densitometry using silica gel 60 F254 for the stationary phase and the optimization of mobile phase toluene:n-hexane:methanol:diethylamine (19,75:3,75:5:1,5).
Validation parameters which are examined in this study are selectivity, linearity, accuracy, precision, and range. The results showed that TLC-densitometry method has complied selectivity with Rs value = 2,95 and linearity with r = 0,9998 (chloramphenicol) and r = 0,9997 (lidocaine HCl). Recovery for chloramphenicol 300 and 600 ng are 92,39-103,01% and 91,29-1-3,13%, and recovery for lidocaine HCl 6000 ng is 95,97-104,38% have complied the parameter of accuracy. CV values for chloramphenicol 300, 600, 900 ng are 4,66; 5,08; and 4,92%, and CV for lidocaine HCl 6000 ng is 3,78% have complied the parameter of precision. Range 300-600 ng for chloramphenicol and range for lidocaine HCl is not found, but there is just one point 6000 ng for lidocaine HCl.
Key words: chloramphenicol, lidocaine HCl, TLC-densitometry, method validation
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
1
BAB I
PENGANTAR
A. Latar Belakang
Antibiotik merupakan obat antiinfeksi yang secara drastis telah berhasil menurunkan morbiditas dan mortalitas berbagai penyakit infeksi, sehingga penggunaan antibiotik meningkat secara tajam. Salah satu penyakit infeksi yang cukup tinggi prevalensinya di Indonesia adalah Otitis Media Supuratif Kronik (OMSK) yaitu 3%. Angka ini termasuk tinggi menurut WHO karena ada di kisaran 2-4% (Anonima, 2010).
Pengobatan penyakit infeksi telinga biasanya menggunakan obat tetes telinga. Obat tetes telinga adalah obat tetes yang digunakan dengan cara meneteskan ke dalam telinga. Kecuali dinyatakan lain, dibuat dengan menggunakan pembawa bukan air (Direktorat Jendral Pengawasan Obat dan Makanan RI, 1995).
Obat tetes telinga yang akan dianalisis adalah Colme®. Di dalam penelitian ini, penulis akan melakukan penjaminan mutu terhadap obat tetes telinga Colme®. Penjaminan mutu dapat dilakukan dengan menetapkan kadar senyawa-senyawa yang terdapat di dalam obat tetes telinga Colme®, yaitu kloramfenikol dan lidokain HCl, sehingga diperoleh jaminan bahwa kadar yang terukur sama dengan kadar yang tertera di dalam kemasan.
Kloramfenikol sukar larut dalam air, mudah larut dalam etanol, propilenglikol, aseton, dan etil asetat. Kloramfenikol memiliki pH antara 4,5
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
2 kloroform, dan tidak larut dalam eter (Clarke, 1986).
Secara umum, penggunaan kromatografi untuk analisis kualitatif dan kuantitatif teridiri dari kromatografi kolom, gas, kertas, lapis tipis, dan KCKT (United States Pharmacopeial Convention, 1995). Di dalam penelitian ini, metode yang dipilih adalah Kromatografi Lapis Tipis (KLT)-densitometri karena dapat digunakan untuk analisis kualitatif dan kuantitatif, serta memiliki beberapa keuntungan dibandingkan dengan Kromatografi Cair Kinerja Tinggi (KCKT) atau kromatografi gas, yaitu pemilihan fase gerak lebih fleksibel, lebih mudah, terdapat beberapa macam teknik optimasi pemisahan seperti pengembangan dua dimensi, pengembangan bertingkat, dan pembaceman fase diam dapat dilakukan pada KLT, serta semua komponen dalam sampel dapat terdeteksi (Rohman, 2009).
Penelitian ini merupakan suatu rangkaian penelitian dalam rangka penjaminan mutu obat tetes telinga Colme® yang terdiri dari optimasi, validasi metode, dan penetapan kadar kloramfenikol dan lidokain HCl dalam obat tetes
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
3
telinga Colme®. Di dalam penelitian ini, penulis mengambil bagian pada tahap validasi metode. Validasi metode adalah proses mendokumentasikan atau membuktikan metode analisis yang digunakan dapat memberikan data analisis yang acceptable untuk penggunaan yang dimaksudkan (Christian, 2004).
Validasi ini bertujuan untuk memberikan jaminan bahwa metode analisis dengan sistem yang telah dioptimasi sebelumnya, yaitu fase gerak toluena:n-heksana:metanol:dietilamin (19,75:3,75:5:1,5) dan fase diam silika gel 60 F254 (Hernat, 2011), telah memenuhi parameter-parameter validasi yaitu selektivitas, linearitas, akurasi, presisi, dan range, sehingga dapat memberikan hasil analisis yang valid. Oleh karena itu, tahap validasi metode KLT-densitometri ini sangat penting untuk dilakukan sebelum melakukan penetepakan kadar kloramfenikol dan lidokain HCl dalam obat tetes telinga Colme®.
1. Permasalahan
Berdasarkan latar belakang di atas maka diperoleh permasalahan yaitu apakah metode KLT-densitometri untuk penetapan kadar kloramfenikol dan lidokain HCl sebagai zat aktif di dalam obat tetes telinga Colme® memenuhi parameter-parameter validasi yang meliputi selektivitas, linearitas, akurasi, presisi, dan range?
2. Keaslian penelitian
Penetapan kadar kloramfenikol dan lidokain HCl yang pernah dilakukan adalah penetapan kadar secara tunggal. Di dalam jurnal karya Vovk dan Simonovska (2005), pengembangan dan validasi metode KLT-densitometri
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
4
untuk menetapkan kadar residu kloramfenikol di peralatan farmasetika menggunakan fase diam silika gel dan fase gerak n-heksana:etil asetat (35:65 v/v). Pada penelitian yang dilakukan oleh Kiszka dan Madro (2002), pemisahan lidokain dilakukan menggunakan KLT dengan fase gerak hexana:toluena:dietilamin dengan perbandingan 65:20:5.
Penelitian yang dilakukan oleh penulis adalah melakukan validasi metode KLT-densitometri untuk menetapkan kadar kloramfenikol dan lidokain HCl di dalam campuran yang belum pernah dilakukan pada penelitian sebelumnya.
3. Manfaat penelitian
a. Manfaat metodologis. Penelitian ini diharapkan dapat memberikan sumbangan ilmiah tentang penggunaan metode KLT-densitometri pada penetapan kadar kloramfenikol dan lidokain HCl dalam campuran.
b. Manfaat praktis. Hasil penelitian diharapkan dapat memberikan informasi mengenai selektivitas, linearitas, akurasi, presisi, dan range metode KLT-densitometriuntuk penetapan kadar kloramfenikol dan lidokain HCl dalam obat tetes telinga Colme®.
B. Tujuan
Penelitian ini bertujuan untuk membuktikan bahwa metode KLT-densitometri telah memenuhi parameter-parameter validasi yaitu selektivitas, linearitas, akurasi, presisi, dan range, sehingga dapatdigunakan untuk penetapan kadar kloramfenikol dan lidokain HCl dalam obat tetes telinga Colme®.
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
5
BAB II
PENELAAHAN PUSTAKA
A. Kloramfenikol
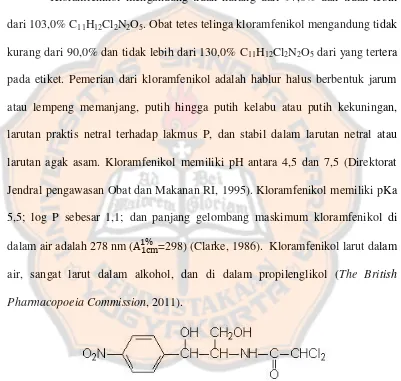
Kloramfenikol mengandung tidak kurang dari 97,0% dan tidak lebih dari 103,0% C11H12Cl2N2O5. Obat tetes telinga kloramfenikol mengandung tidak kurang dari 90,0% dan tidak lebih dari 130,0% C11H12Cl2N2O5 dari yang tertera pada etiket. Pemerian dari kloramfenikol adalah hablur halus berbentuk jarum atau lempeng memanjang, putih hingga putih kelabu atau putih kekuningan, larutan praktis netral terhadap lakmus P, dan stabil dalam larutan netral atau larutan agak asam. Kloramfenikol memiliki pH antara 4,5 dan 7,5 (Direktorat Jendral pengawasan Obat dan Makanan RI, 1995). Kloramfenikol memiliki pKa 5,5; log P sebesar 1,1; dan panjang gelombang maskimum kloramfenikol di
dalam air adalah 278 nm ( =298) (Clarke, 1986). Kloramfenikol larut dalam air, sangat larut dalam alkohol, dan di dalam propilenglikol (The British Pharmacopoeia Commission, 2011).
Gambar 1. Struktur kloramfenikol (Anonima, 2011)
Kloramfenikol merupakan antibiotik yang semula berasal dari sejenis Streptomyces, namun kemudian dibuat secara sintesis. Kloramfenikol dapat berkhasiat sebagai bakteriostatis dan bakterisida. Mekanisme kerjanya dengan menghambat sintesis protein pada bakteri (Tjay Tan dan Rahardja, 2010).
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
6
B. Lidokain HCl
Lidokain HCl mengandung tidak kurang dari 97,5% dan tidak lebih dari 102,5% C14H22N2O.HCl, dihitung terhadap zat anhidrat. Larutan topikal lidokain HCl mengandung C14H22N2O.HCl tidak kurang dari 95,0% dan tidak lebih dari 105,0% dari jumlah yang tertera pada etiket. Pemerian dari lidokain HCl adalah serbuk hablur putih, tidak berbau, dan rasa sedikit pahit. Lidokain HCl sangat mudah larut dalam air dan dalam etanol, larut dalam kloroform, dan tidak larut dalam eter (Direktorat Jendral Pengawasan Obat dan Makanan, 1995). Lidokain HCl memiliki pH 4,5-5 dan titik leleh 74-79 oC (The British Pharmacopoeia Commission, 2011). Lidokain HCl memiliki pKa 7,9 dan panjang gelombang
maskimun di larutan asam yaitu 263 nm ( =19) (Clarke, 1986).
Gambar 2. Struktur lidokain HCl (Anonimb, 2010)
Lidokain (otopain) adalah zat pemati rasa lokal yang pada kulit dan selaput lendir mampu menghalangi rasa nyeri, perasaan terbakar, dan gatal. Terdapat dalam tetes telinga 0,5%, tetapi tidak digunakan pada perforasi selaput gendang dan pada radang telinga atau congek. Berhubung tidak mengakibatkan hipersensitasi, lidokain banyak digunakan dalam banyak sediaan topikal (Tjay Tan dan Rahardja, 2010).
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
7
C. Obat Tetes Telinga
Tetesan (guttae) adalah sediaan cair yang mengandung bahan obat atau obat atau bahan obat dan obat terlarut, teremulsi atau tersuspensi, ditakar berdasar jumlah tetesan, digunakan untuk diminum, dan diisikan ke dalam wadah bertakaran ganda. Untuk tetesan tertentu yang digunakan di telinga, dinamakan tetes telinga (otoguttae) (Voigt, 1994).
Obat tetes telinga adalah obat tetes yang digunakan dengan cara meneteskan ke dalam telinga. Kecuali dinyatakan lain, dibuat dengan menggunakan pembawa bukan air. Cairan pembawa yang digunakan harus mempunyai kekentalan yang cocok agar obat mudah menempel pada dinding telinga, umumnya digunakan gliserol dan propilenglikol, dapat juga digunakan etanol, heksilenglikol, dan minyak lemak nabati (Direktorat Jendral Pengawasan Obat dan Makanan RI, 1974).
D. Obat Tetes Telinga Colme®
Obat tetes telinga Colme® kemasan botol 8 mL yang diproduksi oleh PT. Interbat mengandung kloramfenikol 10% dan lidokain HCl 4%. Indikasi untuk pengobatan otitis ekterna dan media dan dosis pemakaian 1-2 tetes, 3-4 kali sehari untuk anak-anak dan dewasa (Anonimb, 2011). Kontra indikasi bagi penderita yang hipersensitif terhadap kloramfenikol dan lidokain HCl, serta perforasi membran timpani. Colme® disimpan dalam kondisi tertutup, di bawah 25oC, jangan disimpan dalam lemari pembeku, terlindung dari cahaya matahari,
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
8
hindari terjadinya kontaminasi, dan jauhkan dari jangkauan anak-anak (Anonimc, 2011).
Gambar 3. Obat tetes telinga Colme® (Anonimc, 2011)
E. Kromatografi Lapis Tipis
1. Tinjauan umum
Kromatografi didefinisikan sebagai prosedur pemisahan zat terlarut oleh suatu proses migrasi diferensial dinamis dalam sistem yang terdiri dari dua fase atau lebih, salah satu diantaranya bergerak secara berkesinambungan dalam arah tertentu dan di dalamnya zat-zat itu menunjukkan perbedaan mobilitas disebabkan adanya perbedaan dalam adsorbsi, partisi, kelarutan, tekanan uap, ukuran molekul, atau kerapatan muatan ion. Dengan demikian masing-masing zat dapat diidentifikasi atau ditetapkan dengan metode analitik (Direktorat Jendral Pengawasan Obat dan Makanan RI, 1995).
Teknik kromatografi umum membutuhkan zat terlarut terdistribusi diantara dua fase, satu diantaranya diam (fase diam), yang lainnya bergerak (fase gerak). Fase gerak membawa zat terlarut melalui media, hingga terpisah dari zat terlarut lainnya, yang terelusi lebih awal atau lebih akhir. Umumnya zat terlarut dibawa melalui media pemisah oleh aliran suatu pelarut berbentuk cairan atau gas yang disebut eluen. Fase diam dapat berfungsi sebagai penjerap, seperti
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
9
halnya penjerap alumina yang diaktifkan, silika gel, resin penukar ion, atau dapat bertindak melarutkan zat terlarut, sehingga terjadi partisi antara fase diam dan fase gerak. Dalam proses terakhir ini, suatu lapisan cairan pada suatu penyangga yang inert berfungsi sebagai fase diam. Partisi merupakan mekanisme pemisahan yang utama dalam kromatografi cair-gas, kromatografi kertas, dan bentuk kromatografi kolom yang disebut kromatografi cair-cair. Dalam praktek, sering kali pemisahan disebabkan oleh suatu kombinasi efek adsorpsi dan partisi (Direktorat Jendral Pengawasan Obat dan Makanan RI, 1995).
Kromatografi digunakan secara luas untuk mengenali ada atau tidak adanya komponen dalam campuran yang mengandung senyawa dalam jumlah terbatas yang telah diketahui identitasnya. Kromatografi kuantitatif didasarkan pada perbandingan tinggi atau area puncak analit dengan satu atau lebih standar. Jika kondisi dikendalikan dengan benar, kedua parameter ini bervariasi secara linear dengan konsentrasi (Skoog, West, and Holler, 1994).
Kromatografi dapat dibedakan atas berbagai macam tergantung pada pengelompokannya. Berdasarkan pada mekanisme pemisahannya, kromatografi dibedakan menjadi: (a) kromatografi adsorbsi; (b) kromatografi partisi; (c) kromatografi pasangan ion; (d) kromatografi penukar ion; (e) kromatografi eksklusi ukuran; dan (f) kromatografi afinitas. Berdasarkan pada alat yang digunakan, kromatografi dapat dibagi atas: (a) kromatografi kertas; (b) kromatografi lapis tipis, yang keduanya disebut dengan kromatografi planar; (c)
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
10
kromatografi cair kinerja tinggi (KCKT); dan (d) kromatografi gas (KG) (Gandjar dan Rohman, 2007).
Kromatografi lapis tipis adalah bagian dari kromatografi planar yang secara luas digunakan untuk analisis kualitatif dan dapat juga digunakan untuk analisis kuantitatif (Christian, 2004). Kromatografi lapis tipis adalah suatu teknik pemisahan dengan fase diam yang mengandung material tertentu yang tersebar secara merata sebagai suatu lapisan yang tipis di pelat yang berupa gelas, logam, atau plastik. (The British Pharmacopoeia Commission, 2011).
Ismailoff dan Schraiber mengembangkan teknik kromatografi lapis tipis (KLT) pada tahun 1983 yang disebut juga sebagai kromatografi kolom terbuka. Metode ini sederhana, pemisahannya cepat, dan sensitif. Kelebihan lain adalah mudah untuk memperoleh kembali senyawa-senyawa yang terpisahkan. Untuk analisa kuantitatif dapat digunakan plot fotodensitometer (Khopkar, 1990).
Pemisahan pada kromatografi lapis tipis yang optimal akan diperoleh hanya jika menotolkan sampel dengan ukuran bercak sekecil mungkin dan sesempit mungkin. Sebagaimana dalam prosedur kromatografi yang lain, jika sampel yang digunakan terlalu banyak maka akan menurunkan resolusi. Hasil penelitian menunjukkan bahwa penotolan sampel secara otomatis lebih dipilih daripada penotolan secara manual terutama jika sampel yang akan ditotolkan lebih dari 15 μL. Penotolan sampel yang tidak tepat akan menyebakan bercak
yang menyebar dan puncak ganda (Gandjar dan Rohman, 2007).
Sampel ditotolkan di atas pelat dengan mikropipet dan dikembangkan dengan meletakkan bagian bawah dari pelat, bukan totolan sampel, dan di dalam
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
11
fase gerak yang sesuai. Fase gerak akan terelusi dengan adanya gaya kapilaritas, dan senyawa-senyawa yang terdapat dalam sampel akan bergerak naik dengan kecepatan yang berbeda sesuai dengan kelarutannya dan afinitasnya terhadap fase diam (Pecsok, Shields, Cairns, and McWilliam, 1976).
Pelat dengan indikator fluoresensi memfasilitasi untuk visualisasi senyawa yang mengabsorbsi sinar UV. Fluoresensi hijau diproduksi oleh zinc silikat teraktifasi mangan dan fluoresensi biru dihasilkan oleh magnesium tungstat yang terkandung di fase diam. Bagaimanapun, hanya magnesium tungstat yang stabil terhadap asam. Beberapa pelat memiliki kode “F” untuk
fluoresensi dan menjadi indikasi panjang gelombang eksitasi (Spangenberg, Poole, and Weins, 2010).
Gambar 4. Retardation Factor (Rf) (Anonim c
, 2010) A. Jarak yang ditempuh zat terlarut
B. Jarak yang ditempuh fase gerak
Perbandingan antara jarak yang ditempuh zat terlarut dan jarak yang ditempuh oleh fase gerak disebut dengan Retardation factor (Rf), dengan rumus
sebagai berikut:
(1) (Dean, 1995)
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
12
2. Sistem kromatografi lapis tipis
a. Fase diam. Silika gel adalah fase diam yang paling sering digunakan daripada fase diamnya lainnya. Lapisan silika gel terdiri dari partikel yang sangat kecil, sangat rapat, ukuran partikelnya yang seragam (6-13 μm), halus, dan homogen. Bahan pengikat untuk serbuk silika gel adalah 5-20% kalisum sulfat hemihidrat dan gipsum (silika gel G) yang berfungsi untuk meningkatkan kohesi dari partikel adsorben dan meningkatkan adesi lapisan adsorben ke pelat (Dean, 1995).
Semua silika gel adalah silikon dioksida dari sudut pandang kimia. Masing-masing atom silikon dikelilingi oleh empat atom oksigen dengan bentuk tetrahedron. Pada permukaan silika gel, elektron valensi dari oksigen terhubungkan dengan hidrogen (Si-OH, gugus silanol) atau dengan atom silikon lainnya (Si-O-Si, gugus siloksan). Semua silika gel memiliki densitas yang seragam pada gugus silanol yaitu sekitar 8 μmoles/m2. Gugus silanol mewakili
pusat permukaan adosorpsi-aktif yang mampu berinteraksi dengan molekul sampel. Oleh karena itu, silika gel cocok sebagai fase diam di dalam kromatografi. Kemampuan gugus silanol untuk bereaksi secara kimia dengan reagen yang sesuai dapat digunakan untuk modifikasi permukaan silika gel (Kowalska, 1996).
Partikel silika gel mengandung gugus hidroksi pada permukaannya yang akan membentuk ikatan hidrogen dengan molekul yang polar. Adanya air yang teradsorbsi akan mencegah molekul polar untuk membentuk ikatan hidrogen, sehingga silika gel harus diaktifkan dengan pemanasan untuk
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
13
menghilangkan air yang teradsorbsi (Christian, 2004). Kandungan air yang ideal adalah antara 11-12 % b/b (Rohman, 2009).
Gambar 5. Struktur silika gel (Hauck and Mack, 1996)
b. Fase gerak. Pemilihan sistem fase gerak untuk menyempurnakan pemisahan yang dikehendaki mungkin melibatkan sejumlah percobaan, tetapi pemilihan fase gerak tidak terlalu dibatasi dengan pertimbangan adanya gangguan respon detektor atau kemungkinan buruknya fase diam. Sistem fase gerak biasanya terdiri dari dua campuran komponen dari air dan pelarut organik polar yang larut air (Dean, 1995). Berikut adalah beberapa petunjuk dalam memilih dan mengoptimasi fase gerak:
1) Fase gerak harus mempunyai kemurnian yang sangat tinggi karena KLT merupakan teknik yang sangat sensitif.
2) Daya elusi fase gerak harus diatur sedemikian rupa, sehingga harga Rf terletak antara 0,2-0,8 untuk memaksimalkan pemisahan.
3) Untuk memisahkan menggunakan fase diam polar seperti silika gel, polaritas fase gerak akan menentukan kecepatan migrasi solut yang berarti juga mentukan harga Rf. Penambahan pelarut yang bersifat sedikit polar seperti dietil eter ke dalam pelarut seperti metal benzen akan meningkatkan harga Rf secara signifikan.
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
14
4) Solut-solut ionik dan solut-solut polar lebih baik digunakan campuran pelarut sebagai fase geraknya, seperti campuran air dan metanol dengan perbandingan tertentu. Penambahan sedikit asam metanoat atau ammonia masing-masing akan meningkatkan solut-solut yang bersifat basa dan asam (Gandjar dan Rohman, 2007).
Di dalam kromatografi adsorbsi, kekuatan elusi fase gerak meningkat seiring dengan meningkatnya polaritas (misalnya dari heksana ke aseton ke alkohol ke air). Fase gerak tunggal, atau paling banyak dua atau tiga larutan dapat digunakan jika memungkinkan. Fase gerak harus memiliki kemurnian yang tinggi. Keberadaan sejumlah kecil pengotor dapat menghasilkan kromatogram yang tidak reprodusibel (Christian, 2004).
Semakin besar nilai indeks polaritas yang dimiliki oleh pelarut maka pelarut tersebut semakin bersifat non polar (Snyder and Kirkland, 1997). Berikut ini merupakan tabel beberapa nilai indeks polaritas dari beberapa pelarut yang sering digunakan:
Tabel I. Nilai indeks polaritas pelarut (Snyder and Kirkland, 1997)
Solvent Indeks
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
15
Pergerakan fase gerak melintasi fase diam dipengaruhi oleh gaya kapilaritas. Fase diam (baik di dalam kromatografi adsorpsi, size-exclusion, maupun pertukaran ion) dan pendukungnya (di dalam kromatografi partisi) teridiri dari partikel solid yang mikroporus dengan luas permuakaan area yang besar (berkisar antara 50 m2/g untuk selulosa dan sampai 500 m2/g untuk silika) (Kowalska, 1996).
F. Densitometri
Pengukuran secara in situ suatu area dengan scanning densitometer adalah teknik yang digunakan untuk kuantitatif KLT. Relatif standar deviasi dari densitometri dapat diperoleh di bawah 2%, hal ini membuat alat ini reliabel untuk pengukuran secara kuantitatif (Sherma, 1996).
Senyawa yang telah dipisahkan menggunakan KLT atau High Performance Thin Layer Chromatography (HPTLC) diukur secara kuantitatif menggunakan pengukuran in situ dari absorbsi sinar tampak atau lampu ultraviolet atau fluoresensi. Absorbsi sinar UV diukur baik di pelat biasa ataupun pelat yang mengandung fosfor, hasilnya ditunjukkan dengan zona yang gelap di atas latar yang berpendar (Sherma, 1996).
Pada densitometri absorbsi, bercak pada KLT discan oleh seberkas sinar monokromatik selanjutnya di ubah menjadi gambar slit dengan panjang slit yang dipilih sesuai dengan diameter dari bercak yang paling luas. Karena respon dari scan reflektansi-serapan tidak linear dengan konsentrasi, standar kalibrasi disertakan ketika sampel running. Akibatnya, semua sampel, baik standar dan
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
16
senyawa yang tidak diketahui, ditempatkan pada kondisi kromatografi yang sama, dan kesalahan sistematik masih sangat minimal. Tingkat deteksi minimum untuk pengukuran pada sinar tampak atau ultraviolet dari 100 pg sampai 100 ng per totolan (Dean, 1995).
Gambar 6. Densitometer (Jaenchen, 1996)
G. Validasi Metode
1. Tinjauan umum
Validasi metode analisis adalah suatu tindakan penilaian terhadap parameter tertentu, berdasarkan percobaan laboratorium, untuk membuktikan bahwa parameter tersebut memenuhi persyaratan untuk penggunaannya (Harmita, 2004).
Menurut Adamovics (cit., Gandjar dan Rohman, 2007), tujuan utama validasi metode adalah untuk menghasilkan hasil analisis yang paling baik. Untuk memperoleh hasil tersebut, semua variabel yang terkait dengan metode analisis harus dipertimbangkan seperti prosedur pengambilan sampel, tahap penyiapan sampel, jenis penjerap yang digunakan pada kromatografi, fase gerak,
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
17
dan sistem deteksinya. Banyaknya parameter yang harus divalidasi tergantung pada tujuan analisis.
Menurut Swartz dan Krull (cit., Gandjar dan Rohman, 2007), suatu metode analisis harus divalidasi untuk melakukan verifikasi bahwa parameter-parameter kinerjanya cukup mampu mengatasi problem analisis, karenanya suatu metode harus divalidasi ketika:
a. Metode baru dikembangkan untuk mengatasi problem analisis tertentu.
b. Metode yang sudah baku direvisi untuk menyesuaikan perkembangan, atau karena munculnya suatu masalah yang mengarahkan bahwa metode baku tersebut harus direvisi.
c. Penjaminan mutu yang mengindikasikan bahwa metode baku telah berubah seiring dengan berjalannya waktu.
d. Metode baku digunakan di laboratorium yang berbeda dikerjakan oleh analis berbeda, atau dikerjakan dengan alat yang berbeda.
e. Untuk mendemonstrasikan kesetaraan antara dua metode, seperti antara metode baru dan metode baku.
Menurut The United States Pharmacopeia 30th tahun 2007, metode analisis dapat dibedakan menjadi 4 kategori, yaitu:
a. Kategori I. Mencakup prosedur analisis kuantitatif, untuk menetapkan kadar komponen utama bahan obat atau zat aktif dalam sediaan farmasi.
b. Kategori II. Mencakup prosedur analisis kualitatif dan kuantitatif yang digunakan untuk menganalisis impurities dalam sediaan farmasi.
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
18
c. Kategori III. Mencakup prosedur analisis yang digunakan untuk menentukan karakteristik penampilan suatu sediaan farmasi, misalnya disolusi dan pelepasan obat.
d. Kategori IV (tes identifikasi).
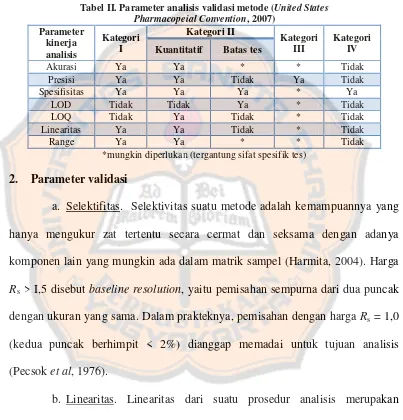
Tabel II. Parameter analisis validasi metode (United States Pharmacopeial Convention, 2007)
Parameter Kuantitatif Batas tes
Akurasi Ya Ya * * Tidak
*mungkin diperlukan (tergantung sifat spesifik tes)
2. Parameter validasi
a. Selektifitas. Selektivitas suatu metode adalah kemampuannya yang hanya mengukur zat tertentu secara cermat dan seksama dengan adanya komponen lain yang mungkin ada dalam matrik sampel (Harmita, 2004). Harga Rs > I,5 disebut baseline resolution, yaitu pemisahan sempurna dari dua puncak dengan ukuran yang sama. Dalam prakteknya, pemisahan dengan harga Rs = 1,0 (kedua puncak berhimpit < 2%) dianggap memadai untuk tujuan analisis (Pecsok et al, 1976).
b. Linearitas. Linearitas dari suatu prosedur analisis merupakan kemampuan (pada rentang tertentu) untuk mendapatkan hasil uji yang secara langsung proporsional dengan konsentrasi (jumlah) analit di dalam sampel. Persyaratan data linearitas yang bisa diterima jika memenuhi nilai koefisien korelasi (r) > 0,999 (Mulja dan Hanwar, 2003). Linearitas dapat diukur dengan
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
19
melakukan pengukuran tunggal pada konsentrasi yang berbeda-beda. Data yang diperoleh selanjutnya diproses dengan metode kuadrat terkecil, selanjutnya dapat ditentukan nilai kemiringan (slope), intersep, dan keofisien korelasinya. Kisaran konsentrasi yang digunakan untuk linearitas harus cukup luas untuk memenuhi kisaran metode yang diharapkan. Minimal 5 kisaran konsentrasi harus diamati dan suatu plot antara respon detektor dengan konsentrasi sampel harus dihasilkan (Rohman, 2009).
c. Akurasi. Akurasi dari suatu metode adalah kedekatan nilai yang diperoleh dengan nilai sebenarnya (true value) dari sampel. Akurasi ini mungkin merupakan parameter validasi yang paling sulit dan yang perlu diperhatikan adalah sampling dan perlakuan terhadap sampel (Christian, 2004).
Tabel III. Kriteria rentang recovery yang dapat diterima (Harmita, 2004) Analit pada matriks sampel (%) Rentang recovery yang diperoleh (%)
100 98-102
d. Presisi. Presisi atau keseksamaan adalah ukuran yang menunjukkan derajat kesesuaian antara hasil uji individual dari rata-rata jika prosedur diterapkan secara berulang pada sampel-sampel yang diambil dari campuran yang homogen. Keseksamaan diukur sebagai simpangan baku atau simpangan baku relatif (koefisien variasi). Keseksamaan dapat dinyatakan sebagai
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
20
keterulangan (repeatability) atau ketertiruan (reproducibility). Kriteria seksama diberikan jika metode memberikan simpangan baku relatif atau koefisien variasi 2% atau kurang. Akan tetapi kriteria ini sangat fleksibel tergantung pada konsentrasi analit yang diperiksa, jumlah sampel, dan kondisi laboratorium. (Harmita, 2004).
Tabel IV. Kriteria KV yang dapat diterima (Harmita, 2004)
Kadar analit KV(%) memenuhi prosedur analisis yang meliputi akurasi, presisi, dan linearitas (The British Pharmacopoeia Commission, 2011).
f. Batas deteksi (Limit of Detection atau LOD). Menurut Swartz dan Krull (cit., Gandjar dan Rohman, 2007), batas deteksi didefinisikan sebagai konsentrasi analit terendah yang masih dapat dideteksi, meskipun tidak selalu dapat dikuantifikasi. LOD merupakan batas uji yang secara spesifik menyatakan apakah analit di atas atau di bawah nilai tertentu. Sebagai contoh, batas deteksi merupakan banyaknya sampel yang menunjukkan respon (S) 3 kali terhadap derau (N) atau LOD = 3 S/N.
g. Batas kuantifikasi (Limit of Quantification atau LOQ). Batas kuantifikasi didefinisikan sebagai analit terendah dalam sampel yang dapat ditentukan dengan presisi akurasi yang dapat diterima pada kondisi operasional
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
21
metode yang digunakan. Sebagaimana LOD, LOQ juga diekspresikan sebagai konsentrasi (dengan akurasi dan presisi juga dilaporkan) dan kadang-kadang rasio signal to noise 10:1 digunakan untuk menentukan LOQ (Gandjar dan Rohman, 2007).
H. Landasan Teori
Kloramfenikol dan lidokain HCl merupakan salah satu kombinasi obat yang digunakan untuk mengobati infeksi telinga luar dan tengah. Obat tetes telinga yang memiliki komposisi kloramfenikol dan lidokain HCl adalah Colme®. Kloramfenikol larut dalam air, sangat larut dalam alkohol, dan di dalam propilenglikol. Kloramfenikol memiliki pH 4,5-7,5; pKa 5,5; log P sebesar 1,1; dan panjang gelombang maskimum kloramfenikol di dalam air adalah 278 nm
( =298). Lidokain HCl sangat mudah larut dalam air dan etanol, larut dalam kloroform, dan tidak larut dalam eter. Lidokain HCl memiliki pH 4,5-5,5; titik leleh 74-79oC; pKa 7,9; dan panjang gelombang maksimun di larutan asam
adalah 263 nm ( =19).
Salah satu metode yang dapat digunakan untuk memisahkan suatu campuran menjadi senyawa-senyawa tunggal dan melakukan analisis kuantitatif adalah KLT-densitometri. Metode KLT dapat digunakan untuk memisahkan campuran senyawa menjadi senyawa-senyawa tunggal karena adanya perbedaan afinitas dan interaksi senyawa terhadap fase diam dan fase gerak. Bercak yang muncul setelah dilakukan elusi dapat dianalisis kuantitatif menggunakan densitometer, sehingga dapat diperoleh nilai Rf dan AUC.
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
22
Suatu metode yang akan digunakan untuk analisis harus memiliki validitas yang baik agar data yang diperoleh dapat dipercaya. Parameter validasi meliputi selektivitas, linearitas, akurasi, presisi, dan range. Suatu metode analisis dikatakan memiliki validitas yang baik apabila memenuhi parameter-parameter validasi tersebut.
I. Hipotesis
Metode KLT-densitometri untuk penetapan kadar kloramfenikol dan lidokain HCl sebagai zat aktif di dalam obat tetes telinga Colme® memenuhi parameter-parameter validasi yang meliputi selektivitas, linearitas, akurasi, presisi, dan range.
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
23
BAB III
METODE PENELITIAN
A. Jenis dan Rancangan Penelitian
Penelitian yang dilakukan bersifat non-eksperimental deskriptif karena tidak terdapat manipulasi dan perlakuan terhadap subjek uji.
B. Variabel Penelitian
1. Variabel bebas adalah sistem KLT yang telah dioptimasi, yaitu jenis dan komposisi fase gerak.
2. Variabel tergantung adalah parameter-parameter validasi yaitu selektivitas, linearitas, akurasi, presisi, dan range.
3. Variabel pengacau terkendali adalah pelarut, bahan baku yang digunakan, dan kejenuhan bejana kromatografi, untuk mengatasinya digunakan pelarut pro analisis yang memiliki kemurnian tinggi, menggunakan bahan baku yang memiliki Certificate of Analysis (CoA), dan menggunakan kertas saring sebagai indikator kejenuhan bejana kromatografi.
C. Definisi Operasional
1. Sistem KLT yang digunakan adalah KLT fase normal dengan fase diam yang berupa silika gel 60 F254 dan fase gerak berupa campuran toluena:n-heksana:metanol:dietilamin (19,75:3,75:5:1,5).
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
24
2. Jumlah kloramfenikol dan lidokain HCl dinyatakan dalam satuan nanogram (ng).
3. Parameter validasi yang digunakan adalah selektivitas, akurasi, presisi, dan range.
D. Bahan Penelitian
Bahan-bahan yang digunakan dalam penelitian ini adalah baku kloramfenikol dari Chemo Lugano Branch dengan nomor batch 80002250001 dan baku lidokain HCl dari Megafine Pharma dengan nomor batch ALH/449/10, pelat KLT silika gel 60 F254 (E. Merck), etanol p.a (E. Merck), toluena p.a (E. Merck), n-heksana p.a (E. Merck), metanol p.a (E. Merck), aquadest, obat tetes
telinga Colme® kemasan botol 8 mL produksi PT. Interbat dengan nomor batch D 016004.
E. Alat Penelitian
Alat-alat yang digunakan dalam penelitian ini adalah seperangkat alat densitometer (Camag TLC Scanner 3 CAT. No. 027.6485 SER. No.160602) autosampler (Linomat 5 No.170610), neraca analitik (OHAOUS Carat Series
PAJ 1003, max 60/120 g, min 0,0001 g, d = 0,01/0,1 mg, e = 1 mg), neraca
analitik (Scaltec SBC 22 max 60/210 g; min 0,001 g; d = 0,01/0,1mg; e = 1mg), mikropipet 1-5 mL (Scorex), mikropipet 100-1000 µL (Scorex), bejana kromatografi (Camag), alat-alat gelas (Pyrex).
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
25
F. Tata Cara Penelitian
1. Pembuatan fase gerak
Fase gerak yang dibuat adalah fase gerak yang telah didapat dari hasil optimasi pada penelitian sebelumnya yaitu toluena:n-heksana:metanol:dietilamin (19,75:3,75:5:1,5). Volume masing-masing pelarut diukur menggunakan buret dan ditampung ke dalam labu takar 50 mL lalu digojog agar homogen.
2. Pembuatan larutan baku kloramfenikol
Baku kloramfenikol ditimbang seksama lebih kurang 10 mg, dimasukkan ke dalam labu takar 10 mL, dan dilarutkan dengan etanol sampai batas tanda, sehingga diperoleh larutan stok kloramfenikol 1000 ppm. Larutan stok diambil 1,5 menggunakan mikropipet, dimasukkan ke dalam labu takar 5 mL, dan diencerkan dengan etanol hingga batas tanda. Larutan digojog, sehingga diperoleh larutan baku kloramfenikol 300 ppm. Larutan ini siap untuk ditotolkan.
3. Pembuatan larutan baku lidokain HCl
Baku lidokain HCl ditimbang seksama lebih kurang 15 mg, dimasukkan ke dalam labu takar 5 ml, dan dilarutkan dengan etanol sampai batas tanda. Larutan digojog, sehingga diperoleh larutan baku lidokain HCl 3000 ppm. Larutan ini siap untuk ditotolkan.
4. Pembuatan larutan baku campuran kloramfenikol:lidokain HCl (1:10)
Baku lidokain HCl ditimbang seksama lebih kurang 15 mg dan dimasukkan ke dalam labu takar 5 mL. Baku kloramfenikol ditimbang seksama lebih kurang 10 mg, dimasukkan ke dalam labu takar 10 mL, dan dilarutkan
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
26
dengan etanol sampai batas tanda (larutan stok kloramfenikol). Larutan stok kloramfenikol diambil 1,5 menggunakan mikropipet, dimasukkan ke dalam labu takar 5 mL yang berisi 15 mg lidokain HCl, diencerkan dengan etanol sampai tanda batas, dan digojog, sehingga diperoleh larutan baku campuran kloramfenikol:lidokain HCl 300:3000 ppm (1:10).
5. Penentuan panjang gelombang pengamatan kloramfenikol dan
lidokain HCl
Larutan baku kloramfenikol 300 ppm dan lidokain HCl 3000 ppm masing-masing ditotolkan sebanyak 1, 2 dan 3 µL pada pelat silika gel dengan jarak antar totolan 1 cm. Setelah totolan kering, pelat dikembangkan di dalam bejana kromatografi yang telah dijenuhi dengan fase gerak. Setelah mencapai jarak pengembangan 10 cm, pelat dikeluarkan, dan dikeringkan. Penentuan panjang gelombang pengamatan dilakukan dengan merekam pola spektra absorbsi masing-masing seri jumlah pada daerah panjang gelombang 200-400 nm menggunakan densitometer. Overlapping spektra kloramfenikol dan lidokain HCl ditentukan secara berturut-turut pada seri jumlah kloramfenikol 300, 600, 900 ng dan lidokain HCl 3000, 6000, 9000 ng.
6. Pembuatan kurva baku
Larutan baku tunggal kloramfenikol 300 ppm dan lidokain HCl 3000 ppm masing-masing ditotolkan dengan volume penotolan 1; 1,5; 2; 2,5; dan 3 µL pada pelat silika gel dengan jarak antar totolan 1 cm. Setelah totolan kering, pelat dikembangkan di dalam bejana kromatografi yang telah jenuh oleh fase gerak. Pelat dikeluarkan dari bejana setelah mencapai jarak pengembangan 10
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
27
cm, dikeringkan, dan diukur AUC-nya dengan densitometer pada panjang gelombang pengamatan. Replikasi dilakukan sebanyak 3 kali. Dibuat kurva baku hubungan antara jumlah analit (ng) dan AUC, sehingga didapatkan persamaan kurva baku masing-masing senyawa. Dipilih persamaan kurva baku yang memiliki nilai r > 0,999 untuk kloramfenikol dan lidokain HCl.
7. Penentuan recovery dan Koefisien Variasi (KV) baku tunggal
Larutan baku tunggal kloramfenikol 300 ppm dan lidokain HCl 3000 ppm masing-masing ditotolkan sebanyak 1, 2 dan 3 µL pada pelat silika gel dengan jarak antar totolan 1 cm. Setelah totolan kering, pelat dikembangkan dalam bejana kromatografi yang telah dijenuhi oleh fase gerak. Setelah mencapai jarak pengembangan 10 cm, pelat dikeluarkan, dikeringkan, dan discanning menggunakan densitometer pada panjang gelombang pengamatan. Nilai AUC yang didapat dimasukkan ke dalam persamaan kurva baku yang telah dibuat pada poin 5, sehingga didapatkan jumlah kloramfenikol dan lidokain HCl. Berdasarkan data yang diperoleh maka recovery dan KV-nya dapat dihitung. Replikasi dilakukan sebanyak 3 kali.
8. Penentuan recovery dan KV baku campuran kloramfenikol:lidokain
HCl 300:3000 ng, 600:6000 ng, dan 900:9000 ng
Larutan baku campuran kloramfenikol:lidokain HCl 1:10 ditotolkan sebanyak 1, 2, dan 3 µL pada pelat silika gel dengan jarak antar totolan 1 cm. Setelah totolan kering, pelat dikembangkan dalam bejana kromatografi yang telah dijenuhi oleh fase gerak. Setelah mencapai jarak pengembangan 10 cm, pelat dikeluarkan, dikeringkan, dan discanning menggunakan densitometer pada
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
28
panjang gelombang pengamatan. Nilai AUC yang didapat dimasukkan ke dalam persamaan kurva baku yang telah dibuat pada poin 5, sehingga didapatkan jumlah kloramfenikol dan lidokain HCl. Berdasarkan data yang diperoleh maka recovery dan KV-nya dapat dihitung. Replikasi dilakukan sebanyak 5 kali.
9. Penentuan recovery dan KV adisi baku dalam sampel
a. Penyiapan larutan stok sampel. Dua sampel obat tetes telinga Colme® dikeluarkan isinya dan dihomogenkan. Sebanyak 1 ml larutan sampel diambil dengan mikropipet, dimasukkan ke dalam labu takar 10 mL, dilarutkan dengan etanol sampai batas tanda, dan digojog agar homogen (LSA). Sebanyak 2 mL larutan sampel diambil dengan mikropipet, dimasukkan ke dalam labu takar 10 mL, dilarutkan dengan etanol sampai batas tanda, dan digojog agar homogen (LSB). Replikasi dilakukan sebanyak 5 kali.
b. Penyiapan larutan sampel tanpa penambahan baku kloramfenikol (LSK). Sebanyak 0,4 mL LSA diambil dengan mikropipet, dimasukkan ke dalam labu takar 10 mL, diencerkan dengan etanol sampai batas tanda, dan digojog agar homogen. Larutan ini siap untuk ditotolkan. Replikasi dilakukan sebanyak 5 kali.
c. Penyiapan larutan sampel tanpa penambahan baku lidokain HCl. (LSL). Sebanyak 2,5 mL LSB diambil dengam mikropipet, dimasukkan ke dalam labu takar 5 mL, diencerkan dengan etanol sampai batas tanda, dan digojog agar homogen. Larutan ini siap untuk ditotolkan. Replikasi dilakukan sebanyak 5 kali.
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
29
d. Penyiapan larutan sampel dengan penambahan baku kloramfenikol (LSAK). Sebanyak 0,4 mL LSA dan 2 mL larutan baku kloramfenikol 1000 ppm dimasukkan ke dalam labu takar 10 mL, diencerkan dengan etanol sampai batas tanda, dan digojog agar homogen. Larutan ini siap untuk ditotolkan. Replikasi dilakukan sebanyak 5 kali.
e. Penyiapan larutan sampel dengan penambahan baku lidokain HCl (LSAL). Sebanyak 5 mL LSB diambil dengan mikropipet, dimasukkan ke dalam labu takar 10 mL yang berisi 20 mg lidokain HCl, diencerkan dengan etanol sampai batas tanda, dan digojog agar homogen. Larutan ini siap untuk ditotolkan. Replikasi dilakukan sebanyak 5 kali.
f. Pengembangan dan pengukuran. LSK, LSL, LSAK, dan LSAL ditotolkan sebanyak 1 µL pada pelat silika gel dengan jarak antar totolan 1 cm. Setelah totolan kering, pelat dikembangkan dalam bejana kromatografi yang telah dijenuhi oleh fase gerak. Setelah mencapai jarak pengembangan 10 cm, pelat dikeluarkan, dikeringkan, dan discanning menggunakan densitometer pada panjang gelombang pengamatan. Nilai AUC yang didapat dimasukkan ke dalam persamaan kurva baku yang telah dibuat pada poin 5, sehingga didapatkan jumlah kloramfenikol dan lidokain HCl yang ditambahkan. Berdasarkan data yang diperoleh maka recovery dan KV-nya dapat dihitung.
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
30
G. Analisis hasil
1. Selektivitas
Selektivitas ditunjukkan dengan nilai resolusi > 1,5. Resolusi dapat dihitung dengan cara berikut:
(2) (Watson, 1999).
Keterangan :
RfA dan RfB = nilai Rf dari peak A dan B wA dan wB = lebar peak A dan B
2. Linearitas
Jumlah baku kloramfenikol dan lidokain HCl (ng) masing-masing diplotkan dengan AUC yang diperoleh, sehingga didapatkan persamaan kurva baku y = bx + a dan nilai koefisien korelasi (r). Suatu metode dapat dikatakan memiliki linearitas yang baik jika r > 0,999 (Mulja dan Hanwar, 2003).
3. Akurasi
Akurasi metode analisis dinyatakan dengan recovery yang dapat dihitung dengan cara berikut:
(3) (Harmita, 2004).
4. Akurasi adisi baku dalam matriks sampel
Nilai recovery adisi baku dalam matriks sampel dapat dihitung dengan cara berikut:
(4)
(Harmita, 2004).
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
31
5. Presisi
Presisi metode analisis dinyatakan dengan KV (koefisien variasi) yang dapat dihitung dengan cara berikut:
(5) (Harmita, 2004).
6. Range
Range merupakan interval jumlah analit yang memenuhi persyaratan linearitas, akurasi, dan presisi (The British Pharmacopoeia Commission, 2011).
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
32
BAB IV
HASIL DAN PEMBAHASAN
A. Pembuatan Fase Gerak
Fase gerak yang digunakan dalam penelitian ini adalah fase gerak yang telah didapat dari hasil optimasi pada penelitian sebelumnya, yaitu toluena:n-heksana:metanol:dietilamin (19,75:3,75:5:1,5) (Hernat, 2011). Fase gerak tersebut merupakan fase gerak yang dapat memisahkan kloramfenikol dan lidokain HCl secara optimal. Penggunaan dietilamin pada fase gerak bertujuan untuk memberikan suasana basa agar lidokain HCl dapat menjadi lidokain basa. Dietilamin memiliki pKb sebesar 2,9 (Quin, 2000). Penggunaan n-heksana bertujuan untuk menurunkan kepolaran dari campuran fase gerak, sedangkan toluena dan metanol berfungsi untuk mengelusi lidokain lebih cepat, sehingga pemisahan lidokain dan kloramfenikol dapat berlangsung dengan baik.
Fase gerak yang digunakan bersifat lebih non polar dengan indeks polaritasnya yaitu 2,53; sedangkan fase diam yang digunakan adalah silika gel yang bersifat lebih polar. Oleh karena itu sistem KLT yang digunakan adalah sistem KLT fase normal, di mana fase diam yang digunakan bersifat lebih polar dibandingkan dengan fase gerak yang digunakan.
B. Pembuatan Larutan Baku
Larutan baku yang dibuat adalah larutan baku kloramfenikol tunggal dan larutan baku lidokain HCl tunggal, serta larutan baku campuran
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
33
kloramfenikol:lidokain HCl. Pada penelitian ini, larutan baku tunggal yang akan ditotolkan adalah larutan baku kloramfenikol 300 ppm dan larutan baku lidokain HCl 3000 ppm, serta larutan baku campuran kloramfenikol:lidokain HCl dengan perbandingan 300:3000 ppm (1:10).
Perbandingan kloramfenikol:lidokain HCl 1:10 didapatkan dari hasil optimasi. Lidokain HCl memiliki perbandingan yang sangat besar dikarenakan
lidokain HCl memiliki =19, sehingga serapan lidokain HCl sangat kecil dan lidokain HCl harus dalam jumlah yang besar agar dapat terdeteksi, sedangkan
kloramfenikol memiliki =298, sehingga dengan jumlah yang kecil, kloramfenikol sudah dapat terdeteksi.
Di dalam penelitian ini tidak menggunakan seri konsentrasi tetapi menggunakan seri jumlah analit yang didapatkan dari volume penotolan yaitu 1; 1,5; 2; 2,5; dan 3 µL, sehingga didapatkan seri jumlah masing-masing analit, yaitu kloramfenikol adalah 300, 450, 600, 750, dan 900 ng, sedangkan untuk lidokain HCl adalah 3000, 4500, 6000, 7500, dan 9000 ng. Penggunaan seri jumlah analit akan mengurangi kesalahan dalam pengenceran apabila menggunakan seri konsentrasi dan proses preparasi larutan baku menjadi lebih singkat.
C. Penentuan Panjang Gelombang Pengamatan
Penentuan panjang gelombang pengamatan bertujuan untuk mengetahui panjang gelombang di mana kloramfenikol dan lidokain HCl dapat memberikan serapan yang optimal ketika dilakukan scanning secara bersamaan. Larutan yang
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
34
digunakan untuk menentukan panjang gelombang pengamatan adalah larutan baku kloramfenikol 300 ppm dan larutan baku lidokain HCl 3000 ppm dengan volume penotolan 1, 2, dan 3 µL. Penggunaan 3 volume totolan ini untuk mendapatkan jumlah analit pada level bawah, sedang, dan tinggi yang dapat mewakili kesulurahan jumlah analit pada seri jumlah analit yang digunakan. Pengukuran panjang gelombang pengamatan diukur pada rentang panjang gelombang 200-400 nm karena rentang tersebut merupakan rentang panjang gelombang daerah UV dan panjang gelombang teoritis dari kloramfenikol dan lidokain HCl berada pada rentang tersebut.
Suatu senyawa dapat diukur serapaannya pada daerah UV jika memiliki gugus kromofor dan auksokrom yang dapat menyerap radiasi sinar pada daerah UV. Pada densitometer, detektor yang digunakan adalah lampu D2 yang menghasilkan sinar UV, sehingga pengukuran panjang gelombang pengamatan dapat langsung dilakukan menggunakan densitometer. Berikut ini adalah gambar struktur kromofor dan auksokrom pada kloramfenikol dan lidokain.
Gambar 7. Gugus kromofor dan auksokrom pada kloramfenikol (A) dan lidokain (B) Panjang gelombang maksimum dapat diperoleh dengan melihat bentuk spektra kloramfenikol dan lidokain HCl. Perbedaan panjang gelombang yang
A B
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
35
didapatkan dari hasil penelitian dan panjang gelombang teoritis yang diperbolehkan adalah sebesar 2 nm (Direktorat Jendral pengawasan Obat dan Makanan RI, 1995). Panjang gelombang maksimum kloramfenikol yang didapatkan adalah 281 nm, sedangkan panjang gelombang maksimum kloramfenikol dalam air secara teoritis adalah 278 nm. Panjang gelombang maksimum lidokain HCl yang didapatkan adalah 263 nm, sama seperti panjang gelombang maksimum lidokain HCl dalam larutan asam secara teoritis. Adanya perbedaan sebesar 3 nm antara panjang gelombang maksimum kloramfenikol yang didapatkan dengan panjang gelombang teoritisnya disebabkan karena adanya perbedaan instrumen yang digunakan.
Panjang gelombang pengamatan didapatkan dengan menumpangtindihkan spektra kloramfenikol dan lidokain HCl seperti yang terlihat pada gambar 8. Panjang gelombang pengamatan yang didapatkan adalah sebesar 242 nm. Selanjutnya, panjang gelombang tersebutlah yang digunakan selama penelitian untuk mendapatkan serapan yang optimal dari kloramfenikol dan lidokain HCl ketika dilakukan scanning secara bersamaan menggunakan densitometer.
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
36
Gambar 8. Spektra kloramfenikol (300, 600, dan 900 ng) dan lidokain HCl (3000, 6000, dan 9000 ng)
D. Analisis Kualitatif
Pengamatan nilai Rf dilakukan di dalam penelitian ini berfungsi sebagai parameter analisis kualitatif untuk mengetahui ada tidaknya analit dalam sampel dengan membandingkan nilai Rf sampel dengan nilai Rf baku. Larutan yang digunakan adalah larutan baku tunggal kloramfenikol 300 ppm dan larutan baku tunggal lidokain HCl 3000 ppm yang masing-masing ditotolkan sebanyak 2 μL serta larutan sampel yang ditotolkan sebanyak 1 μL.
Preparasi dan penotolan sampel dilakukan sebanyak dua kali yaitu pada tahap pertama untuk melihat peak lidokain HCl, di mana jumlah lidokain berdasarkan perhitungan adalah 4000 ng, sedangkan kloramfenikol sebanyak
kloramfenikol Lidokain HCl
242 nm
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
37
10000 ng. Pada penotolan pertama ini, bercak kloramfenikol akan mengalami tailing setelah pengembangan karena jumlah kloramfenikol sangat banyak yang
membuat fase gerak tidak mampu membawa keseluruhan kloramfenikol, sehingga menyebabkan bercak kloramfenikol menjadi tailing. Pada tahap yang kedua bertujuan untuk melihat peak kloramfenikol, sehingga dilakukan pengenceran larutan sampel dan didapatkan jumlah kloramfenikol adalah 400 ng, sedangkan jumlah lidokain HCl adalah 160 ng. Pada penotolan yang kedua ini, bercak lidokain HCl tidak akan tampak setelah pengembangan karena jumlah lidokain HCl sangat kecil, sehingga lidokain HCl tidak akan terdeteksi ketika dilihat di bawah sinar UV. Berikut ini adalah gambar kromatogram sampel, baku lidokain HCl, dan baku kloramfenikol:
A
lidokain HCl
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
38
Gambar 9. Perbandingan nilai Rf baku kloramfenikol dan lidokain HCl dengan Rf sampel A.Rf lidokain HCl dalam sampel = 0,47
B.Rf baku lidokain HCl (3000 ng) = 0,47
C.Rf kloramfenikol dalam sampel = 0,25
D.Rf baku kloramfenikol (300 ng) = 0,25
B
kloramfenikol
C
kloramfenikol
lidokain HCl
D
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
39
Dari gambar 9.A dan 9.B dapat dilihat bahwa Rf sampel yaitu 0,47 sama dengan Rf baku lidokain HCl, sedangkan pada gambar 9.C dan 9.D dapat dilihat bahwa Rf sampel 0,25 sama seperti Rf baku kloramfenikol. Persamaan nilai Rf ini menunjukkan bahwa di dalam sampel benar terdapat kloramfenikol dan lidokain HCl.
Perbedaan nilai Rf kloramfenikol dan lidokain HCl dikarenakan adanya perbedaan afinitas masing-masing senyawa terhadap fase diam dan fase gerak. Berikut ini adalah gambar interaksi kloramfenikol dan lidokain HCl terhadap fase diam dan fase gerak:
Gambar 10. Interaksi kloramfenikol dengan fase diam silika gel - - - interaksi hidrogen
Gambar 11. Interaksi lidokain dengan fase diam silika gel - - - interaksi hidrogen
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
40
Gambar 12. Interaksi kloramfenikol dengan fase gerak toluena: n-heksana:metanol:dietilamin (19,75;3,75;5;1,5)
Gambar 13. Interaksi lidokain dengan fase gerak toluena:n-heksana:metanol:dietilamin(19,75;3,75;5;1,5)