BAB 2
TINJAUAN PUSTAKA
2.1. Uraian Tumbuhan
2.1.1. Klasifikasi tanaman kunyit (Curcuma longa L.)
Klasifikasi tanaman kunyit (Curcuma longa L.) menurut Hapsoh dan Rahmawati (2008) adalah sebagai berikut:
Kingdom : Plantae
Divisio : Spermatophyta
Sub-divisio : Angiospermae
Kelas : Monocotyledoneae
Bangsa : Zingiberales
Suku : Zingiberaceae
Marga : Curcuma
Jenis : Curcuma longa .L
Nama daerah dan nama asing
Nama daerah: kunyir, temu kuning (Jawa), koneng (Sunda), konyet, temu koneng
(Madura), hunik (Batak), kuminu (Ambon), kunidi (Sulawesi Utara), kurlai, tunin
(Maluku), rame, kandeifu (Irian), cekuh (Bali), dan humo poto (Gorontalo).
Nama asing: chiang huang (China), safron (India), turmeric (Inggris),
kurkuma (Italia), acafrao da India (Portugis) (Hapsoh dan Hasanah, 2011).
Morfologi tanaman kunyit (Curcuma longa .L)
Tanaman kunyit tumbuh berumpun dengan tinggi 40-100 cm. Batang merupakan
batang semu, tegak berbentuk bulat, tersusun dari pelepah daun. Daun tunggal,
menyirip dengan warna hijau pucat. Ujung dan pangkal daun runcing tepi daun
rata. Bunga majemuk berambut dan bersisik panjang 10-15 cm dengan mahkota
panjang sekitar 3 cm dan lebar 1,5 cm, berwarna putih/kekuningan. Kulit luar
rimpang berwarna jingga kecoklatan, daging buah merah jingga
kekuning-kuningan (Hapsoh dan Rahmawati, 2011).
Rimpang atau akar tinggal berbentuk bulat memanjang dan memiliki akar
serabut. Rimpang kunyit memiliki dua bagian tanaman yaitu rimpang induk (umbi
utama empu) dan tunas atau rimpang cabang. Rimpang utama ini biasanya
ditumbuhi tunas-tunas yang tumbuh ke arah samping. Jumlah tunas umumnya
banyak, tumbuh mendatar atau melengkung, serta berbuku-buku pendek, lurus
atau melengkung. Kulit rimpang berwarna jingga kecoklatan. Warna daging
jingga kekuningan dengan bau khas dan rasanya agak pahit. Rimpang cabang
akan berkembang secara terus-menerus membentuk cabang-cabang baru dan
batang semu sehingga pada akhirnya terbentuk rumpun (Nugroho, 1988).
2.1.2. Kandungan kimia
Rimpang kunyit mengandung minyak menguap sebanyak 3-5% v/v. Terdiri atas
turmeron, zingiberen, ar-turmeron, sedikit mengandung fellandren, seskiterpen
alkohol, borneol, kurkumin, desmetoksikurkumin, bisdesmetoksikurkumin, pati,
tanin dan damar (Dalimartha, 2009).
Dari segi kimia, C. domestica dicirikan oleh senyawa fenol turunan diarilheptanoid atau kurkuminoid dan senyawa seskuiterpen. Achmad, 2009
melaporkan bahwa dari rimpang Curcuma longa (sinonim C. domestica) ditemukan tiga zat warna fenol turunan diarilheptanoid atau kurkuminoid. Ketiga
senyawa fenol tersebut yang merupakan komponen fenol utama, maing-masing
adalah bisferuloilmetan atau kurkumin, 4-hidroksi-sinamoil feruloil metan atau
demetoksikurkumin dan bis(4-hidroksisinamoil)-metan atau
bisdemektoksikurkumin. Disamping itu, juga ditemukan suatu turunan
Dari C. longa(= C. domestica) selain kurkumin, demetoksi-kurkumin, dan bisdemetoksikurkumin telah ditemukan pula beberapa senyawa turunan
diarilheptanoid, yaitu 1,7-bis(4-hidroksi-3-metoksifenil)-1,4,6-heptatrien-3-on,
1-hidroki-3-metoksifenil)-6-hepten-3,5-dion,
1,7-bis(4-hidroksi-fenil)-1-hepten-3,5-dion, 1,7-bis(4-hidroksifenil)-1,4,6-heptatrien-3-on,
bersama-sama engan suatu ester ferulat yang disebut celebin A (Park, 2002 dalam buku
Achmad, 2009).
Dari C. longa juga ditemukan beberapa turunan kurkumin berupa homolog
dengan rantai-C9 yang diberi nama kurkumin I, kurkumin II, kurkumin III (Gorchakova, 1984 dan Ramsewak, 2000 dalam buku Achmad, 2009).
Selanjutnya, dari rimpang C. domestica diisolasi pula beberapa homolog
kurkumin dengan rantai C5, yaitu 1,5-bis (4-hidroksi-3-metoksifenil)-penta-(1E,4E)-1,4-dien-3-on dan
1-(4-hidroksi-3-metoksifenil)-5-(4-hidroksifenil)-penta-(1E,4E)-1,4-dien-3-on (Masuda, 1993 dan Park, 2002 dalam buku Achmad,
2009).
Kecuali senyawa kurkuminoid, ciri-ciri kimia lainnya tumbuhan kunyit C. domestica (sinonim C. longa) ialah senyawa seskuiterpen keton jenis bisabolen, seperti alpa-turmeron, beta-turmeron, kurlon, 4-hidroksibisabola-2, 10-dien-9-on,
bisakuron, 4-metoksi-5hiroksibisabola-2, 10-dien-9-on, 4,5-dihdroksibisabola-3,
10-dien, bersama-sama dengan alpa-kurkumen atau ar-kurkumen, beta-kurkumen,
gama-kurkumen, beta-seskuifelandren, zingiberen, beta-bisabolen, sebagai
kandungan utama (He, 1998 dalam Achmad, 2009).
Dari C. longa juga ditemukan beberapa senyawa sekuiterpen jenis germakran, seperti germakron-13-al, (4S,5S)-germakron-4,5-epoksida, kurdion,
dan dehidrokurdion (He, 1998 dalam buku Achmad, 2009).
Begitu pula, dari tumbuhan C. longa diperoleh beberapa senyawa seskuiterpen jenis guaian, seperti kurkumenol, prokurkumenol, isoprokurkumenol,
epiprokurkumenol, prokurkumadiol, dan zedoarondiol (He, 1998 dalam buku
Achmad, 2009).
kurzerenon, an jenis karabran, yaitu kurkumenon (He, 1998 dalam buku Achmad,
2009).
Menggunakan kombinasi teknik kromatografi gas (GC) dan kromatografi
gas-spektrometri massa (GC-MS), ternyata minyak atsiri yang berasal dari daun
tumbuhan kunyit C. domestica dan C. longa (= C. domestica) menganung pula beberapa senyawa monoterpen, antara lain yang utama ialah linalol,
alpa-felandren, 1,8-sineol, terpinolen, limonen, para-imen, alpa-pinen, beta-pinen,
kamfen, borneol, isoborneol, kamfor, dan suatu arilpropanoid eugenol (Dung,
1995 dalam buku Achmad, 2009).
2.1.3.Manfaat dan kegunaan kunyit
Rimpang kunyit digunakan sebagai bumbu dapur dan sebagai obat yang
berkhasiat sebagai antikoagulan, menurunkan tekanan darah tinggi, sebagai obat
malaria, obat cacing, bakterisida, obat sakit perut, peluruh ASI, fungisida,
stimulan, mengobati keseleo, memar, rematik, obat asma, diabetes melitus, usus
buntu, amandel, sariawan, tambah darah, menghilangkan jerawat, penurun panas,
menghilangkan rasa gatal, menyembuhkan kejang dan mengobati luka-luka
(Syukur dan Hernani, 2001).
Dilaporkan bahwa rimpang C. domestica banyak digunakan dan terdapat dalam semua ramuan obat traditional jamu. Tumbuhan ini, kecuali sebagai
rempah-rempah, juga digunakan untuk obat-obatan, seperti untuk pengobatan
penyakit kulit umumnya, pengobatan yang berhubhngan dengan saluran
pernapasan, sinusitis, asma, sebagai ekspektoran atau peluruh dahak, pengobatan
yang berhubungan saluran pencernaan, nyeri perut, infeksi saluran kencing,
diuretik atau peluruh kencing, bengkak, rematik, hepatitis, sakit mata, dan
pengobatan wanita sesudah melahirkan. Dilaporkan pula bahwa rimpang
tumbuhan ini, yang disediakan dalam bentuk bubuk, pasta, salep, obat gosok,
anemia, tekanan arah tinggi, penyakit kuning, dan disentri. Rimpang tumbuhan ini
juga digunakan untuk pengobatan diare, menstruasi yang tidak teratur,
tuberkulosis, radang gusi, di samping sebagai insektisida, fungisida, dan
nematisida (Achmad, 2009). Rimpang C. domestica terdaftar dalam Materia Medika Indonesia, Jilid I, Tahun 1977, dan digunakan sebagai kolagogum.
Di Cina, C. domestica juga resmi terdaftar dalam Farmakope Cina, dan digunakan sebagai analgesik yang menghilangkan nyeri, pengobatan menstruasi
yang tidak teratur, rematik, dan epilepsi (Achmad, 2009).
2.2. Lalat Buah (Bactrocersa sp)
Bactrocera sp merupakan spesies lalat buah yang paling melimpah di Bogor, Depok dan Jakarta selain B. papayae. Lalat buah ini selalu ada dan melimpah karena keberadaan tanaman inangnya. Selain menyerang jambu biji, lalat buah ini
menyerang berbagai macam buah-buahan antara lain belimbing, kluwih, cabai,
nangka, jambu bol, tomat, mangga, papaya (Siwi et al, 2006).
Klasifikasi dari lalat buah (Bactrocera sp)
Kingdom : Animalia
Phylum : Arthropoda
Kelas : Insecta
Ordo : Diptera
Famili : Tephritidae
Genus : Batrocera
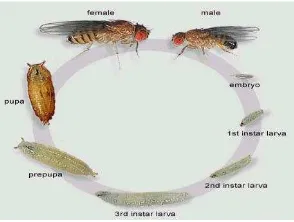
Gambar 2.1. Foto Bactrocera sp. hinggap pada buah jambu biji
Gambar 2.2. Foto daur hidup Bactrocera sp.
Lalat buah genus Bactrocera (Diptrea tephiritidae) merupakan spesies lalat buah yang hidup di daerah tropis dan telah tersebar hampir di seluruh
kawasan Asia-Pasifik (gambar 2.1. dan gambar 2.2.). Salah satu kawasan dengan
penyebaran lalat buah paling banyak ada di Asia Tenggara termasuk Indonesia
(Direktorat Bina Perlindungan Tanaman, 1995).
Menurut Ginting (2009) salah satu lalat jenis buah Bactrocera yang dengan
persebaran luas di Indonesia adalah Bactrocera sp, karena memiliki jenis tanaman inang yang sangat beragam dan hampir tersedia di sepanjang waktu. Bactrocera sp adalah jenis lalat buah yang mempunyai sifat polifag yaitu spesies yang memiliki banyak tanaman inang antara lain belimbing manis, belimbing wuluh,
2.3. Minyak Atsiri
Minyak atsiri dikenal juga dengan nama minyak eteris atau minyak terbang
(ethereal oil, volatile oil) dihasilkan oleh tanaman. Minyak tersebut mudah menguap pada suhu kamar tanpa mengalami dekomposisi, mempunyai rasa getir,
berbau wangi sesuai dengan bau tanaman penghasilnya, umumnya larut dalam
pelarut organik dan tidak larut dalam air (Ketaren, 1985).
2.3.1. Penggunaan dan aktivitas biologis minyak atisiri
Peranan paling utama dari minyak atsiri pada tumbuhan itu sendiri adalah sebagai
pengusir serangga (mencegah daun dan bunga rusak) serta sebagai pengusir
hewan-hewan pemakan daun lainnya (herbivora), bersifat antimikroba dan
menarik serangga membantu penyerbukan bunga (pollination) (Gunawan dan
Mulyani, 2004).
Minyak atsiri digunakan sebagai bahan baku dalam berbagai industri,
misalnya industri parfum, kosmetika, obat-obatan dan sebagai bahan penyedap
(flavoring agent) dalam industri makanan dan minuman (Guenther, 1987).
Pada konsentrasi tinggi, minyak atsiri dapat digunakan sebagai anastetik
lokal, misalnya minyak cengkeh yang digunakan untuk mengatasi sakit gigi, tetapi
dapat merusak selaput lendir. Beberapa minyak atsiri juga digunakan sebagai
emenagogue (pelancar haid) dan abortivum seperti minyak atsiri dari kayu manis (Cinnamomum burmanii), pala (Myristica fragrans). Kebanyakan minyak atsiri juga bersifat antibakteri dan antijamur yang kuat. Minyak daun sirih (Piper betle) adalah salah satu minyak atsiri yang bersifat sebagai antibakteri. Minyak ini dapat
menghambat pertumbuhan beberapa jenis bakteri patogen seperti Escherichia coli, Salmonella sp, Staphylococcus aureus, Klebsiella dan Pasteurella (Agusta, 2000).
Disamping bersifat antibakteri, minyak atsiri juga memiliki sifat
antioksidan dimana pada minyak atsiri tersebut ditemukan adanya senyawa
golongan fenol (Ginting, dkk. 2016).
2.3.2. Komposisi kimia minyak atsiri
Minyak atsiri umumnya terjadi dari berbagai campuran persenyawaan kimia yang
terbentuk dari unsur karbon (C), hidrogen (H) dan oksigen (O) serta beberapa
persenyawaan kimia yang mengandung unsur Nitrogen dan Belerang. Komponen
utama minyak atsiri adalah terpena dan turunan terpena yang mengandung atom
oksigen. Terpenoid merupakan senyawa yang berada pada jumlah cukup besar
pada tanaman. Terpenoid yang terkandung dalam minyak atsiri menimbulkan bau
harum atau bau khas dari tanaman. Secara kimia, terpena minyak atsiri
digolongkan menjadi dua bagian yaitu monoterpenoid dan seskuiterpenoid.
Beberapa contoh monoterpenoid antara lain geraniol, limonena, kamfor, mentol
dan lain-lain. Yang termasuk seskuiterpenoid antara lain kariofilen dan santonin.
Secara ekonomi senyawa terpena tersebut penting sebagai dasar
wewangian alam dan juga untuk remph-rempah serta sebagai senyawa cita rasa
dalam industri makanan. Terpena juga sering kali terdapat dalam fraksi yang
berbau, bersama-sama dengan senyawa aromatik seperti finilpropanoid. Selain
terpena, minyak atsiri juga banyak mengandung senyawa turunan benzena seperti
Eugenol, Kumarin, Sinamaldehid dan lain-lain.
Pada umumnya perbedaan komposisi minyak atsiri disebabkan perbedaan
jenis tanaman penghasil, kondisi iklim, tanah tempat tumbuh, umur panen, metode
ekstraksi yang digunakan dan cara penyimpanan minyak (Ketaren, 1985).
Minyak atsiri biasanya merupakan campuran beberapa senyawa kimia
yang terbentuk dari unsur Karbon (C), Hidrogen (H) dan Oksigen (O). Pada
umumnya komponen kimia minyak atsiri dibagi menjadi dua golongan yaitu:
1) Hidrokarbon, yang terutama terdiri dari persenyawaan terpen dan
a. Golongan hidrokarbon
Persenyawaan yang termasuk golongan ini terbentuk dari unsur Karbon (C)
dan Hidrogen (H). Jenis hidrokarbon yang terdapat dalam minyak atsiri
sebagian besar terdiri dari monoterpen (2 unit isopren), sesquiterpen (3 unit
isopren), dan fenilpropana.
b. Golongan hidrokarbon teroksigenasi
Komponen kimia dari golongan persenyawaan ini terbentuk dari unsur Karbon
(C), Hidrogen (H) dan Oksigen (O). Persenyawaan yang termasuk dalam
golongan ini adalah persenyawaan alkohol, aldehid, keton, ester, eter dan fenol.
Senyawa terpen teroksigenasi dapat terdiri dari monoterpen, seskiterpen
dan fenilpropana. Senyawa terpen mempunyai aroma kurang wangi, sukar larut
dalam alkohol encer dan jika disimpan dalam waktu lama akan membentuk resin.
Golongan hidrokarbon teroksigenasi merupakan senyawa penting dalam minyak
atsiri karena mempunyai aroma yang lebih wangi. Fraksi terpen dapat dipisahkan
untuk tujuan tertentu, misalnya untuk pembuatan parfum (Ketaren, 1985).
2.3.3. Biosintesis minyak atsiri
Berdasarkan proses biosintesisnya atau pembentukan komponen minyak atsiri di
dalam tumbuhan, minyak atsiri dapat dibedakan menjadi dua golongan, Golongan
pertama adalah turunan terpena yang terbentuk dari asam asetat melalui jalur
biosintesis asam mevalonat. Golongan kedua adalah senyawa aromatik yang
terbentuk dari biosintesis asam siklamat melalui jalur fenil propanoid (Agusta,
2000). Mekanisme dari tahap-tahap reaksi biosintesis terpenoid yaitu asam asetat
yang telah diaktifkan oleh koenzim A melakukan kondensasi jenis Clasein
menghasilkan asam asetoasetat.
Senyawa yang dihasilkan ini dengan asetil koenzim A melakukan
ditemukan pada asam mevalonat. Reaksi-reaksi berikutnya ialah fosforilasi,
eliminasi asam fosfat dan dekarboksolasi menghasilkan IPP (isopentenil
pirofosfat) yang selanjutnya berisomerisasi menjadi DMAPP (dimetil alil
pirofosfat) oleh enzim isomerase. IPP sebagai unit merupakan langkah pertama
dari polimerisasi isoterpen untuk menghasilkan terpenoid. Penggabungan ini
terjadi karena serangan elekron diikuti oleh penyingkiran ion pirofosfat. Serangan
ini menghasilkan geranil pirofosfat (GPP) yakni senyawa antara bagi semua
senyawa monoterpen.
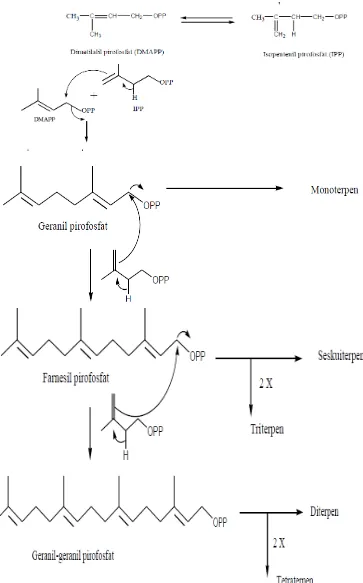
Sintesa terpenoid sangat sederhana sifatnya. Ditinjau dari segi teori reaksi
organik sintesa ini hanya menggunakan beberapa jenis reaksi dasar. Reaksi-reaksi
selanjutnya dari senyawa antara GPP, FPP, GGPP untuk menghasilkan senyawa-senyawa
terpenoid satu per satu hanya melibatkan beberapa jenis reaksi sekunder pula.
Reaksi-reaksi sekunder ini lazimnya adalah hidrolisis, siklisasi, oksidasi, reduksi, dan Reaksi-
reaksi-reaksi spontan yang dapat berlangsung dengan mudah dalam suasana netral dan pada
suhu kamar, seperti isomerisasi, dehidrasi ,dekarbosilasi dan sebagainya, dapat dilihat
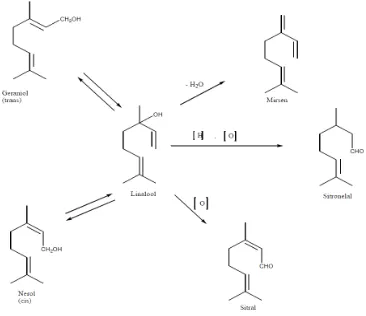
Untuk menjelaskan dapat diambil beberapa contoh monoterpen. Dari segi
biogenetik, perubahan geraniol, nerol dan linalool dari yang satu menjadi yang
lain berlangsung sebagai akibat reaksi isomerisasi. Ketiga alkohol ini, yang
berasal dari hidrolisis geranil pirofosfat (GPP) dapat menjalani reaksi-reaksi
sekunder berikut, misalnya dehidrasi menghasilkan mirsena, oksidasi menjadi
sitral dan oksidasi reduksi menghasilkan sitronelal. Berikut ini adalah contoh
perubahan senyawa monoterpen, dapat dilihat pada gambar 2.4.
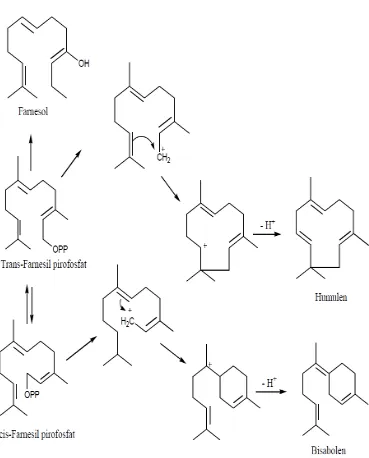
Senyawa- senyawa seskuiterpen diturunkan dari cis-farnesil pirofosfat dan
trans- farnesil pirofosfat melalui reaksi siklisasi dan reaksi sekunder lainnya.
Kedua isomer farnesil pirofosfat ini dihasilkan in vivo melalui mekanisme yang
sama seperti isomerisasi antara geraniol dan nerol. Perubahan farnesil pirofosfat
menjadi seskuiterpen terlihat pada gambar 2.5.
2.3.4. Cara Isolasi Minyak Atsiri
Isolasi minyak atsiri dapat dilakukan dengan metode penyulingan (distilation). Metode penyulingan minyak atsiri terbagi atas tiga bagian, yaitu:
a. Penyulingan dengan air
Pada metode ini, bahan tanaman yang akan disuling mengalami kontak langsung
dengan air mendidih. Bahan dapat mengapung diatas air atau terendam secara
sempurna, tergantung pada berat jenis dan jumlah bahan yang disuling. Ciri khas
model ini yaitu adanya kontak langsung antara bahan dan air mendidih. Oleh
karena itu, sering disebut dengan penyulingan langsung.
Penyulingan dengan cara langsung ini dapat menyebabkan banyaknya
rendemen minyak yang hilang (tidak tersuling) dan terjadi pula penurunan mutu
minyak yang diperoleh.
b. Penyulingan dengan uap
Model ini disebut juga penyulingan uap atau penyulingan tak langsung. Pada
prinsipnya, model ini sama dengan penyulingan langsung. Hanya saja, air
penghasil uap tidak diisikan bersama-sama dalam ketel penyulingan. Uap yang
digunakan berupa uap jenuh atau uap kelewat panas dengan tekanan lebih dari 1
atmosfer.
c. Penyulingan dengan air dan uap
Pada model penyulingan ini, bahan tanaman yang akan disuling diletakkan di atas
rak-rak atau saringan berlubang. Kemudian ketel penyulingan diisi dengan air
sampai permukaannya tidak jauh dari bagian bawah saringan. Ciri khas model ini
yaitu uap selalu dalam keadaan basah, jenuh dan tidak terlalu panas. Bahan
tanaman yang akan disuling hanya berhubungan dengan uap dan tidak dengan air
2.4. Sifat Fisikokimia Minyak Atsiri
Analisis fisikokimia dilakukan untuk mendeteksi pemalsuan, mengevaluasi mutu
dan kemurnian minyak serta mengidentifikasi jenis dan kegunaannya (Gunawan
dan Mulyani, 2004).
Minyak atsiri mempunyai konstituen kimia yang berbeda, tetapi dari segi
fisikanya banyak yang sama. Minyak atsiri yang baru diekstraksi (masih segar)
umumnya tidak berwarna atau berwarna kekuning-kuningan. Sifat-sifat fisika
yang penting dari minyak atsiri, yaitu: berat jenis, mempunyai indeks bias yang
tinggi serta rotasi optik (Koensoemardiyah, 2010).
Parameter yang dapat digunakan untuk tetapan fisik minyak atsiri antara lain:
2.4.1. Berat jenis
Penentuan bobot jenis menggunakan alat piknometer, Bobot jenis minyak atsiri
merupakan perbandingan antara bobot minyak dengan bobot air pada volume air
yang sama dengan volume minyak. Bobot jenis merupakan salah satu kriteria
paling penting dalam menentukan mutu dan kemurnian minyak atsiri (Guenther,
1987).
2.4.2. Indeks bias
Penentuan indeks bias menggunakan alat refraktometer. Indeks bias merupakan
perbandingan antara kecepatan cahaya di dalam udara dengan kecepatan cahaya di
dalam zat tersebut pada suhu tertentu. Indeks bias berguna untuk identifikasi
kemurnian (Guenther, 1987).
2.4.3. Putaran optik
Penentuan putaran optik menggunakan alat polarimeter. Setiap jenis minyak atsiri
kiri. Besarnya perputaran bidang polarisasi ditentukan oleh jenis minyak atsiri,
suhu, panjang kolom yang berisi minyak atsiri dan panjang gelombang cahaya
yang digunakan (Guenther, 1987).
2.5. GC-MS
Analisis dan karakterisasi komponen minyak atsiri merupakan masalah yang
cukup rumit, dikarenakan minyak atsiri mempunyai sifat yang mudah menguap
pada suhu kamar. Kendala yang umumnya dialami saat menganilis komponen
minyak atsiri adalah hilangnya sebagian komponen selama proses preparatif dan
selama berlangsungnya proses analisis. Setelah ditemukan kromatografi gas (GC),
kendala dalam analisis komponen minyak atsiri dapat diatasi. Pada penggunaan
GC ini, efek penguapan dapat dihindari bahkan dihilangkan sama sekali.
Perkembangan teknologi instrumentasi yang sangat pesat melahirkan suatu alat
yang merupakan gabungan dua sistem yang saling menguntungkan, yaitu
gabungan antara kromatografi gas dan spektrofotometri massa (Agusta, 2000).
Pada alat GC-MS, kedua alat dihubungkan. Kromatografi gas disini
berfungsi sebagai alat pemisah berbagai komponen campuran dalam sampel,
sedangkan spektrometer massa berfungsi untuk mendeteksi masing-masing
molekul komponen yang telah dipisahkan pada sistem kromatografi gas. Analisis
dengan GC-MS merupakan metode yang cepat dan akurat untuk menganalisis
senyawa dalam jumlah sangat kecil dan menghasilkan data yang berguna
2.5.1. Kromatografi gas
Kromatografi gas (KG) merupakan metode untuk pemisahan dan deteksi
senyawa-senyawa organik yang mudah menguap dan senyawa-senyawa gas
anorganik dalam suatu campuran. Kegunaan umum dari kromatografi gas adalah
untuk : melakukan pemisahan dan identifikasi semua jenis senyawa-senyawa
organik yang mudah menguap dan juga untuk melakukan analisis kualitatif dan
kuantitatif senyawa dalam suatu campuran.
Ada 2 Jenis kromatografi gas:
1. Kromatografi gas-cair (KGC)
Pada kromatografi ini, fase diam yang digunakan adalah cairan yang diikatkan
pada suatu zat pendukung sehingga solut akan terlarut dalam fase diam sehingga
mekanisme sorpsi-nya adalah partisi. 2. Kromatografi gas-padat
Pada kromatografi ini, digunakan fase diam padatan. Mekanisme sorpsi-nya adalah adsorpsi permukaan (Rohman, 2007).
Kromatografi gas digunakan untuk memisahkan komponen campuran
kimia dalam suatu bahan berdasarkan perbedaan polaritas campuran. Fase gerak
akan membawa campuran menuju kolom. Campuran dalam fase gerak akan
berinteraksi dengan fase diam. Setiap komponen yang terdapat dalam campuran
berinteraksi dengan kecepatan yang berbeda, dimana interaksi komponen dengan
fase diam dengan waktu yang paling cepat akan keluar pertama dari kolom dan
yang paling lambat akan keluar paling akhir (Eaton, 1998).
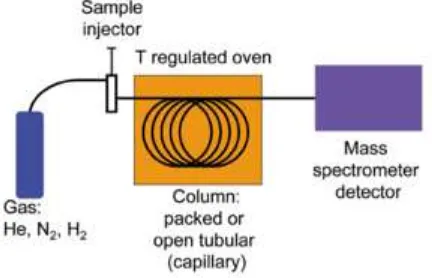
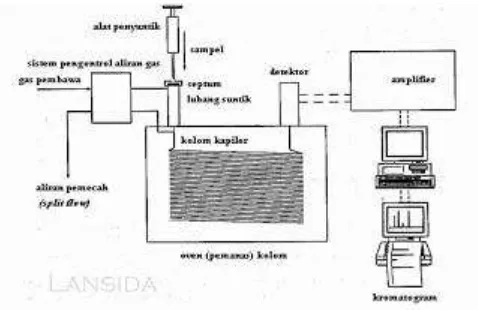
Bagian utama dari kromatografi gas adalah gas pembawa, sistem injeksi,
Gambar 2.7. Diagram blok sistem kromatografi gas secara umum (Gandjar dan
Rohman, 2007)
Gas pembawa
Gas pembawa harus memenuhi persyaratan antara lain harus inert, murni dan
mudah diperoleh. Pemilihan gas pembawa tergantung pada detektor yang dipakai.
Keuntungannya adalah semua gas ini harus tidak reaktif, dapat dibeli dalam
keadaan murni dan kering yang dapat dikemas dalam tangki bertekanan tinggi.
Gas pembawa yang sering dipakai adalah Helium (He), Argon (Ar), Nitrogen (N),
Hidrogen (H) dan karbon dioksida (CO2).
Sistem injeksi
Sampel yang akan dikromatografi dimasukkan kedalam ruang suntik, melalui
gerbang suntik, biasanya berupa lubang yang ditutup septum atau pemisah karet.
Ruang suntik harus dipanaskan tersendiri (terpisah dari kolom) pada suhu
10-15°C lebih tinggi dari suhu kolom maksimum. Jadi seluruh sampel akan menguap
Kolom
Kolom merupakan tempat terjadinya proses pemisahan karena didalamnya
terdapat fase diam. Ada 2 jenis kolom pada kromatografi gas yaitu kolom kemas
dan kolom kapiler
Kolom kemas adalah pipa yang terbuat dari logam, kaca atau plastik berisi
penyangga padat yang inert. Fase diam, berwujud padat maupun cair diserap atau
terikat secara kimia pada permukaan penyangga padat tersebut.
Kolom kapiler banyak digunakan untuk menganalisi komponen minyak
atsiri. Hal ini disebabkan oleh kelebihan kolom tersebut yang memberikan hasil
analisis dengan daya pisah tinggi dan sekaligus memiliki sensitivitas yang tinggi.
Bahan kolom biasanya dari gelas baja tahan karat atau silika. Fase cair berupa
lapisan film dilapiskan pada dinding kolom bagian dalam (Agusta, 2000).
Fase diam
Fase diam disapukan dalam permukaan medium atau dilapiskan pada dinding
kapiler. Fase diam yang umum digunakan pada kolom adalah fase diam padat dan
fase diam cair, akan tetapi pada kolom kapiler lebih banyak digunakan (Agusta,
2000).
Fase diam dibedakan berdasarkan kepolarannya, yaitu non polar, sedikit
polar, semi polar, dan sangat polar. Sifat minyak atsiri yang nonpolar sampai
sedikit polar, sebaiknya digunakan kolom dengan fase diam yang sedikit polar,
misalnya CBP-5, CBJ-5, SE-2 dan SE-54. Jika digunakan kolom yang lebih polar,
sejumlah puncak yang dihasilkan menjadi lebar (tidak tajam) dan sebagian
puncaknya membentuk ekor, garis dasarnya tidak rata dan terlihat bergelombang.
Bahkan kemungkinan komponen yang bersifat non polar tidak terdeteksi sama
Suhu
Suhu merupakan salah satu faktor utama yang menentukan hasil analisis
kromatografi gas dan spektrometri massa. Umumnya yang sangat menentukan
adalah pengaturan suhu injektor dan kolom (Agusta, 2000).
Pemisahan pada Kromatografi Gas dapat dilakukan pada suhu yang tetap biasanya
disebut dengan pemisahan isotermal, dapat dilakukan dengan menggunakan suhu
yang berubah secara terkendali disebut pemisahan dengan suhu terprogram.
Pemisahan isotermal paling baik dipakai pada analisis rutin. Ada dua hal yang
harus diperhatikan terkait dengan pemisahan isotermal, yaitu:
1) jika suhu terlalu tinggi maka komponen akan terelusi tanpa terpisah, sementara
jika suhu terlalu rendah maka komponen yang bertitik didih tinggi akan keluar
sangat lambat bahkan tetap tertinggal didalam kolom.
2) terkait masalah diatas pemisahan dapat dilakukan dengan suhu terprogram.
Pemisahan dengan suhu terprogram mempunyai keuntungan, yakni mampu
meningkatkan resolusi komponen dalam suatu campuran, mempunyai titik didih
pada kisaran yang agak luas. Pemograman suhu dilakukan dengan menaikkan
suhu dari suhu tertentu ke suhu berikutnya dan terkendali dalam waktu tertentu
(Rohman, 2007).
Detektor
Komponen utama lainnya di kromatografi gas adalah detektor. Detektor
merupakan perangkat yang diletakkan pada ujung kolom tempat keluar fase gerak
yang membawa komponen hasil pemisahan. Detektor pada kromatografi gas
adalah suatu sensor elektronik yang berfungsi mengubah sinyal gas pembawa dan
komponen-komponen didalamnya menjadi sinyal elektronik. Sinyal elektronik
komponen-komponen yang terpisah di antara fase diam dan fase gerak (Rohman,
2007).
2.5.2. Spektrometri Massa
Suatu spektrometer massa bekerja dengan menghasilkan molekul- molekul
bermuatan atau fragmen-fragmen dalam keadaan sangat hampa atau segera
sebelum sampel memasuki ruang sangat hampa (Watson, 2010).
Molekul senyawa organik pada spektrometer massa, ditembak dengan
berkas elektron bernergi tinggi dan menghasilkan ion bermuatan positif yang
mempunyai energi yang tinggi karena lepasnya elektron dari molekul yang dapat
pecah menjadi ion-ion yang lebih kecil (Sastrohamidjojo, 2004)
Menurut Dachriyanus (2004), spektrometer massa pada umumnya
digunakan untuk:
1. Menentukan massa molekul (berat molekul).
2. Menentukan rumus molekul dengan menggunakan Spektrum Massa Beresolusi
Tinggi (High Resolution Mass Spectra).
Spektrum massa hasil analisis sistem spektroskopi massa merupakan
gambaran mengenai jenis dan jumlah fragmen molekul yang terbentuk dari suatu
komponen kimia (masing-masing puncak pada kromatogram). Setiap fragmen
yang terbentuk dari pemecahan suatu komponen kimia memiliki berat molekul
yang berbeda dan ditampilkan dalam bentuk diagram dua dimensi, m/z (m/e,
massa/muatan) pada sumbu X dan intensitas pada sumbu Y yang disebut dengan
spektrum massa. Pola pemecahan (fragmentasi) molekul yang terbentuk untuk
setiap komponen kimia sangat spesifik sehingga dapat dijadikan sebagai patokan
untuk menentukan struktur molekul suatu komponen kimia. Selanjutnya,
spektrum massa komponen kimia yang diperoleh dari hasil analisis diidentifikasi
dengan cara dibandingkan dengan spektrum massa yang terdapat dalam suatu
bank data (Agusta, 2000).
Keuntungan utama spektrometri massa sebagai metode analisis yaitu
diketahui atau untuk menetapkan keberadaan senyawa tertentu, hal ini disebabkan
adanya pola fragmentasi yang khas sehingga dapat memberikan informasi
mengenai bobot molekul dan rumus molekul. Puncak ion molekul penting
dikenali karena memberikan bobot molekul senyawa yang diperiksa. Puncak
tertinggi pada spektrum disebut puncak dasar (base peak), dinyatakan dengan nilai 100% dan kekuatan puncak lain, termasuk puncak ion molekulnya
dinyatakan sebagai persentase puncak dasar tersebut (Silverstein, dkk., 1986).
2.6. Pestisida
Pestisida adalah substannsi (zat kimia) yang digunakan untuk membunuh atau
mengendalikan berbagai hama. Berdasarkan asal katanya pestisida berasal dari bahasa Inggris yaitu “pest” berarti hama dan “cida” berarti pembunuh (Djojosumarto,2008).
Asosiasi Kimia Nasional Amerika Serikat menyatakan, bahwa yang juga
termasuk pengertian pestisida ialah agensia yang dipergunakan untuk
keperluan-keperluan khusus seperti zat pengatur tumbuh, zat penggugur daun, zat pengering
dan zat-zat lainnya yang sejenis feromon, zat kimia pemandul, zat anti feedant,
atraktan, repelen, sinergis (Oka dan Ida Nyoman, 1993).
2.6.1. Penggolongan Pestisida
Pestisida mempunyai sifat-sifat fisik, kimia dan daya kerja yang berbeda-beda,
karena itu dikenal banyak macam pestisida. Pestisida dapat digolongkan menurut
berbagai cara tergantung pada kepentingannya, antara lain: berdasarkan sasaran
yang akan dikendalikan, berdasarkan cara kerja, berdasarkan struktur kimianya,
asal dan sifat kimia, berdasarkan bentuknya dan pengaruh fisiologisnya.
A. Berdasarkan asal bahan yang digunakan untuk membuat pestisida, yaitu :
2. Pestisida Nabati, yaitu pestisida yang berasal dari tumbuh-tumbuhan,
contoh: neem oil yang berasal dari pohon mimba.
3. Pestisida Biologi, yaitu pestisida yang berasal dari jasad renik atau
mikrobia, contoh: jamur, bakteri atau virus.
4. Pestisida Alami, yaitu pestisida yang berasal dari bahan alami, contoh:
bubur bordeaux (Jimenez, 2007).
B. Penggolongan pestisida berdasarkan sasaran, yaitu:
1. Insektisida adalah bahan yang mengandung senyawa kimia yang bisa
mematikan semua jenis serangga.
2. Fungisida adalah bahan yang mengandung senyawa kimia beracun dan
bisa digunakan untuk memberantas dan mencegah fungi/cendawan.
3. Bakterisida. Disebut bakterisida karena senyawa ini mengandung bahan
aktif beracun yang bisa membunuh bakteri.
4. Nermatisida, digunakan untuk mengendalikan nematoda.
5. Akarisida atau mitisida adalah bahan yang mengandung senyawa kimia
yang digunakan untuk membunuh tungau, caplak, dan laba-laba.
6. Rodenstisida adalah bahan yang mengandung senyawa kimia beracun
yang digunakan untuk mematikan berbagai jenis binatang pengerat,
misalnya tikus.
7. Moluskisida adalah pestisida untuk membunuh moluska, yaitu siput,
bekicot serta tripisan yang banyak dijumpai di tambak.
8. Herbisida adalah senyawa kimia beracun yang dimanfaatkan untuk
membunuh tumbuhan pengganggu yang disebut gulma.
9. Pestisida lain seperti Pisida, Algisida, Advisida dan lain-lain.
10.Pestisida berperan ganda yaitu pestisida yang berperan untuk membasmi 2
C. Berdasarkan sifat dan cara kerja racun pestisida, yaitu:
1. Racun kontak
Pestisida jenis ini bekerja dengan masuk ke dalam tubuh serangga lewat
kulit (kutikula) dan di transportasikan ke bagian tubuh serangga tempat
pestisida aktif bekerja.
2. Racun pernafasan (Fumigan)
Pestisida jenis ini dapat membunuh serangga dengan bekerja lewat sistem
pernafasan.
3. Racun lambung
Jenis pestisida yang membunuh serangga sasaran jika termakan serta
masuk ke dalam organ penccernaannya.
4. Racun Sistematik
Cara kerja seperti ini dapat dimiliki oleh insektisida, fungisida, dan
herbisida. Racun sistemik disemprotkan atau ditebarkan pada bagian
tanaman akan terserap ke dalam jaringan tanaman melalui akar atau daun,
sehingga dapat membunuh hama yang berada di dalam jaringan tanaman
seperti jamur dan bakteri. Pada insektisida sistemik, serangga akan mati
setelah memakan atau menghisap cairan tanaman yang telah disemprot.
5. Racun metabolisme
Pestisida ini membunuh serangga dengan mengintervensi proses
metabolismenya.
6. Racun protoplasma
Ini akan mengganggu fungsi sel karena protoplasma sel menjadi rusak
(Djojosumarto, 2008).
D. Berdasarkan bentuk formulasi pestisida
Formulasi pestisida yang dipasarkan terdiri atas bahan pokok yang disebut bahan
1. Tepung hembus, debu (dust = D )
Bentuknya tepung kering yang hanya terdiri atas bahan aktif, misalnya
belerang atau dicampur dengan pelarut aktif, kandungan bahan aktifnya
rendah sekitar 2-10%. Dalam penggunaannya pestisida ini harus
dihembuskan menggunakan alat khusus yang disebut duster.
2. Butiran (granula = G) Pestisida ini berbentuk butiran padat yang
merupakan campuran bahan aktif berbentuk cair dengan butiran yang
mudah menyerap, bagian luarnya ditutup dengan suatu lapisan.
3. Tepung yang dapat disuspensikan dalam air (wettable powder = WP) Pestisida berbentuk tepung kering agak pekat ini belum bisa secara
langsung digunakan untuk memberantas jasad sasaran, harus terlebih
dahulu dibasahi air. Hasil campurannya dengan air disebut suspensi.
Pestisida jenis ini tidak larut dalam air, melainkan hanya tercampur saja.
Oleh karena itu, sewaktu disemprotkan harus sering diaduk atau tangki
penyemprotnya digoyang-goyang.
4. Tepung yang larut dalam air (water-sofable powder= SP) Pestisida berbentuk SP ini sepintas mirip WP. Penggunaanya pun ditambahkan air.
Perbedaannya terletak pada kelarutannya. Bila WP tidak bisa terlarut
dalam air, SP bisa larut dalam air. Larutan ini jarang sekali mengendap,
maka dalam penggunaannya dengan penyemprotan, pengadukan hanya
dilakukan sekali pada waktu pencampuran.
5. Suspensi (flowable concentrate = F)
Formulasi ini merupakan campuran bahan aktif yang ditambah pelarut
serbuk yang dicampur dengan sejumlah kecil air. Hasilnya adalah seperti
pasta yang disebut campuran basah. Campuran ini dapat tercampur air
dengan baik dan mempunyai sifat yang serupa dengan formulasi WP yang
ditambah sedikit air.
6. Cairan (emulsifiable concentrare = EC)
Bentuk pestisida ini adalah cairan pekat yang terdiri dari campuran bahan
dicampur dengan bahan pelarut berupa air. Hasil pengencerannya atau
cairan semprotnya disebut emulsi.
7. Solution (S)
Solution merupakan formulasi yang dibuat dengan melarutkan pestisida ke
dalam pelarut organik dan dapat digunakan dalam pengendalian jasad
pengganggu secara langsung tanpa perlu dicampur dengan bahan lain.
Formulasi ini hampir tidak ditemui (Wudianto, 2010).
E. Berdasarkan bahan aktifnya
Penggunaan pestisida yang paling banyak dan luas berkisar pada satu diantara
empat kelompok besar berikut yaitu :
1. Organoklorin
Organoklorin merupakan racun terhadap susunan saraf (neuro toxins) yang merangsang sistem saraf baik pada serangga maupun mamalia,
menyebabkan tremor dan kejang-kejang.
2. Organofosfat
umumnya adalah racun pembasmi serangga yang paling toksik secara akut
terhadap binatang bertulang belakang seperti ikan, burung, kadal (cicak)
dan mamalia), mengganggu pergerakan otot dan dapat menyebabkan
kelumpuhan. Organofosfat dapat menghambat aktifitas dari cholinesterase,
suatu enzim yang mempunyai peranan penting pada transmisi dari signal
saraf.
3. Karbamat
Sama dengan organofosfat, pestisida jenis karbamat menghambat
enzim-enzim tertentu, terutama cholinesterase dan mungkin dapat memperkuat
efek toksik dari efek bahan racun lain. Karbamat pada dasarnya
mengalami proses penguraian yang sama pada tanaman, serangga dan
mamalia. Pada mamalia karbamat dengan cepat diekskresikan dan tidak
terbio konsentrasi namun bio konsentrasi terjadi pada ikan.
ester yang disebut pyretrin yang diektraksi dari bunga dari genus
Chrysantemum. Jenis pyretroid yang relatif stabil terhadap sinar matahari adalah : deltametrin, permetrin, fenvlerate. Sedangkan yang tidak stabil
terhadap sinar matahari dan sangat beracun bagi serangga adalah : difetrin,
sipermetrin, fluvalinate, siflutrin, fenpropatrin, tralometrin, sihalometrin,
flusitrinate. Piretrum mempunyai toksisitas rendah pada manusia tetapi
menimbulkan alergi pada orang yang peka, dan mempunyai keunggulan
diantaranya: diaplikasikan dengan takaran yang relatif sedikit, spekrum
pengendaliannya luas, tidak persisten, dan memiliki efek melumpuhkan
yang sangat baik (Kusnoputranto, 1996).
F. Berdasarkan Jarak/Frekuensi Penyemprotan Pestisida Sesuai Golongan
1. Golongan0Organofosfat
Berdasarkan masa degradasinya dalam lingkungan yaitu sekitar 2 minggu
maka frekuensi/jarak penyemprotan golongan ini adalah 2 minggu sekali
2. Golongano0Karbamat
Golongan ini hampir sama dengan organofosfat, dimana golongan ini juga
tidak persisten, mulai banyak dipasaran. Masa degradasi di lingkungan
hampir sama dengan organofosfat yaitu sekitar 12-14 hari, oleh karena itu
maka frekuensi penyemprotannya berkisar 12-14 hari.
3. Golongano0Piretroid
Dibandingkan dua golongan diatas, golongan Piretroid yang paling baru.
Golongan Piretroid memiliki beberapa keunggulan, diantaranya
diaplikasikan dengan takaran relatif sedikit, spektrum pengendaliannya
luas, tidak persisten, dan memiliki efek melumpuhkan (knock down effect) yang sangat baik, masa terdegradasi dalam lingkungan juga singkat,
berkisar antara 10-12 hari, jadi jarak/frekuensi penyemprotan juga berkisar
2.6.2. Metode Pengendalian Hama Serangga
Pengendalian Mekanik
Pengendalian mekanik bertujuan untuk mematikan atau memindahkan hama
secara langsung baik dengan tangan atau dengan bantuan alat dan bahan lain.
Caranya sederhana dan dapat dilakukan oleh setiap orang tetapi yang jelas
memerlukan tenaga yang banyak yang berarti cukup mahal, harus dilakukan
secara kontinyu dan efisiensi serta efektivitasnya rendah.
Ada beberapa teknik pengendalian mekanik yang sering dilakukan dalam praktek
pengendalian hama.
Pengendalian dengan tangan
Cara ini merupakan teknik yang paling sederhana dan murah tentunya. Yang
dikumpulkan adalah fase hidup hama yang mudah ditemukan seperti telur dan
larva. Kecuali pengambilan dan pengumpulan dilakukan terhadap hama dapat
juga diadakan pengumpulan bagian-bagian tanaman yang terserang (Untung,
2001).
Perangkap umpan
Umpan yang diberikan dapat berupa makanan yang disenangi serangga
misalnya lalat buah maka umpannya adalah buah atau buah-buahan tiruan
yang dilaburi lem dan aroma atau esens buah-buahan yang banyak dijual
ditoko kimia, perangkap umpan ini dapat digunakan untuk menjerat serangga
yang aktif pada siang hari maupun pada malam hari. Kelemahan dari
perangkap ini adalah kesulitan untuk mengidentifikasi umpan yang sesuai
dengan serangga tertentu.
Perangkap bau dan aroma
Umumnya serangga tertarik dengan aroma tertentu, misalnya bau tape, bau
Perangkap kurung
Selain dengan menggunakan perekat atau cairan, dapat pula digunakan
perangkap serangga yang berupa perangkap kurung. Penggunaan perangkap
kurung ini adalah dengan memanfaatkan sifat serangga yang tertarik terhadap
cahaya, warna, dan umpan serta sifat serangga yang mempunyai
kecenderungan terbang menuju ke atas atau ke samping, terutama ke arah