BAB II
TINJAUAN PUSTAKA
2.1Uraian Tanaman Landoyung
2.1.1 Morfologi
Litsea cubeba (Lour.) Pers. berupa pohon dengan diameter batang 6-20
cm, serta tinggi pohon 5 – 10 meter (Marina, 2015). Batangnya tegak, berkayu, bulat, percabangan simpodial, putih kotor. Daun berbentuk tunggal, lonjong, tepi rata ujung runcing, pangkal meruncing, pertulangan menyirip, panjang 10-14 cm, lebar 7-9 cm, berwarna hijau. Bunganya majemuk, bentuk malai, berkelamin dua, kelopak hijau muda berbentuk mangkok, berbulu halus, mahkota bulat melengkung, kepala sari bulat berwarna hijau kehitaman. Memiliki buah bulat, keras, hitam. Bijinya bulat berwarna putih kotor. Akarnya tunggang berwarna coklat kehitaman (Hutapea, 1994).
2.1.2Habitat
Litsea cubeba (Lour.) Pers. tumbuh menyebar di Asia Tenggara, Asia
2.1.3 Sistematika
Menurut Hutapea (1994), klasifikasi tumbuhan landoyung sebagai berikut:
Kerajaan : Plantae
Divisi : Spermatophyta Sub divisi : Angiospermae Kelas : Dicotyledoneae Bangsa : Rhamnales Suku : Lauraceae Marga : Litsea
Jenis : Litsea cubeba (Lour.) Pers. 2.1.4 Sinonim
Sinonim dari Litsea cubeba (Lour.) Pers. adalah Litsea citrate BL.,
Theterantera citrate Ness., dan Theterentera pollyantha Wall (Prapti, 2008).
2.1.5 Nama asing
Litsea cubeba (Lour.) Pers. di China dikenal dengan May Chang (Syamsul
dan Rodame, 2015). 2.1.6Nama daerah
Litsea cubeba (Lour.) Pers. mempunyai nama lain seperti: krangean (Jawa
tengah), ki lemo (Jawa barat), Attarasa (Sumatra utara), sedangkan daerah Kalimantan khususnya pada suku Dayak Kenyan dikenal dengan nama balangla (Marina, dkk., 2015).
2.1.7 Manfaat
Litsea cubeba (Lour.) Pers. kayu, kulit, buah, daun, cabang dan akarnya
a. Kulit sebagai bahan minyak atsiri, pembuat parem, obat penurun panas, obat sakit perut, tonikum, dan obat penawar racun.
b. Daun sebagai obat demam, sakit perut, dan penawar racun.
c. Buah sebagai bahan minyak atsiri, buah muda sebagai bahan sambal, bumbu bandrek, bahan jamu untuk vertigo, dan lemas otot.
d. Batang cabang sebagai alat untuk mengusir binatang berbisa
f. Akar dan cabang sebagai obat sakit pencernaan, sakit kepala, sakit otot, sakit saat menstruasi, dan obat mabuk perjalanan.
2.1.8 Kandungan kimia
Kulit segar kering udara mengandung 1,25% minyak atsiri yang terdiri dari sitronelal dan sitral, serta mengandung 0,4% alkaloid berupa laurotetanin (Heyne, 1987). Buah Litsea mengandung minyak esensial yang biasa disebut may
chang oil. Kulit batang dan daun mengandung saponin, flavonoid dan tanin
(Hutapea, 1994). Susunan minyak Litsea cubeba asal Indonesia memiliki konsentrasi Sineol 30%, Sitronellal 0,94%, Linallol 8,95% dan Sitral 16,02%. Penyulingan kulit kayu segar kering angin 2 kg menghasilkan 25 ml minyak atsiri Penyulingan 100 grambuah l menghasilkan 3,9 ml minyak atsiri (Heryati, dkk., 2009).
2.2 Ekstraksi
Metode ekstraksi yang sering digunakan dalam berbagai penelitian antara lain yaitu:
2.2.1 Cara dingin
2.2.1.1Maserasi
Maserasi adalah proses penyarian simplisia dengan cara perendaman selama 5-12 hari menggunakan pelarut dengan sesekali pengadukan pada temperatur kamar. Maserasi yang dilakukan pengadukan secara terus-menerus disebut maserasi kinetik sedangkan yang dilakukan pengulangan panambahan pelarut setelah dilakukan penyaringan terhadap maserat pertama dan seterusnya disebut remaserasi (Cechinel, 2012).
2.2.1.2Perkolasi
Perkolasi adalah proses penyarian simplisia dengan pelarut yang selalu baru sampai terjadi penyarian sempurna yang umumnya dilakukan pada temperatur kamar. Proses perkolasi terdiri dari tahap pelembaban bahan, tahap perendaman antara, tahap perkolasi sebenarnya (penetesan/penampungan ekstrak) terus-menerus sampai diperoleh perkolat yang jumlahnya 1-5 kali bahan (Raaman, 2006).
2.2.2 Cara panas
2.2.2.1Refluks
Refluks adalah proses penyarian simplisia dengan menggunakan alat pada temperatur titik didihnya, selama waktu tertentu dan jumlah pelarut terbatas yang relatif konstan dengan adanya pendingin balik (Mohan, 2013).
2.2.2.2Digesti
Digesti adalah proses penyarian dengan menggunakan air pada temperatur lebih tinggi daripada temperatur ruangan, yaitu secara umum dilakukan pada temperatur 40-60°C selama 2-6 jam (Cechinel, 2012).
2.2.2.3Sokletasi
Sokletasi adalah proses penyarian dengan menggunakan pelarut yang selalu baru, dilakukan dengan menggunakan alat soklet sehingga menjadi ekstraksi kontinu dengan pelarut relatif konstan dengan adanya pendingin balik (Depkes RI., 2000). Sampel dan pelarut ditempatkan dalam wadah yang terpisah. Pelarut akan menguap sesuai dengan tiitik didihnya dan akan membasahi larutan sampel. Hasil sari akan mengisi sifon sampai tercapai satu siklus. Keuntungannya adalah banyaknya bagian tanaman yang akan terlarut dengan kondisi pemanasan. Kelemahannya tidak dapat digunakan untuk yang tidak tahan pemanasan (Nikhal, et al., 2010).
2.2.2.4Infudasi
Infudasi adalah proses penyarian dengan menggunakan pelarut air pada temperatur 90°C selama 15 menit (Titiek, dkk., 2011).
2.2.2.5Dekoktasi
2.3Radikal Bebas
Radikal bebas adalah setiap molekul yang mengandung satu atau lebih elektron yang tidak berpasangan. Radikal bebas sangat reaktif dan dengan mudah menjurus ke reaksi yang tidak terkontrol, menghasilkan ikatan dengan DNA, protein, lipida, atau kerusakan oksidatif pada gugus fungsional yang penting pada biomolekul ini. Radikal bebas juga terlibat dan berperan dalam patologi dari berbagai penyakit degeneratif, yakni kanker, aterosklerosis, jantung koroner, katarak, dan penyakit degeneratif lainnya (Silalahi, 2006).
Pembentukan radikal bebas dan reaksi oksidasi pada biomolekul akan berlangsung sepanjang hidup. Terbentuk akibat hilangnya maupun penambahan elektron dilintasannya pada saat terputusnya ikatan kovalen atom atau molekul bersangkutan sehingga bersifat amat reaktif. Radikal bebas yang sangat berbahaya dalam makhluk hidup antara lain adalah golongan hidroksil (OH-), superoksida (O-2), nitrogen monooksida (NO), peroksidal (RO-2), peroksinitrit (ONOO-), asam hipoklorit (HOCl), hidrogen peroksida (H2O2) (Kosasih, 2004).
2.4Antioksidan
Antioksidan adalah senyawa yang mempunyai struktur molekul yang dapat memberikan elektronnya kepada molekul radikal bebas dan dapat memutus reaksi berantai dari radikal bebas. Peran positif dari antioksidan adalah membantu sistem pertahanan tubuh bila ada unsur pembangkit penyakit memasuki dan menyerang tubuh (Winarsi, 2007).
1) Antioksidan primer yang berfungsi untuk mencegah pembentuk senyawa radikal baru karena dapat merubah radikal bebas yang ada menjadi molekul yang berkurang dampak negatifnya, sebelum radikal bebas ini sempat bereaksi. Contohnya adalah enzim superoksida dismutase (SOD), glutathion peroksidase, dan katalase.
2) Antioksidan sekunder merupakan senyawa yang berfungsi menangkap senyawa serta mencegah terjadinya reaksi berantai. Contohnya adalah vitamin E, vitamin C, dan betakaroten yang dapat diperoleh dari buah-buahan.
3) Antioksidan tersier merupakan senyawa yang memperbaiki kerusakan
sel-sel dan jaringan yang disebabkan radikal bebas. Contoh enzim yang memperbaiki DNA pada inti sel adalah metionin sulfoksidan reduktase. Adanya enzim ini untuk mencegah penyakit misalnya kanker.
2.4.1 Sumber-Sumber Antioksidan
Berdasarkan sumber perolehannya ada 2 macam antioksidan, yaitu antioksidan alami dan antioksidan buatan (sintetik) (Senja, dkk., 2014).
2.4.1.1Antioksidan alami
Antioksidan alami merupakan jenis antioksidan yang berasal dari tumbuhan dan hewan (Purwaningsih, 2012). Antioksidan alami umumnya mempunyai gugus hidroksi dalam struktur molekulnya. Antioksidan alami yang berasal dari tumbuhan adalah senyawa fenolik berupa golongan betakaroten, flavonoid, tanin, vitamin C dan vitamin E (Isnindar, dkk., 2011).
A. Betakaroten
dari alam jauh lebih berkhasiat daripada yang sudah dikemas dalam bentuk suplemen. (Kosasih, 2004).
B. Flavonoid
Senyawa flavonoid adalah senyawa polifenol yang mempunyai 15 atom karbon yang tersusun dalam konfigurasi C6 -C3 -C6, yaitu dua cincin aromatik yang dihubungkan oleh 3 atom karbon yang dapat atau tidak dapat membentuk cincin ketiga (Markham, 1988).Struktur dasar flavonoid dapat dilihat pada Gambar 2.1 berikut:
Gambar 2.1 Struktur dasar flavonoid(Silalahi, 2006).
Flavonoid bersifat antioksidan yang berperan sebagai penangkap radikal bebas karena mengandung gugus hidroksil. Sebagai reduktor, flavonoid dapat bertindak sebagai donor hidrogen terhadap radikal bebas (Silalahi, 2006).
C. Tanin
Tanin merupakan golongan metabolit fenolik yang unik dan memiliki berat molekul yang tinggi. Tersebar di daun, akar, dan buah untuk melindungi tanaman (Hudaya, dkk., 2015). Senyawa aktif metabolit sekunder yang diketahui mempunyai beberapa khasiat yaitu sebagai astringen, anti diare, anti bakteri dan antioksidan (Malangngi, dkk., 2012).
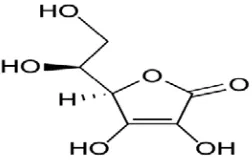
D. Vitamin C
atau agak kuning, tidak berbau, rasa asam, oleh pengaruh cahaya lambat laun menjadi gelap, dalam larutan cepat teroksidasi. Kelarutannya mudah larut dalam air, agak sukar larut dalam etanol (95%) P, praktis tidak larut dalam kloroform P, dalam eter P dan dalam benzen P. Penyimpanan dalam wadah tertutup rapat, terlindung dari cahaya. Vitamin C mengandung khasiat sebagai antiskorbut (Depkes RI., 1979).
Gambar 2.2 Rumus bangun vitamin C (Iqbal, et al., 2004).
Vitamin C berperan dalam pencegahan penyakit jantung koroner, mencegah kanker, meningkatkan sistem kekebalan tubuh terhadap infeksi virus dan bakteri, dan berperan dalam regenerasi vitamin E (Silalahi, 2006).Asam askorbatapabila terkena pengaruh oksigen, zat-zat pengoksidasi lemah, atau oleh pengaruh enzim asam askorbat oksidase, akan mempermudah senyawa ini mengalami oksidasi menjadi asam dehidroaskorbat, karena memiliki sifat mudah teroksidasi, asam askorbat digunakan sebagai antioksidan (Iqbal, et al., 2004). E. Vitamin E
teroksidasi maka dibutuhkan Vitamin C untuk menghentikan reaksi berantai (Pekiner, 2003).
2.4.1.2 Antioksidan sintetik
Antioksidan sintetik yang diizinkan dan umum digunakan untuk makanan yaitu BHA (Butylated hydroxy anisole), BHT ( Butylated hydroxy toluene), dan profil galat. Saat ini penggunaan antioksidan sintetik mulai dibatasi karena ternyata dari hasil penelitian yang telah dilakukan bahwa antioksidan sintetik seperti BHT (Butylated Hydroxy Toluena) ternyata dapat meracuni binatang percobaan dan bersifat karsinogenik (Zuhra, dkk., 2008). Butylated Hydroxyanisol (BHA) dapat menimbulkan akibat buruk terhadap kesehatan manusia seperti gangguan fungsi hati, paru, mukosa usus dan keracunan. Penggunaan antioksidan sintetik dapat menimbulkan keracunan pada dosis tertentu, menurut rekomendasi Food and Drug Administration dosis antioksidan sintetik yang diizinkan dalam pangan adalah 0,01%- 0,1% (Panagan, 2011).
2.4.2 Penentuan Aktivitas Antioksidan
Untuk menentukan aktivitas antioksidan secara in-vitro dapat dilakukan dengan beberapa metode antara lain:
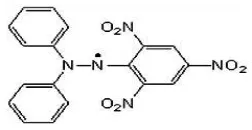
2.4.2.1Metode DPPH (1,1-difenil-2-pikrilhidrazil)
Pada tahun 1922, Goldschmidt dan Renn menemukan senyawa berwarna ungu radikal bebas stabil DPPH. Berwarna sangat ungu dan tidak larut dalam air (Ionita, 2005).
Metode DPPH adalah sebuah metode yang sederhana yang dapat digunakan untuk menguji kemampuan antioksidan yang terkandung dalam makanan. Metode DPPH dapat digunakan untuk sampel yang padat dan juga dalam bentuk larutan. Prinsipnya dimana elektron ganjil pada molekul DPPH memberikan serapan maksimum pada panjang gelombang 517 nm yang berwarna ungu. Warna ini akan berubah dari ungu menjadi kuning lemah apabila elektron ganjil tersebut berpasangan dengan atom hidrogen yang disumbangkan senyawa antioksidan (Prakash, et.al., 2001).
Parameter yang dipakai untuk menunjukan aktivitas antioksidan adalah harga konsentrasi efisien atau efficient concentration (EC50) atau Inhibition
Concentration (IC50) yaitu konsentrasi suatu zat antioksidan yang dapat
menyebabkan 50% DPPH kehilangan karakter radikal atau konsentrasi suatu zat antioksidan yang memberikan % penghambatan 50%. Zat yang mempunyai aktivitas antioksidan tinggi, akan mempunyai harga EC50 atau IC50 yang rendah (Molineux, 2004).
2.4.2.2 Metode kekuatan mereduksi
Prinsip dari metode ini pada kenaikan serapan dari campuran reaksi. Peningkatan serapan menunjukkan peningkatan pada aktivitas antioksidan. Dalam metode ini antioksidan membentuk kompleks berwarna dengan kalium ferrisianida, asam trikloroasetat, dan besi (III) klorida yang diukur pada panjang gelombang 700 nm. Peningkatan pada serapan campuran reaksi menunjukkan kekuatan mereduksi dari sampel (Amelia, 2011).
2.4.2.3 Metode uji kapasitas serapan radikal oksigen (ORAC)
dilakukan dengan menggunakan trolox (analog vitamin E) sebagai standar untuk menentukan trolox ekuivalen (TE). Nilai ORAC dihitung dari TE dan ditunjukkan sebagai satuan atau nilai ORAC. Nilai ORAC yang tinggi akan semakin besar kekuatan antioksidannya (Amelia, 2011).
2.4.2.4 Metode tiosianat
Aktivitas antioksidan sampel dengan metode tiosianat ditunjukkan dengan kekuatan sampel dalam menghambat peroksidasi asam linoleat. Jumlah peroksida yang terbentuk diukur secara tidak langsung dengan pembentukan kompleks ferritiosianat yang berwarna merah (Amelia, 2011).
2.4.2.5 Metode penghambatan radikal superoksida
Secara in vitro diukur oleh reduksi riboflavin/cahaya/nitro blue tetrazolium (NBT). Reduksi NBT adalah metode yang paling dikenal. Didasarkan pada pembangkitan radikal superoksida oleh autooksidasi dari riboflavin dengan adanya cahaya. NBT direduksi menjadi formazon yang berwarna biru dapat diukur pada 560 nm (Amelia, 2011).
2.4.2.6 Metode penghambatan radikal hidroksil
Kapasitas penghambatan radikal hidroksil dari ekstrak yang dihubungkan secara langsung terhadap aktivitas antioksidannya. Metode ini melibatkan pembangkitan in vitro dari radikal hidroksil menggunakan Fe3+/askorbat/EDTA/H2O2 berdasarkan reaksi Fenton (Amelia, 2011).
2.5Spektrofotometri UV-Visible
untuk sinar ultraviolet antara 200-400 nm sedangkan panjang gelombang untuk sinar tampak/visible antara 400-750 nm (Rohman, 2007).
Metode spektrofotometri UV-Vis telah banyak diterapkan untuk penetapan senyawa-senyawa organik yang umumnya dipergunakan untuk penentuan senyawa dalam jumlah yang sangat kecil. Dalam suatu larutan, gugus molekul yang dapat mengabsorpsi cahaya dinamakan gugus kromofor. Molekul-molekul yang hanya mengandung satu gugus kromofor dapat mengalami perubahan pada panjang gelombang. Molekul yang mengandung dua gugus kromofor atau lebih akan mengabsorpsi cahaya pada panjang gelombang yang hampir sama dengan molekul yang hanya mempunyai satu gugus kromofor, intensitas absorpsinya adalah sebanding dengan jumlah kromofor yang ada (Triyati, 1985).
2.6 Kromatografi
Kromatografi didefinisikan sebagai prosedur pemisahan zat terlarut oleh suatu proses migrasi diferensial dinamis dalam sistem yang terdiri dari dua fase atau lebih, salah satu diantaranya bergerak secara berkesinambungan dengan arah tertentu dan zat-zat itu menunjukkan perbedaan mobilitas disebabkan adanya perbedaan dalam adsorpsi partisi, kelarutan, tekanan uap, ukuran molekul atau kerapatan muatan ion. Dengan demikian masing-masing zat dapat diidentifikasi atau ditetapkan dengan metode analitik (Depkes RI., 1995).
2.6.1 Kromatografi lapis tipis
dimuat dalam lempeng. Biasanya ketebalannya 0,2 mm. Campuran senyawa ditotolkan dari tepi dasar lempeng berupa bercak ataupun pita memanjang. Lempeng kemudian dimasukkan ke dalam bejana kromatografi berisi pelarut yang telah ditentukan sebelumnya berdasarkan polaritas komponen campuran senyawa tersebut. KLT pelaksanaannya lebih mudah dan lebih murah dibandingkan dengan kromatografi kolom (Heinrich, dkk., 2009).
Pendeteksian bercak hasil pemisahan dapat dilakukan dengan beberapa cara. Pengamatan dengan sinar ultraviolet adalah cara sederhana yang dilakukan untuk senyawa tak berwarna. Beberapa senyawa organik bersinar atau berfluorosensi jika disinari dengan sinar ultraviolet gelombang pendek (254 nm) atau gelombang panjang (366 nm). Senyawa yang tidak dapat dideteksi menggunakan cara tersebut maka harus dicoba dengan penyemprotan pereaksi yang membuat bercak tersebut tampak yaitu pertama tanpa pemanasan, kemudian bila perlu dengan pemanasan (Rohman, 2007).
2.6.2 Kromatografi kertas
Kromatografi kertas atau KKt pada hakekatnya ialah KLT pada lapisan tipis selulosa atau kertas. Cara ini ditemukan jauh sebelum KLT dan telah dipakai secara efektif selama bertahun-tahun untuk pemisahan molekul biologi yang polar seperti asam amino, gula dan nukleotida. KKt tidak memerlukan plat pendukung dan kertas dapat dengan mudah diperoleh dalam bentuk murni sebagai kertas saring (Gritter, dkk., 1991).
pemisahan. Pemisahan dapat berlangsung menggunakan fase cair tunggal dengan proses yang sama dengan kromatografi adsorpsi dalam kolom (Depkes RI, 1995).