BAB II
TINJAUAN PUSTAKA
2.1 Uraian Tumbuhan
Uraian tumbuhan meliputi morfologi tumbuhan, habitat, klasifikasi
tumbuhan, nama asing, nama daerah, manfaat, kandungan kimia.
2.1.1 Morfologi tumbuhan
Daun kari (Murraya koenigii) termasuk dalam golongan famili Rutaceae. Daun kari memiliki tinggi 0,9 hingga 6 meter dan berdiameter 15-40 cm. Daun
kari memiliki aroma yang sangat khas dan rasa sedikit pahit, bentuknya oval
dengan ujung runcing. Tumbuhan ini dapat tumbuh subur dalam iklim tropis,
memiliki bunga kecil berwarna putih kekuningan, buahnya kecil berwarna hijau
berwarna hijau ketika masih muda dan ungu setelah matang. Tumbuhan ini
berkembang biak melalui biji benih dan turunannya tumbuh melalui akarnya
(Azis, dkk., 2014).
2.1.2 Habitat
Daun kari (Murraya koenigii) adalah salah satu species Murraya yang
ditemukan di Aceh. Tumbuhan ini biasanya dibudidayakan sebagai daun aromatik
dan digunakan untuk penyedap alami dalam kari. Berasal dari Tarai wilayah Utara
Pradesh, India, saat ini daun kari banyak ditemukan diseluruh bagian India, daun
ini juga dibudidayakan di India Selatan,Sri Lanka, China, Australia, pulau-pulau
pasifik, hingga Asia Tenggara. Tumbuhan ini menyebar ke Indonesia, Afrika
2.1.3 Klasifikasi tumbuhan
Menurut MEDA (Herbarium Medanense) Universitas Sumatera Utara
sistematika tumbuhan daun kari adalah sebagai berikut :
Kingdom : Plantae
Devisi : Spermathophyta
Subdivisi : Angiospermae
Kelas : Dicotyledonae
Ordo : Malvales
Famili : Rutaceae
Genus : Murraya
Spesies : Murraya koenigii L
Nama lokal : Daun kari
2.1.4 Nama asing
Nama asing daun kari adalah ma jiao ye (China), curry (English),
garupillai (Malaysia) (Hariana, 2011).
2.1.5 Nama daerah
Daun kari di Indonesia memiliki berbagai macam nama daerah, seperti
temurui (Aceh), sicerek (Maningkabau), ki becetah (Sunda)
2.1.6 Manfaat
Daun kari biasanya digunakan sebagai rempah penyedap masakan. Selain
berperan penting dikuliner, daun kari juga memiliki manfaat didunia pengobatan.
Air rebusan daun kari memiliki manfaat untuk mengatasi anemia, menurunkan
kolesterol, mengobati diare dan mengatasi diabetes karena mempunyai efek
sebagai antioksidan, antidiabetes, antimikroba, anti-inflamasi dan
2.1.7Kandungan kimia
Daun kari memiliki kandungan saponin, terpenoid/triterpenoid, alkaloid,
glikosida, falvonoid, tanin dan antioksidan seperti tokoferol, b-karoten dan lutein.
Daun kari juga memiliki kandungan mineral Cr, Mg, Mn, Zn dan Cu
(Sudrawanto, dkk., 2015). (Gahlawat, dkk. 2014) mengatakan bahwa daun kari
segar mengandung volatil oil yang kaya akan vitamin A, kalsium, girinimbin, koenin, koenigin, koenidin dan koenimbin.
2.2Uraian Golongan Senyawa Kimia Daun kari
Senyawa kimia yang terdapat pada daun kari meliputi tannin, saponin,
glikosida, steroid/triterpenoid, flavonoid dan alkaloid.
2.2.1Tanin
Tanin terdapat luas pada tumbuhan berpembuluh.Sebagian besar
tumbuhan banyak mengandung tanin rasanya sepat.Salah satu fungsi tanin dalam
tumbuhan ialah sebagai penolak hewan pemakan tumbuhan (Robinson, 1995).
Berdasarkan identitas inti fenolit dan cara pembentukannya, tanin dibagi
menjadi tiga yaitu tanin yang terhidrolisis, tanin yang terkondensasi dan tanin
kompleks (Trease dan Evans, 1983).
a. Tanin terhidrolisis (hydrosable tannin)
Tanin jenis ini biasanya berikatan pada karbohidrat dengan membentuk jembatan
oksigen dan dapat dihidrolisis menggunakan asam sulfat atau asam klorida
ataupun dengan enzim.Prekursor pembentukan tanin ini adalah asam fenolit (asam
galat, asam elagit), residu glukosa, serta antara asam fenolit dan glukosa ada
b. Tanin terkondensasi (condesed tannins)
Tanin terkondensasi biasanya tidak dapat dihidrolisis, tetapi terkondensasi
menghasilkan asam klorida.Tanin jenis ini kebanyakan terdiri dari polimer
flavanoida yang merupakan senyawa fenol.Prekursor pembentukan tanin ini
adalah flavanoida, catechin, flavonol-3-4-diol.
c. Tanin kompleks (complex tannin)
Tanin kompleks merupakan campuran antara tanin terhidrolisis dan tanin
terkondensasi.Contoh tumbuhan yang mengandung tanin kompleks adalah teh,
kuercus, dan castanea.
2.2.2Saponin
Saponin adalah glikosida triterpenoida dan sterol.Senyawa golongan ini banyak
terdapat pada tumbuhan tinggi, merupakan senyawa dengan rasa yang pahit dan
mampu membentuk larutan koloidal dalam air serta menghasilkan busa jika
dikocok dalam air.Aglikon dari saponin sering disebut sebagai sapogenin.
Saponin merupakan senyawa aktif permukaan, bersifat seperti sabun dan dapat
diuji berdasarkan kemampuannya membentuk busa. Pembentukan busa yang
mantap sewaktu mengekstraksi tumbuhan atau pada waktu memekatkan ekstrak
tumbuhan merupakan bukti terpercaya akan adanya saponin pada tumbuhan
tersebut (Harbone, 1987).
2.2.3Glikosida
Glikosida adalah suatu senyawa yang jika dihidrolisis akan menghasilkan bagian
gula yang disebut glikon dan bagian bukan gula disebut aglikon. Gula yang
dihasilkan biasanya adalah glukosa, ramnosa, dan lain sebagainya.Jika bagian
gulanya adalah glukosa maka disebut glukosida, sedangkan jika bagian gulanya
Berdasarkan hubungan ikatan antara glikon dan aglikonnya, glikosida dibagi
(Robinson, 1995):
a. O-glikosida, yaitu senyawa glikosida yang ikatan antara glikon dan aglikonnya
dihubungkan oleh atom O. Contoh: Salisin.
b. S-glikosida, yaitu senyawa glikosida yang ikatan antara glikon dan aglikonnya
dihubungkan oleh atom S. Contoh: Sinigrin.
c. N-glikosida, yaitu senyawa glikosida yang ikatan antara glikon dan aglikonnya
dihubungkan oleh atom N. Contoh: Adenosine.
d. C-glikosida, yaitu senyawa glikosida yang ikatan antara glikon dan aglikonnya
dihubungkan oleh atom C. Contoh: Barbaloin.
2.2.4 Triterpenoid/steroid
Triterpenoid adalah senyawa yang kerangka karbonnya berasal dari enam
satuan isopren dan secara biosintesis diturunkan dari hidrokarbon C30 asiklik,
yaitu skualen. Senyawa tersebut mempunyai struktur siklik yang relatif kompleks,
kebanyakan merupakan suatu alkohol, aldehid atau karboksilat (Harbone, 1987).
Steroid adalah triterpen yang kerangka dasarnya sistem cincin
siklopentana perhidrofenantren. Dahulu steroid dianggap sebagai senyawa satwa
(digunakan sebagai hormon kelamin, asam empedu), tetapi pada tahun-tahun
terakhir ini makin banyak senyawa steroid yang ditemukan dalam jaringan
tumbuhan (Harborne, 1987).
Menurut asalnya senyawa steroid dibagi atas:
a. Zoosterol, yaitu steroid yang berasal dari hewan, misalnya kolesterol.
b. Fitosterol, yaitu steroid yang berasal dari tumbuhan, misalnya sitosterol dan
stigmasterol.
d. Marinesterol, yaitu steroid yang berasal dari organisme laut, misalnya
spongesterol.
2.2.5 Flavonoid
Senyawa flavonoid merupakan salah satu senyawa polifenol terbesar,
mengandung 15 atom karbon, terdiri dari dua cincin benzen yang dihubungkan
menjadi satu oleh rantai linier yang terdiri dari 3 atom karbon, tersusun dalam
konfigurasi C6-C3-C6 (Robinson, 1995).
Flavonoid memiliki sifat antioksidan.Senyawa ini berperan sebagai
penangkap radikal bebas karena mengandung gugus hidroksil.Karena bersifat
sebagai reduktor, flavonoid dapat bertindak sebagai donor hidrogen terhadap
radikal bebas (Silalahi, 2006).
Senyawa flavonoid terdapat pada semua bagian tumbuhan termasuk daun,
akar, kayu, kulit, bunga, buah dan biji (Markham, 1988).Flavonoid mengandung
senyawa aromatik terkonjugasi sehingga menunjukkan pita serapan kuat pada
spektrum UV dan sinar tampak.Umumnya terdapat dalam bentuk terikat pada gula
yang disebut dengan glikosida sehingga untuk menganalisis flavonoid, lebih baik
ekstrak tumbuhan dihidrolisis terlebih dahulu untuk memecah ikatan gula dengan
aglikon (Harborne, 1987).
2.2.6 Alkaloid
Alkaloid merupakan senyawa kimia bersifat basa, mengandung satu atau
lebih atom nitrogen, dan biasanya bergabungan sebagai bagian sistem siklik. Sifat
alkaloid yang basa menyebabkan senyawa tersebut mengalami dekomposisi akibat
adanya sinar atau adanya oksigen (Indrawati dkk, 2013). Ada tiga pereaksi yang
digunakan dalam pemeriksaan senyawa kimia untuk mendeteksi golongan
2.3 Ekstraksi
Ekstraksi adalah suatu cara untuk menarik satu atau lebih zat dari bahan
asal menggunakan pelarut (Syamsuni, 2006). Ekstraksi adalah kegiatan penarikan
kandungan kimia yang dapat larut sehingga terpisah dari bahan yang tidak dapat
larut dengan pelarut cair (Depkes RI, 2000)
Tujuan utama ekstraksi adalah umtuk mendapatkan atau memisahkan
sebanyak mungkin zat-zat yang memiliki khasiat pengobatan (consentrata) dari
zat-zat yang tidak bermanfaat, agar lebih mudah dipergunakan dan disimpan
dibandingkan simplisia asal, dan tujuan pengobatan lebih terjamin (Syamsuni,
2006).
2.3.1 Cara dingin
a. Maserasi
Maserasi adalah penyarian simplisia dengan cara perendaman menggunakan
pelarut disertai sesekali pengadukan pada temperatur kamar. Maserasi yang
dilakukan pengadukan secara terus menerus disebut maserasi kinetik sedangkan
yang dilakukan penambahan ulang pelarut setelah dilakukan penyaringan terhadap
maserat pertama dan seterusnya disebut remaserasi.
b. Perkolasi
Perkolasi adalah proses penyarian simplisia menggunakan alat perkolator
dengan pelarut yang selalu baru, umumnya dilakukan pada temperatur kamar.
Proses perkolasi terdiri dari tahap pengembangan bahan, tahap maserasi antara,
tahap perkolasi sebenarnya (penampungan perkolat) terus menerus sampai
2.3.2 Cara panas
a. Digesti
Digesti adalah proses penyarian dengan pengadukan kontinu pada
temperatur lebih tinggi dari temperatur kamar, yaitu secara umum dilakukan pada
temperatur 40-500C.
b. Infundasi
Infundasi adalah proses penyarian dengan menggunakan pelarut air pada
temperatur 900C selama 15 menit.
c. Dekoktasi
Dekoktasi adalah proses penyarian dengan menggunakan pelarut air pada
temperatur 900C selama 30 menit.
d. Refluks
Refluks adalah proses penyarian simplisia pada temperatur titik didihnya
menggunakan alat dengan pendingin balik dalam waktu tertentu dimana pelarut
akan terkondensasi menuju pendingin dan kembali ke labu.
e. Sokletasi
Sokletasi adalah proses penyarian menggunakan pelarut yang selalu baru,
dilakukan dengan menggunakan alat khusus (soklet) dimana pelarut akan
terkondensasi dari labu menuju pendingin, kemudian jatuh membasahi sampel.
2.4 Radikal Bebas
Radikal bebas adalah setiap molekul yang mengandung satu atau lebih
elektron yang tidak berpasangan.radikal bebas sangat reaktif dan dengan mudah
protein, lipida atau kerusakan oksidatif pada gugus fungsional yang penying pada
biomolekul ini.perubahan ini akan menyebabkan proses penuaan. Radikal bebas
juga terlibat dan berperan dalam patologi dari berbagai penyakit degenerative,
yakni kanker, aterosklerosis, rematik, jantung koroner, katarak dann penyakit
degenerasi saraf seperti Parkinson (Silalahi, 2006)
Kerusakan sel akan menyebabkan dampak negatif pada struktur dan
fungsinya.Semakin besar ukuran biomolekul yang mengalami kerusakan, semakin
parah akibatnya.Secara biologis senyawa biomolekul memiliki fungsi yang sangat
penting. Oleh sebab itu, adanya kerusakan struktur dan fungsi sel akan sangat
menggangu sistem kerja organ secara umum (Winarsi, 2007).
Tubuh memiliki mekanisme pertahan antioksidan dalam bentuk enzim
antioksidan dan antioksidan untuk menetralisir radikal bebas. Perkembangan
industri yang pesat menyebabkan manusia berkontak dengan berbagai radikal
bebas yang berasal dari lingkungan dan dari kegiatan fisik yang tinggi
menyebabkan sistem pertahanan antioksidan dalam tubuh tidak memadai
(Silalahi, 2006).
2.5Antioksidan
Antioksidan adalah senyawa yang mampu menangkal atau meredam
dampak negatif oksidan dalm tubuh. Antioksidan bekerja dengan mendonorkan
satu elektronnya kepada senyawa yang bersifat oksidan sehingga aktivitas oksidan
tersebut bias dihambat.
Penyebab utama kerusakan oksidatif didalam tubuh adalah senyawa
oksidan, baik yang berbentuk radikal bebas ataupun bentuk senyawa oksigen
akibat dari rendahnya antioksidan dalam tubuh sehingga tidak dapat mengimbangi
reaktivitas senyawa oksidan.
Khasiat antioksidan untuk mencegah berbagai penyakit akibat pengaruh
oksidatif akan lebih efektif jika kita mengkonsumsi sayur-sayuran dan
buah-buahan yang kaya akan antioksidan dan berbagai jenis dari pada menggunakan
antioksidan tunggal. Efek antioksidan dari sayur-sayuran dan buah-buahan lebih
efektif daripada suplemen antioksidan yang diisolasi dikarenakan oleh adanya
komponen lain dalam sayur-sayuran dan buah-buahan yang berperan secara
positif (Silalahi, 2006).
Secara umum, antioksidan dikelompokkan menjadi 2, yaitu antioksidan
enzimatis dan non-enzimatis. Antioksidan enzimatis misalnya enzim superoksida
dismutase (SOD), katalse dan glutation peroksidase. Antioksidan non-enzimatis
masih dibagi dalam 2 kelompok lagi:
a. antioksidan larut lemak, seperti tokoferol, karotenoid, flavonoid, quinon, dan
bilirubin.
b. Antioksidan larut air,asam askorbat, asam urat, protein pengikat logam, dan
protein pengikat heme.
Berdasarkan mekanisme kerjanya, antioksidan digolongkan menjadi 3
kelompok, yaitu antioksidan primer, sekunder dan tersier.
a. Antioksidan primer meliputi superperoksida dismutase (SOD), katalase dan
glutation perosidase (GSH-Px). Antioksidan primer disebut juga antioksidam
enzimatis. Suatu senyawa dikatakan sebagai antioksidan primer, apabila dapat
memberikan atom hidrogen secara cepat kepada senyawa radikal, kemudian
radikal antioksidan yang terbentuk segera berubah menjadi senyawa yang lebih
b. Antioksidan sekunder disebut juga antioksidan eksogenus atau non-enzimatis.
Antioksidan dalam kelompok ini juga disebut sistem pertahanan preventif.
Dalam sistem pertahanan ini, terbentuknya senyawa oksigen reaktif dihambat
dengan cara merusak pembentukannya. Antioksidan sekunder meliputi vitamin
E, vitamin C, β-karoten,flavonoid, asam urat, bilirubin, dan albumin.
c. Antioksidan tersier meliputi sistem enzim DNA-repair dan metionin
sulfoksida reduktase. Enzim-enzim ini berfungsi dalam perbaikan biomolekuler
yang rusak akibat reaktivitas radikal bebas (Winarsi, 2007).
2.5.1 Vitamin C
Vitamin C atau asam askorbat mempunyai berat molekul 176,13 dengan
rumus molekul C6H8O6. Pemerian vitamin C adalah hablur atau serbuk berwarna
putih atau agak kekuningan. Pengaruh cahaya lambat laun menyebabkan berwarna
gelap, dalam keadaan kering stabil di udara namun dalam larutan cepat
teroksidasi. Vitamin C mudah larut dalam air, agak sukar larut dalam etanol,
praktis tidak larut dalam kloroform, dalam eter dan dalam benzen (Depkes RI,
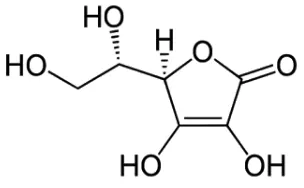
1979). Rumus bangun vitamin C dapat dilihat pada Gambar 2.1.
Gambar 2.1 Rumus vitamin C
Vitamin C merupakan suatu antioksidan penting yang larut dalam
air.Vitamin C mempunyai potensi sebagai antioksidan dengan mendonorkan
pencegahan penyakit jantung koroner, mencegah kanker, meningkatkan sistem
kekebalan tubuh terhadap infeksi virus dan bakteri dan berperan dalam regenerasi
vitamin E (Silalahi, 2006).
2.6Spektrofotometer UV-Visibel
Metode pengukuran menggunakan prinsip spektrofotometri adalah
berdasarkan absorpsi cahaya padapanjan gelombang tertentu melalui suatu larutan
yang mengandung kontaminan yang akan ditentukan konsentrasinya. Prinsip keja
dari metode ini adalah jumlah cahaya yang diabsorpsi oleh larutan sebanding
dengan konsentrasi kontaminan dalam larutan (Lestari, 2009).
Prinsip kerja spektrofotometer UV-Vis berdasarkan penyerapan cahaya
atau energi radiasi oleh suatu larutan. Jumlah cahaya atau energi radiasi yang
diserap memungkinkan pengukuran jumlah zat penyerap dalam larutan secara
kuantitatif (Triyati, 1985). Panjang gelombang untuk sinar ultraviolet antara
200-400 nm sedangkan panjang gelombang untuk sinar tampak/visible antara 400-750 nm (Gandjar dan Rohman, 2007).
Metode spektrofotometri ultra-violet dan sinar tampak (visible) telah
banyak diterapkan untuk penetapan senyawa-senyawa organik yang umumnya
dipergunakan untuk penetuan senyawa dalam jumlah yang sangat kecil. Dalam
suatu larutan, gugus molekul yang dapat mengabsorpsi cahaya dinamakan gugus
kromofor. Molekul-molekul yang mengandung satu gugus kromofor dapat
mengalami perubahan padapanjang gelombang. Molekul mengandung dua gugus
kromofor atau lebih akan mengabsorbsi cahaya pada panjang gelombang yang
tertentu, tetapi intensitas absorpsinya adalah sebanding dengan jumlah kromofor
yang ada (Triyati, 1985).
2.7 Metode Pemerangkapan Radikal Bebas DPPH
Penentuan aktivitas radikal bebas DPPH berdasarkan pengurangan DPPH
radikal dalam metanol yang menyebabkan penurunan absorbansi pada 515 nm.
Warna larutan berubah dari ungu menjadi kuning. Perubahan ini terjadi ketika
DPPH ditangkap oleh antioksidan yang menghilangkan atom H untuk membentuk
stabil DPPH-H.
Metode sederhana yang telah dikembangkan untuk menentukan kapasitas
antioksidan dari makanan memanfaatkan 1,1 –diphenyl-2-picrylhidrazyl. DPPH memberikan serapan maksimum pada panjang gelombang 517 nm dan memiliki
warna ungu (Prakash, 2001).
Prinsip metode pemerangkapan radikal bebas DPPH, yaitu elektron ganjil
pada molekul DPPH memberikan serapan maksimum pada panjang gelombang
517 nm. Interaksi antioksidan dengan DPPH akan menetralkan karakter radikal
bebas dari DPPH (Molyneux, 2004). Warna ungu larutan DPPH akan berubah
menjadi kuning lemah apabila elektron ganjil tersebut berpasangan dengan atom
hidrogen yang dari senyawa antioksidan (Prakash, 2001).
Parameter yang dipakai untuk menunjukkan aktivitas antioksidan adalah
harga konsentrasi efisien atau Efficient Concentration (EC50) atau Inhibitory Concentration (IC50) yaitu konsentrasi suatu zat antioksidan yang dapat
menyebabkan 50% DPPH kehilangan karakter radikal atau konsentrasi suatu zat
2.7.1 Pelarut
Metode DPPH akan memberikan hasil yang baik menggunakan pelarut
metanol atau etanol karena kedua pelarut ini tidak mempengaruhi dalam reaksi
antara sampel uji antioksidan dengan radikal bebas DPPH (Molyneux, 2004).
2.7.2 Pengukuran panjang gelombang
Panjang gelombang yang digunakan untuk analisis kuantitatif adalah
panjang gelombang yang mempunyai absorbansi maksimal. Panjang gelombang
maksimum yang digunakan dalam pengukuran sampel uji pada metode
pemerangkapan radikal bebas DPPH sangat bervariasi. Menurut beberapa
literatur, panjang gelombang maksimum untuk DPPH antara lain 515-520 nm
(Molyneux, 2004).
2.7.3 Waktu pengukuran
Waktu pengukuran atau waktu kerja (operating time) bertujuan untuk mengetahui waktu yang tepat dalam melakukan pengukuran, yakni saat sampel
telah mencapai kesetimbangan sehingga dalam kondisi stabil. Waktu pengukuran
yang digunakan dalam beberapa penelitian sangatlah bervariasi, yaitu 1-240
menit. Waktu pengukuran yang paling banyak direkomendasikan adalah 60 menit.
Kecepatan reaksi dipengaruhi oleh sifat dari aktivitas antioksidan yang terdapat di