STUDI KUALITAS PARAMETER KIMIA AIR UNTUK
USAHA BUDIDAYA IKAN DAN UDANG DI KAWASAN
TAMBAK KURI CADDI KABUPATEN MAROS
SKRIPSI
ARDIANSYAH RUSMADI 105940051410
PROGRAM STUDI BUDIDAYA PERAIRAN
FAKULTAS PERTANIAN
UNIVERSITAS MUHAMMADIYAH MAKASSAR
2014
STUDI KUALITAS PARAMETER KIMIA AIR UNTUK
USAHA BUDIDAYA IKAN DAN UDANG DI KAWASAN
TAMBAK KURI CADDI KABUPATEN MAROS
ARDIANSYAH RUSMADI 105940051410
SKRIPSI
Sebagai Salah Satu Syarat Untuk Memperoleh Gelar Sarjana
Perikanan
Strata Satu (S-1)
PROGRAM STUDI BUDIDAYA PERAIRAN
FAKULTAS PERTANIAN
UNIVERSITAS MUHAMMADIYAH MAKASSAR
2014
HALAMAN PENGESAHAN
Judul Skripsi : Studi Kualitas Parameter Kimia Air Untuk Usaha Budidaya Ikan dan Udang Di Kawasan Tambak Kuri Caddi.
Nama Mahasiswa : Ardiansyah Rusmadi Nomor Induk Mahasiswa : 105940051410
ABSTRAK
ARDIANSYAH RUSMADI. Studi Kualitas Parameter Kimia Air Untuk Usaha
Budidaya Ikan dan Udang Di Kawasan Tambak Kuri Caddi Kabupaten Maros. Desa Nisombalie, Kecamatan Marusu, (dibimbing oleh DARMAWATI dan RAHMI).
Penelitian ini bertujuan untuk menganalisis kualitas parameter kimia air (pH, Salinitas, DO, Nitrat, Phospat, Amonia), tentang studi kelayakan budidaya ikan dan udang di kawasan tambak Kuri Caddi Maros.
Pengambilan data dilakukan dengan melakukan pengukuran langsung (insitu) dan penelitian di Laboratorium. Lokasi penelitian dibagi menjadi tiga blok, dimana setiap blok terdiri dari tiga stasiun. Blok ke 1 terletak di daerah saluran pintu utama pemasukan air, blok ke 2 terletak di daerah tambak (tambak udang windu), dan blok ke 3 terletak di daerah tambak (tambak ikan bandeng). Alat-alat yang digunakan dalam penelitian ini adalah pH meter, DO meter, Hand Refraktometer, Coolbox. Penyajian hasil penelitian dari semua parameter yang diuji disajikan secara deskriptif.
Berdasarkan hasil penelitian ini, hanya kandungan phosfat yang menunjukkan kadar yang melebihi batas toleransi. Sedangkan untuk kandungan amoniak dan nitrat menunjukkan kadar yang masih di bawah batas toleransi. Untuk kandungan pH, Salinitas, dan DO (dissolved oksigen) menunjukkan kadar yang masih berada pada batas toleransi untuk kegiatan budidaya ikan dan udang.
KATA PENGANTAR
Puji syukur penulis panjatkan kehadirat Allah SWT yang telah
memberikan nikmat dan anugrahnya sehingga penulisan skripsi yang berjudul
“Studi Kualitas Parameter Kimia Air Untuk Usaha Budidaya Ikan dan Udang Di Selanjutnya shalawat serta salam penulis hanturkan kepada junjungan Nabi
Muhammad SAW sebagai suri tauladan dalam segala aktifitas yang kita lakukan.
Penulisan skripsi ini didasarkan pada hasil penelitian yang dilakukan pada bulan
mei sampai juni 2014, berlokasi di Dusun Kuri Caddi, Desa Nisombalia,
Kecamatan Marusu, Kabupaten Maros, Provinsi Sulawesi Selatan.
Melalui kesempatan ini penulis ingin mengucapkan terimah kasih kepada
pihak-pihak yang telah membantu dan memberikan dukungan, mulai dari
persiapan sampai dengan selesainya penulisan skripsi ini. Dengan segala
kerendahan hati penulis ingin mengucapkan terimah kasih yang sebesar-besarnya
kepada :
1. Ayahanda Dekan Fakultas Pertanian Ir. H. M. Saleh Molla, M.Si yang telah
memberikan bantuannya, baik bantuan materi dan non materi selama penulis
melakasanakan kegiatan penelitian.
2. Ibunda Ketua Jurusan Budidaya Perairan Murni, S. Pi, M. Si, yang juga telah
memberikan dukungan dan bantuannya mulai dari penelitian berlangsung
sampai dengan selesainya penulisan skripsi ini.
3. Ibunda Ir. Darmawati, M. Si dan Rahmi, S. Pi, M. Si selaku komisi
meluangkan waktunya untuk memberikan bimbingan kepada penulis mulai
dari awal sampai dengan akhir penelitian.
4. Ayahanda Abd. Malik, S. Pi, M. Si dan Ibunda Asni Anwar, S. Pi, M. Si
selaku komisi penguji yang telah meluangkan waktunya dan memberikan
saran-saran yang kepada penulis dalam menjalankan penelitian.
5. Bapak Abd. Haris Sambu, S. Pi, M. Si selaku dosen Pembina yang telah
memberikan banyak bantuan kepada penulis selama melaksanakan penelitian.
6. Bapak Kepala Kecamatan Marusu, Kepala Desa Nisombalia, dan Kepala
Dusun Kuri Caddi beserta seluruh aparat pemerintahannya yang telah bersedia
menerima penulis di daerahnya untuk melakukan penelitian.
7. Kedua orang tua penulis Bapak Ali Rusdi, S. Sos dan Ibu Dra. Mardiah
beserta adik-adik penulis Salman Al-Farizi, Rahmayanti Sri Rejeki, dan
Ashabul kahfi yang tak lelah untuk memberikan dukungan baik moril maupun
materil selama penulis melaksanakan penelitian.
8. Saudara dan saudariku para peneliti yang tergabung dalam kelompok
penelitian terpadu di kawasan tambak Unismuh Makassar yang turut
bekerjasama dalam melakukan penelitian.
9. Semua pihak yang telah berperan serta dalam menyukseskan penelitian
terpadu yang tidak sempat kami sebutkan satu persatu.
Sebagai penutup, mungkin di dalam penulisan skripsi ini masih terdapat
kekurangan dan kesalahan dari penulis, maka dari itu penulis mengharapkan
adanya saran dan kritik yang sifatnya membangun jika memang terdapat
nantinya skripsi ini dapat bermafaat bagi penulis dan juga pembacanya. Semoga
kita bersama-sama mendapatkan ridho dari Allah swt dalam segala aktifitas
keseharian kita. Insyaallah.
Penulis
DAFTAR ISI
HALAMAN JUDUL i
HALAMAN PENGESAHAN ii
ABSTRAK iii
KATA PENGANTAR iv
DAFTAR ISI vii
DAFTAR TABEL viii
DAFTAR GAMBAR ix
DAFTAR LAMPIRAN x
I. PENDAHULUAN 1
1.1. Latar Belakang 1
1.2.Tujuan dan Kegunaan 2
II. TINJAUAN PUSTAKA 3
2.1. Pengertian Budidaya 3
2.2. Kualitas Air 3
2.3. Parameter Kimia 4
III. METODE PENELITIAN 9
3.1. Waktu dan Lokasi Penelititan 9
3.2. Alat dan Bahan 10
3.3. Persiapan 14
3.4. Penentuan Stasiun 15
3.5. Parameter Yang Diamati 16
3.7. Metode Pengambilan/ Pengukuran Sampel 17
3.8. Pengumpulan Data 18
3.9. Analisis Data 18
IV. HASIL DAN PEMBAHASAN 19
4.1. pH 19 4.2. DO (Dissolved Oksigen) 20 4.3. Salinitas 21 4.4. Nitrat 22 4.5. Phospat 23 4.6. Amonia 25 V. PENUTUP 28 5.1. Kesimpulan 28 5.2. Saran 29 DAFTAR PUSTAKA 30 LAMPIRAN 32
DAFTAR TABEL
No. Teks Halaman
1. Waktu pengukuran sampel insitu. 17
2. Waktu pengambilan sampel analisis laboratorium 17
3. Kriteria kualitas air bagi budidaya udang di tambak 18
4. Data hasil pengukuran pH 19
5. Data hasil pengukuran DO 20
6. Data hasil pengukuran Salinitas 21
7. Data hasil penelitian Nitrat (NO3) 22
8. Data hasil penelitian Phosfat (PO4) 23
9. Data hasil penelitian Amonia (NH3) 25
DAFTAR GAMBAR
No.
Teks Halaman1. Lokasi tambak Kuri Caddi Kabupaten Maros 9
DAFTAR LAMPIRAN
No
Teks Halaman1. Data hasil penelitian di Laboratorium BPPBAP Maros 33
2. Data hasil pengukuran di tambak (insitu) Kuri Caddi Maros 35
PENGESAHAN KOMISI PENGUJI
Judul Skripsi : Studi Kualitas Parameter Kimia Air Untuk Usaha Budidaya Ikan dan Udang Di Kawasan Tambak Kuri Caddi.
Nama Mahasiswa : Ardiansyah Rusmadi Nomor Induk Mahasiswa : 105940051410 Program Studi : Budidaya Perairan
1
I. PENDAHULUAN
1.1. Latar Belakang
Dalam kegiatan usaha budidaya ikan, air merupakan media pemeliharaan
yang sangat penting untuk diperhatikan. Keberhasilan suatu usaha budidaya
sangat bergantung pada kualitas air yang digunakan. Kualitas air adalah sifat air
dan kandungan makhluk hidup, zat, energi, atau komponen lain di dalam air.
Kualitas air dinyatakan dengan beberapa parameter, yaitu parameter fisika (suhu,
kekeruhan, dan padatan terlarut, dan sebagainya), parameter kimia (pH, oksigen
terlarut, BOD, kadar logam, dan sebagainya), dan parameter biologi (keberadaan
plankton, bakteri, jamur, dan sebagainya) (Effendi, 2003).
Masalah utama yang dihadapi oleh sumber daya air meliputi kuantitas air
yang sudah tidak mampu memenuhi kebutuhan yang terus menerus meningkat
dan kualitas air untuk keperluan domestik yang semakin menurun. Kegiatan
industri, domestik, dan kegiatan lain berdampak negatif terhadap sumber daya air,
antara lain menyebabkan penurunan kualitas air. Kondisi ini dapat menimbulkan
gangguan, kerusakan, dan bahaya bagi semua makhluk hidup yang bergabung
pada sumber daya air. Oleh karena itu, diperlukan pengelolaan dan perlindungan
sumber daya air secara seksama.
Lokasi pertambakan Kuri Caddi di Kabupaten Maros adalah kawasan yang
merupakan daerah hutan manggrove yang dikonversi menjadi lahan
pertambakan.Lokasi tambak berbatasan langsung dengan Teluk Makassar yang
sangat dipadati oleh lalu lintas pelayaran. Selain itu, perairan laut kuri caddi
2
pesisir pantai dilokasi tersebut. Aktifitas pelayaran dan penangkapan di perairan
ini sedikit banyaknya dapat mempengaruhi kondisi perairan di perairan tersebut.
Berdasarkan hal tersebut, maka perlu untuk melakukan penelitian terhadap
parameter kualitas air pada kawasan tambak Kuri Caddi yang merupakan lokasi
pertambakan yang akan direhabilitasi menjadi tambak yang lebih produktif.
Dengan dasar tersebut penelitian parameter kualitas air secara terpadu ini dapat
memberikan informasi tentang kualitas perairan pada lokasi pertambakan tersebut.
1.2.Tujuan dan Kegunaan
Penelitian ini bertujuan untuk mengetahui kondisi kualitas kimia air di
kawasan Tambak Kuri Caddi dan mengetahui kelayakan lokasi tersebut untuk
digunakan sebagai wadah budidaya. Diharapkan penelitian ini dapat digunakan
3
II. TINJAUAN PUSTAKA
2.1. Pengertian Budidaya Perairan
Istilah budidaya perairan (akuakultur) berasal dari bahasa lnggris
aquaculture yang berarti pengusahaan budidaya organisme akuatik termasuk ikan,
moluska, krustase dan tumbuhan akuatik. Kegiatan budidaya menyiratkan
semacam intervensi dalam proses pemeliharaan untuk meningkatkan produksi,
seperti penebaran yang teratur, pemberian pakan, perlindungan terhadap
pemangsa (predator) pencegahan terhadap serangan penyakit dan sebagainya
(Pusat Riset Perikanan Budidaya, 2001; Hermanto, 2007). Kegiatan budidaya
dapat dilaksanakan di lingkungan air payau, air tawar dan air laut. Pemilihan
jenis (spesies) tertentu akan berkaitan langsung dengan lingkungan perairan
sebagai habitat dari spesies yang dipelihara. (Hermanto, 2007).
Tambak merupakan salah satu jenis habitat yang dipergunakan sebagai
tempat untuk kegiatan budidaya air payau yang berlokasi di daerah pesisir.
Secara umum tambak biasanya dikaitkan langsung dengan pemeliharaan udang
windu, walaupun sebenarya masih banyak spesies yang dapat dibudidayakan di
tambak misalnya ikan bandeng, ikan nila, ikan kerapu, kakap putih dan ikan
bandeng dan sebagainya (Hermanto, 2007).
2.2. Kualitas Air
Air sebagai media tempat hidup ikan yang dibudidayakan harus memenuhi
berbagai persyaratan dari segi fisika, kimia, maupun biologi. Dari segi fisika, air
4
dipelihara. Sedangkan dari segi kimia, air sebagai pembawa unsur-unsur hara,
mineral, vitamin, gas-gas terlarut dan sebagainya. Dari segi biologi, air
merupakan media untuk kegiatan biologis dalam pembentukan dan penguraian
bahan-bahan organik (Buwono, 1993).
Kadar kuantitas dan kualitas air tambak juga ditentukan oleh pasang surut
air laut sebagai suplai air tambak. Pada dasarnya pasang surut yang diterima oleh
daerah pantai dan estuaria adalah pasang surut semi diurnal, dengan dua kali
pasang dan dua kali surut terjadi pergantian dalam satu hari. Tambak-tambak air
payau kebanyakan dibangun di daerah pasang surut yaitu diantara pasang
tertinggi dan surut terendah. Situasi tersebut diperlukan untuk mempermudah
dalam memenuhi kebutuhan air selama masa pemeliharaan udang. Ukuran pasang
surut tertentu sangat diperlukan agar konstruksi tambak dan pengelolaanya dapat
dilakukan secara efisien. Pasang surut yang ideal untuk tambak udang adalah
sebesar 1,5 - 2,5 (Buwono, 1993).
Menurut Rukmini (2012), Kualitas air merupakan salah satu faktor penting
yang harus diperhatikan dalam pemilihan lokasi pemeliharaan ikan. Beberapa
parameter fisika dan kimia perairan yang dapat mempengaruhi kehidupan ikan
adalah suhu, oksigen terlarut, karbon dioksida, ammonia, pH, alkalinitas, dan
kekeruhan.
2.3. Parameter Kimia
Dalam melihat kondisi kelayakan tempat untuk dijadikan sebagai lokasi
budidaya, kita dapat mengukur dari kondisi parameter airnya. Salah satu
5
2.3.1. (pH) Derajat Keasaman
Derajat keasaman atau pH merupakan gambaran jumlah ion hidrogen atau
lebih tepatnya aktivitas ion hidrogen dalam perairan. Secara umum, nilai pH
menggambarkan seberapa dalam atau basa suatu perairan. Nilai pH : 7 dikatakan
netral, lebih besar dari 7 adalah basa, lebih kecil dari 7 adalah asam. Semakin jauh
jaraknya dari angka 7, semakin asam atau semakin basa. Nilai pH yang normal
bagi suatu perairan payau adalah antara 7-9, sementara pH air laut antara 8,0-8,5
(Widigdo, 2013).
2.3.2. DO (Dissolved Oksigen)
Oksigen terlarut atau dikenal dengan istilah DO (Dissolved Oksigen)
adalah parameter yang sangat penting bagi hewan perairan. Sumber utama
oksigen terlarut dalam air adalah proses fotosintesis dari fitoplankton. Semakin
subur perairan, semakin banyak fitoplankton yang hidup di dalamnya. Semakin
banyak fitoplankton akan semakin banyak oksigen yang dihasilkan dan terlarut di
dalam air (Widigdo, 2013).
2.3.3. Salinitas
Salinitas merupakan konsentrasi ion terlarut yang diekspresikan dalam
miligram per liter (mg/L) dalam satuan internasional atau dalam sistem inggris
dikenal dengan nama part per thousand (ppt). Salinitas juga didefenisikan sebagai
jumlah semua garam dalam air setelah semua karbonat dirubah menjadi
6
dalam lambang 0/00. Salinitas membedakan jenis air menjadi air tawar, air laut, dan
air payau (Pramono, 2009).
Masing-masing jenis ikan atau udang mempunyai kisaran toleransi
salinitas yang berbeda antara spesies satu dengan yang lainnya dan antara
kelompok umur spesies yang sama. Meskipun demikian disepakati bahwa
salinitas 10-250/00 adalah baik untuk dipertahankan. Salinitas dapat diukur baik
dengan alat yang praktis yaitu salinometer atau handrefraktometer (Pramono,
2009).
2.3.4. Phosphat
Nitrat adalah sumber nitrogen yang penting bagi fitoplankton baik
diperairan laut maupun di perairan air tawar (Boney, 1983; Erlina, 2006). Nutrien
ini digunakan dalam beberapa proses seperti fotosintesis, sintesa protein dan
penyusun gen serta pertumbuhan organisme (Erlina, 2006). Menurut Erlina (2006)
nitrogen dan phospat kemungkinan besar merupakan faktor pembatas bagi
pertumbuhan fitoplankton. Phospat merupakan salah satu unsur hara yang
potensial dalam pembentukan protein dan metabolisme sel. Kandungan
orthophosphat yang terlarut dalam air dapat menunjukkan kesuburan perairan
(Erlina, 2006).
Anggapan bahwa kadar nitrogen konstan di seluruh kolom air adalah tidak
benar. Lapisan-lapisan air teratas pada umumnya mengandung lebih sedikit
nitrogen dari pada lapisan-lapisan air yang terletak jauh dari permukaan laut. Hal
tersebut sama dengan pengaruh intensitas cahaya bagi produksi fitoplankton.
7
produksi fitoplankton di kedalaman 100 m lebih kecil dari pada produksi
dikedalaman 10 m. Menurunnya kandungan nitrogen di bagian permukaan kolom
air sangat besar dipengaruhi oleh peningkatan jumlah sel fitoplankton. Dengan
semakin besarnya populasi fitoplankton dari permukaan sampai kedalaman 100
m, semakin banyak pula cahaya yang diabsorpsi oleh fitoplankton. Akibatnya
semakin sedikit cahaya yang dapat mencapai kedalaman sekitar 100 m. Bila
intensitas cahaya berkurang, kedalaman kompensasi akan bergeser keatas
mendekati permukaan air. Dengan demikian, persediaan zat hara dalam lapisan air
permukaan setebal 100 m akan makin berkurang dan sejalan dengan
meningkatnya kepadatan populasi fitoplankton, semakin lama kolom air dan zat
hara yang tersedia semakin tidak mencukupi kebutuhan fitoplankton (Erlina,
2006). Lebih lanjut perairan dikatakan baik jika mempunyai kandungan phospat
berada pada kisaran 0,05 – 0,50 ppm (DKP, 2004; Erlina, 2006).
2.3.5. Nitrogen (amoniak), Nitrat, Nitrit
Amonia diperairan berasal dari hasil samping metabolisme hewan (yang
dikeluarkan ekskresi) dan hasil proses dekomposisi bahan organik dan bakteri.
Hasil analisis kandungan amonia di laboratorium adalah amonia total, dimana
belum dipisahkan antara amonia tak terionisasi (amonia bebas, NH3) yang toksik
dan amonium (NH4+) yang relatif tidak bersifat toksik. Kandungan amonia bebas
yang toksik sangat bergantung pada pH, suhu, dan salinitas perairan. Semakin
tinggi pH dan suhu, semakin tinggi persentase amonia bebas yang terkandung
8
Sifat toksik amonia bebas biasanya mulai terjadi pada konsentrasi 0,6-2
mg/L di kolam-kolam budidaya, sedangkan efek sublethal terjadi pada konsentrasi
0,1-0,3 mg/L, idealnya untuk keperluan budidaya kadar amonia di dalam air harus
0 ppm. Kecuali amonia, nitrat, nitrit dan ortophosphat, perairan perlu juga diamati
dalam kaitannya untuk mengetahui sediaan nutrient yang ada. Dalam hal ini
amonia, nitrit, dan nitrat menggambarkan jumlah bioavailablenitrogen, yakni
nutrient N (nitrogen) terlarut yang ada yang dapat langsung digunakan oleh
organisme (fitoplankton, tumbuhan) untuk tumbuh dan berkembang. Sedangkan
orthophosphat merepresentasikan nutrien phospor (P) terlarut dan merupakan
bioavailablephosphorus. Ketersediaan kedua nutrient ini merupakan gambaran
tingkat kesuburan perairan, yang merupakan faktor penting bila perairan hendak
dimanfaatkan untuk keperluan perikanan, khususnya budidaya. Kandungan total P
yang diharapkan pada perairan tambak adalah lebih dari 0,5 ppm. Perbandingan
N:P menentukan komposisi fitoplankton, untuk jenis diatome perbandingan N:P
9
III. METODE PENELITIAN
3.1. Waktu dan Lokasi Penelitian
Penelitian ini dilaksanakan pada bulan April-Mei tahun 2014 yang
berlokasi di Kawasan Tambak Unismuh Makassar tepatnya Di Dusun Kuri Caddi,
Desa Nisombalie, Kecamatan Marusu, Kabupaten Maros, Provinsi Sulawesi
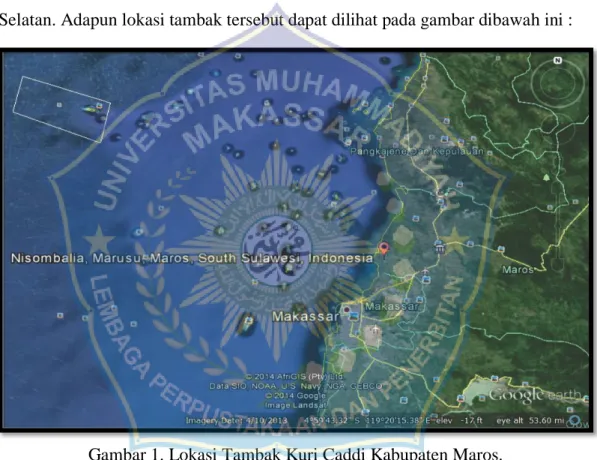
Selatan. Adapun lokasi tambak tersebut dapat dilihat pada gambar dibawah ini :
Gambar 1. Lokasi Tambak Kuri Caddi Kabupaten Maros.
Sedangkan lokasi untuk analisis laboratorium kandungan Nitrat, Phosphat
dan Amonia dilakukan di Laboratorium Kualitas Air Balai Pengembangan dan
10
3.2. Alat dan Bahan
Alat dan bahan yang digunakan dalam melaksanakan penelitian terhadap
parameter kimia air di Kawasan Tambak Kuri Caddi Maros akan diuraikan pada
penjelasan di bawah ini :
3.2.1. pH
Alat yang digunakan dalam mengukur pH adalah pH meter yang berfungsi
untuk mengukur kandungan pH pada sampel yang diukur. Sedangkan bahan yang
digunakan adalah akuades yang digunakan untuk mensterilkan dan membersihkan
elektroda pada pH meter. Tissue yang digunakan untuk membersihkan dan
mengeringkan elektroda.
Sedangkan cara kerja dari alat-alat tersebut adalah dengan menekan tombol
On/Off pada pH meter untuk mengaktifkan alat tersebut. Kemudian mencelupkan
elektroda ke dalam air sampel sambil digoyangkan. Selanjutnya menunggu
sampai nilai pH tidak berubah/stabil dan mencatat hasil yang ditunjukkan pada
layar pH meter. Setelah mencatat nilai pH, diakhiri dengan mencuci elektroda
dengan akuades dan mengeringkannya dengan tissue.
3.2.2. DO (Dissolved Oksigen)
Alat yang digunakan dalam mengukur DO (Dissolved Oksigen) adalah DO
meter yang berfungsi untuk mengukur kandungan DO pada sampel. Sedangkan
bahan yang digunakan adalah akuades yang digunakan untuk membersihkan dan
mensterilkan elektroda pada Do meter. Tissue yang digunakan untuk
11
Sedangkan cara kerja dari alat-alat tersebut adalah yang pertama dengan
menekan tombol On/Off pada DO meter untuk mengaktifkan alat tersebut.
Kemudian mencelupkan elektroda ke dalam air sampel sambil digoyangkan.
Selanjutnya menunggu sampai nilai DO tidak berubah/ stabil pada layar. Mencatat
nilai DO (Dissolved Oksigen) pada layar DO meter. Diakhiri dengan mencuci
elektroda dengan akuades dan mengeringkannya dengan tissue.
3.2.3. Salinitas
Alat yang digunakan dalam mengukur salinitas adalah refraktometer yang
berfungsi untuk mengukur kandungan salinitas sampel. Sedangkan bahan yang
digunakan adalah pipet tetes berfungsi untuk memasukkan sampel air ke dalam
prisma ukur yang terdapat pada alat refraktometer. Tissue berfungsi untuk
membersihkan dan mengeringkan prisma yang terdapat dalam alat refraktometer.
Akuades berfungsi untuk menetralkan kandungan salinitas pada prisma sebelum
mengukur sampel.
Sedangkan cara kerja dari alat-alat tersebut adalah dengan terlebih dahulu
mengkalibrasi refraktometer dengan meneteskan 1 atau 2 tetes akuades pada
prisma. Selanjutnya menutup dan membaca skala salinitas pada refraktometer,
bila batas garis bidang gelap dan terang menunjukkan angka nol, maka
refraktometer siap untuk digunakan. Setelah itu, bersihkan prisma dengan
menggunakan tissue halus sampai kering. Selanjutnya adalah dengan meneteskan
air sampel dan membaca skala yang ditunjukkan pada prisma. Setelah melakukan
pengukuran, tahapan yang terakhir adalah dengan mencuci prisma dengan
12
salinitas dinyatakan dalam ppt (part per thousand), yaitu setara dengan gram
NaCl per liter.
3.2.4. Nitrat
Alat yang digunakan dalam mengukur nitrat yang pertama adalah
spektrofotometer yang berfungsi untuk membaca kadar nitrat sampel. Kedua
adalah kertas saring whatman nomor 42 adalah kertas yang digunakan untuk
menyaring air sampel. Ketiga adalah tabung reaksi 50 ml yang digunakan untuk
menampung air sampel hasil penyaring. Keempat adalah corong yang digunakan
pada saaat melakukan penyaringan sampel. Kelima adalah rak tabung yang
digunakan untuk meletakkan tabung reaksi setelah berisi dengan sampel. Keenam
adalah kolom reduksi yang digunakan untuk menyaring sampel setelah
sebelumnya disaring dengan kertas saring whatman nomor 42. Ketujuh adalah
Labu ukur 25 ml yang digunakan untuk mengukur volume sampel. Kedelapan
adalah Pipet 1 dan 5 ml yang digunakan untuk memberikan pereaksi pada sampel.
Sedangkan tahapan prosedur pengukuran yang dilakukan untuk sampel
nitrat adalah dengan menyaring sampel air dengan kertas saring whatman no. 42.
Tahapan selanjutnya adalah mengambil 50 ml sampel yang telah disaring lalu
memasukkannya dalam tabung tes. Setelah itu, menambahkan 1 ml ammonium
khlorida pekat dan dilanjutkan dengan mengocok sampel dengan hati-hati.
Kemudian melewatkan 15 ml air sampel kekolom reduksi. Membuang 15 ml air
pertama yang keluar melalui kolom reduksi (sebagai pembilas kolom reduksi
13
membuang sampel sebanyak 20 ml. Setelah itu menampung 15 ml air yang keluar
berikutnya dari kolom reduksi untuk dianalisis.
Sebelum dianalisis sampel ditambahkan 0,5 ml larutan sulfanilamide lalu
dikocok dengan hati-hati. Selanjutnya menambahkan 0,5 ml larutan nafthylamin
lalu dikocok. Diamkan sampel tersebut selama 10 menit lalu lanjutkan pembacaan
absorban dengan mengunakan spektrofotometer pada panjang gelombang 543 nm.
Tahapan terakhir adalah menghitung konsentrasi nitrat dengan menggunakan
kurva kalibrasi (r = > 0,95).
3.2.5. Phosfat
Alat yang digunakan dalam mengukur sampel phospat yang pertama adalah
spektrofotometer yang berfungsi untuk membaca kadar phospat pada sampel.
Kedua adalah kertas saring whatman nomor. 42 yang digunakan dalam menyaring
sampel air. Ketiga adalah corong yang digunakan dalam proses penyaringan air
sampel. Keempat adalah tabung reaksi 25 ml yang digunakan untuk menampung
air sampel setelah melalui penyaringan. Kelima adalah rak tabung yang digunakan
untuk meletakkan tabung yang sudah berisi dengan sampel yang telah disaring.
Sedangkan tahapan yang dilakukan untuk pengukuran sampel phospat
adalah dengan memasukkan 25 ml sampel yang telah disaring kedalam tabung tes.
Setelah itu menambahkan 2,5 ml larutan campuran lalu dilanjutkan dengan
mengocok botol sampel dengan hati-hati. Kemudian diamkan selama 20 menit.
Setelah itu, tahap selanjutnya adalah mengukur absorban pada panjang gelombang
14
menghitung konsentrasi phospat dalam sampel dengan menggunakan kurva
standar.
3.2.6. Amonia
Alat yang digunakan dalam mengukur sampel phospat yang pertama adalah
spektrofotometer yang berfungsi untuk membaca kandungan phospat pada
sampel. Kedua adalah kertas saring whatman nomor.42 yang berfungsi sebagai
penyaring sampel. Ketiga adalah tabung reaksi 25 ml yang digunakan untuk
menampung air hasil penyaringan. Keempat adalah rak tabung yang digunakan
untuk meletakkan tabung reaksi yang telah berisi dengan sampel. Kelima adalah
corong yang digunakan pada saat melakukan penyaringan. Keenam adalah pipet
25 cc yang digunakan untuk memasukkan/ memberikan cairan pereaksi pada
sampel.
Tahapan pengukuran pada-hati sampel amonia yang pertama adalah
dengan memasukkan 25 ml sampel yang telah disaring ke dalam tabung tes.
Kedua yaitu menambahkan 1 ml larutan phenol kedalam tabung reaksi lalu
mengocoknya dengan hati-hati. Ketiga yaitu menambahkan 1 ml larutan sodium
nitroprussid lalu mengocoknya. Keempat yaitu menambahkan 2,5 ml larutan
oksidizing lalu mengocoknya. Kelima yaitu membiarkan atau mendiamkan sampel
selama 1 jam. Setelah 1 jam, dilanjutkan dengan mengukur absorban pada
panjang gelombang 640 m dengan menggunakan akuades sebagai blanko.
Tahapan yang terakhir adalah menghitung konsentrasi amonia dalam sampel
15
3.3. Persiapan
Sebelum melakukan penelitian ada beberapa persiapan yang dilakukan
diantaranya adalah dengan melakukan pengumpulan informasi mengenai kondisi
umum lokasi penelitian, studi literatur, observasi lokasi penelitian, penentuan
stasiun pengamatan, serta persiapan alat dan bahan yang akan digunakan dalam
penelitian.
Dalam melakukan penentuan stasiun pengamatan, dilakukan dengan cara
purposive (Nasution, 2001 dalam Alexander, 2006) yang mengacu pada fisiografi
lokasi agar sedapat mungkin bisa mewakili atau menggambarkan keadaan
perairan tersebut.
3.4. Penentuan Stasiun
Dalam pengambilan sampel air, dilakukan pembagian blok yang terdiri
dari blok I, II, III. Dari ketiga blok ini kemudian dibagi kedalam tiga stasiun
pengambilan sampel. Letak dari setiap blok yang ditetapkan adalah sebagai
berikut:
a. Blok I terdapat di pintu utama saluran air yang terdiri dari tiga titik stasiun
dengan titik koordinat S: 05o01.973o,T: 119o28.068o, Elev : -56 ft.
b. Blok II berada di daerah tambak yang terdiri dari 3 stasiun dengan titik
koordinat S: 05o01.403o, T: 119o28.219o, Elev: -49 ft. Adapun letak stasiun I di pintu pemasukan air, stasiun II di pelataran tambak, dan stasiun III di pintu
16
c. Blok III berada di daerah tambak yang terdiri dari 3 stasiun dengan titik
koordinat S: 05o01.301o, T: 119o28.301o, Elev: 37 ft. Adapun letak stasiun I di pintu pemasukan air, stasiun II di pelataran tambak, dan stasiun III di pintu
pengeluaran air.
Pada penelitian tentang kualitas parameter kualitas air ini, pengambilan
sampel air pada setiap blok dilakukan setiap minggu dalam kurun waktu 2 bulan
dengan frekuensi 1 kali pengambilan sampel.
Di bawah ini akan disajikan gambar lokasi stasiun pengambilan sampel
parameter kimia air di pertambakan Kuri Caddi.
Gambar 2. Lokasi pengambilan sampel penelitian.
3.5. Parameter Yang Diamati
Dalam penelitian ini ada 6 parameter kimia air yang akan diamati adalah
17
3.6. Prosedur Penelitian
Dalam penelitian ini ada dua prosedur kerja yang akan dilakukan, yaitu
pengukuran sampel insitu dan pengambilan sampel untuk analisis laboratorium.
Untuk parameter pH, salinitas, dan DO (Dissolved Oksigen) dilakukan
pengukuran dilokasi penelitian insitu. Sedangkan untuk parameter, nitrat, phospat,
dan amonia dilakukan pengukuran di Laboratorium.
Tabel 1. Waktu pengukuran sampel in situ.
No Parameter Waktu Pengukuran Frekuensi
Pertama Kedua
1 pH 08.00 Wita 17.00 Wita
1 X Se-Minggu 2 Salinitas 08.10 Wita 17.10 Wita
3 DO 08.20 Wita 17.20 Wita
Tabel 2. Waktu pengambilan sampel analisis laboratorium
No Parameter Waktu Pengambilan Frekuensi
1 Nitrat 09.00 Wita
2 X Se- Bulan 2 Phosphat 09.00 Wita
3 Amoniak 09.0 Wita
3.7. Metode Pengambilan/ Pengukuran Sampel
Metode yang digunakan dalam pengambilan sampel adalah dengan cara
setiap lokasi pengamatan dibagi menjadi tiga stasiun pengambilan sampel.
Pengambilan sampel dilakukan satu kali dalam seminggu untuk pengukuran in
situ sedangkan pengambilan sampel untuk analsisis di laboratorium dilakukan dua
kalidalam satu bulan. Proses penelitian ini akan berlangsung selama 2 bulan.
Dalam melakukan pengukuran sampel untuk parameter pH, Salinitas, dan
DO dilakukan dengan mengambil sampel pada setiap stasiun menggunakan ember
18
parameter phospat, nitrat, dan amonia dilakukan dengan menggunakan gayung
kemudian dituang kedalam ember. Sempel air yang berada di ember kemudian
dipindahkan kedalam botol-botol sampel yang telah disiapkan. Untuk menjaga
kondisi sampel agar tidak terkontaminasi, botol sampel dimasukkan kedalam
coolbox yang berfungsi untuk melindungi sampel agar kandungannya tidak
mengalami perubahan.
3.8. Pengumpulan Data
Data hasil pengukuran di lapangan dikumpulkan dan digabungkan dengan
data hasil analisa di Laboratorium Kualitas Air BPPBAP (Balai Penelitian dan
Pengembangan Budidaya air Payau) Kabupaten Maros. Data hasil pengujian di
Laboratorium akan diidentifikasi dan dibandingkan dengan kriteria parameter
kualitas air menurut standar kelayakan yang telah dirumuskan oleh para ahli
dibidang kualitas air.
3.9. Analisis Data
Dari semua data yang didapatkan dari hasil pengujian yang dilakukan baik
secara insitu dan analisa laboratorium akan diolah secara deskriptif dengan
membandingkan hasil dari lapangan dengan studi literatur tentang kelayakan
parameter kimia air untuk budidaya tambak. Adapun literatur tentang kelayakan
19
Tabel 3. Kriteria Kualitas Air Bagi Budidaya Udang Di Tambak .
No Parameter Batas Kelayakan Literatur
1 Ph 7,0-9,0 7,5-8,5 Widigdo (2013) 2 DO 4-7 ppm 4-7 ppm Widigdo (2013) 3 Salinitas 5-35 ppt 15-25 ppt Widigdo (2013) 4 Nitrat 0,09-3,5 mg/l 0,09 Mustofa (2008),Widigdo (2013) 5 Phosphat 0,05-0,50 ppm 0,5 ppm Widigdo (2013) 6 Amonia 0,6-2 mg/l ≤ 0,1 mg/l Widigdo (2013) Sumber : Poernomo (1991), KepMenLH (2004), dan Widigdo (2007).
20
IV. HASIL DAN PEMBAHASAN
Proses pengambilan sampel air dilakukan pada saat air laut pasang dan
surut. Selain itu, waktu pengambilan sampel dilakukan pada pagi dan siang hari.
Setelah melakukan penelitian di lapangan (insitu) dan laboratorium. Maka
didapatkan data hasil penelitian yang terdiri dari 6 parameter diantaranya adalah
pH, DO (Dissolved Oksigen), salinitas nitrat, phospat, dan amonia yang akan
dijelaskan pada uraian di bawah ini :
4.1. pH
Berdasarkan hasil pengukuran yang dilakukan untuk kandungan pH pada
lokasi penelitian, didapatkan hasil data yang dapat dilihat pada tabel di bawah ini :
Tabel 4. Data hasil pengukuran pH.
Tabel di atas menunjukkan bahwa konsentrasi pH pada ketiga lokasi
penelitian ini tidak memiliki perbedaan yang signifikan walaupun pengukuran
dilakukan pada waktu yang berbeda. Kandungan pH pada semua lokasi selama
pengukuran berkisar antara 7.4-8,1. Berdasarkan nilai rata-rata tersebut di atas
yang berkisar antara 7,6-7.9, selanjutnya dapat disimpulkan bahwa kandungan pH
pada perairan tambak ini masih dalam kondisi yang layak untuk digunakan
sebagai lokasi budidaya ikan dan udang. Hal ini sesuai dengan pendapat Widigdo
No Sampel Pengamatan Rata-rata
1 2 3 4
1 A 7.8 7.6 8.1 7.7 7.8 2 B 7.7 7.4 7.8 7.5 7.6 3 C 7.8 7.7 8.1 7.9 7.9
21
(2013) yang menyatakan bahwa nilai pH yang normal bagi suatu perairan payau
adalah antara 7-9 dengan kondisi optimum 7.5-8.5.
4.2. DO (Dissolved Oksigen)
Berdasarkan hasil pengukuran yang dilakukan untuk konsentrasi DO
(Dissolved Oksigen) pada lokasi penelitian, didapatkan hasil data yang dapat
dilihat pada tabel di bawah ini:
Tabel 5. Data hasil pengukuran DO.
No Sampel Pengamatan Rata-rata
1 2 3 4
1 A 3.8 1.7 6.2 1.9 3.4 2 B 1.3 1.3 7.3 0.9 2.7 3 C 3 1.9 7.3 2.2 3.6
Tabel di atas dapat dijelaskan bahwa konsentrasi oksigen terlarut pada
lokasi penelitian memiliki perbedaan yang signifikan. Perbedaan ini disebabkan
oleh perbedaan waktu pada saat pengukuran dilakukan. Pada pengukuran minggu
ke-1, 2, dank ke-4 dilakukan pada pagi hari pukul 06.00-08.00 Wita. Hal ini
menyebabkan konsentrasi oksigen terlarut pada minggu tersebut lebih rendah dari
nilai optimum. Sedangkan pada pengukuran minggu ke-3 konsentrasi oksigen
terlarut berada pada kisaran optimum antara 4-7 mg/l. Hal ini disebabkan karena
pada pengukuran minggu ke-3 dilakukan pada siang hari pukul 13.00-14.00 Wita.
Berdasarkan nilai-nilai rata-rata di atas dapat disimpulkan bahwa nilai
oksigen terlarut yang berkisar antara 2.7-3.6 mg/l. Dari kisaran nilai tersebut dapat
disimpulkan bahwa konsentrasi oksigen terlarut pada lokasi pertambakan ini
22
ini berdasarkan pernyataan Widigdo (2013) yang menyatakan bahwa kadar
oksigen terlarut yang ideal untuk budidaya udang adalah antara 4 ppm pada pagi
pagi hari dan mendekati tingkat jenuh (7-9 ppm) pada siang hari.
4.3. Salinitas
Berdasarkan hasil pengukuran yang dilakukan untuk konsentrasi salinitas
pada loksai penelitian, didapatkan hasil data yang dapat dilihat pada tabel di
bawah ini :
Tabel 6. Data hasil pengukuran Salinitas.
No Sampel Pengamatan Rata-rata
1 2 3 4
1 A 35 35 35 35 35
2 B 35 35 30 37 34
3 C 35 33 30 36 34
Tabel di atas menjelaskan bahwa konsentrasi nilai salinitas pada lokasi
pertambakan ini cukup tinggi berkisar antara 30-37 ‰. Nilai yang ditunjukkan
tidak terlalu berbeda walaupun pengukuran dilakukan pada waktu yang berbeda.
Setelah dirata-ratakan, nilai salinitas pada perairan ini berkisar antara 34-35 ‰.
Pada kondisi tersebut, salinitas pada perairan ini masih berada pada kisaran batas
yang ditolerir untuk kegiatan budidaya udang. Hal ini didasarkan pada pendapat
Widigdo (2013) yang menyatakan bahwa batas toleransi nilai salinitas untuk
budidaya udang berkisar antara 5-35 ‰ dengan nilai optimum 15-25 ‰.
4.4. Nitrat (NO3)
Berdasarkan hasil penelitian pada sampel untuk parameter nitrat,
23 Tabel 7. Data hasil penelitian Nitrat (NO3).
No Sampel Pengamatan Rata-rata
1 2 3 4
1 A 2.020 0.058 0.030 0.096 0.551 2 B 0.227 0.063 0.039 0.052 0.095 3 C 2.656 0.055 0.015 0.097 0.706
Tabel di atas menjelaskan bahwa konsentrasi nilai nitrat pada semua lokasi
berkisar antara 0,015-2,656 mg/l. Setelah dirata-ratakan, nilai nitrat pada ketiga
lokasi berkisar antara 0.095-0.706 mg/l. Dari nilai hasil rata-rata di atas,
menunjukkan kadar nitrat yang masih memenuhi standar mutu yang diatur di PP
NO. 82 tahun 2001 kelas III yaitu 20 mg/l. Selain itu, menurut Resti (2007) dalam
Mustofa (2008) alga khususnya fitoplankton dapat tumbuh optimal pada
kandungan nitrat sebesar 0,09-3,5 mg/l. Pada konsentrasi di bawah 0,01 mg/l atau
diatas 4,5 mg/l nitrat dapat menjadi faktor pembatas.
Tabel di atas menunjukkan bahwa kadar nitrat yang terendah terdapat pada
blok C (Tambak) sampel minggu ke 3 yang pengambilan sampelnya dilakukan
pada pukul 13.00-14.30 WITA dengan nilai 0,015 mg/l. Rendahnya nilai sampel
pada blok ini selain dipengaruhi oleh kondisi air laut yang sedang surut juga
dipengaruhi oleh tidak adanya kegiatan budidaya yang dilakukan pada lokasi
penelitian tersebut. Dengan tidak adanya kegiatan budidaya diperairan tersebut
mengakibatkan kurangnya limbah domestik atau pemupukan yang dapat
meningkatkan kandungan nitrat pada lokasi penelitian tersebut. Sedangkan kadar
nitrat tertinggi terdapat pada blok C (Tambak) sampel minggu ke 1 dengan nilai
2,656 mg/l. Sampling dilakukan pada pukul 05.30-08.00 Wita dimana kondisi air
24
dengan pendapat Hutagalung dan Rozak (1997) dalam Hendrawati, dkk (2008)
yang menyatakan bahwa meningkatnya kadar nitrat pada perairan disebabkan oleh
masuknya limbah domestik atau pertanian (pemupukan) yang banyak
mengandung nitrat. Selain itu, sumber potensial lain yang dapat memperkaya
nitrat di perairan adalah hujan dan bahan-bahan buangan dari daratan, termasuk
limbah (Faizal, 2007).
4.5. Phospat (PO4)
Berdasarkan hasil penelitian pada sampel untuk parameter phosfat,
didapatkan data hasil penelitian pada tabel di bawah ini :
Tabel 8. Data hasil penelitian Phosfat (PO4).
No Sampel Pengamatan Rata-rata
1 2 3 4
1 A 0.221 0.093 0.653 0.002 0.242 2 B 0.022 0.119 0.636 0.002 0.195 3 C 0.072 0.063 1.014 0.002 0.288
Tabel di atas menunjukkan bahwa nilai konsentrasi phosfat berkisar antara
0,002-1,014 mg/l. Berdasarkan nilai rata-rata dari ketiga lokasi berkisar antara
0.195-0.288 mg/l. Dari kisaran nilai tersebut dapat diuraikan bahwa konsentrasi
phospat pada lokasi pertambakan ini masih dalam kondisi yang layak untuk
dijadikan sebagai lahan budidaya ikan dan udang. Hal ini didasari oleh pernyataan
Widigdo (2013) yang menyatakan bahwa batas nilai optimum bagi phospat adalah
0,5 mg/l dengan batas toleransi 0,05-0,5 mg/l.
Tabel di atas menunjukkan bahwa nilai kadar phospat yang terendah
25
Pengambilan sampel minggu ke 4 dilakukan pada waktu pagi hari pukul
07.00-08.00 Wita dengan kondisi air laut dalam keadaan pasang. Dari semua hasil
pengamatan, peningkatan kadar phospat yang signifikan hanya terjadi pada
pengamatan minggu ke 3 di blok C dengan nilai 1.014 mg/l. Dimana nilai pada
pengamatan minggu sebelumnya adalah 0.063 mg/l. Peningkatan nilai kadar
phospat pada blok C ini dapat dipengaruhi oleh fraksi lain, seperti hasil ekskresi
organisme dan hasil autolisis organisme yang mati.
Konsentrasi phospat yang tergolong rendah ini dipengaruhi oleh masih
kurangnya pengaruh dari luar tambak yang masuk kedalam tambak yang
mengandung unsur-unsur yang dapat menghasilkan senyawa tersebut. Keberadaan
fosfor secara berlebihan yang disertai keberadaan nitrat dapat menstimulir ledakan
pertumbuhan alga di perairan yang dapat menggunakan oksigen dalam jumlah
besar sehingga berdampak pada penurunan kadar oksigen terlarut. Berdasarkan
kadar fosfor total, perairan diklasifikasikan menjadi tiga, yaitu : perairan dengan
tingkat kesuburan rendah kadar fosfor total berkisar antara 0 – 0.02 mg/liter;
perairan dengan tingkat kesuburan sedang yang memiliki kadar fosfor total
berkisar antara 0.021 – 0.05 mg/l; dan perairan dengan tingkat kesuburan tinggi
yang memiliki kadar phospat total 0.051 – 0.1 mg/l (Faizal, 2007).
Menurut Hutagalung dan Rozak (1997) dalam Hendrawati (2008)
menyatakan bahwa keberadaan phospat yang tinggi disebabkan oleh masuknya
limbah domestik, pertanian, insdustri dan perikanan yang mengandung phospat.
Pada sedimen, sumber utama fosfor adalah dari endapan terestrial yang
26
dari phospat yang terlarut yang sebagian berbentuk koloid berasal dari ekskresi
organisme dan juga terbentuk dari hasil autolisis organisme yang mati (Faizal
2007). Keberadaan berbagai bentuk phospat di laut dikendalikan oleh proses
biologi dan fisika, diantaranya penyerapan oleh fitoplankton pada proses
fotosintesis, penggunaan oleh bakteri serta adanya absorpsi oleh lumpur dasar
akibat kelebihan Ca2+ pada pH tinggi.
Sumber-sumber alami fosfor di perairan adalah pelapukan batuan mineral
dan dekomposisi bahan organik. Sumber antropogenik fosfor adalah dari limbah
industri dan limbah domestik, yakni yang berasal dari deterjen. Sumbangan dari
daerah pertanian yang menggunakan pupuk juga memberikan kontribusi yang
cukup besar bagi keberadaan fosfor. (Effendi, 2003 dalam Faizal 2007).
4.6. Amoniak (NH3)
Berdasarkan hasil penelitian pada sampel untuk parameter amoniak,
didapatkan data hasil penelitian yang dapat dilihat pada tabel di bawah ini :
Tabel 9. Data hasil penelitian Amoniak (NH3).
No Sampel Pengamatan Rata-rata
1 2 3 4
1 A 0.231 0.084 0.002 0.003 0.080 2 B 0.156 0.090 0.003 0.002 0.063 3 C 0.173 0.145 0.002 0.003 0.081
Tabel di atas menunjukkan bahwa nilai konsentrasi amoniak berkisar
antara 0.002-0.231 mg/l. Berdasarkan nilai rata-rata amoniak yang berkisar antara
0.063-0.081 mg/l, dapat dijelaskankan bahwa konsentrasi amoniak pada perairan
27
udang. Hal ini didasarkan pada pendapat Widigdo (2013) yang menyatakan
bahwa sifat toksik amonia bebas biasanya mulai terjadi pada konsentrasi 0,6-2
mg/l di kolam-kolam budidaya, sedangkan efek sublhetal terjadi pada konsentrasi
0,1-0,3 mg/l. Akan tetapi idealnya konsentrasi amonia pada perairan untuk
keperluan budidaya harus 0 ppm.
Setelah melihat tabel di atas dapat dijelaskan bahwa kadar amonia yang
tertinggi dengan nilai 0,231 mg/l terdapat di sampel minggu pertama pada sampel
blok A (Saluran utama pintu air). Dimana pengambilan sampel pada minggu
pertama dilakukan pada pagi hari pukul 05.30-07.30 wita dengan kondisi air laut
dalam keadaan pasang. Tingginya kandungan amonia pada sampel tersebut dapat
disebabkan oleh masih tingginya suhu air di lokasi tersebut. Hal ini didukung oleh
waktu pengambilan sampel yang dilakukan pada waktu pagi hari sehingga suhu di
perairan tersebut belum mengalami penurunan. Hal ini sesuai dengan sifat air
yang mempunyai panas laten yang tinggi, air dapat menyimpan panas cukup baik
dan melepaskannya dengan bertahap (Hamdani, 2014).
Jika melihat kondisi lingkungan ada beberapa hal yang dapat
menyebabkan keadaan ini terjadi diantaranya adalah lokasi saluran utama yang
berdekatan dengan laut dan daerah mangrove, masih tingginya suhu perairan di
lokasi sampling yaitu 30oC. Hal ini sesuai dengan pendapat Raswin (2003) amonia diperairan berasal dari hasil pemecahan nitrogen organik (protein dan
urea) dan nitrogen anorganik yang terdapat dalam tanah dan air, dapat pula berasal
dari dekomposisi bahan organik (tumbuhan dan biota akuatik yang telah mati)
28
pembesaran juga dipengaruhi oleh konsentrasi pH dan suhu. Semakin tinggi
konsentrasi pH dan suhu air maka semakin tinggi pula kadar NH3 perairan
tersebut.
Sedangkan kadar amoniak yang memiliki nilai terendah dengan nilai 0,002
mg/l terdapat di sampel minggu ke 3 pada sampel blok A (Saluran utama pintu
air), dan blok C (Tambak) dimana pengambilan sampel dilakukan pada pukul
13.00-14.30 WITA dengan kondisi air laut pada saat itu dalam kondisi surut.
Selain itu, nilai terendah juga berada pada sampel minggu ke 4 di blok B
(Tambak) yang mempunyai nilai yang sama dengan nilai sampel minggu ke 3
pada blok A (saluran utama pintu air) dan C (Tambak) dengan nilai 0,002 mg/l.
Pengambilan sampel dilakukan pada pukul 06.30-08.00 wita disertai dengan
kondisi air pada saat itu sedang pasang.
Hasil analisis kandungan amoniak di laboratorium adalah amonia total,
dimana belum dipisahkan antara amonia tak terionisasi (amonia bebas, NH3) yang
toksik dan ammonium (NH4+) yang relatif tidak bertoksik. Kandungan amonia
bebas yang toksik sangat bergantung pada pH, suhu, dan Salinitas perairan.
Semakin tinggi pH dan suhu, semakin tinggi persentase amonia bebas yang
terkandung dalam amonia total yang ada. Sedangkan faktor salinitas bersifat
sebaliknya, semakin tinggi salinitas, kandungan amonia bebas cenderung semakin
rendah. Di antara ketiga faktor ini, pH yang paling berperan, peningkatan pH
sedikit saja menyebabkan peningkatan amonia bebas yang cukup besar (Widigdo,
29
V. PENUTUP
5.1. Kesimpulan
Berdasarkan hasil penelitian yang dilakukan, penulis dapat menyimpulkan
bahwa :
1. Konsentrasi nilai pH, DO, dan salinitas di perairan tambak Kuri Caddi Maros
menunjukkan nilai yang masih layak untuk digunakan sebagai lokasi budidaya
ikan dan udang.
2. Kandungan nitrat, phospat, dan amoniak di perairan tambak Kuri Caddi Maros
masih berada pada kisaran nilai yang optimal dan batas toleransi untuk
kegiatan budidaya ikan dan udang.
5.2. Saran
Untuk melakukan kegiatan budidaya pada lokasi pertambakan Kuri Caddi
Maros, kita memerlukan sarana dan prasarana yang menunjang untuk melakukan
kegiatan budidaya. Di samping itu penerapan ilmu pengetahuan dan teknologi
adalah hal yang terpenting untuk diterapkan pada lokasi pertambakan Kuri Caddi
30
DAFTAR PUSTAKA
Alexander. 2006.Studi Penentuan Lokasi Untuk Pengembangan Budidaya Laut Berdasarkan Parameter Fisika, Kimia, dan Biologi Di Teluk Kupang Nusa Tenggara Timur. UNDIP. Semarang.
Buwono. 1993. Tambak Udang Windu Sistem Pengelolaan Berpola Intensif. Yogyakarta. Penerbit Kanisius.
Efendi H. 2003.Telaah Kualitas Air Bagi Pengelolaan Sumber Daya dan Lingkungan Perairan. Yogyakarta. Penerbit Kanisius.
Erlina A. 2006. Kualitas Perairan Di Sekitar BBPBAP Jepara Ditinjau Dari Aspek produktivitas Primer Sebagai Landasan Operasional Pengembangan Budidaya Udang dan Ikan.UNDIP. Semarang.
Faizal, 2010. Analisis Nitrat dan Fosfat Pada Sedimen Manggrove. Kabupaten Barru.(onlne),(andifaizalbahriskel.blogspot.com/.../analisis-nitrat-dan-fosfat-pada-sedim. Diakses senin,10 Agustus 2014).
Hamdani, 2014. Sifat-Sifat Air (online) (http://catatankimia.com/catatan/sifat-air.html.diakses senin, 10 Agustus 2014).
Hendrawati. et.all, 2008. Analisis Kadar Phosfat dan N-Nitrogen (Amonia, Nitrat, Nitrit) pada Tambak Air Payau Akibat Rembesan Lumpur Lapindo di Sidoarjo, Badan Riset Kelautan dan Perikanan, Jakarta Selatan. UIN Syarif Hidayatullah. Jakarta.
Hermanto.2007.PengelolaanBudidayaTambakBerwawasan Lingkungan.Widya iswara BPPP Belawan-Medan.
Mustofa, 2008. Daya Dukung Lingkungan Perairan Tambak Desa Mororejo Kabupaten Kendal. (online) Jurnal Saintek Perikanan UNDIP. Vol. 4.No. 1, 2008:50:55. Diakses 10 Agustus 2014).
Pramono B, Soedibya PHT. 2009.Aquaculture Engineering. Jakarta. Penerbit Cahaya Pineleng.
31
Raswin, 2003. Pembesaran Ikan Bandeng, Modul Pengelolaan Air Tambak. Direktorat Jenderal Pendidikan Dasar dan Menengah Departemen Pendidikan Nasional.
Rukmini. 2012. Teknologi Budidaya Biota Air. Bandung. Penerbit Karya Putra Darwati.
Sutrisyani, dkk. 2009. Panduan Praktis Analisis Kualitas Air Payau. Pusat Riset Perikanan Budidaya. Jakarta Selatan.
Widigdo B. 2013.Bertambak Udang Dengan Teknologi Biocrete.Jakarta. Penerbit Buku Kompas.
37 Lampiran 3. Foto kegiatan penelitian
DO Meter pH Meter
Pengukuran Kadar DO Pengukuran Kadar pH
38
Pengambilan sampel Pengambilan sampel
Botol sampel Kertas saring
39
33 Lampiran 1. Data Hasil Penelitian di Laboratorium BPPBAP Kab. Maros.
Sampel 23 Mei 2014
Sampel 30 Mei 2013
No Parameter Satuan Kode sampel Spesifikasi
Metode A1 A2 A3 B1 B2 B3 C1 C2 CC3 1 Nitrat,NO3-N mg/L 0.0677 0.0657 0.0405 0.0709 0.0352 0.0815 0.0415 0.0657 0.0574 Spektrofotometrik 2 Amonia, NH3-N mg/L 0.0900 0.0988 0.0628 0.0831 0.0943 0.0925 0.1168 0.1305 0.187 Spektrofotometrik 3 Fosfat, PO4-P mg/L 0.1232 0.0828 0.0730 0.0849 0.0685 0.2027 0.0582 0.0662 0.0631 Spektrofotometrik Sampel 06 Juni 2013
No Parameter Satuan Kode sampel Spesifikasi
Metode
A1 A2 A3 B1 B2 B3 C1 C2 CC3
1 Nitrat,NO3-N mg/L 0.0331 0.0051 0.0520 0.0102 0.0229 0.0841 0.0061 ttd 0.0243 Spektrofotometrik
2 Amonia, NH3-N mg/L 0.0018 0.0024 0.0029 0.0025 0.0034 0.0026 0.0018 0.0030 0.0022 Spektrofotometrik
3 Fosfat, PO4-P mg/L 0.1620 0.8947 0.9031 0.1154 1.3006 0.4912 1.5920 0.9663 0.4837 Spektrofotometrik
No Parameter Satuan Kode sampel Spesifikasi
Metode
A1 A2 A3 B1 B2 B3 C1 C2 CC3
1 Nitrat,NO3-N mg/L 5.3407 0.2502 0.4696 0.2079 0.3101 0.1614 1.3830 5.6002 0.9852 Spektrofotometrik
2 Amonia, NH3-N mg/L 0.2710 0.2050 0.2165 0.1919 0.1461 0.1295 0.1887 0.1830 0.1469 Spektrofotometrik
34
Sampel 13 Juni 2013
No Parameter Satuan Kode sampel Spesifikasi Metode
A1 A2 A3 B1 B2 B3 C1 C2 CC3
1 Nitrat,NO3-N mg/L 0.0794 0.0488 0.1611 0.0551 0.0523 0.0480 0.0524 0.131 0.1076 Spektrofotometrik
2 Amonia, NH3-N mg/L 0.0021 0.0047 0.0031 0.0017 0.0025 0.0030 0.0021 0.0028 0.0028 Spektrofotometrik
35 Lampiran 2. Data hasil pengukuran di tambak (insitu) Kuri Caddi Maros.
Sampel 23 Mei 2013
No Parameter Satuan Kode sampel
Spesifikasi Metode A B C 1 Salinitas - 35 35 35 Insitu 2 pH Ppt 7.78 7.66 7.82 Insitu 3 DO Mg/l 3.81 1.33 3.04 Insitu Sampel 30 Mei 2013
No Parameter Satuan Kode sampel Spesifikasi Metode
A B C
1 Salinitas - 35 35 33 Insitu
2 pH Ppt 7.64 7.42 7.69 Insitu
3 DO Mg/l 1.68 1.28 1.85 Insitu
Sampel 06 Juni 2013
No Parameter Satuan Kode sampel Spesifikasi Metode
A B C
1 Salinitas - 35 30 30 insitu
2 pH Ppt 8.1 7.8 8.1 insitu
36
Sampel 13 Juni 2013
No Parameter Satuan Kode sampel Spesifikasi Metode
A B C
1 Salinitas - 35 37 36 insitu
2 pH ppt 7.7 7.5 7.9 insitu